2 ГИДРОКСИСОЕДИН.ppt
- Количество слайдов: 78
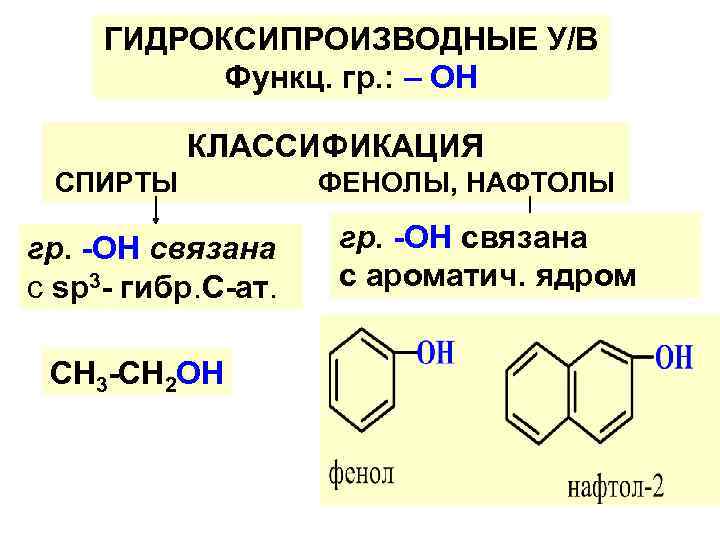 ГИДРОКСИПРОИЗВОДНЫЕ У/В Функц. гр. : – OH КЛАССИФИКАЦИЯ СПИРТЫ гр. -ОН связана с sp 3 - гибр. С-ат. СН 3 -СН 2 ОН ФЕНОЛЫ, НАФТОЛЫ гр. -ОН связана с ароматич. ядром
ГИДРОКСИПРОИЗВОДНЫЕ У/В Функц. гр. : – OH КЛАССИФИКАЦИЯ СПИРТЫ гр. -ОН связана с sp 3 - гибр. С-ат. СН 3 -СН 2 ОН ФЕНОЛЫ, НАФТОЛЫ гр. -ОН связана с ароматич. ядром
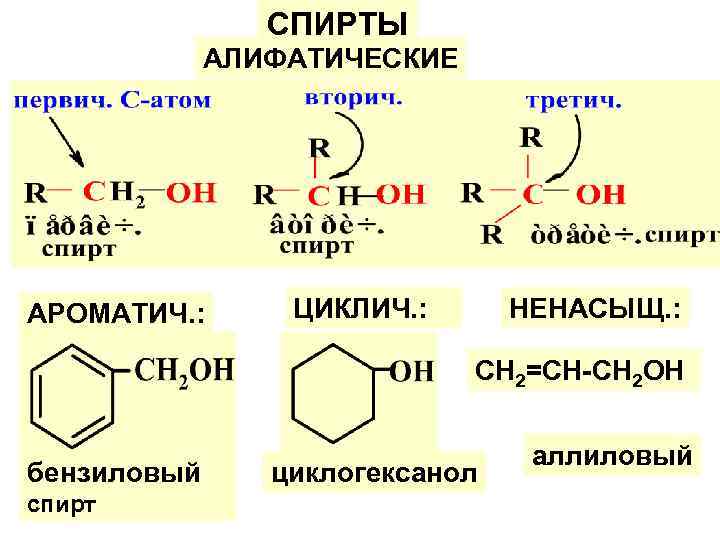 СПИРТЫ АЛИФАТИЧЕСКИЕ АРОМАТИЧ. : ЦИКЛИЧ. : НЕНАСЫЩ. : CH 2=CH-CH 2 OH бензиловый спирт циклогексанол аллиловый
СПИРТЫ АЛИФАТИЧЕСКИЕ АРОМАТИЧ. : ЦИКЛИЧ. : НЕНАСЫЩ. : CH 2=CH-CH 2 OH бензиловый спирт циклогексанол аллиловый
 В завис-ти от числа ОН-гр. различ. : одноатомные; двух-; -трехатомные НОМЕНКЛАТУРА Для спиртов 3 вида номенк. : • ТРИВИАЛ. назв. : (винный спирт C 2 H 5 OH); РАЦИОНАЛЬНАЯ ном-ра: • радикально – функцион. : назв. алкила +слово спирт ; • карбинольная: спирты рассматр. как произв. карбинола H 3 C-OH;
В завис-ти от числа ОН-гр. различ. : одноатомные; двух-; -трехатомные НОМЕНКЛАТУРА Для спиртов 3 вида номенк. : • ТРИВИАЛ. назв. : (винный спирт C 2 H 5 OH); РАЦИОНАЛЬНАЯ ном-ра: • радикально – функцион. : назв. алкила +слово спирт ; • карбинольная: спирты рассматр. как произв. карбинола H 3 C-OH;
 По ИЮПАК : выбор главн. цепи и начало нумер. определяет старш. функц. гр. (OH), оконч. –ОЛ, напр. :
По ИЮПАК : выбор главн. цепи и начало нумер. определяет старш. функц. гр. (OH), оконч. –ОЛ, напр. :
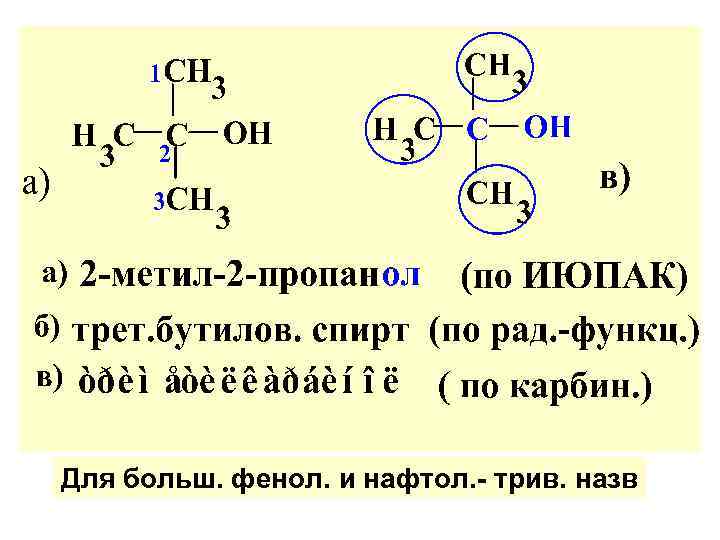 Для больш. фенол. и нафтол. - трив. назв
Для больш. фенол. и нафтол. - трив. назв
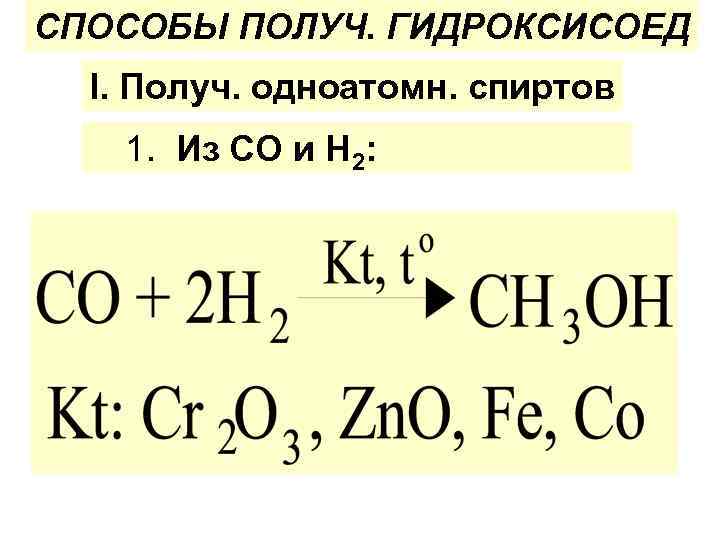 СПОСОБЫ ПОЛУЧ. ГИДРОКСИСОЕД I. Получ. одноатомн. спиртов 1. Из СО и Н 2:
СПОСОБЫ ПОЛУЧ. ГИДРОКСИСОЕД I. Получ. одноатомн. спиртов 1. Из СО и Н 2:
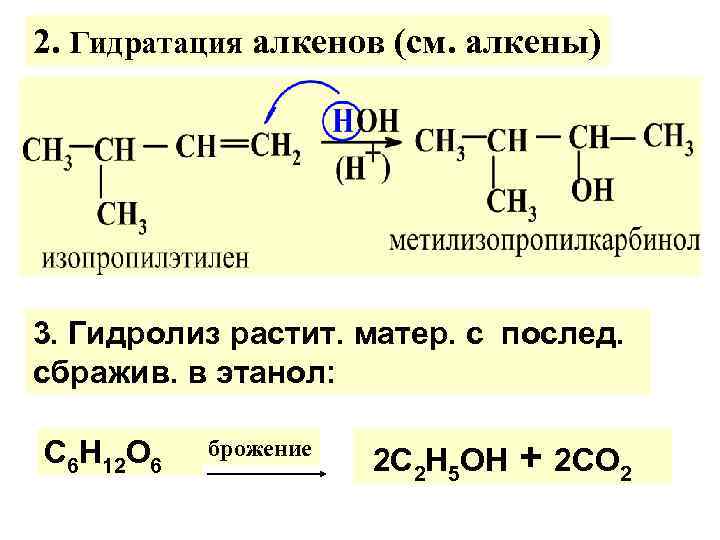 2. Гидратация алкенов (см. алкены) 3. Гидролиз растит. матер. с послед. сбражив. в этанол: С 6 Н 12 О 6 брожение 2 С 2 Н 5 ОН + 2 СО 2
2. Гидратация алкенов (см. алкены) 3. Гидролиз растит. матер. с послед. сбражив. в этанол: С 6 Н 12 О 6 брожение 2 С 2 Н 5 ОН + 2 СО 2
 4. Гидролиз сложных эфиров:
4. Гидролиз сложных эфиров:
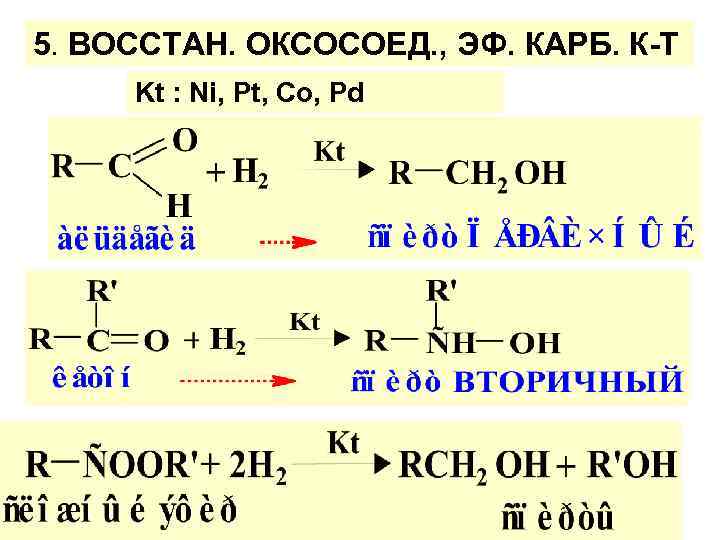 5. ВОССТАН. ОКСОСОЕД. , ЭФ. КАРБ. К-Т Kt : Ni, Pt, Co, Pd
5. ВОССТАН. ОКСОСОЕД. , ЭФ. КАРБ. К-Т Kt : Ni, Pt, Co, Pd
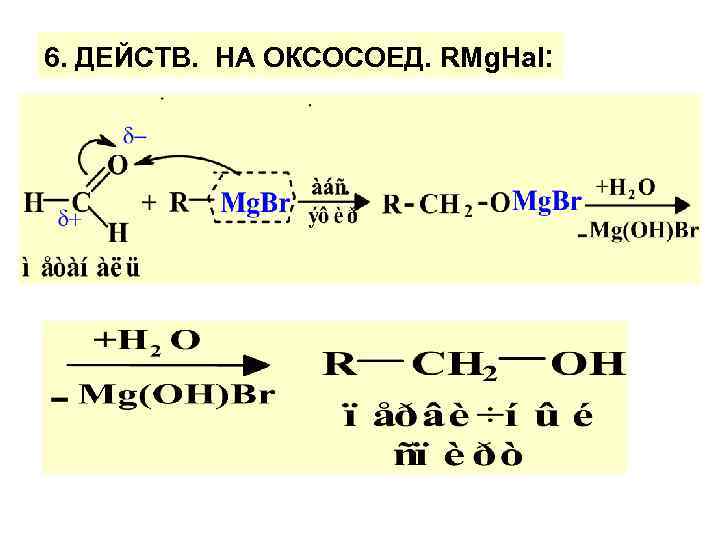 6. ДЕЙСТВ. НА ОКСОСОЕД. RMg. Hal:
6. ДЕЙСТВ. НА ОКСОСОЕД. RMg. Hal:
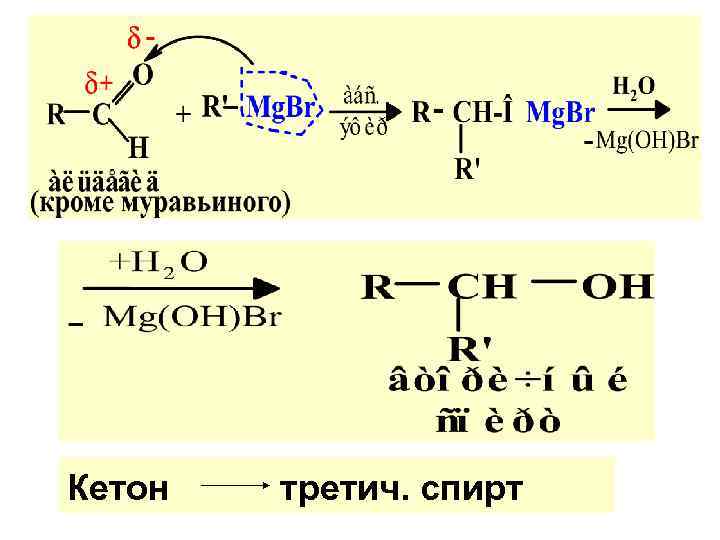 Кетон третич. спирт
Кетон третич. спирт
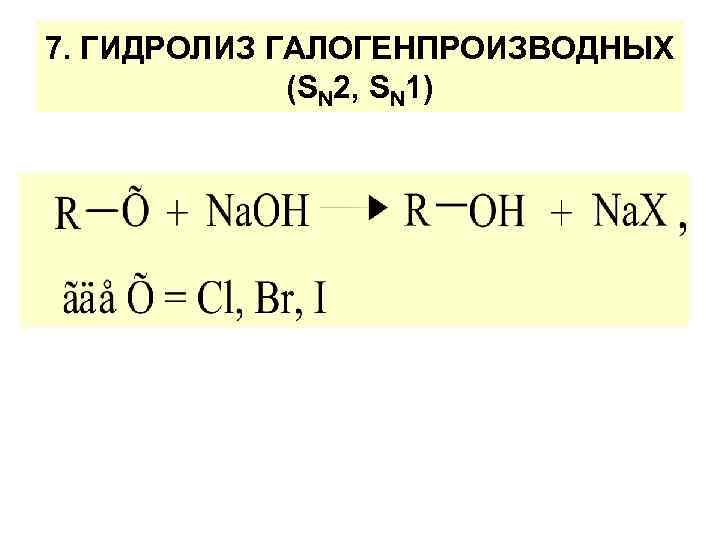 7. ГИДРОЛИЗ ГАЛОГЕНПРОИЗВОДНЫХ (SN 2, SN 1)
7. ГИДРОЛИЗ ГАЛОГЕНПРОИЗВОДНЫХ (SN 2, SN 1)
 Р-ЦИИ НУКЛЕОФ. ЗАМЕЩ. ( SN ) У НАСЫЩЕН. АТОМА УГЛЕРОДА Р-ции SN могут протекать по механизмам SN 2 и SN 1. SN 2 – бимолекуляр. нуклеоф. замещ. SN 1 – мономолекул. нуклеф. замещ
Р-ЦИИ НУКЛЕОФ. ЗАМЕЩ. ( SN ) У НАСЫЩЕН. АТОМА УГЛЕРОДА Р-ции SN могут протекать по механизмам SN 2 и SN 1. SN 2 – бимолекуляр. нуклеоф. замещ. SN 1 – мономолекул. нуклеф. замещ
 Молекулярность р-ции – число мол-л, в которых происх. изменение ковалентности связей в одной элементарной р -ции. В многостадийном процессе молекулярность - число мол-л, претерпевающих химич. превращ. , на лимитирующей ( самой медлен. ) стадии процесса.
Молекулярность р-ции – число мол-л, в которых происх. изменение ковалентности связей в одной элементарной р -ции. В многостадийном процессе молекулярность - число мол-л, претерпевающих химич. превращ. , на лимитирующей ( самой медлен. ) стадии процесса.
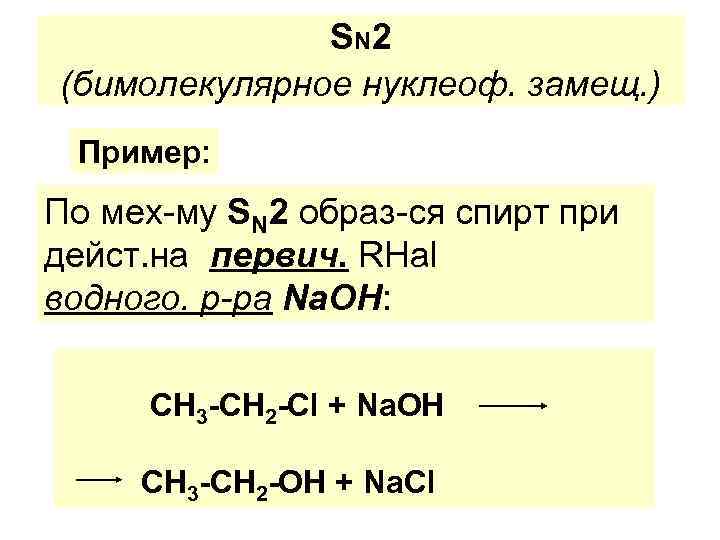 S N 2 (бимолекулярное нуклеоф. замещ. ) Пример: По мех-му SN 2 образ-ся спирт при дейст. на первич. RHal водного. р-ра Na. OH: СН 3 -СН 2 -Сl + Na. OH СН 3 -СН 2 -ОН + Na. Cl
S N 2 (бимолекулярное нуклеоф. замещ. ) Пример: По мех-му SN 2 образ-ся спирт при дейст. на первич. RHal водного. р-ра Na. OH: СН 3 -СН 2 -Сl + Na. OH СН 3 -СН 2 -ОН + Na. Cl
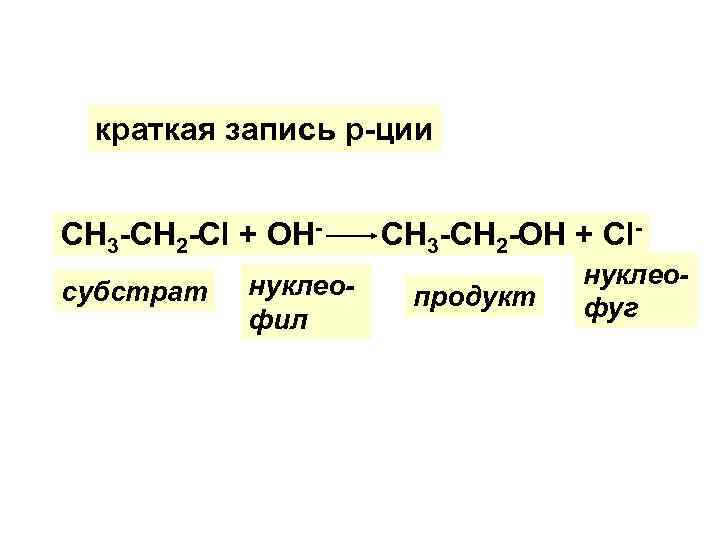 краткая запись р-ции СН 3 -СН 2 -Сl + ОНсубстрат нуклеофил СН 3 -СН 2 -ОН + Сlпродукт нуклеофуг
краткая запись р-ции СН 3 -СН 2 -Сl + ОНсубстрат нуклеофил СН 3 -СН 2 -ОН + Сlпродукт нуклеофуг
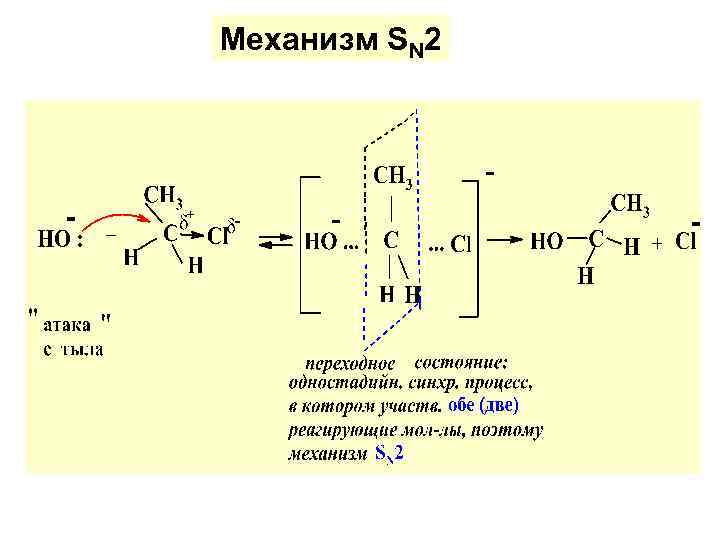 Механизм SN 2
Механизм SN 2
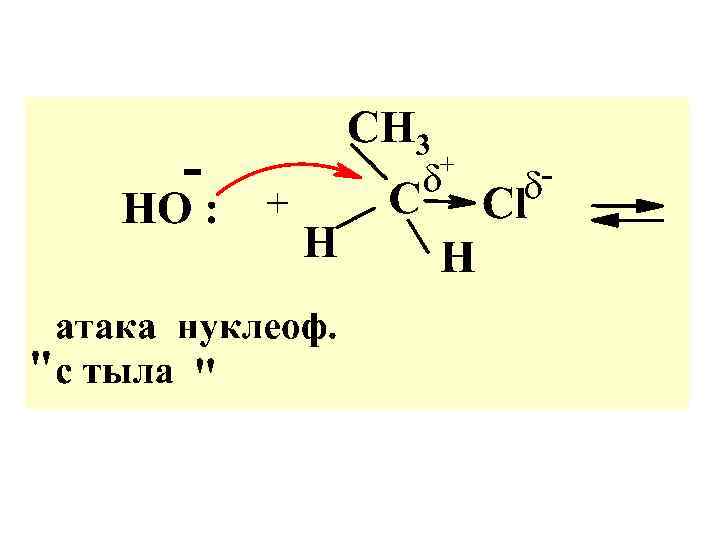
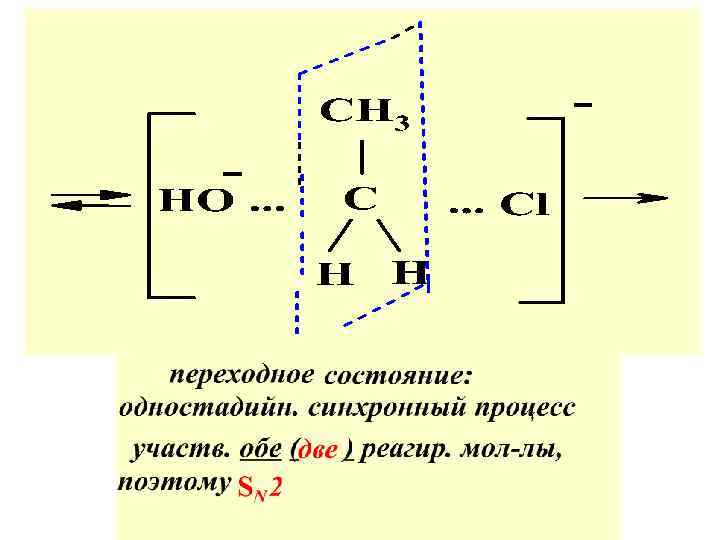
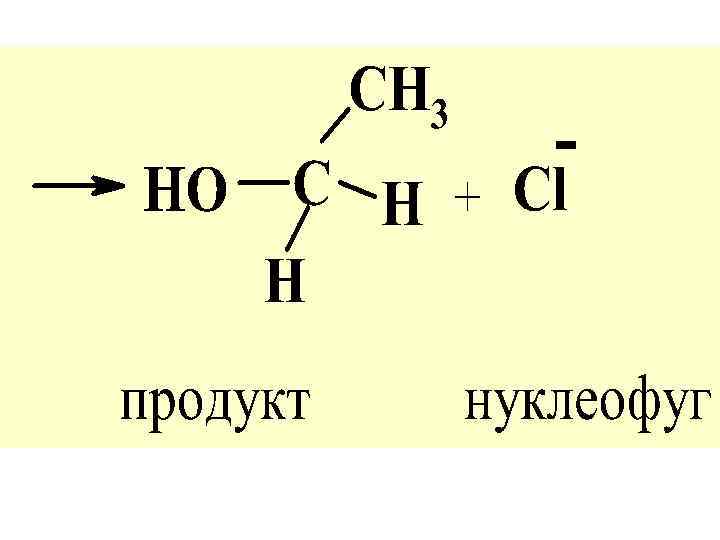
 На лимитир. стадии процессапереход. сост. одновременно претерпевают измен. ковален-сти связей обе ( две) реагирующ. мол-лы, поэтому молекулярность р-ции в целом равна двум, т. е. SN 2.
На лимитир. стадии процессапереход. сост. одновременно претерпевают измен. ковален-сти связей обе ( две) реагирующ. мол-лы, поэтому молекулярность р-ции в целом равна двум, т. е. SN 2.
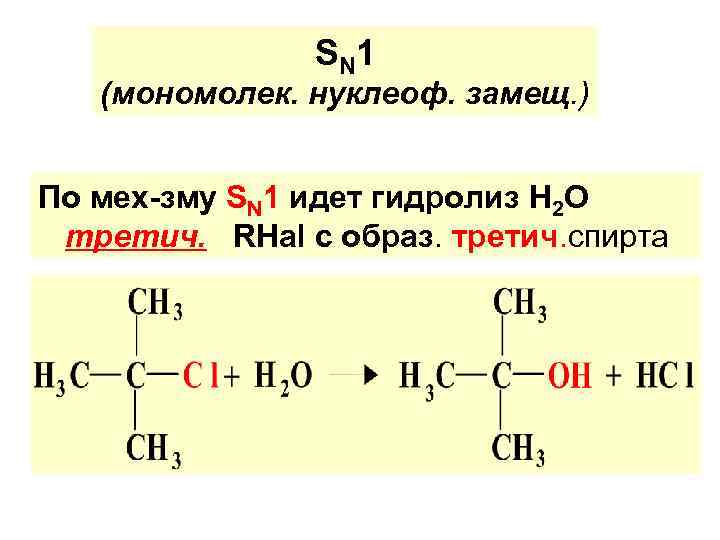 S N 1 (мономолек. нуклеоф. замещ. ) По мех-зму SN 1 идет гидролиз Н 2 О третич. RHal с образ. третич. спирта
S N 1 (мономолек. нуклеоф. замещ. ) По мех-зму SN 1 идет гидролиз Н 2 О третич. RHal с образ. третич. спирта
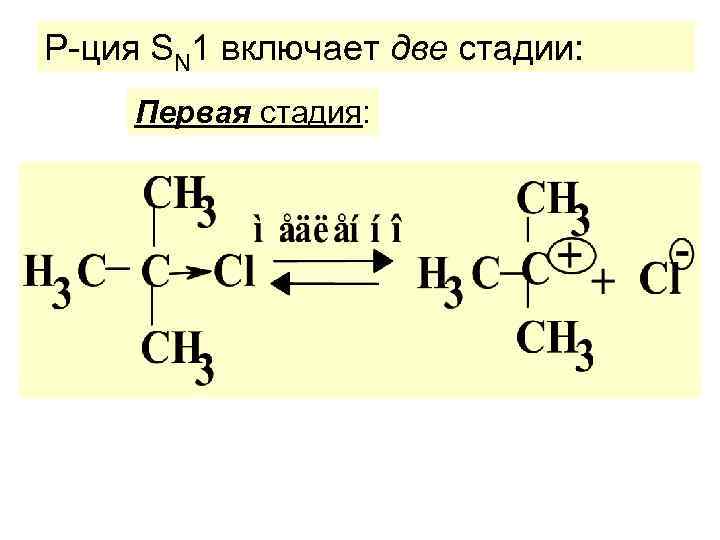 Р-ция SN 1 включает две стадии: Первая стадия:
Р-ция SN 1 включает две стадии: Первая стадия:
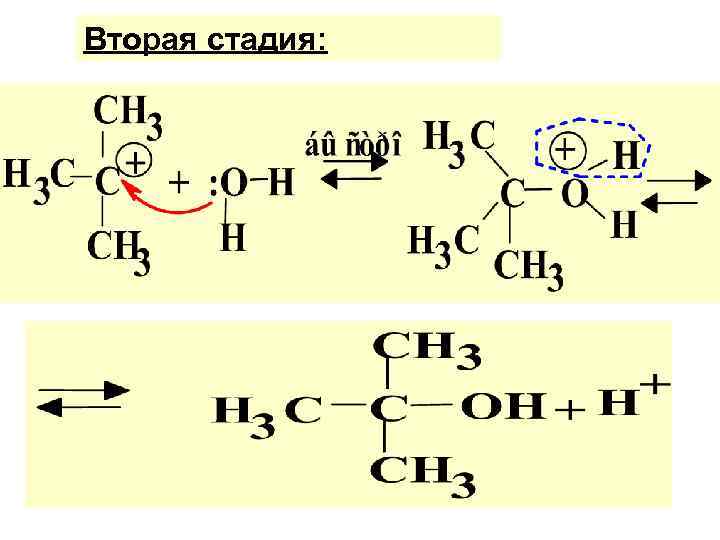 Вторая стадия:
Вторая стадия:
 Процесс двухстадийный В первой стадии участвует только ОДНА мол-ла - молекула субстрата. Она относит. медленно диссоц. на карбкатион и уходящ. группу. Стадия медл. , поэтому лимитирующая. Bо второй. стадии нуклеофил быстро атакует карбкатион, образуя продукт р-ции.
Процесс двухстадийный В первой стадии участвует только ОДНА мол-ла - молекула субстрата. Она относит. медленно диссоц. на карбкатион и уходящ. группу. Стадия медл. , поэтому лимитирующая. Bо второй. стадии нуклеофил быстро атакует карбкатион, образуя продукт р-ции.
 Т. о. , на лимитир. стадии проц-са, самой медленной (первая стадия) измен. ковалент. связей происх. только в одной реагир. мол-ле (алкилгалогенид), поэтому общ. мех-зм р-ции опред-ся как SN 1.
Т. о. , на лимитир. стадии проц-са, самой медленной (первая стадия) измен. ковалент. связей происх. только в одной реагир. мол-ле (алкилгалогенид), поэтому общ. мех-зм р-ции опред-ся как SN 1.
 ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВ. Р-ЦИЙ SN 2 И SN 1 1. ВЛИЯНИЕ СТРОЕНИЯ СУБСТРАТА. Реакц. способн. RHal в р-ции SN 2 : CH 3 Cl >первич. > вторич. » » третич. Причина: пространств. доступность реакц. центра
ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВ. Р-ЦИЙ SN 2 И SN 1 1. ВЛИЯНИЕ СТРОЕНИЯ СУБСТРАТА. Реакц. способн. RHal в р-ции SN 2 : CH 3 Cl >первич. > вторич. » » третич. Причина: пространств. доступность реакц. центра
 В р-циях SN 1 лимит. стадия – стадия образов. карбкатиона. В связи с этим, актив. RHal изм-ся в том же порядке, что и устойчивость карбкатионов: бензилгалогениды ≈ аллил… > третич. > > вторич. > первич. > метилгалог-ды.
В р-циях SN 1 лимит. стадия – стадия образов. карбкатиона. В связи с этим, актив. RHal изм-ся в том же порядке, что и устойчивость карбкатионов: бензилгалогениды ≈ аллил… > третич. > > вторич. > первич. > метилгалог-ды.
 2. Влияние нукл-ла и раствор-ля. По периоду табл. Мендел. нуклеоф-сть уменьш-ся слева направо: NН 3 > НОН; NН 2¯>ОН¯>F¯ По группе табл. Мендел. нуклеоф-сть возрастает в протонных раствор-х сверху вниз: I¯ > Br¯ >Cl¯; НS¯ > ОН¯
2. Влияние нукл-ла и раствор-ля. По периоду табл. Мендел. нуклеоф-сть уменьш-ся слева направо: NН 3 > НОН; NН 2¯>ОН¯>F¯ По группе табл. Мендел. нуклеоф-сть возрастает в протонных раствор-х сверху вниз: I¯ > Br¯ >Cl¯; НS¯ > ОН¯
 В р-циях SN 2, примен. сильные нуклеоф. (ОН¯) и апротон. раствор-ли. Процес. SN 1 реализ-ся в поляр-ных раств-лях для расщепл. связи С–Наl. Прим. слабые нуклеоф. (H 2 O)
В р-циях SN 2, примен. сильные нуклеоф. (ОН¯) и апротон. раствор-ли. Процес. SN 1 реализ-ся в поляр-ных раств-лях для расщепл. связи С–Наl. Прим. слабые нуклеоф. (H 2 O)
 3. Природа нуклеофуга (уходящ. гр. ). В р-циях SN 2 и SN 1 в ряду связей С-F, С-Cl, С- Br, С-I реакц. способ. возрастает, т. к. в этом ряду увелич-ся поляриз. связи С-Х и устойч. уходящ. гр. : I> Br > Cl > F
3. Природа нуклеофуга (уходящ. гр. ). В р-циях SN 2 и SN 1 в ряду связей С-F, С-Cl, С- Br, С-I реакц. способ. возрастает, т. к. в этом ряду увелич-ся поляриз. связи С-Х и устойч. уходящ. гр. : I> Br > Cl > F
 Получение многоатомных спиртов • Синтез этиленгликоля из этилена:
Получение многоатомных спиртов • Синтез этиленгликоля из этилена:
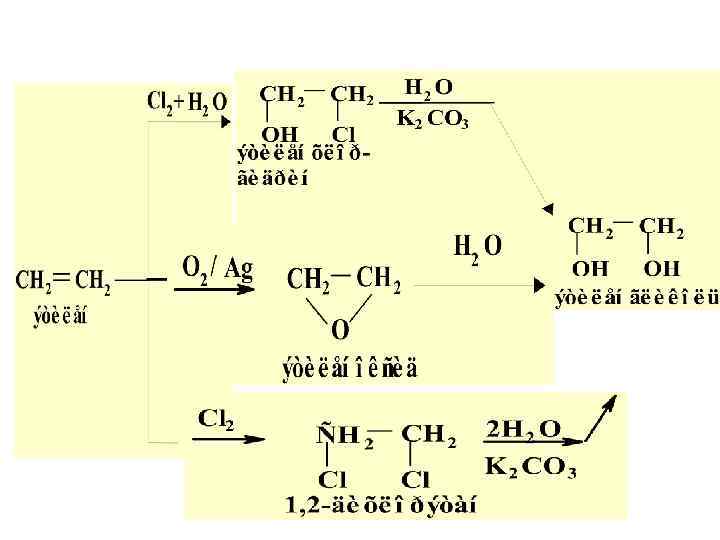
 2. ПОЛУЧЕНИЕ ГЛИЦЕРИНА: а) ИЗ ПРОПИЛЕНА
2. ПОЛУЧЕНИЕ ГЛИЦЕРИНА: а) ИЗ ПРОПИЛЕНА
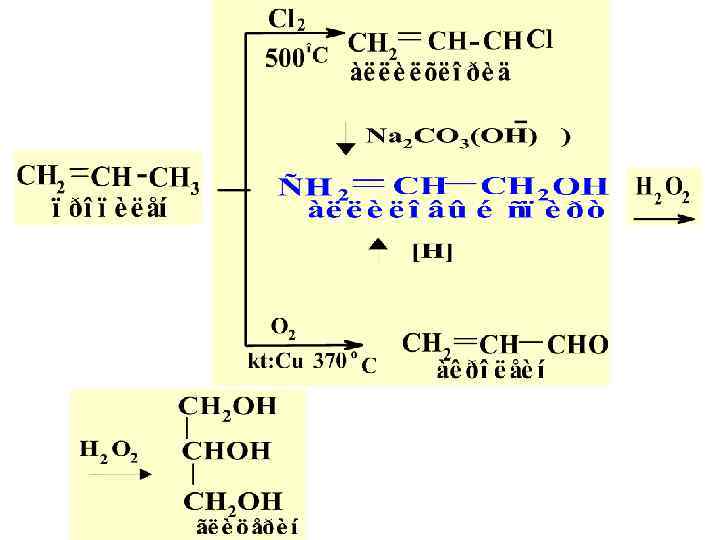
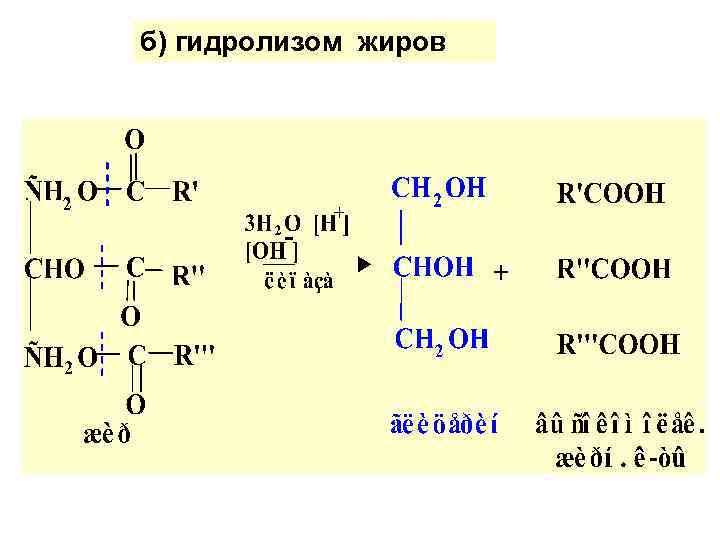 б) гидролизом жиров
б) гидролизом жиров
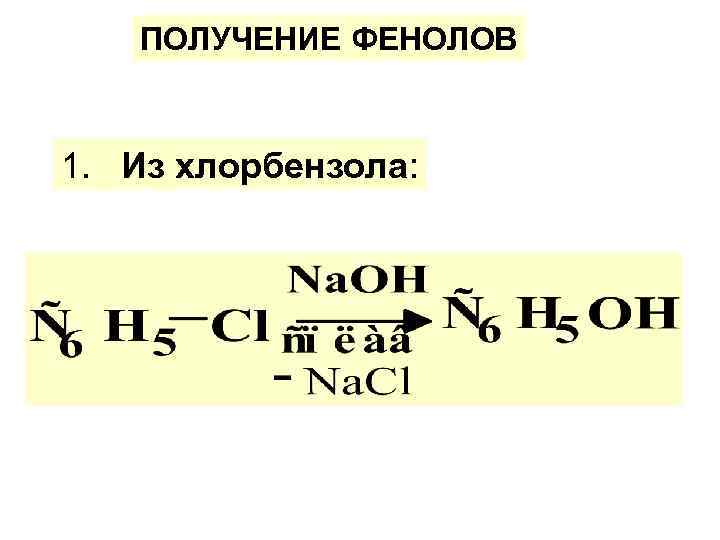 ПОЛУЧЕНИЕ ФЕНОЛОВ 1. Из хлорбензола:
ПОЛУЧЕНИЕ ФЕНОЛОВ 1. Из хлорбензола:
 2. Сплавл. солей бензолсульфок-т со щелоч. :
2. Сплавл. солей бензолсульфок-т со щелоч. :
 3. Окислением кумола:
3. Окислением кумола:
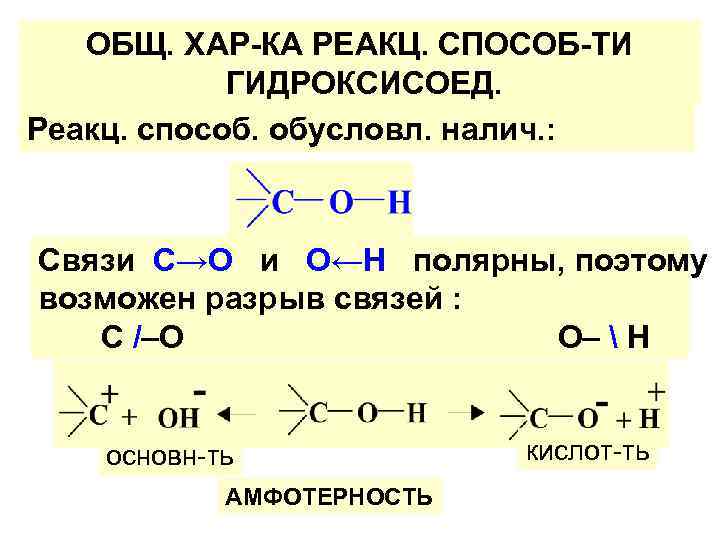 ОБЩ. ХАР-КА РЕАКЦ. СПОСОБ-ТИ ГИДРОКСИСОЕД. Реакц. способ. обусловл. налич. : Связи С→О и О←Н полярны, поэтому возможен разрыв связей : C /–O O– H основн-ть АМФОТЕРНОСТЬ кислот-ть
ОБЩ. ХАР-КА РЕАКЦ. СПОСОБ-ТИ ГИДРОКСИСОЕД. Реакц. способ. обусловл. налич. : Связи С→О и О←Н полярны, поэтому возможен разрыв связей : C /–O O– H основн-ть АМФОТЕРНОСТЬ кислот-ть
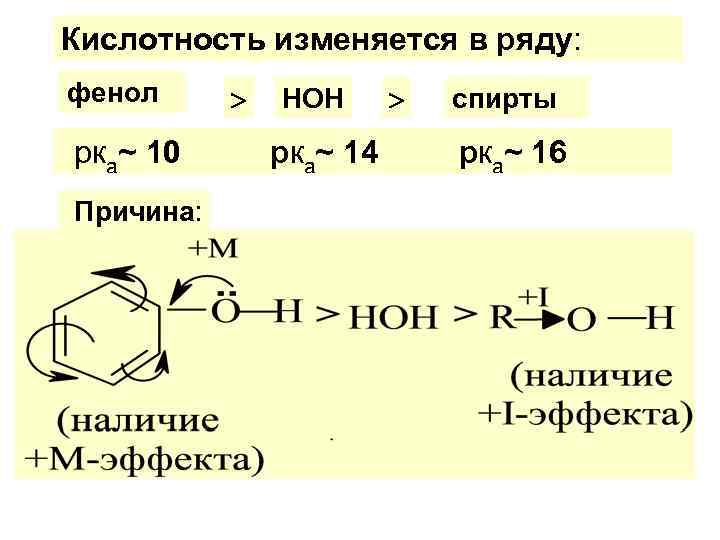 Кислотность изменяется в ряду: фенол рка~ 10 Причина: НОН рка~ 14 спирты рка~ 16
Кислотность изменяется в ряду: фенол рка~ 10 Причина: НОН рка~ 14 спирты рка~ 16
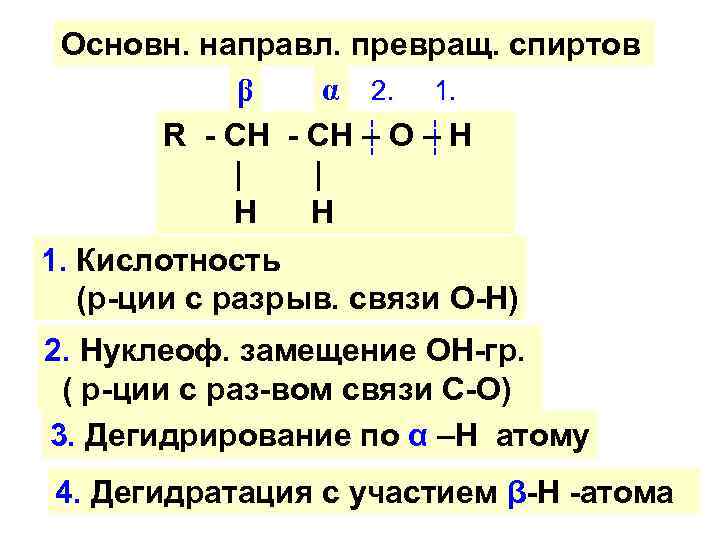 ---- Основн. направл. превращ. спиртов α 2. 1. β R - CH – O – H | | H H 1. Кислотность (р-ции с разрыв. связи О-Н) 2. Нуклеоф. замещение ОН-гр. ( р-ции с раз-вом связи С-О) 3. Дегидрирование по α –Н атому 4. Дегидратация с участием β-Н -атома
---- Основн. направл. превращ. спиртов α 2. 1. β R - CH – O – H | | H H 1. Кислотность (р-ции с разрыв. связи О-Н) 2. Нуклеоф. замещение ОН-гр. ( р-ции с раз-вом связи С-О) 3. Дегидрирование по α –Н атому 4. Дегидратация с участием β-Н -атома
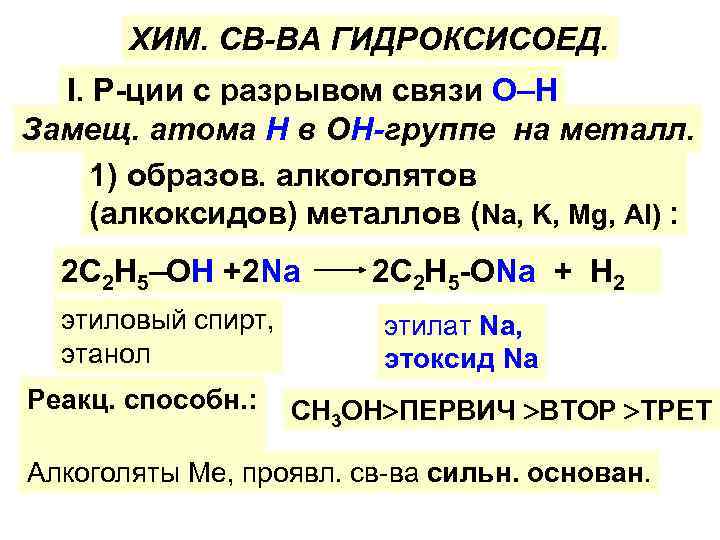 ХИМ. СВ-ВА ГИДРОКСИСОЕД. I. Р-ции с разрывом связи O–H Замещ. атома Н в ОН-группе на металл. 1) образов. алкоголятов (алкоксидов) металлов (Na, K, Mg, Al) : 2 С 2 Н 5–OH +2 Na этиловый спирт, этанол Реакц. способн. : 2 С 2 Н 5 -ONa + H 2 этилат Na, этоксид Na СН 3 ОН ПЕРВИЧ ВТОР ТРЕТ Алкоголяты Ме, проявл. св-ва сильн. основан.
ХИМ. СВ-ВА ГИДРОКСИСОЕД. I. Р-ции с разрывом связи O–H Замещ. атома Н в ОН-группе на металл. 1) образов. алкоголятов (алкоксидов) металлов (Na, K, Mg, Al) : 2 С 2 Н 5–OH +2 Na этиловый спирт, этанол Реакц. способн. : 2 С 2 Н 5 -ONa + H 2 этилат Na, этоксид Na СН 3 ОН ПЕРВИЧ ВТОР ТРЕТ Алкоголяты Ме, проявл. св-ва сильн. основан.
 2) Взаимодейст. с Мg-органич. соед. (Л. А. Чугаев, Ф. В. Церевитинов): Р-ция прим. для опред. кол-ва ОН-групп в мол-ле спирта (по объему СН 4 ).
2) Взаимодейст. с Мg-органич. соед. (Л. А. Чугаев, Ф. В. Церевитинов): Р-ция прим. для опред. кол-ва ОН-групп в мол-ле спирта (по объему СН 4 ).
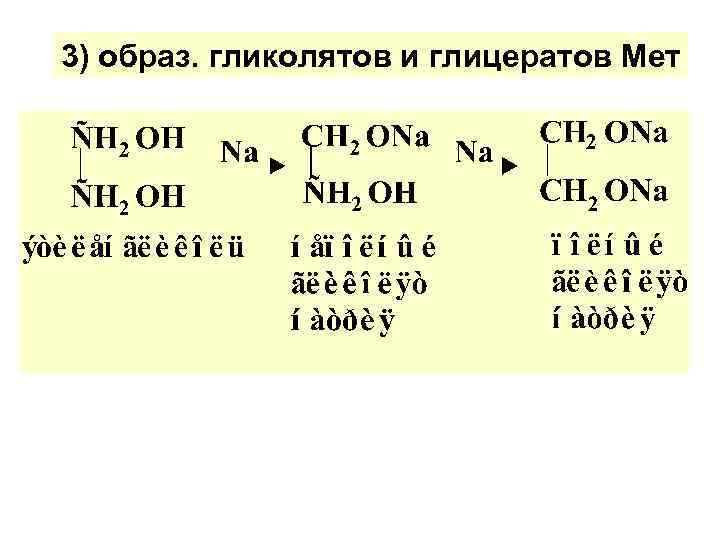 3) образ. гликолятов и глицератов Мет
3) образ. гликолятов и глицератов Мет
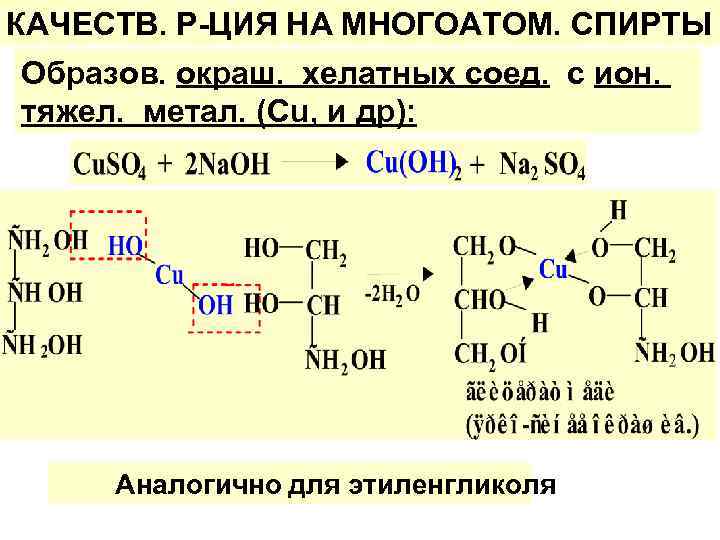 КАЧЕСТВ. Р-ЦИЯ НА МНОГОАТОМ. СПИРТЫ Образов. окраш. хелатных соед. с ион. тяжел. метал. (Сu, и др): Аналогично для этиленгликоля
КАЧЕСТВ. Р-ЦИЯ НА МНОГОАТОМ. СПИРТЫ Образов. окраш. хелатных соед. с ион. тяжел. метал. (Сu, и др): Аналогично для этиленгликоля

 4) Образ. фенолятов (феноксидов) метал. Феноляты легко разлаг-ся СО 2: Р-ции примен. для разд. фенолов и спиртов. Для кач. обнар. фенол. : цвет. р-ции с Fe. Cl 3. . Фенол с Fe. Cl 3 дает фиолет. окраску
4) Образ. фенолятов (феноксидов) метал. Феноляты легко разлаг-ся СО 2: Р-ции примен. для разд. фенолов и спиртов. Для кач. обнар. фенол. : цвет. р-ции с Fe. Cl 3. . Фенол с Fe. Cl 3 дает фиолет. окраску

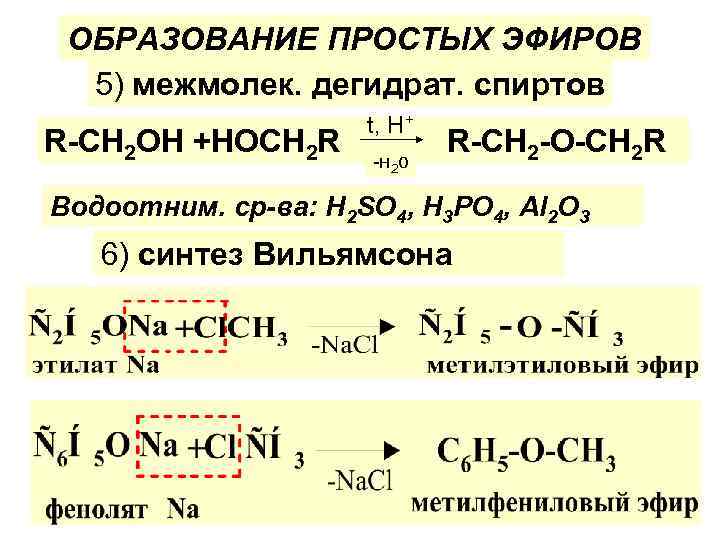 ОБРАЗОВАНИЕ ПРОСТЫХ ЭФИРОВ 5) межмолек. дегидрат. спиртов R-CH 2 OH +HOCH 2 R t, H+ -н 2 о R-CH 2 -O-CH 2 R Водоотним. ср-ва: H 2 SO 4, H 3 PO 4, Al 2 O 3 6) синтез Вильямсона
ОБРАЗОВАНИЕ ПРОСТЫХ ЭФИРОВ 5) межмолек. дегидрат. спиртов R-CH 2 OH +HOCH 2 R t, H+ -н 2 о R-CH 2 -O-CH 2 R Водоотним. ср-ва: H 2 SO 4, H 3 PO 4, Al 2 O 3 6) синтез Вильямсона
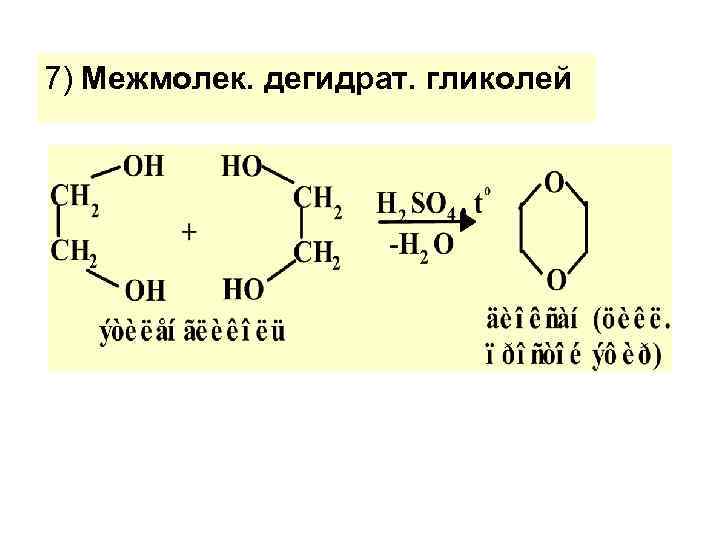 7) Mежмолек. дегидрат. гликолей
7) Mежмолек. дегидрат. гликолей
 ОБРАЗОВ. СЛОЖНЫХ ЭФИРОВ 8) взаимодейс. с минер. кисл-ми а) одноатом. спиртов
ОБРАЗОВ. СЛОЖНЫХ ЭФИРОВ 8) взаимодейс. с минер. кисл-ми а) одноатом. спиртов
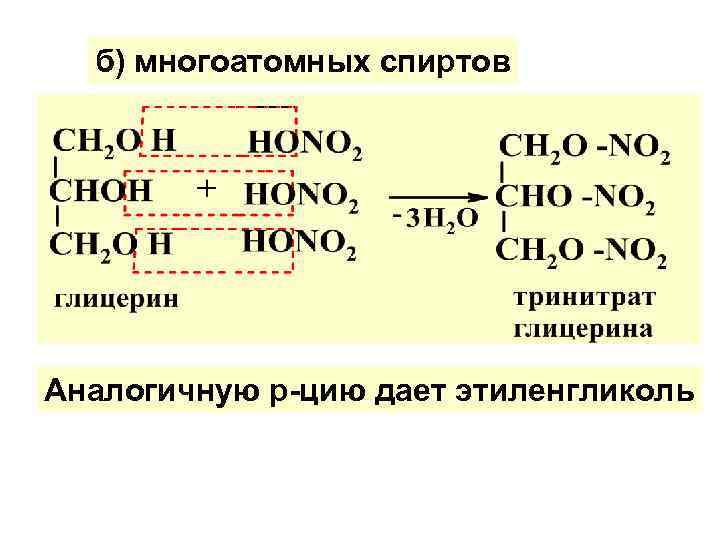 б) многоатомных спиртов Аналогичную р-цию дает этиленгликоль
б) многоатомных спиртов Аналогичную р-цию дает этиленгликоль
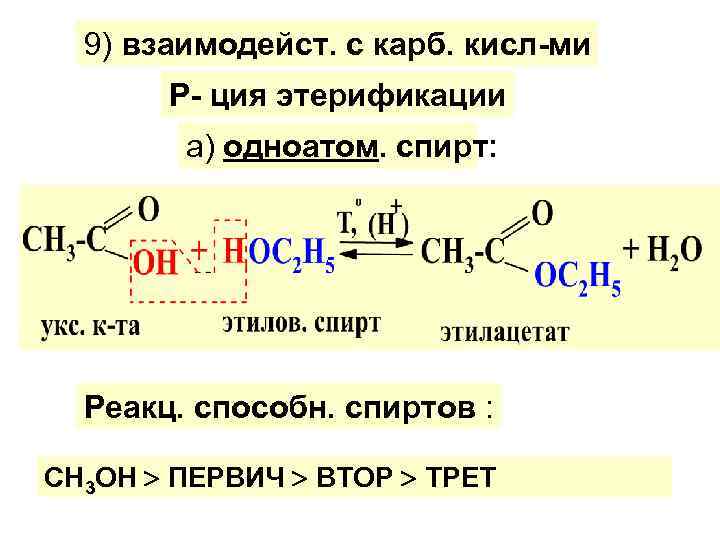 9) взаимодейст. с карб. кисл-ми Р- ция этерификации а) одноатом. спирт: Реакц. способн. спиртов : СН 3 ОН ПЕРВИЧ ВТОР ТРЕТ
9) взаимодейст. с карб. кисл-ми Р- ция этерификации а) одноатом. спирт: Реакц. способн. спиртов : СН 3 ОН ПЕРВИЧ ВТОР ТРЕТ
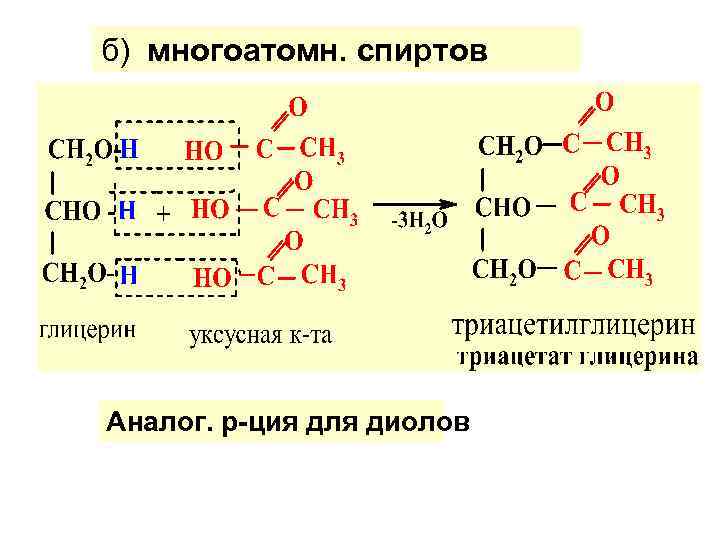 б) многоатомн. спиртов Аналог. р-ция для диолов
б) многоатомн. спиртов Аналог. р-ция для диолов
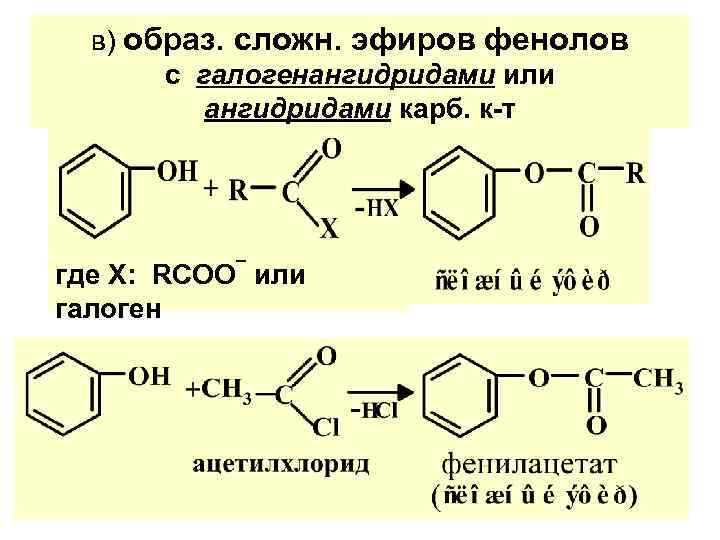 в) образ. сложн. эфиров фенолов с галогенангидридами или ангидридами карб. к-т где X: RCOO¯ или галоген
в) образ. сложн. эфиров фенолов с галогенангидридами или ангидридами карб. к-т где X: RCOO¯ или галоген
 II. Р-ЦИИ С РАЗРЫВОМ C – O СВЯЗИ Нуклеоф. замещ. ОН-гр. на галоген (SN ) 1) образ. алкилгалогенидов (R - Наl) а) R– ОН + HX R – Х + Н 2 О где HX: НCl, HBr, HI; kt: Zn. Cl 2, H 2 SO 4 Реакц. способн. : HX: HI > HBr > HCl; спиртов: аллил. >бензил. >трет. >втор. >перв. >CH 3 OH
II. Р-ЦИИ С РАЗРЫВОМ C – O СВЯЗИ Нуклеоф. замещ. ОН-гр. на галоген (SN ) 1) образ. алкилгалогенидов (R - Наl) а) R– ОН + HX R – Х + Н 2 О где HX: НCl, HBr, HI; kt: Zn. Cl 2, H 2 SO 4 Реакц. способн. : HX: HI > HBr > HCl; спиртов: аллил. >бензил. >трет. >втор. >перв. >CH 3 OH
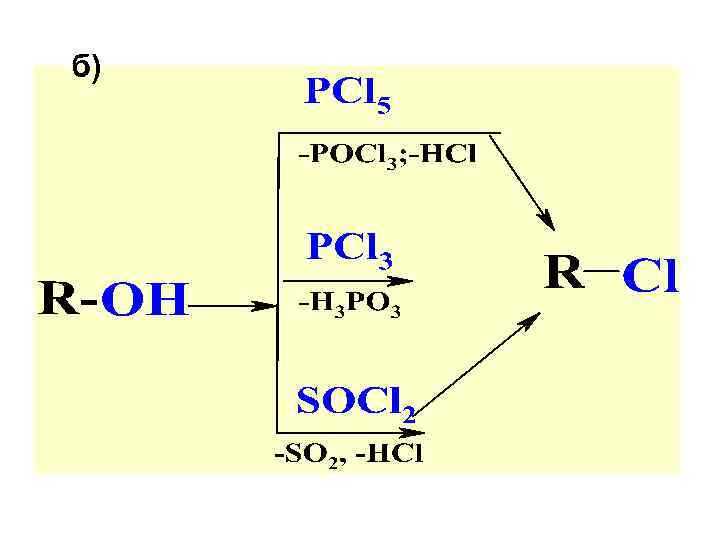 б)
б)
 3 R-OH + PBr 3 6 R-OH + 2 P +3 I 2 R-Br + H 3 PO 3 6 R-I + 2 H 3 PO 3 Р-ции идут с промеж. образ. эфира:
3 R-OH + PBr 3 6 R-OH + 2 P +3 I 2 R-Br + H 3 PO 3 6 R-I + 2 H 3 PO 3 Р-ции идут с промеж. образ. эфира:
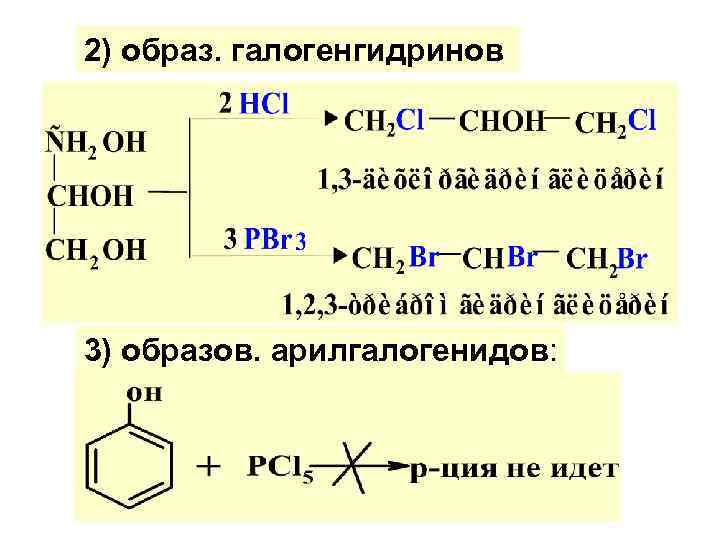 2) образ. галогенгидринов 3) образов. арилгалогенидов:
2) образ. галогенгидринов 3) образов. арилгалогенидов:
 ВНУТРИМОЛ. ДЕГИДРАТ. СПИРТ. Kt : H 2 SO 4 , T°C 1) ДЕГИДРАТАЦ. ОДНОАТОМ. СПИРТ. В завис. от усл. р-ции : а) в мяг. усл. (O°C) при изб. Н 2 SO 4 – алкилсульфат (R-О –SО 3 Н) - слож. эфир CH 3 -CH 2 -OH+HОSO 3 Н CH 3 -CH 2 -OSO 3 H этилсульфат б) при умерен. Т°С и избыт. спирта – - простые эфиры (R-О- R); в) при высок. Т°С – алкены
ВНУТРИМОЛ. ДЕГИДРАТ. СПИРТ. Kt : H 2 SO 4 , T°C 1) ДЕГИДРАТАЦ. ОДНОАТОМ. СПИРТ. В завис. от усл. р-ции : а) в мяг. усл. (O°C) при изб. Н 2 SO 4 – алкилсульфат (R-О –SО 3 Н) - слож. эфир CH 3 -CH 2 -OH+HОSO 3 Н CH 3 -CH 2 -OSO 3 H этилсульфат б) при умерен. Т°С и избыт. спирта – - простые эфиры (R-О- R); в) при высок. Т°С – алкены
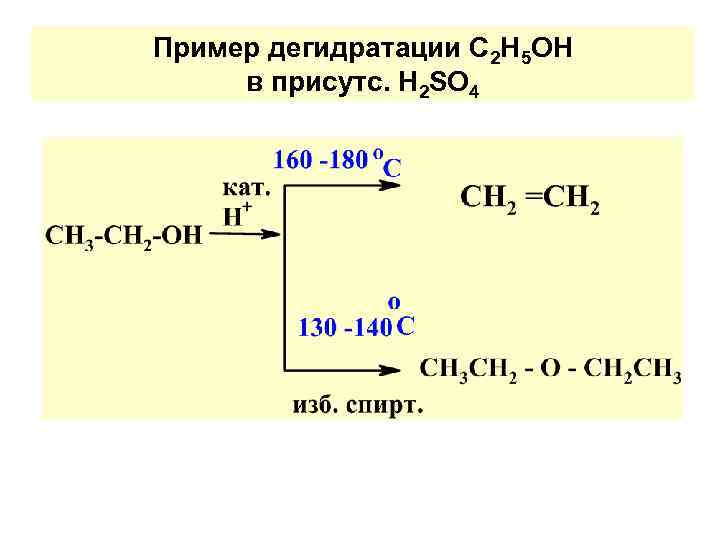 Пример дегидратации С 2 Н 5 ОН в присутс. H 2 SO 4
Пример дегидратации С 2 Н 5 ОН в присутс. H 2 SO 4
 2) вторич. и третич. спирты отщепл. Н 2 О с образ. алкенов. Р-ции идут в соотв. с прав. Зайцева(преимущ. ) :
2) вторич. и третич. спирты отщепл. Н 2 О с образ. алкенов. Р-ции идут в соотв. с прав. Зайцева(преимущ. ) :
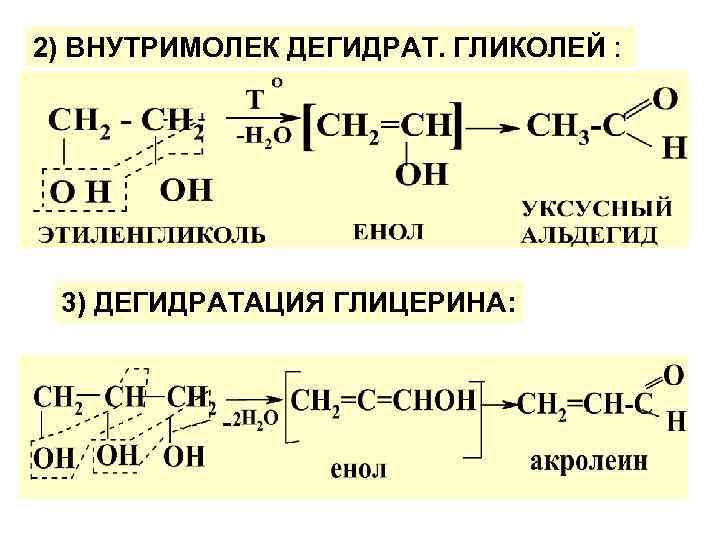 2) ВНУТРИМОЛЕК ДЕГИДРАТ. ГЛИКОЛЕЙ : 3) ДЕГИДРАТАЦИЯ ГЛИЦЕРИНА:
2) ВНУТРИМОЛЕК ДЕГИДРАТ. ГЛИКОЛЕЙ : 3) ДЕГИДРАТАЦИЯ ГЛИЦЕРИНА:
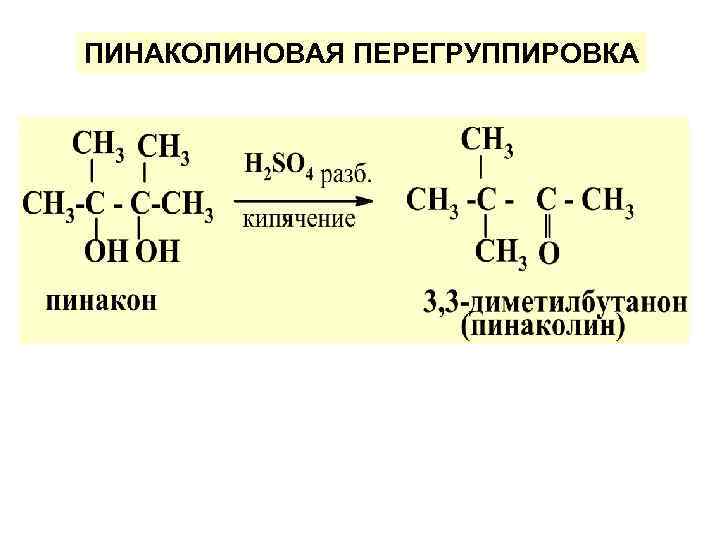 ПИНАКОЛИНОВАЯ ПЕРЕГРУППИРОВКА
ПИНАКОЛИНОВАЯ ПЕРЕГРУППИРОВКА
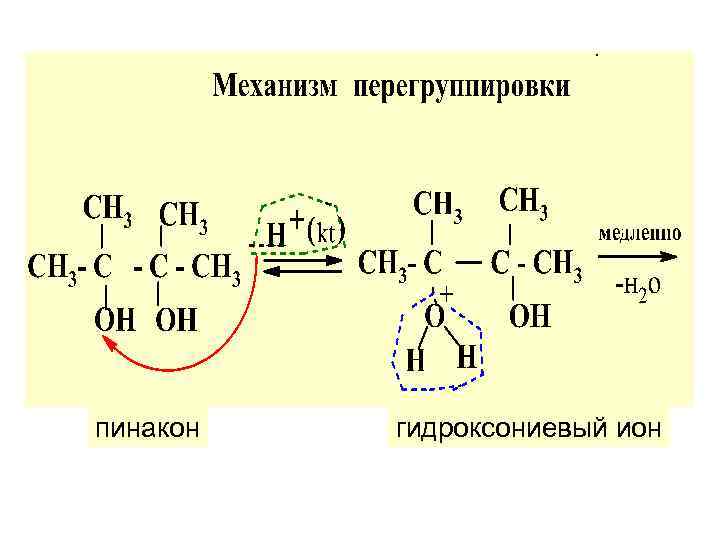 пинакон гидроксониевый ион
пинакон гидроксониевый ион
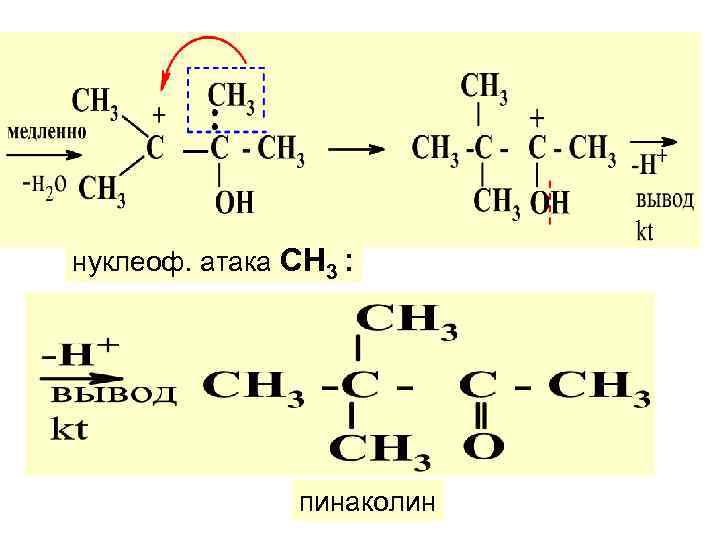 нуклеоф. атака СН 3 : пинаколин
нуклеоф. атака СН 3 : пинаколин
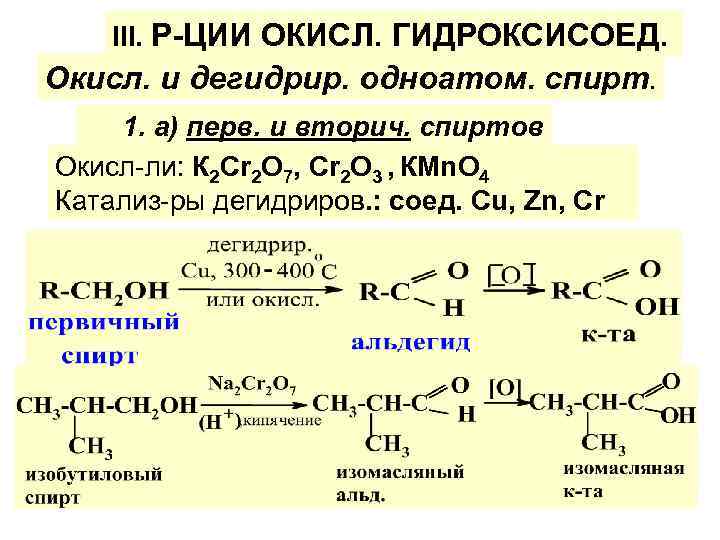 III. Р-ЦИИ ОКИСЛ. ГИДРОКСИСОЕД. Окисл. и дегидрир. одноатом. спирт. 1. а) перв. и вторич. спиртов Окисл-ли: К 2 Сr 2 О 7, Сr 2 О 3 , КМn. О 4 Катализ-ры дегидриров. : соед. Cu, Zn, Cr
III. Р-ЦИИ ОКИСЛ. ГИДРОКСИСОЕД. Окисл. и дегидрир. одноатом. спирт. 1. а) перв. и вторич. спиртов Окисл-ли: К 2 Сr 2 О 7, Сr 2 О 3 , КМn. О 4 Катализ-ры дегидриров. : соед. Cu, Zn, Cr
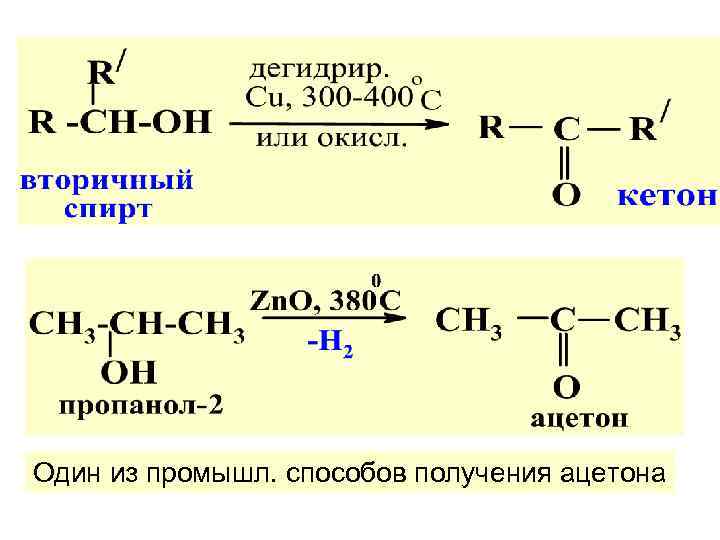 Один из промышл. способов получения ацетона
Один из промышл. способов получения ацетона
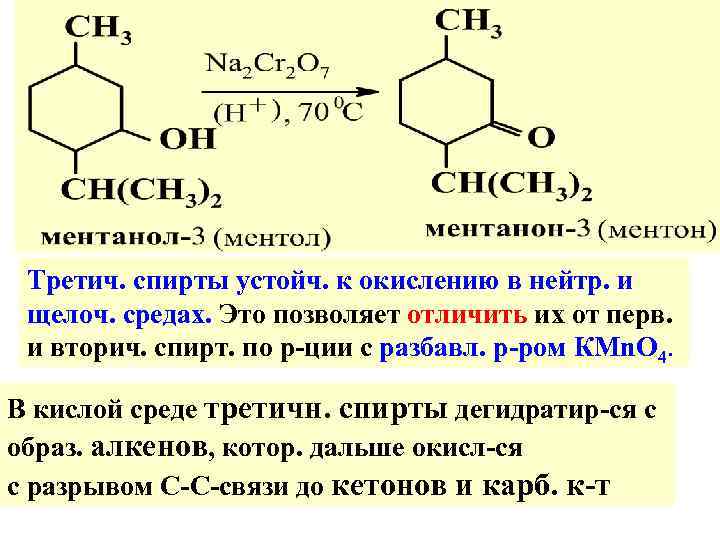 Третич. спирты устойч. к окислению в нейтр. и щелоч. средах. Это позволяет отличить их от перв. и вторич. спирт. по р-ции с разбавл. р-ром КMn. O 4. В кислой среде третичн. спирты дегидратир-ся с образ. алкенов, котор. дальше окисл-ся с разрывом С-С-связи до кетонов и карб. к-т
Третич. спирты устойч. к окислению в нейтр. и щелоч. средах. Это позволяет отличить их от перв. и вторич. спирт. по р-ции с разбавл. р-ром КMn. O 4. В кислой среде третичн. спирты дегидратир-ся с образ. алкенов, котор. дальше окисл-ся с разрывом С-С-связи до кетонов и карб. к-т
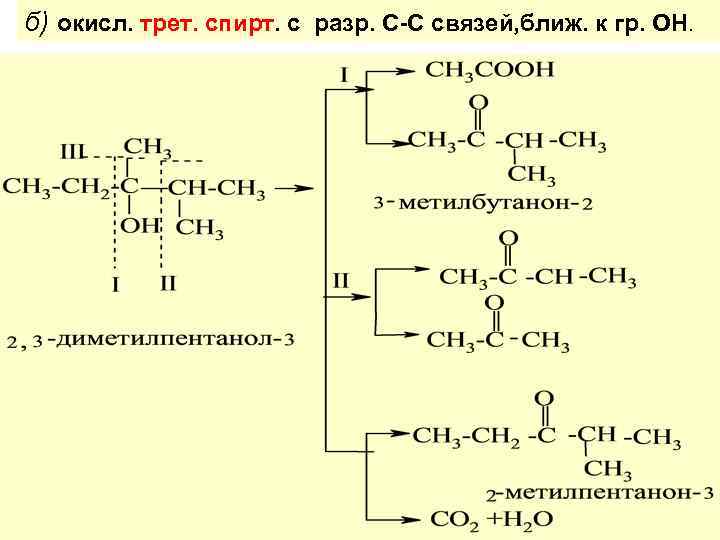 б) окисл. трет. спирт. с разр. С-С связей, ближ. к гр. ОН.
б) окисл. трет. спирт. с разр. С-С связей, ближ. к гр. ОН.
![ОКИСЛЕНИЕ МНОГОАТОМНЫХ СПИРТОВ а) окисл. этиленгликоля [O] ОКИСЛЕНИЕ МНОГОАТОМНЫХ СПИРТОВ а) окисл. этиленгликоля [O]](https://present5.com/presentation/3/-30283012_63980984.pdf-img/-30283012_63980984.pdf-72.jpg) ОКИСЛЕНИЕ МНОГОАТОМНЫХ СПИРТОВ а) окисл. этиленгликоля [O]
ОКИСЛЕНИЕ МНОГОАТОМНЫХ СПИРТОВ а) окисл. этиленгликоля [O]
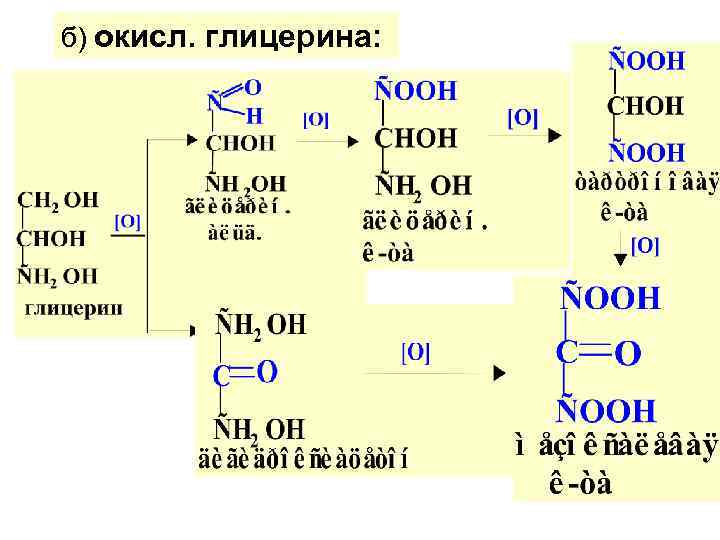 б) окисл. глицерина:
б) окисл. глицерина:
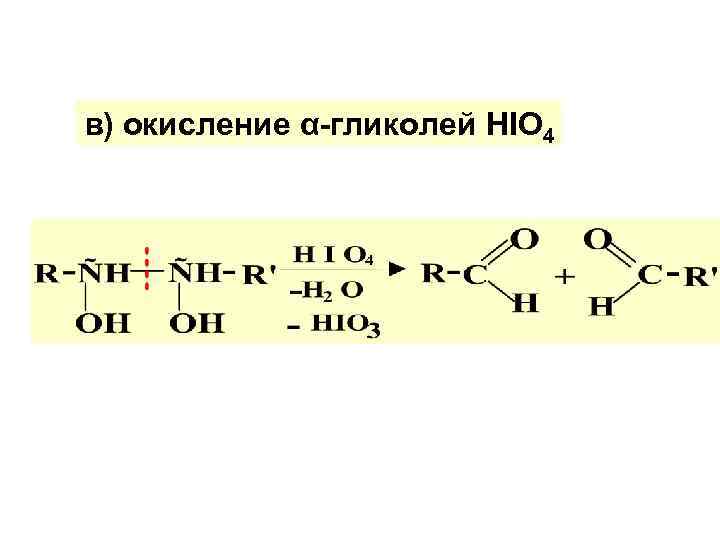 в) окисление α-гликолей HIO 4
в) окисление α-гликолей HIO 4
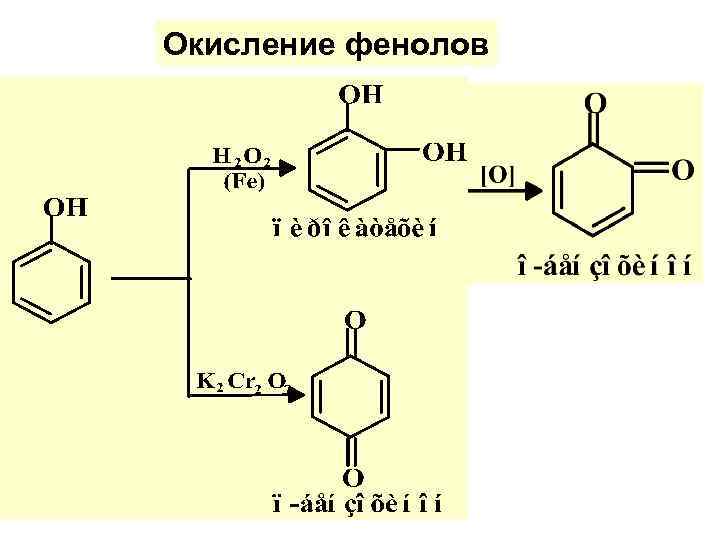 Окисление фенолов
Окисление фенолов
 Понятие о простых эфирах. Общая фор-ла: R-O-R‘ или R- O- Ar Способы получения 1. Межмолек. дегидратац. спиртов (см. спирты) 2. Синтез Вильямсона: взаимодейст. алкоголят. спиртов (R-O-Na) с алкилгалогенид. (R‘-Сl)(см. св-ва спиртов) 3. Присоед. спиртов к ненасыщ. углеводор.
Понятие о простых эфирах. Общая фор-ла: R-O-R‘ или R- O- Ar Способы получения 1. Межмолек. дегидратац. спиртов (см. спирты) 2. Синтез Вильямсона: взаимодейст. алкоголят. спиртов (R-O-Na) с алкилгалогенид. (R‘-Сl)(см. св-ва спиртов) 3. Присоед. спиртов к ненасыщ. углеводор.
 ХИМ. СВ-ВА Простые эфиры- малореакц. соед. , примен-ся как инертные растворители. 1. Прост. эфиры проявл. св-ва оснований (за счет атома своб. пары ē кислорода). Они раствор-ся в холодн. Н 2 SO 4, образуя соли: Соли- нестойк. , легко разлаг. Н 2 О до исх. соед. Это исп-ся для отдел. прост. эф. от алканов.
ХИМ. СВ-ВА Простые эфиры- малореакц. соед. , примен-ся как инертные растворители. 1. Прост. эфиры проявл. св-ва оснований (за счет атома своб. пары ē кислорода). Они раствор-ся в холодн. Н 2 SO 4, образуя соли: Соли- нестойк. , легко разлаг. Н 2 О до исх. соед. Это исп-ся для отдел. прост. эф. от алканов.
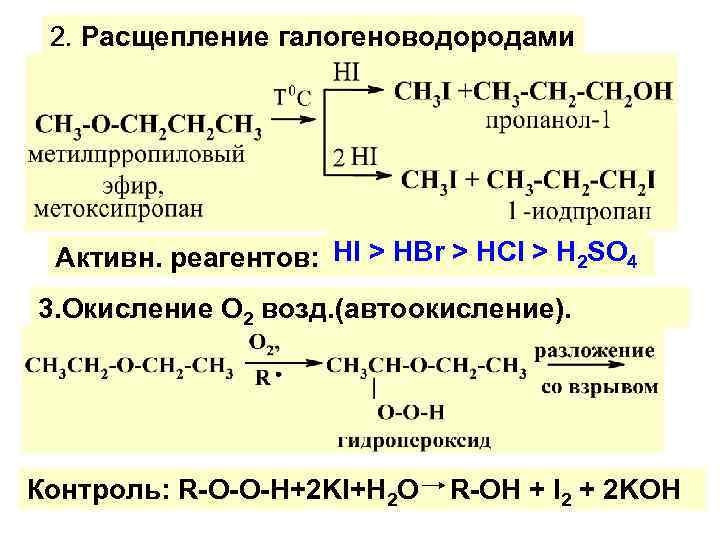 2. Расщепление галогеноводородами Активн. реагентов: НI > НВr > HCl > H 2 SO 4 3. Окисление О 2 возд. (автоокисление). Контроль: R-O-O-H+2 KI+H 2 O R-OH + I 2 + 2 KOH
2. Расщепление галогеноводородами Активн. реагентов: НI > НВr > HCl > H 2 SO 4 3. Окисление О 2 возд. (автоокисление). Контроль: R-O-O-H+2 KI+H 2 O R-OH + I 2 + 2 KOH


