ГИДРОКСИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРОИЗВОДНЫЕ Важнейшие подгруппы: СПИРТЫ














21344-1_spirty_fenoly_tioly.ppt
- Количество слайдов: 42
 ГИДРОКСИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРОИЗВОДНЫЕ Важнейшие подгруппы: СПИРТЫ И ФЕНОЛЫ
ГИДРОКСИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРОИЗВОДНЫЕ Важнейшие подгруппы: СПИРТЫ И ФЕНОЛЫ
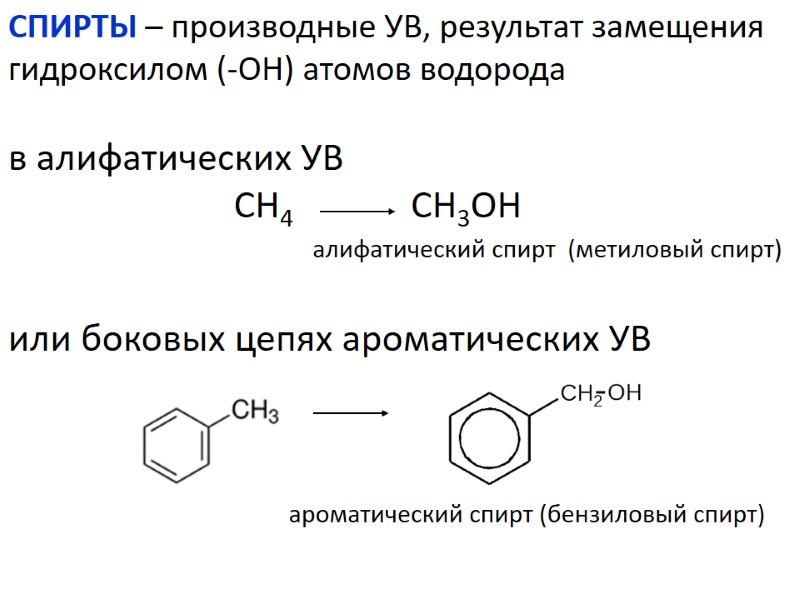
 СПИРТЫ – производные УВ, результат замещения гидроксилом (-ОН) атомов водорода в алифатических УВ СН4 СН3ОН алифатический спирт (метиловый спирт) или боковых цепях ароматических УВ ароматический спирт (бензиловый спирт)
СПИРТЫ – производные УВ, результат замещения гидроксилом (-ОН) атомов водорода в алифатических УВ СН4 СН3ОН алифатический спирт (метиловый спирт) или боковых цепях ароматических УВ ароматический спирт (бензиловый спирт)
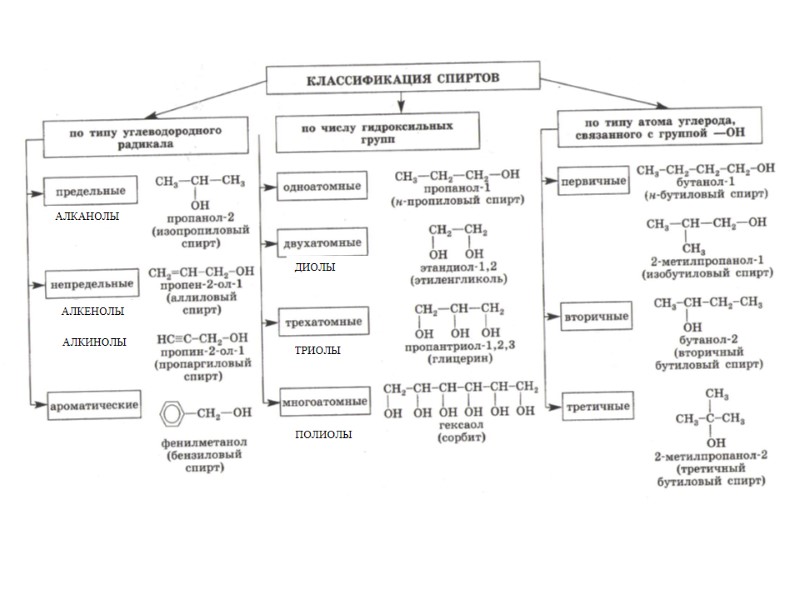
 АЛКАНОЛЫ АЛКЕНОЛЫ АЛКИНОЛЫ ДИОЛЫ ТРИОЛЫ ПОЛИОЛЫ
АЛКАНОЛЫ АЛКЕНОЛЫ АЛКИНОЛЫ ДИОЛЫ ТРИОЛЫ ПОЛИОЛЫ
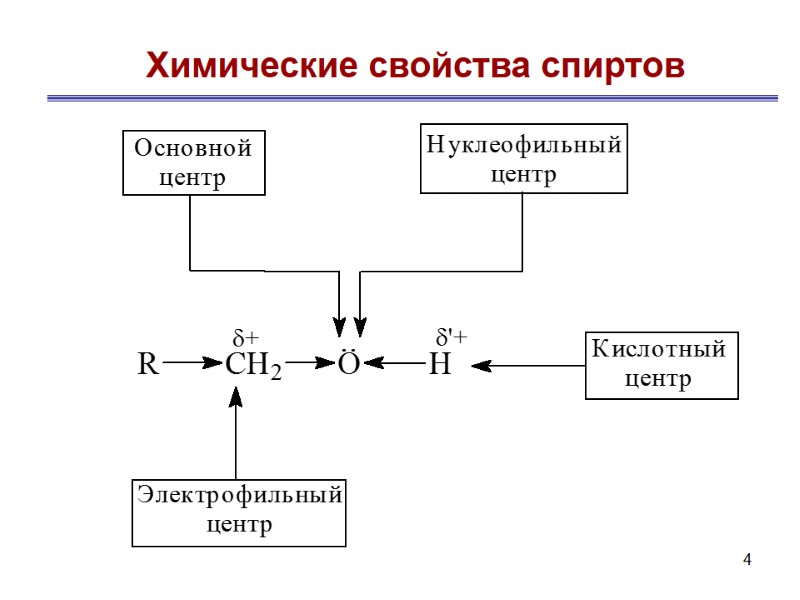
 4 Химические свойства спиртов
4 Химические свойства спиртов
 5 Химические свойства одноатомных спиртов Химические свойства спиртов связаны с наличием в их молекуле группы –ОН. Для спиртов характерны два типа реакций: разрыв связи С-О и связи О-Н. Cпирты взаимодействуют с: 1. Меакт 2. ННal 3. Карбоновыми кислотами 4. NH3 5. РCl5 и SOCl2 6. H2SO4 7. HNO3 8. Подвергаются межмолекулярной и внутримолекулярной дегидратации
5 Химические свойства одноатомных спиртов Химические свойства спиртов связаны с наличием в их молекуле группы –ОН. Для спиртов характерны два типа реакций: разрыв связи С-О и связи О-Н. Cпирты взаимодействуют с: 1. Меакт 2. ННal 3. Карбоновыми кислотами 4. NH3 5. РCl5 и SOCl2 6. H2SO4 7. HNO3 8. Подвергаются межмолекулярной и внутримолекулярной дегидратации
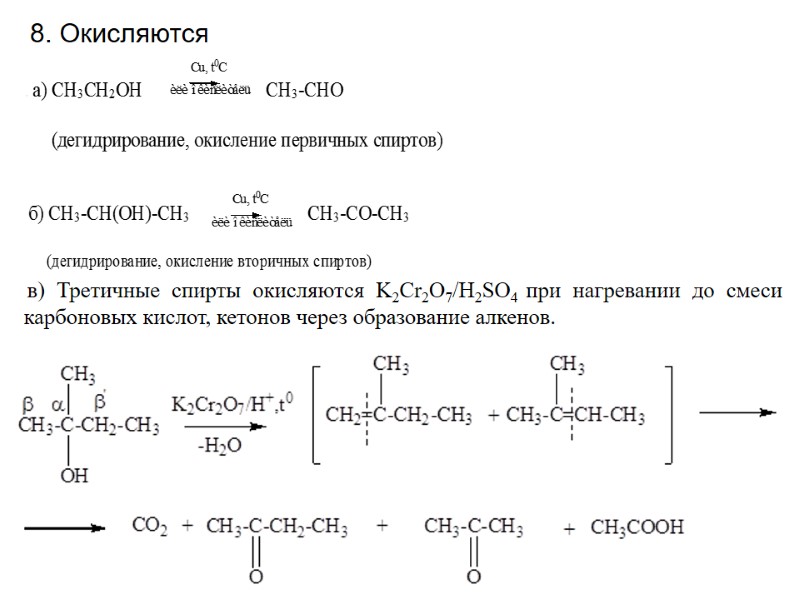
 в) Третичные спирты окисляются K2Cr2O7/H2SO4 при нагревании до смеси карбоновых кислот, кетонов через образование алкенов. 8. Окисляются
в) Третичные спирты окисляются K2Cr2O7/H2SO4 при нагревании до смеси карбоновых кислот, кетонов через образование алкенов. 8. Окисляются
 Окисление спирта в клетке: (дегидрирование) Образование ацетальдегида из этанола катализируется специфическим ферментом алкогольдегидрогеназой, связанной с НАД (кофермент) НАД+ CH3-CH2-OH CH3-CH=O + НАДН+ Н+ Алькогольдегидрогеназа окисляет и метанол до формальдегида (сильный яд) СН3ОН НСН=О +2Н
Окисление спирта в клетке: (дегидрирование) Образование ацетальдегида из этанола катализируется специфическим ферментом алкогольдегидрогеназой, связанной с НАД (кофермент) НАД+ CH3-CH2-OH CH3-CH=O + НАДН+ Н+ Алькогольдегидрогеназа окисляет и метанол до формальдегида (сильный яд) СН3ОН НСН=О +2Н
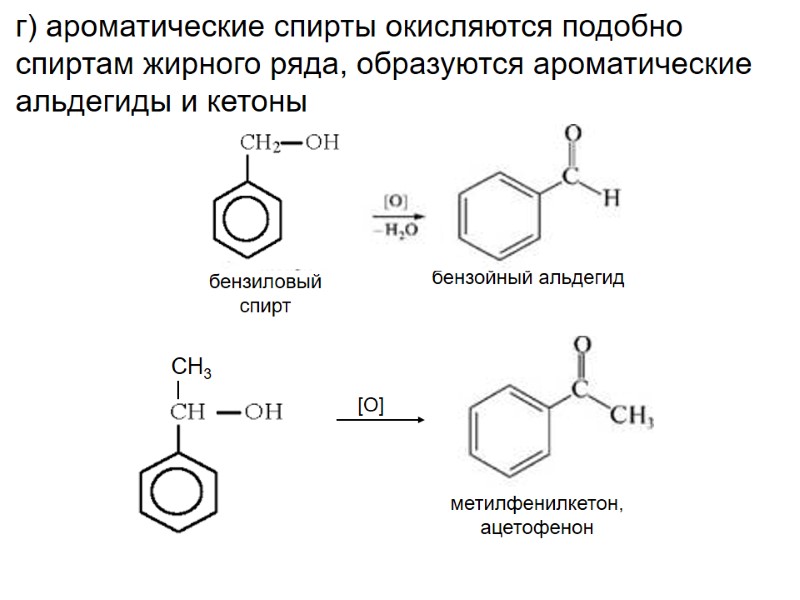
 г) ароматические спирты окисляются подобно спиртам жирного ряда, образуются ароматические альдегиды и кетоны метилфенилкетон, ацетофенон [O] бензойный альдегид
г) ароматические спирты окисляются подобно спиртам жирного ряда, образуются ароматические альдегиды и кетоны метилфенилкетон, ацетофенон [O] бензойный альдегид
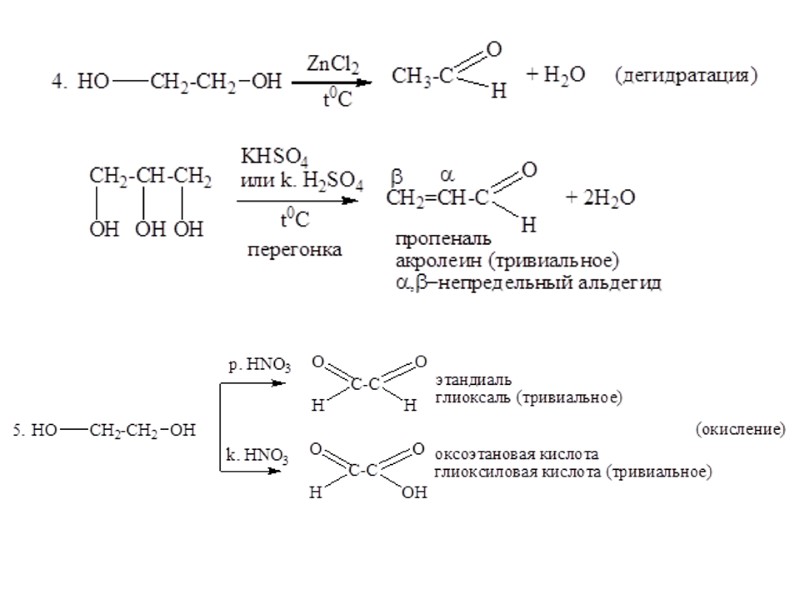
 Дегидратация спиртов 1. Межмолекулярная дегидратация спиртов. При нагревании спирта в присутствии каталитических количеств сильной кислоты происходит отщепление молекулы воды от двух молекул спирта и образуется простой эфир: Простые эфиры — это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода: R'—О—R", где R' и R" — радикалы, которые могут быть различными или одинаковыми. Диэтиловый эфир используется в медицине при хирургических операциях, так как обладает анестезирующим действием. 2. Реакция элиминирования, или внутримолекулярной дегидратации .
Дегидратация спиртов 1. Межмолекулярная дегидратация спиртов. При нагревании спирта в присутствии каталитических количеств сильной кислоты происходит отщепление молекулы воды от двух молекул спирта и образуется простой эфир: Простые эфиры — это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода: R'—О—R", где R' и R" — радикалы, которые могут быть различными или одинаковыми. Диэтиловый эфир используется в медицине при хирургических операциях, так как обладает анестезирующим действием. 2. Реакция элиминирования, или внутримолекулярной дегидратации .
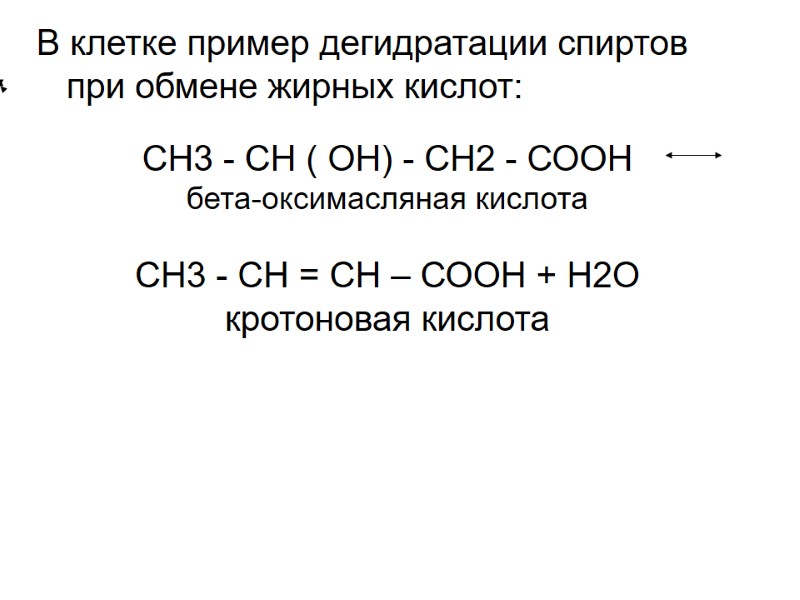
 В клетке пример дегидратации спиртов при обмене жирных кислот: СН3 - СН ( ОН) - СН2 - СООН бета-оксимасляная кислота СН3 - СН = СН – СООН + Н2О кротоновая кислота
В клетке пример дегидратации спиртов при обмене жирных кислот: СН3 - СН ( ОН) - СН2 - СООН бета-оксимасляная кислота СН3 - СН = СН – СООН + Н2О кротоновая кислота
 1-бутилпропаноат и 2-пропилбутаноат. бутиловый эфир пропионовой кислоты, бутилпропионат изопропиловый эфир масляной кислоты, изопропилбутират.
1-бутилпропаноат и 2-пропилбутаноат. бутиловый эфир пропионовой кислоты, бутилпропионат изопропиловый эфир масляной кислоты, изопропилбутират.
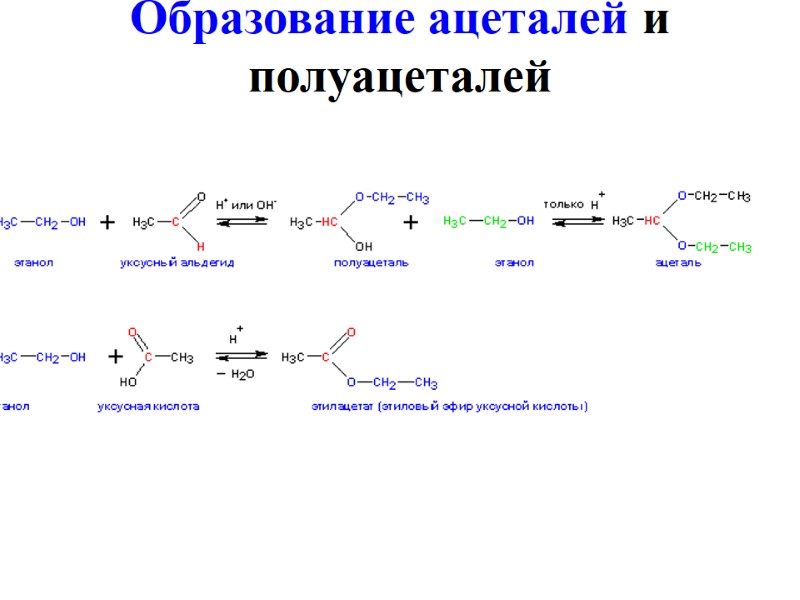
 Образование ацеталей и полуацеталей
Образование ацеталей и полуацеталей
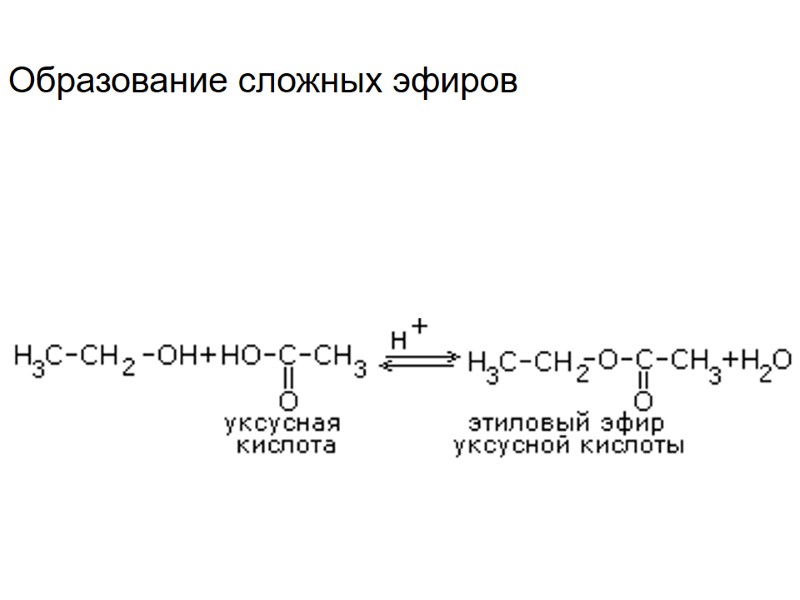
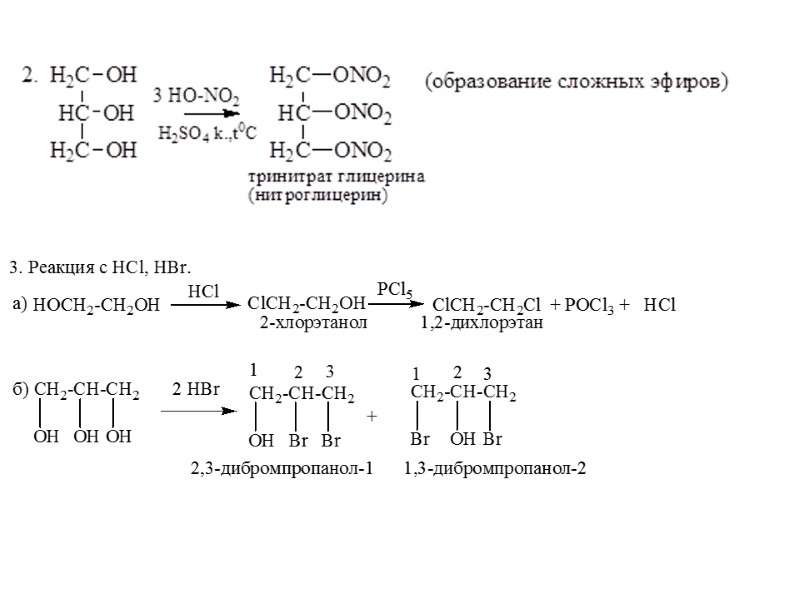
 Образование сложных эфиров
Образование сложных эфиров
 14 Химические свойства многоатомных спиртов 1. Многоатомные спирты более сильные кислоты, чем одноатомные спирты. Гликоли и глицерины образуют алкоголяты, аналогично одноатомным спиртам. Отличительным свойством является образование соединений типа хелатов с ионами тяжелых металлов. С Cu(ОН)2 образуется раствор ярко-синего цвета (качественная реакция).
14 Химические свойства многоатомных спиртов 1. Многоатомные спирты более сильные кислоты, чем одноатомные спирты. Гликоли и глицерины образуют алкоголяты, аналогично одноатомным спиртам. Отличительным свойством является образование соединений типа хелатов с ионами тяжелых металлов. С Cu(ОН)2 образуется раствор ярко-синего цвета (качественная реакция).


 Отдельные представители Метанол (метиловый спирт). Принятие внутрь вызывает опьянение и тяжелое отравление, потерю зрения и часто смерть. Этанол (этиловый спирт). Обеззараживающее средство. В небольших дозах действует опьяняюще, при больших количествах вызывает состояние близкое к наркозу, иногда заканчивающееся смертью.
Отдельные представители Метанол (метиловый спирт). Принятие внутрь вызывает опьянение и тяжелое отравление, потерю зрения и часто смерть. Этанол (этиловый спирт). Обеззараживающее средство. В небольших дозах действует опьяняюще, при больших количествах вызывает состояние близкое к наркозу, иногда заканчивающееся смертью.

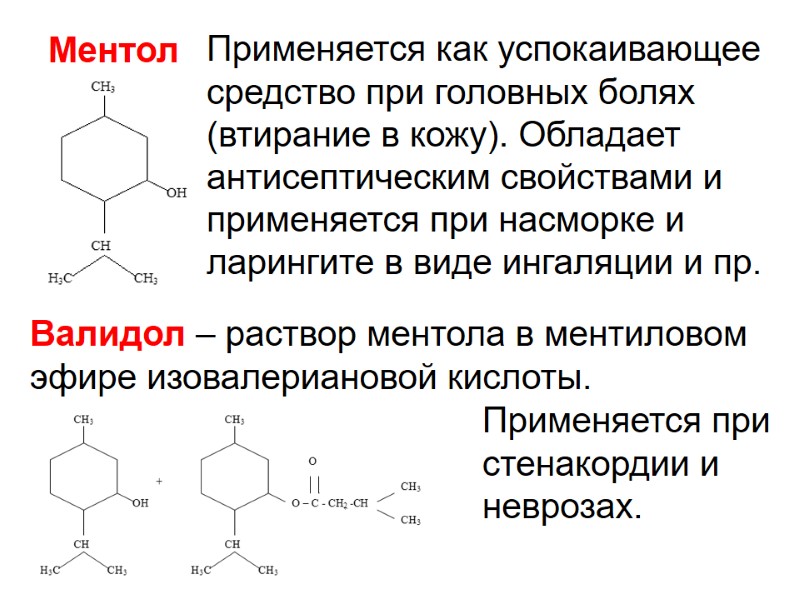
 Ментол Применяется как успокаивающее средство при головных болях (втирание в кожу). Обладает антисептическим свойствами и применяется при насморке и ларингите в виде ингаляции и пр. Валидол – раствор ментола в ментиловом эфире изовалериановой кислоты. Применяется при стенакордии и неврозах.
Ментол Применяется как успокаивающее средство при головных болях (втирание в кожу). Обладает антисептическим свойствами и применяется при насморке и ларингите в виде ингаляции и пр. Валидол – раствор ментола в ментиловом эфире изовалериановой кислоты. Применяется при стенакордии и неврозах.
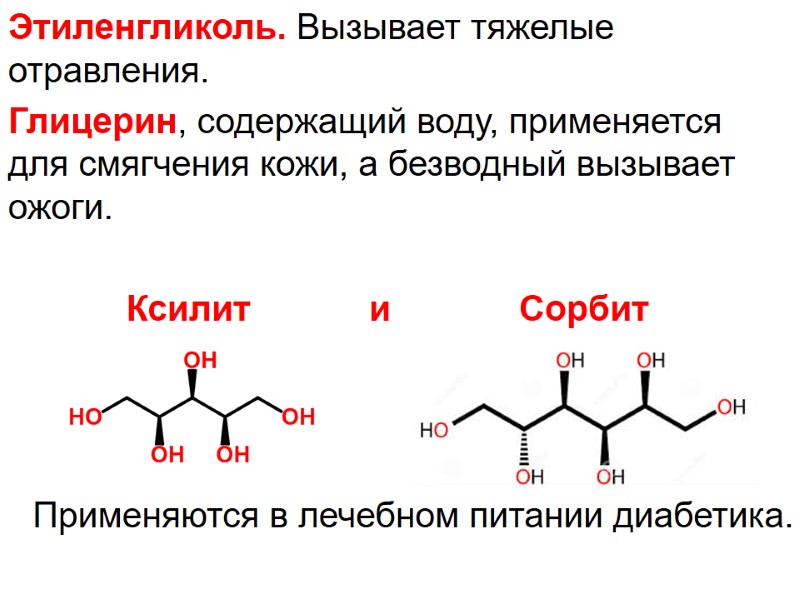
 Этиленгликоль. Вызывает тяжелые отравления. Глицерин, содержащий воду, применяется для смягчения кожи, а безводный вызывает ожоги. Ксилит и Сорбит Применяются в лечебном питании диабетика.
Этиленгликоль. Вызывает тяжелые отравления. Глицерин, содержащий воду, применяется для смягчения кожи, а безводный вызывает ожоги. Ксилит и Сорбит Применяются в лечебном питании диабетика.
 ОКСИСОЕДИНЕНИЯ ФЕНОЛЫ
ОКСИСОЕДИНЕНИЯ ФЕНОЛЫ
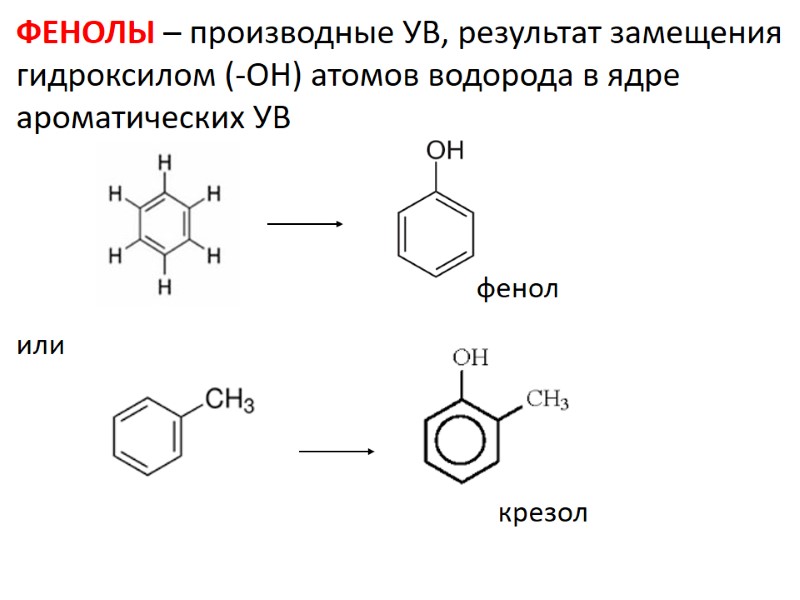
 ФЕНОЛЫ – производные УВ, результат замещения гидроксилом (-ОН) атомов водорода в ядре ароматических УВ фенол или крезол
ФЕНОЛЫ – производные УВ, результат замещения гидроксилом (-ОН) атомов водорода в ядре ароматических УВ фенол или крезол
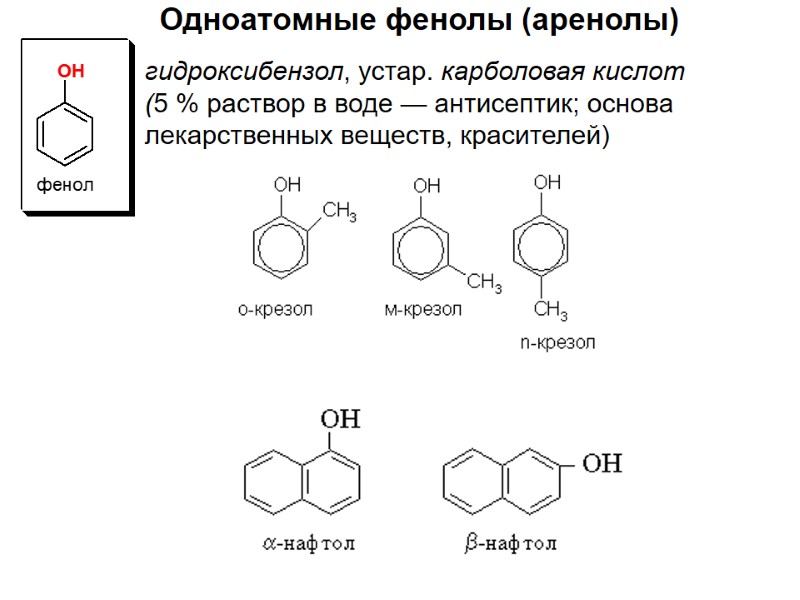
 гидроксибензол, устар. карболовая кислот (5 % раствор в воде — антисептик; основа лекарственных веществ, красителей) Одноатомные фенолы (аренолы)
гидроксибензол, устар. карболовая кислот (5 % раствор в воде — антисептик; основа лекарственных веществ, красителей) Одноатомные фенолы (аренолы)


 26 Гидроксильная группа – ориентант I рода, облегчает реакции по бензольному кольцу, направляя атаку электрофильного реагента в орто-, пара-положения. хинон ацилирования
26 Гидроксильная группа – ориентант I рода, облегчает реакции по бензольному кольцу, направляя атаку электрофильного реагента в орто-, пара-положения. хинон ацилирования
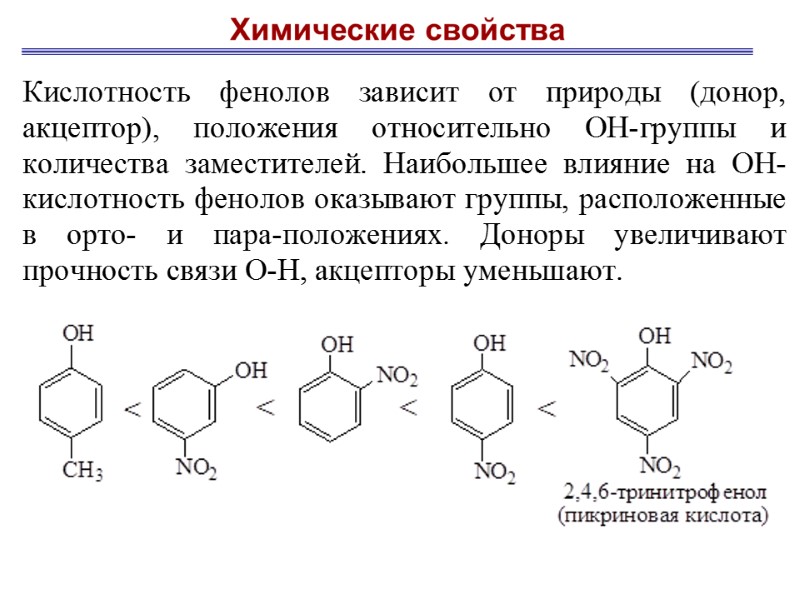
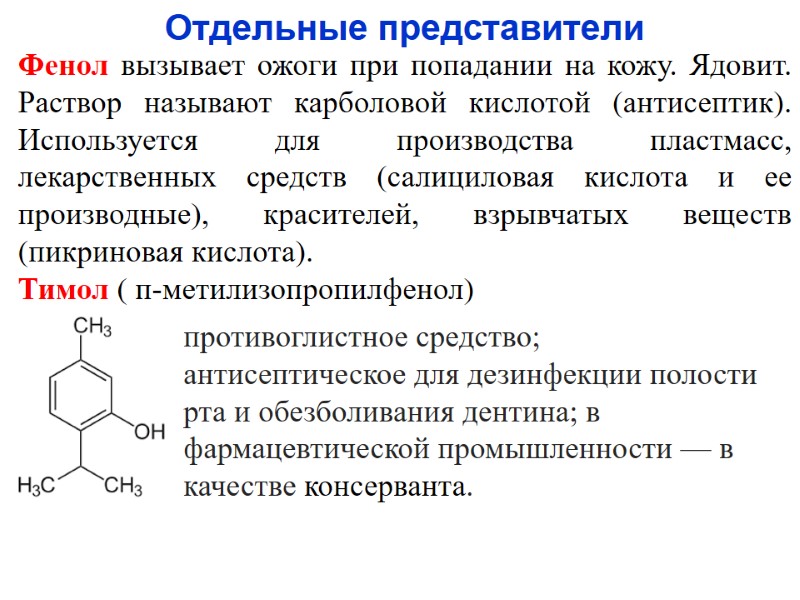
 Отдельные представители Фенол вызывает ожоги при попадании на кожу. Ядовит. Раствор называют карболовой кислотой (антисептик). Используется для производства пластмасс, лекарственных средств (салициловая кислота и ее производные), красителей, взрывчатых веществ (пикриновая кислота). Тимол ( п-метилизопропилфенол) противоглистное средство; антисептическое для дезинфекции полости рта и обезболивания дентина; в фармацевтической промышленности — в качестве консерванта.
Отдельные представители Фенол вызывает ожоги при попадании на кожу. Ядовит. Раствор называют карболовой кислотой (антисептик). Используется для производства пластмасс, лекарственных средств (салициловая кислота и ее производные), красителей, взрывчатых веществ (пикриновая кислота). Тимол ( п-метилизопропилфенол) противоглистное средство; антисептическое для дезинфекции полости рта и обезболивания дентина; в фармацевтической промышленности — в качестве консерванта.
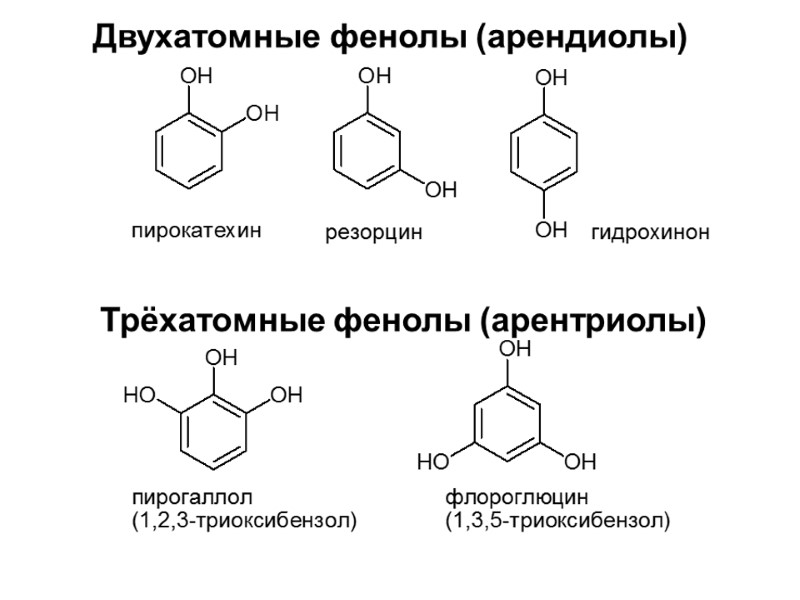
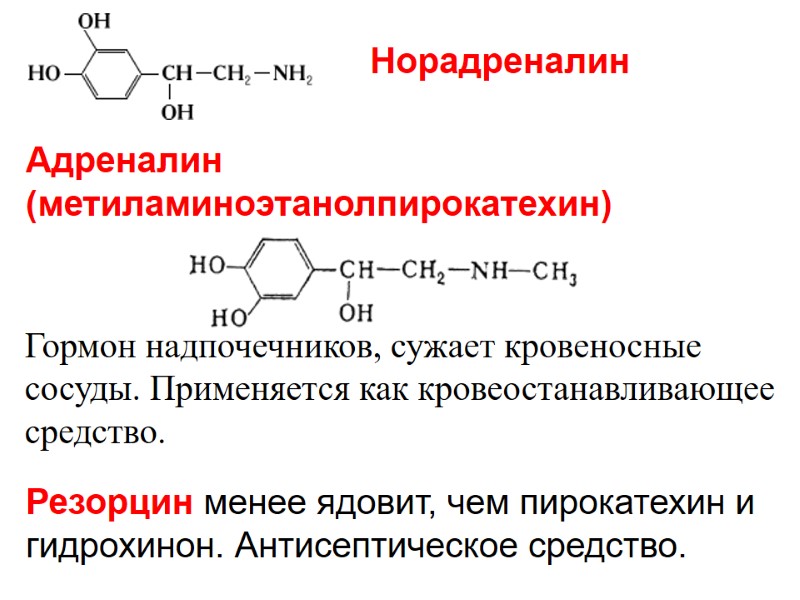
 Адреналин (метиламиноэтанолпирокатехин) Гормон надпочечников, сужает кровеносные сосуды. Применяется как кровеостанавливающее средство. Резорцин менее ядовит, чем пирокатехин и гидрохинон. Антисептическое средство. Норадреналин
Адреналин (метиламиноэтанолпирокатехин) Гормон надпочечников, сужает кровеносные сосуды. Применяется как кровеостанавливающее средство. Резорцин менее ядовит, чем пирокатехин и гидрохинон. Антисептическое средство. Норадреналин
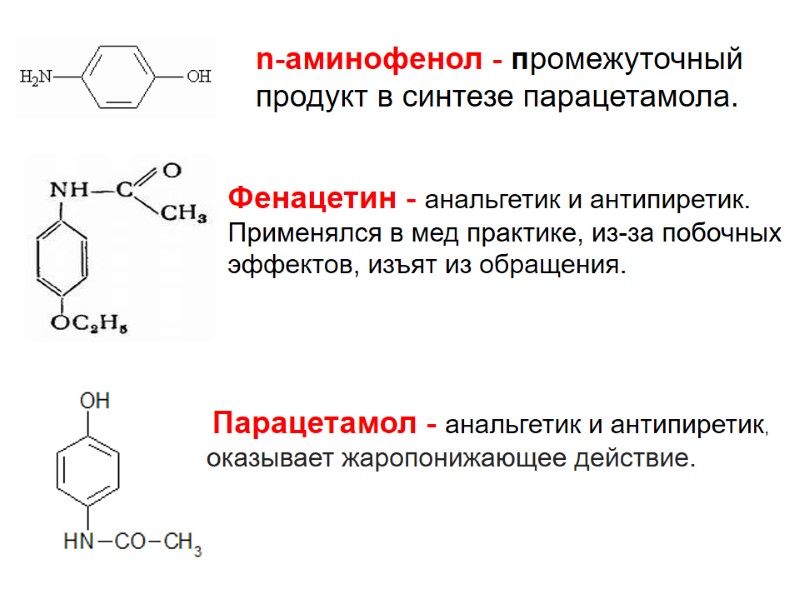
 n-аминофенол - промежуточный продукт в синтезе парацетамола. Парацетамол - анальгетик и антипиретик, оказывает жаропонижающее действие. Фенацетин - анальгетик и антипиретик. Применялся в мед практике, из-за побочных эффектов, изъят из обращения.
n-аминофенол - промежуточный продукт в синтезе парацетамола. Парацетамол - анальгетик и антипиретик, оказывает жаропонижающее действие. Фенацетин - анальгетик и антипиретик. Применялся в мед практике, из-за побочных эффектов, изъят из обращения.
 ТИОЛЫ
ТИОЛЫ
 ХИМИЧЕСКИЕ СВОЙСТВА Тиолы проявляют слабые кислотные свойства (на 5-6 порядков больше, чем у спиртов) С2Н5SH + Na = C2H5SNa + H2O 2. С2Н5SH + NaOH = C2H5SNa + H2O 3. С2Н5SH + HgO = (C2H5S)2Hg + H2O 4. С2Н5SH + HgCl2 = (C2H5 S)2Hg + H2 O этантиолят натрия этантиол (этилмеркаптан) этантиолят ртути (II) ТИОЛЫ (меркаптаны) R – SH - сернистые аналоги спиртов (производные сероводорода).
ХИМИЧЕСКИЕ СВОЙСТВА Тиолы проявляют слабые кислотные свойства (на 5-6 порядков больше, чем у спиртов) С2Н5SH + Na = C2H5SNa + H2O 2. С2Н5SH + NaOH = C2H5SNa + H2O 3. С2Н5SH + HgO = (C2H5S)2Hg + H2O 4. С2Н5SH + HgCl2 = (C2H5 S)2Hg + H2 O этантиолят натрия этантиол (этилмеркаптан) этантиолят ртути (II) ТИОЛЫ (меркаптаны) R – SH - сернистые аналоги спиртов (производные сероводорода).
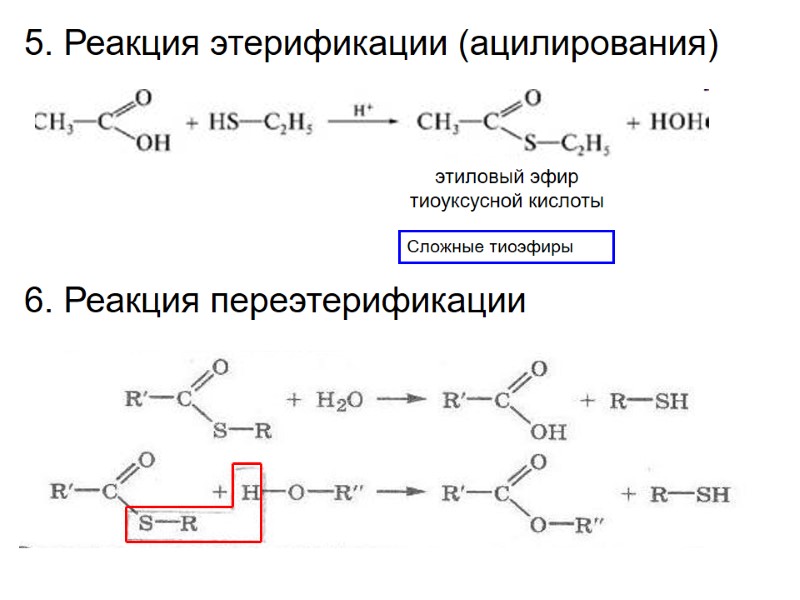
 5. Реакция этерификации (ацилирования) Сложные тиоэфиры этиловый эфир тиоуксусной кислоты 6. Реакция переэтерификации
5. Реакция этерификации (ацилирования) Сложные тиоэфиры этиловый эфир тиоуксусной кислоты 6. Реакция переэтерификации
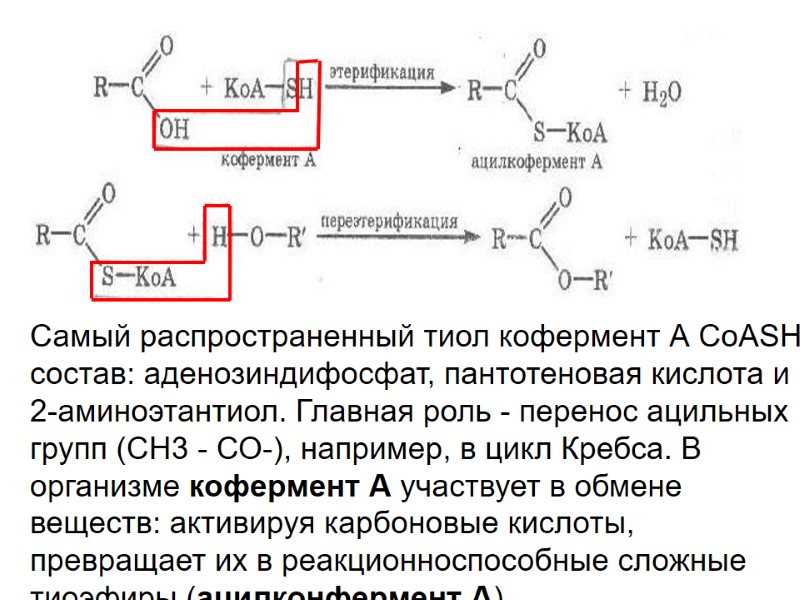
 Самый распространенный тиол кофермент А СоАSH состав: аденозиндифосфат, пантотеновая кислота и 2-аминоэтантиол. Главная роль - перенос ацильных групп (СН3 - СО-), например, в цикл Кребса. В организме кофермент А участвует в обмене веществ: активируя карбоновые кислоты, превращает их в реакционноспособные сложные тиоэфиры (ацилконфермент А).
Самый распространенный тиол кофермент А СоАSH состав: аденозиндифосфат, пантотеновая кислота и 2-аминоэтантиол. Главная роль - перенос ацильных групп (СН3 - СО-), например, в цикл Кребса. В организме кофермент А участвует в обмене веществ: активируя карбоновые кислоты, превращает их в реакционноспособные сложные тиоэфиры (ацилконфермент А).
 7. Окислительно-восстановительные реакции. Тиолы сильные восстановители. 2RSH R – S – S –R + 2H+ окисление восстановление Дисульфид Тиол Тиол-дисульфидная система – сопряженная окислительно-восстановительная пара. Используется для поддержания Ox/Red гомеостата в организме и в работе антиоксидантной системы.
7. Окислительно-восстановительные реакции. Тиолы сильные восстановители. 2RSH R – S – S –R + 2H+ окисление восстановление Дисульфид Тиол Тиол-дисульфидная система – сопряженная окислительно-восстановительная пара. Используется для поддержания Ox/Red гомеостата в организме и в работе антиоксидантной системы.
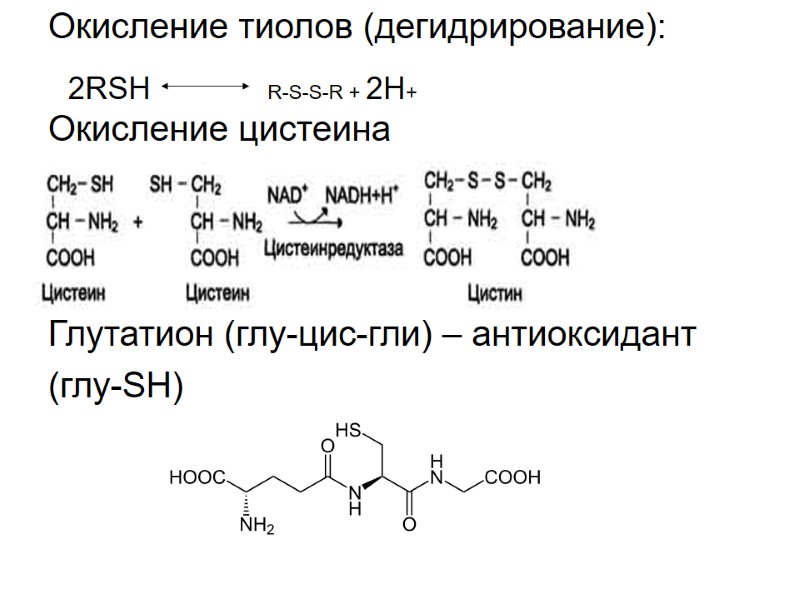
 Окисление тиолов (дегидрирование): Окисление цистеина Глутатион (глу-цис-гли) – антиоксидант (глу-SH) 2RSH R-S-S-R + 2H+
Окисление тиолов (дегидрирование): Окисление цистеина Глутатион (глу-цис-гли) – антиоксидант (глу-SH) 2RSH R-S-S-R + 2H+
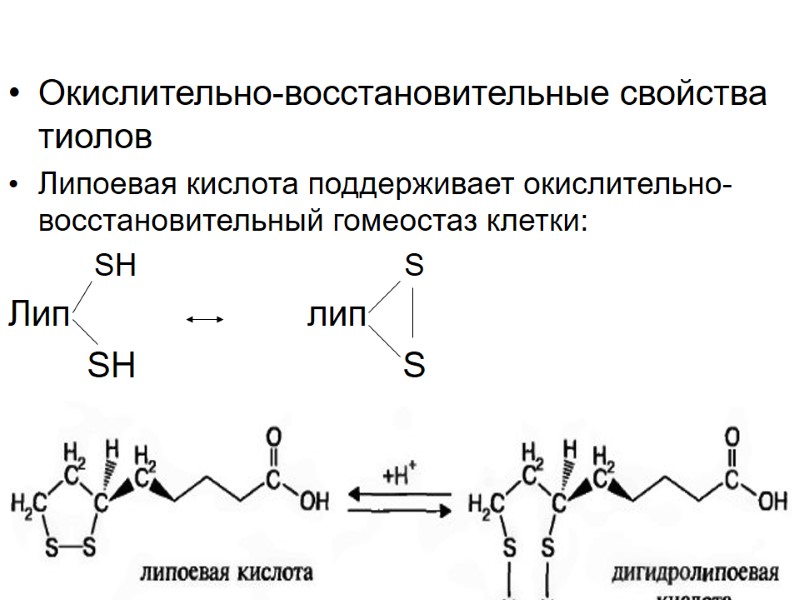
 Окислительно-восстановительные свойства тиолов Липоевая кислота поддерживает окислительно-восстановительный гомеостаз клетки: SH S Лип лип SH S
Окислительно-восстановительные свойства тиолов Липоевая кислота поддерживает окислительно-восстановительный гомеостаз клетки: SH S Лип лип SH S
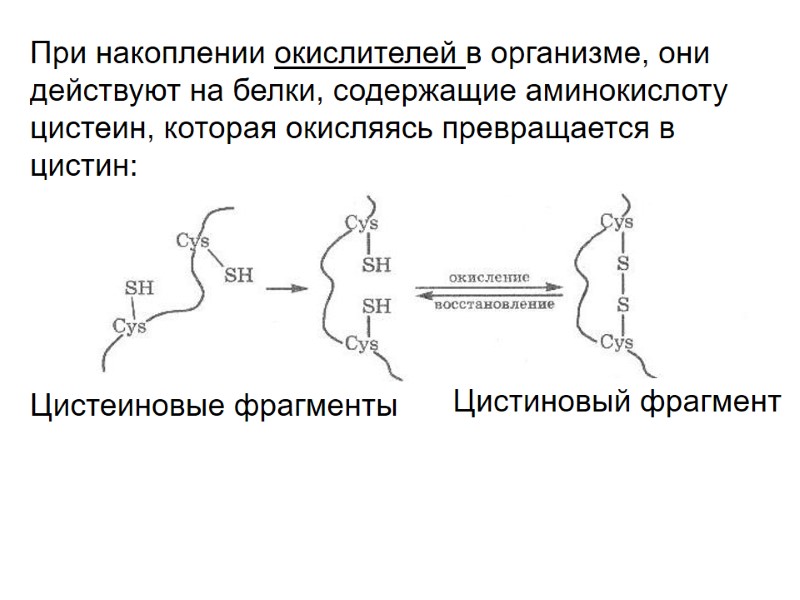
 При накоплении окислителей в организме, они действуют на белки, содержащие аминокислоту цистеин, которая окисляясь превращается в цистин: Цистеиновые фрагменты Цистиновый фрагмент
При накоплении окислителей в организме, они действуют на белки, содержащие аминокислоту цистеин, которая окисляясь превращается в цистин: Цистеиновые фрагменты Цистиновый фрагмент
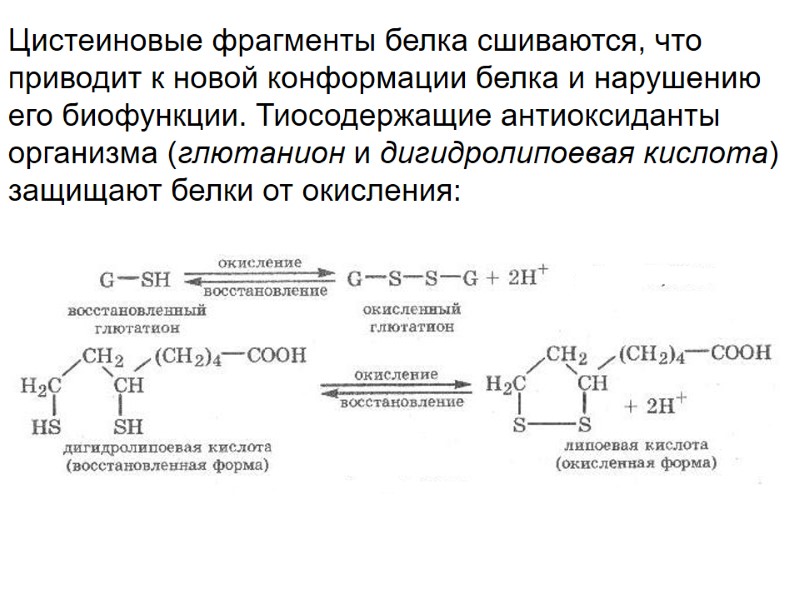
 Цистеиновые фрагменты белка сшиваются, что приводит к новой конформации белка и нарушению его биофункции. Тиосодержащие антиоксиданты организма (глютанион и дигидролипоевая кислота) защищают белки от окисления:
Цистеиновые фрагменты белка сшиваются, что приводит к новой конформации белка и нарушению его биофункции. Тиосодержащие антиоксиданты организма (глютанион и дигидролипоевая кислота) защищают белки от окисления:
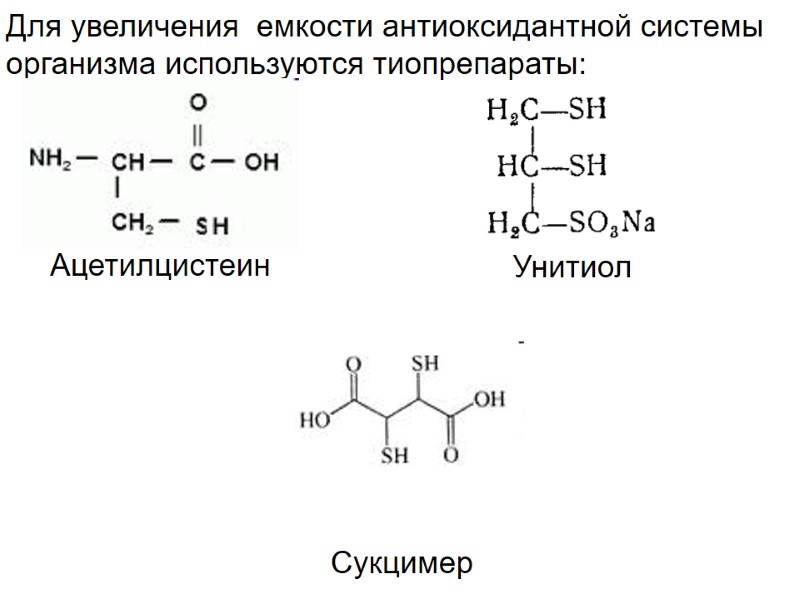
 Для увеличения емкости антиоксидантной системы организма используются тиопрепараты: Сукцимер Унитиол Ацетилцистеин
Для увеличения емкости антиоксидантной системы организма используются тиопрепараты: Сукцимер Унитиол Ацетилцистеин
 Эти же препараты являются антидотами металлов-токсикантов, а также отравляющего вещества люизит (схожее с ипритом действие).
Эти же препараты являются антидотами металлов-токсикантов, а также отравляющего вещества люизит (схожее с ипритом действие).
 Нарушение окислительно-восстановительного гомеостаза наблюдается при радиоактивном облучении. Для предотвращения тяжелых последствий используют радиопротекторы (вещества, смягчающие последствия радиации), например меркамин (аминотиол) меркамин цистамин
Нарушение окислительно-восстановительного гомеостаза наблюдается при радиоактивном облучении. Для предотвращения тяжелых последствий используют радиопротекторы (вещества, смягчающие последствия радиации), например меркамин (аминотиол) меркамин цистамин
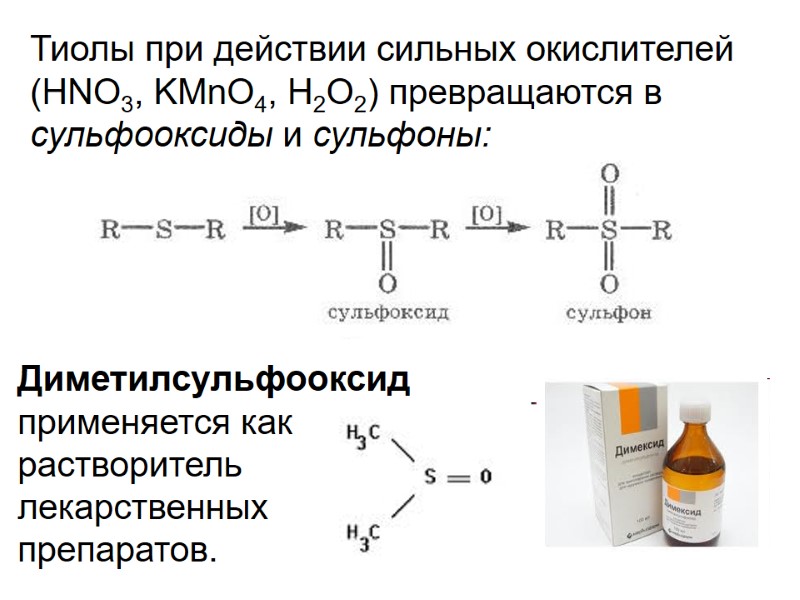
 Тиолы при действии сильных окислителей (HNO3, KMnO4, H2O2) превращаются в сульфооксиды и сульфоны: Диметилсульфооксид применяется как растворитель лекарственных препаратов.
Тиолы при действии сильных окислителей (HNO3, KMnO4, H2O2) превращаются в сульфооксиды и сульфоны: Диметилсульфооксид применяется как растворитель лекарственных препаратов.

