ГИДРОКСИКИСЛОТЫ (Г/К) Функц. группы Г/К : ОН и








![Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина](https://present5.com/presentacii-2/20171208\15614-5_gidroksik-t_oksok-ty_prezentatsii.ppt\15614-5_gidroksik-t_oksok-ty_prezentatsii_34.jpg)















15614-5_gidroksik-t_oksok-ty_prezentatsii.ppt
- Количество слайдов: 71
 ГИДРОКСИКИСЛОТЫ (Г/К) Функц. группы Г/К : ОН и СООН (старшая) Классификация 1) по у/в скелету: алифат.; аромат., циклич. 2) по кол-ву СООН –групп: моно-, ди- или трикарбоновые к-ты; По взаимн. располож. функц. гр.: различ. α-, β-, γ-, δ- г/к. 3) по кол-ву ОН-гр.: ди-, три- , тетраГ/К.
ГИДРОКСИКИСЛОТЫ (Г/К) Функц. группы Г/К : ОН и СООН (старшая) Классификация 1) по у/в скелету: алифат.; аромат., циклич. 2) по кол-ву СООН –групп: моно-, ди- или трикарбоновые к-ты; По взаимн. располож. функц. гр.: различ. α-, β-, γ-, δ- г/к. 3) по кол-ву ОН-гр.: ди-, три- , тетраГ/К.
 НОМЕНКЛАТУРА Системат. назв. Г/К : выбор главн. цепи и начало ее нумерации определ. старшая функц. гр. СООН Часто предпочтит. явл-ся тривиал. назв
НОМЕНКЛАТУРА Системат. назв. Г/К : выбор главн. цепи и начало ее нумерации определ. старшая функц. гр. СООН Часто предпочтит. явл-ся тривиал. назв
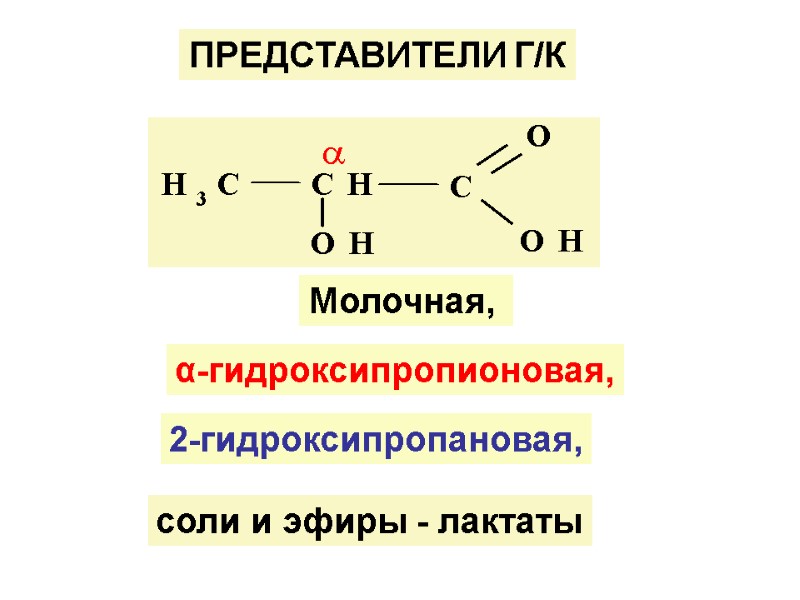
 ПРЕДСТАВИТЕЛИ Г/К соли и эфиры - лактаты Молочная, 2-гидроксипропановая, α-гидроксипропионовая,
ПРЕДСТАВИТЕЛИ Г/К соли и эфиры - лактаты Молочная, 2-гидроксипропановая, α-гидроксипропионовая,
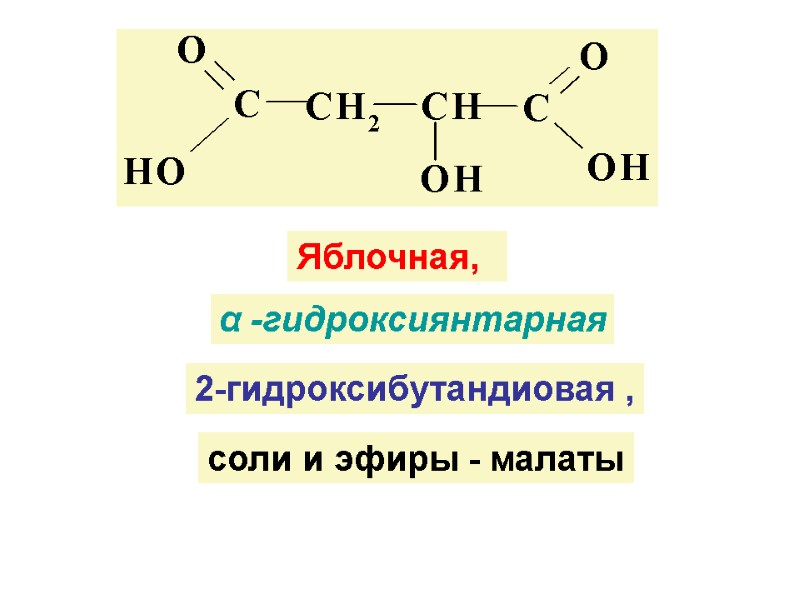
 Яблочная, 2-гидроксибутандиовая , α -гидроксиянтарная соли и эфиры - малаты
Яблочная, 2-гидроксибутандиовая , α -гидроксиянтарная соли и эфиры - малаты
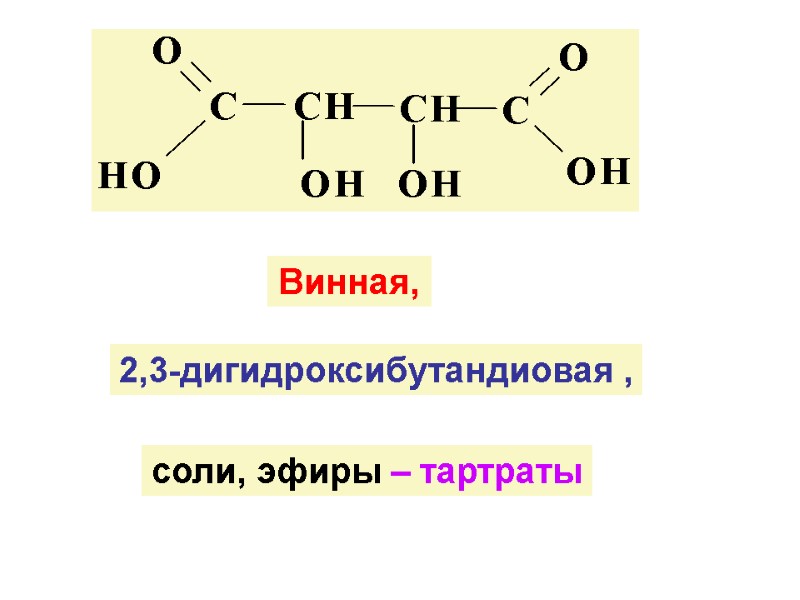
 Винная, 2,3-дигидроксибутандиовая , соли, эфиры – тартраты
Винная, 2,3-дигидроксибутандиовая , соли, эфиры – тартраты
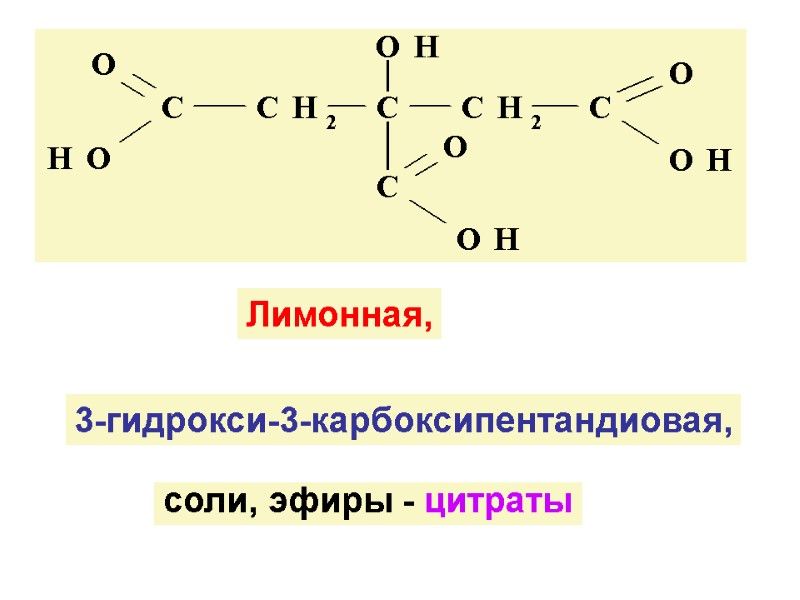
 Лимонная, 3-гидрокси-3-карбоксипентандиовая, соли, эфиры - цитраты
Лимонная, 3-гидрокси-3-карбоксипентандиовая, соли, эфиры - цитраты
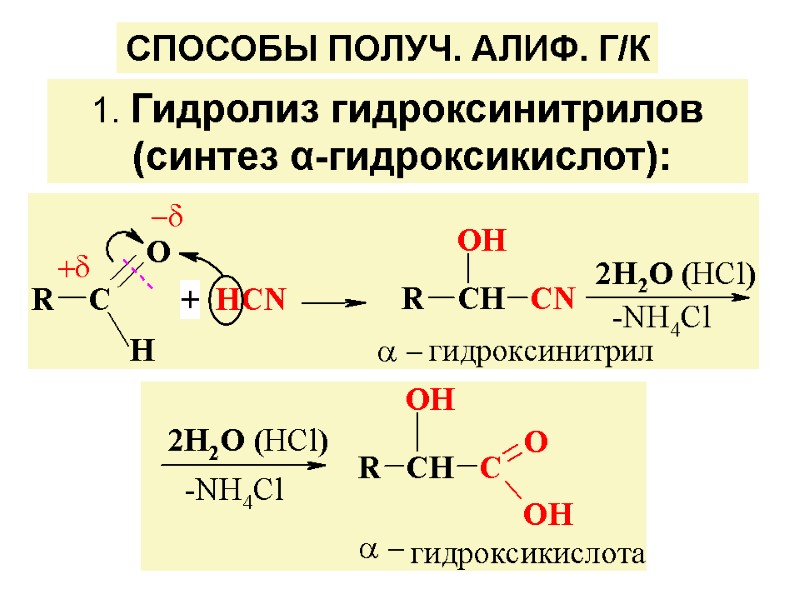
 1. Гидролиз гидроксинитрилов (синтез α-гидроксикислот): СПОСОБЫ ПОЛУЧ. АЛИФ. Г/К
1. Гидролиз гидроксинитрилов (синтез α-гидроксикислот): СПОСОБЫ ПОЛУЧ. АЛИФ. Г/К
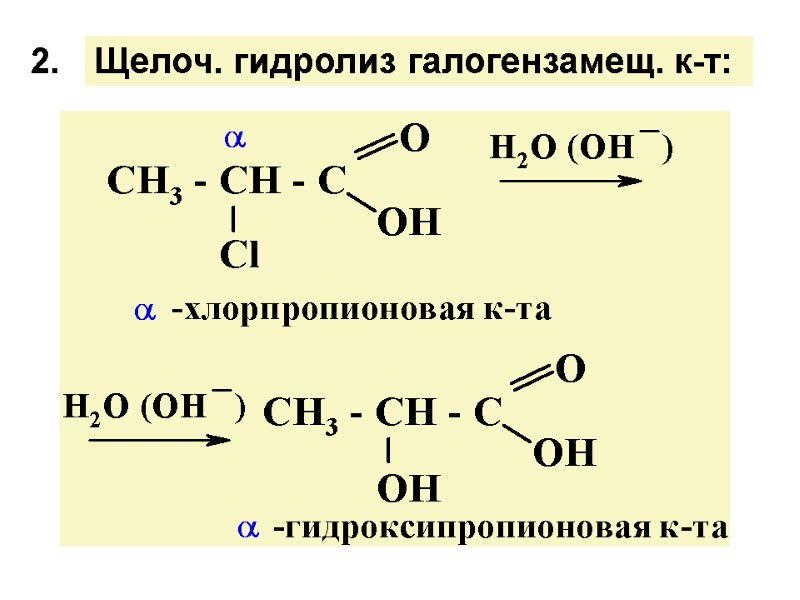
 2. Щелоч. гидролиз галогензамещ. к-т:
2. Щелоч. гидролиз галогензамещ. к-т:
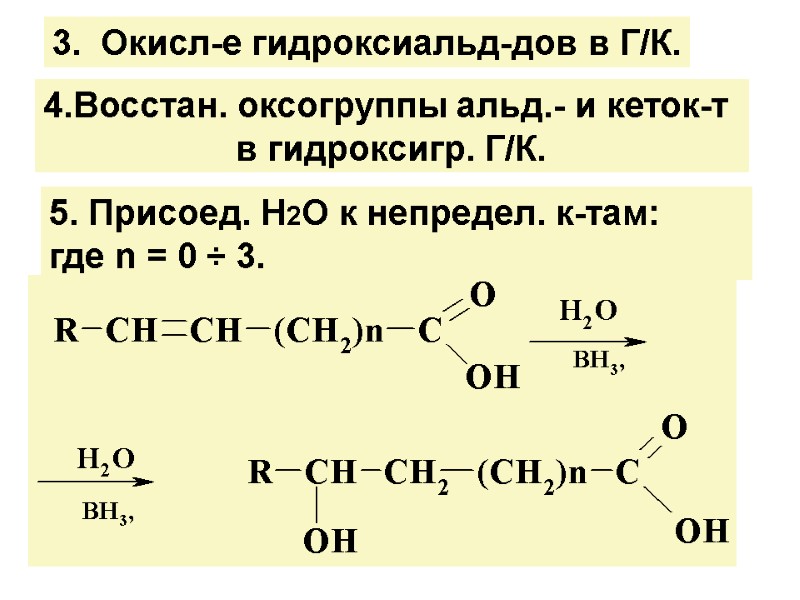
 5. Присоед. Н2О к непредел. к-там: где n = 0 ÷ 3. 3. Окисл-е гидроксиальд-дов в Г/К. 4.Восстан. оксогруппы альд.- и кеток-т в гидроксигр. Г/К.
5. Присоед. Н2О к непредел. к-там: где n = 0 ÷ 3. 3. Окисл-е гидроксиальд-дов в Г/К. 4.Восстан. оксогруппы альд.- и кеток-т в гидроксигр. Г/К.
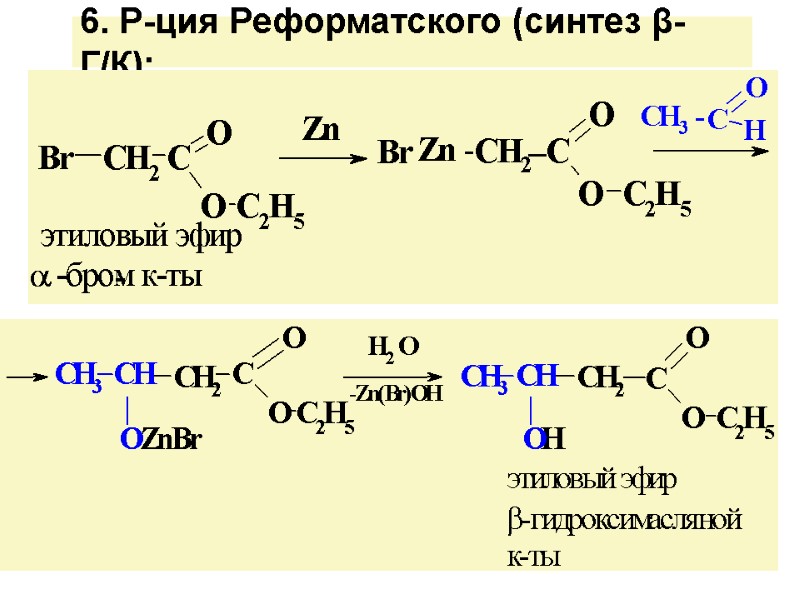
 6. Р-ция Реформатского (синтез β- Г/К):
6. Р-ция Реформатского (синтез β- Г/К):
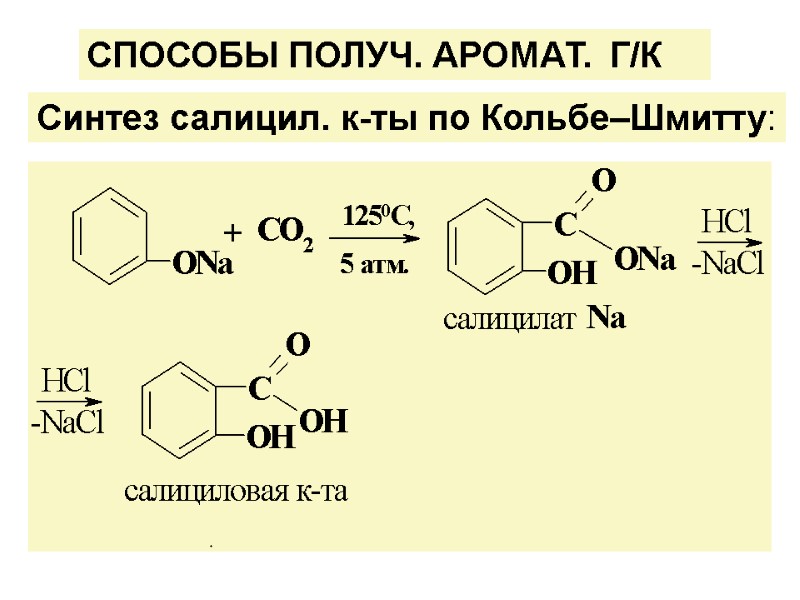
 СПОСОБЫ ПОЛУЧ. АРОМАТ. Г/К Синтез салицил. к-ты по Кольбе–Шмитту:
СПОСОБЫ ПОЛУЧ. АРОМАТ. Г/К Синтез салицил. к-ты по Кольбе–Шмитту:
 по ОН-гр.; по –СООН –гр. обусловл. взаим. полож. функц. гр. ХИМИЧ. СВ-ВА ГИДРОКСИК-Т Хим. св-ва Г/К обусл. принадлежн. одноврем. к спиртам и карб. кисл. и зависят от взаим. располож. функц. гр. Р-ЦИИ Г/К:
по ОН-гр.; по –СООН –гр. обусловл. взаим. полож. функц. гр. ХИМИЧ. СВ-ВА ГИДРОКСИК-Т Хим. св-ва Г/К обусл. принадлежн. одноврем. к спиртам и карб. кисл. и зависят от взаим. располож. функц. гр. Р-ЦИИ Г/К:
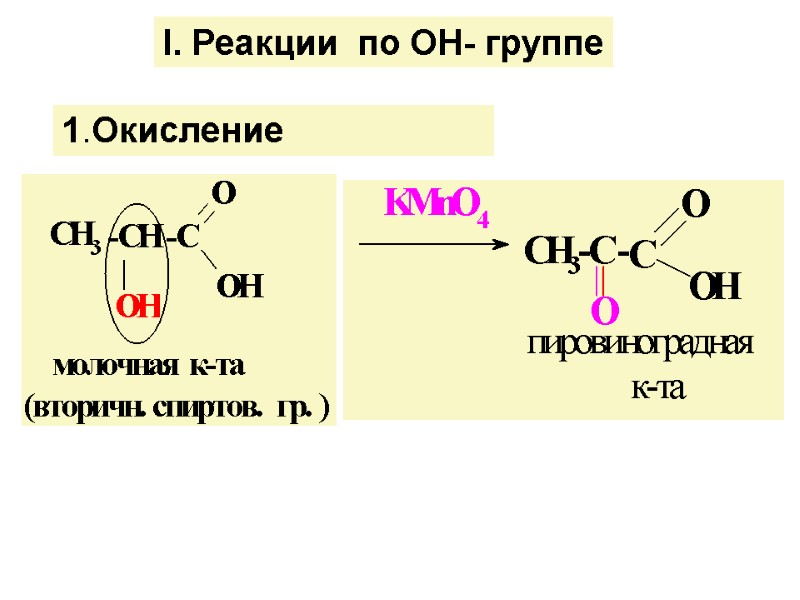
 І. Реакции по ОН- группе 1.Окисление
І. Реакции по ОН- группе 1.Окисление
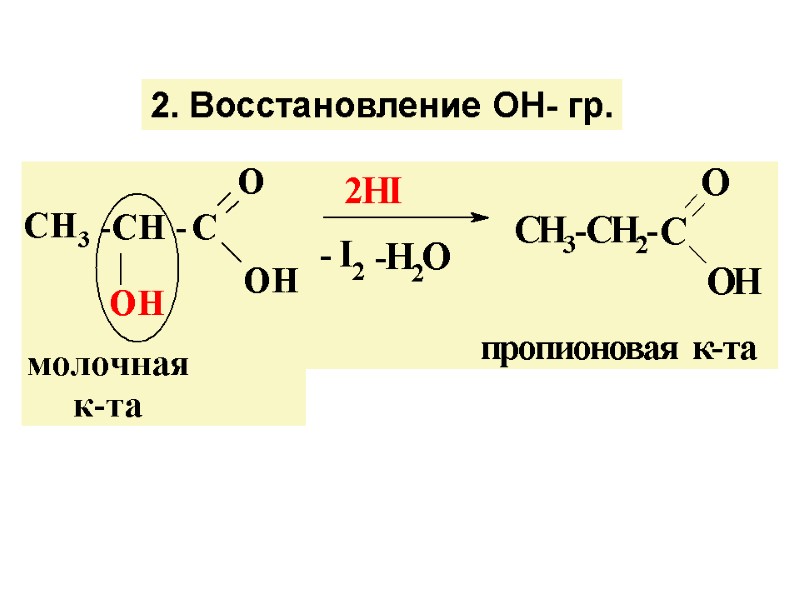
 2. Восстановление ОН- гр.
2. Восстановление ОН- гр.
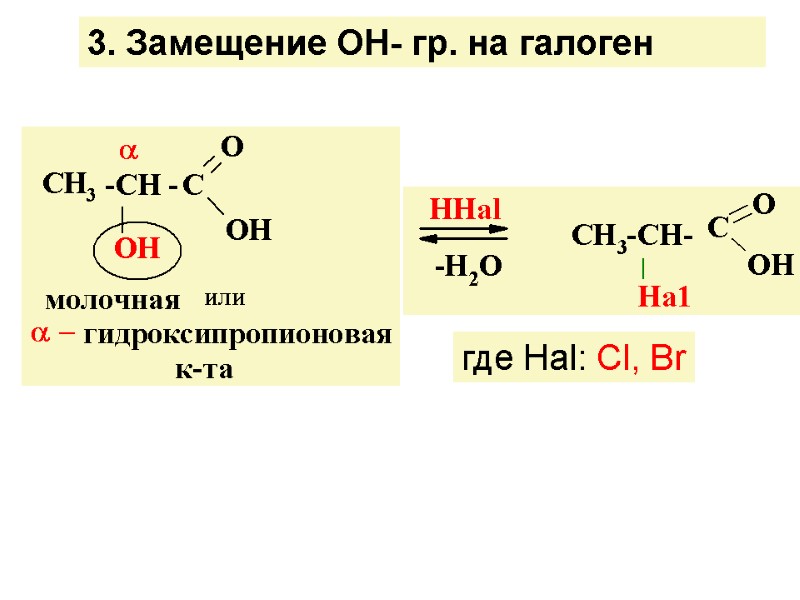
 3. Замещение ОН- гр. на галоген где Наl: Сl, Вr
3. Замещение ОН- гр. на галоген где Наl: Сl, Вr
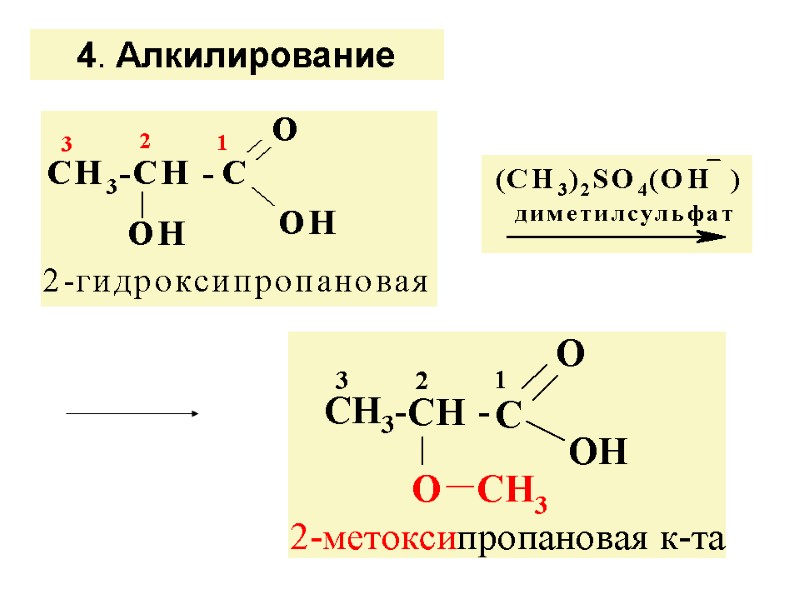
 4. Алкилирование
4. Алкилирование
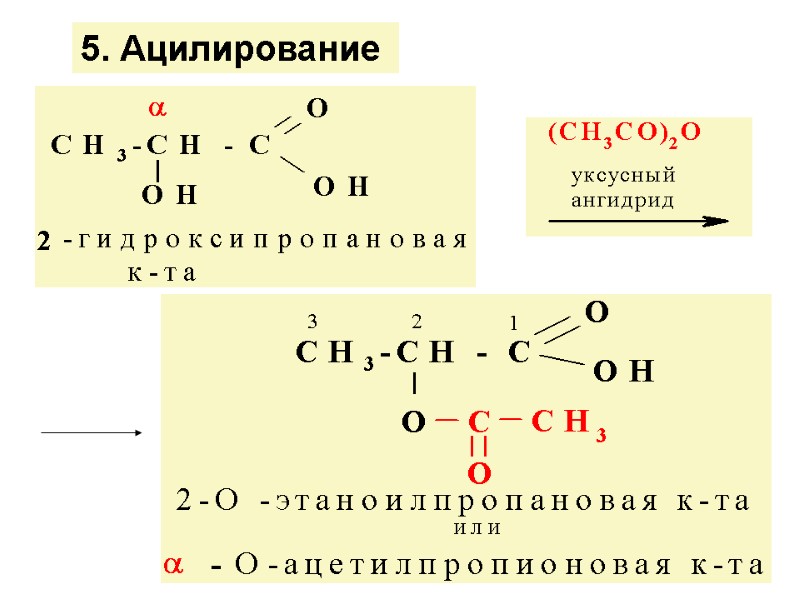
 5. Ацилирование
5. Ацилирование
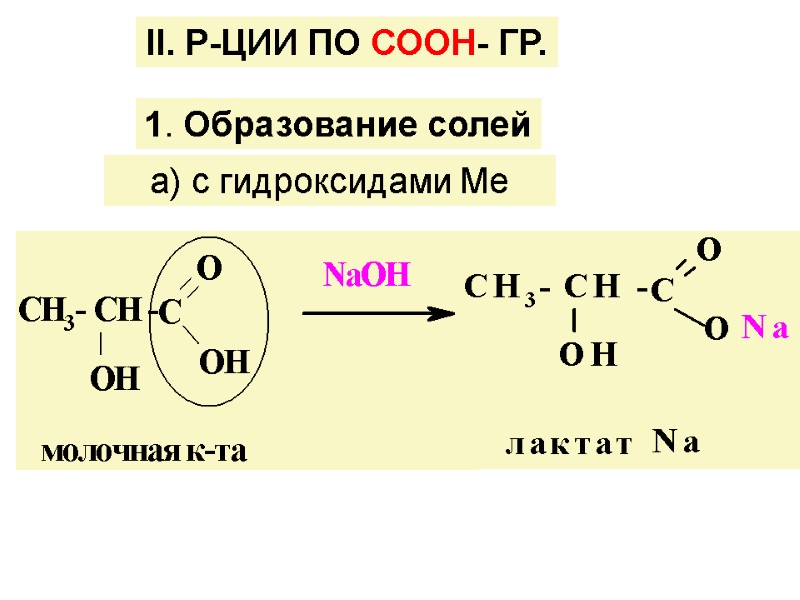
 ІІ. Р-ЦИИ ПО СООН- ГР. 1. Образование солей а) с гидроксидами Ме
ІІ. Р-ЦИИ ПО СООН- ГР. 1. Образование солей а) с гидроксидами Ме
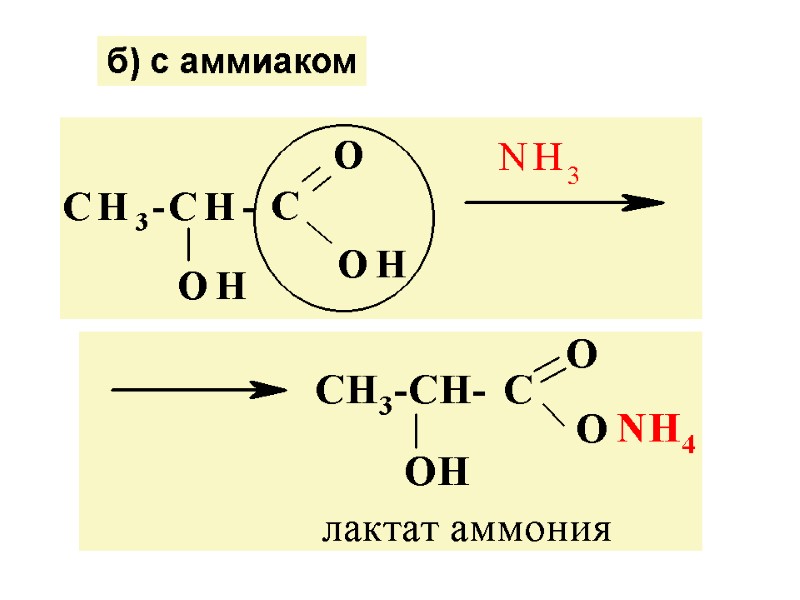
 б) с аммиаком
б) с аммиаком
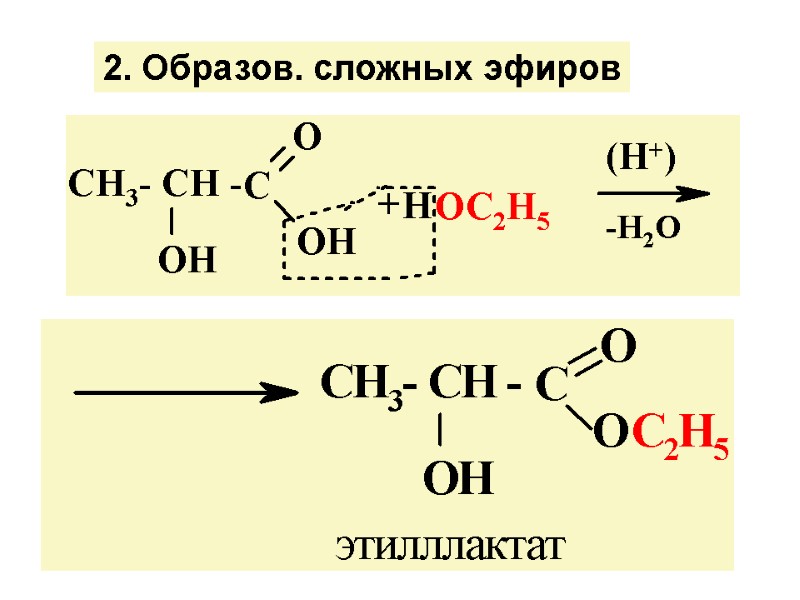
 2. Образов. сложных эфиров
2. Образов. сложных эфиров
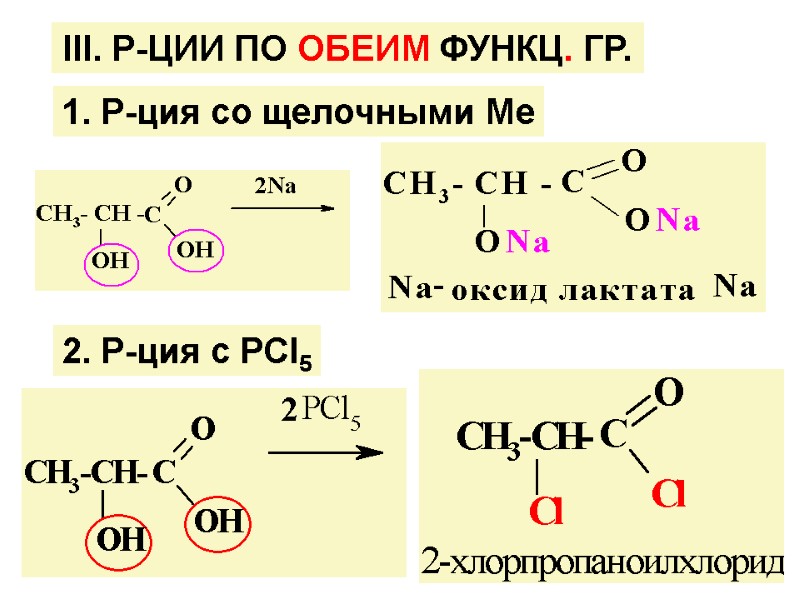
 1. Р-ция со щелочными Ме ІІI. Р-ЦИИ ПО ОБЕИМ ФУНКЦ. ГР. 2. Р-ция с РСI5
1. Р-ция со щелочными Ме ІІI. Р-ЦИИ ПО ОБЕИМ ФУНКЦ. ГР. 2. Р-ция с РСI5
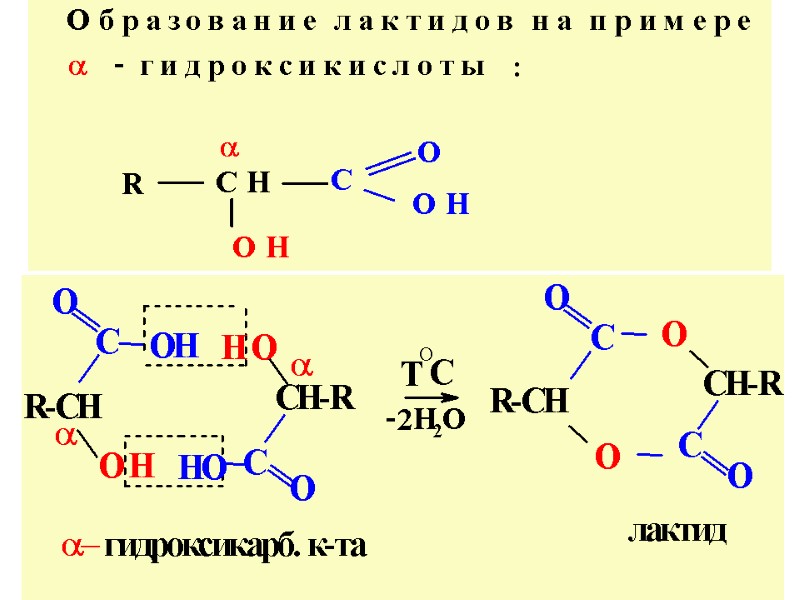
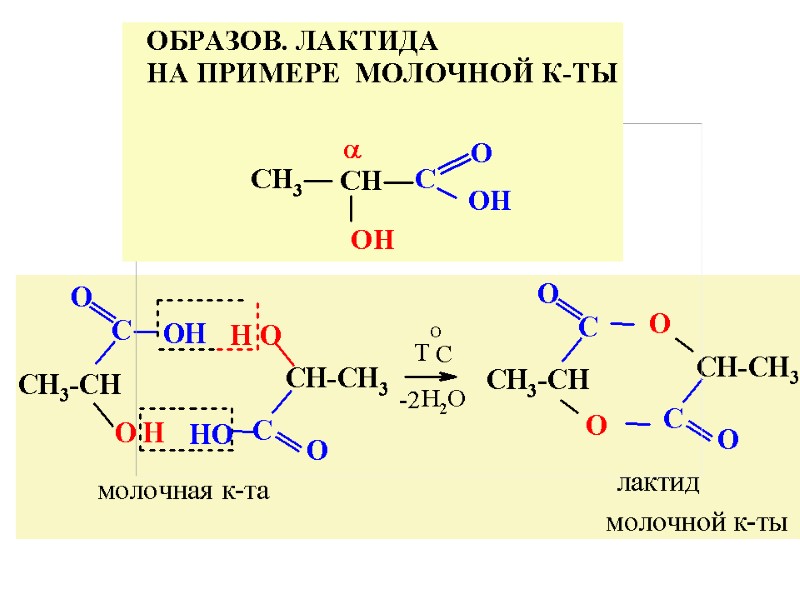
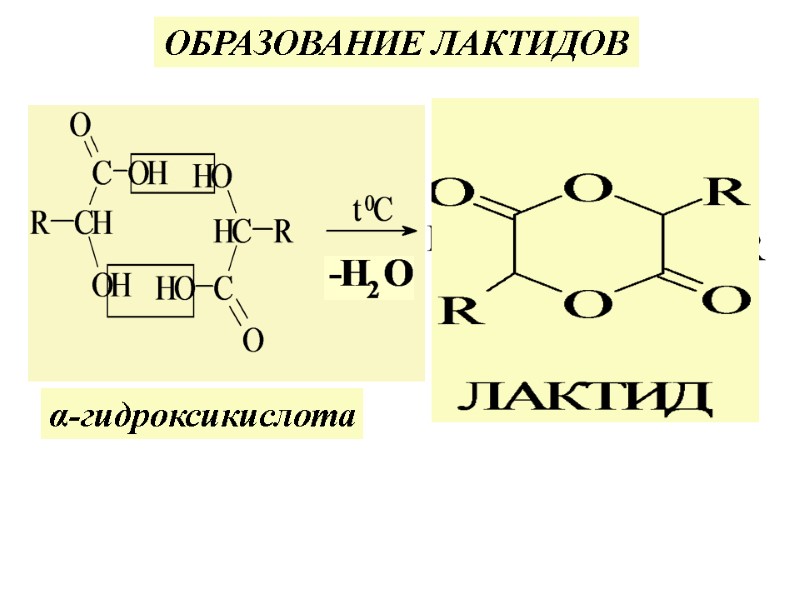
 ЛАКТИДЫ -циклич. эфиры, построен. из двух и более ост. Г/К ІІІ. Взаим. влиян. функц. групп. Отнош. к нагрев. α, β, γ- и δ- Г/К α-ГИДРОКСИКИСЛОТЫ 1. α-Г/К при Т°C дегидратируются с образов. ЛАКТИДОВ.
ЛАКТИДЫ -циклич. эфиры, построен. из двух и более ост. Г/К ІІІ. Взаим. влиян. функц. групп. Отнош. к нагрев. α, β, γ- и δ- Г/К α-ГИДРОКСИКИСЛОТЫ 1. α-Г/К при Т°C дегидратируются с образов. ЛАКТИДОВ.


 ОБРАЗОВАНИЕ ЛАКТИДОВ α-гидроксикислота
ОБРАЗОВАНИЕ ЛАКТИДОВ α-гидроксикислота
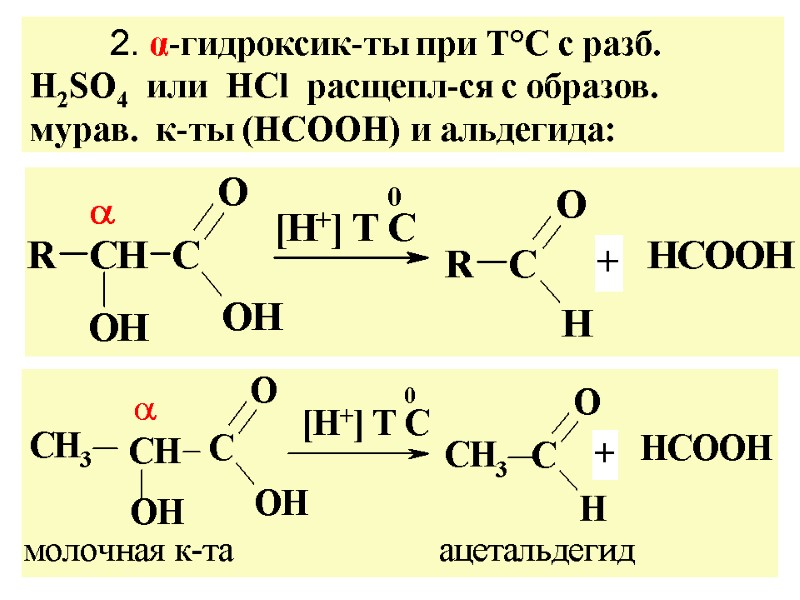
 2. α-гидроксик-ты при Т°C с разб. H2SO4 или HCl расщепл-ся с образов. мурав. к-ты (НСООН) и альдегида:
2. α-гидроксик-ты при Т°C с разб. H2SO4 или HCl расщепл-ся с образов. мурав. к-ты (НСООН) и альдегида:
 β-Гидроксик-ты при Т°C или при действ. к-т дегидратир-ся с образ. α-, β-ненасыщ. к-т: Отнош. к нагрев. β-гидроксикислот
β-Гидроксик-ты при Т°C или при действ. к-т дегидратир-ся с образ. α-, β-ненасыщ. к-т: Отнош. к нагрев. β-гидроксикислот
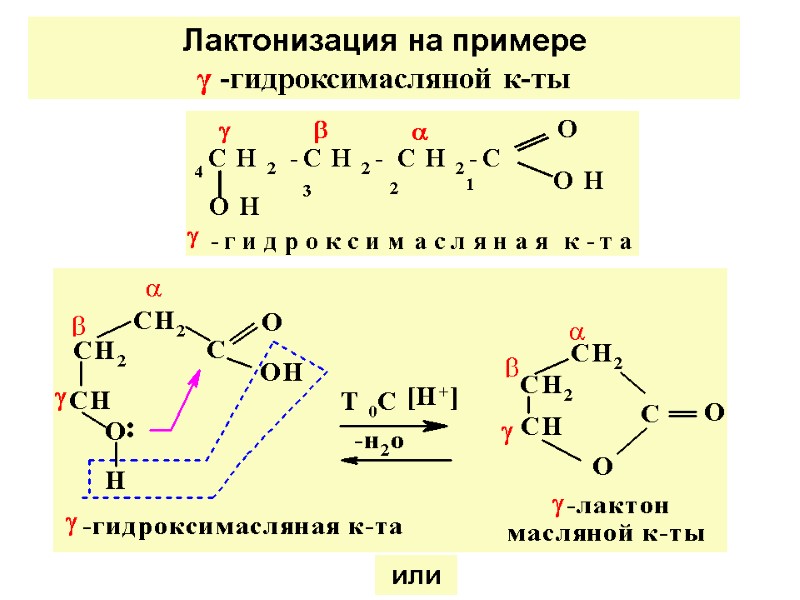
 Отношение к нагреванию γ - и δ- гидроксикислот γ- и δ-гидроксик-ты при Т°C в кисл. среде подверг-ся внутримолекул. этерификации с образ. пяти- и шестичлен. лактонов ЛАКТОНЫ – внутрен. сложн. эфиры гидроксик-т, в которых сложноэфир. групп-ка включена в циклич. струк-ру.
Отношение к нагреванию γ - и δ- гидроксикислот γ- и δ-гидроксик-ты при Т°C в кисл. среде подверг-ся внутримолекул. этерификации с образ. пяти- и шестичлен. лактонов ЛАКТОНЫ – внутрен. сложн. эфиры гидроксик-т, в которых сложноэфир. групп-ка включена в циклич. струк-ру.
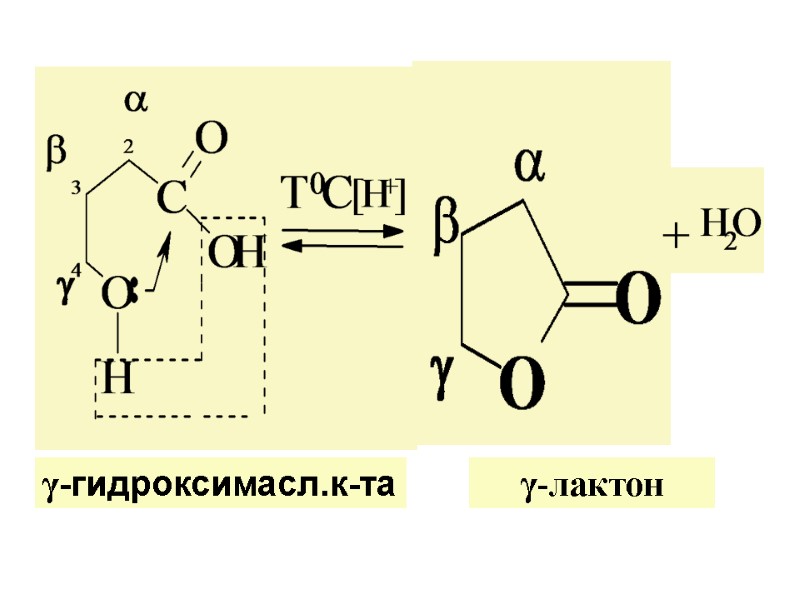
 или Лактонизация на примере γ -гидроксимасляной к-ты
или Лактонизация на примере γ -гидроксимасляной к-ты
 γ-гидроксимасл.к-та γ-лактон
γ-гидроксимасл.к-та γ-лактон
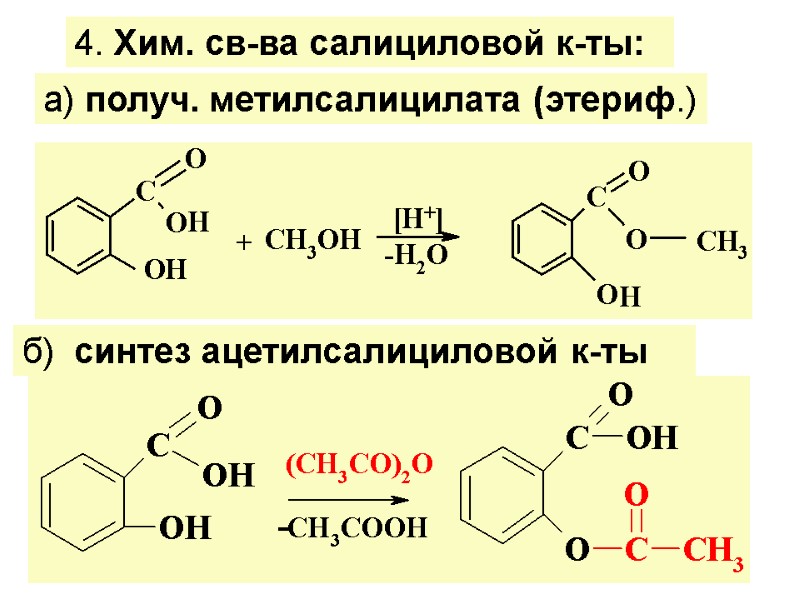
 4. Хим. св-ва салициловой к-ты: а) получ. метилсалицилата (этериф.) б) синтез ацетилсалициловой к-ты
4. Хим. св-ва салициловой к-ты: а) получ. метилсалицилата (этериф.) б) синтез ацетилсалициловой к-ты
 Различают.: право- (+) и левовращащие (-) изомеры Оптическая (зеркальная) изомерия ОСНОВНЫЕ ПОНЯТИЯ Оптическая активность – способность объектов взаимодействовать с плоскополяризованным светом (вращать плоскополяризованный свет)
Различают.: право- (+) и левовращащие (-) изомеры Оптическая (зеркальная) изомерия ОСНОВНЫЕ ПОНЯТИЯ Оптическая активность – способность объектов взаимодействовать с плоскополяризованным светом (вращать плоскополяризованный свет)
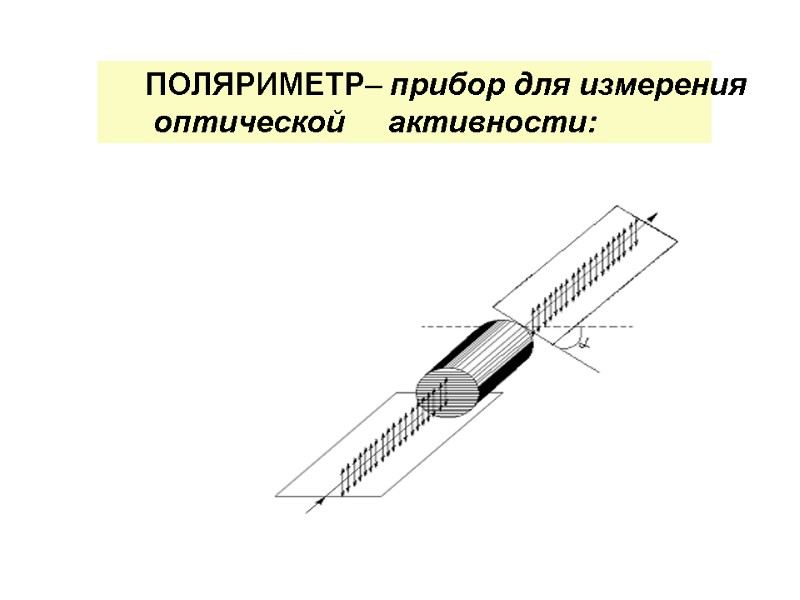
 ПОЛЯРИМЕТР– прибор для измерения оптической активности:
ПОЛЯРИМЕТР– прибор для измерения оптической активности:
![>Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина >Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина](https://present5.com/presentacii-2/20171208\15614-5_gidroksik-t_oksok-ty_prezentatsii.ppt\15614-5_gidroksik-t_oksok-ty_prezentatsii_34.jpg) Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина трубки
Единица измерения –удельное вращение [α] α –наблюдаемое вращение с – концентрация, l –длина трубки
 Причины оптической активности: Наличие асимметрического атома С (С*); 2. Отсутст. плоскости и центра симметрии.
Причины оптической активности: Наличие асимметрического атома С (С*); 2. Отсутст. плоскости и центра симметрии.
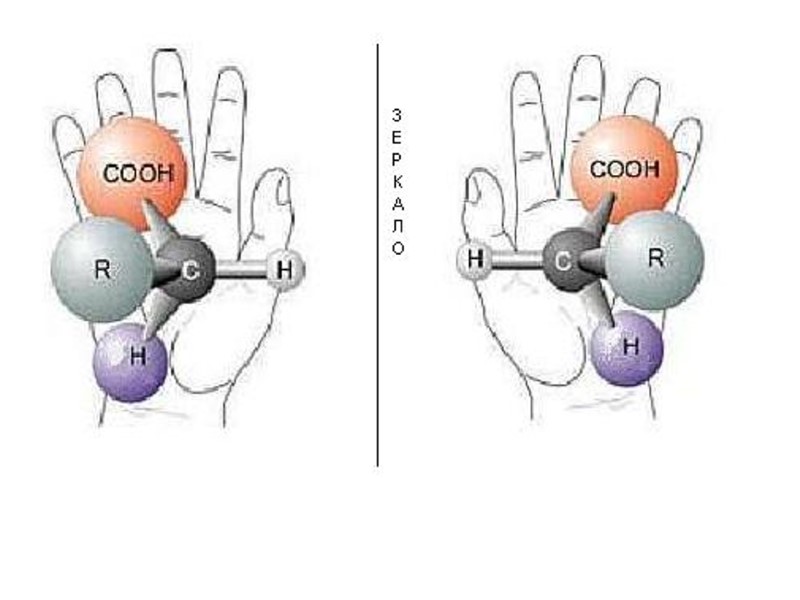
 Они отлич-ся друг от друга как предмет от своего зеркального изображения, как правая рука отлич-ся от левой. Любое орган. соед., содерж. С*, можно представ. в виде двух несовместимых в пространстве стереоизомеров. Такая изомерия назыв-ся «зеркальной». Асимметрич. атом С (С*)- С-атом, у которого все 4 валент-ти затрачены на соедин. с различ. атомами или гр. атомов.
Они отлич-ся друг от друга как предмет от своего зеркального изображения, как правая рука отлич-ся от левой. Любое орган. соед., содерж. С*, можно представ. в виде двух несовместимых в пространстве стереоизомеров. Такая изомерия назыв-ся «зеркальной». Асимметрич. атом С (С*)- С-атом, у которого все 4 валент-ти затрачены на соедин. с различ. атомами или гр. атомов.

 Рацемическая смесь – смесь равных кол-ств энантиомеров, оптически недеятельна, обозначается (±). При наличии в мол-ле нескол. асимм. С-атом. (С*), общее кол-во стереоизом. определ. по фор-ле N = 2n , где Ν –общ кол-во стереоизом., n - кол-во асиммет. С-атомов Стереоизомеры подразд. на : энантиомеры (зеркальные изомеры) и диастереомеры – незеркальные изом.
Рацемическая смесь – смесь равных кол-ств энантиомеров, оптически недеятельна, обозначается (±). При наличии в мол-ле нескол. асимм. С-атом. (С*), общее кол-во стереоизом. определ. по фор-ле N = 2n , где Ν –общ кол-во стереоизом., n - кол-во асиммет. С-атомов Стереоизомеры подразд. на : энантиомеры (зеркальные изомеры) и диастереомеры – незеркальные изом.
 б) наложением проекций с разворотом чертежа на 180 град. При изображ. оптически актив. соед. обычно используют проекционнные формулы Э. Фишера. По Фишеру: углерод. цепь располаг. вертикально, вверху – наиболее окислен. атом С. Проверка на совместимость в простр-ве: а) наложением проекций одна на другую;
б) наложением проекций с разворотом чертежа на 180 град. При изображ. оптически актив. соед. обычно используют проекционнные формулы Э. Фишера. По Фишеру: углерод. цепь располаг. вертикально, вверху – наиболее окислен. атом С. Проверка на совместимость в простр-ве: а) наложением проекций одна на другую;
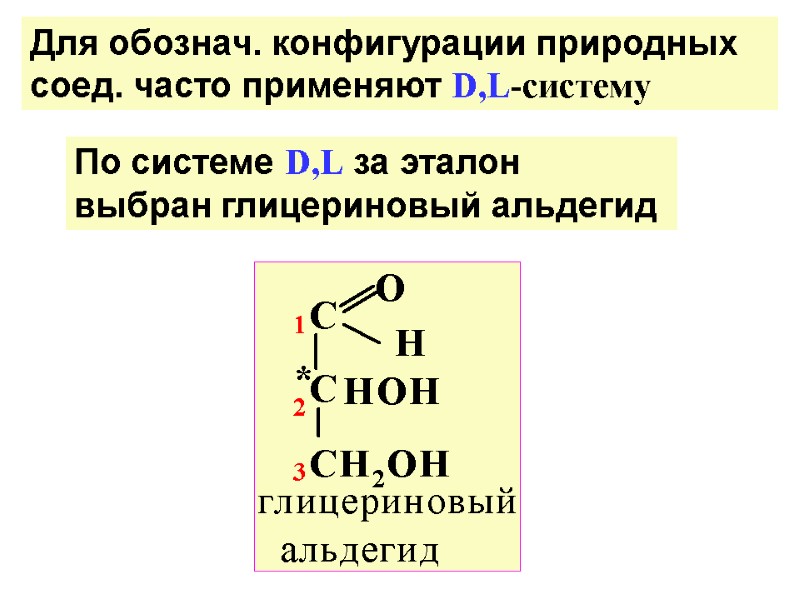
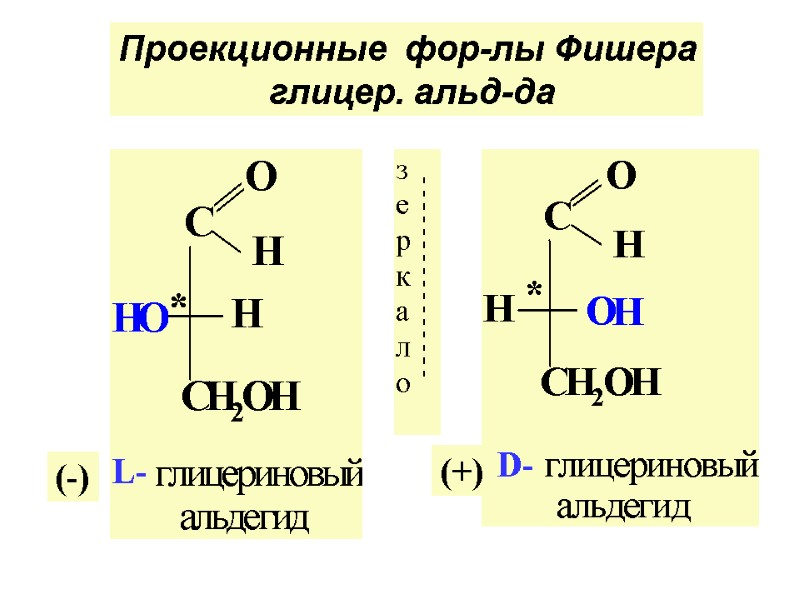
 Для обознач. конфигурации природных соед. часто применяют D,L-систему По системе D,L за эталон выбран глицериновый альдегид
Для обознач. конфигурации природных соед. часто применяют D,L-систему По системе D,L за эталон выбран глицериновый альдегид
 Проекционные фор-лы Фишера глицер. альд-да L- D- (-) (+)
Проекционные фор-лы Фишера глицер. альд-да L- D- (-) (+)
 Знак и конфигурация напрямую не связаны ! Сравнивая строение оптически активного соединения с конфигур. глицер. альд-да, его относят к D- или L –ряду. Знак определ. на поляриметре (+)или (-): правовращ.(+); левовращ. (–)
Знак и конфигурация напрямую не связаны ! Сравнивая строение оптически активного соединения с конфигур. глицер. альд-да, его относят к D- или L –ряду. Знак определ. на поляриметре (+)или (-): правовращ.(+); левовращ. (–)
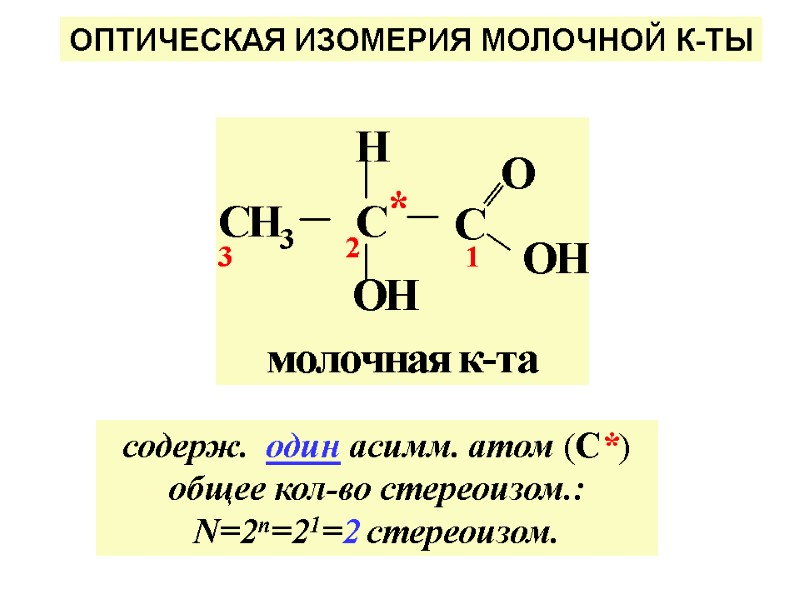
 ОПТИЧЕСКАЯ ИЗОМЕРИЯ МОЛОЧНОЙ К-ТЫ содерж. один асимм. атом (С*) общее кол-во стереоизом.: N=2n=21=2 стереоизом.
ОПТИЧЕСКАЯ ИЗОМЕРИЯ МОЛОЧНОЙ К-ТЫ содерж. один асимм. атом (С*) общее кол-во стереоизом.: N=2n=21=2 стереоизом.
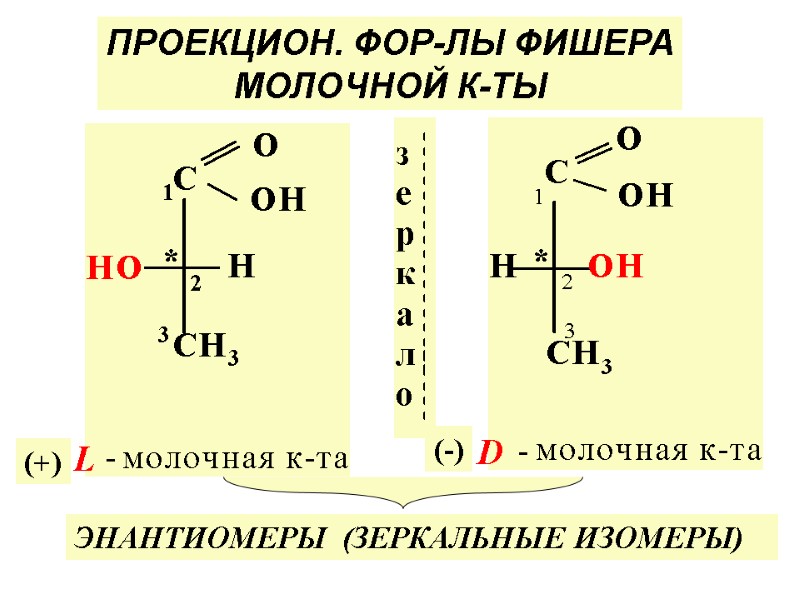
 ПРОЕКЦИОН. ФОР-ЛЫ ФИШЕРА МОЛОЧНОЙ К-ТЫ L D (+) (-) ЭНАНТИОМЕРЫ (ЗЕРКАЛЬНЫЕ ИЗОМЕРЫ)
ПРОЕКЦИОН. ФОР-ЛЫ ФИШЕРА МОЛОЧНОЙ К-ТЫ L D (+) (-) ЭНАНТИОМЕРЫ (ЗЕРКАЛЬНЫЕ ИЗОМЕРЫ)
 Смесь равных количеств энантиомеров – рацемическая смесь(±). Соли и слож. эфиры молоч. к-ты - лактаты. L(+) молоч. к-та образ-ся в мышеч. ткани как продукт расщепл. гликогена. D(–) молоч. к-та может быть получена под действием микроорг. Рацемич. смесь(±) - молоч. к-та брожения.
Смесь равных количеств энантиомеров – рацемическая смесь(±). Соли и слож. эфиры молоч. к-ты - лактаты. L(+) молоч. к-та образ-ся в мышеч. ткани как продукт расщепл. гликогена. D(–) молоч. к-та может быть получена под действием микроорг. Рацемич. смесь(±) - молоч. к-та брожения.
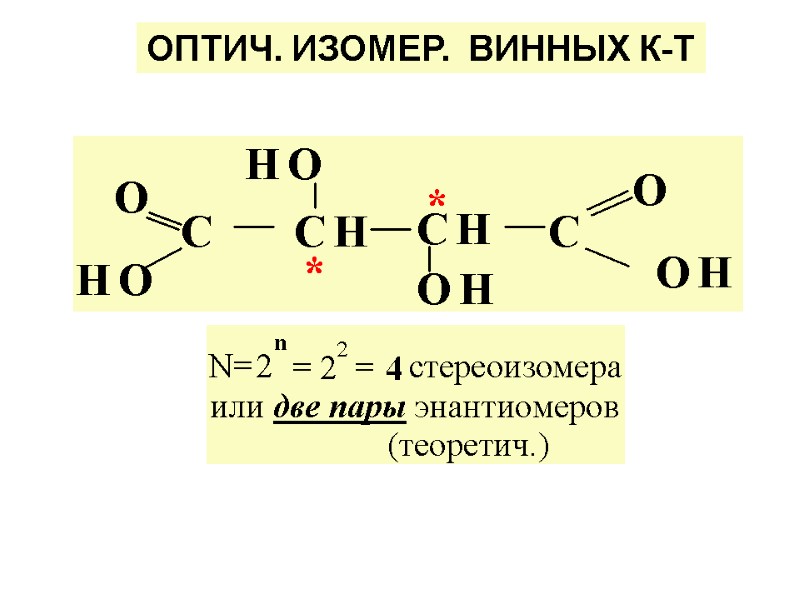
 ОПТИЧ. ИЗОМЕР. ВИННЫХ К-Т
ОПТИЧ. ИЗОМЕР. ВИННЫХ К-Т
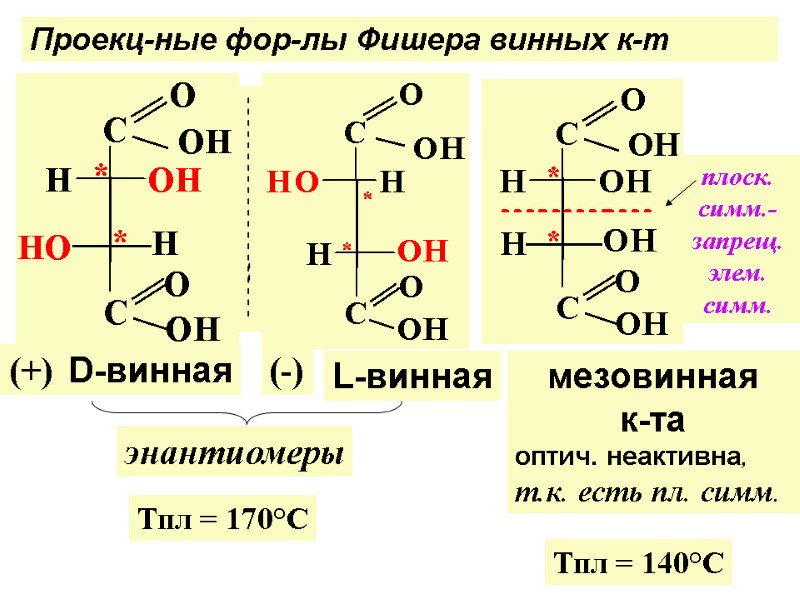
 Тпл = 140°С Проекц-ные фор-лы Фишера винных к-т D-винная L-винная мезовинная к-та оптич. неактивна, т.к. есть пл. симм. (+) (-) энантиомеры Тпл = 170°С плоск. симм.- запрещ. элем. симм.
Тпл = 140°С Проекц-ные фор-лы Фишера винных к-т D-винная L-винная мезовинная к-та оптич. неактивна, т.к. есть пл. симм. (+) (-) энантиомеры Тпл = 170°С плоск. симм.- запрещ. элем. симм.
 D и L-винные к-ты – энантиомеры (зеркальные изомеры) D – и мезовинная , L- и мезовинная диастереомеры (незеркальные изом.) Рацемическая смесь D и L винных к-т или рацемат (±) наз-ся виноградной к-той с Т пл= 205°С Соли и эфиры винной кислоты - тартраты.
D и L-винные к-ты – энантиомеры (зеркальные изомеры) D – и мезовинная , L- и мезовинная диастереомеры (незеркальные изом.) Рацемическая смесь D и L винных к-т или рацемат (±) наз-ся виноградной к-той с Т пл= 205°С Соли и эфиры винной кислоты - тартраты.
 D-винная к-та содер. в виноградном соке и некот. растениях. Двойная соль — тартрат калия-натрия, (сегнетова соль), использ-ся для качест. и колич. опред. альдегидов и моносахаридов под назв. реакт. Фелинга. L-винную к-ту получают расщепл. виноградной к-ты на энантиомеры. В очень небольшом количестве она также содер-ся в виноградных винах.
D-винная к-та содер. в виноградном соке и некот. растениях. Двойная соль — тартрат калия-натрия, (сегнетова соль), использ-ся для качест. и колич. опред. альдегидов и моносахаридов под назв. реакт. Фелинга. L-винную к-ту получают расщепл. виноградной к-ты на энантиомеры. В очень небольшом количестве она также содер-ся в виноградных винах.
 Методы расщепления рацемических смесей. 1.Механический отбор 2. Биологический отбор 3. Химический метод 4. Асимметрический синтез.
Методы расщепления рацемических смесей. 1.Механический отбор 2. Биологический отбор 3. Химический метод 4. Асимметрический синтез.
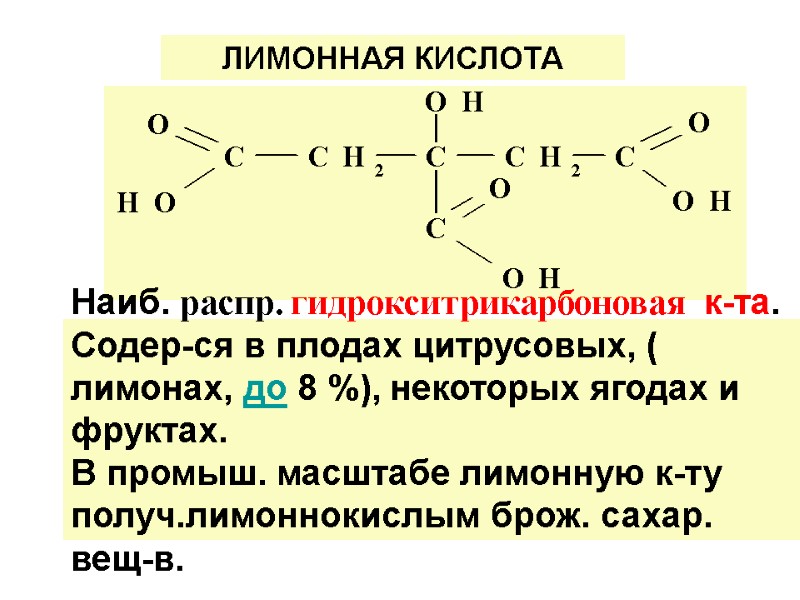
 ЛИМОННАЯ КИСЛОТА Наиб. распр. гидрокситрикарбоновая к-та. Содер-ся в плодах цитрусовых, ( лимонах, до 8 %), некоторых ягодах и фруктах. В промыш. масштабе лимонную к-ту получ.лимоннокислым брож. сахар. вещ-в.
ЛИМОННАЯ КИСЛОТА Наиб. распр. гидрокситрикарбоновая к-та. Содер-ся в плодах цитрусовых, ( лимонах, до 8 %), некоторых ягодах и фруктах. В промыш. масштабе лимонную к-ту получ.лимоннокислым брож. сахар. вещ-в.
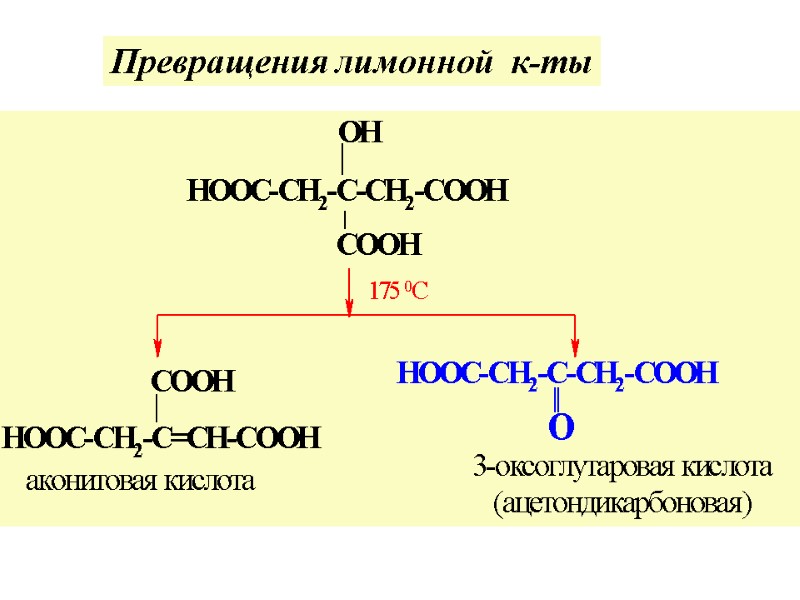
 Превращения лимонной к-ты
Превращения лимонной к-ты

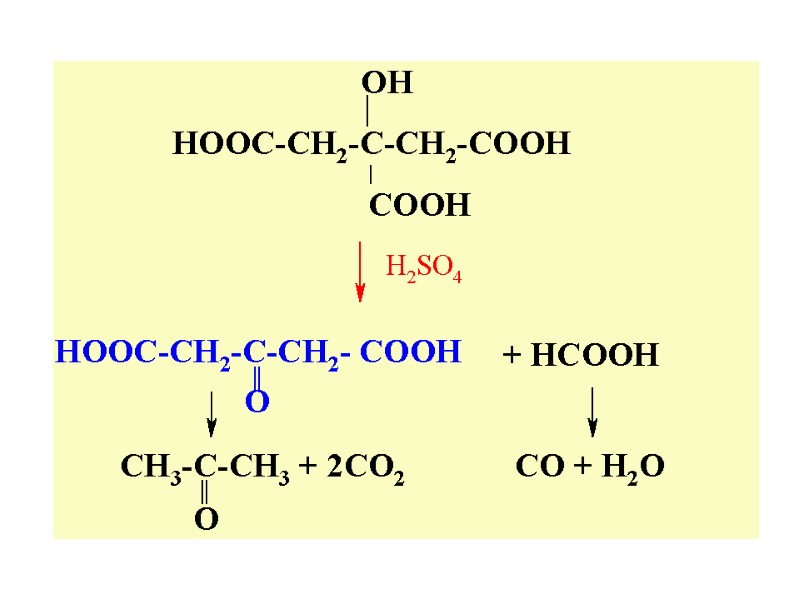
 Нагрев. лимонной к-ты до 175 °С приводит к дегидратации (как β-гидроксик-ты), с образ. аконитовой к-ты. Лимонная к-та и ее соли (цитраты) широко использ. в разл. областях пищ. пром-ти . Нагрев. с H2SO4 приводит к расщепл. лимонной к-ты на ацетондикарбоновую и муравьиную, с последующим разлож. до СО2 и СО.
Нагрев. лимонной к-ты до 175 °С приводит к дегидратации (как β-гидроксик-ты), с образ. аконитовой к-ты. Лимонная к-та и ее соли (цитраты) широко использ. в разл. областях пищ. пром-ти . Нагрев. с H2SO4 приводит к расщепл. лимонной к-ты на ацетондикарбоновую и муравьиную, с последующим разлож. до СО2 и СО.
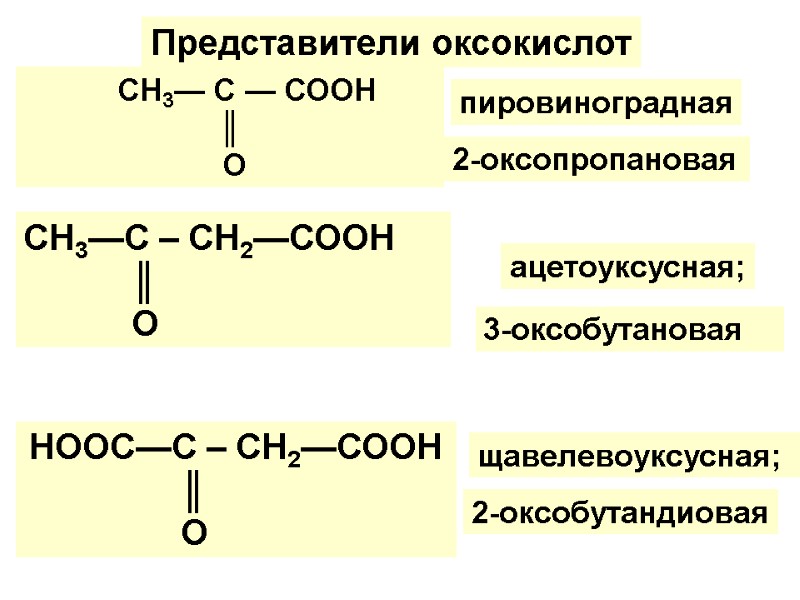
 Оксо- гр. в назв. обозн. префикс оксо-. ОКСОКИСЛОТЫ альдегидо- или кетокис-ты. По кол-ву СООН- гр.: моно-,ди-, трикарбоновые По взаимн. располож. функц. гр.: α-, β-, γ- оксокарб. к-ты. Трив. назв. : (пировиноградная, левулиновая). Классификация Номенклатура
Оксо- гр. в назв. обозн. префикс оксо-. ОКСОКИСЛОТЫ альдегидо- или кетокис-ты. По кол-ву СООН- гр.: моно-,ди-, трикарбоновые По взаимн. располож. функц. гр.: α-, β-, γ- оксокарб. к-ты. Трив. назв. : (пировиноградная, левулиновая). Классификация Номенклатура
 Представители оксокислот СН3— С — СООН ║ О пировиноградная 2-оксопропановая СН3—С – СН2—СООН ║ О 3-оксобутановая НООС—С – СН2—СООН ║ О щавелевоуксусная; 2-оксобутандиовая ацетоуксусная;
Представители оксокислот СН3— С — СООН ║ О пировиноградная 2-оксопропановая СН3—С – СН2—СООН ║ О 3-оксобутановая НООС—С – СН2—СООН ║ О щавелевоуксусная; 2-оксобутандиовая ацетоуксусная;
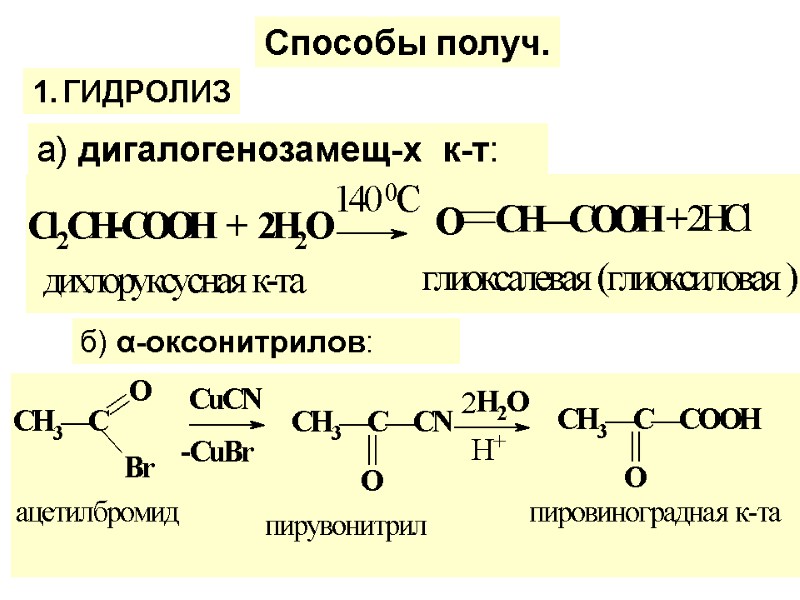
 а) дигалогенозамещ-х к-т: б) α-оксонитрилов: Способы получ. ГИДРОЛИЗ
а) дигалогенозамещ-х к-т: б) α-оксонитрилов: Способы получ. ГИДРОЛИЗ
 2. Получение β-оксокислот сложно-эфирной конденсацией
2. Получение β-оксокислот сложно-эфирной конденсацией
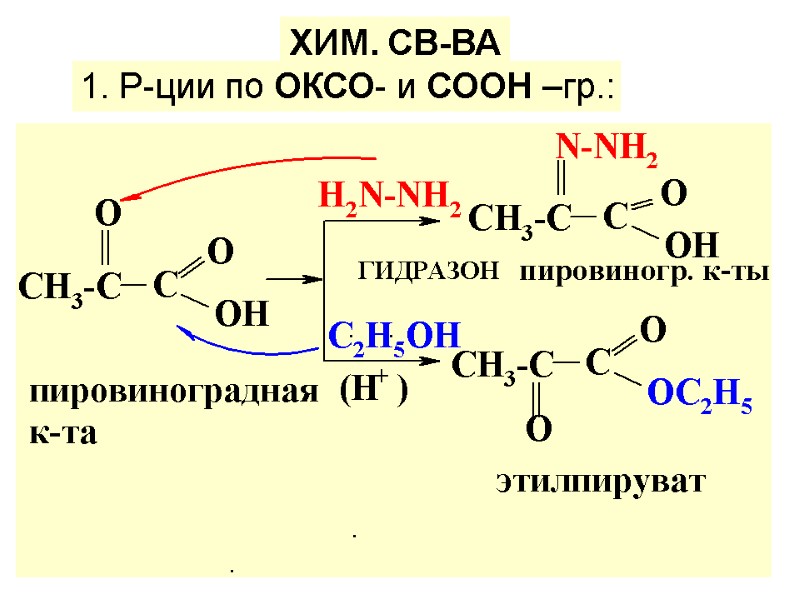
 1. Р-ции по ОКСО- и СООН –гр.: ХИМ. СВ-ВА
1. Р-ции по ОКСО- и СООН –гр.: ХИМ. СВ-ВА
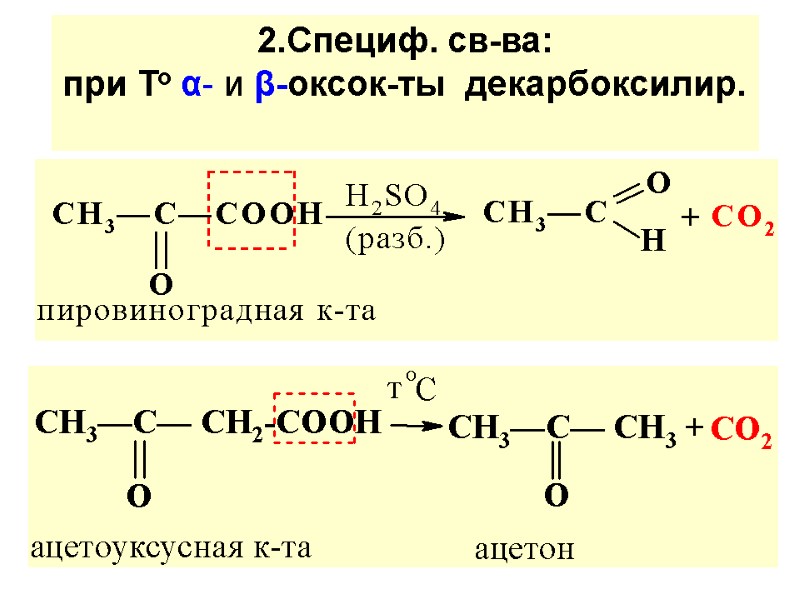
 2.Специф. св-ва: при То α- и β-оксок-ты декарбоксилир.
2.Специф. св-ва: при То α- и β-оксок-ты декарбоксилир.
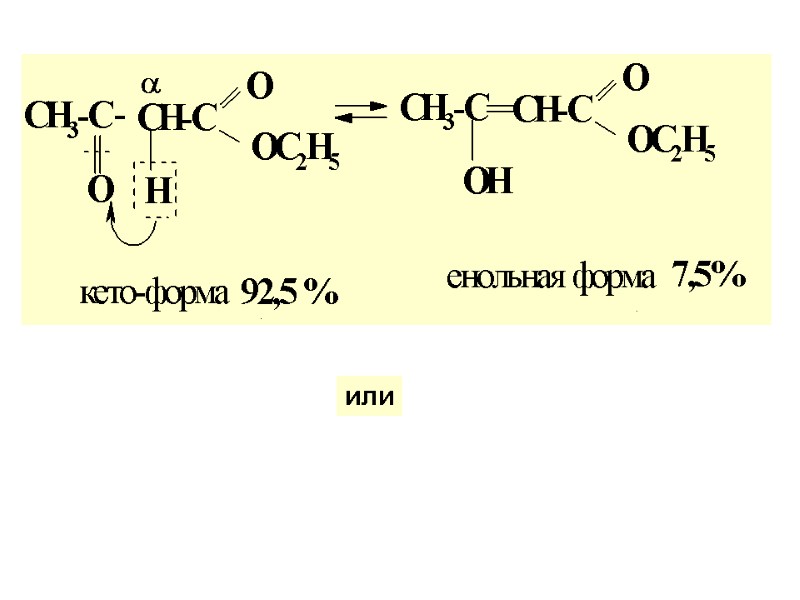
 Таутомерия — способн. хим. соед. существ. в виде струк. изомеров, находящихся в равновесии. Кето-енольная таутомерия АУЭ Сущн. кето-енольной таутомерии: перенос Н+ от α-СН-кислотного центра оксосоед-я к «О» оксо- группы:
Таутомерия — способн. хим. соед. существ. в виде струк. изомеров, находящихся в равновесии. Кето-енольная таутомерия АУЭ Сущн. кето-енольной таутомерии: перенос Н+ от α-СН-кислотного центра оксосоед-я к «О» оксо- группы:
 или
или
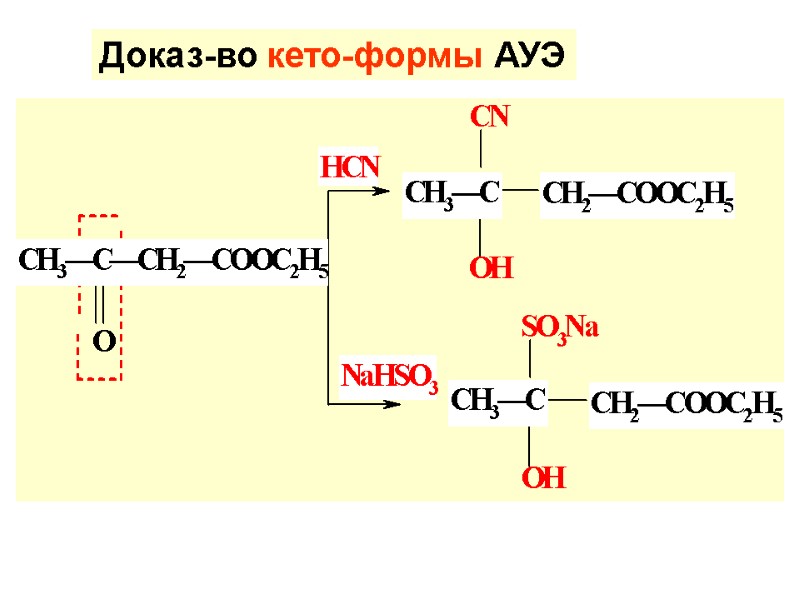
 Доказ-во кето-формы АУЭ
Доказ-во кето-формы АУЭ
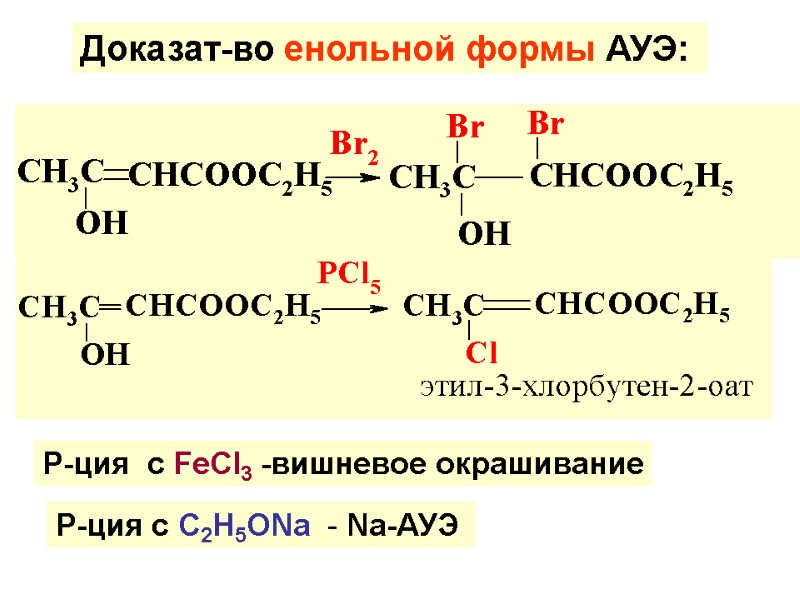
 Доказат-во енольной формы АУЭ: Р-ция с FeCl3 -вишневое окрашивание Р-ция с С2Н5ОNа - Nа-АУЭ
Доказат-во енольной формы АУЭ: Р-ция с FeCl3 -вишневое окрашивание Р-ция с С2Н5ОNа - Nа-АУЭ
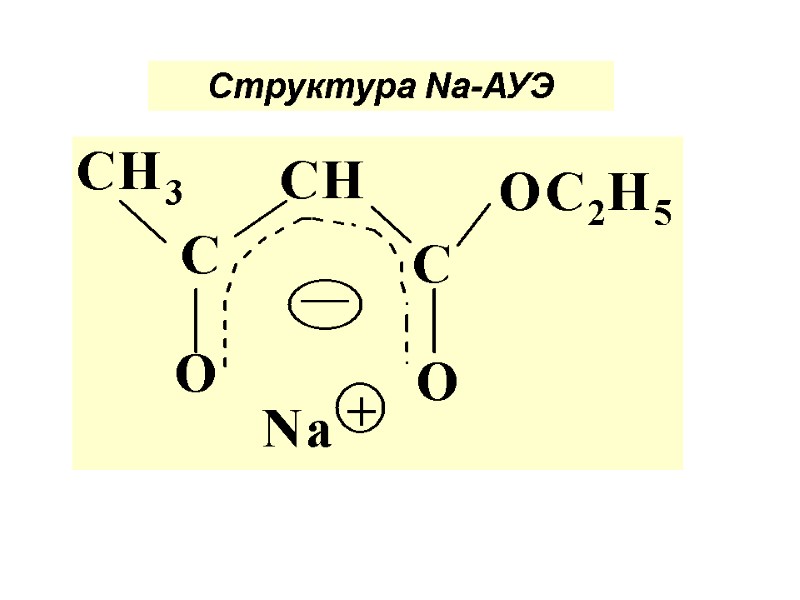
 Структура Nа-АУЭ
Структура Nа-АУЭ
 Структура аниона АУЭ Na-АУЭ возможно алкилир. и ацилир. При этом получ-ся О- и С- производные. Р-ции использ. для получ. кетонов и карб к-т. АМБИДЕНТНЫЙ ИОН (с двойств. реакц. способ.) При дейст. концентр. щелоч. образ-ся к-ты , при действии разбавл. щелочей – кетоны.
Структура аниона АУЭ Na-АУЭ возможно алкилир. и ацилир. При этом получ-ся О- и С- производные. Р-ции использ. для получ. кетонов и карб к-т. АМБИДЕНТНЫЙ ИОН (с двойств. реакц. способ.) При дейст. концентр. щелоч. образ-ся к-ты , при действии разбавл. щелочей – кетоны.
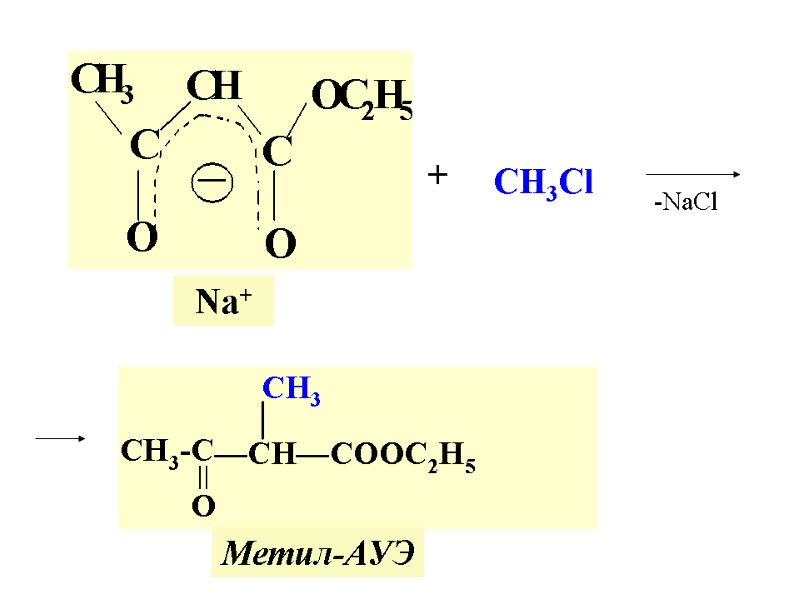
 Na+ + CH3Cl -NaCl Метил-АУЭ
Na+ + CH3Cl -NaCl Метил-АУЭ
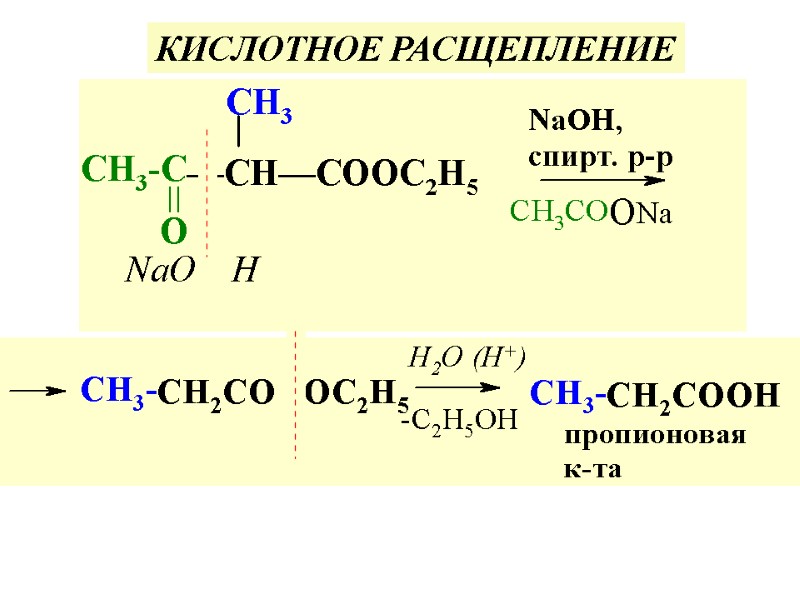
 КИСЛОТНОЕ РАСЩЕПЛЕНИЕ
КИСЛОТНОЕ РАСЩЕПЛЕНИЕ
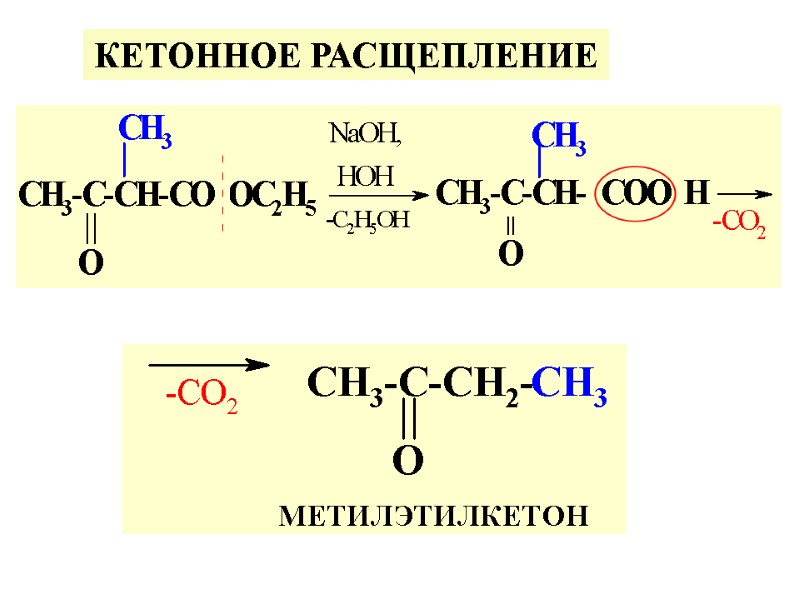
 КЕТОННОЕ РАСЩЕПЛЕНИЕ
КЕТОННОЕ РАСЩЕПЛЕНИЕ
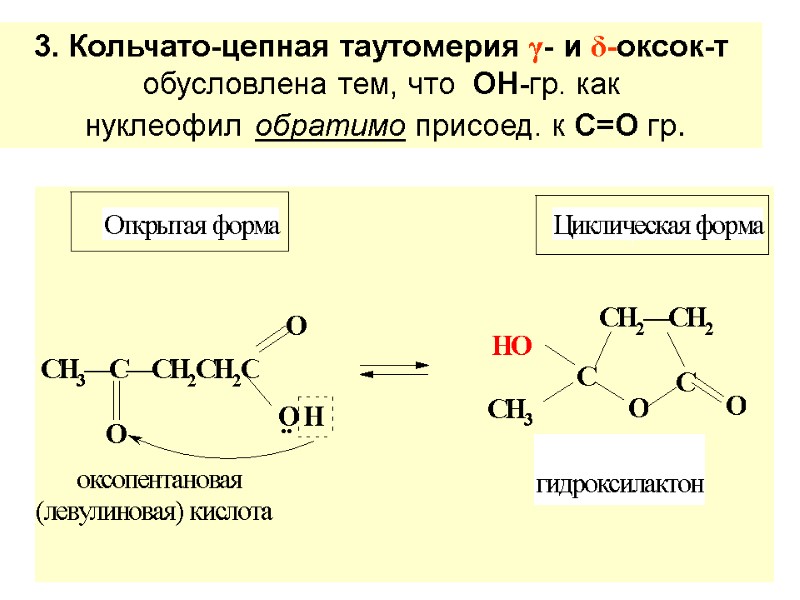
 3. Кольчато-цепная таутомерия γ- и δ-оксок-т обусловлена тем, что ОН-гр. как нуклеофил обратимо присоед. к С=О гр.
3. Кольчато-цепная таутомерия γ- и δ-оксок-т обусловлена тем, что ОН-гр. как нуклеофил обратимо присоед. к С=О гр.
 Открытая форма γ- и δ-оксок-т нах-ся в равновесии с гидроксилактоном- циклич. полуацеталем. Кольч.-цепная таутомерия более известна для моносахаридов.
Открытая форма γ- и δ-оксок-т нах-ся в равновесии с гидроксилактоном- циклич. полуацеталем. Кольч.-цепная таутомерия более известна для моносахаридов.

