Oksi-kisloti-10.ppt
- Количество слайдов: 13

ГІДРОКСИКАРБОНОВІ КИСЛОТИ – похідні вуглеводнів, які мають у молекулі два види функціональних груп: гідроксильні –OH та карбоксильні –COOH. Завдяки цьому гідроксикислоти можна розглядати як гідроксильні похідні відповідних карбонових кислот. Залежно від кількості карбоксильних груп розрізняють одно , дво та багатоосновні гідроксикислоти. Кількість гідроксильних груп, у тому числі і гідроксил карбоксильної групи, визначають атомність гідроксикислоти. Отже, гідроксикислоти можуть бути дво , три і багатоатомними, наприклад: Гідроксикислоти поділяють на аліфатичні (насичені й ненасичені), ароматичні та гетероциклічні. Гомологічний ряд гідроксикислот починається з гідроксимурашиної HO– : COOH (карбонатної) кислоти: Ізомерія гідроксикислот. Структурна ізомерія визначається будовою карбонового ланцюга та взаємоположенням функціональних груп. Залежно від положення ОН-груп по відношенню до СООН розрізняють α (С 2), β (С 3), γ (С 4), δ (С 5), ε(С 6). . . гідроксикислоти:

Міжкласова ізомерія: Оптична ізомерія: Номенклатура гідроксикислот. Для назви гідроксикислот вживають історичну (тривіальну), раціональну та систематичну номенклатури. Часто історичні назви походять від назв природних джерел знаходження цих гідроксикислот (молочна, яблучна, виноградна). В основі раціональної номенклатури лежить тривіальна назва відповідної карбонової кислоти, а положення гідроксильної групи визначається буквами грецького алфавіту α, β, γ, δ, ε тощо. За систематичною (IUPAC) номенклатурою назву гідроксикислоти утворюють з систематичної назви відповідної карбонової кислоти, до якої добавляють префікс гідрокси- і номер (локант) атома Карбону, з яким сполучена гідроксигрупа, наприклад: НОСН 2 СООН (гідроксиетанова, гліколева, гідроксиацетатна); СН 3 СН(ОН) СООН (2 гідроксипропанова, молочна, α гідроксипропіонова); НООС СН(ОН) СН 2 СООН (2 гідроксибутандіова, яблучна, гідроксибурштинова); НООС СН(ОН) СООН (2, 3 дигідроксибутандіова, винна, α, β дигідроксибурштинова).

ОДНООСНОВНІ ГІДРОКСИКИСЛОТИ. Методи одержання. Ряд гідроксикислот (яблучна, винна, лимонна, галова) є продуктами життєдіяльності мікроорганізмів. Це й стало основою створення біотехнологій синтезу таких гідроксикислот при зброджуванні цукропродуктів (рафінадної патоки, меляси) – відходів цукрового виробництва. Синтетичні способи одержання гідроксикислот передбачають введення в молекулу карбонової кислоти гідроксигрупи, або введення карбоксильної групи у молекулу спирту. Гідроліз галогенозаміщених кислот: Синтез α-гідроксикислот із альдегідів і кетонів: Приєднання води до α , β-ненасичених кислот: Одержання β-гідроксикислот за реакцією C. M. Реформатського (1889 р) естери αгалогенокарбонових кислот за наявності цинку взаємодіють з карбонільними сполуками з утворенням естерів β-гідроксикислот, які омилюються до βгідроксикислот:

Фізичні властивості. Одноосновні гідроксикислоти – безбарвні густі сиропоподібні рідини або кристалічні речовини, мають значно вищі Тпл. та Ткип. , ніж аналогічні карбонові кислоти завдяки утворенню водневих зв’язків. Вони краще розчиняються у воді, ніж відповідні їм карбонові кислоти, обмежено розчинні в етерах та інших органічних розчинниках. Наявність хіральних атомів С зумовлює їх оптичну активність. Хімічні властивості. Як і в інших гетерофункціональних сполуках, хімічні властивості гідроксикислот визначаються природою цих груп. Тому гідроксикислоти беруть участь у більшості хімічних реакцій, характерних для карбонових кислот (наявність групи –COOH) і спиртів (наявність групи –OH). Залежно від реакційних умов кожна із зазначених функціональних груп може реагувати незалежно одна від іншої, але взаємно впливають і можуть взаємодіяти між собою. До реакцій, що відбуваються за участі карбоксильної групи належать: електролітична дисоціація, утворення солей, естерів, галогенангідридів та ангідридів: R–CH(OH)–COOH +2 Na R–CH(ONa)–COONa + H 2 R–CH(OH)–COOH + Na. OH R–CH(OH)–COONa + H 2 O R–CH(OH)–COOH + HO–R 1(H+) R–CH(OH)–COOR 1 + H 2 O R–CH(OH)–COOH + PCl 5 R–CH(Cl)–COCl + POCl 3+ H 2 O RCH(Cl)COCl + RCH(OH)COOH + 2 Na. OH (RCH(OH)CO)2 O + 2 Na. Cl + H 2 O Реакції гідроксильної групи. Утворення кетокислоти (1), заміна спиртової групи атомом галогену (2), утворення етерів (3), естерів (4). R–CH(OH)–COOH + [O] R–CO–COOH + H 2 O (1) R–CH(OH)–COOH + HCl R–CH(Cl)–COOH + H 2 O (2) R–CH(OH)–COOH + (CH 3)2 SO 2 R–CH(OCH 3)–COOH + CH 3 SO 2 OH (3) R–CH(OH)–COOH + CH 3–COCl R–CH(OCOCH 3)–COOH + HCl (4)
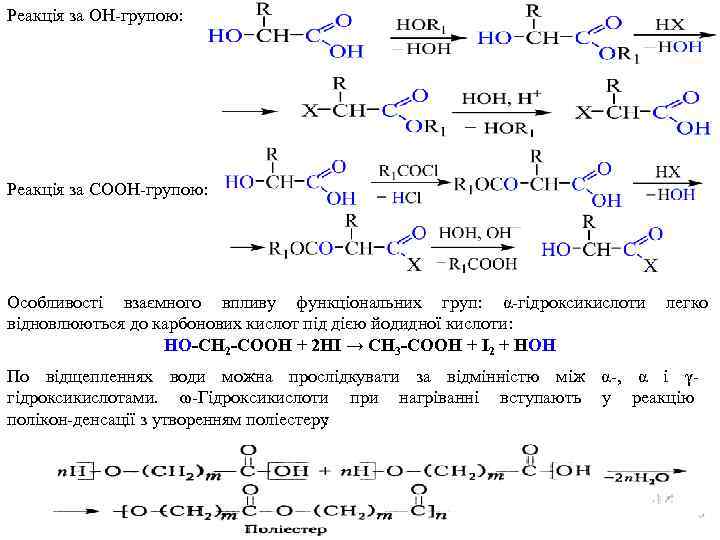
Реакція за ОН групою: Реакція за COОН групою: Особливості взаємного впливу функціональних груп: α гідроксикислоти відновлюються до карбонових кислот під дією йодидної кислоти: HO-CH 2 -COOH + 2 HI → CH 3 -COOH + I 2 + HOH легко По відщепленнях води можна прослідкувати за відмінністю між α , α і γ гідроксикислотами. ω Гідроксикислоти при нагріванні вступають у реакцію полікон денсації з утворенням поліестеру :
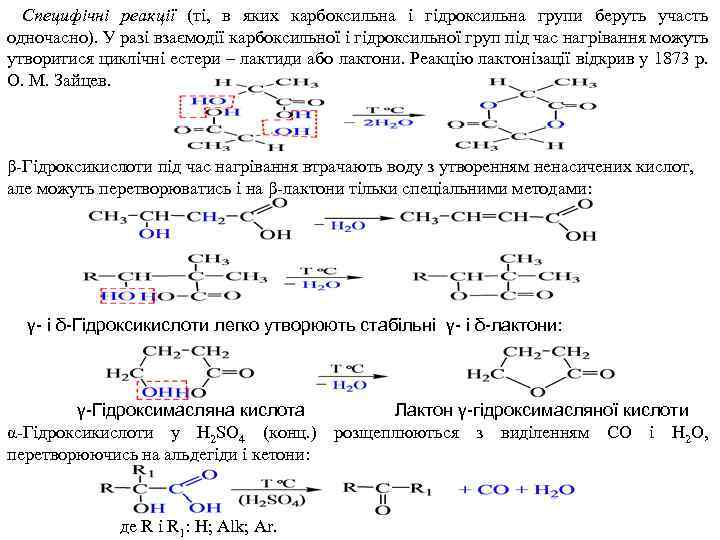
Специфічні реакції (ті, в яких карбоксильна і гідроксильна групи беруть участь одночасно). У разі взаємодії карбоксильної і гідроксильної груп під час нагрівання можуть утворитися циклічні естери – лактиди або лактони. Реакцію лактонізації відкрив у 1873 p. O. M. Зайцев. β Гідроксикислоти під час нагрівання втрачають воду з утворенням ненасичених кислот, але можуть перетворюватись і на β лактони тільки спеціальними методами: γ- і δ-Гідроксикислоти легко утворюють стабільні γ- і δ-лактони: γ-Гідроксимасляна кислота Лактон γ-гідроксимасляної кислоти α Гідроксикислоти у H 2 SO 4 (конц. ) розщеплюються з виділенням CO і H 2 O, перетворюючись на альдегіди і кетони: де R i R 1: H; Alk; Ar.

Окремі представники. Гліколева кислота HOCH 2 COOH – безбарвна, кристалічна речовина, добре розчинна у воді. Вона міститься у природних продуктах (у соці цукрового буряка, цукрової тростини, винограду). Її синтезують кількома методами: з хлороцтової кислоти, окисненням етиленгліколю або електролітичним відновленням щавлевої кислоти. Молочна кислота CH 3 CH(OH)COOH уперше була відкрита в 1870 р. K. Шеєле у кислому молоці, що і зумовило її історичну назву. Існує в трьох формах: дві оптично активні (енантіомери) й оптично неактивна рацемічна суміш. Визначена абсолютна конфігурація правообертаючої (D ряду) і лівообертаючої (L ряду) молочних кислот: У молекулі молочної кислоти міститься один С*, що зумовлює існування двох просторових ізомерів цієї кислоти. Ю. Лібіх (1847 р. ) виділив із м’язів молочну кислоту, яку назвав м’ясо молочною кислотою. (+)L Молочна кислота – безбарвна, дуже гігроскопічна кристалічна речовина, Tпл = 26 °С. Проте переважно вона перебуває в стані в’язкої рідини. Кут питомого обертання [α] = +3, 8°. Лівообертаюча (–)D молочна кислота є в’язкою рідиною, Tпл =18 °С, кут питомого обертання [α] = – 3, 8°. (–)D Молочна кислота утворюється також в умовах лужної обробки соку цукрового буряка. Вона міститься у кислому молоці, квашеній капусті і солоних огірках. Молочну кислоту використовують у харчовій (у виробництві кондитерських, хлібо пекарських виробів, у консервуванні, у виготовленні фруктових вод). , фармацевтичній, шкіряній та текстильній промисловості для фарбування тканин. Одержують зброджуванням сахарози під дією молочнокислих бактерій (50 °С) за схемою: C 6 H 12 O 6 2 CH 3–CH(OH)–COOH

БАГАТООСНОВНІ І БАГАТОАТОМНІ ГІДРОКСИКИСЛОТИ Гідроксибурштинова (яблучна) кислота НООССН(ОН)СН 2 СООН уперше виділена з яблук K. Шеєле у 1785 р. Вона дуже поширена у природі (міститься в яблуках, горобині, аґрусі, барбарисі, махорці тощо) кристалічна речовина з приємним кислим смаком, добре розчинна у воді. Відомі два енантіомери яблучної кислоти та оптично неактивна рацемічна яблучна кислота: (–)L–Яблучна кислота (+)D–Яблучна кислота (–)L Яблучна кислота Тпл = 99 100 °С, [α] = – 5, 7°, її добувають з ягід і незрілих яблук. (+)D Яблучна кислота має таку саму Тпл. , проте [α] = +5, 7°. Одержують відновленням (+) винної кислоти. (±) Яблучна кислота має Тпл= 129 130 °С, синтезують гідролізом галогенбурштинових кислот або приєднанням води до малеїнової кислоти. П. Вальден (1896 p. ), вивчаючи реакції яблучної кислоти, виявив, що з (+) ізомеру можна синтезувати (–) ізомер або з (+) яблучної кислоти – (–) хлоробурштинову, а потім – (–) яблучну кислоту. Отже, Вальдену вперше вдалося здійснити перетворення конфігурації біля асиметричного атома Карбону. Це явище дістало назву – вальденівське обертання:
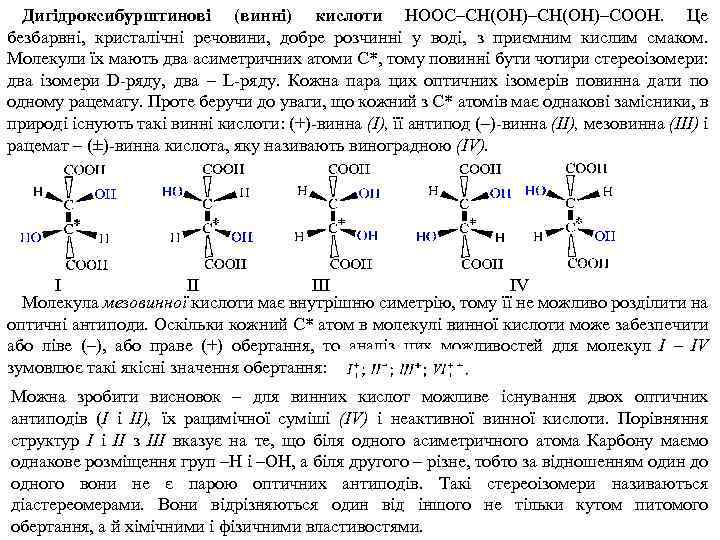
Дигідроксибурштинові (винні) кислоти НООС–СН(ОН)–СООН. Це безбарвні, кристалічні речовини, добре розчинні у воді, з приємним кислим смаком. Молекули їх мають два асиметричних атоми C*, тому повинні бути чотири стереоізомери: два ізомери D ряду, два – L ряду. Кожна пара цих оптичних ізомерів повинна дати по одному рацемату. Проте беручи до уваги, що кожний з С* атомів має однакові замісники, в природі існують такі винні кислоти: (+) винна (І), її антипод (–) винна (II), мезовинна (III) і рацемат – (±) винна кислота, яку називають виноградною (IV). I II IV Молекула мезовинної кислоти має внутрішню симетрію, тому її не можливо розділити на оптичні антиподи. Оскільки кожний С* атом в молекулі винної кислоти може забезпечити або ліве (–), або праве (+) обертання, то аналіз цих можливостей для молекул I – IV зумовлює такі якісні значення обертання: Можна зробити висновок – для винних кислот можливе існування двох оптичних антиподів (I і II), їх рацимічної суміші (IV) і неактивної винної кислоти. Порівняння структур I і II з III вказує на те, що біля одного асиметричного атома Карбону маємо однакове розміщення груп –H і –OH, а біля другого – різне, тобто за відношенням один до одного вони не є парою оптичних антиподів. Такі стереоізомери називаються діастереомерами. Вони відрізняються один від іншого не тільки кутом питомого обертання, а й хімічними і фізичними властивостями.
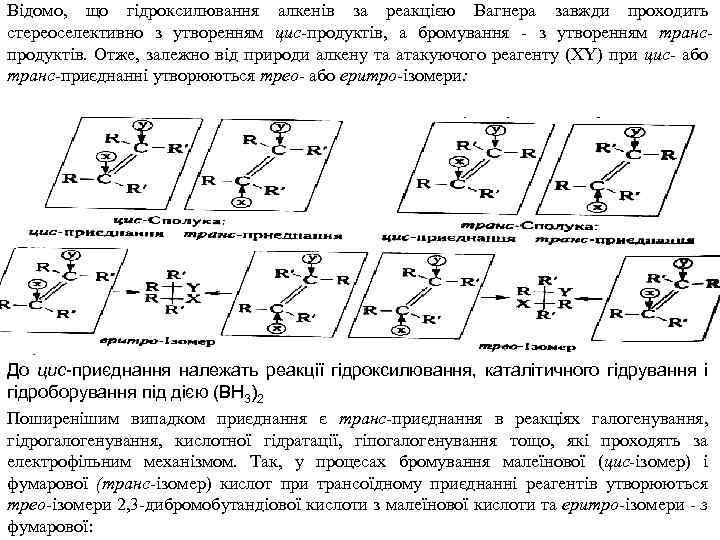
Відомо, що гідроксилювання алкенів за реакцією Вагнера завжди проходить стереоселективно з утворенням цис продуктів, а бромування з утворенням транс продуктів. Отже, залежно від природи алкену та атакуючого реагенту (XY) при цис- або транс приєднанні утворюються трео- або еритро ізомери: До цис-приєднання належать реакції гідроксилювання, каталітичного гідрування і гідроборування під дією (ВН 3)2 Поширенішим випадком приєднання є транс приєднання в реакціях галогенування, гідрогалогенування, кислотної гідратації, гіпогалогенування тощо, які проходять за електрофільним механізмом. Так, у процесах бромування малеїнової (цис ізомер) і фумарової (транс-ізомер) кислот при трансоїдному приєднанні реагентів утворюються трео ізомери 2, 3 дибромобутандіової кислоти з малеїнової кислоти та еритро-ізомери - з фумарової:
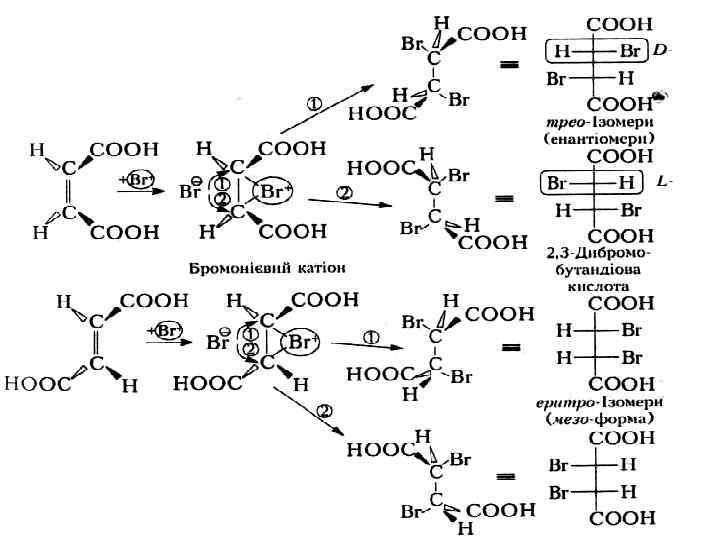
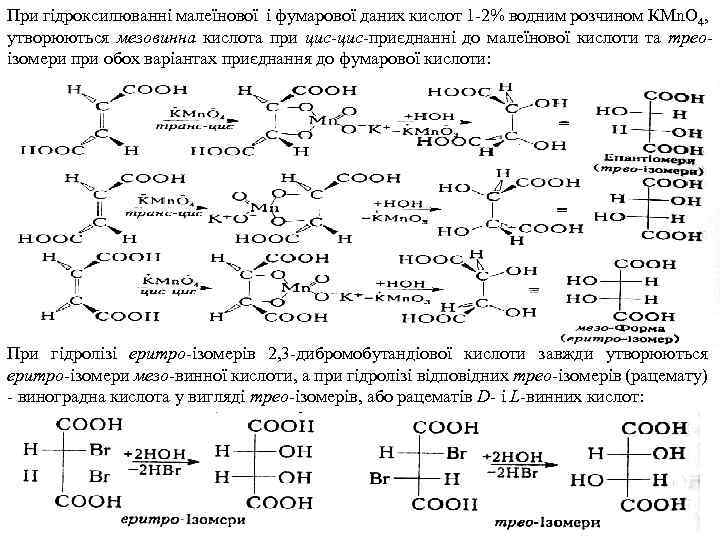
При гідроксилюванні малеїнової і фумарової даних кислот 1 2% водним розчином КМn. О 4, утворюються мезовинна кислота при цис-приєднанні до малеїнової кислоти та трео ізомери при обох варіантах приєднання до фумарової кислоти: При гідролізі еритро ізомерів 2, 3 дибромобутандіової кислоти завжди утворюються еритро-ізомери мезо винної кислоти, а при гідролізі відповідних трео ізомерів (рацемату) виноградна кислота у вигляді трео ізомерів, або рацематів D- і L винних кислот:
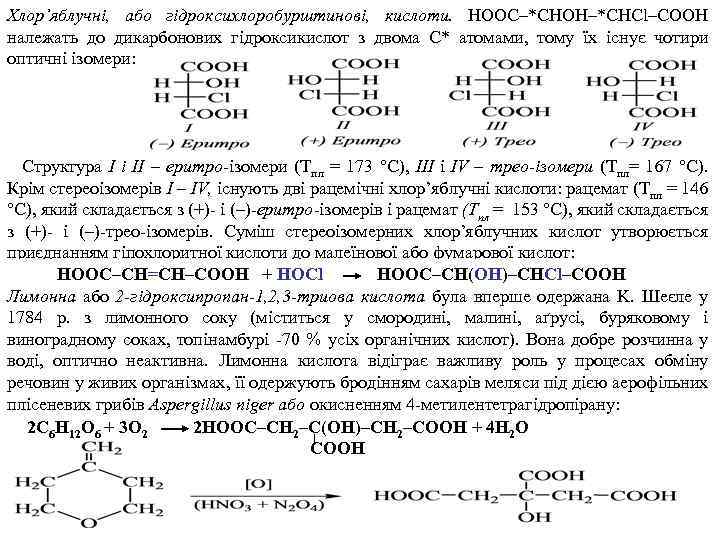
Хлор’яблучні, або гідроксихлоробурштинові, кислоти. НООС–*CHOH–*CHCl–COOH належать до дикарбонових гідроксикислот з двома С* атомами, тому їх існує чотири оптичні ізомери: Структура І і II – еритро ізомери (Тпл = 173 °C), III і IV – трео-ізомери (Тпл= 167 °С). Крім стереоізомерів І – IV, існують дві рацемічні хлор’яблучні кислоти: рацемат (Тпл = 146 °С), який складається з (+) і (–) еритро ізомерів і рацемат (Тпл = 153 °С), який складається з (+) і (–) трео ізомерів. Суміш стереоізомерних хлор’яблучних кислот утворюється приєднанням гіпохлоритної кислоти до малеїнової або фумарової кислот: НООС–СН=СН–СООН + HOCl НООС–СН(ОН)–СНCl–СООН Лимонна або 2 -гідроксипропан-1, 2, 3 -триова кислота була вперше одержана K. Шеєле у 1784 р. з лимонного соку (міститься у смородині, малині, аґрусі, буряковому і виноградному соках, топінамбурі 70 % усіх органічних кислот). Вона добре розчинна у воді, оптично неактивна. Лимонна кислота відіграє важливу роль у процесах обміну речовин у живих організмах, її одержують бродінням сахарів меляси під дією аерофільних плісеневих грибів Aspergillus niger або окисненням 4 метилентетрагідропірану: 2 C 6 H 12 O 6 + 3 О 2 2 НООС–СН 2–С(ОН)–CН 2–СООН + 4 H 2 O СООН
Oksi-kisloti-10.ppt