8 в основания.ppt
- Количество слайдов: 34

Гидроксиды. Основания: способы получения.

Цель урока: Углубить знания о важнейших классах веществ неорганической химии

Формулы только оксидов приведены в ряду: 1. 2. 3. 4. H 2 SO 3, Be. O, Cu. Cl 2 Na 2 CO 3, Na 2 O, Cl 2 O 7 CO 2, Li 2 O, Cr. O 3 KOH, K 2 O, Ba. O

Не характеризует свойство основных оксидов: 1. 2. 3. 4. Ca. O + H 2 O → Ca(OH)2 SO 3 + Na 2 O → Na 2 SO 4 K 2 O + 2 HCl → 2 KCl + H 2 O Zn(OH)2 → Zn. O + H 2 O

Назовите вещества: CO Na 2 O

Гидроксиды. Основания: способы получения.

План урока: Гидроксиды. Основания: способы получения Что надо узнать: Состав и названия Физические свойства Способы получения Определение Классификаци я Роль в жизни человека

K 2 O + H 2 O → 2 KOH

K 2 O + H 2 O → 2 KOH Гидроксиды – это сложные вещества в состав которых входят атомы металлов и гидроксогруппы ОН. !!! Число гидроксогрупп в формуле гидроксида соответствует валентности металла

Гидроксиды. Основания: способы получения.

Основания - это гидроксиды металлов IА и IIА (кроме Be), а также металлов в минимальной степени окисления (если она имеет переменное значение) • Например: Na. OH, Li. OH, Mg(OH)2, Ca(OH)2, Cr(OH)2, Mn(OH)2.

Работа с учебником: Стр 137 «Классификация гидроксидов» Стр 139 «Физические свойства оснований» ? На какие группы можно классифицировать основания? ? Физические свойства оснований?

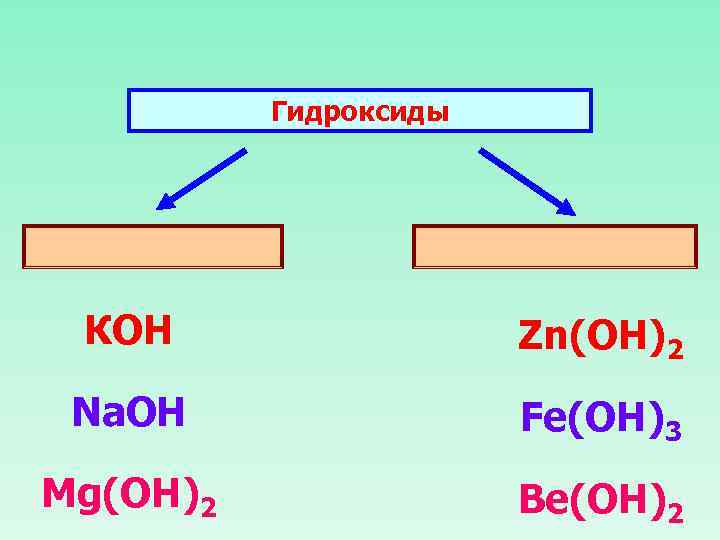
Гидроксиды КОН Zn(ОН)2 Na. OH Fe(OH)3 Mg(OH)2 Be(OH)2
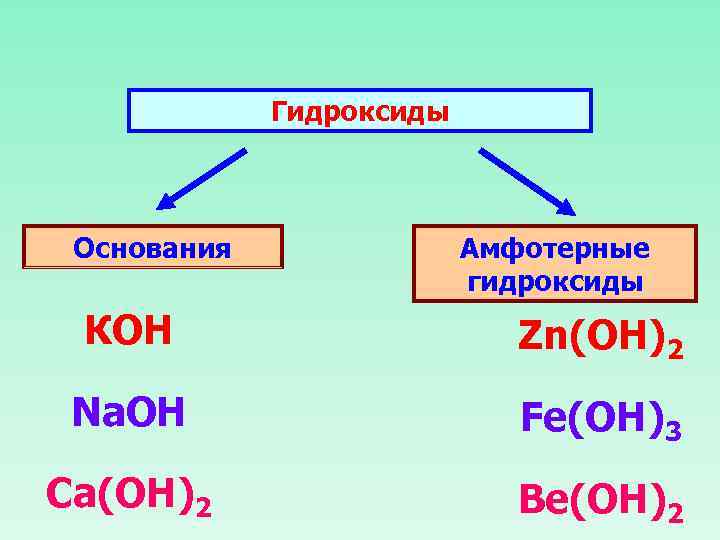
Гидроксиды Основания Амфотерные гидроксиды КОН Zn(ОН)2 Na. OH Fe(OH)3 Ca(OH)2 Be(OH)2
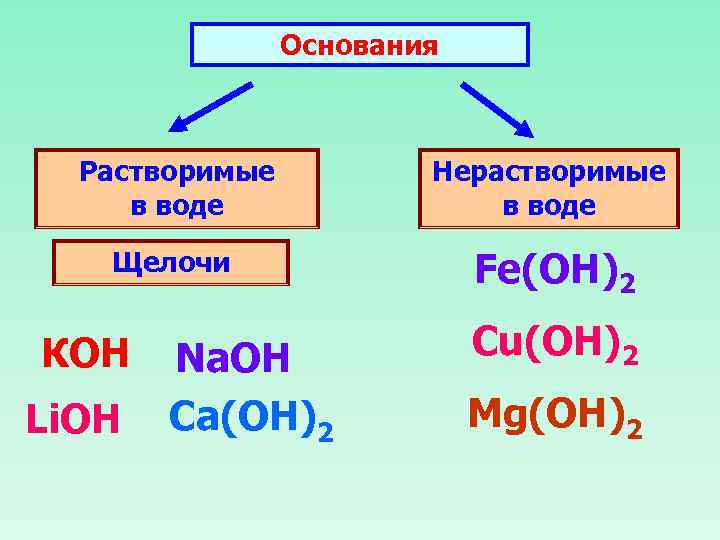
Основания Растворимые в воде Щелочи КОН Li. OH Na. OH Ca(ОН)2 Нерастворимые в воде Fe(OH)2 Cu(OH)2 Mg(ОН)2

Na. OH – гидроксид натрия, едкий каустическая сода натр,
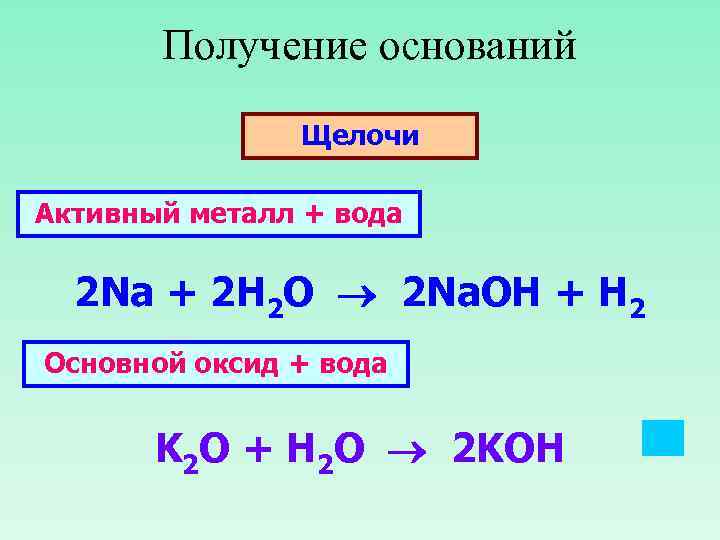
Получение оснований Щелочи Активный металл + вода 2 Na + 2 H 2 O 2 Na. OH + H 2 Основной оксид + вода K 2 O + H 2 O 2 KOH
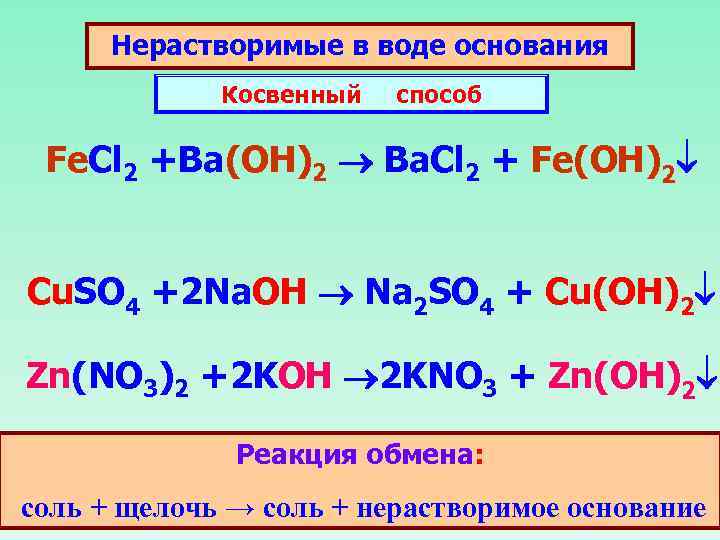
Нерастворимые в воде основания Косвенный способ Fe. Cl 2 +Ba(OH)2 Ba. Cl 2 + Fe(OH)2 Cu. SO 4 +2 Na. OH Na 2 SO 4 + Cu(OH)2 Zn(NO 3)2 +2 KOH 2 KNO 3 + Zn(OH)2 Реакция обмена: соль + щелочь → соль + нерастворимое основание

План урока: Гидроксиды. Основания: способы получения Что надо узнать: Состав и названия Определение Физические свойства Способы получения Классификация Роль в жизни человека

Домашнее задание: • § 41 • По задачнику

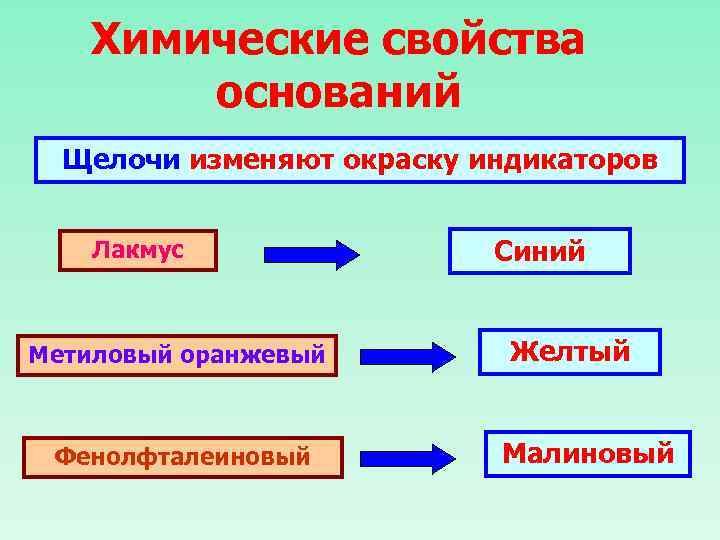
Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
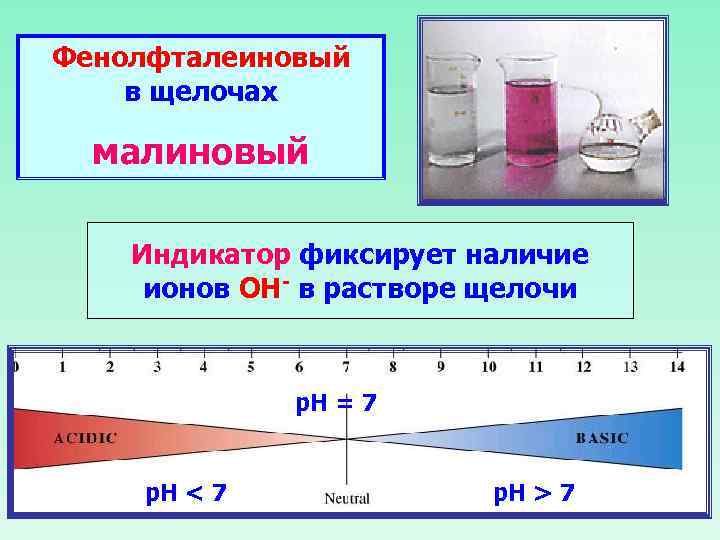
Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи р. Н = 7 р. Н < 7 р. Н > 7
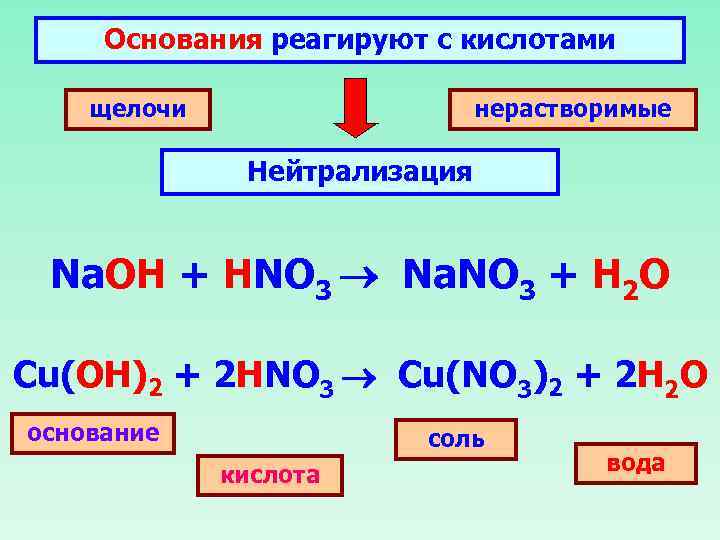
Основания реагируют с кислотами щелочи нерастворимые Нейтрализация Na. OH + HNO 3 Na. NO 3 + H 2 O Cu(OH)2 + 2 HNO 3 Cu(NO 3)2 + 2 H 2 O основание соль кислота вода
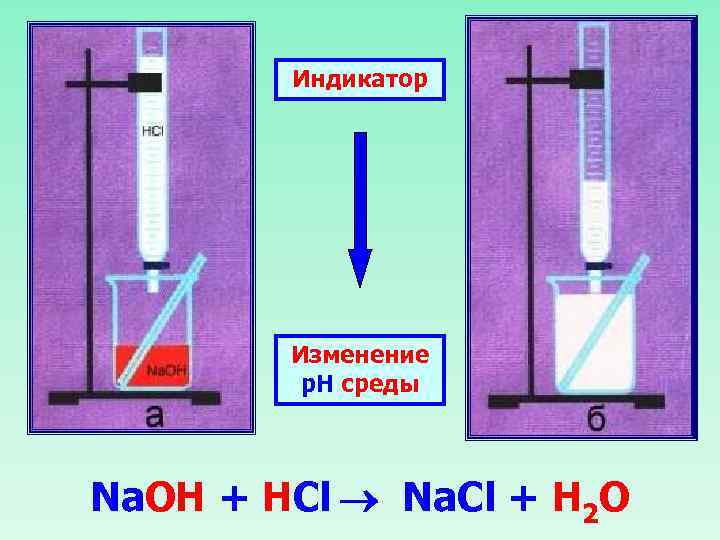
Индикатор Изменение р. Н среды Na. OH + HCl Na. Cl + H 2 O
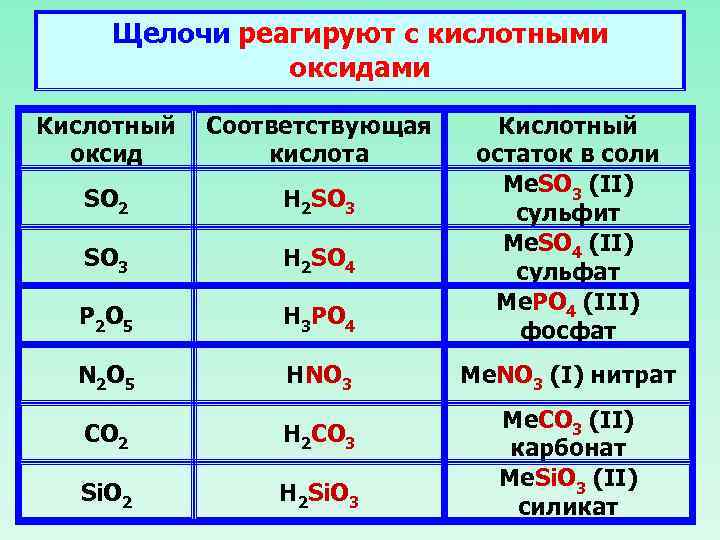
Щелочи реагируют с кислотными оксидами Кислотный Соответствующая оксид кислота SO 2 H 2 SO 3 H 2 SO 4 P 2 O 5 H 3 PO 4 Кислотный остаток в соли Me. SO 3 (II) сульфит Me. SO 4 (II) сульфат Me. PO 4 (III) фосфат N 2 O 5 HNO 3 Me. NO 3 (I) нитрат CO 2 H 2 CO 3 Si. O 2 H 2 Si. O 3 Me. CO 3 (II) карбонат Me. Si. O 3 (II) силикат
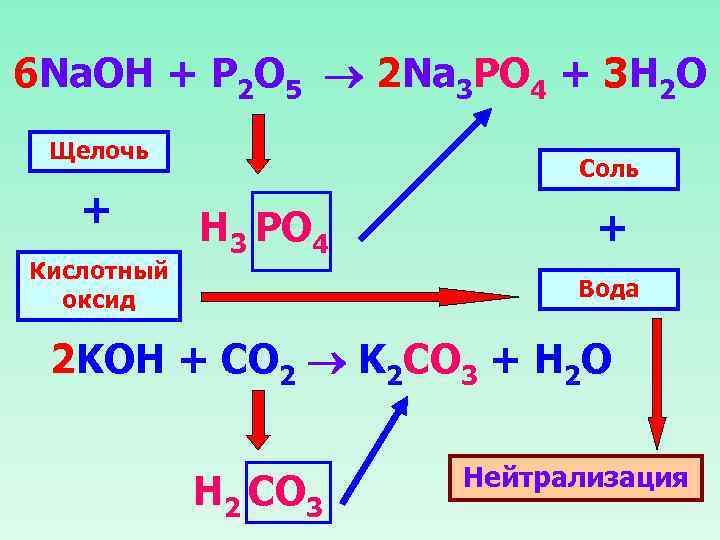
6 Na. OH + P 2 O 5 2 Na 3 PO 4 + 3 H 2 O Щелочь + Кислотный оксид Соль Н 3 PO 4 + Вода 2 KOH + CO 2 K 2 CO 3 + H 2 O Н 2 CO 3 Нейтрализация
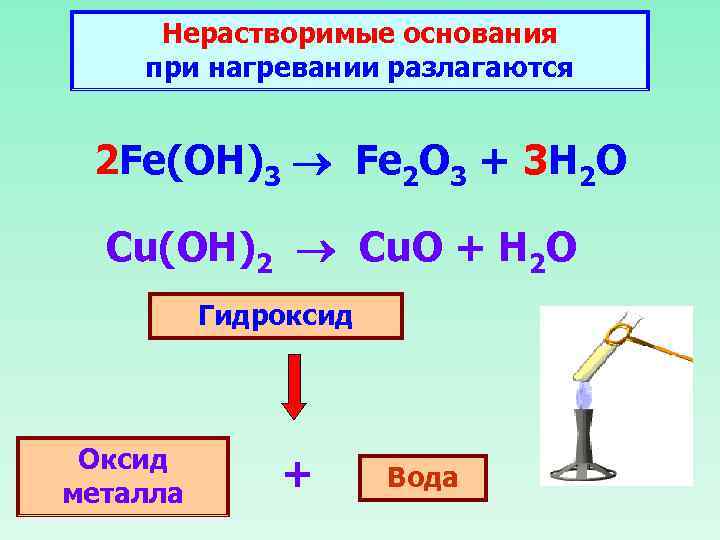
Нерастворимые основания при нагревании разлагаются 2 Fe(OH)3 Fe 2 O 3 + 3 H 2 O Cu(OH)2 Cu. O + H 2 O Гидроксид Оксид металла + Вода
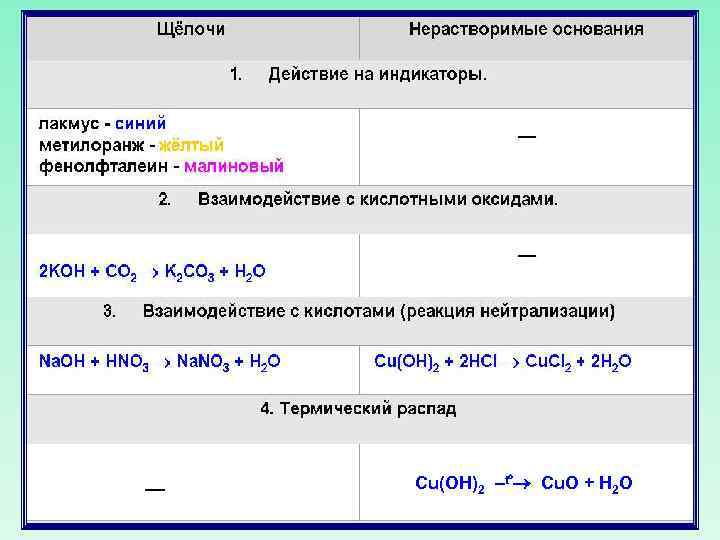
–– Cu(OH)2 –t° Cu. O + H 2 O

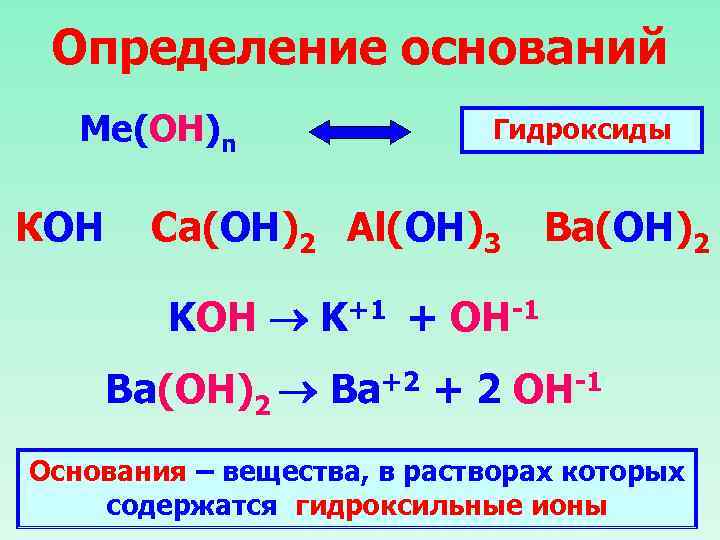
Определение оснований Ме(ОН)n Гидроксиды КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 KOH K+1 + OH-1 Ba(ОН)2 Ba+2 + 2 OH-1 Основания – вещества, в растворах которых содержатся гидроксильные ионы

Сильные и слабые основания Сильные основания Слабые основания Na. OH гидроксид Mg(OH)2 гидроксид натрия (едкий натр) магния KOH гидроксид калия Fe(OH)2 гидроксид (едкое кали) железа (II) Li. OH гидроксид Zn(OH)2 гидроксид лития цинка Ba(OH)2 гидроксид NH 4 OH гидроксид бария аммония Ca(OH)2 гидроксид Fe(OH)3 гидроксид кальция железа (III)
8 в основания.ppt