гидратация этилена Промышленные способы производства этанола


гидратация этилена
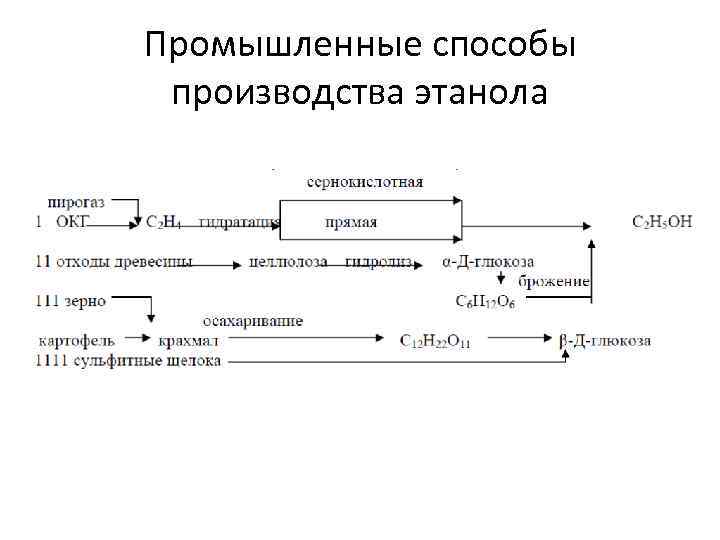
Промышленные способы производства этанола

Сернокислотная гидратация • 1 стадия 2 стадия

Прямая гидратация этилена • Основные условия взаимодействия газообразного этилена и водяных паров следующие: – температура 280 -3000 С; - давление 70 -80 атм. ; – концентрация этилена в циркулирующем газе 80 -85% об. , молярное отношение воды к этилену 0. 6 -0. 75: 1; – концентрация фосфорной кислоты на поверхности катализатора не ниже 83%, -объемная

Термодинамика количественно По Вант – Гоффу ln. Kp = ; +Qэкзо = -ΔН экзо; ln. Kp = Из этого уравнения следует: 1. С понижением температуры константа равновесия увеличивается, т. е. равновесие смещается направо. 2. Отвод тепла, связанный с температурой , также смещает равновесие направо. Концентрационная зависимость константы равновесия выражается уравнением: Хсп = Кр Хэтил Хводы Робщ Следовательно, при t =Const Kp = Const: для увеличения мольной доли спирта Хсп необходимо: 3. Увеличение чистоты этилена Хэтил. 4. Увеличение давления Робщ до 70 – 80 атм. 5. Небольшой избыток этилена, равный 1, 4 – 1, 8 по сравнением со стехиометрическим. При этом не вступивший в реакцию этилен легко отделяется от спирта и воды. Если взять избыток воды, то спирт сильно разбавляется водой и увеличиваются энергетические затраты по выделению спирта из водного раствора ректификацией.
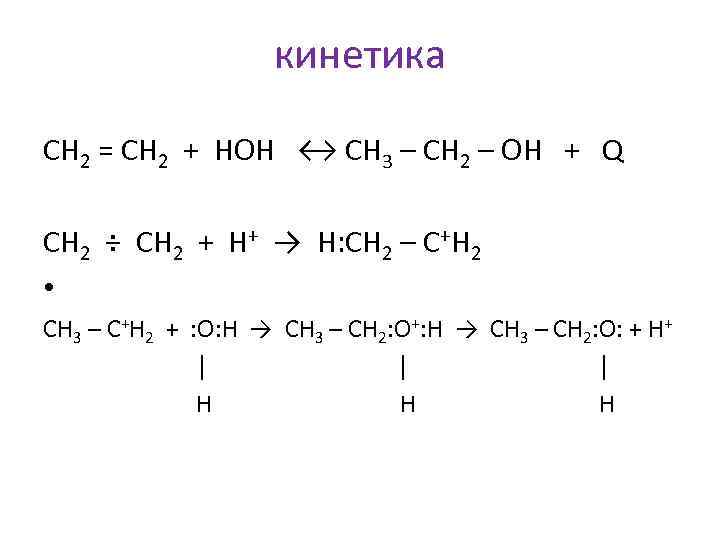
кинетика CH 2 = CH 2 + HOH ↔ CH 3 – CH 2 – OH + Q CH 2 ÷ CH 2 + H+ → H: CH 2 – C+H 2 • CH 3 – C+H 2 + : O: H → CH 3 – CH 2: O+: H → CH 3 – CH 2: O: + H+ │ H

W 1 = k 1 Pэтил Pводы F, где: Рэтил – парциальное давление этилена, Рводы – парциальное давление воды, F – удельная поверхность катализатора. Рэтил = Хэтил Робщ, Рводы = Хводы Робщ Хэтил, Хводы – мольные доли этилена и паров воды, Робщ – общее давление в реакционной системе. Тогда: W 1 = k 1 XC 2 H 4 XHOH Po 2 F, где: Po – Общее давление в реакционной системе. • Для увеличения скорости реакции необходимо: Увеличить чистоту этилена Хэтил ( чистота 75 – 80% ). Увеличить общее давление в системе Ро до 70 – 80 атмосфер. По Аррениусу: lnk 1 = lnko – E/RT Для увеличения константы скорости реакции k 1 необходимо повысить • температуру до 280 – 320 о. С. Выбор температуры сделан из требований кинетики, поэтому реакция проводится в условиях не благоприятных для термодинамики этого превращения. • Понизить энергию активации реакции Е за счет применения катализатора. В качестве катализатора применяют ортофосфорную кислоту H 3 PO 4. • Увеличить поверхность контакта в системе Г – Т. Для чего фосфорную кислоту на твердое тело окись кремния Si. O 2, имеющую развитую поверхность равную 150 – 200 м 2/г. 2 H 3 PO 4 → H 4 P 2 O 7 + H 2 O - Q 2.

Оптимальные условия – температура 280 -2900 С, давление 70 -80 атм. ; – концентрация этилена в циркулирующем газе 80 -85% об. , молярное отношение воды к этилену 0. 6 -0. 75: 1; – концентрация фосфорной кислоты на поверхности катализатора не ниже 83%, -объемная скорость 1800 -2500 ч-1.

Технологические стадии 1) приготовление исходной парогазовой смеси, 2) гидратация этилена, 3) нейтрализация паров продуктов, образующихся в результате реакции, 4) рекуперация тепла рециркулирующих потоков, 5) очистка циркулирующего газа.

Состав спирта–ректификата: этанол – 94% вода - 6% эфир - следы

Сравнение методов прямой и сернокислотной гидратации этилена Прямая гидратация этилена: Преимущества: • Более высокий выход спирта - 95% на превращенный этилен • Процесс проводится в одну стадию • Меньше расход этилена на 1 т. спирта. Недостатки: • Высокие требования к чистоте этилена до 75 – 80%. • Необходимость периодической смены катализатора и его захоронение. Сернокислотная гидратация этилена: Преимущества: Можно перерабатывать газы с низким содержанием этилена. На этом основана утилизация этилена из отходящих газов нефтепереработки. Недостатки: • Ниже выход спирта – 85%, поэтому более высокий расход этилена на 1 т. спирта. • В процессе получается большое количество разбавленной серной кислоты с концентрацией 65 – 67%, имеющей ограниченное применение. • В процессе много кислых стоков, что ухудшает экологическую обстановку водных бассейнов.
гидратация этилена.pptx
- Количество слайдов: 11

