Гибридизация.ppt
- Количество слайдов: 13

Гибридизация, её типы

КОНЦЕПЦИЯ ГИБРИДИЗАЦИИ ВАЛЕНТНЫХ АТОМНЫХ ОРБИТАЛЕЙ… …была предложена американским химиком Лайнусом Полингом для ответа на вопрос, почему при наличии у центрального атома разных (s, p, d) валентных орбиталей, образованные им связи в многоатомных молекулах с одинаковыми лигандами (атом, ион или молекула, связанные с неким центром) оказываются эквивалентными по своим энергетическим и пространственным характеристикам. Представления о гибридизации занимают центральное место в методе валентных связей. Сама гибридизация не является реальным физическим процессом, а только удобной моделью, позволяющей объяснить электронное строение молекул, в частности гипотетические видоизменения атомных орбиталей при образовании ковалентной химической связи, в частности, выравнивание длин химических связей и валентных углов в молекуле.
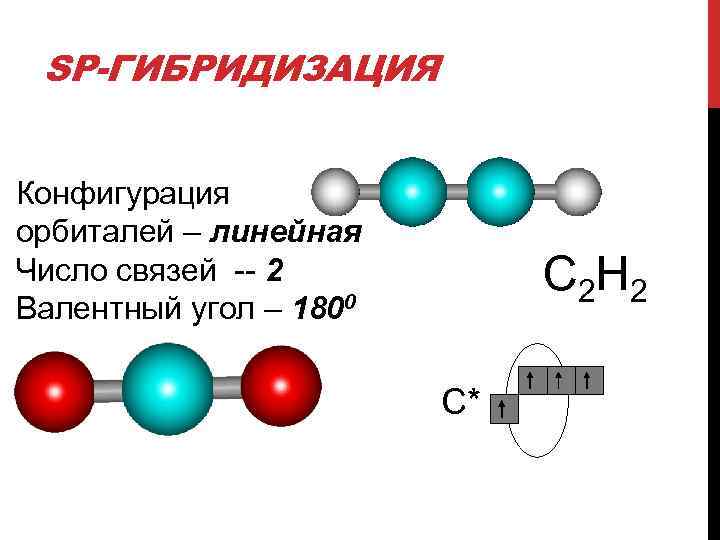
SP-ГИБРИДИЗАЦИЯ Конфигурация орбиталей – линейная Число связей -- 2 Валентный угол – 1800 C 2 H 2 СО 2 С*
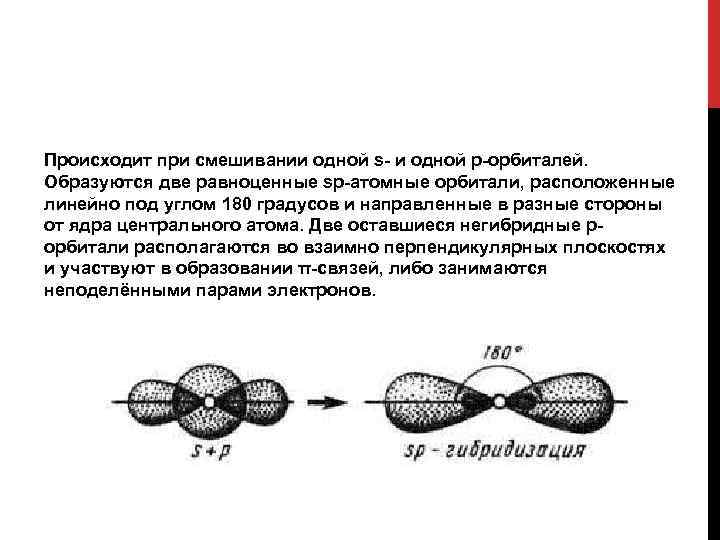
Происходит при смешивании одной s- и одной p-орбиталей. Образуются две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра центрального атома. Две оставшиеся негибридные pорбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются неподелёнными парами электронов.
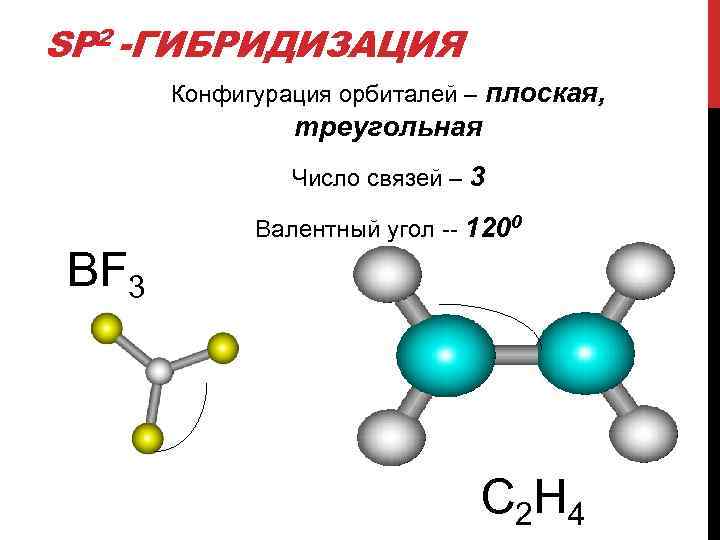
SP 2 -ГИБРИДИЗАЦИЯ Конфигурация орбиталей – плоская, треугольная Число связей – 3 Валентный угол -- 1200 BF 3 C 2 H 4
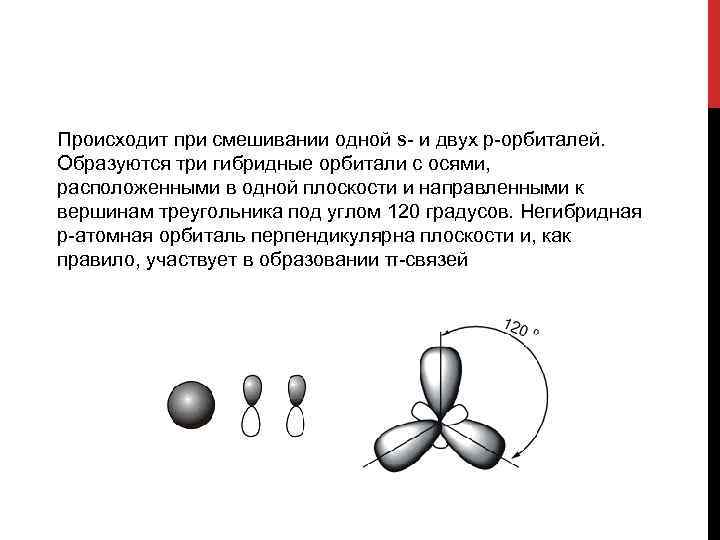
Происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей
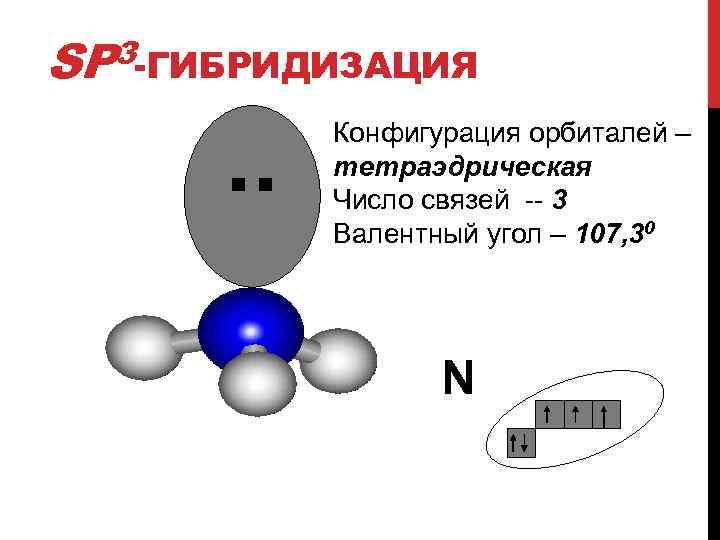
3 -ГИБРИДИЗАЦИЯ SP . . Конфигурация орбиталей – тетраэдрическая Число связей -- 3 Валентный угол – 107, 30 N

Происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp 3 -гибридные орбитали. Могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов. Оси sp 3 -гибридных орбиталей направлены к вершинам правильного тетраэдра, тогда как ядро центрального атома расположено в центре описанной сферы этого тетраэдра. Угол между любыми двумя осями приближённо равен 109° 28', что соответствует наименьшей энергии отталкивания электронов. Также sp 3 -орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов. Такое состояние характерно для атомов углерода в насыщенных углеводородах и соответственно в алкильных радикалах и их производных.
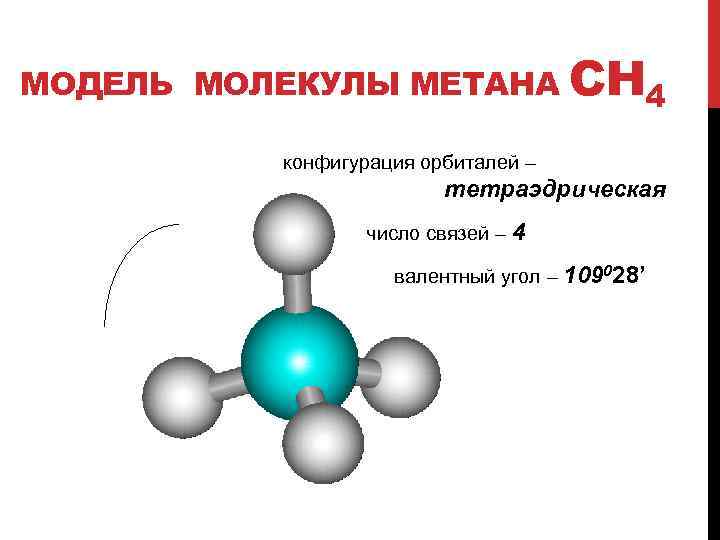
МОДЕЛЬ МОЛЕКУЛЫ МЕТАНА СН 4 конфигурация орбиталей – тетраэдрическая число связей – 4 валентный угол – 109028’
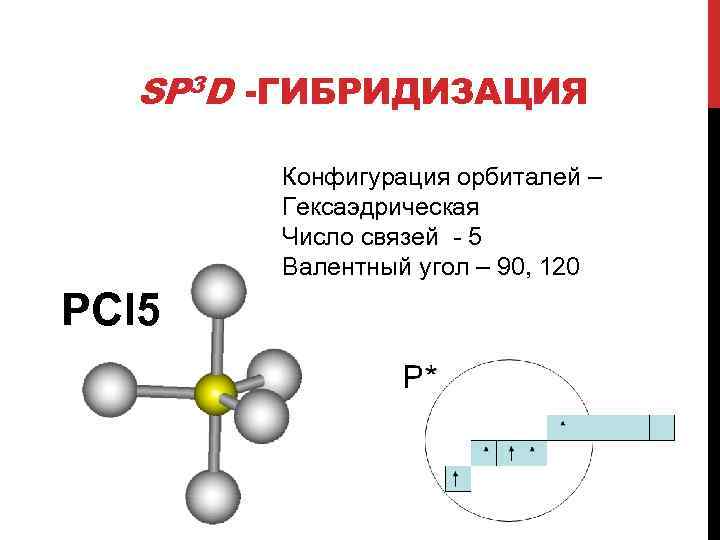
SP 3 D -ГИБРИДИЗАЦИЯ Конфигурация орбиталей – Гексаэдрическая Число связей - 5 Валентный угол – 90, 120 PCl 5
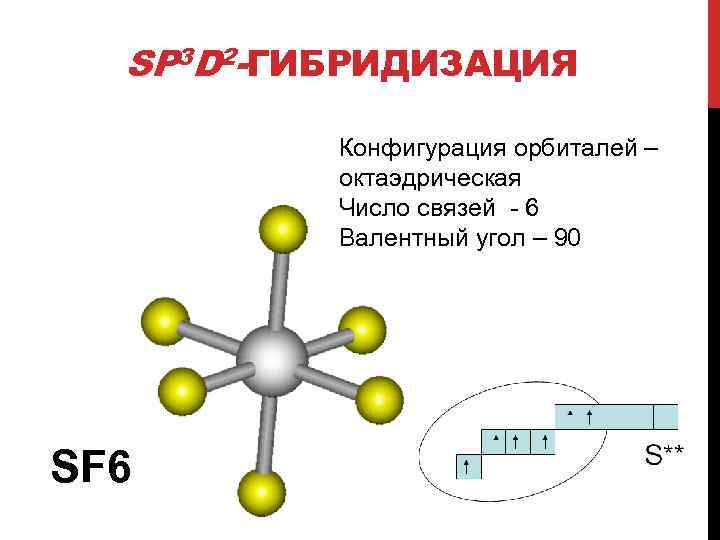
SP 3 D 2 -ГИБРИДИЗАЦИЯ Конфигурация орбиталей – октаэдрическая Число связей - 6 Валентный угол – 90 SF 6

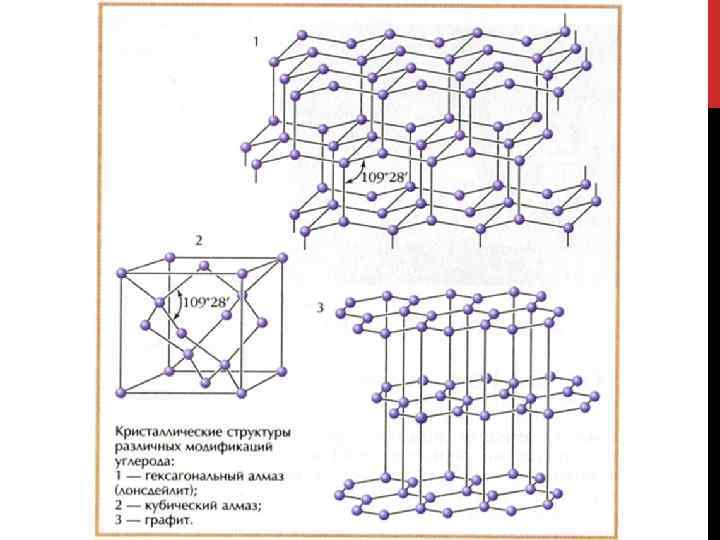
АЛЛОТРОПНЫЕ МОДИФИКАЦИИ УГЛЕРОДА 3 Алмаз - sp Графит - sp 2 Карбин - sp 2 Фуллерен - sp Аллотропия — существование двух и более простых веществ одного и того же химического элемента, различных по строению и свойствам — так называемых аллотропных (или аллотропических) модификаций или форм
Гибридизация.ppt