Гибридизация.ppt
- Количество слайдов: 8

Гибридизация -это смешение близких по энергии атомных орбиталей по форме и энергии

Условия гибридизации 1. число гибридных орбиталей ровно числу исходных 2. гибридные орбитали образуют только σ связи 3. подвергаются гибридизации могут одноэлектронные и двухэлектронные орбитали с близкими значениями энергии 4. гибридизация наиболее характерна для элементов 2 периода II и VI групп
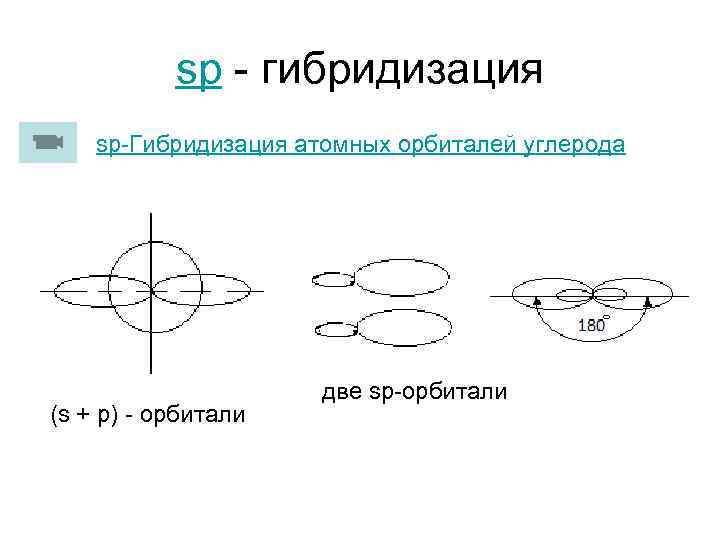
sp - гибридизация sp-Гибридизация атомных орбиталей углерода (s + p) - орбитали две sp-орбитали
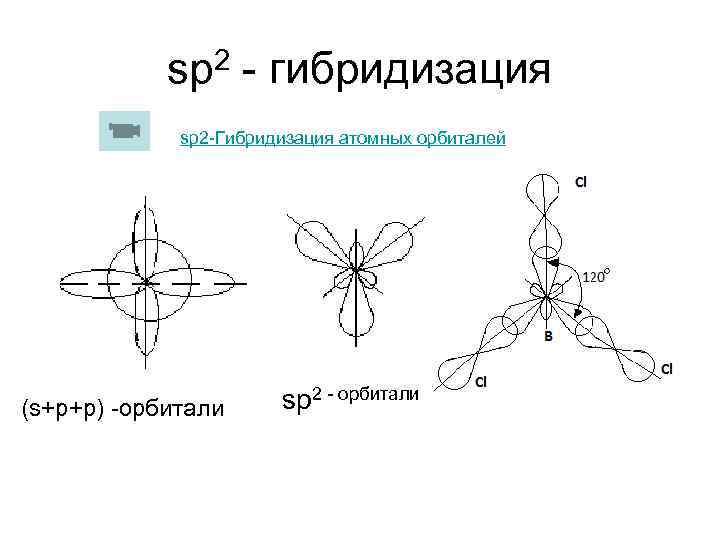
sp 2 - гибридизация sp 2 -Гибридизация атомных орбиталей (s+p+p) -орбитали sp 2 - орбитали
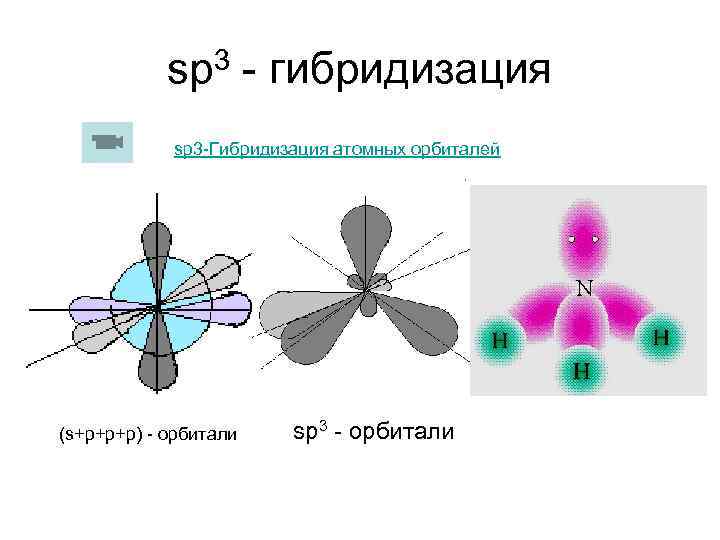
sp 3 - гибридизация sp 3 -Гибридизация атомных орбиталей (s+p+p+p) - орбитали sp 3 - орбитали

Задание • Определите элементы, которым соответствуют электронные конфигурации валентных электронов: • … 2 s 22 p 2 и . . . 3 s 23 p 5 • а) напишите формулы молекулы, образованной атомами этих элементов • б) определите тип химической связи в этой молекуле, составьте ее электронную формулу и изобразите схему перекрывания атомных орбиталей
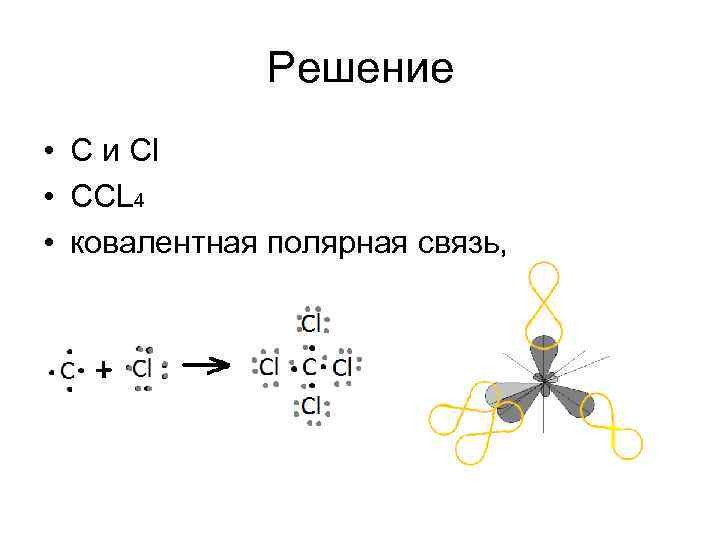
Решение • С и Cl • CCL 4 • ковалентная полярная связь,

Домашнее задание • • Выучить лекцию Изобразить схему типы гибридизации в формате А 4. Подготовиться к контрольной работе. Повторить конспекты 1 -6 урок
Гибридизация.ppt