Гибридизация атомных орбиталей.ppt
- Количество слайдов: 15

«Гибридизация атомных орбиталей и геометрия молекул. »

Лайнус Полинг 1901 – 1994 • Американский химик, лауреат 2 -х Нобелевских премий, а также Международной Ленинской премии «За укрепление мира между народами» • Главное научное достижение Полинга — теория химической связи, разработанная им в конце 1920 -х — начале 1930 -х годов и полностью изложенная в его книге «Природа химической связи» • В 1954 году Нобелевский комитет удостоил Полинга премии по химии «за изучение природы химической связи и его применение к объяснению строения сложных молекул» • Полинг был президентом Американского химического общества, Тихоокеанского отделения Американской ассоциации содействия развитию науки и вице-президентом Американского философского общества • Имя Полинга включено в список 20 величайших учёных всех времён, составленный по результатам опроса учёных
2 SP 3 SP SP Гибридизация 3 d SP 3 d 2 SP 3 d 3 SP

Основные положения теории гибридизации Тип гибридизации определяется числом образованных атомом σ-связей + свободные неподелённые электронные пары или неспаренные электроны. Геометрия молекулы или иона определяется типом гибридизации центрального атома с учётом его координационного числа. Координационное число (к. ч. ) определяется числом σ-связей, которые образует центральный атом с другими атомами. 4
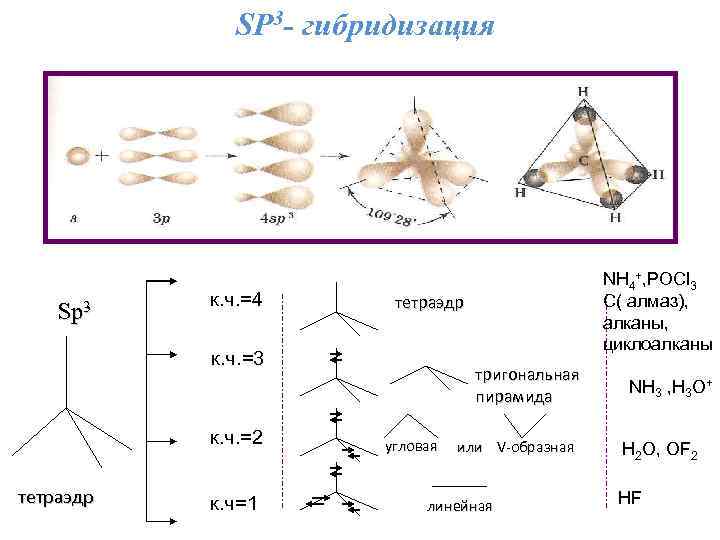
SР 3 - гибридизация Sp 3 к. ч. =4 тетраэдр к. ч. =3 к. ч. =2 тетраэдр к. ч=1 NH 4+, РОСl 3 С( алмаз), алканы, циклоалканы тригональная пирамида угловая или V-образная линейная NH 3 , H 3 O+ H 2 O, OF 2 НF
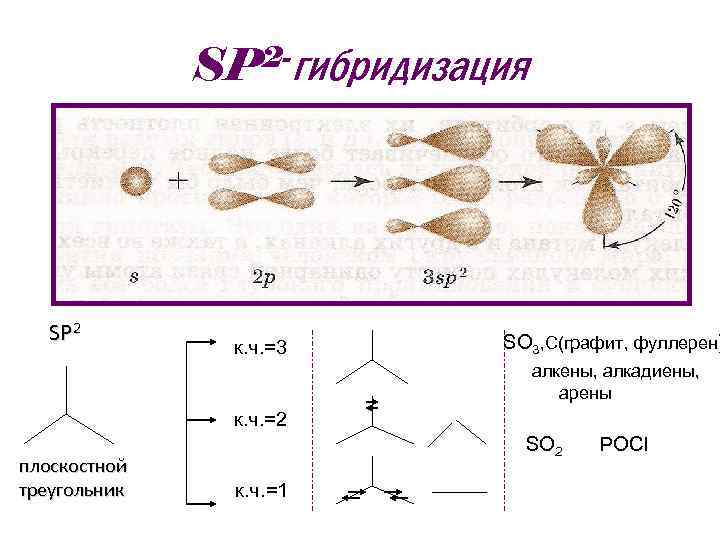
2 SP SP 2 к. ч. =3 гибридизация SO 3, С(графит, фуллерен) алкены, алкадиены, арены к. ч. =2 плоскостной треугольник к. ч. =1 SO 2 РОCI
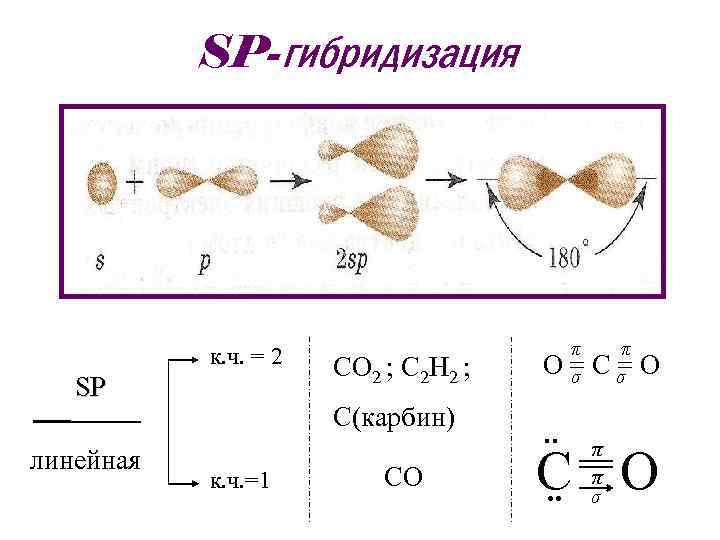
SP-гибридизация к. ч. = 2 SP линейная СО 2 ; С 2 Н 2 ; С(карбин) к. ч. =1 СО О π = σ ¨ С ¨ π Сσ = π π σ О О
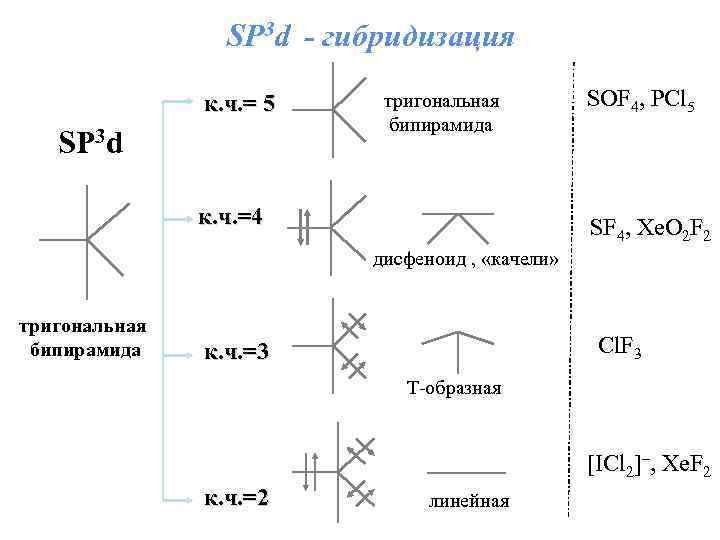
SР 3 d - гибридизация к. ч. = 5 SР 3 d тригональная бипирамида к. ч. =4 SOF 4, PCl 5 SF 4, Хе. О 2 F 2 дисфеноид , «качели» тригональная бипирамида Сl. F 3 к. ч. =3 Т-образная [IСl 2]–, Xe. F 2 к. ч. =2 линейная
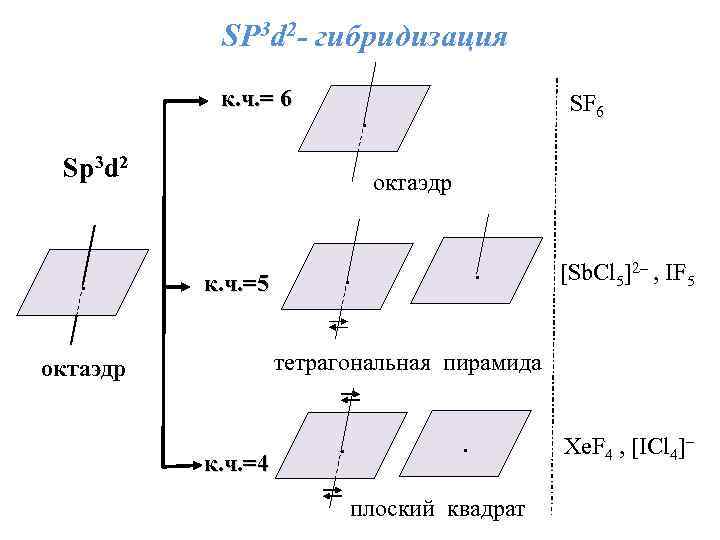
SР 3 d 2 - гибридизация к. ч. = 6 . Sp 3 d 2 . SF 6 октаэдр к. ч. =5 . . [Sb. Сl 5]2– , IF 5 тетрагональная пирамида октаэдр к. ч. =4 . . плоский квадрат Xe. F 4 , [ICl 4]–
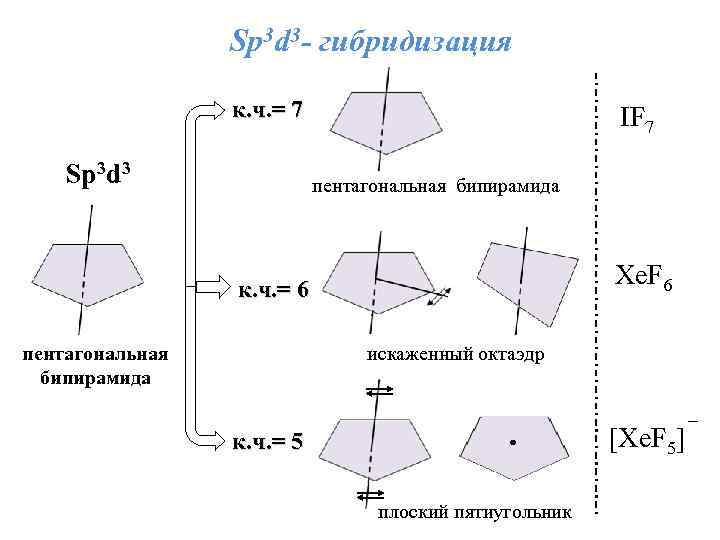
Sр3 d 3 - гибридизация к. ч. = 7 Sр3 d 3 IF 7 пентагональная бипирамида Хе. F 6 к. ч. = 6 пентагональная бипирамида искаженный октаэдр [Хе. F 5] к. ч. = 5 плоский пятиугольник –
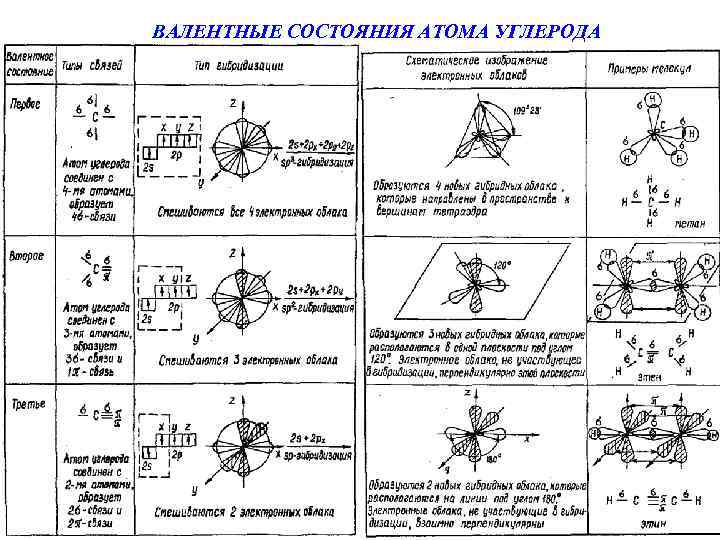
ВАЛЕНТНЫЕ СОСТОЯНИЯ АТОМА УГЛЕРОДА

Алгоритм для определения гибридизации и геометрии

CH 4 1) Пишем электронную формулу атома углерода 2) Пишем графическую формулу, анализируем связи C – 1 S 2 2 p 2 6 C – [2 He] 2 S 2 2 p 2 6 H σ σ σ H – C – H σ H 3) Определяем сколько валентных электронов расходуется на образование связей 4ē → 4σ 4) Тип гибридизации определяем по числу σ-связей + НП 4σ → SР 3 5) Координационное число (к. ч. ) определяем по количеству σ-связей 4σ → к. ч. (C) = 4 6) Определяем гибридные АО и геометрию молекулы H C к. ч. =4 Sр3 - гибридизация тетраэдр H H H
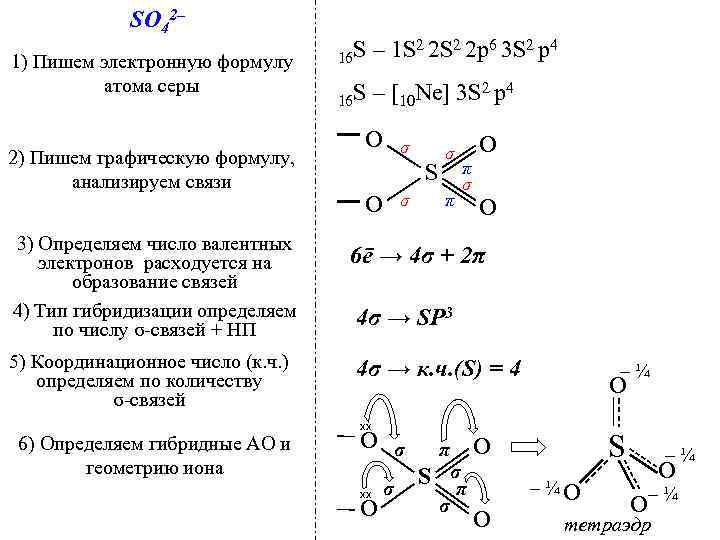
SО 42– 1) Пишем электронную формулу атома серы 2) Пишем графическую формулу, анализируем связи 16 S – 1 S 2 2 p 6 3 S 2 p 4 16 S – [10 Ne] 3 S О σ 2 p 4 σ О π S σ 3) Определяем число валентных электронов расходуется на образование связей 4) Тип гибридизации определяем по числу σ-связей + НП 6ē → 4σ + 2π 5) Координационное число (к. ч. ) определяем по количеству σ-связей 4σ → к. ч. (S) = 4 4σ → SР 3 – ¼ О хх 6) Определяем гибридные АО и геометрию иона О σ π σ S σ π хх О σ S О – ¼ О О – ¼ тетраэдр
![[SF 5] – 1) S 16 – [10 Ne] 3 S 2 p 4 [SF 5] – 1) S 16 – [10 Ne] 3 S 2 p 4](https://present5.com/presentation/33004594_131834747/image-15.jpg)
[SF 5] – 1) S 16 – [10 Ne] 3 S 2 p 4 2) F F σ S+4 – [10 Ne] 3 S 2 σ σ S окисления +4 образовались по донорноакцепторному механизму и осталась одна НП σ σ F F 3) 5 σ-связей фторид ионов с серой в степени F 5σ + НП→ SР 3 d 2 4) 5σ → к. ч. (S) = 5 5) — F. F F S F F тетрагональная пирамида
Гибридизация атомных орбиталей.ppt