важнейшие классы неорганических соеденений.ppt
- Количество слайдов: 58
 ГИА. 9 класс Государственная (итоговая) аттестация 2011 года (в новой форме) по ХИМИИ обучающихся, освоивших основные общеобразовательные программы 120 минут
ГИА. 9 класс Государственная (итоговая) аттестация 2011 года (в новой форме) по ХИМИИ обучающихся, освоивших основные общеобразовательные программы 120 минут
 Часть А 2 -3 минуты на задание 15 заданий
Часть А 2 -3 минуты на задание 15 заданий
 А 1 Число электронов во внешнем электронном слое атома, ядро которого содержит 8 протонов, равно 1) 8 2) 2 3) 6 4) 4 Строение атома. Строение электронных оболочек атомов первых 20 элементов периодической системы Д. И. Менделеева.
А 1 Число электронов во внешнем электронном слое атома, ядро которого содержит 8 протонов, равно 1) 8 2) 2 3) 6 4) 4 Строение атома. Строение электронных оболочек атомов первых 20 элементов периодической системы Д. И. Менделеева.
 А 1 • Атому какого химического элемента соответствует приведенная ниже схема строения? 1) аргона 2) кислорода 3) серы 4) кальция
А 1 • Атому какого химического элемента соответствует приведенная ниже схема строения? 1) аргона 2) кислорода 3) серы 4) кальция
 А 2 Неметаллические свойства фосфора выражены сильнее, чем неметаллические свойства 1) кислорода 2) азота 3) алюминия 4) хлора Периодический закон и периодическая система химических элементов Д. И. Менделеева.
А 2 Неметаллические свойства фосфора выражены сильнее, чем неметаллические свойства 1) кислорода 2) азота 3) алюминия 4) хлора Периодический закон и периодическая система химических элементов Д. И. Менделеева.
 А 2 От кислотных к оснóвным меняются свойства оксидов в ряду 1) Ca. O → Si. O 2 → SO 3 2) CO 2 → Al 2 O 3 → Mg. O 3) SO 3 → P 2 O 5 → Al 2 O 3 4) Na 2 O → Mg. O → Al 2 O 3
А 2 От кислотных к оснóвным меняются свойства оксидов в ряду 1) Ca. O → Si. O 2 → SO 3 2) CO 2 → Al 2 O 3 → Mg. O 3) SO 3 → P 2 O 5 → Al 2 O 3 4) Na 2 O → Mg. O → Al 2 O 3
 А 3 Ковалентная полярная связь образуется между атомами 1) натрия и брома 2) серы и кислорода 3) водорода 4) калия и хлора Строение молекул. Химическая связь: ковалентная (полярная и неполярная), ионная, металлическая.
А 3 Ковалентная полярная связь образуется между атомами 1) натрия и брома 2) серы и кислорода 3) водорода 4) калия и хлора Строение молекул. Химическая связь: ковалентная (полярная и неполярная), ионная, металлическая.
 А 3 Какой вид химической связи в молекуле аммиака? 1) ковалентная неполярная 2) ковалентная полярная 3) металлическая 4) ионная
А 3 Какой вид химической связи в молекуле аммиака? 1) ковалентная неполярная 2) ковалентная полярная 3) металлическая 4) ионная
 А 4 Атомы азота и углерода имеют одинаковую степень окисления в соединениях 1) NH 3 и CO 2) NO 2 и ССl 4 3) N 2 O 3 и СО 2 4) Na 3 N и CH 4 Валентность химических элементов. Степень окисления химических элементов.
А 4 Атомы азота и углерода имеют одинаковую степень окисления в соединениях 1) NH 3 и CO 2) NO 2 и ССl 4 3) N 2 O 3 и СО 2 4) Na 3 N и CH 4 Валентность химических элементов. Степень окисления химических элементов.
 А 4 Такую же степень окисления, как и в SO 2, сера имеет в соединении 1) K 2 SO 4 2) H 2 SO 3 3) (NH 4)2 S 4) SO 3
А 4 Такую же степень окисления, как и в SO 2, сера имеет в соединении 1) K 2 SO 4 2) H 2 SO 3 3) (NH 4)2 S 4) SO 3
 А 5 Сложным является каждое из двух веществ: 1) аммиак и серная кислота 2) медь и гидроксид натрия 3) сульфат бария и водород 4) вода и алмаз Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура неорганических соединений.
А 5 Сложным является каждое из двух веществ: 1) аммиак и серная кислота 2) медь и гидроксид натрия 3) сульфат бария и водород 4) вода и алмаз Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура неорганических соединений.
 А 5 Оснóвным оксидом и кислотой, соответственно, являются 1) Fe. O, Ba(OН)2 2) K 2 O, (NH 4)2 S 3) Mg. O, H 2 SO 4 4) SO 2, HNO 3
А 5 Оснóвным оксидом и кислотой, соответственно, являются 1) Fe. O, Ba(OН)2 2) K 2 O, (NH 4)2 S 3) Mg. O, H 2 SO 4 4) SO 2, HNO 3
 А 6 К химическим явлениям относится процесс 1) образования инея 2) плавления парафиновой свечи 3) горения древесины 4) распространения запаха духов Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях. Классификация химических реакций по различным признакам: числу и составу исходных и полученных веществ, изменению степеней окисления химических элементов, поглощению и выделению энергии.
А 6 К химическим явлениям относится процесс 1) образования инея 2) плавления парафиновой свечи 3) горения древесины 4) распространения запаха духов Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях. Классификация химических реакций по различным признакам: числу и составу исходных и полученных веществ, изменению степеней окисления химических элементов, поглощению и выделению энергии.
 А 6 Какая из записей соответствует уравнению окислительновосстановительной реакции? 1) CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O 2) 2 HBr + Na 2 O = 2 Nа. Br + H 2 O 3) H 2 SО 4 + Bа. O = Bа. SО 4 + H 2 O 4) 2 NO 2 + H 2 O = HNO 3 + HNO 2
А 6 Какая из записей соответствует уравнению окислительновосстановительной реакции? 1) CO 2 + Ca(OH)2 = Ca. CO 3 + H 2 O 2) 2 HBr + Na 2 O = 2 Nа. Br + H 2 O 3) H 2 SО 4 + Bа. O = Bа. SО 4 + H 2 O 4) 2 NO 2 + H 2 O = HNO 3 + HNO 2
 А 6 К химическим явлениям относится процесс 1) измельчения сахара до состояния пудры 2) превращения воды в лед 3) появления капель воды на крышке чайника 4) горения свечи
А 6 К химическим явлениям относится процесс 1) измельчения сахара до состояния пудры 2) превращения воды в лед 3) появления капель воды на крышке чайника 4) горения свечи
 А 7 Вещество, при диссоциации которого образуется сульфид-ион, имеет формулу 1) Na 2 S 2) S Электролиты и неэлектролиты. 3) K 2 SO 3 Катионы и анионы 4) Cu. SO 4 Электролитическая диссоциация кислот, щелочей и солей (средних).
А 7 Вещество, при диссоциации которого образуется сульфид-ион, имеет формулу 1) Na 2 S 2) S Электролиты и неэлектролиты. 3) K 2 SO 3 Катионы и анионы 4) Cu. SO 4 Электролитическая диссоциация кислот, щелочей и солей (средних).
 А 7 3 моль катионов образуется при полной диссоциации 1 моль 1) фосфата натрия 2) нитрата алюминия 3) хлорида железа(III) 4) гидроксида кальция
А 7 3 моль катионов образуется при полной диссоциации 1 моль 1) фосфата натрия 2) нитрата алюминия 3) хлорида железа(III) 4) гидроксида кальция
 А 7 Наименьшее число ионов образуется в растворе при полной диссоциации 1 моль 1) Fe. Cl 3 2) Na 2 S 3) KNO 3 4) Ba. Cl 2
А 7 Наименьшее число ионов образуется в растворе при полной диссоциации 1 моль 1) Fe. Cl 3 2) Na 2 S 3) KNO 3 4) Ba. Cl 2
 А 8 Выделение газа происходит при нагревании раствора, содержащего ионы 1) NH 4+ и SO 42– 2) H+ и Si. O 32– 3) H+ и OH– 4) NH 4+ и OH– Реакции ионного обмена и условия их осуществления.
А 8 Выделение газа происходит при нагревании раствора, содержащего ионы 1) NH 4+ и SO 42– 2) H+ и Si. O 32– 3) H+ и OH– 4) NH 4+ и OH– Реакции ионного обмена и условия их осуществления.
 А 8 Сокращенному ионному уравнению Ba 2+ + SO 42 - = Ba. SO 4↓ соответствует левая часть схемы химической реакции 1) Ba. Сl 2 + H 2 SO 4 → 2) Ba. CO 3 + Na 2 SO 4 → 3) Ba. O + SO 3 → 4) Ba + H 2 SO 4 →
А 8 Сокращенному ионному уравнению Ba 2+ + SO 42 - = Ba. SO 4↓ соответствует левая часть схемы химической реакции 1) Ba. Сl 2 + H 2 SO 4 → 2) Ba. CO 3 + Na 2 SO 4 → 3) Ba. O + SO 3 → 4) Ba + H 2 SO 4 →
 А 9 И кислород, и водород вступают в кислород реакцию с 1) Fe. O 2) Ca. O 3) NH 3 4) H 2 S Химические свойства простых веществ: металлов и неметаллов
А 9 И кислород, и водород вступают в кислород реакцию с 1) Fe. O 2) Ca. O 3) NH 3 4) H 2 S Химические свойства простых веществ: металлов и неметаллов
 А 9 И литий, и железо при комнатной литий температуре реагируют с 1) гидроксидом натрия 2) водой 3) серой 4) соляной кислотой
А 9 И литий, и железо при комнатной литий температуре реагируют с 1) гидроксидом натрия 2) водой 3) серой 4) соляной кислотой
 А 10 Оксид магния реагирует с 1) KCl 2) Na. OH 3) SO 3 4) Ba. SO 4 Химические свойства оксидов: основных, амфотерных, кислотных.
А 10 Оксид магния реагирует с 1) KCl 2) Na. OH 3) SO 3 4) Ba. SO 4 Химические свойства оксидов: основных, амфотерных, кислотных.
 А 10 Химическая реакция возможна между 1) оксидом фосфора(V) и оксидом калия 2) оксидом алюминия и водой 3) оксидом кремния и соляной кислотой 4) оксидом цинка и кислородом
А 10 Химическая реакция возможна между 1) оксидом фосфора(V) и оксидом калия 2) оксидом алюминия и водой 3) оксидом кремния и соляной кислотой 4) оксидом цинка и кислородом
 А 11 При взаимодействии гидроксида железа(II) с раствором серной кислоты образуются 1) Fe. SO 4 и H 2 O 2) Fe 2(SO 4)3 и H 2 O 3) Fe. SO 4 и H 2 4) Fe 2(SO 4)3 и H 2 Химические свойства оснований. Химические свойства кислот.
А 11 При взаимодействии гидроксида железа(II) с раствором серной кислоты образуются 1) Fe. SO 4 и H 2 O 2) Fe 2(SO 4)3 и H 2 O 3) Fe. SO 4 и H 2 4) Fe 2(SO 4)3 и H 2 Химические свойства оснований. Химические свойства кислот.
 А 11 В реакцию с соляной кислотой вступает 1) хлорид натрия 2) карбонат натрия 3) нитрат натрия 4) сульфат натрия
А 11 В реакцию с соляной кислотой вступает 1) хлорид натрия 2) карбонат натрия 3) нитрат натрия 4) сульфат натрия
 А 11 Химическая реакция возможна между 1) оксидом фосфора(V) и оксидом калия 2) оксидом алюминия и водой 3) оксидом кремния и соляной кислотой 4) оксидом цинка и кислородом
А 11 Химическая реакция возможна между 1) оксидом фосфора(V) и оксидом калия 2) оксидом алюминия и водой 3) оксидом кремния и соляной кислотой 4) оксидом цинка и кислородом
 А 12 С раствором сульфата меди(II) реагирует 1) Fe(OH)3 2) Zn 3) H 2 Si. O 3 Химические свойства солей (средних). 4) Mg. O
А 12 С раствором сульфата меди(II) реагирует 1) Fe(OH)3 2) Zn 3) H 2 Si. O 3 Химические свойства солей (средних). 4) Mg. O
 А 12 И нитрат аммония, и нитрат цинка могут взаимодействовать с 1) гидроксидом калия 2) раствором хлорида натрия 3) раствором серной кислоты 4) железом
А 12 И нитрат аммония, и нитрат цинка могут взаимодействовать с 1) гидроксидом калия 2) раствором хлорида натрия 3) раствором серной кислоты 4) железом
 А 13 • Чистые вещества и смеси. • Правила безопасной работы в школьной лаборатории. Лабораторная посуда и оборудование. Человек в мире веществ, материалов и химических реакций. • Проблемы безопасного использования веществ и химических реакций в повседневной жизни. • Разделение смесей и очистка веществ. Приготовление растворов. Химическое загрязнение окружающей среды и его последствия.
А 13 • Чистые вещества и смеси. • Правила безопасной работы в школьной лаборатории. Лабораторная посуда и оборудование. Человек в мире веществ, материалов и химических реакций. • Проблемы безопасного использования веществ и химических реакций в повседневной жизни. • Разделение смесей и очистка веществ. Приготовление растворов. Химическое загрязнение окружающей среды и его последствия.
 А 13 Верны ли следующие суждения об использовании лабораторного оборудования и правилах хранения препаратов бытовой химии? А. Для отбора определенного объема жидкости используют мерный цилиндр. Б. Средства бытовой химии следует хранить отдельно от продуктов питания. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
А 13 Верны ли следующие суждения об использовании лабораторного оборудования и правилах хранения препаратов бытовой химии? А. Для отбора определенного объема жидкости используют мерный цилиндр. Б. Средства бытовой химии следует хранить отдельно от продуктов питания. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
 А 13 Верны ли следующие суждения о правилах хранения витаминов и предназначении моющих средств? А. Хранение витаминов не требует строгого соблюдения указанных в инструкции правил. Б. Для удаления жирных пятен с поверхности посуды целесообразно использовать моющие средства, имеющие щелочную среду. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
А 13 Верны ли следующие суждения о правилах хранения витаминов и предназначении моющих средств? А. Хранение витаминов не требует строгого соблюдения указанных в инструкции правил. Б. Для удаления жирных пятен с поверхности посуды целесообразно использовать моющие средства, имеющие щелочную среду. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
 А 14 • Определение характера среды раствора кислот и щелочей с помощью индикаторов. • Качественные реакции на ионы в растворе (хлорид-, сульфат-, карбонат-ионы, ион аммония). • Получение газообразных веществ. Качественные реакции на газообразные вещества (кислород, водород, углекислый газ, аммиак).
А 14 • Определение характера среды раствора кислот и щелочей с помощью индикаторов. • Качественные реакции на ионы в растворе (хлорид-, сульфат-, карбонат-ионы, ион аммония). • Получение газообразных веществ. Качественные реакции на газообразные вещества (кислород, водород, углекислый газ, аммиак).
 А 14 В лаборатории имеются следующие растворы реактивов А) лакмус Б) K 2 SO 4 В) фенолфталеин Г) Ca(OH)2 Д) метилоранж Е) Ag. NO 3 Ж) Na. OH З) Ba(NO 3)2 Для установления качественного состава соляной кислоты необходимо воспользоваться реактивами, указанными под буквами: 1) А и Б 2) В и Г 3) Д и Е 4) Ж и З
А 14 В лаборатории имеются следующие растворы реактивов А) лакмус Б) K 2 SO 4 В) фенолфталеин Г) Ca(OH)2 Д) метилоранж Е) Ag. NO 3 Ж) Na. OH З) Ba(NO 3)2 Для установления качественного состава соляной кислоты необходимо воспользоваться реактивами, указанными под буквами: 1) А и Б 2) В и Г 3) Д и Е 4) Ж и З
 А 14 В приборе, изображённом на рисунке, получают и подтверждают наличие 1) аммиака 2) водорода 3) кислорода 4) азота
А 14 В приборе, изображённом на рисунке, получают и подтверждают наличие 1) аммиака 2) водорода 3) кислорода 4) азота
 А 15 Массовая доля хлора в оксиде хлора(VII) равна 1) 19, 4% 2) 24, 0% 3) 30, 5% 4) 38, 8% Вычисления массовой доли химического элемента в веществе.
А 15 Массовая доля хлора в оксиде хлора(VII) равна 1) 19, 4% 2) 24, 0% 3) 30, 5% 4) 38, 8% Вычисления массовой доли химического элемента в веществе.
 А 15 Массовая доля азота в нитрате цинка равна 1) 7, 4% 2) 11, 0% 3) 14, 8% 4) 22, 2%
А 15 Массовая доля азота в нитрате цинка равна 1) 7, 4% 2) 11, 0% 3) 14, 8% 4) 22, 2%
 Часть В 5 -8 минут на задание 8 баллов
Часть В 5 -8 минут на задание 8 баллов
 B 1 Периодический закон Д. И. Менделеева. Закономерности изменения свойств элементов и их соединений в связи с положением в периодической системе химических элементов.
B 1 Периодический закон Д. И. Менделеева. Закономерности изменения свойств элементов и их соединений в связи с положением в периодической системе химических элементов.
 B 1 В ряду химических элементов As – P – N 1) увеличиваются радиусы атомов 2) увеличивается электроотрицательность 3) усиливаются кислотные свойства их высших оксидов 4) возрастает значение высшей степени окисления 5) увеличивается число электронов во внешнем электронном слое атомов
B 1 В ряду химических элементов As – P – N 1) увеличиваются радиусы атомов 2) увеличивается электроотрицательность 3) усиливаются кислотные свойства их высших оксидов 4) возрастает значение высшей степени окисления 5) увеличивается число электронов во внешнем электронном слое атомов
 B 1 В ряду химических элементов Si – Ge – Sn 1) увеличивается число электронных слоев 2) уменьшается число протонов в ядре 3) увеличивается значение электроотрицательности 4) усиливается оснóвный характер высших оксидов 5) увеличивается число электронов во внешнем слое
B 1 В ряду химических элементов Si – Ge – Sn 1) увеличивается число электронных слоев 2) уменьшается число протонов в ядре 3) увеличивается значение электроотрицательности 4) усиливается оснóвный характер высших оксидов 5) увеличивается число электронов во внешнем слое
 B 2 • Первоначальные сведения об органических веществах: предельных и непредельных углеводородах (метане, этилене, ацетилене) и кислородсодержащих веществах: спиртах (метаноле, этаноле, глицерине), карбоновых кислотах (уксусной и стеариновой). • Биологически важные вещества: белки, жиры, углеводы.
B 2 • Первоначальные сведения об органических веществах: предельных и непредельных углеводородах (метане, этилене, ацетилене) и кислородсодержащих веществах: спиртах (метаноле, этаноле, глицерине), карбоновых кислотах (уксусной и стеариновой). • Биологически важные вещества: белки, жиры, углеводы.
 В 2 Метан 1) является составной частью природного газа 2) относится к непредельным углеводородам 3) хорошо растворяется в воде 4) не реагирует с кислородом 5) вступает в реакцию с хлором
В 2 Метан 1) является составной частью природного газа 2) относится к непредельным углеводородам 3) хорошо растворяется в воде 4) не реагирует с кислородом 5) вступает в реакцию с хлором
 B 3 Установите соответствие между схемами превращения веществ и изменениями степени окисления серы. СХЕМА ПРЕВРАЩЕНИЙ A) H 2 S + O 2 → SO 2 + H 2 O Б) H 2 SO 4 + Na → Na 2 SO 4 + H 2 S + H 2 O В) SO 2 + Br 2 + H 2 O → H 2 SO 4 + HBr Степень окисления химических элементов. Окислительно-восстановительные реакции. Окислитель и восстановитель. ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ 1) Э+4 → Э+6 2) Э+6 → Э-2 3) Э+6 → Э+4 4) Э-2 → Э+6 5) Э-2 → Э+4
B 3 Установите соответствие между схемами превращения веществ и изменениями степени окисления серы. СХЕМА ПРЕВРАЩЕНИЙ A) H 2 S + O 2 → SO 2 + H 2 O Б) H 2 SO 4 + Na → Na 2 SO 4 + H 2 S + H 2 O В) SO 2 + Br 2 + H 2 O → H 2 SO 4 + HBr Степень окисления химических элементов. Окислительно-восстановительные реакции. Окислитель и восстановитель. ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ 1) Э+4 → Э+6 2) Э+6 → Э-2 3) Э+6 → Э+4 4) Э-2 → Э+6 5) Э-2 → Э+4
 B 3 Установите соответствие между схемой превращения и изменением степени окисления окислителя в ней. СХЕМА ПРЕВРАЩЕНИЙ A)Cl 2 + K 2 Mn. O 4 → KMn. O 4 + KCl Б) NH 4 Cl + KNO 3 → KCl + N 2 O + H 2 O В) HI + Fe. Cl 3 → Fe. Cl 2 + HCl + I 2 ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ 1) Э+6 → Э+7 2) Э+5 → Э+1 3) Э+3 → Э+2 4) Э 0 → Э-1 5) Э-1 → Э 0
B 3 Установите соответствие между схемой превращения и изменением степени окисления окислителя в ней. СХЕМА ПРЕВРАЩЕНИЙ A)Cl 2 + K 2 Mn. O 4 → KMn. O 4 + KCl Б) NH 4 Cl + KNO 3 → KCl + N 2 O + H 2 O В) HI + Fe. Cl 3 → Fe. Cl 2 + HCl + I 2 ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ 1) Э+6 → Э+7 2) Э+5 → Э+1 3) Э+3 → Э+2 4) Э 0 → Э-1 5) Э-1 → Э 0
 Задания В 1 – В 2 считаются выполненными верно, если в каждом из них правильно выбраны два варианта ответа. За неполный ответ - правильно назван 1 из 2 -х ответов, или названы 3 ответа, из которых два верные – 1 балл. Остальные варианты ответов считаются неверными и оцениваются в 0 баллов. Задание В 3 -В 4 считается выполненным верно, если правильно установлено 3 соответствия; частично верным, если установлено 2 соответствия из 3. Остальные варианты считаются неверным ответом
Задания В 1 – В 2 считаются выполненными верно, если в каждом из них правильно выбраны два варианта ответа. За неполный ответ - правильно назван 1 из 2 -х ответов, или названы 3 ответа, из которых два верные – 1 балл. Остальные варианты ответов считаются неверными и оцениваются в 0 баллов. Задание В 3 -В 4 считается выполненным верно, если правильно установлено 3 соответствия; частично верным, если установлено 2 соответствия из 3. Остальные варианты считаются неверным ответом
 B 4 Установите соответствие между исходными веществами и продуктами реакции. ПРОДУКТЫ РЕАКЦИИ ИСХОДНЫЕ ВЕЩЕСТВА t А) Fe(OH)2 = Б) Fe. Cl 3 + Na. OH = В) H 2 SO 4(р-р) + Fe = 1) Fe(OH)3↓ + Na. Cl 2) Fe + H 2 O 3) Fe. SO 4 + H 2↑ 4) Fe. O + H 2 O 5) Fe 2(SO 4)3 + H 2↑ 6) Fe 2 O 3 + H 2 O Химические свойства простых веществ. Химические свойства сложных веществ.
B 4 Установите соответствие между исходными веществами и продуктами реакции. ПРОДУКТЫ РЕАКЦИИ ИСХОДНЫЕ ВЕЩЕСТВА t А) Fe(OH)2 = Б) Fe. Cl 3 + Na. OH = В) H 2 SO 4(р-р) + Fe = 1) Fe(OH)3↓ + Na. Cl 2) Fe + H 2 O 3) Fe. SO 4 + H 2↑ 4) Fe. O + H 2 O 5) Fe 2(SO 4)3 + H 2↑ 6) Fe 2 O 3 + H 2 O Химические свойства простых веществ. Химические свойства сложных веществ.
 B 4 Установите соответствие между веществом и реагентами, с которыми оно может вступать в реакцию. ВЕЩЕСТВО A) железо Б) оксид углерода(IV) В) гидроксид натрия РЕАГЕНТЫ 1) K 2 O, Mg 2) Na 2 SO 4, HNO 3 3) HCl, O 2 4) Cu. SO 4, Al(OH)3
B 4 Установите соответствие между веществом и реагентами, с которыми оно может вступать в реакцию. ВЕЩЕСТВО A) железо Б) оксид углерода(IV) В) гидроксид натрия РЕАГЕНТЫ 1) K 2 O, Mg 2) Na 2 SO 4, HNO 3 3) HCl, O 2 4) Cu. SO 4, Al(OH)3
 Часть С 12 -15 минут на задания 3 задания 10 баллов
Часть С 12 -15 минут на задания 3 задания 10 баллов
 С 1 Взаимосвязь различных классов неорганических веществ. Реакции ионного обмена и условия их осуществления. 4 балла
С 1 Взаимосвязь различных классов неорганических веществ. Реакции ионного обмена и условия их осуществления. 4 балла
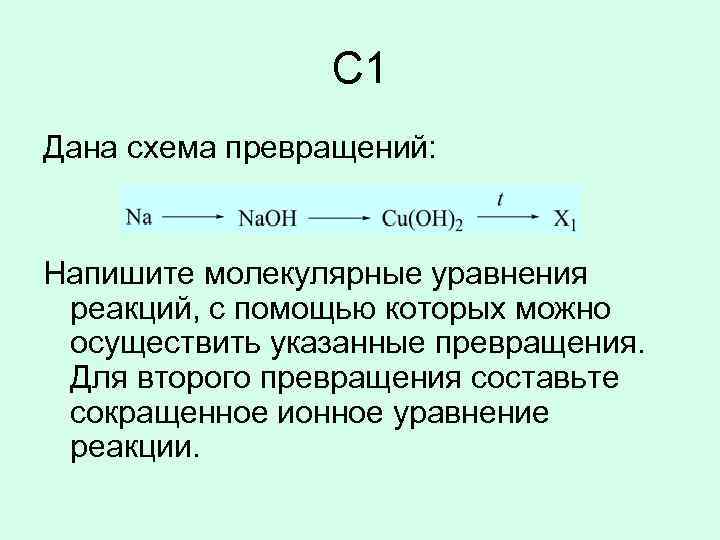 C 1 Дана схема превращений: Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращенное ионное уравнение реакции.
C 1 Дана схема превращений: Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращенное ионное уравнение реакции.
 С 2 Вычисления массовой доли растворенного вещества в растворе. Вычисление количества вещества, массы или объема по количеству вещества, массе или объему одного из реагентов или продуктов реакции. 3 балла
С 2 Вычисления массовой доли растворенного вещества в растворе. Вычисление количества вещества, массы или объема по количеству вещества, массе или объему одного из реагентов или продуктов реакции. 3 балла
 C 2 Через 40 г раствора с массовой долей гидроксида натрия 6% пропустили углекислый газ до образования карбоната натрия. Вычислите объем (н. у. ) вступившего в реакцию газа.
C 2 Через 40 г раствора с массовой долей гидроксида натрия 6% пропустили углекислый газ до образования карбоната натрия. Вычислите объем (н. у. ) вступившего в реакцию газа.
 C 3 • Химические свойства простых веществ • Химические свойства сложных веществ. • Качественные реакции на ионы в растворе (хлорид-, сульфат-, карбонатионы, ион аммония). • Получение газообразных веществ. • Качественные реакции на газообразные вещества (кислород, водород, углекислый газ, аммиак). З балла
C 3 • Химические свойства простых веществ • Химические свойства сложных веществ. • Качественные реакции на ионы в растворе (хлорид-, сульфат-, карбонатионы, ион аммония). • Получение газообразных веществ. • Качественные реакции на газообразные вещества (кислород, водород, углекислый газ, аммиак). З балла
 С 3 На занятиях химического кружка учащиеся исследовали кристаллическое вещество белого цвета. • В результате добавления к нему гидроксида калия и последующего нагревания полученной смеси выделился газ с резким специфическим запахом, при горении которого образуется азот. • После растворения исследуемого вещества в воде и приливания к нему раствора нитрата серебра образовался осадок белого цвета, не растворимый в кислотах. • Определите состав неизвестного вещества и запишите 3 уравнения реакций, которые были проведены учащимися в процессе его распознавания.
С 3 На занятиях химического кружка учащиеся исследовали кристаллическое вещество белого цвета. • В результате добавления к нему гидроксида калия и последующего нагревания полученной смеси выделился газ с резким специфическим запахом, при горении которого образуется азот. • После растворения исследуемого вещества в воде и приливания к нему раствора нитрата серебра образовался осадок белого цвета, не растворимый в кислотах. • Определите состав неизвестного вещества и запишите 3 уравнения реакций, которые были проведены учащимися в процессе его распознавания.
 Отметка по пятибалльной шкале « 2» Общий балл 0– 8 « 3» 9 – 17 « 4» 18 – 26 « 5» 27 – 32
Отметка по пятибалльной шкале « 2» Общий балл 0– 8 « 3» 9 – 17 « 4» 18 – 26 « 5» 27 – 32
 Изменения в ЕГЭ 2011 г. В 2010 г. В 2011 г. А 3 → А 5 А 4 → А 6 А 5 → А 7 А 6 → А 8 А 7 → А 3 А 8 → А 4 А 18 → А 20 А 19 → А 21 А 20 → А 22 А 21 → А 23 А 22 → А 24 А 23 → А 25 А 24 → А 27 А 25 → А 26 → А 18 А 27 → А 19
Изменения в ЕГЭ 2011 г. В 2010 г. В 2011 г. А 3 → А 5 А 4 → А 6 А 5 → А 7 А 6 → А 8 А 7 → А 3 А 8 → А 4 А 18 → А 20 А 19 → А 21 А 20 → А 22 А 21 → А 23 А 22 → А 24 А 23 → А 25 А 24 → А 27 А 25 → А 26 → А 18 А 27 → А 19
 Спасибо за внимание!
Спасибо за внимание!


