21_Heterogen_Catalysis.ppt
- Количество слайдов: 62
 Гетерогенний каталіз
Гетерогенний каталіз
 Кінетика гетерогеннокаталітичних реакцій
Кінетика гетерогеннокаталітичних реакцій
 Основні стадії гетерогенно-каталітичних процесів 1) дифузія речовини до поверхні каталізатора; 2) оборотна адсорбція речовини; 3) реакція на поверхні, в адсорбційному шарі; 4) оборотна десорбція продуктів з поверхні; 5) дифузія продуктів реакції від поверхні в об'єм. Загальна швидкість каталітичної реакції визначається швидкістю найповільнішої з цих стадій.
Основні стадії гетерогенно-каталітичних процесів 1) дифузія речовини до поверхні каталізатора; 2) оборотна адсорбція речовини; 3) реакція на поверхні, в адсорбційному шарі; 4) оборотна десорбція продуктів з поверхні; 5) дифузія продуктів реакції від поверхні в об'єм. Загальна швидкість каталітичної реакції визначається швидкістю найповільнішої з цих стадій.
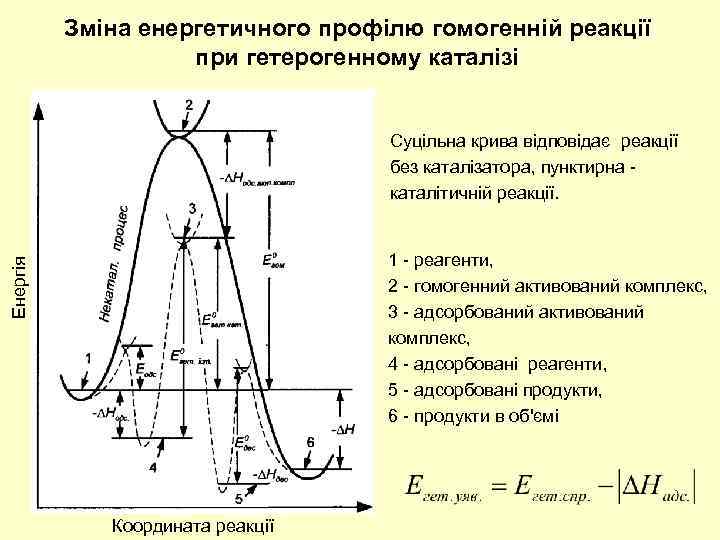 Зміна енергетичного профілю гомогенній реакції при гетерогенному каталізі Енергія Суцільна крива відповідає реакції без каталізатора, пунктирна каталітичній реакції. і Координата реакції 1 - реагенти, 2 - гомогенний активований комплекс, 3 - адсорбований активований комплекс, 4 - адсорбовані реагенти, 5 - адсорбовані продукти, 6 - продукти в об'ємі
Зміна енергетичного профілю гомогенній реакції при гетерогенному каталізі Енергія Суцільна крива відповідає реакції без каталізатора, пунктирна каталітичній реакції. і Координата реакції 1 - реагенти, 2 - гомогенний активований комплекс, 3 - адсорбований активований комплекс, 4 - адсорбовані реагенти, 5 - адсорбовані продукти, 6 - продукти в об'ємі
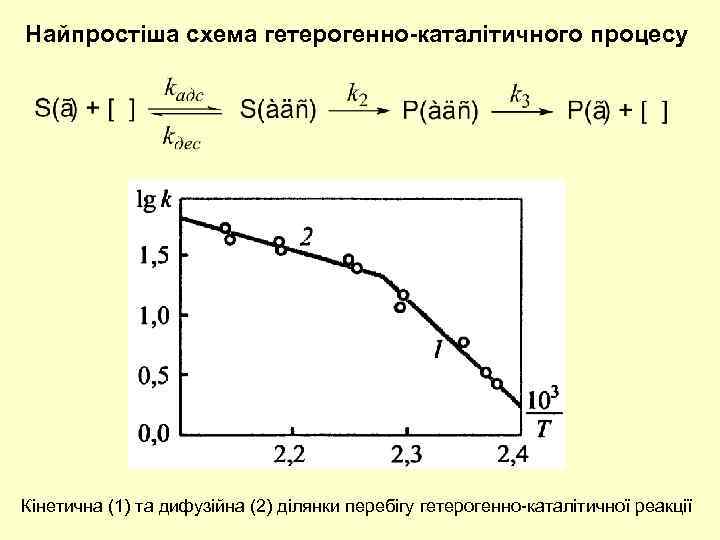 Найпростіша схема гетерогенно-каталітичного процесу Кінетична (1) та дифузійна (2) ділянки перебігу гетерогенно-каталітичної реакції
Найпростіша схема гетерогенно-каталітичного процесу Кінетична (1) та дифузійна (2) ділянки перебігу гетерогенно-каталітичної реакції
 Швиідкість гетерогенно-каталітичної реакції
Швиідкість гетерогенно-каталітичної реакції
 Реакція ізомерізації на поверхні гетерогенного каталізатора
Реакція ізомерізації на поверхні гетерогенного каталізатора
 Реакція ізомерізації на поверхні гетерогенного каталізатора Якщо і Експериментальна енергія активації складається з енергії активації гетерогенної реакції і ентальпії адсорбції (яка зазвичай є від'ємною)
Реакція ізомерізації на поверхні гетерогенного каталізатора Якщо і Експериментальна енергія активації складається з енергії активації гетерогенної реакції і ентальпії адсорбції (яка зазвичай є від'ємною)
 Реакція ізомерізації на поверхні гетерогенного каталізатора Якщо Майже уся поверхня заповнена молекулами реагенту (режим максимального завантаження каталізатора).
Реакція ізомерізації на поверхні гетерогенного каталізатора Якщо Майже уся поверхня заповнена молекулами реагенту (режим максимального завантаження каталізатора).
 Швидкість гетерогенно-каталітичної реакції а) реакція перебігає між двома адсорбованими реагентами
Швидкість гетерогенно-каталітичної реакції а) реакція перебігає між двома адсорбованими реагентами
 Швиідкість гетерогенно-каталітичної реакції б) один із субстратів реагує безпосередньо з газової фази
Швиідкість гетерогенно-каталітичної реакції б) один із субстратів реагує безпосередньо з газової фази
![Схема Ленгмюра-Гіншельвуда H 2 + 2[ ] = 2[H] D 2 + 2[ ] Схема Ленгмюра-Гіншельвуда H 2 + 2[ ] = 2[H] D 2 + 2[ ]](https://present5.com/presentation/15901622_151345155/image-12.jpg) Схема Ленгмюра-Гіншельвуда H 2 + 2[ ] = 2[H] D 2 + 2[ ] = 2[D] [H] + [D] = HD + 2[ ] Схема Ілі-Ріділа [H] + D 2 = HD + [D] + H 2 = HD + [H] Обидві кінетичні схеми відносяться до моделі однорідної поверхні каталізатора
Схема Ленгмюра-Гіншельвуда H 2 + 2[ ] = 2[H] D 2 + 2[ ] = 2[D] [H] + [D] = HD + 2[ ] Схема Ілі-Ріділа [H] + D 2 = HD + [D] + H 2 = HD + [H] Обидві кінетичні схеми відносяться до моделі однорідної поверхні каталізатора
 Приклад: окиснення СО на Pd-Ag каталізаторах Pd/Ag 2 СO + O 2 2 СO 2 Порядки реакції як за СО, так і за О 2 змінюються від 1 до 0 Емпіричне рівняння: При фіксованих концентраціях СО або О 2: При с→ 0 n = 1, при с →∞ n = 0
Приклад: окиснення СО на Pd-Ag каталізаторах Pd/Ag 2 СO + O 2 2 СO 2 Порядки реакції як за СО, так і за О 2 змінюються від 1 до 0 Емпіричне рівняння: При фіксованих концентраціях СО або О 2: При с→ 0 n = 1, при с →∞ n = 0
 Окиснення СО на Pd-Ag каталізаторах Схема Ленгмюра-Гіншельвуда:
Окиснення СО на Pd-Ag каталізаторах Схема Ленгмюра-Гіншельвуда:
 Окиснення СО на Pd-Ag каталізаторах
Окиснення СО на Pd-Ag каталізаторах
 Окиснення СО на Pd-Ag каталізаторах Схема Ленгмюра-Гіншельвуда При великих значеннях K 2 c. CO та K 2 c. O 2 рівняння дає від'ємні порядки за CO (-1) та O 2 (-0, 5). Емпіричне рівняння:
Окиснення СО на Pd-Ag каталізаторах Схема Ленгмюра-Гіншельвуда При великих значеннях K 2 c. CO та K 2 c. O 2 рівняння дає від'ємні порядки за CO (-1) та O 2 (-0, 5). Емпіричне рівняння:
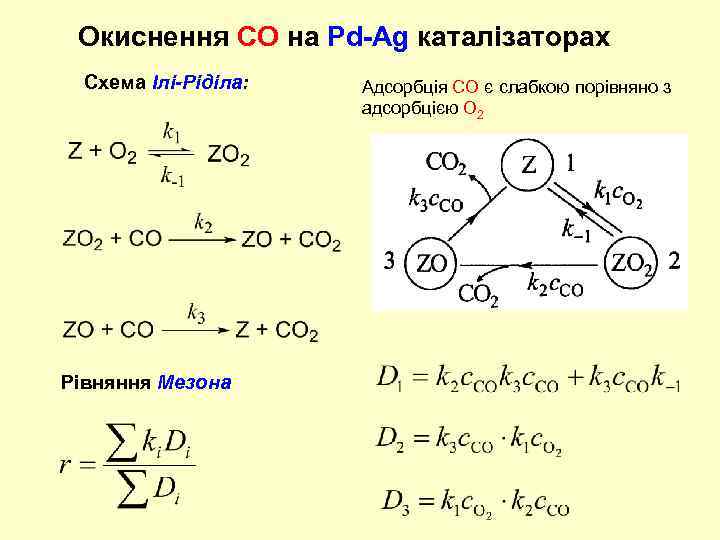 Окиснення СО на Pd-Ag каталізаторах Схема Ілі-Ріділа: Рівняння Мезона Адсорбція СО є слабкою порівняно з адсорбцією О 2
Окиснення СО на Pd-Ag каталізаторах Схема Ілі-Ріділа: Рівняння Мезона Адсорбція СО є слабкою порівняно з адсорбцією О 2
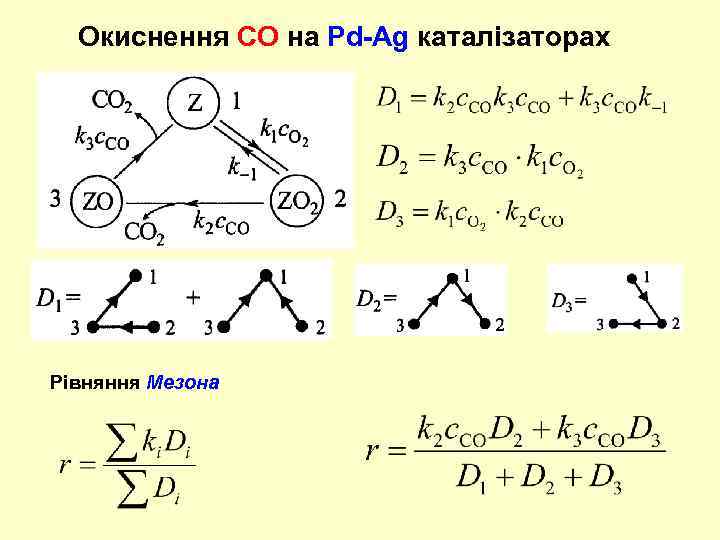 Окиснення СО на Pd-Ag каталізаторах Рівняння Мезона
Окиснення СО на Pd-Ag каталізаторах Рівняння Мезона
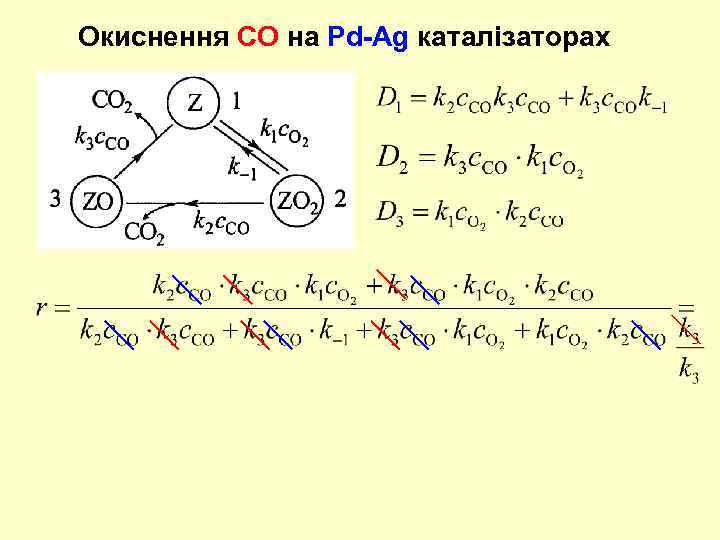 Окиснення СО на Pd-Ag каталізаторах
Окиснення СО на Pd-Ag каталізаторах
 Окиснення СО на Pd-Ag каталізаторах Емпіричне рівняння:
Окиснення СО на Pd-Ag каталізаторах Емпіричне рівняння:
 Гідрування алкенів на перехідних металах (Ni, Pd, Pt) Адсорбція алкенів є сильною, а водню слабкою Для відносно низьких температур та високих тисків етилену: Для малих тисків етилену та відносно високих температур
Гідрування алкенів на перехідних металах (Ni, Pd, Pt) Адсорбція алкенів є сильною, а водню слабкою Для відносно низьких температур та високих тисків етилену: Для малих тисків етилену та відносно високих температур
 Теорія проміжних поверхневих сполук Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 1 стадія 2 стадія k 1 HCOOH + [ ] ½H 2 + [HCOO] k 2 [HCOO] CO 2 + ½H 2 + [ ]
Теорія проміжних поверхневих сполук Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 1 стадія 2 стадія k 1 HCOOH + [ ] ½H 2 + [HCOO] k 2 [HCOO] CO 2 + ½H 2 + [ ]
 Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 1 стадія 2 стадія k 1 HCOOH + [ ] ½H 2 + [HCOO] k 2 [HCOO] CO 2 + ½H 2 + [ ]
Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 1 стадія 2 стадія k 1 HCOOH + [ ] ½H 2 + [HCOO] k 2 [HCOO] CO 2 + ½H 2 + [ ]
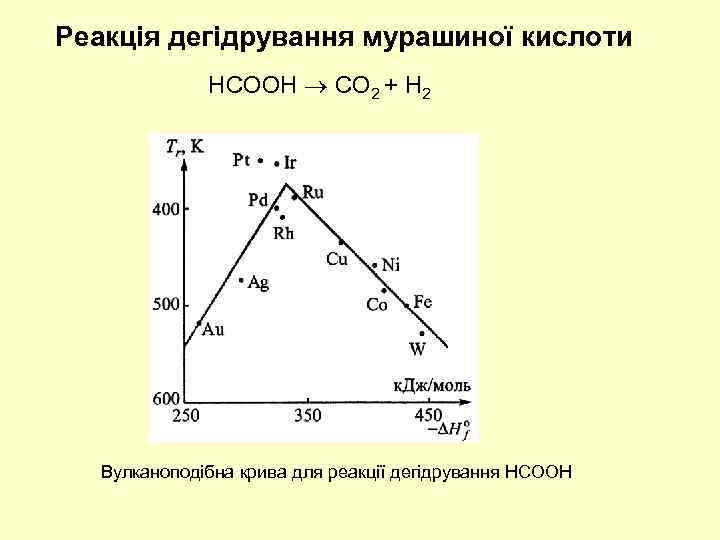 Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 Вулканоподібна крива для реакції дегідрування НСООН
Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 Вулканоподібна крива для реакції дегідрування НСООН
 Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 Каталізатори – перехідні метали Селективність каталітичного процесу HCOOH СO + H 2 О Каталізатори кислотно-основного типу (Al 2 O 3) Дегідратація та дегідрування спиртів
Реакція дегідрування мурашиної кислоти HCOOH СO 2 + H 2 Каталізатори – перехідні метали Селективність каталітичного процесу HCOOH СO + H 2 О Каталізатори кислотно-основного типу (Al 2 O 3) Дегідратація та дегідрування спиртів
 Реакція дегідрування циклогексану на Ni За
Реакція дегідрування циклогексану на Ni За
 Реакція каталітичного синтезу аміаку на перехідних металах Азот і водень можуть сорбуватися як у молекулярній, так і в атомарній формі Аміак може реагувати з поверхнею при відносно високих температурах Двостадійна схема: 1) 2)
Реакція каталітичного синтезу аміаку на перехідних металах Азот і водень можуть сорбуватися як у молекулярній, так і в атомарній формі Аміак може реагувати з поверхнею при відносно високих температурах Двостадійна схема: 1) 2)
 Реакція каталітичного синтезу аміаку на перехідних металах Двостадійна схема: 1) 2) K 2
Реакція каталітичного синтезу аміаку на перехідних металах Двостадійна схема: 1) 2) K 2
 Реакція каталітичного синтезу аміаку на перехідних металах Двостадійна схема: 1) 2) При
Реакція каталітичного синтезу аміаку на перехідних металах Двостадійна схема: 1) 2) При
 Реакція каталітичного синтезу аміаку на перехідних металах Міцно хемосорбують азот: Ti, Zr, V, Cr Слабко хемосорбують азот (або взагалі не сорбують): Ag, Cu, Ni, Pd, Pt Проміжна здатність: Fe, Ru, Os
Реакція каталітичного синтезу аміаку на перехідних металах Міцно хемосорбують азот: Ti, Zr, V, Cr Слабко хемосорбують азот (або взагалі не сорбують): Ag, Cu, Ni, Pd, Pt Проміжна здатність: Fe, Ru, Os
 Активні центри гетерогенних каталізаторів
Активні центри гетерогенних каталізаторів
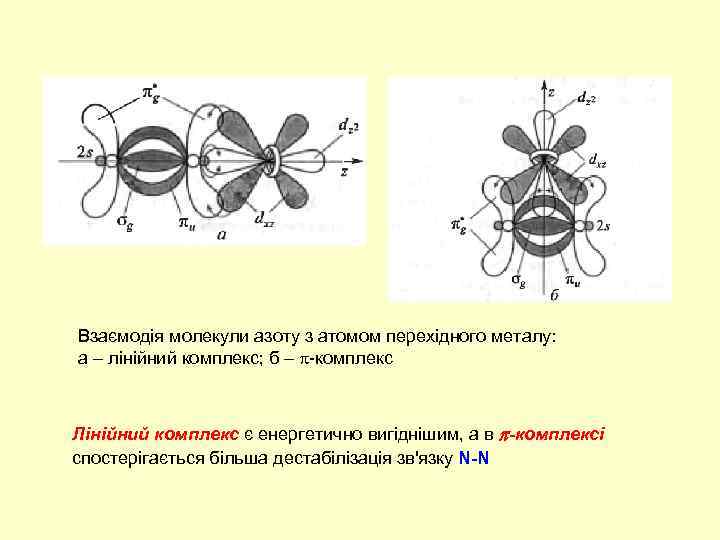 Взаємодія молекули азоту з атомом перехідного металу: а – лінійний комплекс; б – -комплекс Лінійний комплекс є енергетично вигіднішим, а в -комплексі спостерігається більша дестабілізація зв'язку N-N
Взаємодія молекули азоту з атомом перехідного металу: а – лінійний комплекс; б – -комплекс Лінійний комплекс є енергетично вигіднішим, а в -комплексі спостерігається більша дестабілізація зв'язку N-N
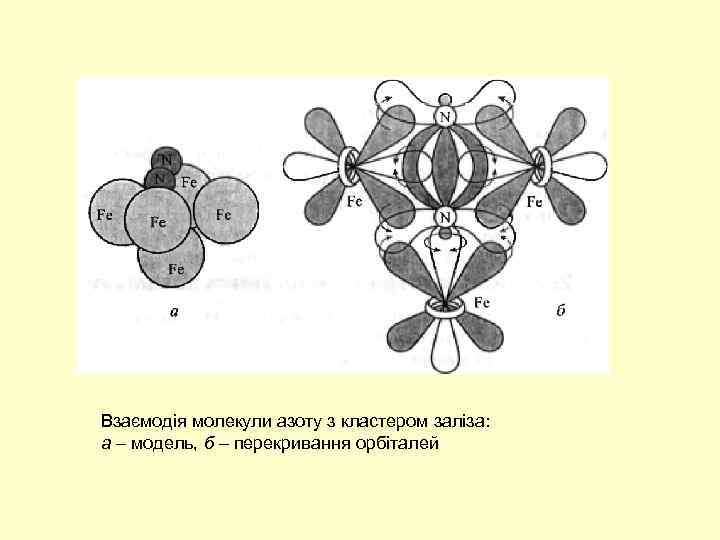 Взаємодія молекули азоту з кластером заліза: а – модель, б – перекривання орбіталей
Взаємодія молекули азоту з кластером заліза: а – модель, б – перекривання орбіталей
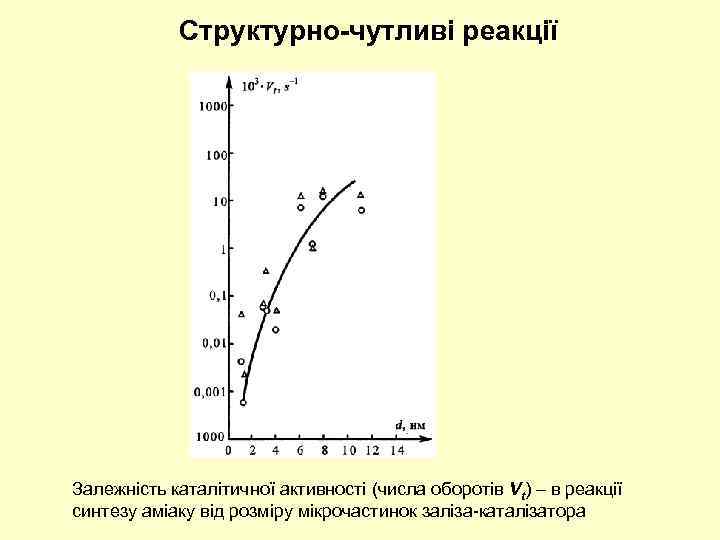 Структурно-чутливі реакції Залежність каталітичної активності (числа оборотів Vt) – в реакції синтезу аміаку від розміру мікрочастинок заліза-каталізатора
Структурно-чутливі реакції Залежність каталітичної активності (числа оборотів Vt) – в реакції синтезу аміаку від розміру мікрочастинок заліза-каталізатора
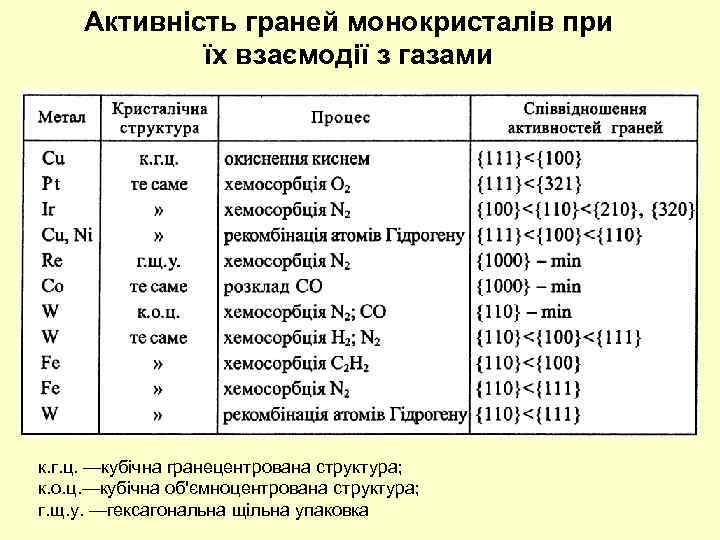 Активність граней монокристалів при їх взаємодії з газами к. г. ц. —кубічна гранецентрована структура; к. о. ц. —кубічна об'ємноцентрована структура; г. щ. у. —гексагональна щільна упаковка
Активність граней монокристалів при їх взаємодії з газами к. г. ц. —кубічна гранецентрована структура; к. о. ц. —кубічна об'ємноцентрована структура; г. щ. у. —гексагональна щільна упаковка
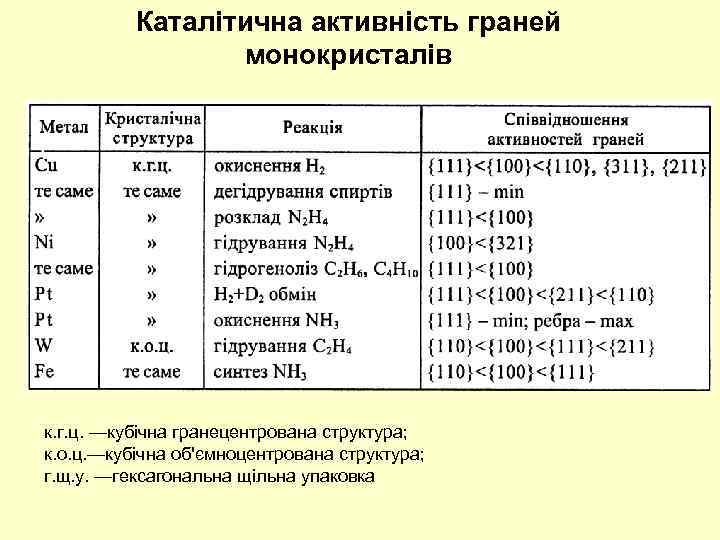 Каталітична активність граней монокристалів к. г. ц. —кубічна гранецентрована структура; к. о. ц. —кубічна об'ємноцентрована структура; г. щ. у. —гексагональна щільна упаковка
Каталітична активність граней монокристалів к. г. ц. —кубічна гранецентрована структура; к. о. ц. —кубічна об'ємноцентрована структура; г. щ. у. —гексагональна щільна упаковка
 Промотори, отрути, нанесені каталізатори
Промотори, отрути, нанесені каталізатори
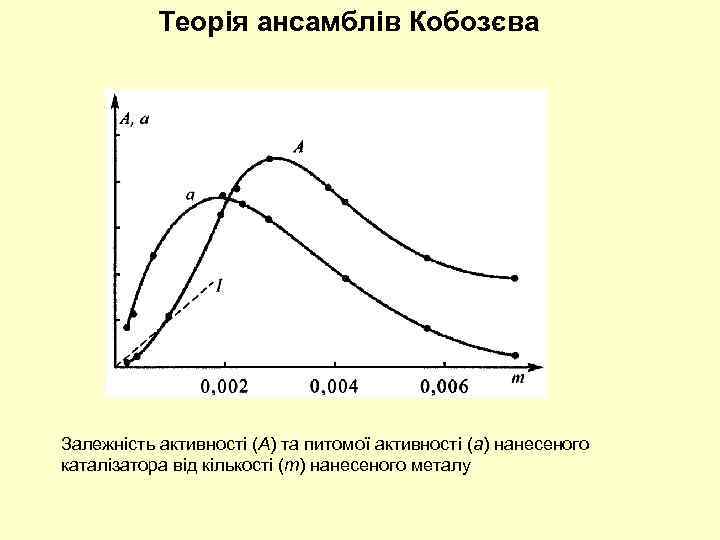 Теорія ансамблів Кобозєва Залежність активності (А) та питомої активності (а) нанесеного каталізатора від кількості (m) нанесеного металу
Теорія ансамблів Кобозєва Залежність активності (А) та питомої активності (а) нанесеного каталізатора від кількості (m) нанесеного металу
 Теорія ансамблів Кобозєва Закон рідкісних подій – розподілення Пуассона: імовірність утворення k-атомного ансамблю дорівнює - середня кількість атомів у комірці А – активність нанесеного каталізатора, Положення максимуму на кривій:
Теорія ансамблів Кобозєва Закон рідкісних подій – розподілення Пуассона: імовірність утворення k-атомного ансамблю дорівнює - середня кількість атомів у комірці А – активність нанесеного каталізатора, Положення максимуму на кривій:
 Теорія ансамблів Кобозєва
Теорія ансамблів Кобозєва
 Теорія ансамблів Кобозєва
Теорія ансамблів Кобозєва
 Теорія ансамблів Кобозєва
Теорія ансамблів Кобозєва
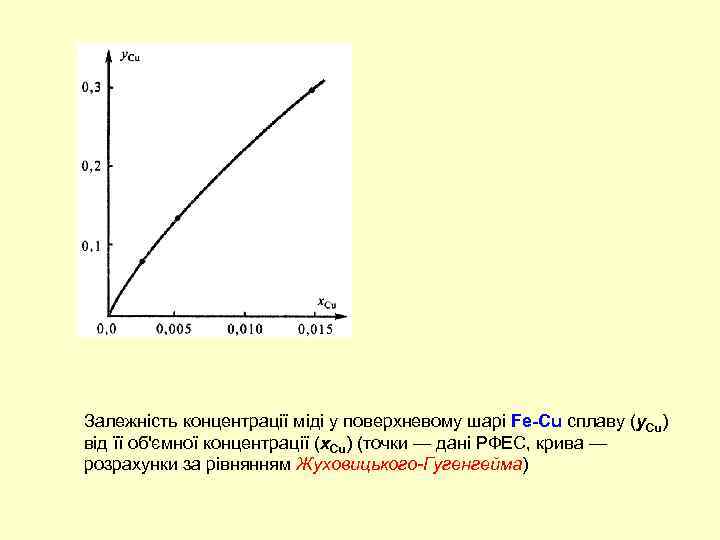 Залежність концентрації міді у поверхневому шарі Fe-Cu сплаву (y. Cu) від її об'ємної концентрації (x. Cu) (точки — дані РФЕС, крива — розрахунки за рівнянням Жуховицького-Гугенгейма)
Залежність концентрації міді у поверхневому шарі Fe-Cu сплаву (y. Cu) від її об'ємної концентрації (x. Cu) (точки — дані РФЕС, крива — розрахунки за рівнянням Жуховицького-Гугенгейма)
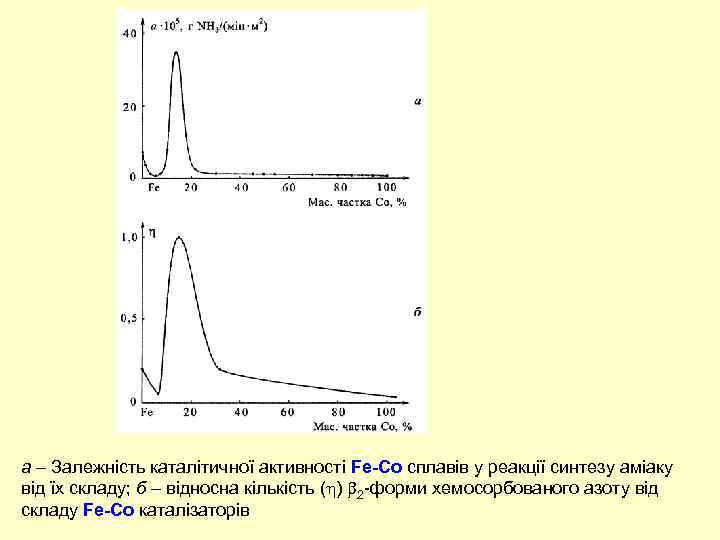 a – Залежність каталітичної активності Fe-Co сплавів у реакції синтезу аміаку від їх складу; б – відносна кількість ( ) 2 -форми хемосорбованого азоту від складу Fe-Co каталізаторів
a – Залежність каталітичної активності Fe-Co сплавів у реакції синтезу аміаку від їх складу; б – відносна кількість ( ) 2 -форми хемосорбованого азоту від складу Fe-Co каталізаторів
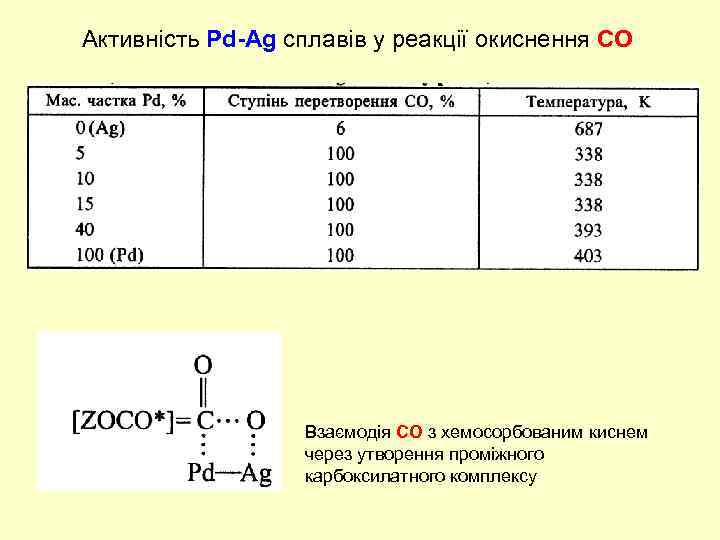 Активність Pd-Ag сплавів у реакції окиснення СО Взаємодія СО з хемосорбованим киснем через утворення проміжного карбоксилатного комплексу
Активність Pd-Ag сплавів у реакції окиснення СО Взаємодія СО з хемосорбованим киснем через утворення проміжного карбоксилатного комплексу
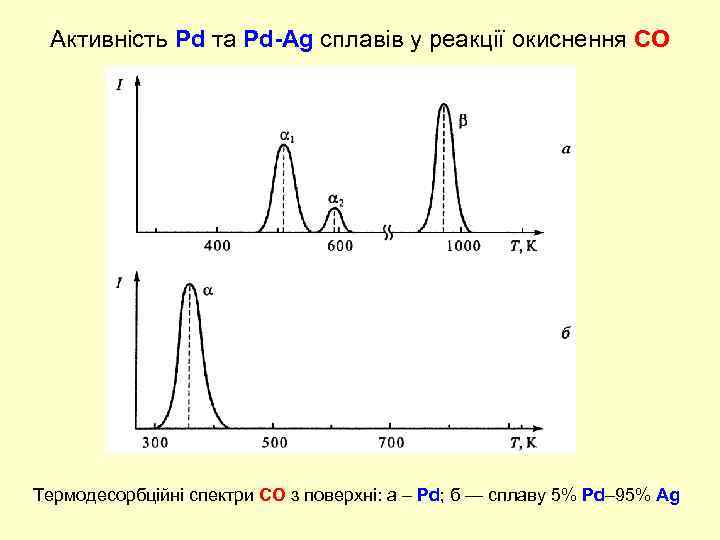 Активність Pd та Pd-Ag сплавів у реакції окиснення СО Термодесорбційні спектри СО з поверхні: а – Pd; б — сплаву 5% Pd– 95% Аg
Активність Pd та Pd-Ag сплавів у реакції окиснення СО Термодесорбційні спектри СО з поверхні: а – Pd; б — сплаву 5% Pd– 95% Аg
 Нестаціонарні явища у гетерогенному каталізі
Нестаціонарні явища у гетерогенному каталізі
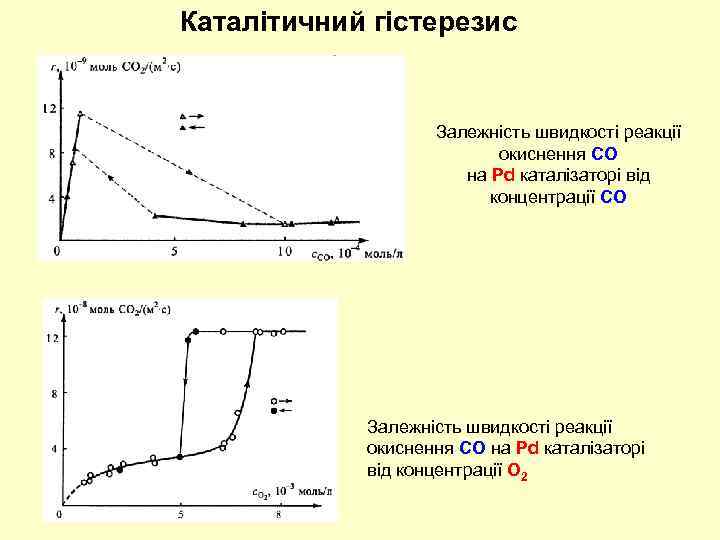 Каталітичний гістерезис Залежність швидкості реакції окиснення СО на Рd каталізаторі від концентрації СО Залежність швидкості реакції окиснення СО на Рd каталізаторі від концентрації O 2
Каталітичний гістерезис Залежність швидкості реакції окиснення СО на Рd каталізаторі від концентрації СО Залежність швидкості реакції окиснення СО на Рd каталізаторі від концентрації O 2
 Каталітичний гістерезис Наявність двох стаціонарних станів: • високоактивний (з майже повним переторвенням СО у СО 2 (порядки: за СО – 1, 0; за О 2 – 0, 0) • низькоактивний (порядки: за СО – 0, 0; за О 2 – 0, 3)
Каталітичний гістерезис Наявність двох стаціонарних станів: • високоактивний (з майже повним переторвенням СО у СО 2 (порядки: за СО – 1, 0; за О 2 – 0, 0) • низькоактивний (порядки: за СО – 0, 0; за О 2 – 0, 3)
 Можливі причини каталітичного гістерезису • наявність стадії взаємодії проміжних речовин; • зміна швидкості елементарних стадій при зміні концентрацій реагентів у поверхневому шарі; • перегрів поверхневого шару каталізатора; • ланцюгові процеси на поверхні каталізатора; • зміна структури поверхні під дією реакційної суміші, зокрема фазові перетворення у поверхневому шарі каталізатора; • гетерогенно-гомогенний механізм – гомогенне подовження гетерогенно-каталітичної реакції.
Можливі причини каталітичного гістерезису • наявність стадії взаємодії проміжних речовин; • зміна швидкості елементарних стадій при зміні концентрацій реагентів у поверхневому шарі; • перегрів поверхневого шару каталізатора; • ланцюгові процеси на поверхні каталізатора; • зміна структури поверхні під дією реакційної суміші, зокрема фазові перетворення у поверхневому шарі каталізатора; • гетерогенно-гомогенний механізм – гомогенне подовження гетерогенно-каталітичної реакції.
 Можливісь реалізації стаціонарних станів при окисненні СО за двомаршрутним мезанізмом
Можливісь реалізації стаціонарних станів при окисненні СО за двомаршрутним мезанізмом
 Фактори, що обумовлюють можливість реалізації гетерогенногомогенного механізму • можливість перебігу ланцюгового процесу у газовій фазі; • можливість генерації радикалів на поверхні каталізатора.
Фактори, що обумовлюють можливість реалізації гетерогенногомогенного механізму • можливість перебігу ланцюгового процесу у газовій фазі; • можливість генерації радикалів на поверхні каталізатора.
 Гетерогенно-гомогенний механізм CO + O 2 CO 2 + O: CO + O: CO 2 OH + CO 2 + H H + O 2 OH + O: H + O 2 + M HO 2 + M (при відносно низьких температурах) HO 2 + CO 2 + OH (при високих температурах) H + O 2 HO 2 (при відносно низьких температурах) [O 2] + H 2 OH + [OH] [O 2] + H 2 O HO 2 + [OH]
Гетерогенно-гомогенний механізм CO + O 2 CO 2 + O: CO + O: CO 2 OH + CO 2 + H H + O 2 OH + O: H + O 2 + M HO 2 + M (при відносно низьких температурах) HO 2 + CO 2 + OH (при високих температурах) H + O 2 HO 2 (при відносно низьких температурах) [O 2] + H 2 OH + [OH] [O 2] + H 2 O HO 2 + [OH]
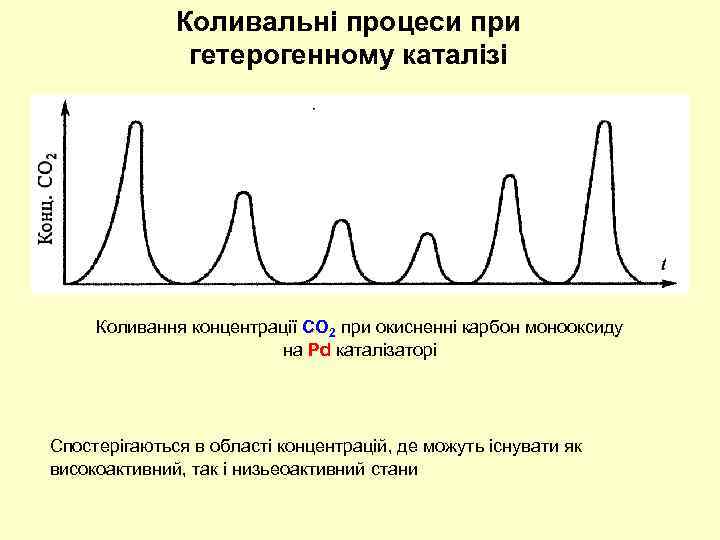 Коливальні процеси при гетерогенному каталізі Коливання концентрації СO 2 при окисненні карбон монооксиду на Рd каталізаторі Спостерігаються в області концентрацій, де можуть існувати як високоактивний, так і низьеоактивний стани
Коливальні процеси при гетерогенному каталізі Коливання концентрації СO 2 при окисненні карбон монооксиду на Рd каталізаторі Спостерігаються в області концентрацій, де можуть існувати як високоактивний, так і низьеоактивний стани
 Проблеми каталізу за участю складних молекул
Проблеми каталізу за участю складних молекул
 Мультиплетна теорія каталізу • принцип енергетичної відповідності • принцип геометричної відповідності • подолання інформаційного бар'єру Принцип енергетичної відповідності: «мультиплетний комплекс» повинен мати деяку оптимальну енергію зв'язку з поверхнею каталізатора. Принцип геометричної відповідності: легкість перебігу каталітичної реакції залежить від просторового співвідношення між будовою активного центру на поверхні каталізатора і геометричними параметрами тієї частини молекули, що перетворюється у ході реакції ( «індексної групи» ).
Мультиплетна теорія каталізу • принцип енергетичної відповідності • принцип геометричної відповідності • подолання інформаційного бар'єру Принцип енергетичної відповідності: «мультиплетний комплекс» повинен мати деяку оптимальну енергію зв'язку з поверхнею каталізатора. Принцип геометричної відповідності: легкість перебігу каталітичної реакції залежить від просторового співвідношення між будовою активного центру на поверхні каталізатора і геометричними параметрами тієї частини молекули, що перетворюється у ході реакції ( «індексної групи» ).
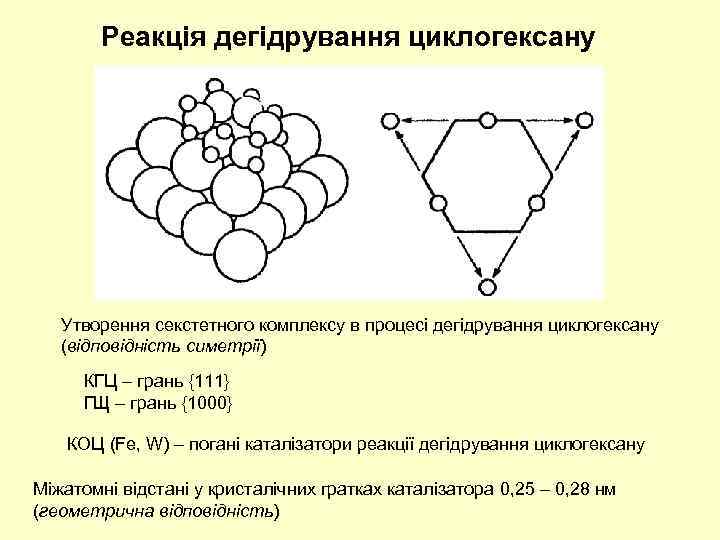 Реакція дегідрування циклогексану Утворення секстетного комплексу в процесі дегідрування циклогексану (відповідність симетрії) КГЦ – грань {111} ГЩ – грань {1000} КOЦ (Fe, W) – погані каталізатори реакції дегідрування циклогексану Міжатомні відстані у кристалічних гратках каталізатора 0, 25 – 0, 28 нм (геометрична відповідність)
Реакція дегідрування циклогексану Утворення секстетного комплексу в процесі дегідрування циклогексану (відповідність симетрії) КГЦ – грань {111} ГЩ – грань {1000} КOЦ (Fe, W) – погані каталізатори реакції дегідрування циклогексану Міжатомні відстані у кристалічних гратках каталізатора 0, 25 – 0, 28 нм (геометрична відповідність)
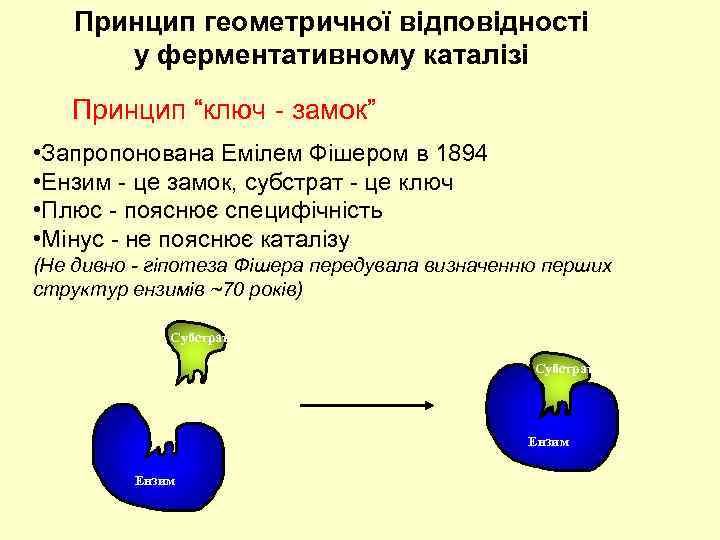 Принцип геометричної відповідності у ферментативному каталізі Принцип “ключ - замок” • Запропонована Емілем Фішером в 1894 • Eнзим - це замок, субстрат - це ключ • Плюс - пояснює специфічність • Мінус - не пояснює каталізу (Не дивно - гіпотеза Фішера передувала визначенню перших структур ензимів ~70 років) Субстрат Ензим
Принцип геометричної відповідності у ферментативному каталізі Принцип “ключ - замок” • Запропонована Емілем Фішером в 1894 • Eнзим - це замок, субстрат - це ключ • Плюс - пояснює специфічність • Мінус - не пояснює каталізу (Не дивно - гіпотеза Фішера передувала визначенню перших структур ензимів ~70 років) Субстрат Ензим
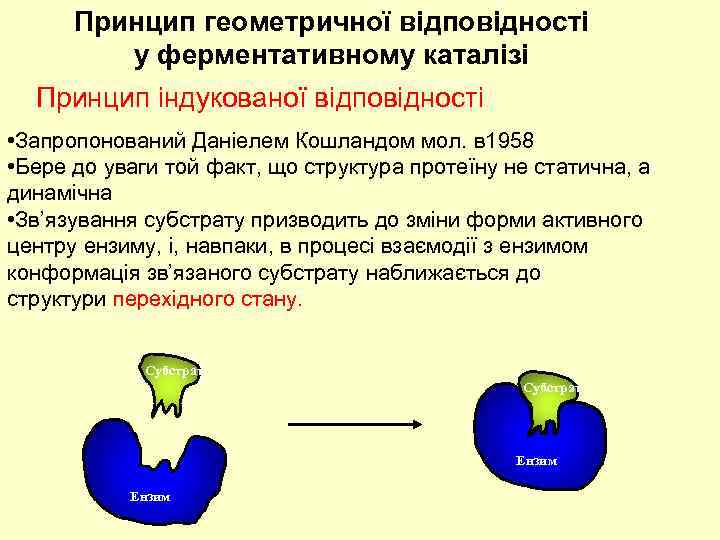 Принцип геометричної відповідності у ферментативному каталізі Принцип індукованої відповідності • Запропонований Даніелем Кошландом мол. в 1958 • Бере до уваги той факт, що структура протеїну не статична, а динамічна • Зв’язування субстрату призводить до зміни форми активного центру ензиму, і, навпаки, в процесі взаємодії з ензимом конформація зв’язаного субстрату наближається до структури перехідного стану. Субстрат Ензим
Принцип геометричної відповідності у ферментативному каталізі Принцип індукованої відповідності • Запропонований Даніелем Кошландом мол. в 1958 • Бере до уваги той факт, що структура протеїну не статична, а динамічна • Зв’язування субстрату призводить до зміни форми активного центру ензиму, і, навпаки, в процесі взаємодії з ензимом конформація зв’язаного субстрату наближається до структури перехідного стану. Субстрат Ензим
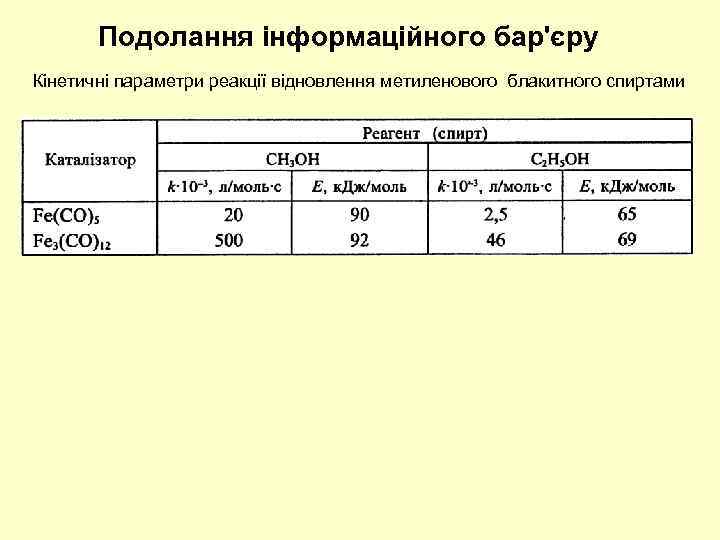 Подолання інформаційного бар'єру Кінетичні параметри реакції відновлення метиленового блакитного спиртами
Подолання інформаційного бар'єру Кінетичні параметри реакції відновлення метиленового блакитного спиртами
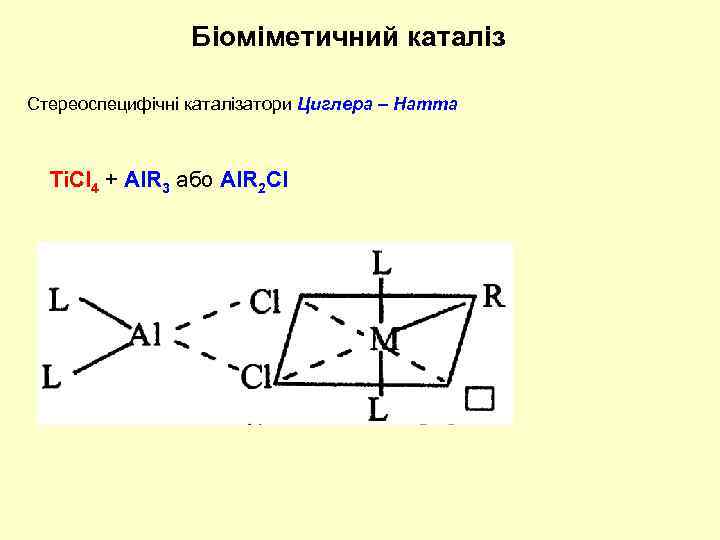 Біоміметичний каталіз Стереоспецифічні каталізатори Циглера – Натта Ti. Cl 4 + Al. R 3 або Al. R 2 Cl
Біоміметичний каталіз Стереоспецифічні каталізатори Циглера – Натта Ti. Cl 4 + Al. R 3 або Al. R 2 Cl
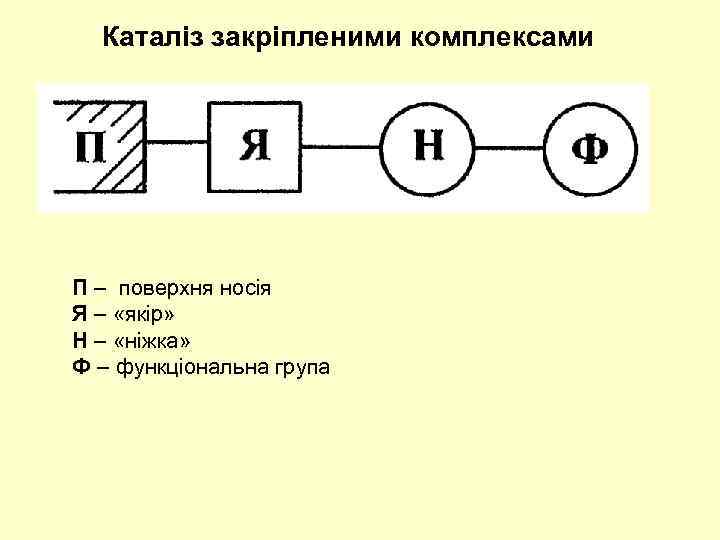 Каталіз закріпленими комплексами П – поверхня носія Я – «якір» Н – «ніжка» Ф – функціональна група
Каталіз закріпленими комплексами П – поверхня носія Я – «якір» Н – «ніжка» Ф – функціональна група


