3874203_Geterofunkcionalnuye__karb_ktuy.ppt
- Количество слайдов: 55
 Гетерофункциональные соединения
Гетерофункциональные соединения
 Цель лекции Получить четкое представление о химическом строении и свойствах гетерофункциональных соединений, взаимосвязи химического строения и биологической активности.
Цель лекции Получить четкое представление о химическом строении и свойствах гетерофункциональных соединений, взаимосвязи химического строения и биологической активности.
 План лекции 1. 2. 3. 4. 5. 6. Классификация Номенклатура Физические свойства Способы получения Химические свойства Медико-биологические свойства
План лекции 1. 2. 3. 4. 5. 6. Классификация Номенклатура Физические свойства Способы получения Химические свойства Медико-биологические свойства
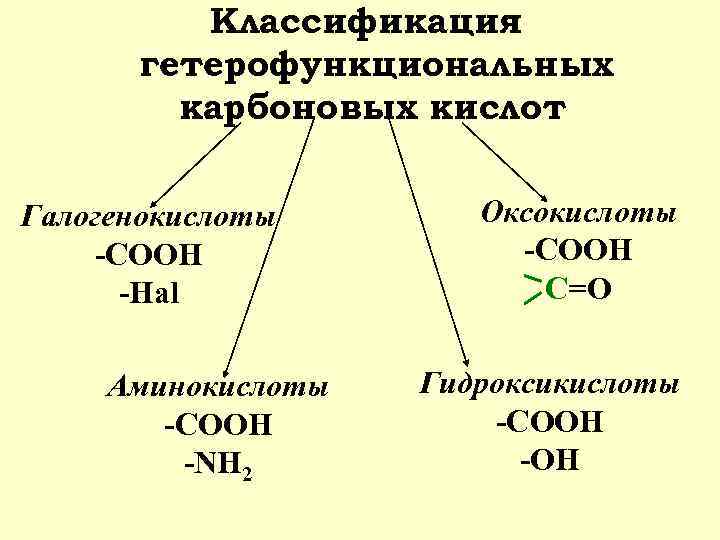 Классификация гетерофункциональных карбоновых кислот Галогенокислоты -СООН -Hal Аминокислоты -COOH -NH 2 Оксокислоты -COOH C=O Гидроксикислоты -COOH -OH
Классификация гетерофункциональных карбоновых кислот Галогенокислоты -СООН -Hal Аминокислоты -COOH -NH 2 Оксокислоты -COOH C=O Гидроксикислоты -COOH -OH
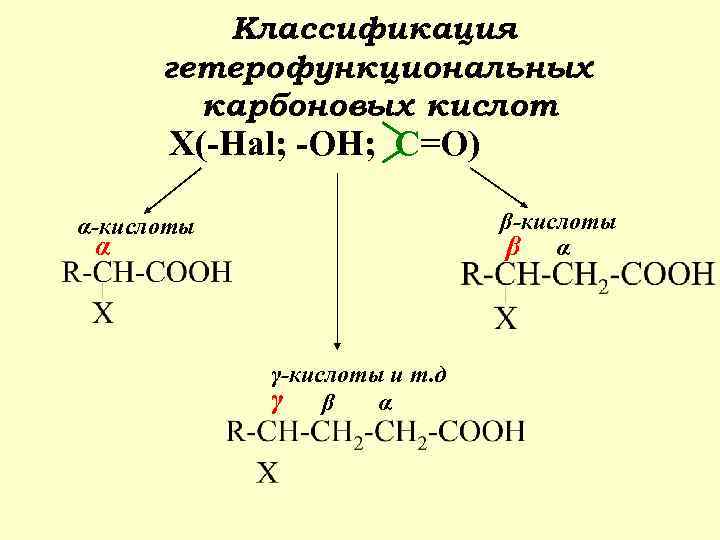 Классификация гетерофункциональных карбоновых кислот Х(-Hal; -OH; C=O) β-кислоты β α α-кислоты α γ-кислоты и т. д γ β α
Классификация гетерофункциональных карбоновых кислот Х(-Hal; -OH; C=O) β-кислоты β α α-кислоты α γ-кислоты и т. д γ β α
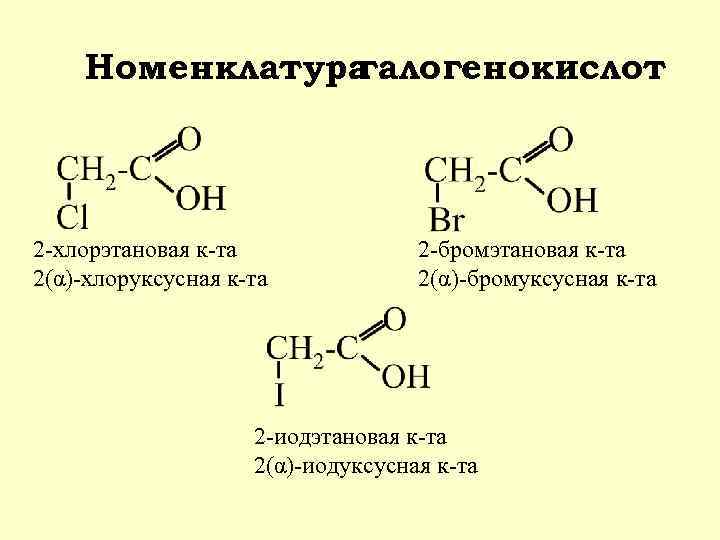 Номенклатура галогенокислот 2 -хлорэтановая к-та 2(α)-хлоруксусная к-та 2 -бромэтановая к-та 2(α)-бромуксусная к-та 2 -иодэтановая к-та 2(α)-иодуксусная к-та
Номенклатура галогенокислот 2 -хлорэтановая к-та 2(α)-хлоруксусная к-та 2 -бромэтановая к-та 2(α)-бромуксусная к-та 2 -иодэтановая к-та 2(α)-иодуксусная к-та
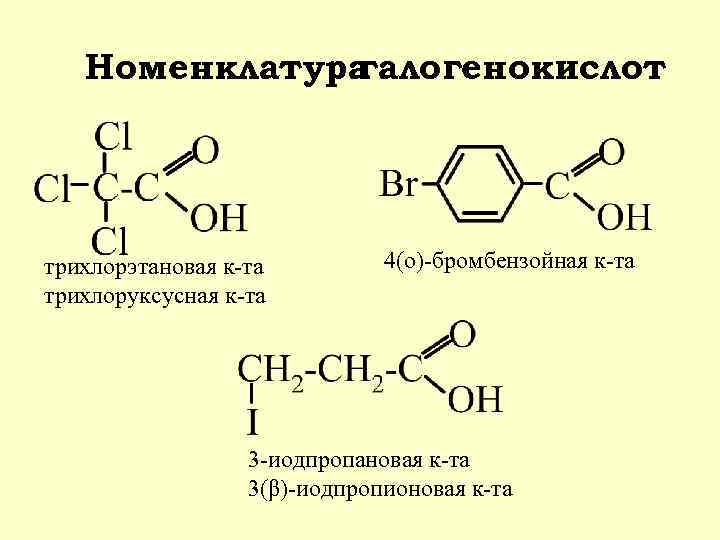 Номенклатура галогенокислот трихлорэтановая к-та трихлоруксусная к-та 4(о)-бромбензойная к-та 3 -иодпропановая к-та 3(β)-иодпропионовая к-та
Номенклатура галогенокислот трихлорэтановая к-та трихлоруксусная к-та 4(о)-бромбензойная к-та 3 -иодпропановая к-та 3(β)-иодпропионовая к-та
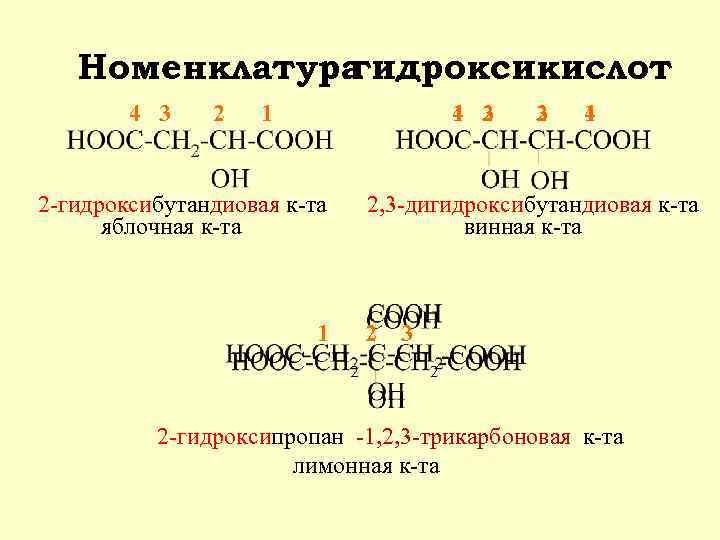 Номенклатура гидроксикислот 4 3 2 1 1 2 4 3 2 -гидроксибутандиовая к-та яблочная к-та 1 3 2 4 1 2, 3 -дигидроксибутандиовая к-та винная к-та 2 3 2 -гидроксипропан -1, 2, 3 -трикарбоновая к-та лимонная к-та
Номенклатура гидроксикислот 4 3 2 1 1 2 4 3 2 -гидроксибутандиовая к-та яблочная к-та 1 3 2 4 1 2, 3 -дигидроксибутандиовая к-та винная к-та 2 3 2 -гидроксипропан -1, 2, 3 -трикарбоновая к-та лимонная к-та
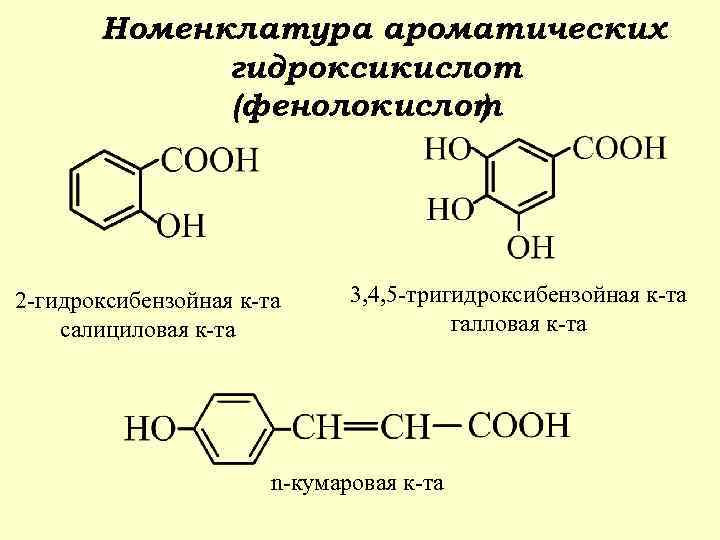 Номенклатура ароматических гидроксикислот (фенолокислот ) 2 -гидроксибензойная к-та салициловая к-та 3, 4, 5 -тригидроксибензойная к-та галловая к-та n-кумаровая к-та
Номенклатура ароматических гидроксикислот (фенолокислот ) 2 -гидроксибензойная к-та салициловая к-та 3, 4, 5 -тригидроксибензойная к-та галловая к-та n-кумаровая к-та
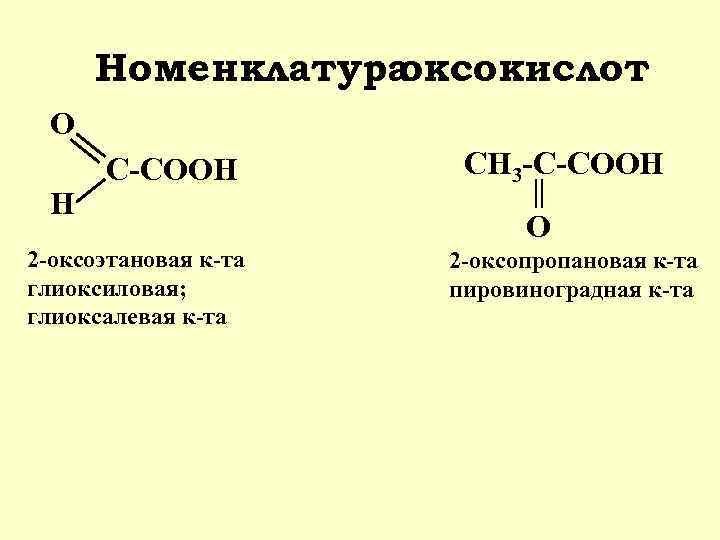 Номенклатура оксокислот O H C-COOH 2 -оксоэтановая к-та глиоксиловая; глиоксалевая к-та CH 3 -C-COOH O 2 -оксопропановая к-та пировиноградная к-та
Номенклатура оксокислот O H C-COOH 2 -оксоэтановая к-та глиоксиловая; глиоксалевая к-та CH 3 -C-COOH O 2 -оксопропановая к-та пировиноградная к-та
 Номенклатура оксокислот CH 3 -C-CH 2 -COOH O 3 -оксобутановая к-та ацетоуксусная к-та HOOC-C-CH 2 -COOH O 2 -оксобутандиовая к-та щавелевоуксусная к-та
Номенклатура оксокислот CH 3 -C-CH 2 -COOH O 3 -оксобутановая к-та ацетоуксусная к-та HOOC-C-CH 2 -COOH O 2 -оксобутандиовая к-та щавелевоуксусная к-та
 Способы получения
Способы получения
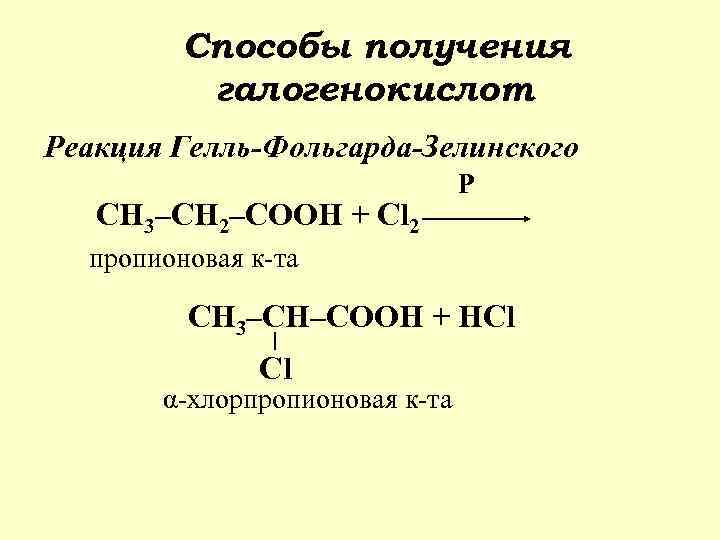 Способы получения галогенокислот Реакция Гелль-Фольгарда-Зелинского СН 3–СН 2–СООН + Cl 2 Р пропионовая к-та СН 3–СН–СООН + НCl Cl α-хлорпропионовая к-та
Способы получения галогенокислот Реакция Гелль-Фольгарда-Зелинского СН 3–СН 2–СООН + Cl 2 Р пропионовая к-та СН 3–СН–СООН + НCl Cl α-хлорпропионовая к-та
 Способы получения галогенокислот Реакция галогенирования СН 2=СН–СООН + Br 2 пропеновая к-та СН 2–СН–СООН Br Br 2, 3 -дибромпропановая к-та H 2 O
Способы получения галогенокислот Реакция галогенирования СН 2=СН–СООН + Br 2 пропеновая к-та СН 2–СН–СООН Br Br 2, 3 -дибромпропановая к-та H 2 O
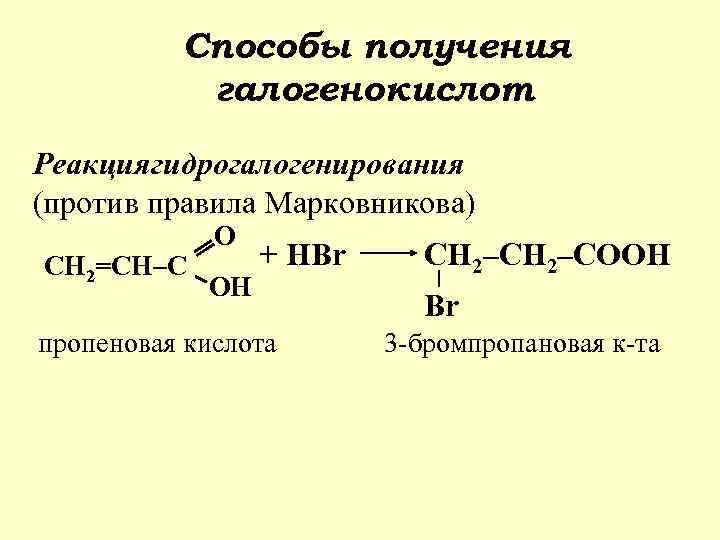 Способы получения галогенокислот Реакциягидрогалогенирования (против правила Марковникова) СН 2=СН–С О ОН + НBr пропеновая кислота СН 2–СООН Br 3 -бромпропановая к-та
Способы получения галогенокислот Реакциягидрогалогенирования (против правила Марковникова) СН 2=СН–С О ОН + НBr пропеновая кислота СН 2–СООН Br 3 -бромпропановая к-та
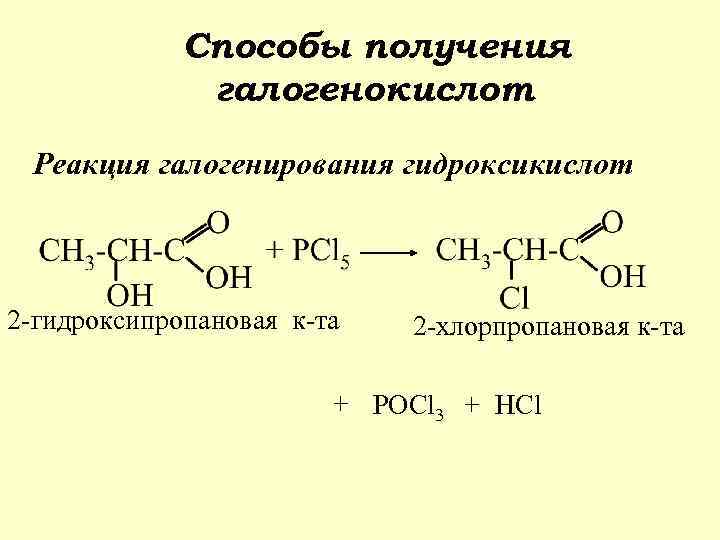 Способы получения галогенокислот Реакция галогенирования гидроксикислот 2 -гидроксипропановая к-та 2 -хлорпропановая к-та + РOCl 3 + HCl
Способы получения галогенокислот Реакция галогенирования гидроксикислот 2 -гидроксипропановая к-та 2 -хлорпропановая к-та + РOCl 3 + HCl
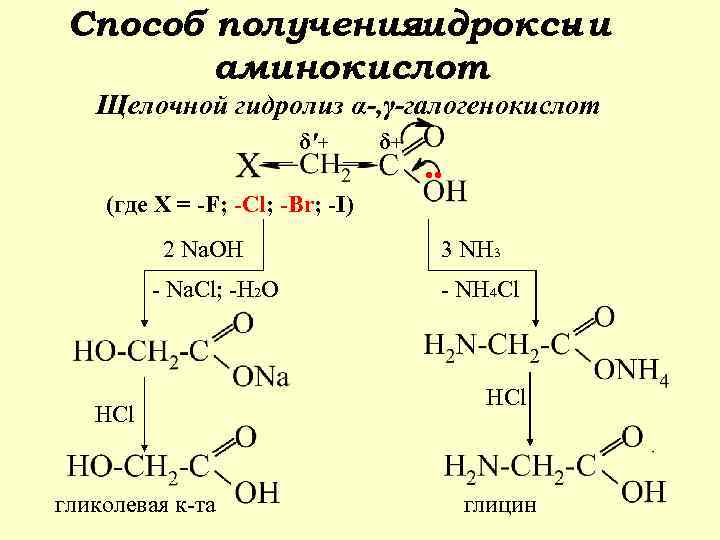 Способ получения гидрокси и аминокислот Щелочной гидролиз α-, γ-галогенокислот δ′+ δ+ . . (где Х = -F; -Cl; -Br; -I) 2 Na. OH - Na. Cl; -H 2 O HCl гликолевая к-та 3 NH 3 - NH 4 Сl HCl глицин
Способ получения гидрокси и аминокислот Щелочной гидролиз α-, γ-галогенокислот δ′+ δ+ . . (где Х = -F; -Cl; -Br; -I) 2 Na. OH - Na. Cl; -H 2 O HCl гликолевая к-та 3 NH 3 - NH 4 Сl HCl глицин
![Способы получения гидроксикислот Неполное окисление гликолей [O] этиленгликоль [O] гликолевый альдегид гликолевая к-та Способы получения гидроксикислот Неполное окисление гликолей [O] этиленгликоль [O] гликолевый альдегид гликолевая к-та](https://present5.com/presentation/-45206947_146669242/image-18.jpg) Способы получения гидроксикислот Неполное окисление гликолей [O] этиленгликоль [O] гликолевый альдегид гликолевая к-та
Способы получения гидроксикислот Неполное окисление гликолей [O] этиленгликоль [O] гликолевый альдегид гликолевая к-та
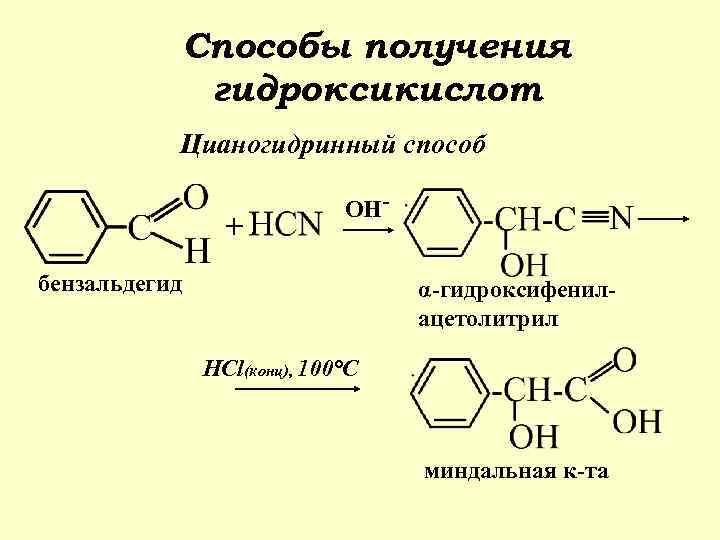 Способы получения гидроксикислот Цианогидринный способ + ОН- бензальдегид α-гидроксифенилацетолитрил HCl(конц), 100°С миндальная к-та
Способы получения гидроксикислот Цианогидринный способ + ОН- бензальдегид α-гидроксифенилацетолитрил HCl(конц), 100°С миндальная к-та
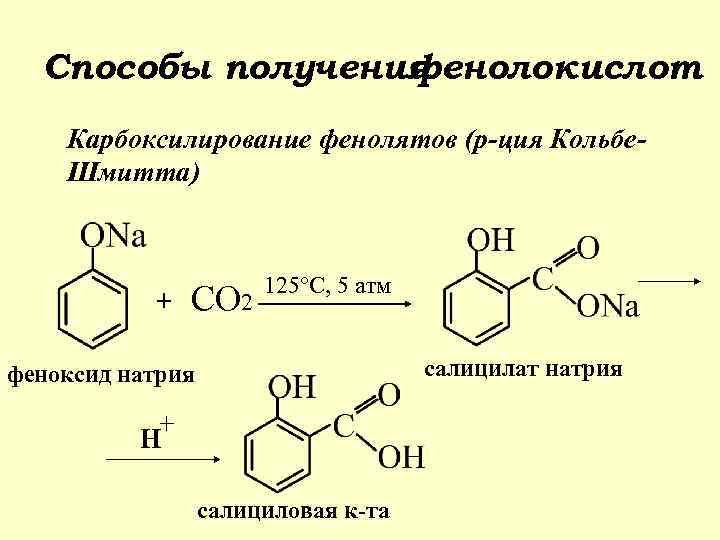 Способы получения фенолокислот Карбоксилирование фенолятов (р-ция Кольбе. Шмитта) + СО 2 125°C, 5 атм салицилат натрия феноксид натрия + H салициловая к-та
Способы получения фенолокислот Карбоксилирование фенолятов (р-ция Кольбе. Шмитта) + СО 2 125°C, 5 атм салицилат натрия феноксид натрия + H салициловая к-та
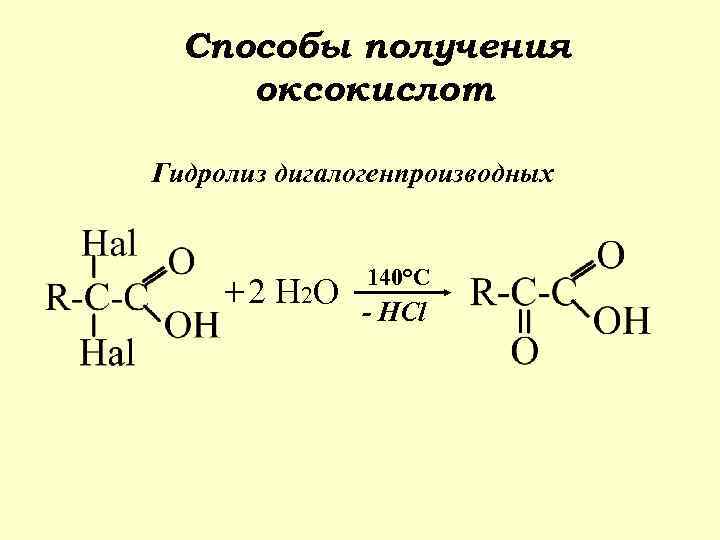 Способы получения оксокислот Гидролиз дигалогенпроизводных + 2 H 2 O 140°C - HCl
Способы получения оксокислот Гидролиз дигалогенпроизводных + 2 H 2 O 140°C - HCl
![Способы получения оксокислот Окисление гидроксикослот [O] молочная к-та пировиноградная к-та Способы получения оксокислот Окисление гидроксикослот [O] молочная к-та пировиноградная к-та](https://present5.com/presentation/-45206947_146669242/image-22.jpg) Способы получения оксокислот Окисление гидроксикослот [O] молочная к-та пировиноградная к-та
Способы получения оксокислот Окисление гидроксикослот [O] молочная к-та пировиноградная к-та
 Химические свойства обусловленные наличием карбоксильной группы
Химические свойства обусловленные наличием карбоксильной группы
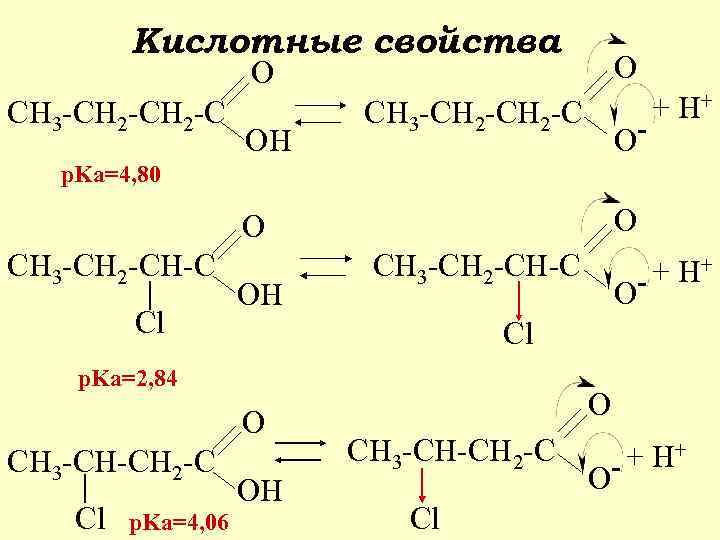 Кислотные свойства O O CH 3 -CH 2 -C OH CH 3 -CH 2 -C O- + H+ p. Ka=4, 80 O O CH 3 -CH 2 -CH-C Cl OH CH 3 -CH 2 -CH-C Cl p. Ka=2, 84 O CH 3 -CH-CH 2 -C Cl p. Ka=4, 06 O + H+ - OH O CH 3 -CH-CH 2 -C Cl O + H+ -
Кислотные свойства O O CH 3 -CH 2 -C OH CH 3 -CH 2 -C O- + H+ p. Ka=4, 80 O O CH 3 -CH 2 -CH-C Cl OH CH 3 -CH 2 -CH-C Cl p. Ka=2, 84 O CH 3 -CH-CH 2 -C Cl p. Ka=4, 06 O + H+ - OH O CH 3 -CH-CH 2 -C Cl O + H+ -
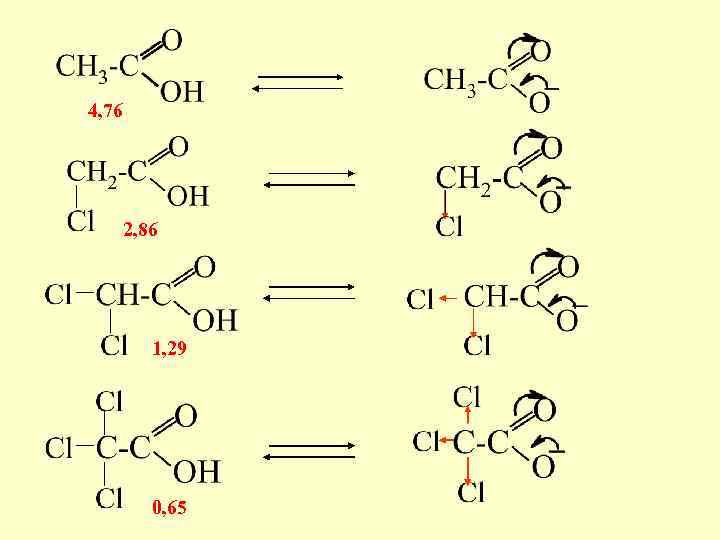 4, 76 2, 86 1, 29 0, 65
4, 76 2, 86 1, 29 0, 65
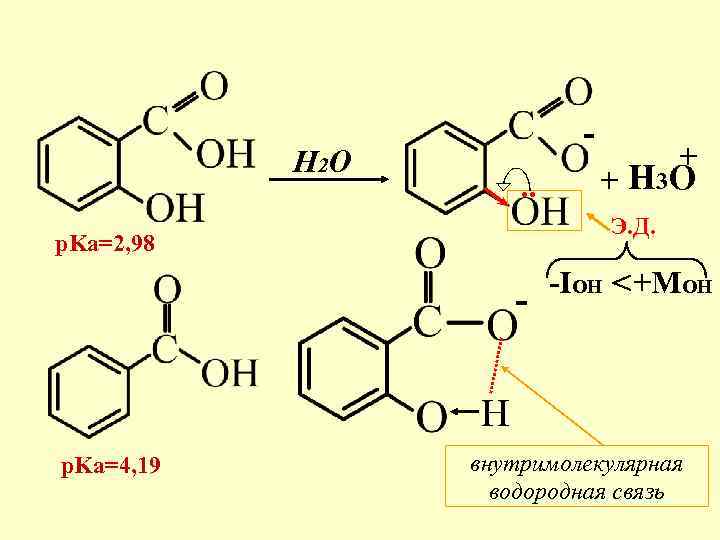 - H 2 O . . + + H 3 O Э. Д. - > p. Ka=2, 98 -IOH +MOH H p. Ka=4, 19 внутримолекулярная водородная связь
- H 2 O . . + + H 3 O Э. Д. - > p. Ka=2, 98 -IOH +MOH H p. Ka=4, 19 внутримолекулярная водородная связь
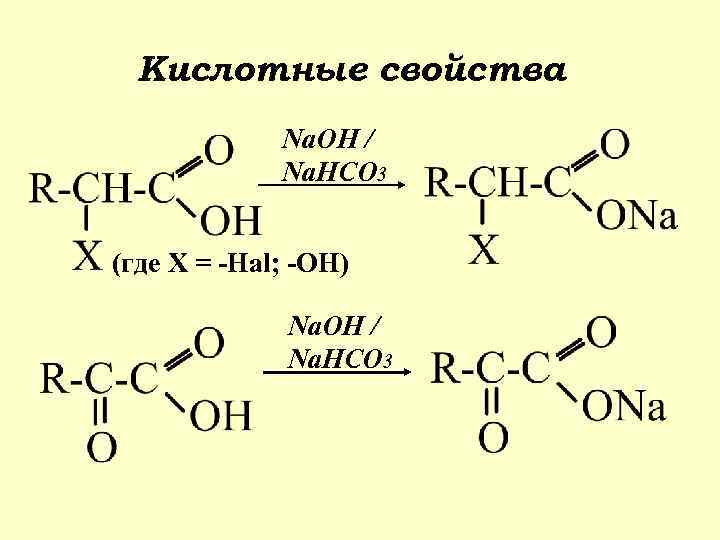 Кислотные свойства Na. OH / Na. HCO 3 (где Х = -Hal; -OH) Na. OH / Na. HCO 3
Кислотные свойства Na. OH / Na. HCO 3 (где Х = -Hal; -OH) Na. OH / Na. HCO 3
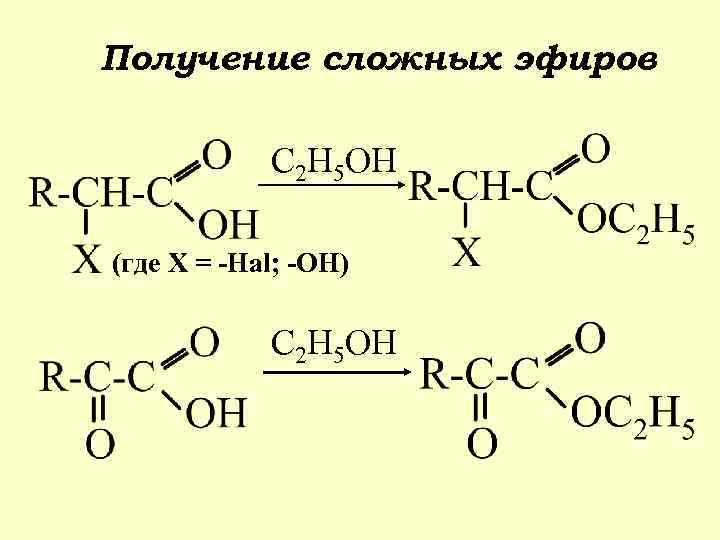 Получение сложных эфиров C 2 H 5 OH (где Х = -Hal; -OH) C 2 H 5 OH
Получение сложных эфиров C 2 H 5 OH (где Х = -Hal; -OH) C 2 H 5 OH
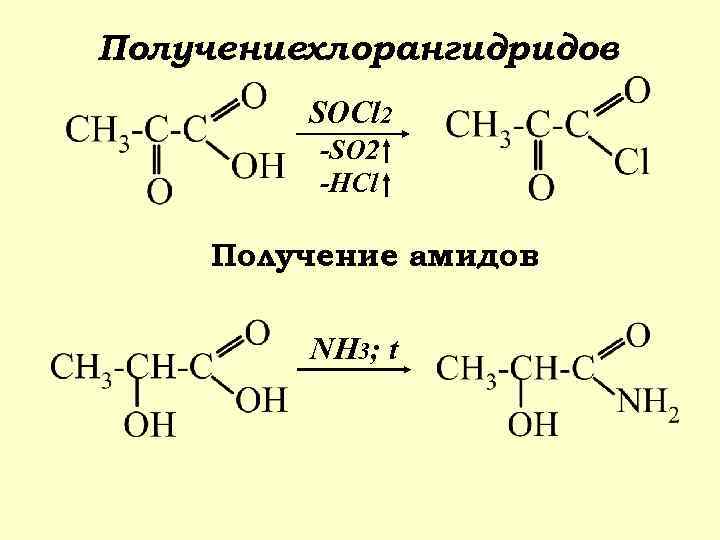 Получениехлорангидридов SOCl 2 -SO 2 -HCl Получение амидов NH 3; t
Получениехлорангидридов SOCl 2 -SO 2 -HCl Получение амидов NH 3; t
 Химические свойства обусловленные наличием гидроксильной группой -OH
Химические свойства обусловленные наличием гидроксильной группой -OH
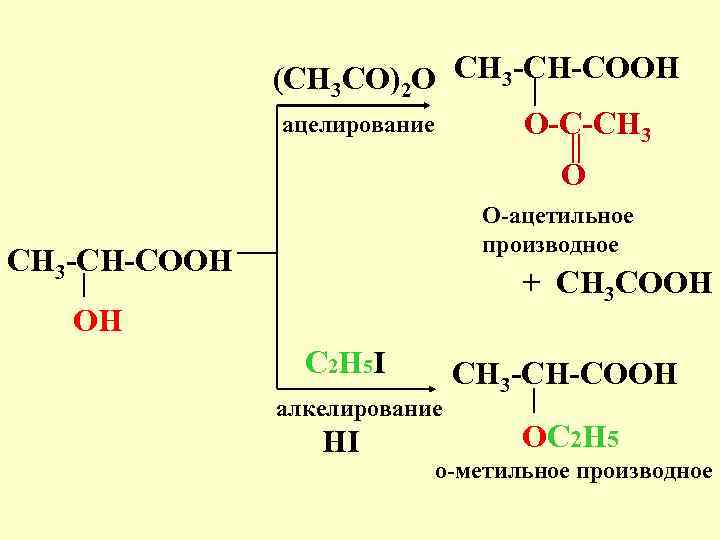 (CH 3 СO)2 O CH 3 -CH-COOH ацелирование O-C-CH 3 O O-ацетильное производное CH 3 -CH-COOH + CH 3 COOH OH C 2 H 5 I алкелирование HI CH 3 -CH-COOH OC 2 H 5 o-метильное производное
(CH 3 СO)2 O CH 3 -CH-COOH ацелирование O-C-CH 3 O O-ацетильное производное CH 3 -CH-COOH + CH 3 COOH OH C 2 H 5 I алкелирование HI CH 3 -CH-COOH OC 2 H 5 o-метильное производное
![CH 3 -CH-COOH OH молочная к-та [O] CH 3 -C-COOH O пировиноградная кислота CH 3 -CH-COOH OH молочная к-та [O] CH 3 -C-COOH O пировиноградная кислота](https://present5.com/presentation/-45206947_146669242/image-32.jpg) CH 3 -CH-COOH OH молочная к-та [O] CH 3 -C-COOH O пировиноградная кислота
CH 3 -CH-COOH OH молочная к-та [O] CH 3 -C-COOH O пировиноградная кислота
 Химические свойства обусловленные наличием карбонильной группой
Химические свойства обусловленные наличием карбонильной группой
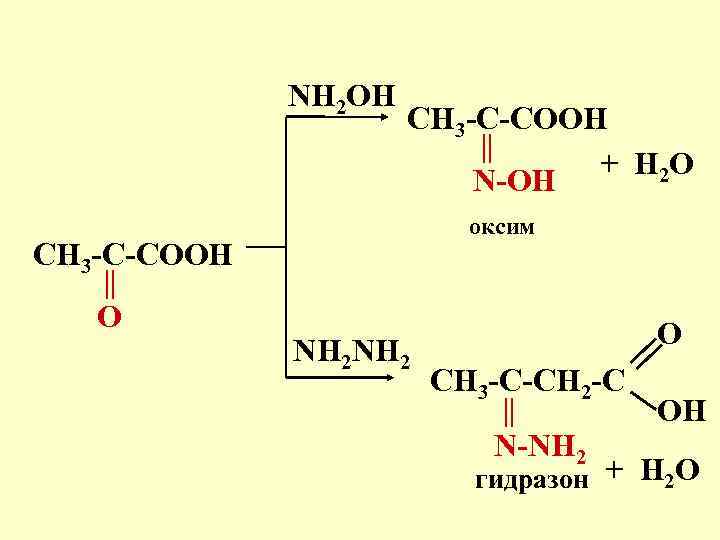 NH 2 OH CH 3 -C-COOH + H 2 O N-OH оксим CH 3 -C-COOH O NH 2 O CH 3 -C-CH 2 -C N-NH 2 OH гидразон + H 2 O
NH 2 OH CH 3 -C-COOH + H 2 O N-OH оксим CH 3 -C-COOH O NH 2 O CH 3 -C-CH 2 -C N-NH 2 OH гидразон + H 2 O
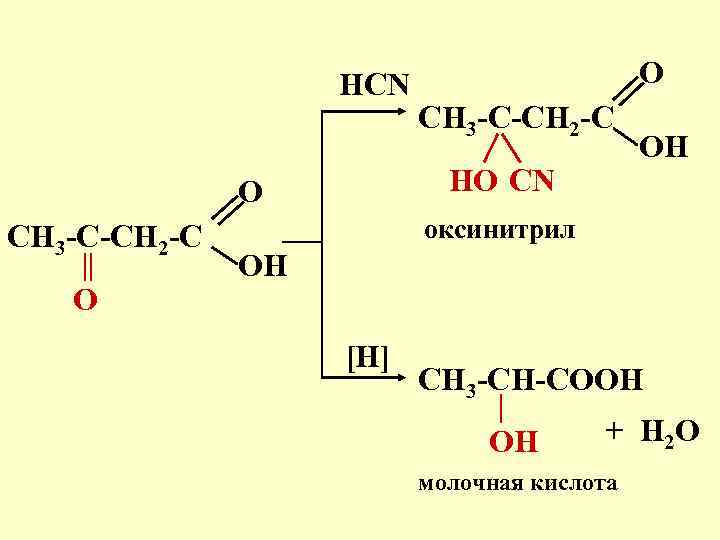 HCN O CH 3 -C-CH 2 -C HO CN O CH 3 -C-CH 2 -C O OH оксинитрил OH [H] CH 3 -CH-COOH OH + H 2 O молочная кислота
HCN O CH 3 -C-CH 2 -C HO CN O CH 3 -C-CH 2 -C O OH оксинитрил OH [H] CH 3 -CH-COOH OH + H 2 O молочная кислота
 Специфические свойства
Специфические свойства
 Специфические свойства α-оксикислот CH 3 -CH-COOH OH o конц. H 2 SO 4 t H-COOH + муравьиная кислота O CH 3 -C уксусный альдегид H
Специфические свойства α-оксикислот CH 3 -CH-COOH OH o конц. H 2 SO 4 t H-COOH + муравьиная кислота O CH 3 -C уксусный альдегид H
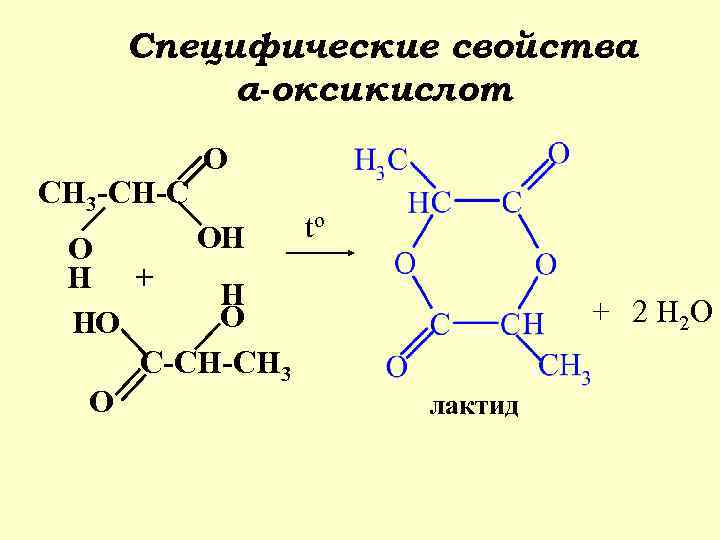 Специфические свойства α-оксикислот CH 3 -CH-C O OH O H + H O HO C-CH-CH 3 O to + 2 H 2 O лактид
Специфические свойства α-оксикислот CH 3 -CH-C O OH O H + H O HO C-CH-CH 3 O to + 2 H 2 O лактид
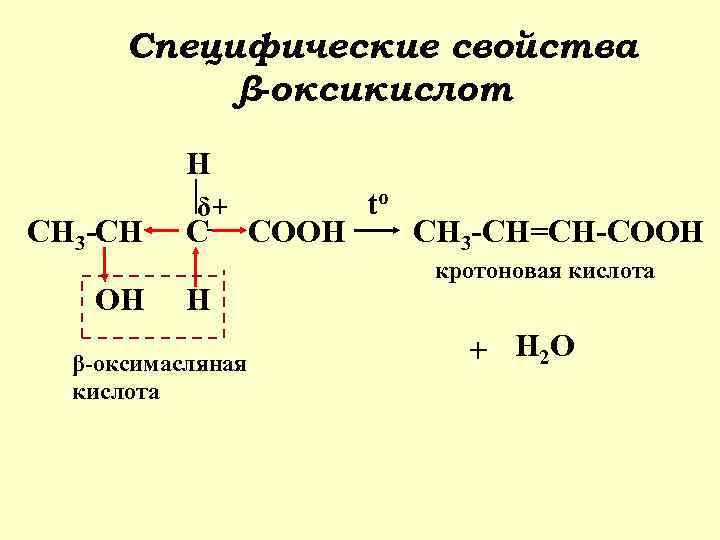 Специфические свойства β-оксикислот H CH 3 -CH OH δ+ C H β-оксимасляная кислота COOH to CH 3 -CH=CH-COOH кротоновая кислота + H 2 O
Специфические свойства β-оксикислот H CH 3 -CH OH δ+ C H β-оксимасляная кислота COOH to CH 3 -CH=CH-COOH кротоновая кислота + H 2 O
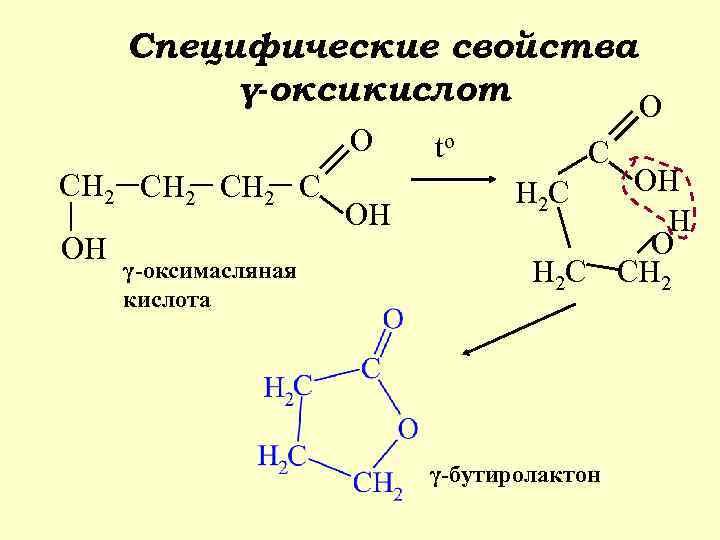 Специфические свойства γ-оксикислот O O CH 2 C OH γ-оксимасляная кислота OH to C OH H O H 2 C CH 2 H 2 C γ-бутиролактон
Специфические свойства γ-оксикислот O O CH 2 C OH γ-оксимасляная кислота OH to C OH H O H 2 C CH 2 H 2 C γ-бутиролактон
 Гидролиз лактонов H 2 O, HCl to CH 2 -CH 2 -COOH OH γ-оксимасляная кислота γ-бутиролактон H 2 O, Na. OH to CH 2 -CH 2 -COONa OH γ-оксибутират натрия
Гидролиз лактонов H 2 O, HCl to CH 2 -CH 2 -COOH OH γ-оксимасляная кислота γ-бутиролактон H 2 O, Na. OH to CH 2 -CH 2 -COONa OH γ-оксибутират натрия
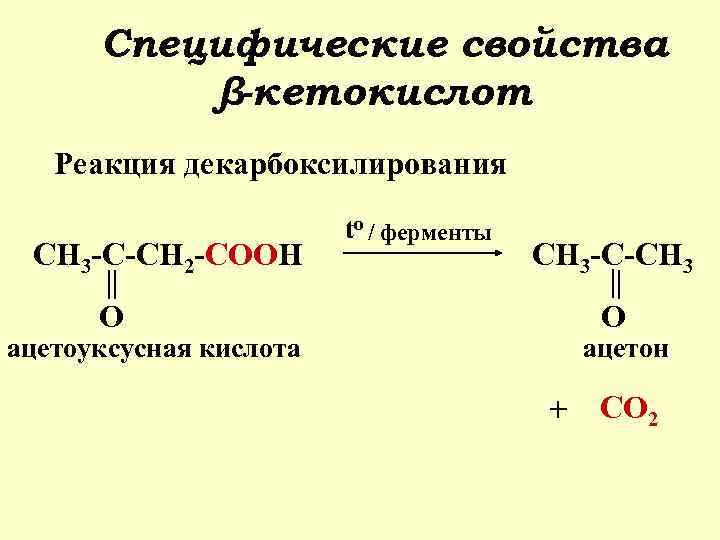 Специфические свойства β-кетокислот Реакция декарбоксилирования CH 3 -C-CH 2 -COOH to / ферменты CH 3 -C-CH 3 O O ацетоуксусная кислота ацетон + CO 2
Специфические свойства β-кетокислот Реакция декарбоксилирования CH 3 -C-CH 2 -COOH to / ферменты CH 3 -C-CH 3 O O ацетоуксусная кислота ацетон + CO 2
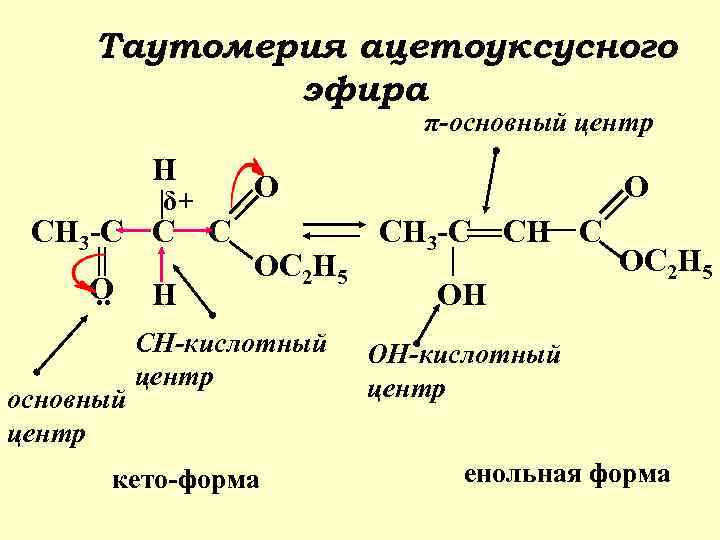 Таутомерия ацетоуксусного эфира π-основный центр H δ+ CH 3 -C C O. . основный центр H O C OC 2 H 5 CH-кислотный центр кето-форма O CH 3 -C CH C OH OC 2 H 5 OH-кислотный центр енольная форма
Таутомерия ацетоуксусного эфира π-основный центр H δ+ CH 3 -C C O. . основный центр H O C OC 2 H 5 CH-кислотный центр кето-форма O CH 3 -C CH C OH OC 2 H 5 OH-кислотный центр енольная форма
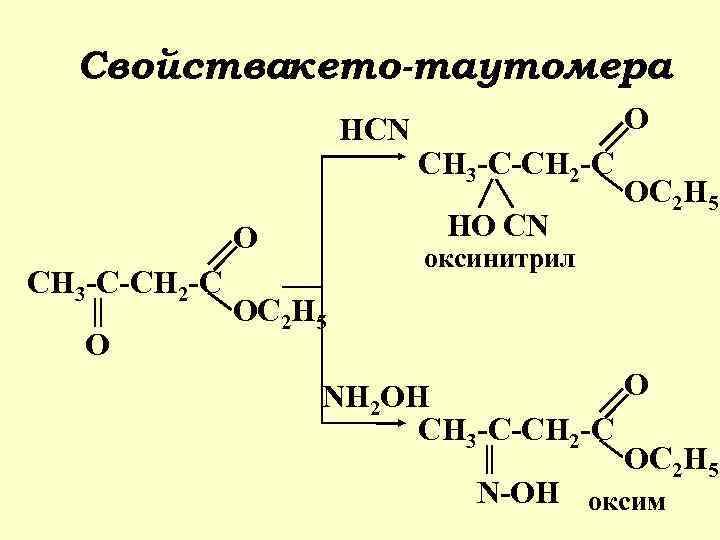 Свойствакето-таутомера HCN O CH 3 -C-CH 2 -C HO CN O CH 3 -C-CH 2 -C O OC 2 H 5 оксинитрил OC 2 H 5 O NH 2 OH CH 3 -C-CH 2 -C OC 2 H 5 N-OH оксим
Свойствакето-таутомера HCN O CH 3 -C-CH 2 -C HO CN O CH 3 -C-CH 2 -C O OC 2 H 5 оксинитрил OC 2 H 5 O NH 2 OH CH 3 -C-CH 2 -C OC 2 H 5 N-OH оксим
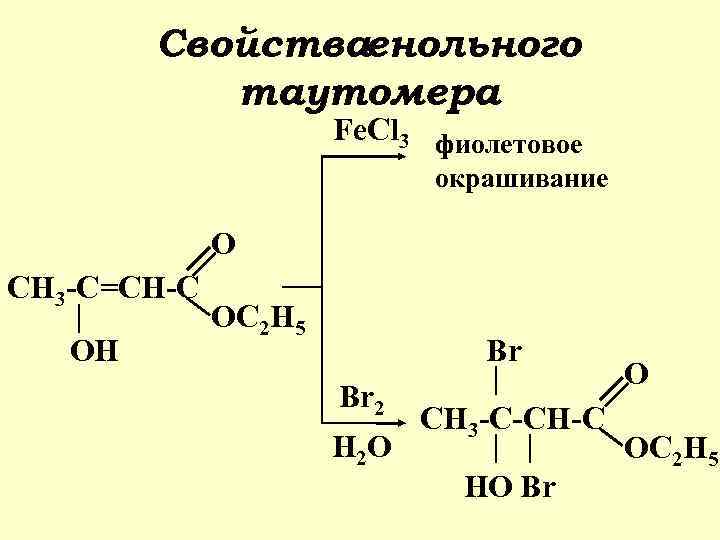 Свойстваенольного таутомера Fe. Cl 3 фиолетовое окрашивание O CH 3 -C=CH-C OH OC 2 H 5 Br Br 2 H 2 O CH 3 -C-CH-C HO Br O OC 2 H 5
Свойстваенольного таутомера Fe. Cl 3 фиолетовое окрашивание O CH 3 -C=CH-C OH OC 2 H 5 Br Br 2 H 2 O CH 3 -C-CH-C HO Br O OC 2 H 5
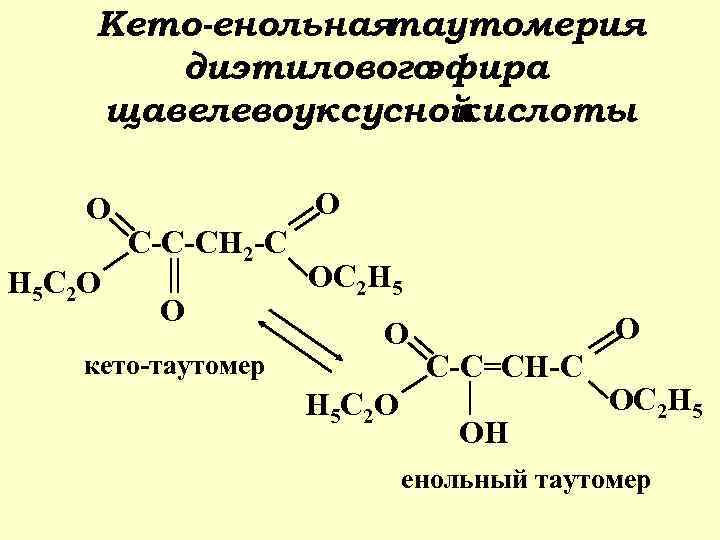 Кето-енольная таутомерия диэтилового эфира щавелевоуксусной кислоты O H 5 C 2 O O C-C-CH 2 -C O кето-таутомер OC 2 H 5 O H 5 C 2 O O C-C=CH-C OH OC 2 H 5 енольный таутомер
Кето-енольная таутомерия диэтилового эфира щавелевоуксусной кислоты O H 5 C 2 O O C-C-CH 2 -C O кето-таутомер OC 2 H 5 O H 5 C 2 O O C-C=CH-C OH OC 2 H 5 енольный таутомер
 Кислотное и кетонное расщепление O C OC 2 H 5 = = ие R ен л ие н еп ле щ сеп СH C CH 3 ра сщ е ора О O е тн 2 ло о , Н нн с т ки о OH е к R Na этиловый эфир O карбоновой к-ты Na + ир O т. р H - сп -р = -OH R R CH C O β OC 2 H 5 O t α СH 3 C CH C + OC 2 H 5 O H -CO 2 OН O O СHкетон 3 C O уксусная к-та = = _ = =
Кислотное и кетонное расщепление O C OC 2 H 5 = = ие R ен л ие н еп ле щ сеп СH C CH 3 ра сщ е ора О O е тн 2 ло о , Н нн с т ки о OH е к R Na этиловый эфир O карбоновой к-ты Na + ир O т. р H - сп -р = -OH R R CH C O β OC 2 H 5 O t α СH 3 C CH C + OC 2 H 5 O H -CO 2 OН O O СHкетон 3 C O уксусная к-та = = _ = =
 Отдельные представители
Отдельные представители
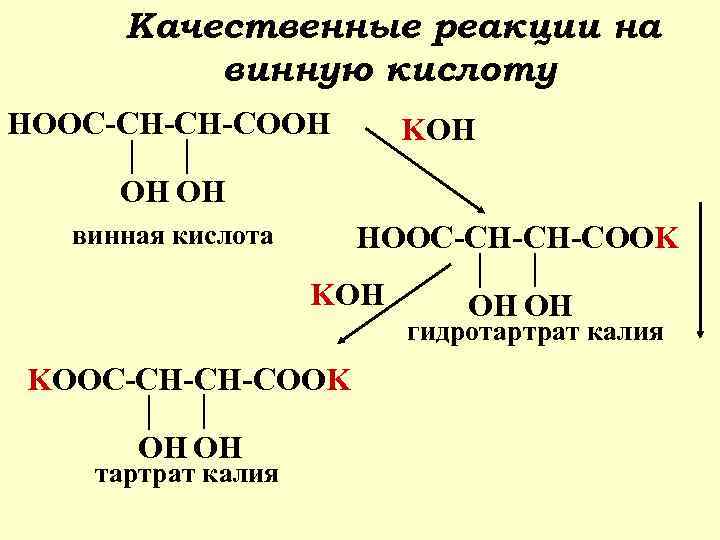 Качественные реакции на винную кислоту HOOC-CH-CH-COOH KOH OH OH винная кислота HOOC-CH-CH-COOK KOH OH OH гидротартрат калия KOOC-CH-CH-COOK OH OH тартрат калия
Качественные реакции на винную кислоту HOOC-CH-CH-COOH KOH OH OH винная кислота HOOC-CH-CH-COOK KOH OH OH гидротартрат калия KOOC-CH-CH-COOK OH OH тартрат калия
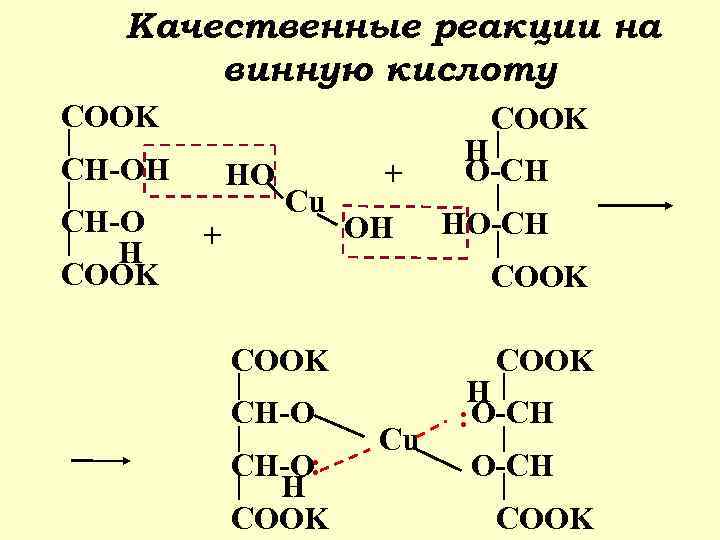 Качественные реакции на винную кислоту COOK CH-OH CH-O H COOK HO + Cu + H O-CH OH HO-CH COOK CH-O: H COOK Cu H : O-CH COOK
Качественные реакции на винную кислоту COOK CH-OH CH-O H COOK HO + Cu + H O-CH OH HO-CH COOK CH-O: H COOK Cu H : O-CH COOK
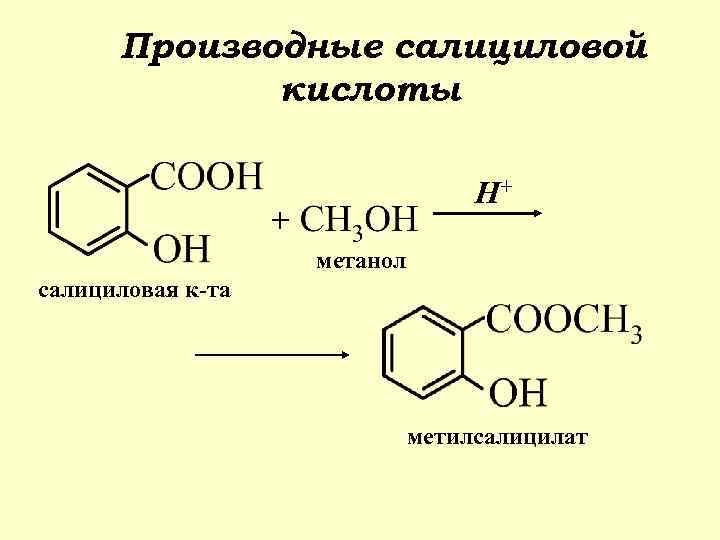 Производные салициловой кислоты H+ + метанол салициловая к-та метилсалицилат
Производные салициловой кислоты H+ + метанол салициловая к-та метилсалицилат
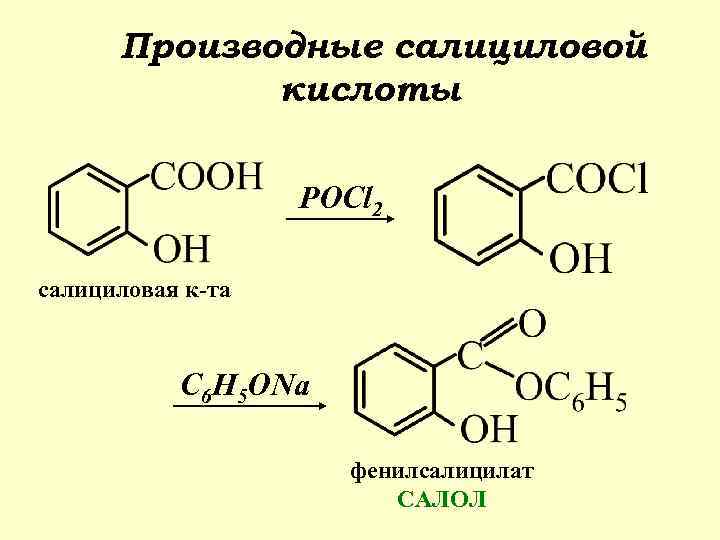 Производные салициловой кислоты POCl 2 салициловая к-та C 6 H 5 ONa фенилсалицилат САЛОЛ
Производные салициловой кислоты POCl 2 салициловая к-та C 6 H 5 ONa фенилсалицилат САЛОЛ
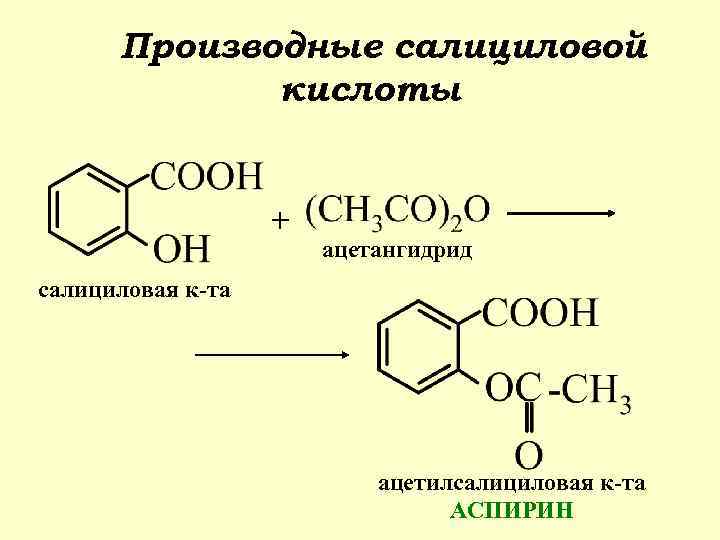 Производные салициловой кислоты + ацетангидрид салициловая к-та ацетилсалициловая к-та АСПИРИН
Производные салициловой кислоты + ацетангидрид салициловая к-та ацетилсалициловая к-та АСПИРИН
![«Кетоновые тела» [O] CH 3 -CH-CH 2 -COOH OH CH 3 -C-CH 2 «Кетоновые тела» [O] CH 3 -CH-CH 2 -COOH OH CH 3 -C-CH 2](https://present5.com/presentation/-45206947_146669242/image-54.jpg) «Кетоновые тела» [O] CH 3 -CH-CH 2 -COOH OH CH 3 -C-CH 2 -COOH β-оксимасляная кислота O CH 3 -C-CH 3 O ацетон ацетоуксусная кислота + CO 2
«Кетоновые тела» [O] CH 3 -CH-CH 2 -COOH OH CH 3 -C-CH 2 -COOH β-оксимасляная кислота O CH 3 -C-CH 3 O ацетон ацетоуксусная кислота + CO 2
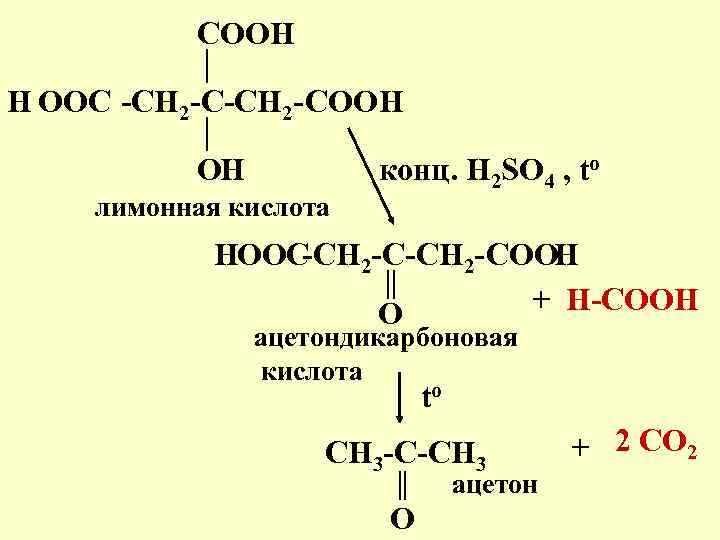 COOH H OOC -CH 2 -С-CH 2 - COOH OH лимонная кислота конц. H 2 SO 4 , to HOOC -CH 2 -С-CH 2 - COOH + H-COOH O ацетондикарбоновая кислота to CH 3 -С-CH 3 ацетон O + 2 CO 2
COOH H OOC -CH 2 -С-CH 2 - COOH OH лимонная кислота конц. H 2 SO 4 , to HOOC -CH 2 -С-CH 2 - COOH + H-COOH O ацетондикарбоновая кислота to CH 3 -С-CH 3 ацетон O + 2 CO 2


