23 гетероциклические соединения.ppt
- Количество слайдов: 28
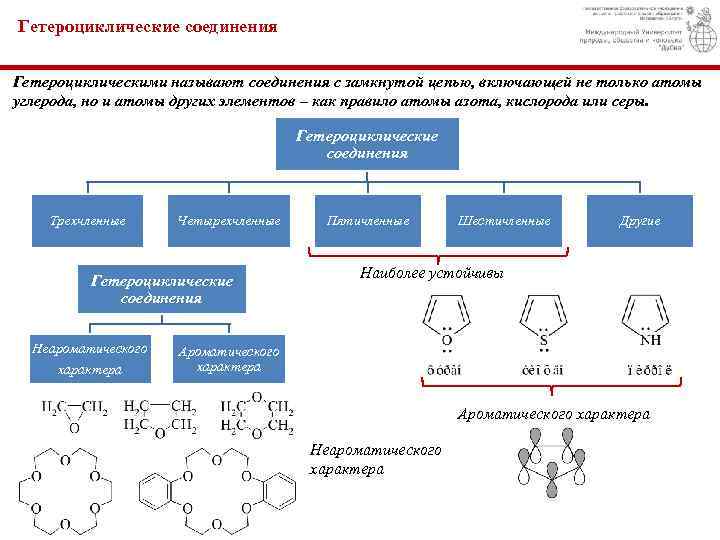 Гетероциклические соединения Гетероциклическими называют соединения с замкнутой цепью, включающей не только атомы углерода, но и атомы других элементов – как правило атомы азота, кислорода или серы. Гетероциклические соединения Трехчленные Четырехчленные Гетероциклические соединения Неароматического характера Пятичленные Шестичленные Другие Наиболее устойчивы Ароматического характера Неароматического характера
Гетероциклические соединения Гетероциклическими называют соединения с замкнутой цепью, включающей не только атомы углерода, но и атомы других элементов – как правило атомы азота, кислорода или серы. Гетероциклические соединения Трехчленные Четырехчленные Гетероциклические соединения Неароматического характера Пятичленные Шестичленные Другие Наиболее устойчивы Ароматического характера Неароматического характера
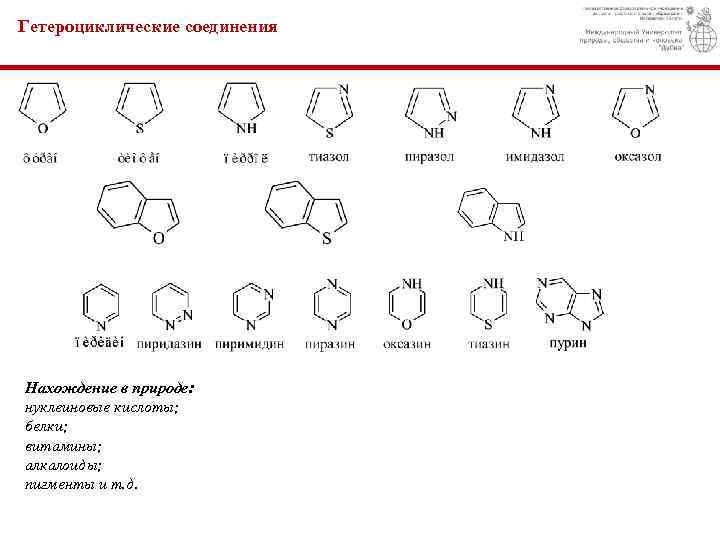 Гетероциклические соединения Нахождение в природе: нуклеиновые кислоты; белки; витамины; алкалоиды; пигменты и т. д.
Гетероциклические соединения Нахождение в природе: нуклеиновые кислоты; белки; витамины; алкалоиды; пигменты и т. д.
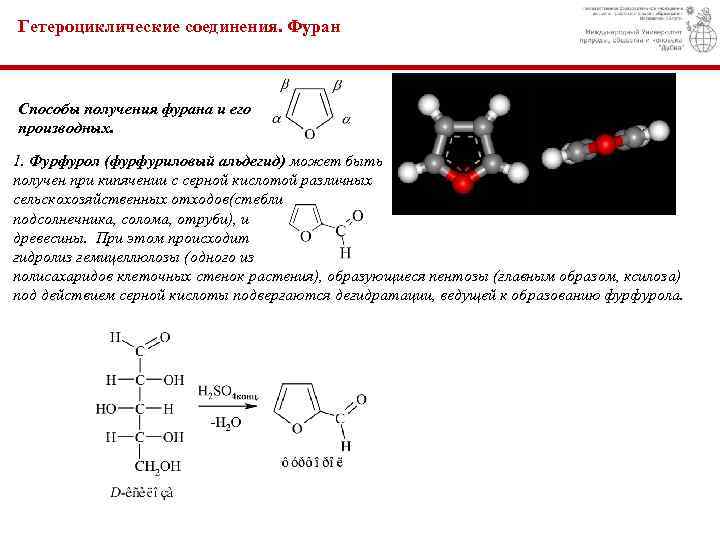 Гетероциклические соединения. Фуран Способы получения фурана и его производных. 1. Фурфурол (фурфуриловый альдегид) может быть получен при кипячении с серной кислотой различных сельскохозяйственных отходов(стебли подсолнечника, солома, отруби), и древесины. При этом происходит гидролиз гемицеллюлозы (одного из полисахаридов клеточных стенок растения), образующиеся пентозы (главным образом, ксилоза) под действием серной кислоты подвергаются дегидратации, ведущей к образованию фурфурола.
Гетероциклические соединения. Фуран Способы получения фурана и его производных. 1. Фурфурол (фурфуриловый альдегид) может быть получен при кипячении с серной кислотой различных сельскохозяйственных отходов(стебли подсолнечника, солома, отруби), и древесины. При этом происходит гидролиз гемицеллюлозы (одного из полисахаридов клеточных стенок растения), образующиеся пентозы (главным образом, ксилоза) под действием серной кислоты подвергаются дегидратации, ведущей к образованию фурфурола.
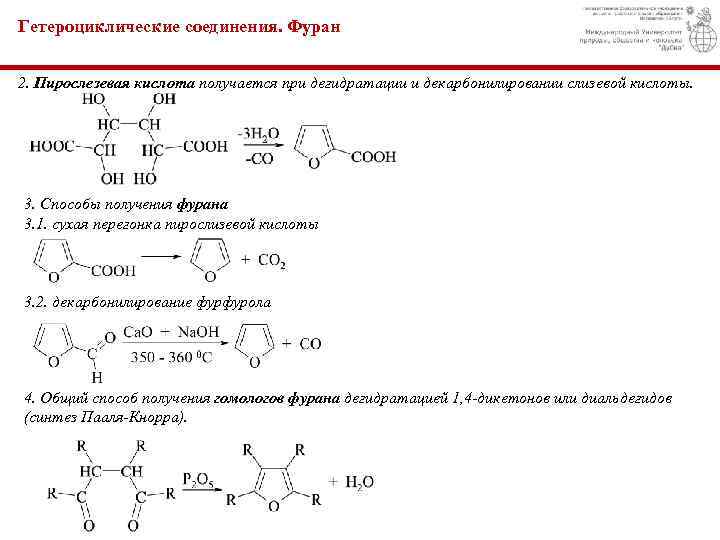 Гетероциклические соединения. Фуран 2. Пирослезевая кислота получается при дегидратации и декарбонилировании слизевой кислоты. 3. Способы получения фурана 3. 1. сухая перегонка пирослизевой кислоты 3. 2. декарбонилирование фурфурола 4. Общий способ получения гомологов фурана дегидратацией 1, 4 -дикетонов или диальдегидов (синтез Пааля-Кнорра).
Гетероциклические соединения. Фуран 2. Пирослезевая кислота получается при дегидратации и декарбонилировании слизевой кислоты. 3. Способы получения фурана 3. 1. сухая перегонка пирослизевой кислоты 3. 2. декарбонилирование фурфурола 4. Общий способ получения гомологов фурана дегидратацией 1, 4 -дикетонов или диальдегидов (синтез Пааля-Кнорра).
 Гетероциклические соединения. Фуран Химические свойства фурана 1. Раскрытие кольца. Ядро фурана устойчиво к действию щелочей и очень неустойчиво к действию кислот (ацидофобность): • с концентрированной HCl реагирует со взрывом; • с разбавленной HCl дает бурый осадок; • с метанолом, насыщенным HCl, образует ацеталь янтарного альдегида 2. Реакции электрофильного замещения происходят преимущественно в α-положения значительно легче, чем в бензоле (6 π-электронов на 5 атомов) 2. 1. галогенирование
Гетероциклические соединения. Фуран Химические свойства фурана 1. Раскрытие кольца. Ядро фурана устойчиво к действию щелочей и очень неустойчиво к действию кислот (ацидофобность): • с концентрированной HCl реагирует со взрывом; • с разбавленной HCl дает бурый осадок; • с метанолом, насыщенным HCl, образует ацеталь янтарного альдегида 2. Реакции электрофильного замещения происходят преимущественно в α-положения значительно легче, чем в бензоле (6 π-электронов на 5 атомов) 2. 1. галогенирование
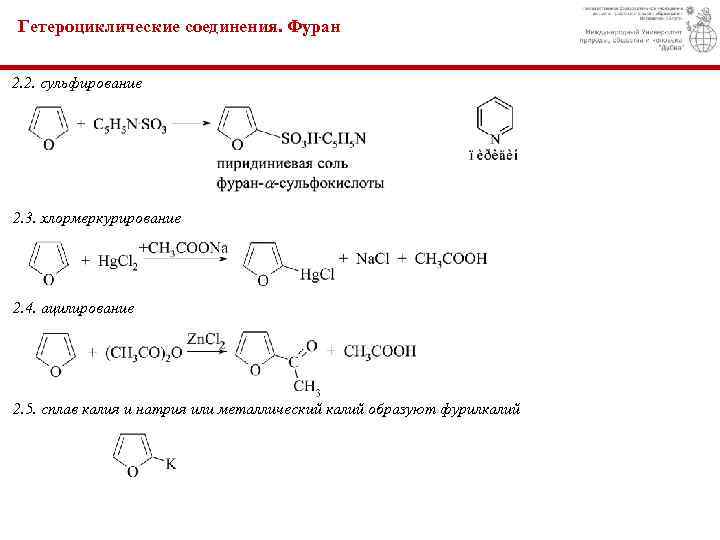 Гетероциклические соединения. Фуран 2. 2. сульфирование 2. 3. хлормеркурирование 2. 4. ацилирование 2. 5. сплав калия и натрия или металлический калий образуют фурилкалий
Гетероциклические соединения. Фуран 2. 2. сульфирование 2. 3. хлормеркурирование 2. 4. ацилирование 2. 5. сплав калия и натрия или металлический калий образуют фурилкалий
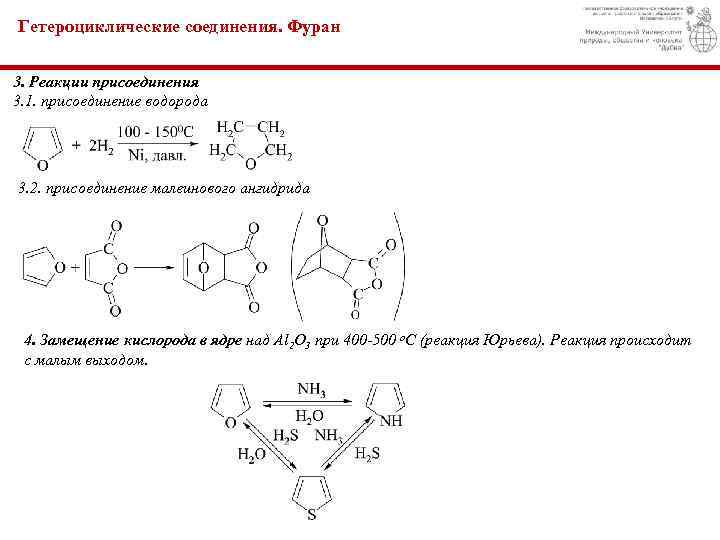 Гетероциклические соединения. Фуран 3. Реакции присоединения 3. 1. присоединение водорода 3. 2. присоединение малеинового ангидрида 4. Замещение кислорода в ядре над Al 2 O 3 при 400 -500 о. С (реакция Юрьева). Реакция происходит с малым выходом.
Гетероциклические соединения. Фуран 3. Реакции присоединения 3. 1. присоединение водорода 3. 2. присоединение малеинового ангидрида 4. Замещение кислорода в ядре над Al 2 O 3 при 400 -500 о. С (реакция Юрьева). Реакция происходит с малым выходом.
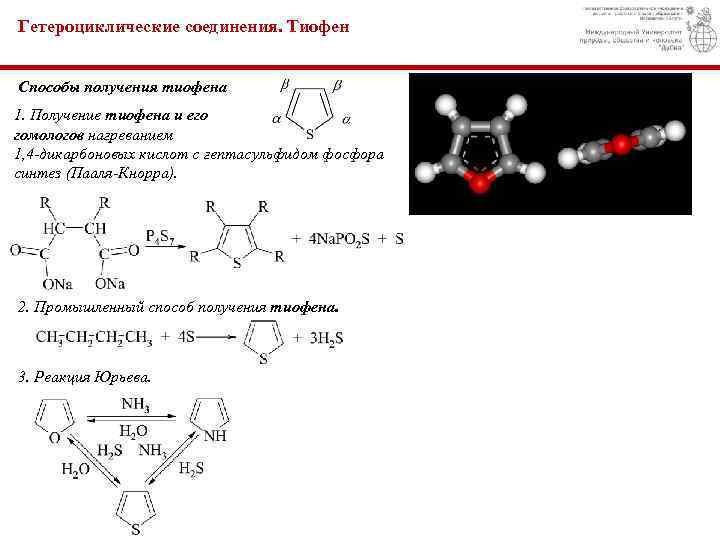 Гетероциклические соединения. Тиофен Способы получения тиофена 1. Получение тиофена и его гомологов нагреванием 1, 4 -дикарбоновых кислот с гептасульфидом фосфора синтез (Пааля-Кнорра). 2. Промышленный способ получения тиофена. 3. Реакция Юрьева.
Гетероциклические соединения. Тиофен Способы получения тиофена 1. Получение тиофена и его гомологов нагреванием 1, 4 -дикарбоновых кислот с гептасульфидом фосфора синтез (Пааля-Кнорра). 2. Промышленный способ получения тиофена. 3. Реакция Юрьева.
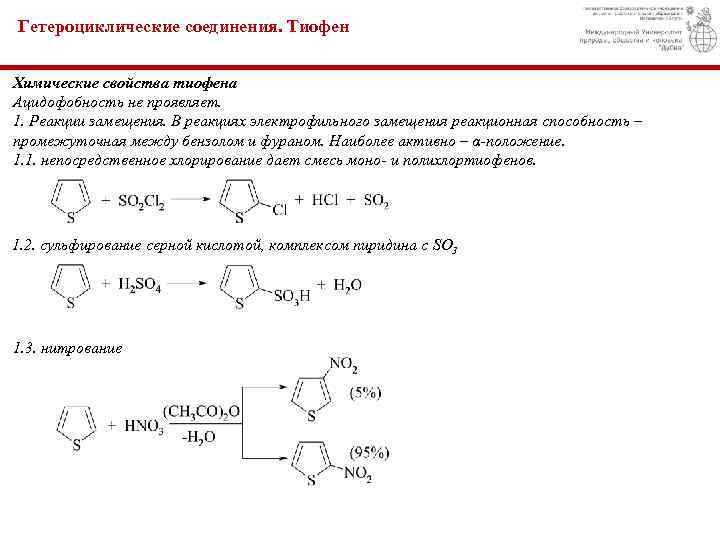 Гетероциклические соединения. Тиофен Химические свойства тиофена Ацидофобность не проявляет. 1. Реакции замещения. В реакциях электрофильного замещения реакционная способность – промежуточная между бензолом и фураном. Наиболее активно – α-положение. 1. 1. непосредственное хлорирование дает смесь моно- и полихлортиофенов. 1. 2. сульфирование серной кислотой, комплексом пиридина с SO 3 1. 3. нитрование
Гетероциклические соединения. Тиофен Химические свойства тиофена Ацидофобность не проявляет. 1. Реакции замещения. В реакциях электрофильного замещения реакционная способность – промежуточная между бензолом и фураном. Наиболее активно – α-положение. 1. 1. непосредственное хлорирование дает смесь моно- и полихлортиофенов. 1. 2. сульфирование серной кислотой, комплексом пиридина с SO 3 1. 3. нитрование
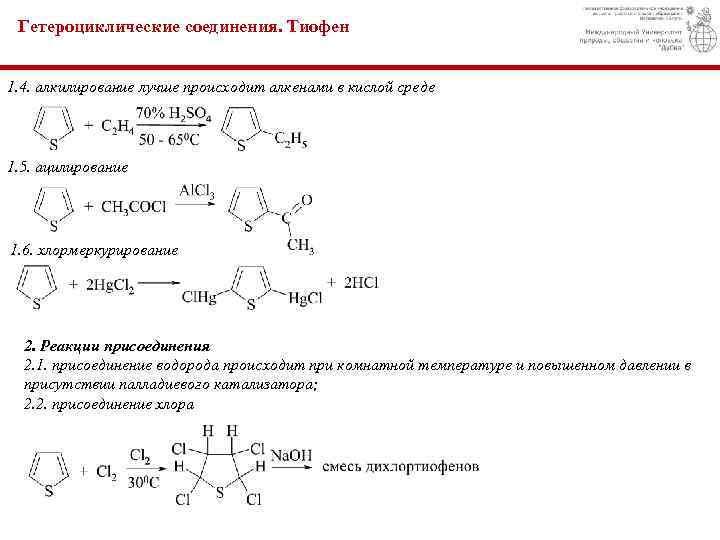 Гетероциклические соединения. Тиофен 1. 4. алкилирование лучше происходит алкенами в кислой среде 1. 5. ацилирование 1. 6. хлормеркурирование 2. Реакции присоединения 2. 1. присоединение водорода происходит при комнатной температуре и повышенном давлении в присутствии палладиевого катализатора; 2. 2. присоединение хлора
Гетероциклические соединения. Тиофен 1. 4. алкилирование лучше происходит алкенами в кислой среде 1. 5. ацилирование 1. 6. хлормеркурирование 2. Реакции присоединения 2. 1. присоединение водорода происходит при комнатной температуре и повышенном давлении в присутствии палладиевого катализатора; 2. 2. присоединение хлора
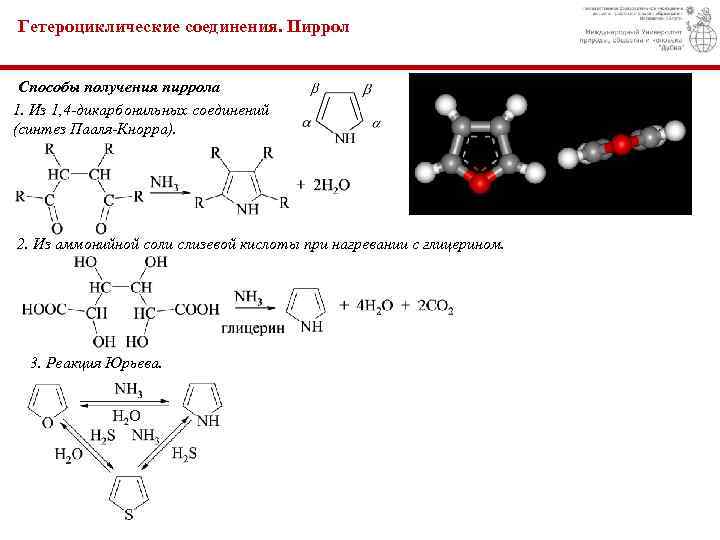 Гетероциклические соединения. Пиррол Способы получения пиррола 1. Из 1, 4 -дикарбонильных соединений (синтез Пааля-Кнорра). 2. Из аммонийной соли слизевой кислоты при нагревании с глицерином. 3. Реакция Юрьева.
Гетероциклические соединения. Пиррол Способы получения пиррола 1. Из 1, 4 -дикарбонильных соединений (синтез Пааля-Кнорра). 2. Из аммонийной соли слизевой кислоты при нагревании с глицерином. 3. Реакция Юрьева.
 Гетероциклические соединения. Пиррол Химические свойства 1. Кислотно-основные свойства Пирролкалий может быть получен сплавлением пиррола с калием в отсутствие влаги. Основные свойства не наблюдаются, т. к. в присутствие кислот пиррол полимеризуется. 2. Реакции замещения. В реакциях электрофильного замещения активен, как фенол. 2. 1. Хлор дает нестойкий тетрахлорид. Пиррол легко хлорируется хлористым сульфурилом 2. 2. Из-за нестойкости к кислотам сульфируется комплексом серного ангидрида с пиридином
Гетероциклические соединения. Пиррол Химические свойства 1. Кислотно-основные свойства Пирролкалий может быть получен сплавлением пиррола с калием в отсутствие влаги. Основные свойства не наблюдаются, т. к. в присутствие кислот пиррол полимеризуется. 2. Реакции замещения. В реакциях электрофильного замещения активен, как фенол. 2. 1. Хлор дает нестойкий тетрахлорид. Пиррол легко хлорируется хлористым сульфурилом 2. 2. Из-за нестойкости к кислотам сульфируется комплексом серного ангидрида с пиридином
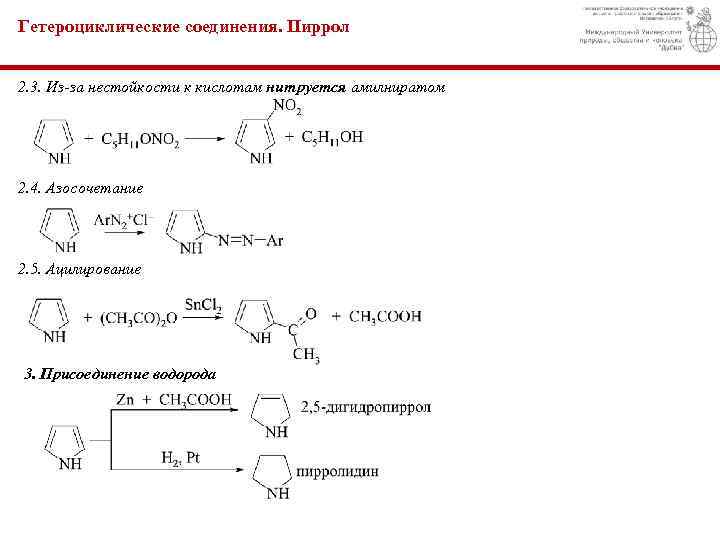 Гетероциклические соединения. Пиррол 2. 3. Из-за нестойкости к кислотам нитруется амилниратом 2. 4. Азосочетание 2. 5. Ацилирование 3. Присоединение водорода
Гетероциклические соединения. Пиррол 2. 3. Из-за нестойкости к кислотам нитруется амилниратом 2. 4. Азосочетание 2. 5. Ацилирование 3. Присоединение водорода
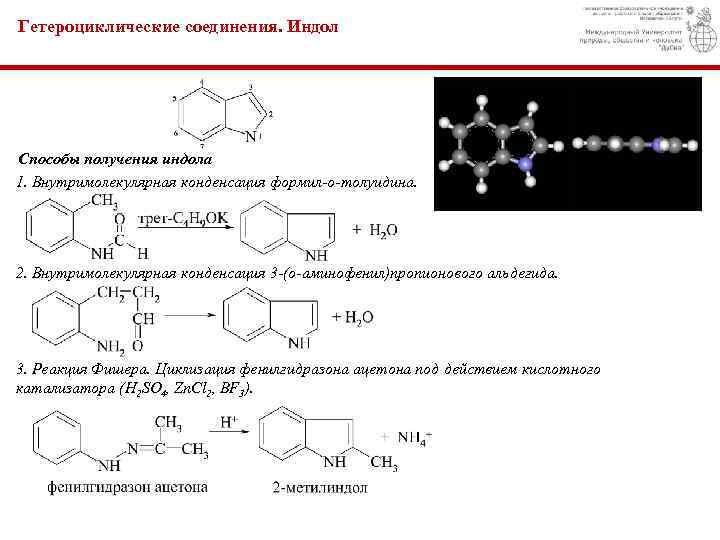 Гетероциклические соединения. Индол Способы получения индола 1. Внутримолекулярная конденсация формил-о-толуидина. 2. Внутримолекулярная конденсация 3 -(о-аминофенил)пропионового альдегида. 3. Реакция Фишера. Циклизация фенилгидразона ацетона под действием кислотного катализатора (H 2 SO 4, Zn. Cl 2, BF 3).
Гетероциклические соединения. Индол Способы получения индола 1. Внутримолекулярная конденсация формил-о-толуидина. 2. Внутримолекулярная конденсация 3 -(о-аминофенил)пропионового альдегида. 3. Реакция Фишера. Циклизация фенилгидразона ацетона под действием кислотного катализатора (H 2 SO 4, Zn. Cl 2, BF 3).
 Гетероциклические соединения. Индол Химические свойства индола 1. Образование металлических производных 2. Реакции электрофильного замещения происходят, в основном в положение 2. Если оно занято, то в положение 3. 2. 1. Галогенируется только мягко действующими реагентами (хлористый сульфурил, диоксандибромид). 2. 2. Нитруется этилнитратом. 2. 3. Вступает в реакции азосочетания
Гетероциклические соединения. Индол Химические свойства индола 1. Образование металлических производных 2. Реакции электрофильного замещения происходят, в основном в положение 2. Если оно занято, то в положение 3. 2. 1. Галогенируется только мягко действующими реагентами (хлористый сульфурил, диоксандибромид). 2. 2. Нитруется этилнитратом. 2. 3. Вступает в реакции азосочетания
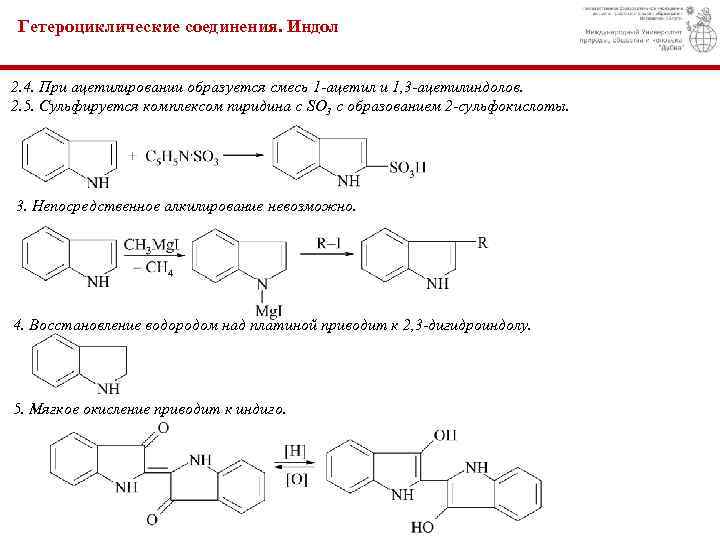 Гетероциклические соединения. Индол 2. 4. При ацетилировании образуется смесь 1 -ацетил и 1, 3 -ацетилиндолов. 2. 5. Сульфируется комплексом пиридина с SO 3 с образованием 2 -сульфокислоты. 3. Непосредственное алкилирование невозможно. 4. Восстановление водородом над платиной приводит к 2, 3 -дигидроиндолу. 5. Мягкое окисление приводит к индиго.
Гетероциклические соединения. Индол 2. 4. При ацетилировании образуется смесь 1 -ацетил и 1, 3 -ацетилиндолов. 2. 5. Сульфируется комплексом пиридина с SO 3 с образованием 2 -сульфокислоты. 3. Непосредственное алкилирование невозможно. 4. Восстановление водородом над платиной приводит к 2, 3 -дигидроиндолу. 5. Мягкое окисление приводит к индиго.
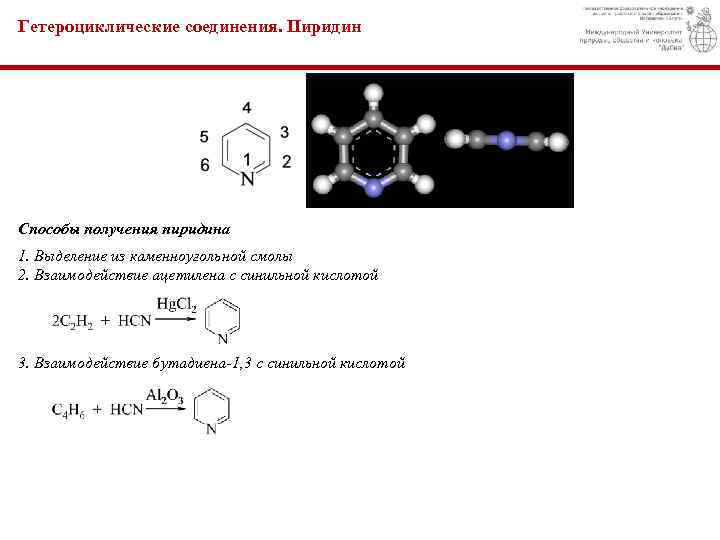 Гетероциклические соединения. Пиридин Способы получения пиридина 1. Выделение из каменноугольной смолы 2. Взаимодействие ацетилена с синильной кислотой 3. Взаимодействие бутадиена-1, 3 с синильной кислотой
Гетероциклические соединения. Пиридин Способы получения пиридина 1. Выделение из каменноугольной смолы 2. Взаимодействие ацетилена с синильной кислотой 3. Взаимодействие бутадиена-1, 3 с синильной кислотой
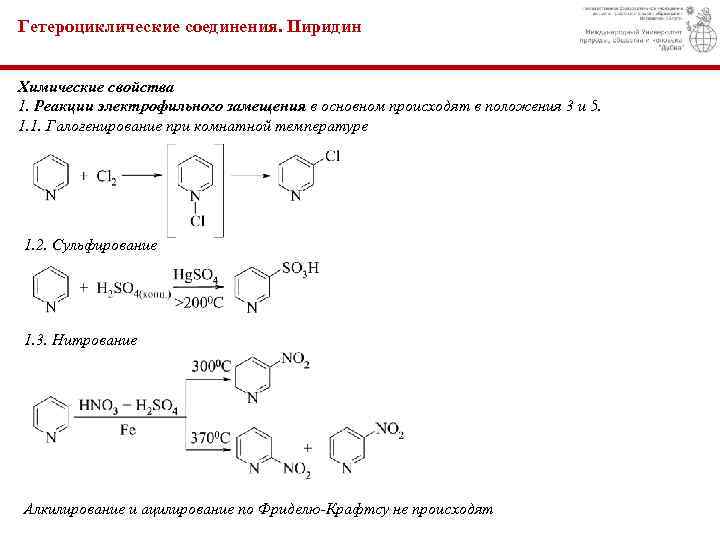 Гетероциклические соединения. Пиридин Химические свойства 1. Реакции электрофильного замещения в основном происходят в положения 3 и 5. 1. 1. Галогенирование при комнатной температуре 1. 2. Сульфирование 1. 3. Нитрование Алкилирование и ацилирование по Фриделю-Крафтсу не происходят
Гетероциклические соединения. Пиридин Химические свойства 1. Реакции электрофильного замещения в основном происходят в положения 3 и 5. 1. 1. Галогенирование при комнатной температуре 1. 2. Сульфирование 1. 3. Нитрование Алкилирование и ацилирование по Фриделю-Крафтсу не происходят
 Гетероциклические соединения. Пиридин 2. Реакции нуклеофильного замещения в основном происходят в положения 2 и 4. 2. 1. Аминирование 2. 2. Гидроксилирование 2. 3. Алкилирование бутиллитием
Гетероциклические соединения. Пиридин 2. Реакции нуклеофильного замещения в основном происходят в положения 2 и 4. 2. 1. Аминирование 2. 2. Гидроксилирование 2. 3. Алкилирование бутиллитием
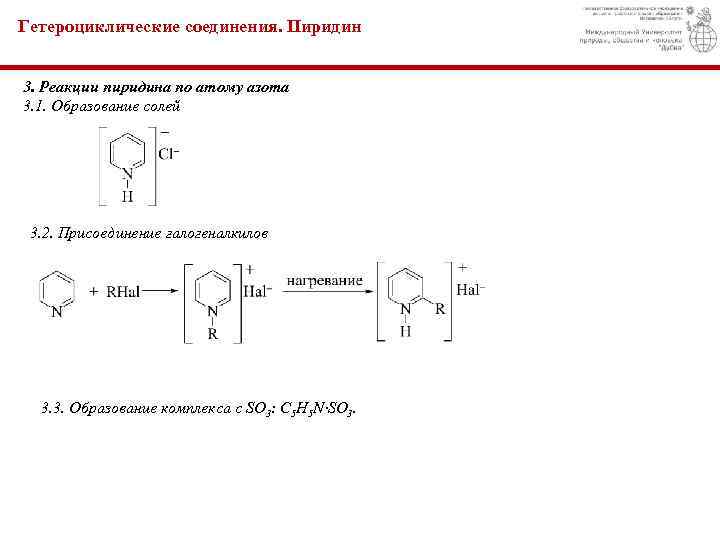 Гетероциклические соединения. Пиридин 3. Реакции пиридина по атому азота 3. 1. Образование солей 3. 2. Присоединение галогеналкилов 3. 3. Образование комплекса с SO 3: C 5 H 5 N·SO 3.
Гетероциклические соединения. Пиридин 3. Реакции пиридина по атому азота 3. 1. Образование солей 3. 2. Присоединение галогеналкилов 3. 3. Образование комплекса с SO 3: C 5 H 5 N·SO 3.
 Гетероциклические соединения. Пиридин 4. Реакции раскрытия пиридинового кольца 4. 1. Взаимодействие с иодоводородом 4. 2. Присоединение водорода
Гетероциклические соединения. Пиридин 4. Реакции раскрытия пиридинового кольца 4. 1. Взаимодействие с иодоводородом 4. 2. Присоединение водорода
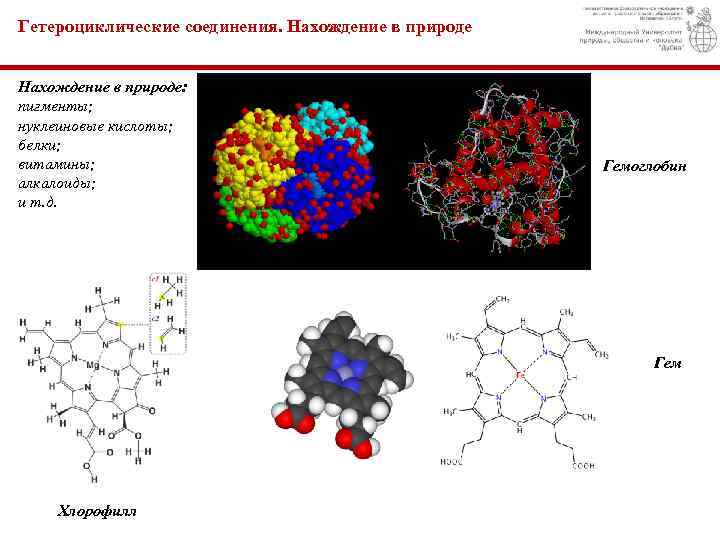 Гетероциклические соединения. Нахождение в природе: пигменты; нуклеиновые кислоты; белки; витамины; алкалоиды; и т. д. Гемоглобин Гем Хлорофилл
Гетероциклические соединения. Нахождение в природе: пигменты; нуклеиновые кислоты; белки; витамины; алкалоиды; и т. д. Гемоглобин Гем Хлорофилл
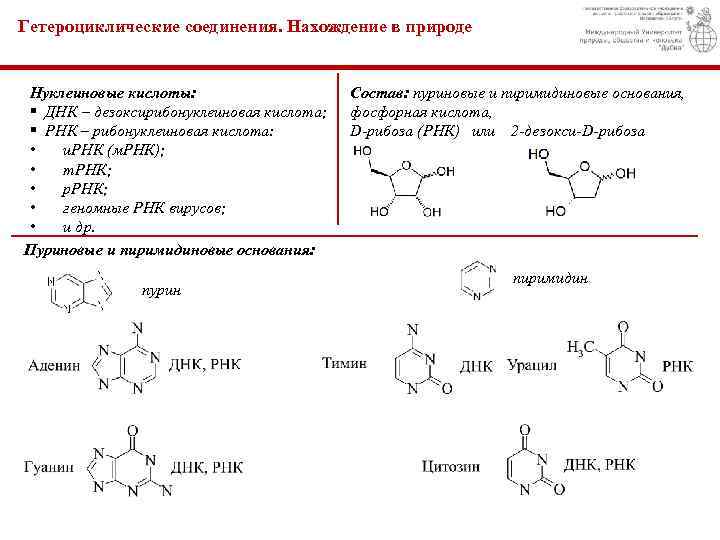 Гетероциклические соединения. Нахождение в природе Нуклеиновые кислоты: § ДНК – дезоксирибонуклеиновая кислота; § РНК – рибонуклеиновая кислота: • и. РНК (м. РНК); • т. РНК; • р. РНК; • геномные РНК вирусов; • и др. Пуриновые и пиримидиновые основания: пурин Состав: пуриновые и пиримидиновые основания, фосфорная кислота, D-рибоза (РНК) или 2 -дезокси-D-рибоза пиримидин
Гетероциклические соединения. Нахождение в природе Нуклеиновые кислоты: § ДНК – дезоксирибонуклеиновая кислота; § РНК – рибонуклеиновая кислота: • и. РНК (м. РНК); • т. РНК; • р. РНК; • геномные РНК вирусов; • и др. Пуриновые и пиримидиновые основания: пурин Состав: пуриновые и пиримидиновые основания, фосфорная кислота, D-рибоза (РНК) или 2 -дезокси-D-рибоза пиримидин
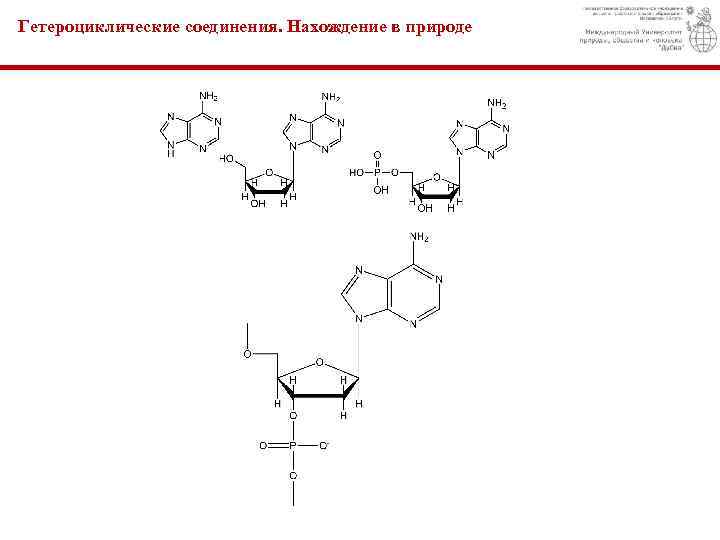 Гетероциклические соединения. Нахождение в природе
Гетероциклические соединения. Нахождение в природе
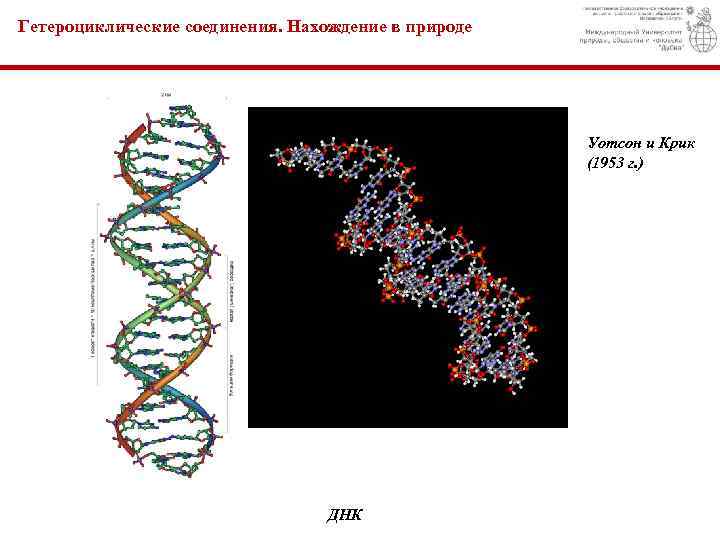 Гетероциклические соединения. Нахождение в природе Уотсон и Крик (1953 г. ) ДНК
Гетероциклические соединения. Нахождение в природе Уотсон и Крик (1953 г. ) ДНК
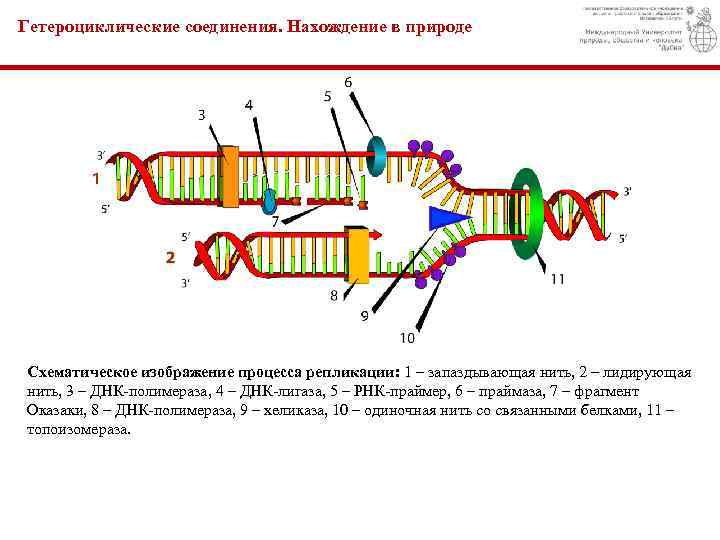 Гетероциклические соединения. Нахождение в природе Схематическое изображение процесса репликации: 1 – запаздывающая нить, 2 – лидирующая нить, 3 – ДНК-полимераза, 4 – ДНК-лигаза, 5 – РНК-праймер, 6 – праймаза, 7 – фрагмент Оказаки, 8 – ДНК-полимераза, 9 – хеликаза, 10 – одиночная нить со связанными белками, 11 – топоизомераза.
Гетероциклические соединения. Нахождение в природе Схематическое изображение процесса репликации: 1 – запаздывающая нить, 2 – лидирующая нить, 3 – ДНК-полимераза, 4 – ДНК-лигаза, 5 – РНК-праймер, 6 – праймаза, 7 – фрагмент Оказаки, 8 – ДНК-полимераза, 9 – хеликаза, 10 – одиночная нить со связанными белками, 11 – топоизомераза.
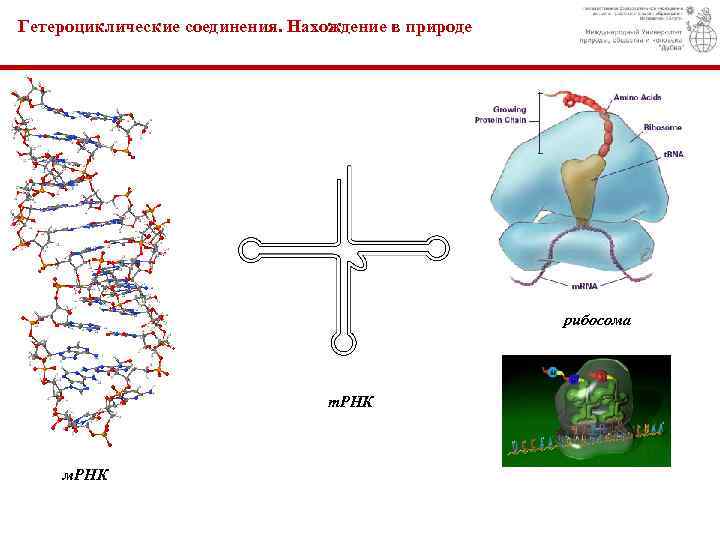 Гетероциклические соединения. Нахождение в природе рибосома т. РНК м. РНК
Гетероциклические соединения. Нахождение в природе рибосома т. РНК м. РНК
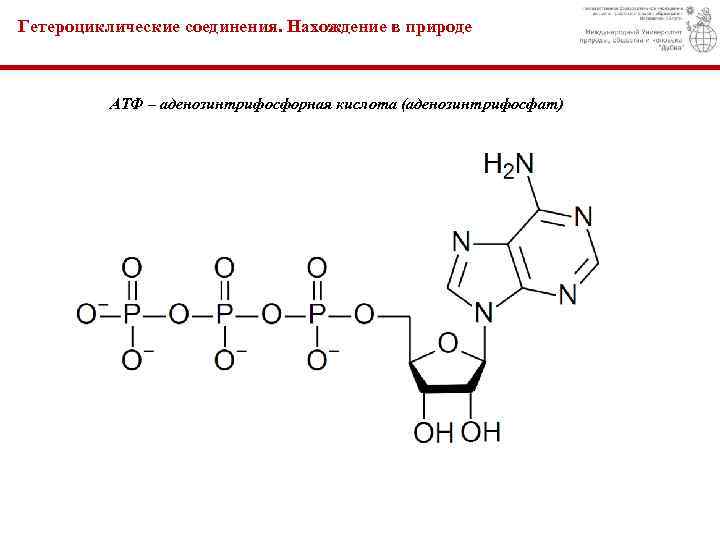 Гетероциклические соединения. Нахождение в природе АТФ – аденозинтрифосфорная кислота (аденозинтрифосфат)
Гетероциклические соединения. Нахождение в природе АТФ – аденозинтрифосфорная кислота (аденозинтрифосфат)


