herpes_adeno_virusi.ppt
- Количество слайдов: 62

Герпесвіруси і аденовіруси людини. Біологічні властивості. Лабораторна діагностика захворювань ВНМУ ім. М. І. Пирогова Кафедра мікробіології

Класифікація герпесвірусів людини Родина Herpesviridae (3 підродини і 9 родів) Alphaherpesvirinae – віруси характеризуються коротким репродуктивним циклом, тропністю до клітин базального шару епітелію і слизових оболонок; здатністю до персистенції в нервових гангліях Роди: Simplexvirus – збудники простого герпесу (1 і 2 типів); Varicellovirus – збудник вітряної віспи/оперізуючого лишаю (Varicella/zoster virus)-вірус герпесу людини 3 типу

Класифікація герпесвірусів людини Betaherpesvirinae: віруси характеризуються тривалим репродуктивним циклом, тропністю до клітин залозистої і лімфоїдної тканин, персистенцією в паренхіматозних органах людини Роди: Cytomegalovirus – вірус герпесу людини 5 типу (ЦМВ); Roseolovirus - віруси герпесу людини 6 і 7 типів

Класифікація герпесвірусів людини Gammaherpesvirinae: віруси характеризуються тропністю до Т- і Влімфоцитів людини, здатні викликати персистуючий і літичний типи інфекції. Роди: Lymphocryptovirus: Вірус Епштейна – Бара (ВЕБ, вірус герпесу людини 4 типу) – збудник інфекційного мононуклеозу/лімфоми Беркіта; Rhadinovirus: Вірус герпесу людини 8 типу, асоційований з саркомою Капоші

Морфологія вірусів простого герпесу Будова віріону складний, сферичної форми 110 -120 нм, ікосаедральний тип симетрії Суперкапсид – глікопротеїни (А-І) Між капсидом і суперкапсидом – додаткова білкова оболонка – тегумент Капсид – містить геном, представлений двохнитковою ДНК, а також вірусну ДНКполімеразу, структурні білки
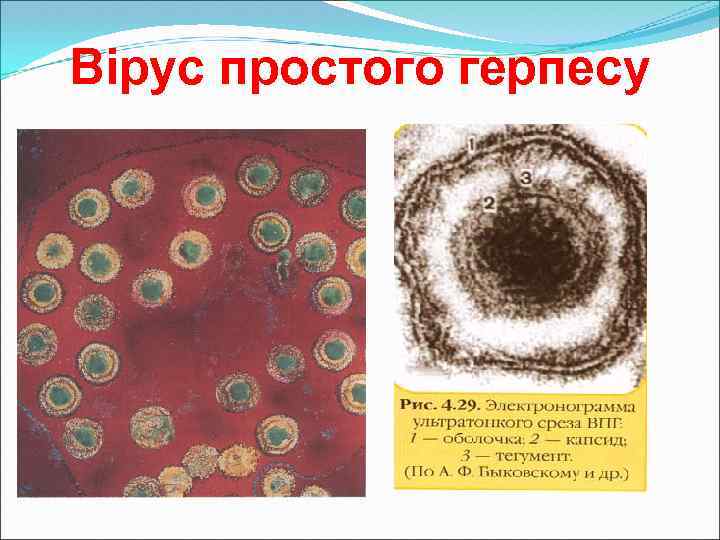
Вірус простого герпесу

Антигенна структура вірусів простого герпесу Розрізняють 2 серотипи ВПГ людини (ВПГ-1 і ВПГ-2) Типоспецифічні Аг: глікопротеїни суперкапсиду Групоспецифічні Аг: білки нуклеокапсиду

Резистентність Чутливі до: високих температур (600 С) УФО жиророзчинників кислого р. Н Стійкі до: низьких температур При кімнатній температурі зберігають життєздатність протягом 10 год

Біологічні властивості Здатність до персистенції і спроможність викликати латентні інфекції; Здатність утворювати внутрішньоядерні включення в інфікованих клітинах; Убіквітарність поширення (по кількості інфікованих на планеті ВПГ посідає 1 -е місце); Можуть приймати в свій геном велику кількість чужорідної ДНК, тому використовуються в якості векторів в генній інженерії; Найменш виражені онкогенні властивості в родині

Культивування Курячі ембріони (клітини ХАО) Через 2 -3 доби утворюють білі бляшки на ХАО Культури клітин (усі типи) ЦПД – утворення багатоядерних клітин і внутрішньоядерних тілець-включень Культивування в організмі лабораторних тварин (модель герпетичного кератокон΄юнктивіту на кролях)

Епідеміологія лабіального і генітального герпесу Джерело інфекції: хворі і вірусоносії (70 -90% населення інфіковано ВПГ-1) Механізм зараження – контактний і трансплацентарний Шляхи зараження – побутовий контакт, статевий контакт, інфікування при проходженні через родові шляхи, через плаценту
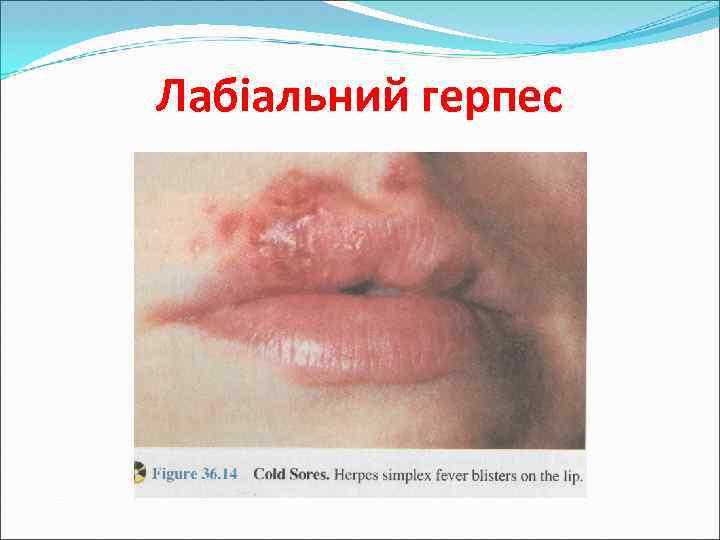
Лабіальний герпес

Патогенез Інфікування клітин слизової оболонки ротової порожнини або статевих органів (первинна реплікація вірусу) Поширення вірусу по чутливим нейронам в ганглії потрійного нерву або спиномозкові ганглії (латентна форма інфекції) При імуносупресивних станах – проникнення вірусу у кров і виникнення генералізованих форм інфекцій Рецидиви характеризуються поширенням вірусу по чутливим нейронам у клітини слизової оболонки (рецидивуючий герпетичний гінгівостоматит)

Імунітет Нестерильний Забезпечує повний імунітет до гомологічного типу і частковий до гетерологічного типу вірусу Носить клітинний і гуморальний характер

Лабораторна діагностика Експрес – діагностика Матеріал для дослідження: вміст везикул, зіскоби з слизової оболонки, ліквор, кров Методи: 1. РІФ 2. Цитоскопічний – в мазках, забарвленних за Романовським. Гімзою виявляють багатоядерні клітини з внутрішньоядерними включеннями (тільця Ліпшютца)

Лабораторна діагностика Вірусологічний метод Матеріал для дослідження: вміст везикул Вірус культивують у КЕ на ХАО або на КК Індикація: утворення бляшок на ХАО або ЦПД у КК Ідентифікація: РН з врахуванням по бляшкоутворенню або відсутності ЦПД

Лабораторна діагностика Біологічний метод Кон’юнктивальне зараження мишей або кролів і відтворення герпетичного кератокон’юнктивіту Серологічний метод: ІФА Матеріал для дослідження: сироватка крові Виявлення Ig M (первинна інфекція) або Ig. G (рецидив латентної інфекції) за допомогою ІФА

Профілактика Неспецифічна: розрив механізмів і шляхів передачі інфекції Специфічна: жива генно-інженерна і субодинична вакцини (США);

Лікування Неспецифічне етіотропне: Інгібітори вірусних ферментів Ацикловір – герпервір, ацигерпін, герпесин, гевіран (місцево); віролекс, зовіракс, медовір (місцево і парентерально); Ганцикловір; Валацикловір – вальтрекс Аденінарабінозид – відарабін Фосковір. Інтерферони і інтерфероногени При частих рецидивах – застосування інактивованої герпетичної вакцини

Вірус вітряної віспи / оперізуючого лишаю Особливості морфології: розміри 150 -200 нм Особливості культивування: 1. Культивують у КК нирок, легенів і фібробластів ембріону людини 2. Непатогенний для лабораторних тварин 3. Не культивується у курячому ембріоні

Епідеміологія вітряної віспи і оперізуючого лишаю Вітряна віспа виникає при первинному інфікуванні вірусом в дитячому віці Оперізуючий лишай виникає внаслідок ендогенного інфікування із спинномозкових чутливих нервових ганглієв Джерело інфекції хворий на вітряну віспу(рідше хворий на оперізуючий лишай) Механізм передачі: аерогенний (рідше контактний) Шлях передачі: повітряно-краплинний

Патогенез Інкубаційний період при вітряній віспі – 10 -20 діб Вхідні ворота – клітини слизової оболонки ВДШ і реґіонарні лімфатичні вузли Стадії патогенезу: 1. Первинна реплікація вірусу у вхідних воротах 2. Вірусемія 3. Ураження клітин шипуватого шару епідермісу (літична інфекція) з утворенням характерних везикул 4. В деяких випадках - проникнення вірусу у спиномозкові ганглії (персистуюча інфекція)

Патогенез оперізуючого лишаю При травмах, стресах, імуносупресії вірус активується у гангліях і по чутливим нейронам проникає у шкіру Ураження епідермісу по ходу міжреберних проміжків (оперізуючий лишай)
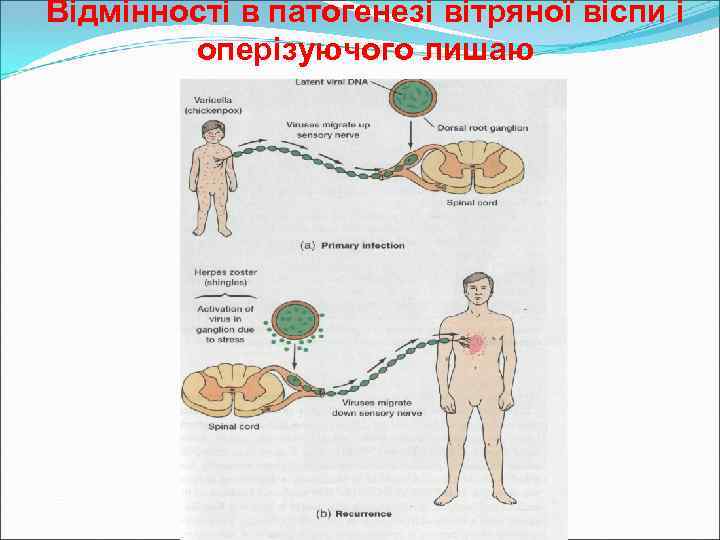
Відмінності в патогенезі вітряної віспи і оперізуючого лишаю
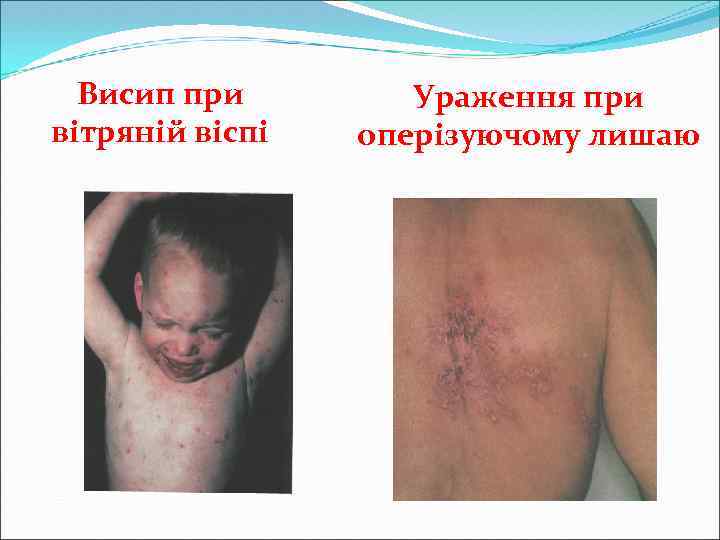
Висип при вітряній віспі Ураження при оперізуючому лишаю

Імунітет При циклічному перебігу інфекції – стійкий, стерильний, напружений, довічний При ациклічному перебігу – імунні реакції не забезпечують звільнення організму від збудника

Лабораторна діагностика Експрес – діагностика Матеріал для дослідження: вміст везикул Методи: 1. РІФ 2. Цитоскопічний – в мазках, забарвленних за Романовським-Гімзою виявляють клітини з внутрішньоядерними включеннями (тільця Арагао)

Лабораторна діагностика Вірусологічний метод Матеріал для дослідження: вміст везикул Вірус культивують на КК Індикація: ЦПД у КК Ідентифікація: РЗК або РН з врахуванням відсутності ЦПД

Лабораторна діагностика Серологічний метод Матеріал для дослідження: парні сироватки крові РЗК, ІФА, РН

Лікування і профілактика Профілактика Екстренна (особливим категоріям, що були в контакті з хворим) – людський імуноглобулін Жива атенуйована вакцина (штам ОКА) Лікування Неспецифічне етіотропне – ацикловір, ганцикловір, фосковір Інтерферони, інтерфероногени Людський гамма-глобулін

Цитомегаловірус (ЦМВ) або вірус герпесу людини 5 типу (ВГЛ-5) Особливості морфології і будови рецепторного апарату: діаметр віріону 230 нм, видоспецифічний рецептор утворений глікопротеїном В і зумовлює тропізм вірусів до лімфоцитів і клітин-попередників червоного мозку

Цитомегаловірус (ЦМВ) Особливості культивування: Не культивується в КЕ; Спроможний репродукуватись в КК фібробластів шкіри і легень ембріона людини, диплоїдних КК ЦПД в інфікованих клітинах з’являється через декілька тижнів і характеризується утворенням гігантських клітин з внутрішньоядерними включеннями ( в вигляді “совиного ока”) Особливості епідеміології: Механізм зараження: перкутанний, статевий, аерогенний, трансплацентарний, аліментарний Інфікованність ЦМВ відбувається в дитячому віці, але перебіг інфекції субклінічний (латентна інфекція)
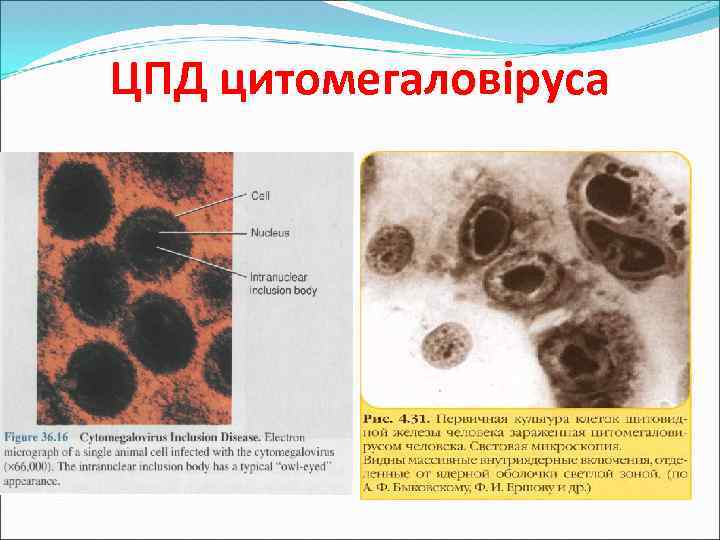
ЦПД цитомегаловіруса

Патогенез ЦМВ інфекції Первинна репродукція вірусу– в клітинах слинних залоз, епітеліоцитах слизових оболонок, шкіри При інфікуванні лімфоцитів вірус заноситься у внутрішні органи, в клітинах яких він персистує (латентна інфекція) Клінічні прояви ЦМВ-інфекція набуває при інфікуванні вірусом людей з імунодефіцитами або при трансплацентарному інфікуванні Вроджена ЦМВ-інфекція має прояви гепатиту, пневмонії, мікроцефалії, атрофії зорового нерва, хоріоретиніту У імунодефіцитних осіб ЦМВ викликає ретиніт, пневмонію, гастроентерит або ЦМВ- мононуклеозоподібне захворювання

Лабораторна діагностика Матеріал для дослідження: слина, зіскоби зі слизових оболонок, сеча та ін. Мікроскопічні методи: ЕМ, виявлення внутрішньоядерних включень в уражених клітинах Експрес діагностика: РІФ Вірусологічний метод: культивування вірусу в пермісивних КК, індикація за ЦПД, ідентифікація за РН, РЗК Серологічний метод: виявлення в сироватці хворих Ig. G і Ig. M за допомогою ІФА; виявлення специфічних антитіл до ЦМВ за допомогою РЗК, РПГА, РН

Вірус Епштейна-Бара (ВЕБ) Особливості морфології: діаметр 120 нм Особливості антигенної структури: має 2 типи (А і В) Біологічні особливості: має тропізм до В-лімфоцитів і епітеліальних клітин носоглотки, містить онкогени Культивування: в КК В-лімфоцитів людини, при репродукції – бласттрансформація уражених клітин
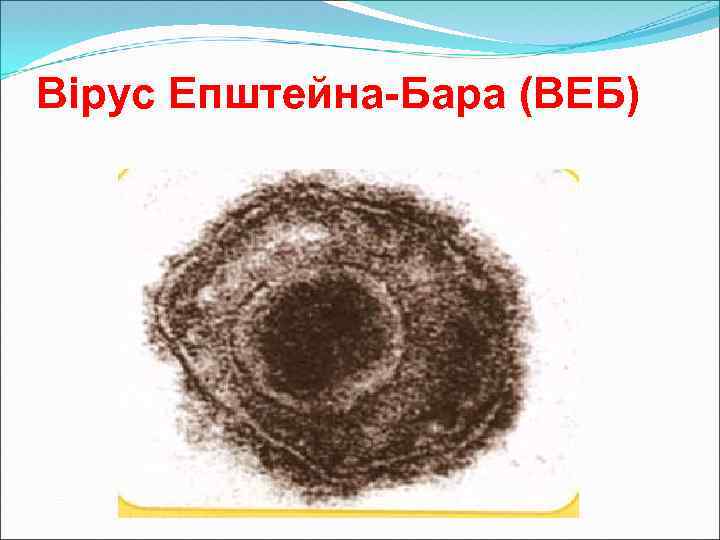
Вірус Епштейна-Бара (ВЕБ)

Епідеміологія і патогенез ВЕБінфекції Джерело інфекції – хворий або вірусоносій Механізм передачі: аерогенний і перкутанний Викликає інфекційний мононуклеоз (доброякісний перебіг) або провокує пухлинні захворювання (волохатоклітинну лейкоплакію, назофарінгеальну карциному, лімфому Беркіта, карциному слинних залоз, хворобу Ходжкіна)

Лабораторна діагностика Характерна клінічна картина (ангіна, збільшення шийних лімфоузлів) і різке збільшення кількості мононуклеарів в перифірійній крові (до 10 -15% ) дозволяють поставити попередній діагноз Для лабораторного підтвердження використовують РІФ, вірусологічний і серологічний (ІФА) методи, ПЛР

Класифікація аденовірусів людини Родина Adenoviridae Рід Mastadenovirus 6 підродів: A, B (B 1, B 2 ), C, D, E, F 47 серотипів

Властивості серотипів аденовірусів людини Підрід Серотип Захворювання A 12, 18, 31 Кишкові інфекції крипт B 1 3, 7, 16, 21 Респіраторні захворювання B 2 11, 14, 34, Персистуючі інфекції нирок 35 C 1, 2, 5, 6 Респіраторні захворювання з персистенцією в лімфоїдній тканині
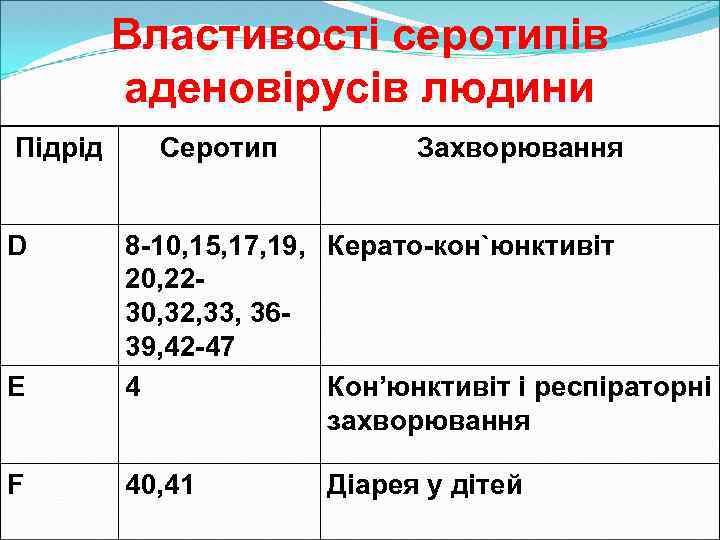
Властивості серотипів аденовірусів людини Підрід D E F Серотип Захворювання 8 -10, 15, 17, 19, Керато-кон`юнктивіт 20, 2230, 32, 33, 3639, 42 -47 4 Кон’юнктивіт і респіраторні захворювання 40, 41 Діарея у дітей

Морфологія Будова віріону: простий, ікосаедральної форми 65 -90 нм Двохнитковий ДНК-геном ДНК-полімераза регуляторні білки пухлинні білки
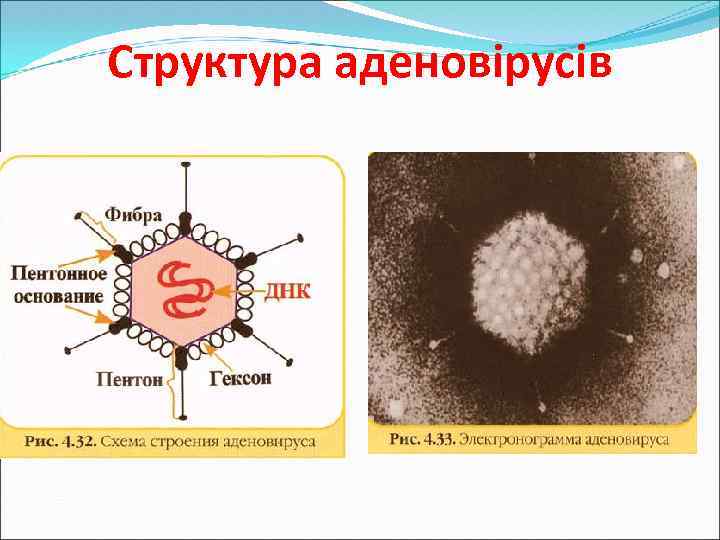
Структура аденовірусів

Антигенна структура Розрізняють 7 антигенів: A-антиген (гексон) – загальний групоспецифічний B-антиген (основа пентону) – ділить на 3 підгрупи C-антиген (спікули) – типоспецифічний, ділить на 47 серотипів, які складають 6 підродів (A, B, C, D, E, F)

Резистентність Чутливий до: трипсину багаторазового заморожування та відтаювання високих температур дезінфектантів

Резистентність Стійкий до: р. Н 5, 0 -9, 0 нагрівання ліофілізації заморожування детергентів жиророзчинників

Культивування В культурах клітин усіх типів ЦПД: - лізис клітин - округлення клітин - внутрішньоядерні включення - відшаровування клітин - пухлинна трансформація

Епідеміологія Джерело інфекції: - хвора людина - вірусоносій Механізми зараження: - аерогенний - фекально-оральний - перкутанний

Епідеміологія Шляхи зараження: - повітряно-краплинний - водний - харчовий - контактно-побутовий - статевий

Епідеміологія Захворювання мають осінньо-зимову сезонність Переважно хворіють діти

Патогенез Реплікація вірусів в ядрах епітеліальних клітин вхідних воріт: - ВДШ - кон’юнктива - тонкий кишечник - сечо-статеві органи - регіонарні лімфовузли

Патогенез Уражені клітини десквамують, виникає ексудативний і запальнопроліферативний процес в слизових оболонках, лімфоїдній тканині, склері і кон’юнктиві Пентони пригнічують активність мононуклеарів, виникає вірусемія, генералізація процесу

Патогенез На відміну від інших ГРВІ, виникає широке первинне ураження органів, розмаїття клінічних проявів Вірус проявляє онкогенні властивості

Патогенез 12 S-протеїн пригнічує ген апоптозу та ген-інгібітор росту і проліферації Білки E 1 A гена віруса пригнічують: - презентацію антигена системи HLA, що веде до невпізнавання клітин Ткіллерами - продукцію матриксних протеаз, які інгібують метастазування клітин

Імунітет Типоспецифічний, тривалий У дорослих виявляють антитіла до багатьох серотипів У дітей виділяють антитіла лише до деяких з них

Імунітет Забезпечується: - інтерфероном - противірусними інгібіторами та кофакторами - антигензалежними Т-кіллерами - віруснейтралізуючими антитілами (Ig A, G)

Лабораторна діагностика Матеріал для дослідження: - мазки та змиви з ротоглотки - харкотиння - зіскоби з конюнктиви - ліквор - випорожнення - сироватка крові - секційний матеріал

Лабораторна діагностика Експрес-метод: РІФ, ІФА, ІЕМ Вірусологічний метод: - вірус культивують в культурі клітин - індикацію проводять за ЦПД - ідентифікацію проводять в РН та РГГА з еритроцитами щурів або макак -резус, залежно від серотипу

Лабораторна діагностика Серологічний метод: Досліджують парні сироватки з інтервалом 18 -20 днів - РЗК, РНГА - РН, РГГА - ІФА, РІА При гострому перебігу виявляють Ig M, в анамнезі – Ig G

Лікування інтерферон індуктори інтерферону розчин дезоксирибонуклеази мазі з теброфеном мазі з оксоліном

Профілактика Неспецифічна: - розрив механізмів передачі інфекції Специфічна: - пероральна жива атенуйована вакцина серотипів 3, 4, 7, 21 Вакцина має обмежене використання через онкогенні властивості
herpes_adeno_virusi.ppt