05_Геохимия_изотопов_ 2.ppt
- Количество слайдов: 68

Геохимия изотопов geology. spbu. ru/oldsite «лекции on-line» http: //ansatte. uit. no/kku 000/webgeology/

Зачем нужна изотопная геохимия?

М. : Мир, 1989 Н. А. Титаева Ядерная геохимия М. : Изд-во МГУ, 2000

М. : Мир, 1983

2004 2005 (фр. ) 2008

W. White Isotope geochemistry 2012 (в планах издательства) 2005
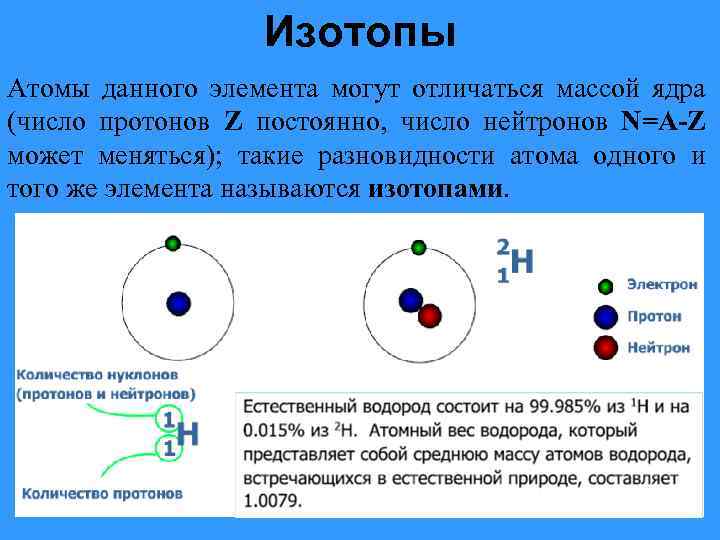
Изотопы Атомы данного элемента могут отличаться массой ядра (число протонов Z постоянно, число нейтронов N=А-Z может меняться); такие разновидности атома одного и того же элемента называются изотопами.

Изотопы – атомы одного элемента, имеющие в ядрах одинаковое число протонов, но различное число нейтронов. Изотопы занимают одну и ту же клетку в Периодической таблице. Следовательно, атомная масса элемента, имеющего несколько изотопов, не является целочисленной. Атомы имеют одинаковое строение электронных оболочек и одинаковое число электронов. Поэтому химические и ряд физических свойств у различных изотопов практически тождественны, т. е. в химических реакциях они ведут себя одинаково.
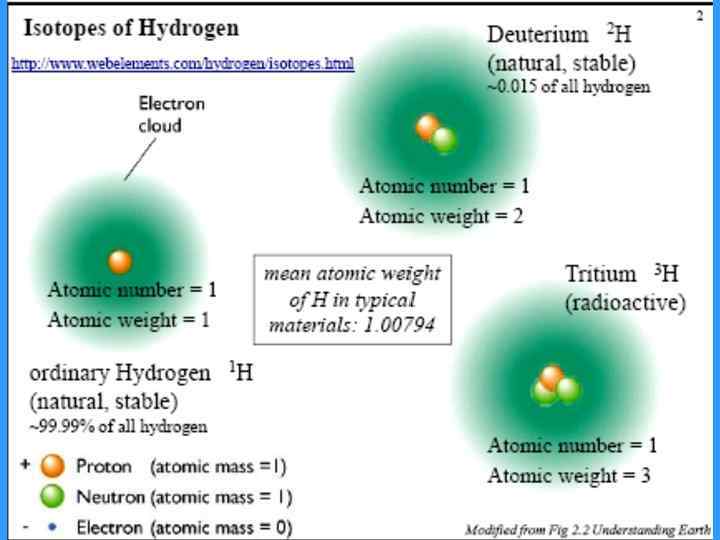
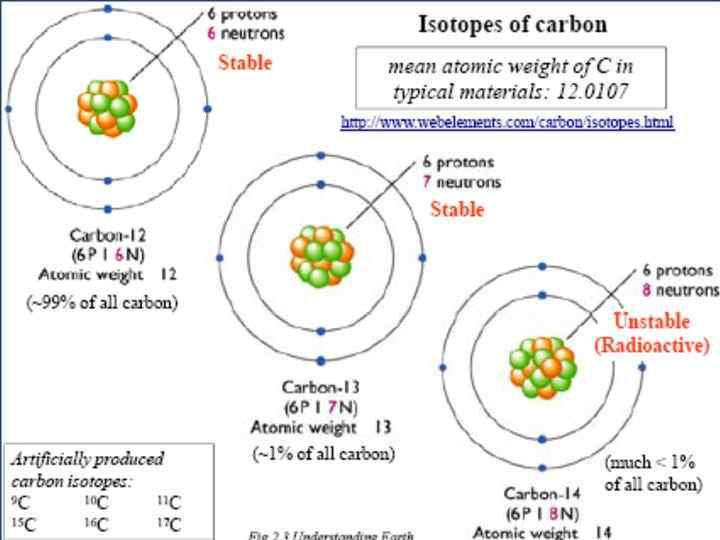

Изобары – атомы различных элементов, ядра которых содержат одинаковое число нуклонов (протонов и нейтронов в сумме), и, следовательно, имеющие одинаковые массовые числа. 19 K 40 (Z=19, N=21) и 20 Са 40 (Z=20, N=20). Изотоны – атомы различных элементов, имеющие одинаковое число нейтронов, но разные массы A и числа протонов Z. Изомеры – атомы одного элемента, имеющие одинаковое число как протонов, так и нейтронов, но различную энергию ядер (и период полураспада). Обозначаются: m-метастабильное ядро.
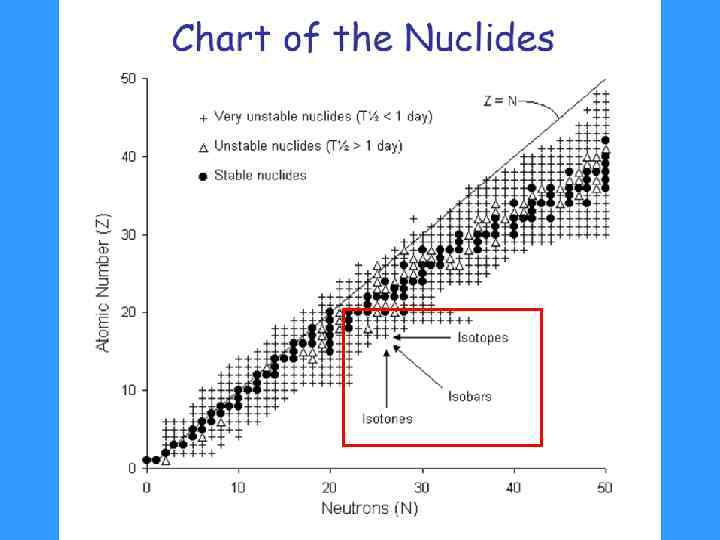
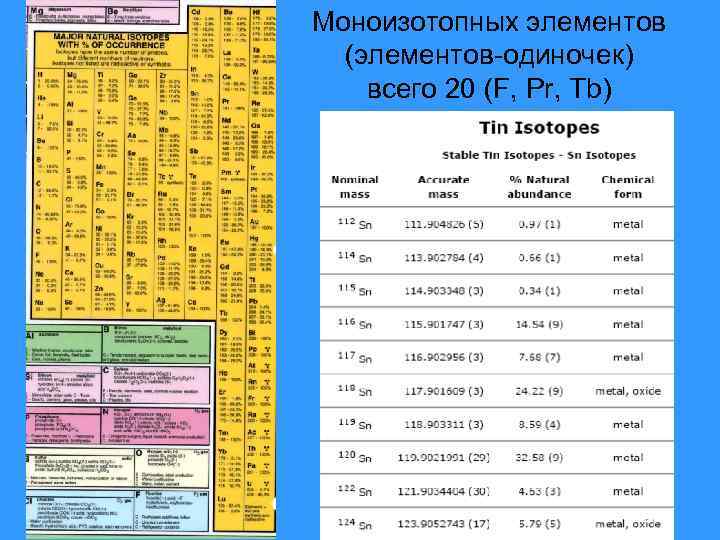
Моноизотопных элементов (элементов-одиночек) всего 20 (F, Pr, Tb)

Все известные изотопы могут быть распределены на четыре типа по зависимости от четного или нечетного числа протонов и нейтронов в их составе: четно-четный 8 O 16, четно-нечетный 9 7 10 4 Be , нечетно-четный 3 Li , нечетно-нечетный 5 B. Количественные соотношения ядер различного вида представлены в таблице: Тип Z - число N – число А – полное число протонов в ядре нейтронов в ядре нуклонов (массовое число) Четно-четный Четное Четно-нечетный Четное Нечетное Нечетно-четный Нечетное Четное Нечетно - нечетный Нечетное Четное Изотопы с четным Z и четным N резко преобладают над изотопами с нечетными соотношениями.
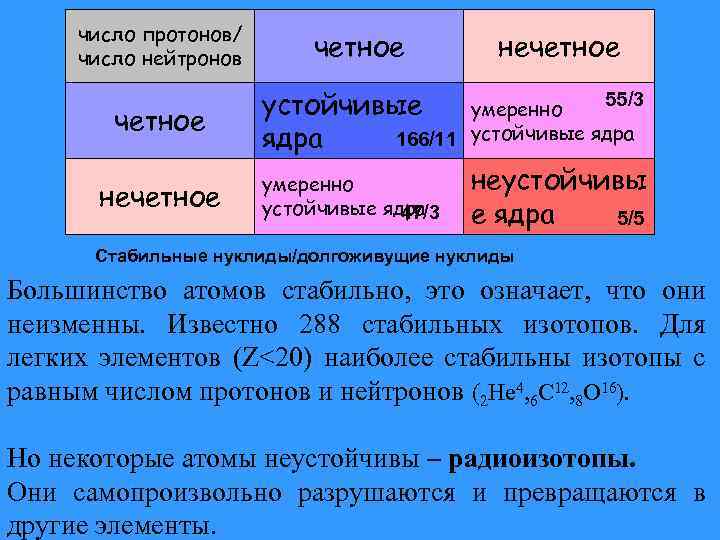
число протонов/ число нейтронов четное нечетное устойчивые 166/11 ядра 55/3 умеренно устойчивые ядра 47/3 неустойчивы е ядра 5/5 нечетное Стабильные нуклиды/долгоживущие нуклиды Большинство атомов стабильно, это означает, что они неизменны. Известно 288 стабильных изотопов. Для легких элементов (Z<20) наиболее стабильны изотопы с равным числом протонов и нейтронов (2 He 4, 6 C 12, 8 O 16). Но некоторые атомы неустойчивы – радиоизотопы. Они самопроизвольно разрушаются и превращаются в другие элементы.

• Резко преобладают в природе изотопы с четным числом и протонов и нейтронов — ЧЕТНО-ЧЕТНЫЕ (166 изотопов). Действительно, из восьми наиболее распространенных элементов литосферы пять сложены преимущественно изотопами этого типа: О, Mg, Si, Ca, Fe. • НЕЧЕТНО-ЧЕТНЫЕ изотопы занимают второе место по распространению (47 изотопов). К ним относятся изотопы трех важнейших элементов литосферы Na, Al, K с соответствующим относительным распространением. • Третье место по распространению занимают ЧЕТНОНЕЧЕТНЫЕ изотопы (55 изотопов), хотя их число несколько превышает число нечетно-четных. • НЕЧЕТНО-НЕЧЕТНЫЕ изотопы в природе чрезвычайно редки. К этому типу относятся только пять изотопов Li, B, N, V, Ta. Изотоп азота, вероятно, занимает ведущее место в космических скоплениях газов после водорода и гелия.

ЗАКОНОМЕРНОСТИ В РАСПРОСТРАНЕННОСТИ ИЗОТОПОВ: • У легких элементов с четным значением Z более распространены самые легкие изотопы, преобладает изотоп с минимальным значением N. • У средних и тяжелых элементов (с Z > 32, тяжелее Ge) характерно повышенное распространение средних и тяжелых стабильных изотопов, самые легкие изотопы встречаются в незначительном количестве, среди тяжелых обычно отсутствует резко доминирующий изотоп, наиболее обильный изотоп составляет 60% и наиболее распространены средние и тяжелые изотопы.

ЗАКОНОМЕРНОСТИ В РАСПРОСТРАНЕННОСТИ ИЗОТОПОВ: • У элементов с нечетным значением Z число стабильных изотопов не превышает 2. Исключением не является и нечетный K, состоящий из трех изотопов. Cредний изотоп 40 К сам радиоактивный. • У двух изотопных нечетных элементов преобладает изотоп с четным N. Изотоп с нечетным N значительно менее распространен. Единственное исключение представляет изотоп азота, имеющий семь нейтронов и относительное распространение 99, 63%.
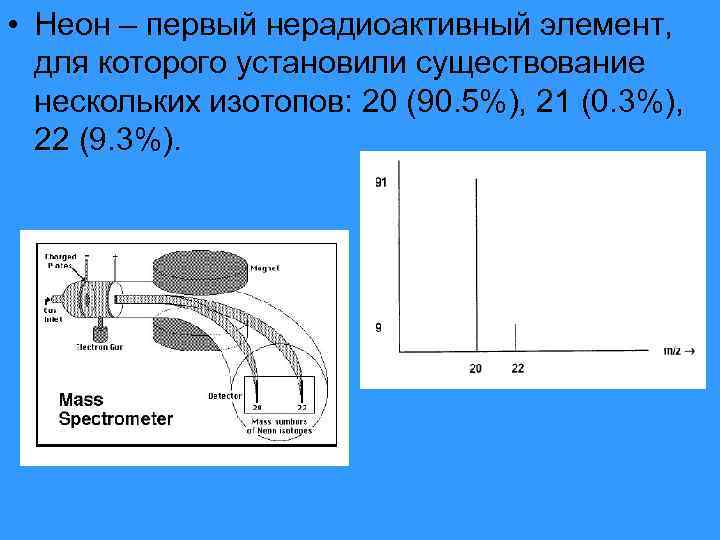
• Неон – первый нерадиоактивный элемент, для которого установили существование нескольких изотопов: 20 (90. 5%), 21 (0. 3%), 22 (9. 3%).

Радиоактивность (Э. Резерфорд 1903 г. , Ф. Содди) Радиоактивность (от лат. radio - излучаю, radius - луч и activus - самопроизвольное (спонтанное) превращение неустойчивого изотопа химического элемента в другой изотоп (обычно изотоп другого элемента). действенный), Все тяжелые изотопы с Z>82 радиоактивны. 209 Bi (Z=83, N=126) – наиболее тяжелый стабильный нуклид. Эффект открыл А. Беккерель в 1896 г. , установивший способность солей урана засвечивать фотопластинки, не подвергавшиеся предварительному освещению. Открытие было сделано после открытия В. К. Рентгеном Х-лучей в 1885 г.

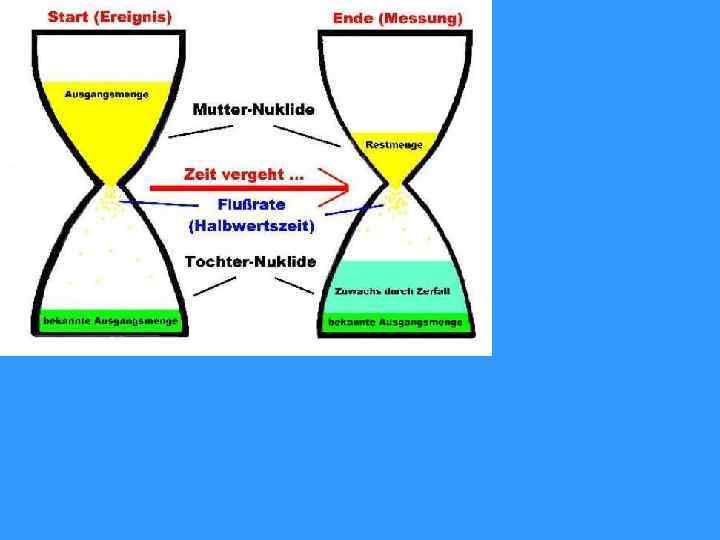
Принципиальная схема радиоактивного распада: радиоактивный (материнский) изотоп М превращается в радиогенный (дочерний) стабильный (иногда радиоактивный) изотоп D. λ – константа распада (не зависит от внешних условий !!! – температуры, давления и пр. ).
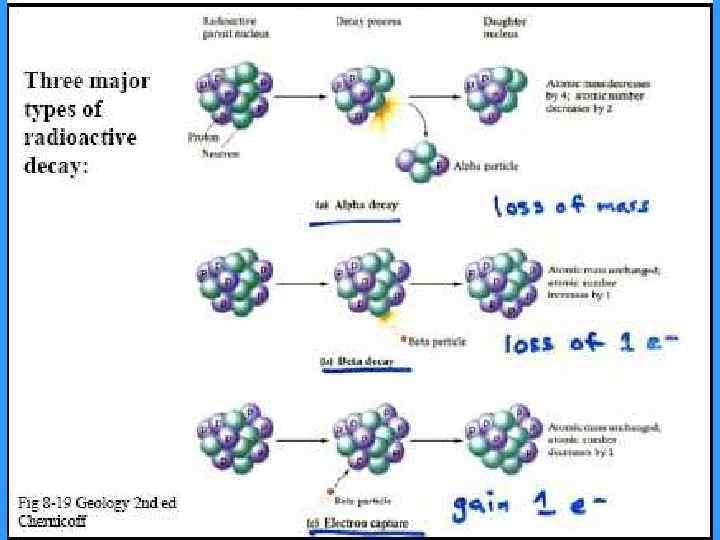

Основные виды самопроизвольных ядерных превращений α-распад Компоненты радиоактивного излучения в магнитном поле. Ядро испускает α-частицу, которая представляет собой ядро атома гелия (4 He) и состоит из двух протонов и двух нейтронов. При α-распаде массовое число изотопа уменьшится на 4, а заряд ядра - на 2. Так, например, радий испускает αчастицу и переходит в радон (22688 Ra→ 22286 Rn + 42 He). Скорость α-частиц ~16 000 км/с.
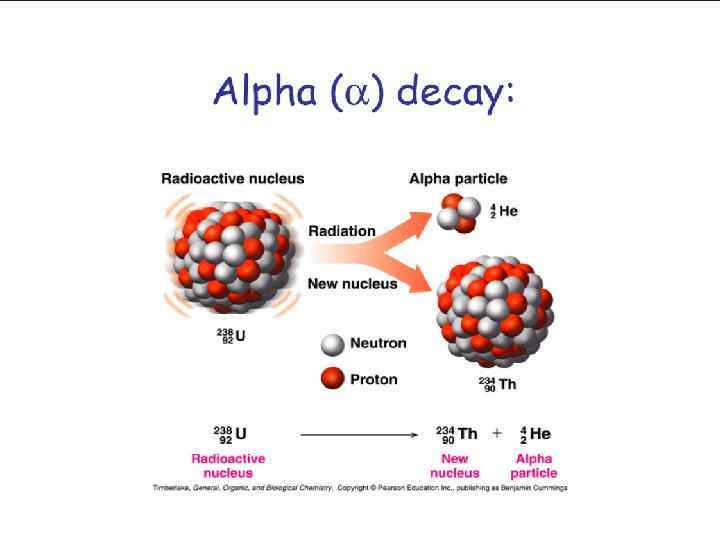

Фотография следов α-частиц, испускаемых при α-распаде. Известно более 200 α-радиоактивных ядер; большая часть их тяжелее свинца (Z > 82). Некоторое количество α-радиоактивных изотопов имеется в области значений Z < 82 среди ядер с недостаточным количеством нейтронов, т. н. нейтронодефицитных ядер.

Три типа β-распада: 1. β- - электронный В неустойчивом ядре нейтрон превращается в протон, при этом ядро испускает «электрон» (β-частицу - негатрон). При β-распаде массовое число изотопа не изменяется, поскольку общее число протонов и нейтронов сохраняется, а заряд ядра увеличивается на 1. β-активность атомных ядер можно рассматривать как распад одного ядерного нейтрона на протон и электрон (+ антинейтрино) MA Z+1 MA + Z При этом положение нового элемента (изотопа) в таблице Менделеева определяется правилом сдвига: образующийся при распаде атом занимает следующую клетку вправо от изначального (масса его практически не меняется, так как масса электрона в ~2000 раз меньше массы нейтрона). V электрона 150 -300 тыс. км/с.


2. Е-захват – электронный захват (K-захват, редко L-захват) Явление электронного захвата противоположно β-распаду: электрон с нижнего К-уровня поглощается ядром, то есть протон в ядре реагирует с электроном, образуя нейтрон (и испускается нейтрино). При этом атомный номер элемента уменьшается на 1, то есть перемещается в таблице Менделеева на одну клетку влево. Среди естественных радиоизотопов существуют такие, которые одновременно испытывают Кзахват и β-распад (40 К). Схема электронного захвата: A A ZM + е Z-1 M
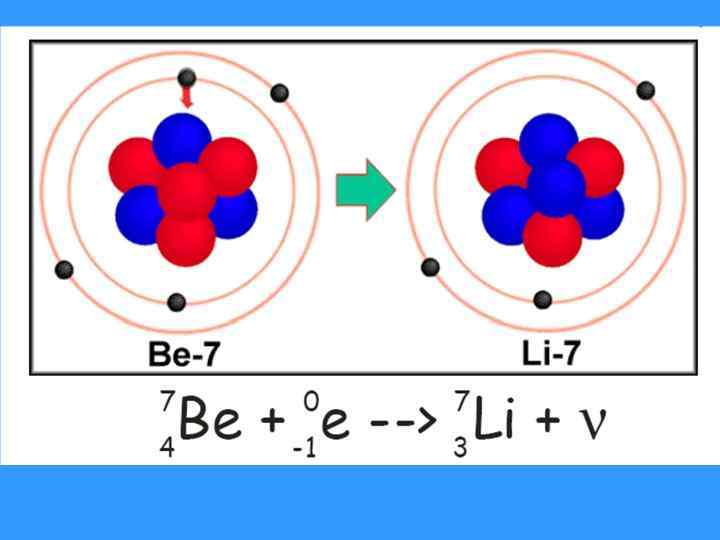
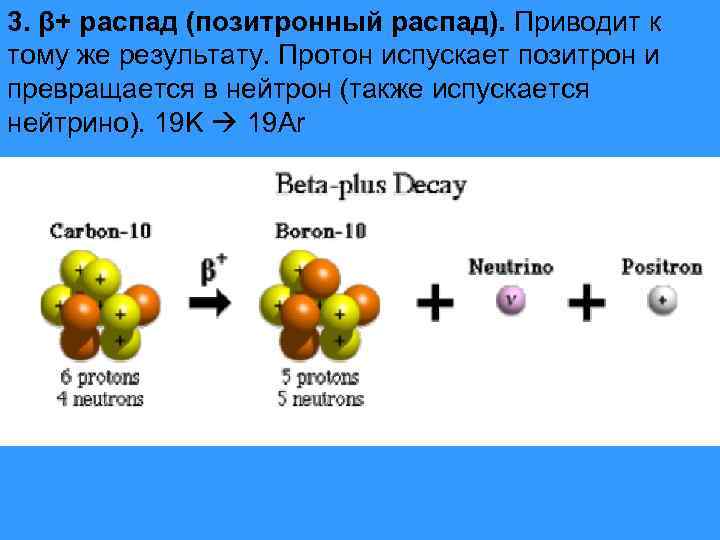
3. β+ распад (позитронный распад). Приводит к тому же результату. Протон испускает позитрон и превращается в нейтрон (также испускается нейтрино). 19 K 19 Ar

Спонтанное деление (кластерная радиоактивность) • Наблюдается только у ядер тяжелых элементов с Z≥ 90. При этом типе радиоактивности образуются два новых ядра с массами с соотношением приблизительно 2: 3. Часто сопровождается испусканием 2 -3 нейтронов. Обозначается как f. • U 238 Ba 144 + Kr 92 + 2 n
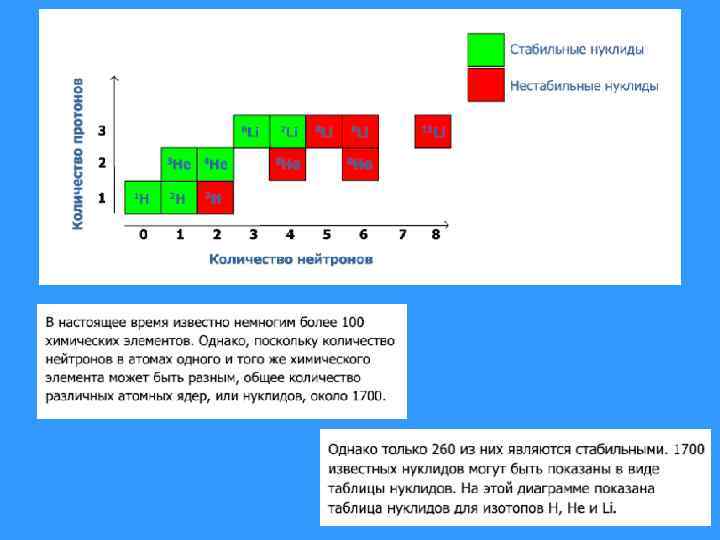
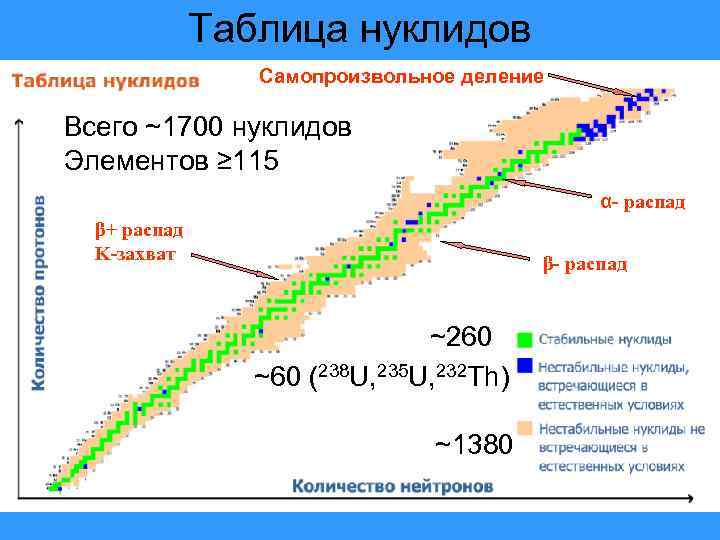
Таблица нуклидов Самопроизвольное деление Всего ~1700 нуклидов Элементов ≥ 115 α- распад β+ распад K-захват β- распад ~260 ~60 (238 U, 235 U, 232 Th) ~1380
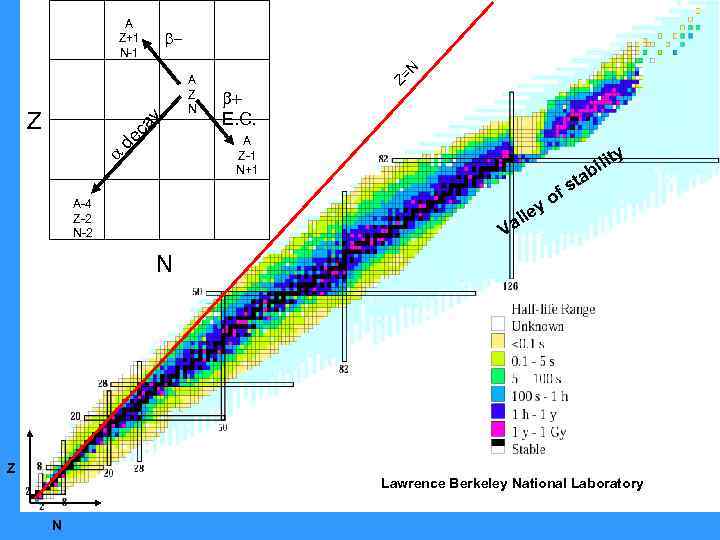
A Z+1 N-1 ca y Z A Z N N + E. C. Z= a de A Z-1 N+1 A-4 Z-2 N-2 y ilit tab s of y e all V N Z Lawrence Berkeley National Laboratory N
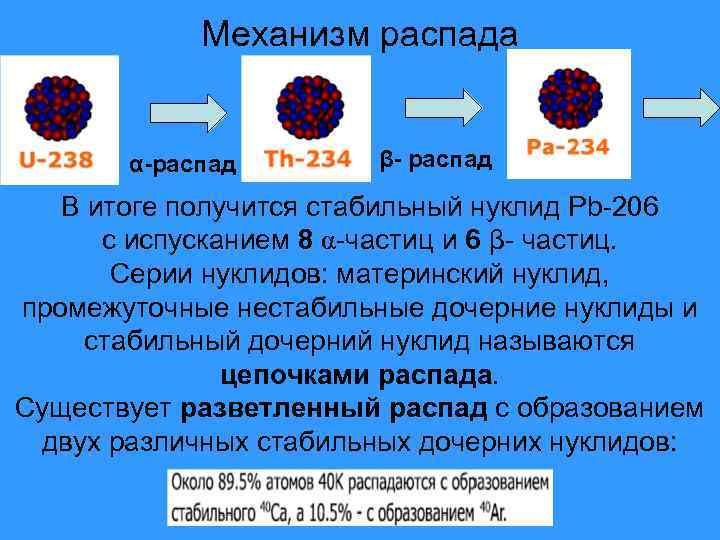
Механизм распада α-распад β- распад В итоге получится стабильный нуклид Pb-206 с испусканием 8 α-частиц и 6 β- частиц. Серии нуклидов: материнский нуклид, промежуточные нестабильные дочерние нуклиды и стабильный дочерний нуклид называются цепочками распада. Существует разветленный распад с образованием двух различных стабильных дочерних нуклидов:

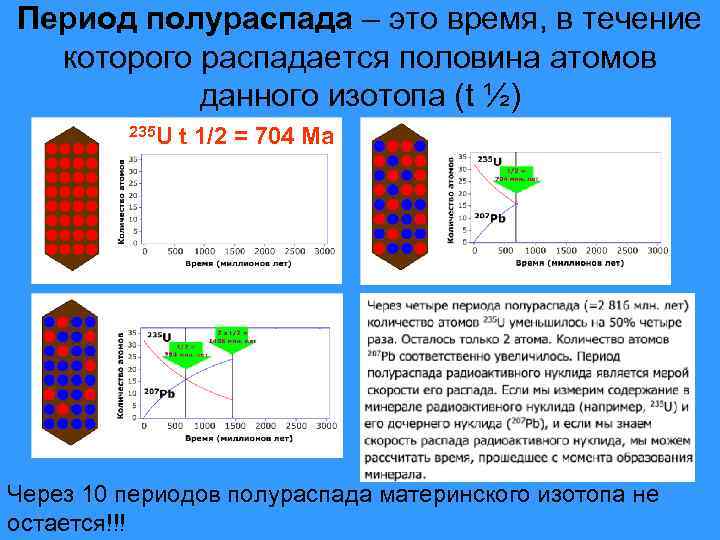
Период полураспада – это время, в течение которого распадается половина атомов данного изотопа (t ½) 235 U t 1/2 = 704 Ma Через 10 периодов полураспада материнского изотопа не остается!!!
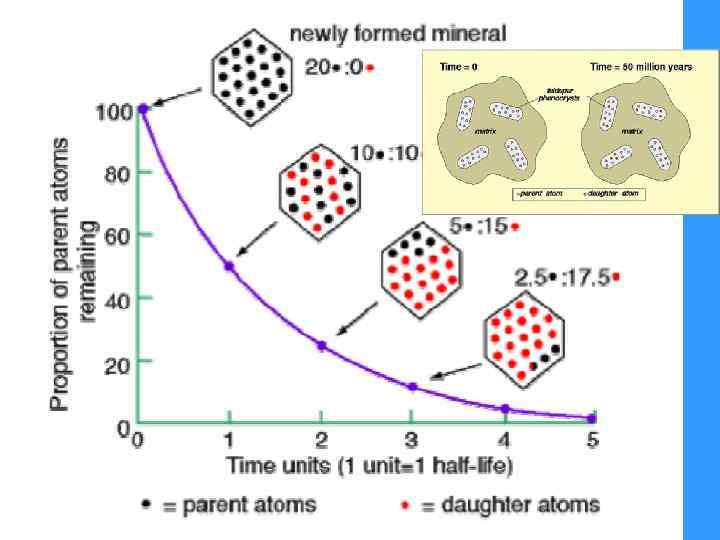

Как вычислить возраст минерала (породы)? N – материнский радиоактивный нуклид D – стабильный дочерний радиогенный нуклид t – время с момента образования минерала λ - константа распада T ½ - период полураспада Вычисленный возраст является истинным, только если минерал (порода) представлял собой все это время закрытую химическую систему, то есть никакого обмена атомами (естественная миграция элементов) материнского и дочернего нуклидов между кристаллом и окружающей средой после его образования не происходило и не содержал атомов дочернего нуклида на время образования.

Масс-спектрометр Triton T 1
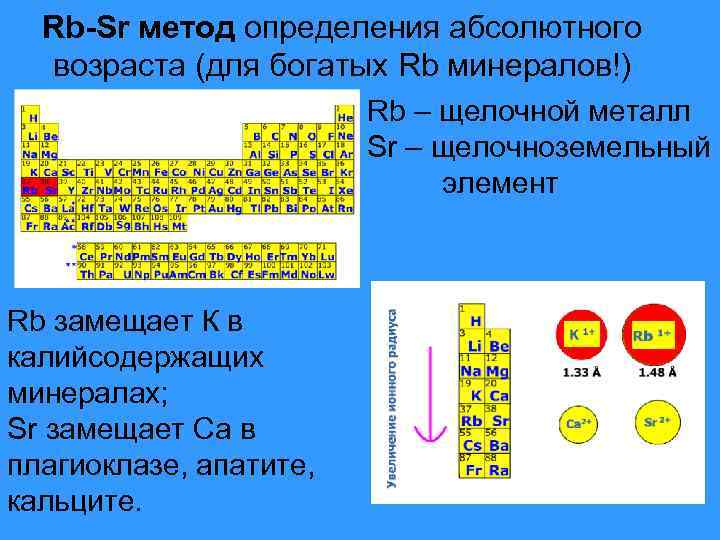
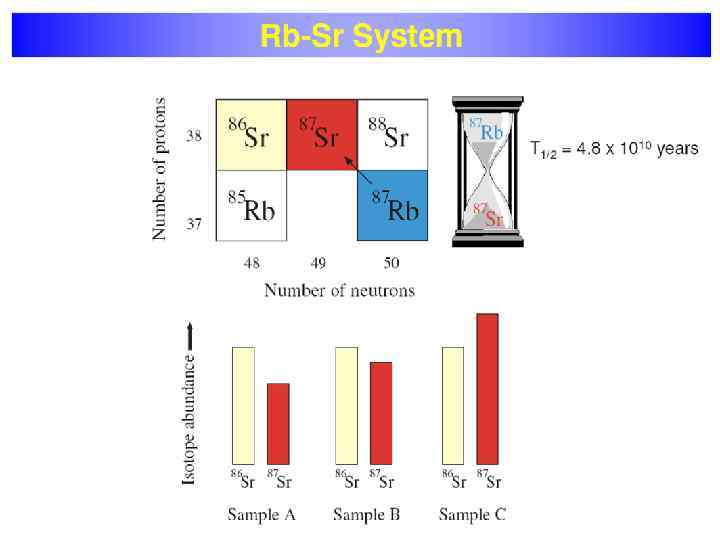
Rb-Sr метод определения абсолютного возраста (для богатых Rb минералов!) Rb – щелочной металл Sr – щелочноземельный элемент Rb замещает К в калийсодержащих минералах; Sr замещает Са в плагиоклазе, апатите, кальците.

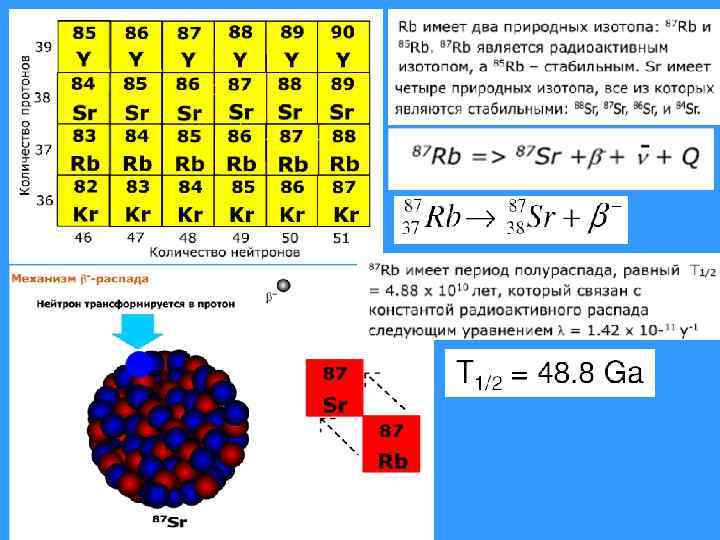
• Rb - щелочной металл. Его ионный радиус (1, 48 А) весьма близок к ионному K калий во всех Kсодержащих минералах. Rb является рассеянным элементом, который не образует своих собственных минералов, но он содержится в легко определимых количествах в обычных Kсодержащих минералах, таких, как слюды (мусковит, биотит, флогопит и лепидолит), Кполевой шпат (ортоклаз и микроклин), некоторые глинистые минералы и минералы эвапоритов, например сильвин и карналлит. • Rb имеет два природных изотопа - 85 Rb и 87 Rb- с распространенностью соответственно 72, 2% и 27, 8%. 87 Rb- радиоактивен и распадается с образованием стабильного 87 Sr путем испускания отрицательной бета-частицы.

• Sr - член группы щелочноземельных элементов. Его ионный радиус (1, 13 А) несколько больше, чем у Ca (0, 99 А), который он может замещать во многих минералах. Таким образом, Sr также является рассеянным элементом и входит в состав Ca-содержащих минералов, таких, как плагиоклаз, апатит и карбонаты кальция, в особенности арагонит. • Sr имеет четыре стабильных изотопа (88 Sr, 87 Sr, 86 Sr и 84 Sr). Их распространенность составляет соответственно около 82. 58, 7. 00, 9. 86 и 0. 56%. Распространенность изотопов стронция варьирует в связи с образованием радиогенного 87 Sr за счет распада природного 87 Rb. • По этой причине точный изотопный состав стронция в породе или минерале, которые содержат рубидий, зависит от возраста и отношения Rb/Sr в этой породе или минерале.
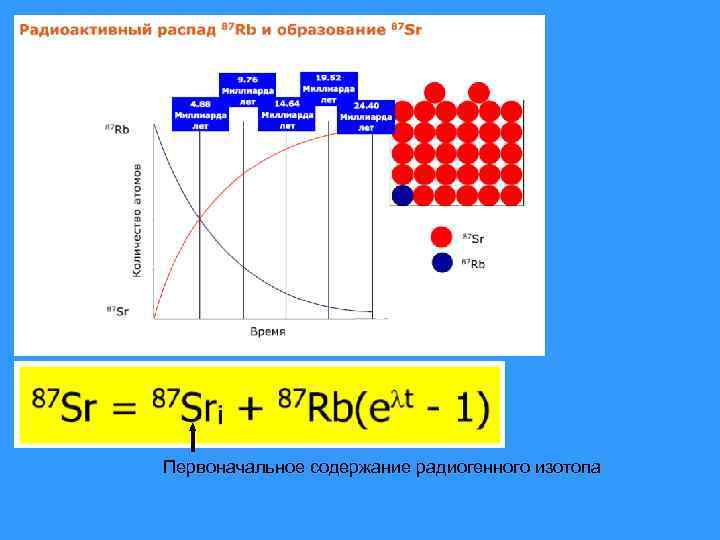
Первоначальное содержание радиогенного изотопа

• Для расчета возраста требуется знать содержание изотопов. Современные массспектрометры, приборы, предназначенные для определения изотопов, могут определять лишь их отношения. • Поэтому каждый член уравнения делим на содержание изотопа 86 Sr является стабильным изотопом и не образуется в результате радиоактивного распада существующих в природе изотопов какихлибо элементов.
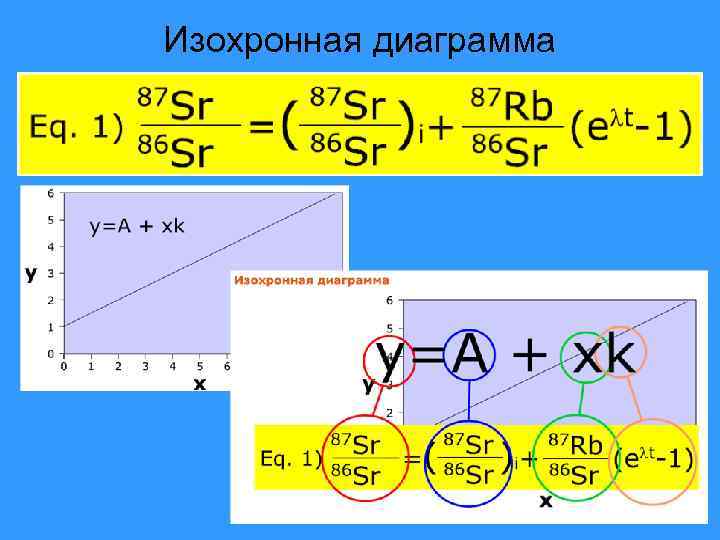
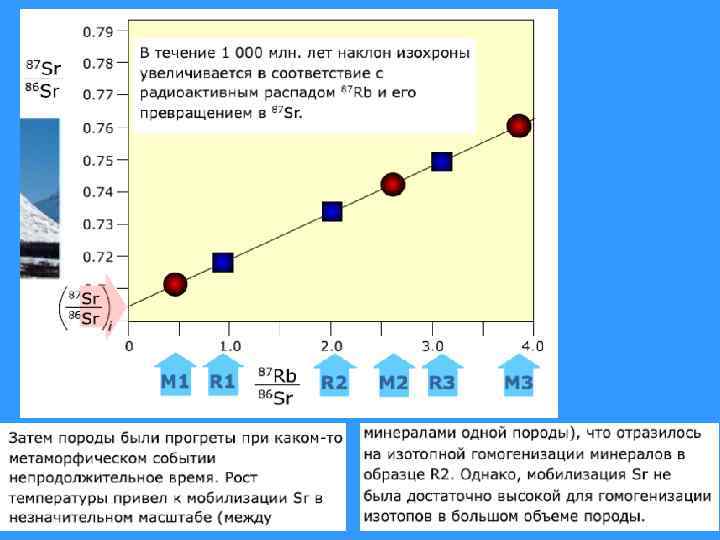
Изохронная диаграмма
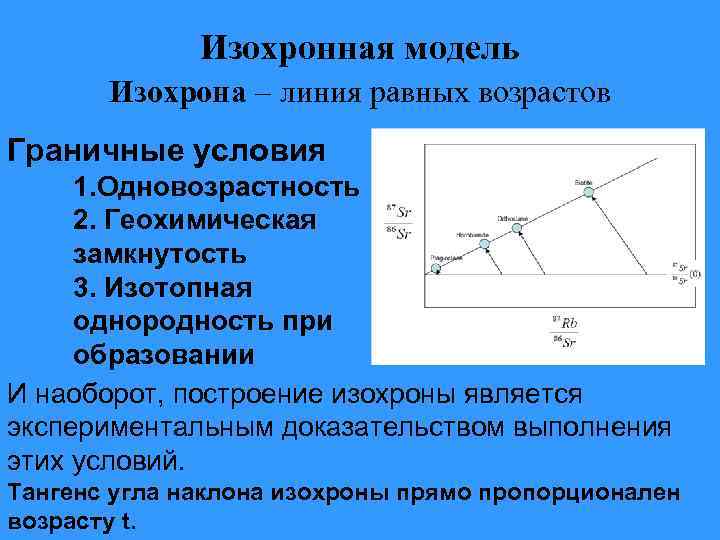
Изохронная модель Изохрона – линия равных возрастов Граничные условия 1. Одновозрастность 2. Геохимическая замкнутость 3. Изотопная 86 однородность при образовании И наоборот, построение изохроны является экспериментальным доказательством выполнения этих условий. Тангенс угла наклона изохроны прямо пропорционален возрасту t.
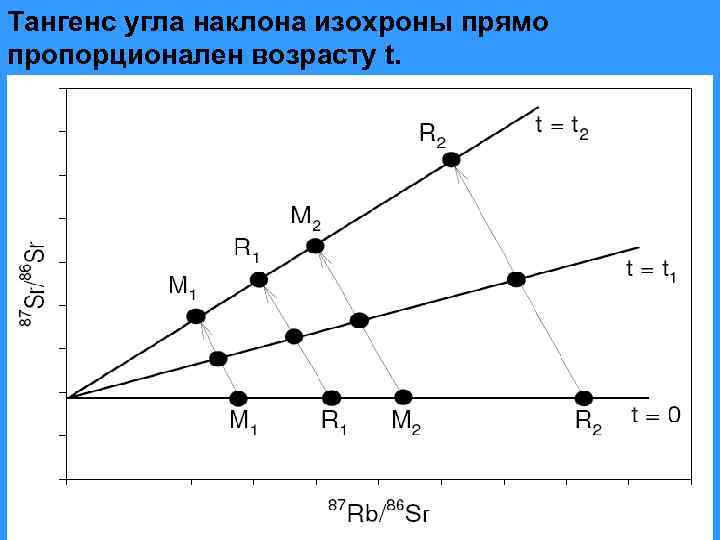
Тангенс угла наклона изохроны прямо пропорционален возрасту t.
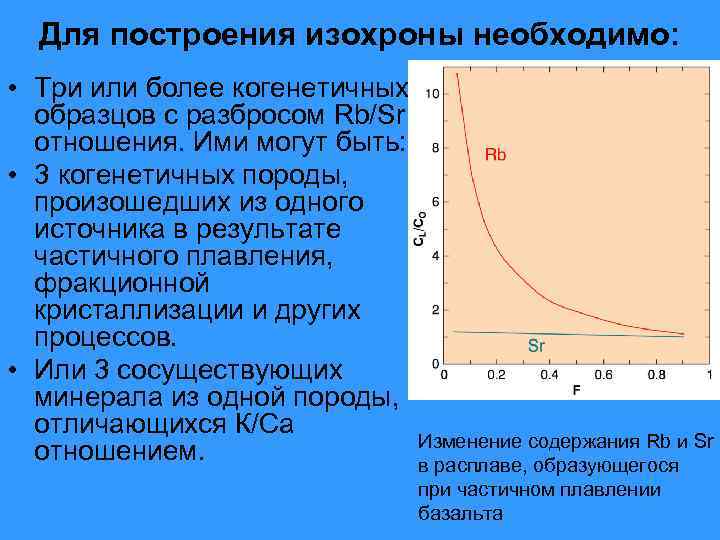
Для построения изохроны необходимо: • Три или более когенетичных образцов с разбросом Rb/Sr отношения. Ими могут быть: • 3 когенетичных породы, произошедших из одного источника в результате частичного плавления, фракционной кристаллизации и других процессов. • Или 3 сосуществующих минерала из одной породы, отличающихся К/Са отношением. Изменение содержания Rb и Sr в расплаве, образующегося при частичном плавлении базальта

• В ходе фракционной кристаллизации магмы Sr имеет тенденцию концентрироваться в плагиоклазе, тогда как Rb остается в жидкой фазе. Вследствие этого в ходе прогрессивной кристаллизации отношение Rb/Sr в остаточной магме может постепенно возрастать. • Поэтому серии дифференцированных магматических пород имеют тенденцию к повышению отношения Rb/Sr с увеличением степени дифференциации. Наивысшие значения этого отношения, достигающие 10 и более, наблюдаются в дифференциатах последних стадий, включая пегматиты.

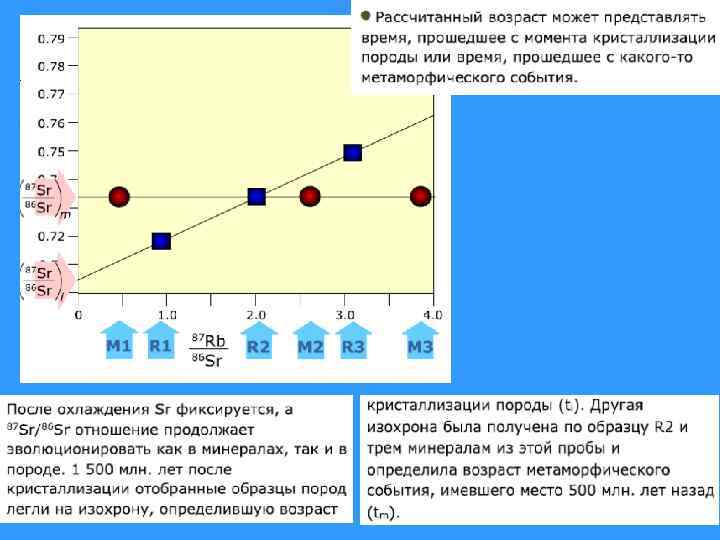
Геохронология и геохимия радиогенных изотопов На основе этих уравнений можно решать два вида задач: • Определение возраста по изотопному составу и по отношению материнского изотопа к дочернему – ГЕОХРОНОЛОГИЯ • Оценка отношения материнского элемента к дочернему в источнике вещества по изотопному составу и возрасту его производных – ГЕОХИМИЯ РАДИОГЕННЫХ ИЗОТОПОВ
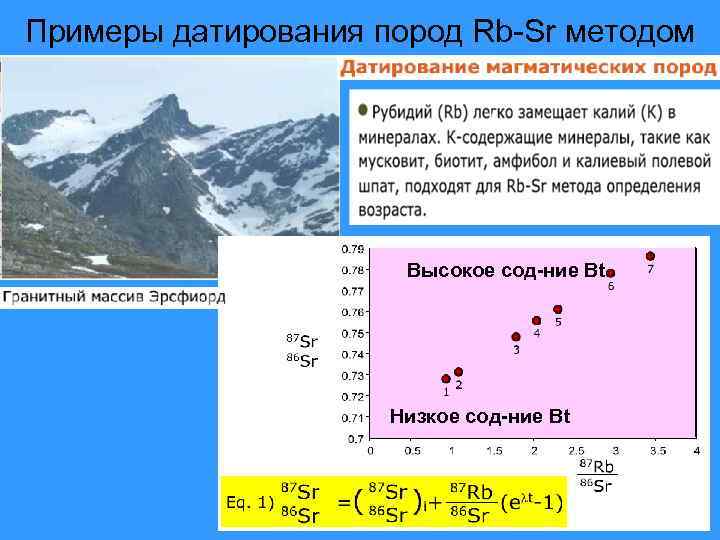
Примеры датирования пород Rb-Sr методом Высокое сод-ние Bt Низкое сод-ние Bt


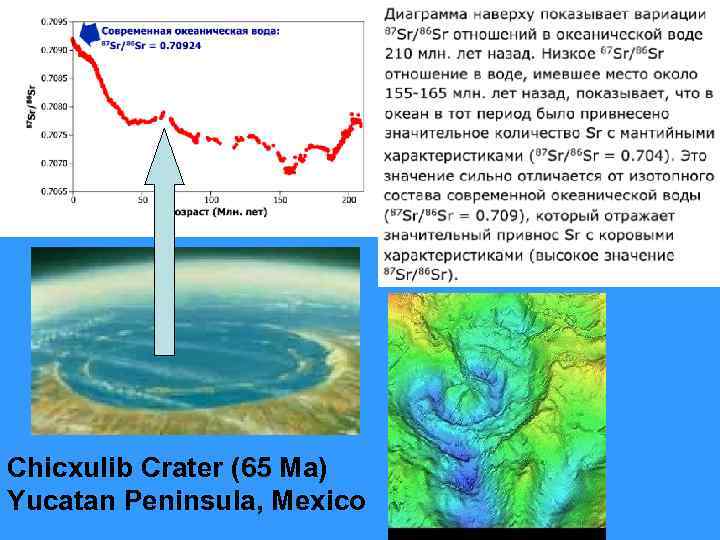
Chicxulib Crater (65 Ma) Yucatan Peninsula, Mexico
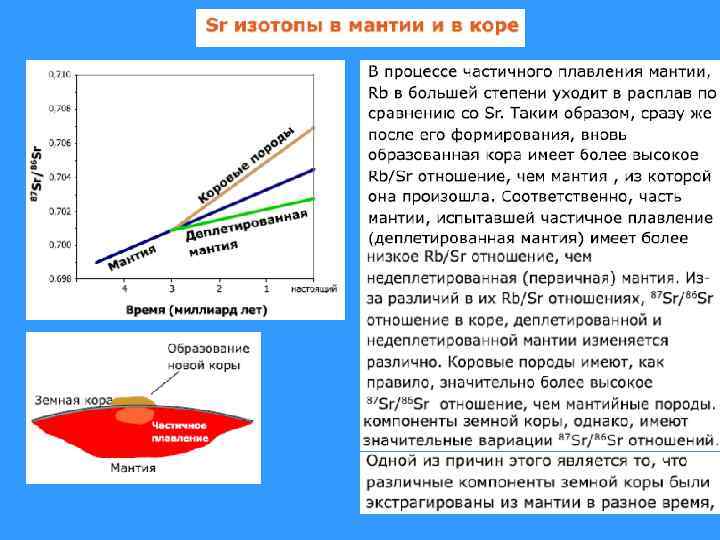
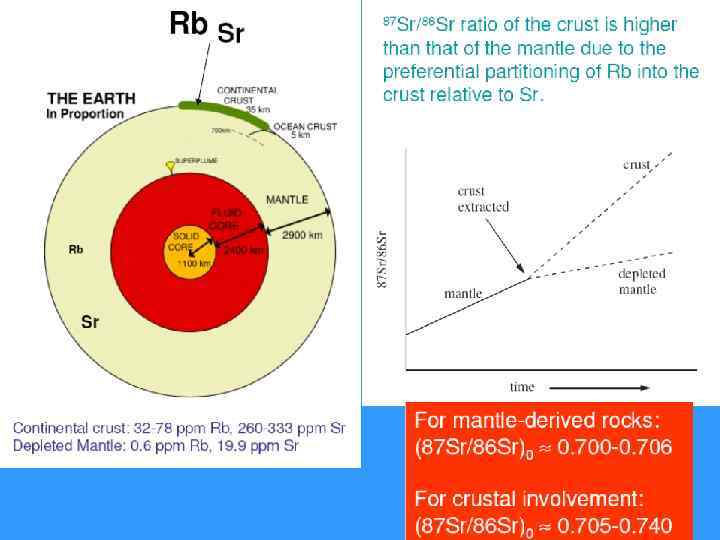
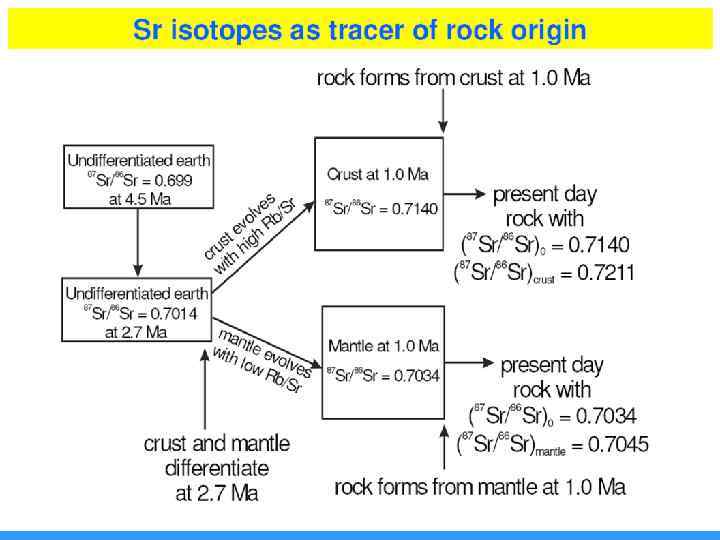

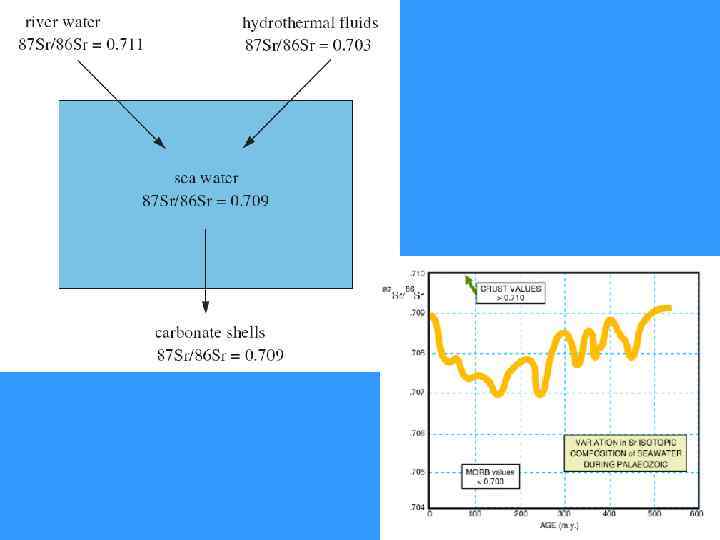
• Первичное отношение изотопов Sr имеет наиболее низкие значения 0, 699 в метеоритном веществе; несколько повышаясь для пород, имеющих мантийное происхождение. Для океанических пород (MORB, OIB) это отношение еще выше 0, 706 -0, 708. Для типично коровых пород (Sгранитов) отношение достигает 0, 715 -0, 720. • Высокие значения отношений для основных и ультраосновных пород – явления контаминации глубинного вещества коровым материалом. • Rb-Sr метод чаще всего используют для интрузивных пород кислого состава.

• Применение Rb-Sr метода ограничивается двумя факторами: • Большим периодом полураспада 87 Rb, который составляет 48, 8 х109 лет. • Тем, что обычный стронций содержит около 7 % 87 Sr. • Из-за такого большого периода полураспада 87 Rb в образцах, особенно молодых, накапливается очень малое количество 87 Srрад. Эту малую добавку очень трудно измерить, если в пробе содержится большое количество обычного стронция. • ПОЭТОМУ ДЛЯ ДАТИРОВАНИЯ ПРИГОДНЫ ТОЛЬКО ОБРАЗЦЫ С ВЫСОКИМИ ОТНОШЕНИЯМИ Rb/Sr, ПРИЧЕМ БОЛЬШЕ ВОЗРАСТ, ТЕМ ЭТО ОТНОШЕНИЕ ДОЛЖНО БЫТЬ ВЫШЕ.
05_Геохимия_изотопов_ 2.ppt