Лекция Геохимия гидросферы и атмосферы.ppt
- Количество слайдов: 16
![Геохимия гидросферы Химия воды Характеристики растворов ПР = [Ag+]х[Cl-] р. Н= - lg [H+] Геохимия гидросферы Химия воды Характеристики растворов ПР = [Ag+]х[Cl-] р. Н= - lg [H+]](https://present5.com/presentation/10348059_98706891/image-1.jpg) Геохимия гидросферы Химия воды Характеристики растворов ПР = [Ag+]х[Cl-] р. Н= - lg [H+] р. Н природных вод колеблется в широких пределах: • • • Н 2 О щелочных почв р. Н= 9 -10 морская вода 8 речная вода 7 дождевая вода 6 болотная вода 4 вода термальных источников 1 1
Геохимия гидросферы Химия воды Характеристики растворов ПР = [Ag+]х[Cl-] р. Н= - lg [H+] р. Н природных вод колеблется в широких пределах: • • • Н 2 О щелочных почв р. Н= 9 -10 морская вода 8 речная вода 7 дождевая вода 6 болотная вода 4 вода термальных источников 1 1
 Общие сведения о Мировом океане Температура Давление Глубина р. Н Средняя Пределы 5 о. С 1 о. С(глубин. ) - 30 о. С (поверх. тропики) Среднее 200 бар Обычный диапазон от 1 бар до 540 бар Средняя Наибольшая 3730 м 10850 м 8, 1+/- 0, 2 2
Общие сведения о Мировом океане Температура Давление Глубина р. Н Средняя Пределы 5 о. С 1 о. С(глубин. ) - 30 о. С (поверх. тропики) Среднее 200 бар Обычный диапазон от 1 бар до 540 бар Средняя Наибольшая 3730 м 10850 м 8, 1+/- 0, 2 2
 Максимальные концентрации имеют ионы Na и Cl. 99, 9% растворенных солей образованы 11 элементами – Cl, Na, Mg, S, Ca, K, Br, C, Sr, B, F. S(соленость) = 1, 80655× Cl(хлорность) или S = 0, 03 +1, 805 × Cl Соленость морской воды в среднем - 35‰ или 3, 5%. При изучении хим. состава океанической воды рассматривается три типа обменных реакций: 1) с атмосферой, 2) с донными осадками, 3) с живыми организмами. Реакция морской воды с твердым веществом, представленным в виде донных осадков или магматических пород океанической коры, называется гальмиролизом. 3
Максимальные концентрации имеют ионы Na и Cl. 99, 9% растворенных солей образованы 11 элементами – Cl, Na, Mg, S, Ca, K, Br, C, Sr, B, F. S(соленость) = 1, 80655× Cl(хлорность) или S = 0, 03 +1, 805 × Cl Соленость морской воды в среднем - 35‰ или 3, 5%. При изучении хим. состава океанической воды рассматривается три типа обменных реакций: 1) с атмосферой, 2) с донными осадками, 3) с живыми организмами. Реакция морской воды с твердым веществом, представленным в виде донных осадков или магматических пород океанической коры, называется гальмиролизом. 3
 Формы нахождения элементов в океане Важнейшие ионы, присутствующие в морской воде включают следующие: K+ KSO 4 Na+ Na. CO 3 - Na. HCO 3 Na. SO 4 Ca 2+ Ca. HCO 3+ Mg 2+ Mg. HCO 3+ HCO 3 - SO 42 - Cl- 4
Формы нахождения элементов в океане Важнейшие ионы, присутствующие в морской воде включают следующие: K+ KSO 4 Na+ Na. CO 3 - Na. HCO 3 Na. SO 4 Ca 2+ Ca. HCO 3+ Mg 2+ Mg. HCO 3+ HCO 3 - SO 42 - Cl- 4
 Существует несколько способов накопления элементов в осадках: 1. биогенное поглощение, 2. захват органическими частицами, 3. захват, сорбция или реакции с глинистыми частицами, 4. осаждение или сорбция гидроокислами и окислами, 5. диффузия растворенных веществ в осадок и из осадка. 5
Существует несколько способов накопления элементов в осадках: 1. биогенное поглощение, 2. захват органическими частицами, 3. захват, сорбция или реакции с глинистыми частицами, 4. осаждение или сорбция гидроокислами и окислами, 5. диффузия растворенных веществ в осадок и из осадка. 5
 МАТЕРИКОВЫЕ ВОДЫ К материковым водам относятся воды ледников, озер, болот, рек, подземные воды, включая термальные воды вулканических областей. Разнообразие состава природных вод определяется соотношением в них условно выделяемых пяти групп компонентов: главные ионы; растворенные газы; биогенные элементы (соединения N, P, Si); микроэлементы; органические вещества. 6
МАТЕРИКОВЫЕ ВОДЫ К материковым водам относятся воды ледников, озер, болот, рек, подземные воды, включая термальные воды вулканических областей. Разнообразие состава природных вод определяется соотношением в них условно выделяемых пяти групп компонентов: главные ионы; растворенные газы; биогенные элементы (соединения N, P, Si); микроэлементы; органические вещества. 6
 Основными источниками минерализации вод в пределах ЗК являются: 1. изверженные и метаморфические породы, дающие при выветривании растворимые соединения, 2. залежи некоторых осадочных пород (известняки, доломиты, мергели, гипсы, каменная соль), состоящие из растворимых солей (карбонаты, сульфаты, хлориды), 3. соли, рассеянные и адсорбированные в осадочных породах, коре выветривания и почвах. 7
Основными источниками минерализации вод в пределах ЗК являются: 1. изверженные и метаморфические породы, дающие при выветривании растворимые соединения, 2. залежи некоторых осадочных пород (известняки, доломиты, мергели, гипсы, каменная соль), состоящие из растворимых солей (карбонаты, сульфаты, хлориды), 3. соли, рассеянные и адсорбированные в осадочных породах, коре выветривания и почвах. 7
 ОВ (океаническая) РВ (речная) Na>Mg>Ca Ca>Na>Mg Cl>SO 4>HCO 3>SO 4>Cl Зависимость состава подземных вод от состава вмещающих пород можно продемонстрировать следующей таблицей Тип породы Гранит, диорит Габбро, базальт Алевролит, глина Известняк, доломит, мрамор Характеристика воды Низкое содержание ионов, преобладание Na, HCO 3, содержание Si. O 2 от умеренного до высокого, р. Н=6, 3 -7, 9 Среднее содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 высокое, р. Н=6, 7 -8, 5 Высокое содержание ионов, преобладание Na, Сa, Mg, , HCO 3, SO 4, Cl, содержание Si. O 2 от низкого до умеренного, р. Н=4 -8, 6 Высокое содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 низкое, р. Н=7 -8, 2 Природные воды и их геохимическая 8 классификация
ОВ (океаническая) РВ (речная) Na>Mg>Ca Ca>Na>Mg Cl>SO 4>HCO 3>SO 4>Cl Зависимость состава подземных вод от состава вмещающих пород можно продемонстрировать следующей таблицей Тип породы Гранит, диорит Габбро, базальт Алевролит, глина Известняк, доломит, мрамор Характеристика воды Низкое содержание ионов, преобладание Na, HCO 3, содержание Si. O 2 от умеренного до высокого, р. Н=6, 3 -7, 9 Среднее содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 высокое, р. Н=6, 7 -8, 5 Высокое содержание ионов, преобладание Na, Сa, Mg, , HCO 3, SO 4, Cl, содержание Si. O 2 от низкого до умеренного, р. Н=4 -8, 6 Высокое содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 низкое, р. Н=7 -8, 2 Природные воды и их геохимическая 8 классификация
 Зависимость состава подземных вод от состава вмещающих пород можно продемонстрировать следующей таблицей Тип породы Гранит, диорит Габбро, базальт Алевролит, глина Известняк, доломит, мрамор Характеристика воды Низкое содержание ионов, преобладание Na, HCO 3, содержание Si. O 2 от умеренного до высокого, р. Н=6, 3 -7, 9 Среднее содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 высокое, р. Н=6, 7 -8, 5 Высокое содержание ионов, преобладание Na, Сa, Mg, , HCO 3, SO 4, Cl, содержание Si. O 2 от низкого до умеренного, р. Н=4 -8, 6 Высокое содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 низкое, р. Н=7 -8, 2 9
Зависимость состава подземных вод от состава вмещающих пород можно продемонстрировать следующей таблицей Тип породы Гранит, диорит Габбро, базальт Алевролит, глина Известняк, доломит, мрамор Характеристика воды Низкое содержание ионов, преобладание Na, HCO 3, содержание Si. O 2 от умеренного до высокого, р. Н=6, 3 -7, 9 Среднее содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 высокое, р. Н=6, 7 -8, 5 Высокое содержание ионов, преобладание Na, Сa, Mg, , HCO 3, SO 4, Cl, содержание Si. O 2 от низкого до умеренного, р. Н=4 -8, 6 Высокое содержание ионов, преобладание Сa, Mg, , HCO 3, содержание Si. O 2 низкое, р. Н=7 -8, 2 9
 Геохимическая классификация вод включает 6 основных классификационных параметров, позволяющих выделять группы, типы, классы, семейства, роды и виды вод. Общая ее схема имеет следующий вид: I группа (по температуре): (1 -4) II тип (по окислительно-восстановительным условиям): 1) кислородные воды (окислительные) 2) сероводородные (сульфидные) 3) глеевые (восстановительные бессероводородные) III класс (по кислотно-щелочным условиям): 1) сильнокислые (р. Н<3) 2) слабокислые (3 -6, 5) 3) нейтральные и слабощелочные (6, 5 -8, 5) 4) сильнощелочные (>8, 5) 10
Геохимическая классификация вод включает 6 основных классификационных параметров, позволяющих выделять группы, типы, классы, семейства, роды и виды вод. Общая ее схема имеет следующий вид: I группа (по температуре): (1 -4) II тип (по окислительно-восстановительным условиям): 1) кислородные воды (окислительные) 2) сероводородные (сульфидные) 3) глеевые (восстановительные бессероводородные) III класс (по кислотно-щелочным условиям): 1) сильнокислые (р. Н<3) 2) слабокислые (3 -6, 5) 3) нейтральные и слабощелочные (6, 5 -8, 5) 4) сильнощелочные (>8, 5) 10
 IV семейство (по общей минерализации): 1) ультрапресные (<0, 1 г/л) 2) пресные (0, 1 -1 г/л) 3) солоноватые (1 -3 г/л) 4) соленые (3 -36 г/л) 5) рассолы (>36 г/л) V род (по содержанию растворимых органических веществ - РОВ): 1) богатые РОВ гумусового ряда 2) богатые РОВ нефтяного ряда 3) бедные РОВ 4) промежуточные по содержанию РОВ VI вид (по ионному составу): (обычно анионному) 1) гидрокарбонатные (карбонатные), 2) сульфатные, 3) хлоридные 11
IV семейство (по общей минерализации): 1) ультрапресные (<0, 1 г/л) 2) пресные (0, 1 -1 г/л) 3) солоноватые (1 -3 г/л) 4) соленые (3 -36 г/л) 5) рассолы (>36 г/л) V род (по содержанию растворимых органических веществ - РОВ): 1) богатые РОВ гумусового ряда 2) богатые РОВ нефтяного ряда 3) бедные РОВ 4) промежуточные по содержанию РОВ VI вид (по ионному составу): (обычно анионному) 1) гидрокарбонатные (карбонатные), 2) сульфатные, 3) хлоридные 11
 Лекция № 15. Геохимия атмосферы Атмосфера - газообразная воздушная оболочка Земли, простирающаяся до более чем 1100 км. Основная масса атмосферы сосредоточена в слое высотой около 16 км. Строение атмосферы Нижний слой атмосферы, имеющий мощность 8 -10 км в полярных областях и 16 -18 км у экватора, называется тропосферой. Тропопауза. Выше, до высоты 50 -55 км простирается стратосфера. На высоте около 25 -30 км расположен слой озона. Стратопауза. Слое от 55 до 80 км называется мезосферой. Мезопауза. От 80 -100 км до 1000 км слой ионосферы. 12 С 1000 км простирается экзосфера (метасфера).
Лекция № 15. Геохимия атмосферы Атмосфера - газообразная воздушная оболочка Земли, простирающаяся до более чем 1100 км. Основная масса атмосферы сосредоточена в слое высотой около 16 км. Строение атмосферы Нижний слой атмосферы, имеющий мощность 8 -10 км в полярных областях и 16 -18 км у экватора, называется тропосферой. Тропопауза. Выше, до высоты 50 -55 км простирается стратосфера. На высоте около 25 -30 км расположен слой озона. Стратопауза. Слое от 55 до 80 км называется мезосферой. Мезопауза. От 80 -100 км до 1000 км слой ионосферы. 12 С 1000 км простирается экзосфера (метасфера).
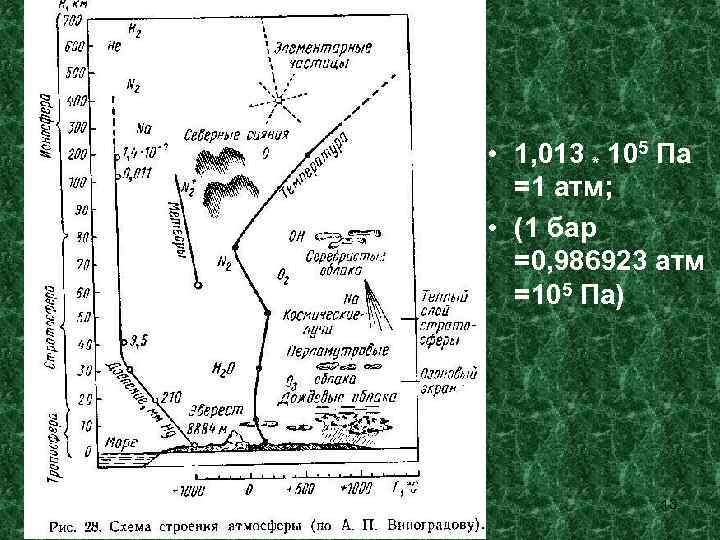 • 1, 013 * 105 Па =1 атм; • (1 бар =0, 986923 атм =105 Па) 13
• 1, 013 * 105 Па =1 атм; • (1 бар =0, 986923 атм =105 Па) 13
 Химический состав наземной атмосферы. Главными компонентами атмосферы являются азот, кислород, аргон и углекислый газ, составляющие до 99, 99% сухого воздуха. На границе с океаном с поверхности морской воды в приводные слои атмосферы поступают такие элементы как K, Cs, Rb, Cr, Cu и др. Вулканические газы СО 2, Н 2 О, H 2, CО, N 2, Cl 2, HСl, NH 3, CH 4 и др. Природные газы земных недр и их состав 1) газы биохимического происхождения, к ним относятся CH 4, CO 2, тяжелые углеводороды, N 2, H 2 S, H 2, O 2, 2) газы воздушного происхождения, образуются при проникновении в литосферу атмосферного воздуха, 3) газы химического происхождения, к ним относятся CO 2, H 2 S, H 2, CH 4, CO, N 2, HСl, HF, NH 3, SO 2, Cl, S, 14 4) газы радиоактивного происхождения, включающие He, Ar, Rn.
Химический состав наземной атмосферы. Главными компонентами атмосферы являются азот, кислород, аргон и углекислый газ, составляющие до 99, 99% сухого воздуха. На границе с океаном с поверхности морской воды в приводные слои атмосферы поступают такие элементы как K, Cs, Rb, Cr, Cu и др. Вулканические газы СО 2, Н 2 О, H 2, CО, N 2, Cl 2, HСl, NH 3, CH 4 и др. Природные газы земных недр и их состав 1) газы биохимического происхождения, к ним относятся CH 4, CO 2, тяжелые углеводороды, N 2, H 2 S, H 2, O 2, 2) газы воздушного происхождения, образуются при проникновении в литосферу атмосферного воздуха, 3) газы химического происхождения, к ним относятся CO 2, H 2 S, H 2, CH 4, CO, N 2, HСl, HF, NH 3, SO 2, Cl, S, 14 4) газы радиоактивного происхождения, включающие He, Ar, Rn.
 Происхождение и эволюция атмосферы Атмосфера возникла около 3, 8 -3, 9 млрд. лет назад за счет дегазации Земли. Давление составляло 4 – 4, 7 бар, а температура у поверхности Земли была +1000 С. В протерозое атмосфера стала азотной, а в палеозое – азотнокислородной. В конце палеозоя Ро 2 достигло современного (0, 23 бар). Атмосфера в наше время испытывает огромное антропогенное воздействие, нарушающее ее состав. Главные антропогенные воздействия: 1. Возрастающее поступление индустриального тепла. 2. Чрезмерное потребление О 2, N 2 и огромные выбросы СО 2. 3. Сброс вредных газов СО, H 2 S, SO 3, NO 2 и других предприятиями металлургии, химической промышленности, автотранспортом и др. 4. Загрязнение антропогенной минеральной пылью, свинцом, тяжелыми металлами, радиоактивными отходами, продуктами химизации сельского хозяйства. 15 5. Сброс огромного количества бытовых отходов и др.
Происхождение и эволюция атмосферы Атмосфера возникла около 3, 8 -3, 9 млрд. лет назад за счет дегазации Земли. Давление составляло 4 – 4, 7 бар, а температура у поверхности Земли была +1000 С. В протерозое атмосфера стала азотной, а в палеозое – азотнокислородной. В конце палеозоя Ро 2 достигло современного (0, 23 бар). Атмосфера в наше время испытывает огромное антропогенное воздействие, нарушающее ее состав. Главные антропогенные воздействия: 1. Возрастающее поступление индустриального тепла. 2. Чрезмерное потребление О 2, N 2 и огромные выбросы СО 2. 3. Сброс вредных газов СО, H 2 S, SO 3, NO 2 и других предприятиями металлургии, химической промышленности, автотранспортом и др. 4. Загрязнение антропогенной минеральной пылью, свинцом, тяжелыми металлами, радиоактивными отходами, продуктами химизации сельского хозяйства. 15 5. Сброс огромного количества бытовых отходов и др.
 Большая часть газов Земли сосредоточена в литосфере и верхней мантии и значительно меньшая в самой атмосфере, соотношение между ними таково: атмосфера : литосфера: верхняя мантия = 1: 2: 80. 16
Большая часть газов Земли сосредоточена в литосфере и верхней мантии и значительно меньшая в самой атмосфере, соотношение между ними таково: атмосфера : литосфера: верхняя мантия = 1: 2: 80. 16


