Геохимия.ppt
- Количество слайдов: 47

Геохимия

Геохимия как наука Объекты изучения геохимии Связь геохимии с другими науками Геохимия – наука, которая изучает историю атомов химических элементов и их поведение в различных природных физико-химических процессах. Объект изучения геохимии – атом химического элемента. Геохимия изучает историю атомов химических элементов в земной коре, в глубоких частях нашей планеты, в космическом пространстве и космических телах.

По своему содержанию геохимия делится на две части. I. Общая (теоретическая) геохимия – решает две проблемы: 1) закономерности распределения атомов химических элементов в природных объектах, а также в космических телах (космохимия); 2) закономерности поведения атомов химических элементов в природных процессах. II. Прикладная геохимия. Изучает следующие вопросы: 1) распределение атомов химических элементов в небольших объектах; 2) геохимия отдельных элементов; 3) поисковая геохимия.

Геохимия тесно связана со многими науками. С геологическими – минералогия, кристаллография, петрография, учение о МПИ. С математикой, физикой, химией – использует методы исследований и обработки аналитических данных. С астрономией, биолого-почвенными науками. Таким образом, геохимия – наука синтетическая.

Общие сведения о строении атома Заварицкий А. Н. сформулировал общий закон геохимии: распространенность атомов химических элементов в природе зависит от их строения. Распространенность атомов химических элементов определяется устойчивостью их ядер, а движение атомов химических элементов определяется особенностями строения электронных оболочек.

В строении атома принимают участие около 40 элементарных частиц, из которых три являются фундаментальными: протон, нейтрон, электрон. Электроны находятся на орбитах вокруг атомного ядра. Радиус атомов ≈ 10 -8 см. Радиус атомного ядра ≈ 10 -12 см. Атом – электрически нейтральная частица. Но он может отдавать или принимать электроны на своих орбитах. При этом атом становится заряженным – ионом. Ион, который отдает свои электроны, становится положительно заряженным и называется катион. Ион, получивший электрон, несет отрицательный заряд и называется анион.

Ядро атома состоит из ядерных частиц – нуклонов. Это протоны Z и нейтроны N. Массовое число атома А равно сумме протонов и нейтронов. А=Z+N Выделяют нуклиды: Изотопы Изобары Изотоны

Изотопы – ядра, у которых одинаковое число Z и разные числа N и А. Изотопы находятся в одной клетке таблицы Менделеева и обладают одинаковыми химическими свойствами. Изобары – ядра, у которых одинаковое число А и разные числа Z и N. Изобары находятся в разных клетках таблицы Менделеева и имеют разные химические свойства. Изотоны – ядра, у которых одинаковое число N и разные числа Z и А. Изотоны находятся в разных клетках таблицы Менделеева и обладают разными химическими свойствами.
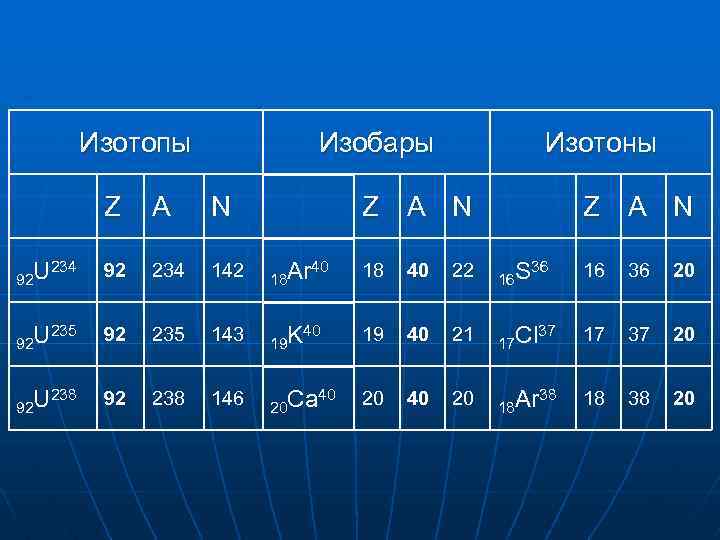
Изотопы Изобары Изотоны Z A N U 234 92 92 234 142 Ar 40 18 18 40 22 S 36 16 16 36 20 U 235 92 92 235 143 K 40 19 19 40 21 Cl 37 17 17 37 20 U 238 92 92 238 146 Ca 40 20 20 40 20 Ar 38 18 18 38 20

Соотношение Z: N в начале и конце таблицы Менделеева разное. Для начала таблицы Z: N = 1: 1. В середине и конце таблицы Z: N=2: 3. В настоящее время среди химических элементов известно 286 стабильных и долгоживущих радиоактивных изотопов, а всего в природных процессах известно 340 стабильных изотопов и 162 изобара. В геохимии для решения геологических задач используют радиоактивные и стабильные изотопы. В тех случаях, когда отношение Z: N отличается от оптимального, ядра являются радиоактивными. Т. о. радиоактивность – переход к оптимальному соотношению нуклонов.

Электроны, входящие в состав атомов, располагаются на орбитах, при этом, электроны на внешних орбитах могут самопроизвольно переходить на внутренние орбиты. Такой переход сопровождается выделением энергии. Обратный переход называется рекомбинация и всегда требует затрат внешней энергии.

Типы химической связи Атомы химических элементов взаимодействуют друг с другом и образуют различные типы химической связи. Различают 4 крайние типа химической связи: ионная, атомная, молекулярная, металлическая.

Геохимическая классификация химических элементов Каждая классификация должна отвечать двум требованиям: 1) Она должна характеризовать поведение химического элемента в природных физикохимических процессах. 2) Должна определять ассоциацию химических элементов. Существует несколько классификаций, наиболее ранние из них – Вернадского В. И. , Ферсмана А. Е. , Заварицкого А. Н. , Гольдшмидта В. М. , Садецки-Кардоша Э.

Классификация Гольдшмидта 1. Атмофильные элементы (атмофилы) – H, He, N, Xe, N 2. Литофилы – характерно сродство к кислороду, легко образуют кислородные соединения – Na, K, Ca, Mg, Si, Al, … 3. Халькофилы – обладают сродством к сере – Cu, Pb, Zn, As, Hg, Bi, Sb, Au. 4. Сидерофилы – обладают сродством к мышьяку, образуют арсениды, встречаются в самородном состоянии – Fe, Pt, Os, Ir, Co, Ni, V, … 5. Биофилы – элементы всех 4 -х групп, участвующие в органических веществах.

Классификация Садецки-Кардоша 1. Атмофилы. 2. Литофилы (в меньшем объеме). 3. Сидерофилы 4. Оксихалькофилы (образуют соединения и с S, и с O) – Sn, As, Bi, Pb. 5. Сульфохалькофилы (кислородные соединения мало характерны) – Cu, Zn, Hg. 6. Пегматофилы – Nb, Ta, U, Th, W … 7. Седиментофилы – C, B, Cl, F, Br, I. 8. Биофилы.

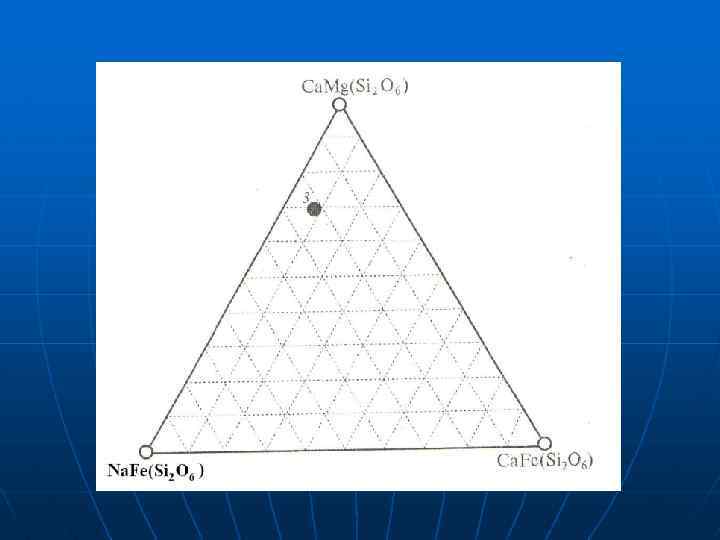
Геохимическая классификация химических элементов В. М. Гольдшмидта
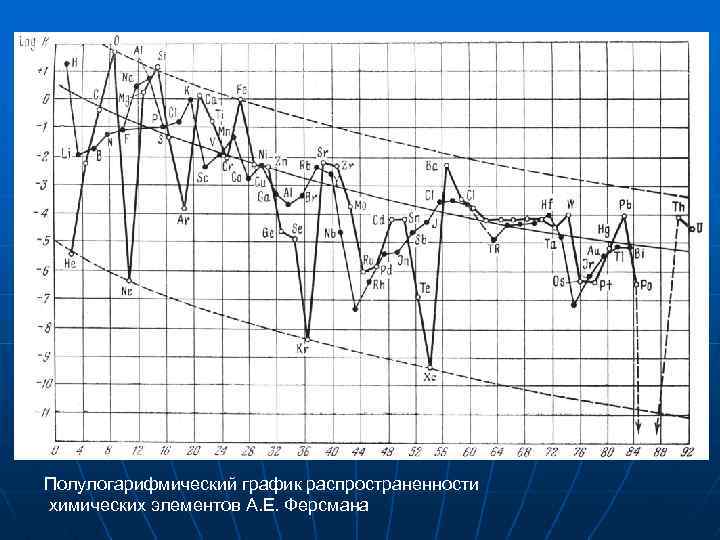
Полулогарифмический график распространенности химических элементов А. Е. Ферсмана

Выводы из графика 1. Наиболее распространенный элемент – кислород. 2. Химические элементы пользуются неодинаковой распространенностью. Наиболее распространены элементы начала таблицы № 1 -28. 3. По распространенности выделяют 3 группы элементов: избыточные, нормальной распространенности, дефицитные. 4. Четные и нечетные элементы распространены неодинаково, как правило, кларк четного элемента на порядок выше соседнего нечетного. 5. Особую геохимическую роль играют 4 наиболее распространенных элемента: O, H, Si, Al. O – важная составная часть атмосферы. H и O – основные компоненты гидросферы. Все 4 элемента преобладают в литосфере, например, каолинит Al 4[Si 4 O 10](OH)8 – наиболее распространенный минерал.

Формы нахождения химических элементов в земной коре I. Самостоятельные минеральные виды (минералы). II. Примеси и смеси неструктурные (состояние рассеяния) структурные (изоморфные) III. Водные растворы (коллоидные и истинные) и газовые смеси. IV. Силикатные расплавы. V. Биогенная форма.

Самостоятельные минеральные виды По распространенности все минералы объединяются в 5 групп. 1. Весьма распространенные. 2. Распространенные минералы. 3. Распространенные рудные минералы. 4. Редкие минералы. 5. Очень редкие минералы. Среди химических элементов выделяют элементы минералообразователи: O, Si, Al, H, Fe, Ca, Mg, Mn, Ti, Na, K, C, P, S. Остальные элементы образуют или небольшое количество минералов, или вообще их не образуют, а находятся в виде примесей в кристаллических решетках других минералов (группа рассеянных элементов).

Неструктурные примеси Не входят в кристаллическую решетку минерала, находятся в дефектах решетки. Ферсман А. Е. называл такое состояние эндокриптным рассеянием. В любом земном образце можно найти атомы всех химических элементов в количествах 10 -10%. Нижний предел рассеяния – 1 атом в 1 см 3 вещества. Исландский шпат (Ca. CO 3) содержит 10 -6% I. В 1 см 3 исландского шпата 1014 атомов I.
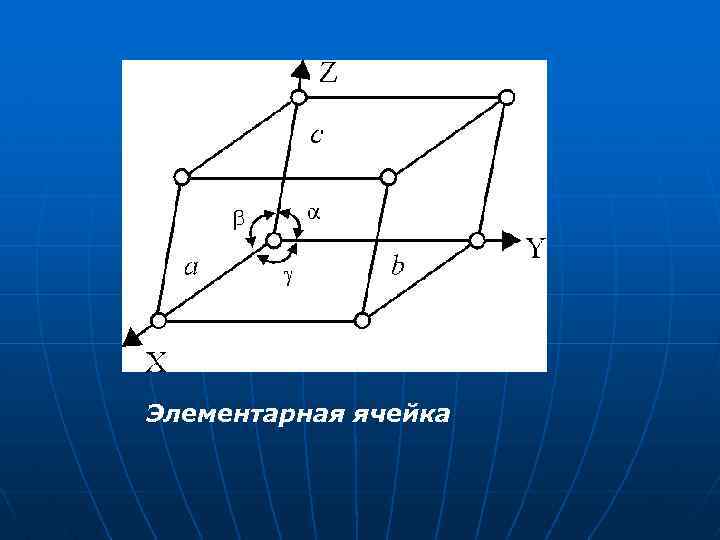
Элементарная ячейка

Структурные примеси и смеси Типы изоморфизма I. На основе изоморфной смесимости 1. Совершенный изоморфизм 2. Несовершенный изоморфизм. II. На основе валентности ионов 1. Изовалентный изоморфизм. Правило: если ион может быть замещен ионом большего или меньшего радиуса, то в кристаллическую решетку входит в первую очередь ион меньшего радиуса. 2. Гетеровалентный изоморфизм. В замещениях участвуют ионы разного заряда. 1 правило: если ион может быть замещен ионом большего или меньшего заряда, то в кристаллическую решетку в первую очередь входит ион большего заряда, затем меньшего.

2 закон: закон диагональных рядов. Радиусы ионов меньше всего изменяются по диагоналям таблицы Менделеева (правило диагональных рядов Гольдшмидта). Ферсман показал, что гетеровалентный изоморфизм развивается по диагоналям таблицы – закон диагональных рядов Ферсмана. III. По механизму вхождения иона в I кристаллическую решетку I 1. Изоморфизм замещения (изоморфизм I рода). 2. Изоморфизм внедрения 3. Изоморфизм вычитания (2 и 3 изоморфизм 2 рода)
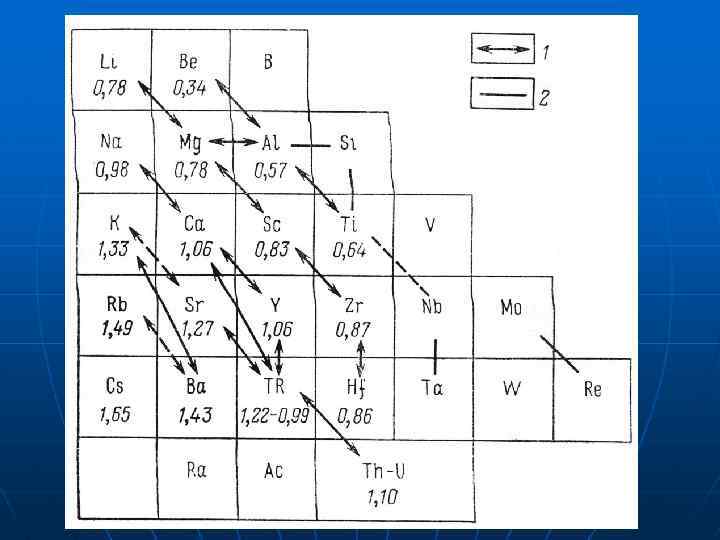

IV. Изоморфизм блоковый. Характерен для минералов группы колумбитатанталита (Mn, Fe)(Nb, Ta)2 O 6 V. Полярный изоморфизм. Однонаправленный. Ферсман составил ряды полярного изоморфизма Sr 2+ K+ Ca 2+ K+ Ce 3+ Ba 2+ Th 4+ U 4+ Zn 2+ Pb 2+ Fe 2+

VI. Цепочечный изоморфизм. VII. Диадохия. Несовершенный полярный изоморфизм компонентов, которые кристаллизуются в разных сингониях. Изоморфизм компенсационный. Факторы изоморфизма Внутренние факторы – обусловлены особенностями строения атома или кристаллической решетки. Внешние факторы – характеризуют среду, в которой образуется смешанный кристалл.

Внутренние факторы I. Химическая индифферентность компонентов. Изоморфные компоненты не должны вступать в химическую реакцию друг с другом. Мерой индифферентности является электроотрицательность элементов. Чем больше разница электроотрицательностей, тем активней химический элемент. Замещения возможны для элементов с близкими значениями электроотрицательностей. II. Радиус ионов или атомов. Гольдшмидт показал, что изоморфные замещения возможны в случае разницы радиусов ионов не более, чем на 15%. III. Типы химической связи изоморфных компонентов должны быть одинаковыми.

IV. Размеры и форма элементарных ячеек кристаллических решеток изоморфных компонентов должны быть близкими. V. Должны сохраняться электростатические равновесия при изоморфных замещениях. Внешние факторы I. Температура. При повышении температуры изоморфная смесимость повышается, и наоборот. II. Давление. Повышение давления способствует вхождению в кристаллическую решетку ионов меньшего радиуса. III. Совместное влияние температуры и давления. Изоморфные ряды Вернадского.

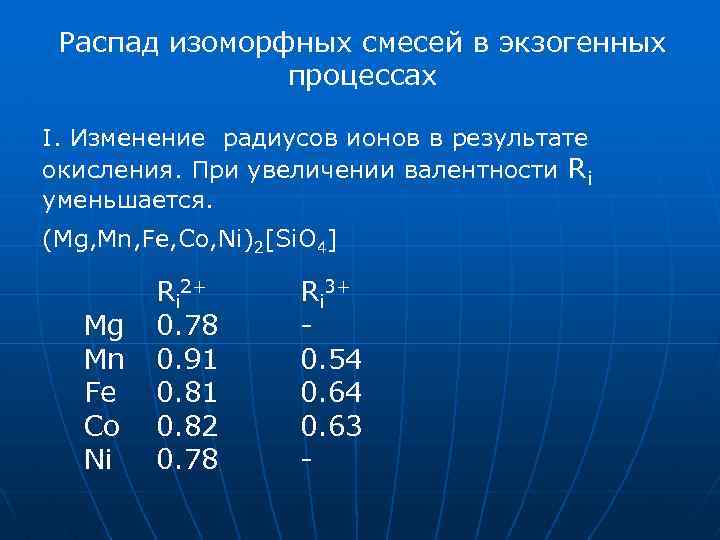
Распад изоморфных смесей в экзогенных процессах I. Изменение радиусов ионов в результате окисления. При увеличении валентности Ri уменьшается. (Mg, Mn, Fe, Co, Ni)2[Si. O 4] Mg Mn Fe Co Ni Ri 2+ 0. 78 0. 91 0. 82 0. 78 Ri 3+ 0. 54 0. 63 -

II. Изменение типа химической связи продуктов окисления. Глаукодот (Fe, Co)As. S при окислении образуется лимонит (ионная связь) и эритрин (ковалентная связь) III. Различная растворимость изоморфных компонентов при изменении кислотности-щелочности p. H
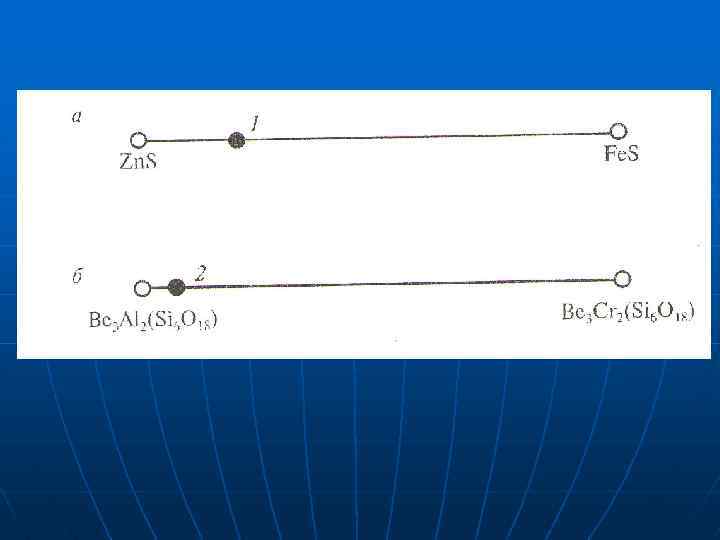
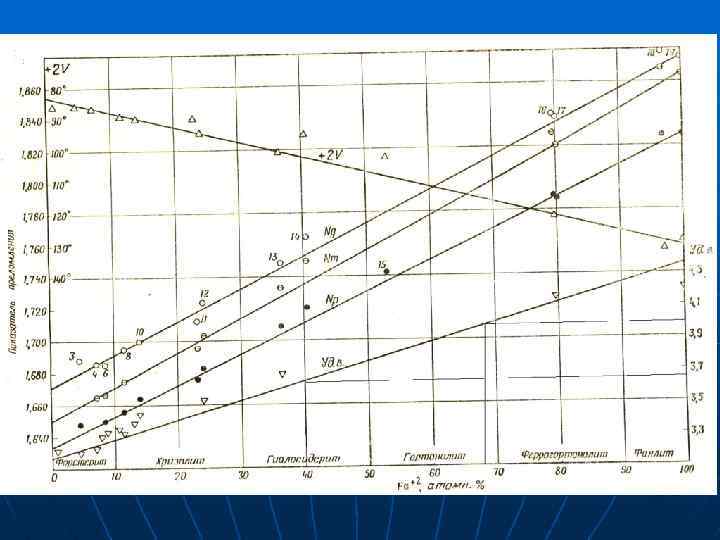


3. Энергия радиоактивного распада. 4 3 2 В млрд. лет назад млрд. лет наст. Время - 128, 59· 1016 ккал/час 87, 58∙ 1016 ккал/час 65, 48∙ 1016 ккал/час 44, 76· 1016 ккал/час Факторы миграции химических элементов I. Внутренние факторы – обусловлены особенностями строения атомов. II. Внешние факторы – характеризуют среду миграции.

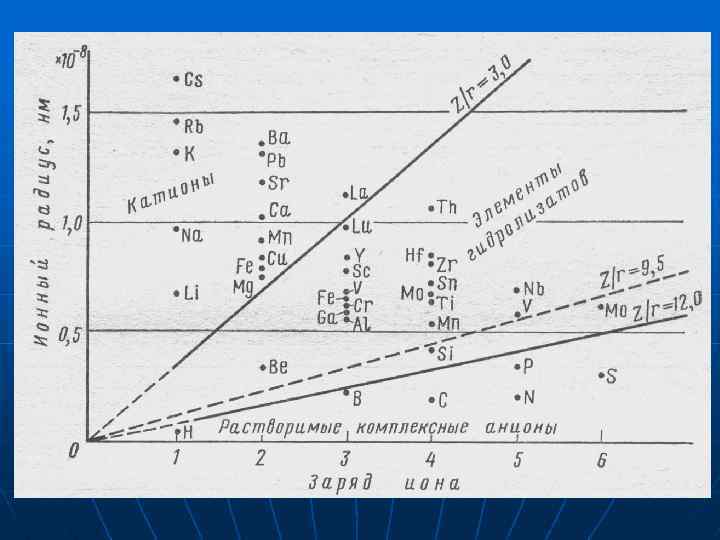
Внутренние факторы миграции 1. Ионный потенциал. Отношение заряда иона к его радиусу. Z<3 мигрируют в виде истинных растворов Z от 3 до 12 мигрируют в виде тонких взвесей Z>12 мигрируют в виде истинных растворов комплексных соединений 2. Гравитационные свойства атомов. Проявляются в дифференциации вещества по массе. 3. Термические свойства атомов. При температуре испарения <400°С, миграция в газообразном состоянии имеет основное значение. Для элементов с tисп. 400 -600°С миграция в газообразном состоянии играет заметную роль. При tисп. >600°С миграция в газообр. сост. роли не играет.

4. Свойство химической связи. 5. Радиоактивные свойства атомов. 6. Электрические свойства атомов. Внешние факторы миграции Концентрация вещества, С Роль С определяется законом действующих масс. m. A + n. B + … + p. Q = m 1 A 1 + n 1 B 1 + … + p 1 Q 1 CA 1 m 1×CB 1 n 1× … ×CQ 1 p 1 CAm×CBn× … ×CQ p =const

Изменение концентрации любого вещества, участвующего в реакции, всегда нарушает равновесие. Si. F 4 + 2 H 2 O = Si. O 2 + 4 HF CSi. O 2×CHF 4 CSi. F 4×CH 2 O 2 =const

p. H среды. Определяется концентрацией водородных ионов. p. H = 7 – раствор нейтральный p. H<7 – раствор кислый, чем меньше p. H, тем более кислый раствор p. H>7 – щелочной раствор, чем больше p. H, тем выше щелочность p. H изменяется от 1 до 14 В эндогенных процессах повышение кислотности благоприятствует замещению сильных оснований более слабыми. Повышение щелочности способствует замене слабых оснований более сильными. В экзогенных и гидротермальных процессах при повышении кислотности образуется каолинит, при повышении щелочности – монтмориллонит.

Окислительно-восстановительный потенциал Eh Реакции обмена Ba. Cl 2 + H 2 SO 4 = Ba. SO 4 + 2 HCl Валентности не меняются. Окислительно-восстановительные реакции Zn + 2 HCl = Zn. Cl 2 + H 2 В окислительно-восстановительной реакции (ОВР) участвуют два вида веществ. Окислители – приобретают электроны (восстанавливаются) Fe 3++ē Fe 2+ Восстановители – отдают электроны (окисляются) Fe 2+-ē Fe 3+

В природе наиболее сильные окислители – O 2, Fe 3+, Mn 4+, U 6+, S 6+, Cl 2, F. Наиболее сильные восстановители – H 2, Fe 2+, Mn 2+, U 4+, S 2 -, Fe 0, Zn 0, Cu 0 и органические вещества. В каждой реакции ОВ сумма окислителя и восстановителя носит название окислительновосстановительного элемента. В отдельности окислитель (или восстановитель) образуют полуэлемент. Для характеристики силы окислителей и восстановителей используется окислительновосстановительный потенциал Eh.

За нулевой потенциал условно принята реакция ионизации водорода. H 2 -2ē 2 H+ Eh=0 Полуэлементы, у которых Eh<0 являются восстановителями, чем меньше Eh, тем сильнее восстановитель. Полуэлементы, у которых Eh>0 являются окислителями, чем выше Eh, тем сильнее окислитель. Окислительно-восстановительный потенциал Eh связан с p. H среды. С повышением p. H на 1 единицу Eh уменьшается на 0, 06 v. Следовательно, в щелочной среде процессы окислениявосстановления протекают легче.

Фильтрационный эффект.
Геохимия.ppt