 Геология нефти и газа Лекция 3 -4 Кафедра динамической геологии
Геология нефти и газа Лекция 3 -4 Кафедра динамической геологии
 Нефть – физико-химическая система природного углеводородного раствора, многокомпонентного, разнообразного по составу и соотношению компонентов. Единственный неводный жидкий раствор на Земле. Растворитель – жидкие углеводороды Растворенное вещество – твердые : ( высокомолекулярные парафины, полициклические нафтены, некоторые арены и др. ), газы, неуглеводородные соединения (низкомолекулярные и высокомолекулярные – смолы, асфальтены). С одной стороны – это истинный раствор, с другой коллоидальный. Размер частиц колеблется от 0, 1 до 1 нм, коллоидного – от 1 до 100 нм. Свойства нефти и состав
Нефть – физико-химическая система природного углеводородного раствора, многокомпонентного, разнообразного по составу и соотношению компонентов. Единственный неводный жидкий раствор на Земле. Растворитель – жидкие углеводороды Растворенное вещество – твердые : ( высокомолекулярные парафины, полициклические нафтены, некоторые арены и др. ), газы, неуглеводородные соединения (низкомолекулярные и высокомолекулярные – смолы, асфальтены). С одной стороны – это истинный раствор, с другой коллоидальный. Размер частиц колеблется от 0, 1 до 1 нм, коллоидного – от 1 до 100 нм. Свойства нефти и состав
 Нефть – это сложная коллоидная гидрофобная система, состоящая из углеводородов различного строения и гетероатомных или неуглеводородных соединений (кислородных, сернистых, азотистых и высокомолекулярных металлорганических смолистоасфальтеновых соединений), которая распространена в породах осадочного чехла и фундамента осадочных бассейнов. Среди углеводородных и неуглеводородных компонентов нефти содержатся так называемые реликтовые структуры или хемофоссилии, которые по своему составу близки к некоторым биологическим веществам или их фрагментам.
Нефть – это сложная коллоидная гидрофобная система, состоящая из углеводородов различного строения и гетероатомных или неуглеводородных соединений (кислородных, сернистых, азотистых и высокомолекулярных металлорганических смолистоасфальтеновых соединений), которая распространена в породах осадочного чехла и фундамента осадочных бассейнов. Среди углеводородных и неуглеводородных компонентов нефти содержатся так называемые реликтовые структуры или хемофоссилии, которые по своему составу близки к некоторым биологическим веществам или их фрагментам.
 Органолептические – свойства, воспринимаемые с помощью органов чувств. Цвет – зависит от группового и углеводородного состава нефти Обычно нефть имеет черный или темнокоричневый цвет, иногда, при солнечном свете, зеленовато-желтый оттенок и реже она почти бесцветная. Консистенция – агрегатное состояние, зависит от фракционного, группового и углеводородного состава Запах – определяется присутствием сернистых соединений Вкус Органолептические свойства
Органолептические – свойства, воспринимаемые с помощью органов чувств. Цвет – зависит от группового и углеводородного состава нефти Обычно нефть имеет черный или темнокоричневый цвет, иногда, при солнечном свете, зеленовато-желтый оттенок и реже она почти бесцветная. Консистенция – агрегатное состояние, зависит от фракционного, группового и углеводородного состава Запах – определяется присутствием сернистых соединений Вкус Органолептические свойства
 Плотность Показатель преломления Вязкость – 1. динамическая, или абсолютная ; 2. кинематическая; 3. условная Молекулярная масса Температура застывания Поверхностное натяжение Оптическая активность Парамагнетизм Физические свойства нефти
Плотность Показатель преломления Вязкость – 1. динамическая, или абсолютная ; 2. кинематическая; 3. условная Молекулярная масса Температура застывания Поверхностное натяжение Оптическая активность Парамагнетизм Физические свойства нефти
 Физические свойства нефти косвенно отражают её химический состав и определяют товарные качества нефти. Они учитываются при составлении технологической схемы эксплуатации залежей, проектировании нефтепроводов. Диэлектрические свойства нефти и её способность люминесцировать используются при проведении поисковоразведочных работ. Плотность нефти определяется ее массой в единице объема. В нормальных условиях она лежит в пределах от 0, 73 до 1, 04 г/см 3. В условиях залежи нефть содержит растворенный газ и отличается более высокой температурой. Поэтому в недрах плотность нефти меньше, чем в стандартных условиях от 15 до 40 % и более и может составлять всего 0, 3 -0, 4 г/см 3. Физические свойства нефти
Физические свойства нефти косвенно отражают её химический состав и определяют товарные качества нефти. Они учитываются при составлении технологической схемы эксплуатации залежей, проектировании нефтепроводов. Диэлектрические свойства нефти и её способность люминесцировать используются при проведении поисковоразведочных работ. Плотность нефти определяется ее массой в единице объема. В нормальных условиях она лежит в пределах от 0, 73 до 1, 04 г/см 3. В условиях залежи нефть содержит растворенный газ и отличается более высокой температурой. Поэтому в недрах плотность нефти меньше, чем в стандартных условиях от 15 до 40 % и более и может составлять всего 0, 3 -0, 4 г/см 3. Физические свойства нефти
 Плотность нефти в зависимости от химического состава и количества растворенного газа изменяется от 0, 7 до 1 г/см 3 и более. По плотности нефти разделяются на: легкие – до 0, 810 г/см 3; средние – 0, 822– 0, 870 г/см 3; тяжелые – 0, 870–, 90 г/см 3; очень тяжелые – более 0, 900 г/см 3. Она возрастает с увеличением содержания смолисто-асфальтеновых соединений. Плотность нефти и отдельных ее фракций зависит от их состава. Плотность углеводородов заметно изменяется с температурой. Коэффициент термического расширения (изменение плотности на 1º ) составляет для различных нефтей от 0, 0006 до 0, 0009 (для пластовых нефтей он равен 0, 0008). Коэффициент сжимаемости – изменение плотности нефтей в зависимости от давления (в среднем 0, 0009 на 1 атм) Плотность нефти
Плотность нефти в зависимости от химического состава и количества растворенного газа изменяется от 0, 7 до 1 г/см 3 и более. По плотности нефти разделяются на: легкие – до 0, 810 г/см 3; средние – 0, 822– 0, 870 г/см 3; тяжелые – 0, 870–, 90 г/см 3; очень тяжелые – более 0, 900 г/см 3. Она возрастает с увеличением содержания смолисто-асфальтеновых соединений. Плотность нефти и отдельных ее фракций зависит от их состава. Плотность углеводородов заметно изменяется с температурой. Коэффициент термического расширения (изменение плотности на 1º ) составляет для различных нефтей от 0, 0006 до 0, 0009 (для пластовых нефтей он равен 0, 0008). Коэффициент сжимаемости – изменение плотности нефтей в зависимости от давления (в среднем 0, 0009 на 1 атм) Плотность нефти
 Вязкость нефти – способность оказывать сопротивление при перемещении одной части флюида относительно другой. Вязкость определяет масштабы миграции при формировании залежей и играет важную роль при добыче нефти. Единица вязкости – Стокс. Для практических целей принят санти Стокс (1 с. Ст – вязкость воды при 20 ºС). Вязкость нефти
Вязкость нефти – способность оказывать сопротивление при перемещении одной части флюида относительно другой. Вязкость определяет масштабы миграции при формировании залежей и играет важную роль при добыче нефти. Единица вязкости – Стокс. Для практических целей принят санти Стокс (1 с. Ст – вязкость воды при 20 ºС). Вязкость нефти
 Растворимость газов в жидких углеводородах и нефтях. Вязкость нефти и ее плотность в пластовых условиях зависят в первую очередь от количества растворенного в ней газа. Чем меньше плотность нефти, тем больше газа растворяется при одном и том же давлении, а, чем выше молекулярный вес газового углеводорода, тем лучше он растворим в жидких углеводородах и нефтях Растворимость газов
Растворимость газов в жидких углеводородах и нефтях. Вязкость нефти и ее плотность в пластовых условиях зависят в первую очередь от количества растворенного в ней газа. Чем меньше плотность нефти, тем больше газа растворяется при одном и том же давлении, а, чем выше молекулярный вес газового углеводорода, тем лучше он растворим в жидких углеводородах и нефтях Растворимость газов
 Нефть, за исключением высоковязких гипергенно измененных нефтей, всегда содержит в своем составе растворенные газы. Газонасыщенность или газовый фактор (ГФ) – это количество кубических метров природного газа, выделившегося в нормальных условиях при дегазации 1 м 3 или 1 т пластовой нефти. Газонасыщенность нефти растет с ростом давления и может достигать значений 600 -750 м 3/т и более. Давление насыщения пластовой нефти газом. Это давление, при котором нефть предельно насыщена газом, или давление, при снижении которого растворённый газ начинает выделяться из нефти. Газонасыщенность нефти.
Нефть, за исключением высоковязких гипергенно измененных нефтей, всегда содержит в своем составе растворенные газы. Газонасыщенность или газовый фактор (ГФ) – это количество кубических метров природного газа, выделившегося в нормальных условиях при дегазации 1 м 3 или 1 т пластовой нефти. Газонасыщенность нефти растет с ростом давления и может достигать значений 600 -750 м 3/т и более. Давление насыщения пластовой нефти газом. Это давление, при котором нефть предельно насыщена газом, или давление, при снижении которого растворённый газ начинает выделяться из нефти. Газонасыщенность нефти.
 Температура застывания и плавления. Эти параметры у различных нефтей зависят от их состава и лежат в широких пределах, от минус 35 до плюс 40 °С. Высокая температура застывания обусловливается высоким содержанием парафинов, а низкая температура – высоким содержанием смол. Температура застывания и плавления
Температура застывания и плавления. Эти параметры у различных нефтей зависят от их состава и лежат в широких пределах, от минус 35 до плюс 40 °С. Высокая температура застывания обусловливается высоким содержанием парафинов, а низкая температура – высоким содержанием смол. Температура застывания и плавления
 Это важнейшее свойство нефти. От неё зависит способность нефти перемещаться в пористых водонасыщенных пластах. С увеличением поверхностного натяжения растёт капиллярное давление. У воды поверхностное натяжение почти в три раза больше, чем у нефти, поэтому вода быстрее движется по мелким капиллярам. Молекулярные силы сцепления между водой и породами также больше, чем между нефтью и породами, поэтому вода вытесняет нефть из мелких пустот пород в более крупные. Это обусловливает возможность самостоятельной струйной миграции нефти в водонасыщенных породах по системе сообщающихся крупных пор. Сила поверхностного натяжения
Это важнейшее свойство нефти. От неё зависит способность нефти перемещаться в пористых водонасыщенных пластах. С увеличением поверхностного натяжения растёт капиллярное давление. У воды поверхностное натяжение почти в три раза больше, чем у нефти, поэтому вода быстрее движется по мелким капиллярам. Молекулярные силы сцепления между водой и породами также больше, чем между нефтью и породами, поэтому вода вытесняет нефть из мелких пустот пород в более крупные. Это обусловливает возможность самостоятельной струйной миграции нефти в водонасыщенных породах по системе сообщающихся крупных пор. Сила поверхностного натяжения
 Поверхностное натяжение – сила, с которой нефть, сопротивляется изменению своей поверхности. Удельная поверхностная энергия рассчитывается на единицу площади поверхностного слоя. У метановых углеводородов поверхностное натяжение на границе с собственным паром зависит от их молекулярного веса. Чем выше температура кипения метанового углеводорода и его плотность, тем больше его поверхностное натяжение. При том же содержании атомов углерода в молекуле для ароматических углеводородов оно заметно больше, чем у метановых. Поверхностное натяжение
Поверхностное натяжение – сила, с которой нефть, сопротивляется изменению своей поверхности. Удельная поверхностная энергия рассчитывается на единицу площади поверхностного слоя. У метановых углеводородов поверхностное натяжение на границе с собственным паром зависит от их молекулярного веса. Чем выше температура кипения метанового углеводорода и его плотность, тем больше его поверхностное натяжение. При том же содержании атомов углерода в молекуле для ароматических углеводородов оно заметно больше, чем у метановых. Поверхностное натяжение
 Оптические свойства. Нефть имеет цвет, обладает свойством вращать плоскость поляризации света, люминесцировать, преломлять проходящие световые лучи. УВ бесцветны, поэтому цвет нефти зависит от содержания в ней неуглеводородных компонентов - в основном смол и асфальтенов. Чем их больше, темнее цвет нефти. Оптические свойства
Оптические свойства. Нефть имеет цвет, обладает свойством вращать плоскость поляризации света, люминесцировать, преломлять проходящие световые лучи. УВ бесцветны, поэтому цвет нефти зависит от содержания в ней неуглеводородных компонентов - в основном смол и асфальтенов. Чем их больше, темнее цвет нефти. Оптические свойства
 Оптические свойства. Нефть является оптически активной и способна вращать плоскость поляризованного луча света, люминесцировать, преломлять проходящие лучи. Образование оптически активных веществ характерно для живого ОВ, поэтому оптическая активность нефти часто приводится в качестве доказательства органического источника нефтяных углеводородов.
Оптические свойства. Нефть является оптически активной и способна вращать плоскость поляризованного луча света, люминесцировать, преломлять проходящие лучи. Образование оптически активных веществ характерно для живого ОВ, поэтому оптическая активность нефти часто приводится в качестве доказательства органического источника нефтяных углеводородов.
 Показатель преломления нефти зависит от относительного содержания углерода и водорода в гомологических рядах и растет с увеличением числа атомов углерода. У метановых углеводородов показатель преломления варьирует от 1, 3575 до 1, 4119. Ароматические углеводороды имеют немного более высокие показатели преломления (у бензола n = 1, 5011). Показатель преломления
Показатель преломления нефти зависит от относительного содержания углерода и водорода в гомологических рядах и растет с увеличением числа атомов углерода. У метановых углеводородов показатель преломления варьирует от 1, 3575 до 1, 4119. Ароматические углеводороды имеют немного более высокие показатели преломления (у бензола n = 1, 5011). Показатель преломления
 Способность нефтей к люминесценции обусловлена, главным образом, наличием в нефти смол, асфальтенов и других люминофоров. При облучении ультрафиолетовыми лучами нефти люминесцируют по-разному в зависимости от химического состава. Легкие нефти имеют голубой и синий цвета люминесценции, а тяжелые — желтый и желто-бурый. люминесценция
Способность нефтей к люминесценции обусловлена, главным образом, наличием в нефти смол, асфальтенов и других люминофоров. При облучении ультрафиолетовыми лучами нефти люминесцируют по-разному в зависимости от химического состава. Легкие нефти имеют голубой и синий цвета люминесценции, а тяжелые — желтый и желто-бурый. люминесценция
 Температура кипения. Чем больше атомов углерода входит в состав молекул углеводородных соединений нефти, тем выше их температура кипения Углеводородов, кипящих приблизительно до 0ºС, всего 4 - это газы. От состава нефти зависит теплота сгорания (количество теплоты, выделяемое при сгорании 1 кг топлива). Температура плавления углеводородов и нефтей. У метановых углеводородов нормального строения с повышением количества атомов углерода в молекуле, заметно возрастает температура плавления. Так, температура плавления С 5 Н 12 – -130ºС, С 10 Н 22 – -30ºС, С 20 Н 42 – + 37ºС, С 30 Н 62 – + 65ºС. Температура кипения
Температура кипения. Чем больше атомов углерода входит в состав молекул углеводородных соединений нефти, тем выше их температура кипения Углеводородов, кипящих приблизительно до 0ºС, всего 4 - это газы. От состава нефти зависит теплота сгорания (количество теплоты, выделяемое при сгорании 1 кг топлива). Температура плавления углеводородов и нефтей. У метановых углеводородов нормального строения с повышением количества атомов углерода в молекуле, заметно возрастает температура плавления. Так, температура плавления С 5 Н 12 – -130ºС, С 10 Н 22 – -30ºС, С 20 Н 42 – + 37ºС, С 30 Н 62 – + 65ºС. Температура кипения
 Электрические свойства. Нефть является диэлектриком и при трении электризуется. Удельное электрическое сопротивление обезвоженной нефти равно 1010 -1014 Ом·м. Сопротивление нефтегазонасыщенных пород зависит от соотношения в пласте нефти и воды. глины имеют удельное сопротивление от 1 до 10 Ом·м, а нефтенасыщенный песчаник – от 10 -15 до 1000 Ом·м. Предельные значения электропроводности пород и минералов могут различаться в 1010 раз, то есть в 10 млрд. раз. Электрические свойства
Электрические свойства. Нефть является диэлектриком и при трении электризуется. Удельное электрическое сопротивление обезвоженной нефти равно 1010 -1014 Ом·м. Сопротивление нефтегазонасыщенных пород зависит от соотношения в пласте нефти и воды. глины имеют удельное сопротивление от 1 до 10 Ом·м, а нефтенасыщенный песчаник – от 10 -15 до 1000 Ом·м. Предельные значения электропроводности пород и минералов могут различаться в 1010 раз, то есть в 10 млрд. раз. Электрические свойства
 Элементный состав Главные элементы: Основные гетероэлементы: Микрогетероэлементы: С – 82 -87 %, Н – 12 -14 % S – до 6 -8 %, О – до 3, 6 %, N - до 1, 7 % S+О+N – от 0, 5 -2 до 8 и более % Металлы: V, Ni, Fe, Zn, Mо, Co, W, Hg, U, и др. Галогены: Cl, Br, I Неметаллы: Р, Si, Аs Всего более 70 элементов, с содержанием от 10 -1 до 10 -7 % Состав нефти (В. В. Доценко; 2007)
Элементный состав Главные элементы: Основные гетероэлементы: Микрогетероэлементы: С – 82 -87 %, Н – 12 -14 % S – до 6 -8 %, О – до 3, 6 %, N - до 1, 7 % S+О+N – от 0, 5 -2 до 8 и более % Металлы: V, Ni, Fe, Zn, Mо, Co, W, Hg, U, и др. Галогены: Cl, Br, I Неметаллы: Р, Si, Аs Всего более 70 элементов, с содержанием от 10 -1 до 10 -7 % Состав нефти (В. В. Доценко; 2007)
 Компонентный (групповой) состав (около 1300 химических соединений) Углеводородные (УВ) Неуглеводородные компоненты (около 370 химических (более 900 химических соединений): сернистые соединения (более алканы – от 10 до 70 %, 250), цикланы – от 25 до 80 %, кислородные соединения (более арены – от 10 до 25 %, иногда 70), до 50 %, азотистые соединения (более гибридные УВ – от 20 до 50 %, 50), алкены (олефины) – иногда до 8 смолы, -10 % асфальтены
Компонентный (групповой) состав (около 1300 химических соединений) Углеводородные (УВ) Неуглеводородные компоненты (около 370 химических (более 900 химических соединений): сернистые соединения (более алканы – от 10 до 70 %, 250), цикланы – от 25 до 80 %, кислородные соединения (более арены – от 10 до 25 %, иногда 70), до 50 %, азотистые соединения (более гибридные УВ – от 20 до 50 %, 50), алкены (олефины) – иногда до 8 смолы, -10 % асфальтены
 Реликтовые соединения (хемофоссилии) Углеводородные структуры: нормальные и изопреноидные алканы; полициклические изопреноидные УВ (стераны, терпаны, гопаны) Неуглеводородные структуры: металлопорфирины
Реликтовые соединения (хемофоссилии) Углеводородные структуры: нормальные и изопреноидные алканы; полициклические изопреноидные УВ (стераны, терпаны, гопаны) Неуглеводородные структуры: металлопорфирины
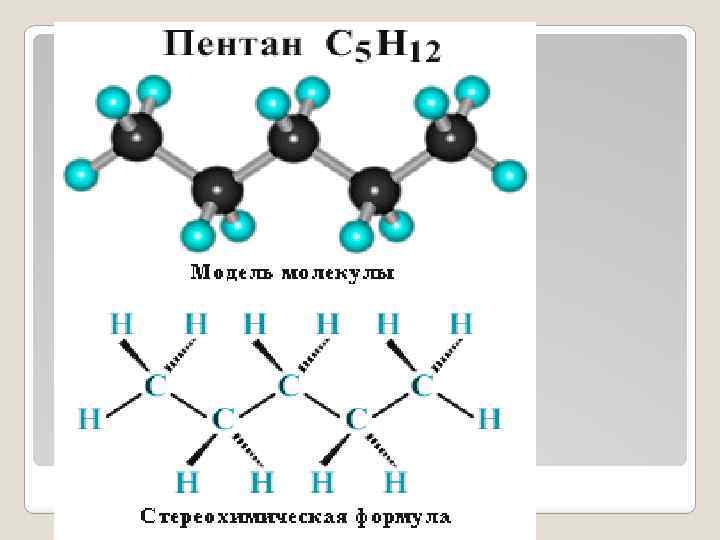
 Фракционный состав Легкие светлые фракции УВ (температура кипения (т. к. ) 35 -350 °С): бензин – УВ С 5 -С 10 (т. к. 35 -200 °С), керосин – УВ С 11 -С 13 (т. к. 200 -250 °С), газойль – УВ С 14 -С 21 (т. к. 250 -350 °С) Тяжелые темные Остаток после фракции термической или мазут обработки гудрона: (температура технический битум, кипения (т. к. ) 350 -600 кокс °С): масла соляровые - УВ С 22 -С 25, масла смазочные - УВ С 26 -С 35, гудрон или нефтяной пек - смолы, асфальтены и УВ С 36 -С 60 и более
Фракционный состав Легкие светлые фракции УВ (температура кипения (т. к. ) 35 -350 °С): бензин – УВ С 5 -С 10 (т. к. 35 -200 °С), керосин – УВ С 11 -С 13 (т. к. 200 -250 °С), газойль – УВ С 14 -С 21 (т. к. 250 -350 °С) Тяжелые темные Остаток после фракции термической или мазут обработки гудрона: (температура технический битум, кипения (т. к. ) 350 -600 кокс °С): масла соляровые - УВ С 22 -С 25, масла смазочные - УВ С 26 -С 35, гудрон или нефтяной пек - смолы, асфальтены и УВ С 36 -С 60 и более
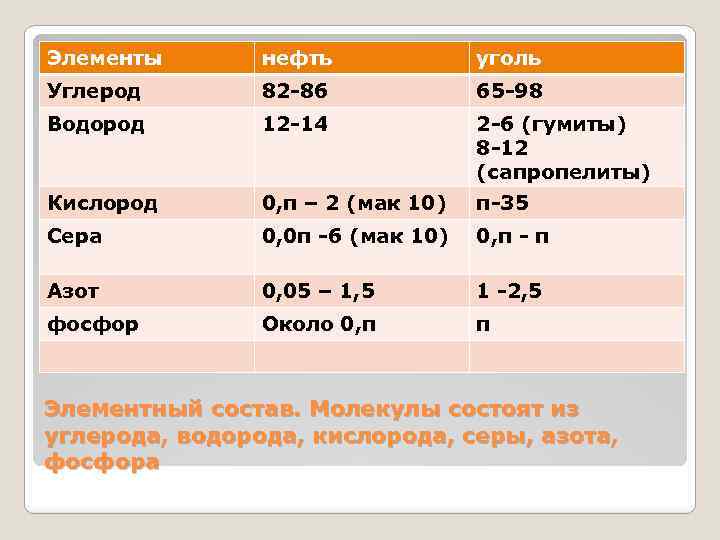 Элементы нефть уголь Углерод 82 -86 65 -98 Водород 12 -14 2 -6 (гумиты) 8 -12 (сапропелиты) Кислород 0, п – 2 (мак 10) п-35 Сера 0, 0 п -6 (мак 10) 0, п - п Азот 0, 05 – 1, 5 1 -2, 5 фосфор Около 0, п п Элементный состав. Молекулы состоят из углерода, водорода, кислорода, серы, азота, фосфора
Элементы нефть уголь Углерод 82 -86 65 -98 Водород 12 -14 2 -6 (гумиты) 8 -12 (сапропелиты) Кислород 0, п – 2 (мак 10) п-35 Сера 0, 0 п -6 (мак 10) 0, п - п Азот 0, 05 – 1, 5 1 -2, 5 фосфор Около 0, п п Элементный состав. Молекулы состоят из углерода, водорода, кислорода, серы, азота, фосфора
 Определяется при ее разделении по температурам кипения входящих соединений Метановая – 60 С Бензольная – 60 -95 Толуольная – 95 -122 Ксилольная – 122 -150 Цимольная – 150 -200 В геохимии нефти До 200 С – бензиновые 200 -300 С- керосиновые Все остальные - масляные От 200 до 350 С – керосино-газойлевые Выше 300 С – мазут Все остальное (до 550 С – гудрон) Отличаются по фракционному составу даже в пределах одной залежи Ф. С зависит от степени катагенетического преобразования нефти, условий аккумуляции и консервации нефти в залежи, связан с вторичными процессами изменения Фракционный состав нефти
Определяется при ее разделении по температурам кипения входящих соединений Метановая – 60 С Бензольная – 60 -95 Толуольная – 95 -122 Ксилольная – 122 -150 Цимольная – 150 -200 В геохимии нефти До 200 С – бензиновые 200 -300 С- керосиновые Все остальные - масляные От 200 до 350 С – керосино-газойлевые Выше 300 С – мазут Все остальное (до 550 С – гудрон) Отличаются по фракционному составу даже в пределах одной залежи Ф. С зависит от степени катагенетического преобразования нефти, условий аккумуляции и консервации нефти в залежи, связан с вторичными процессами изменения Фракционный состав нефти
 Официальная технологическая классификация нефти по их производственно-товарным признакам. По технологической классификации нефти разделяются на три класса по содержанию серы: I – малосернистые (не более 0, 5 %); II – сернистые (0, 51– 2 %); III – высокосернистые (более 2 %). По содержанию фракций, перегоняющихся до 350 ºС нефти разделяются на три типа: Т 1 – не менее 45 %; Т 2 – 30– 44, 9 %; Т 3 – менее 30 %. Классификация промышленных нефтей
Официальная технологическая классификация нефти по их производственно-товарным признакам. По технологической классификации нефти разделяются на три класса по содержанию серы: I – малосернистые (не более 0, 5 %); II – сернистые (0, 51– 2 %); III – высокосернистые (более 2 %). По содержанию фракций, перегоняющихся до 350 ºС нефти разделяются на три типа: Т 1 – не менее 45 %; Т 2 – 30– 44, 9 %; Т 3 – менее 30 %. Классификация промышленных нефтей
 По потенциальному содержанию масел выделяются четыре группы: М 1 – не менее 25 % в расчете на нефть; М 2 – 15– 25 % в расчете на нефть и не менее 45 % в расчете на мазут; М 3 – 15– 25 % в расчете на нефть и 30– 45 % в расчете на мазут; М 4 – менее 15 % в расчете на нефть. по качеству масел, оцениваемому индексом вязкости (относительная величина вязкости испытуемого масла к эталонному) на две группы: И 1 – более 86; И 2 – 40 -85. Классификация промышленных нефтей
По потенциальному содержанию масел выделяются четыре группы: М 1 – не менее 25 % в расчете на нефть; М 2 – 15– 25 % в расчете на нефть и не менее 45 % в расчете на мазут; М 3 – 15– 25 % в расчете на нефть и 30– 45 % в расчете на мазут; М 4 – менее 15 % в расчете на нефть. по качеству масел, оцениваемому индексом вязкости (относительная величина вязкости испытуемого масла к эталонному) на две группы: И 1 – более 86; И 2 – 40 -85. Классификация промышленных нефтей
 По содержанию парафина нефти делятся на: П 1 – малопарафиновые (не более 1, 5 %); П 2 – парафиновые (1, 51– 6 %); П 3 – высокопарафиновые (более 6 %). Таким образом, для любой промышленной нефти можно составить свой шифр. Например, для нефти п-ова Мангышлак) индекс нефти следующий: IТ 2 М 3 И 1 П 3. схема классификации – технологическая, определяющая пути переработки. Классификация промышленных нефтей
По содержанию парафина нефти делятся на: П 1 – малопарафиновые (не более 1, 5 %); П 2 – парафиновые (1, 51– 6 %); П 3 – высокопарафиновые (более 6 %). Таким образом, для любой промышленной нефти можно составить свой шифр. Например, для нефти п-ова Мангышлак) индекс нефти следующий: IТ 2 М 3 И 1 П 3. схема классификации – технологическая, определяющая пути переработки. Классификация промышленных нефтей
 Г. С. определяется классами, входящих в нефть углеводородов нефти в основном состоят из смеси углеводородных соединений трех групп: метановых, или парафиновых, УВ (алканы); нафтеновых УВ (цикланы) и ароматических, или бензольных, УВ (арены). В зависимости от преобладания той или иной группы УВ в составе нефтей последние делятся на метановые, нафтеновые и ароматические. Кроме того, выделяются промежуточные типы нефтей метано-нафтеновые, нафтенометано-ароматические, нафтено-ароматические и др. Асфальтены - 0 -20% (чаще 0, п – 2): Асфальтены и асфальтогеновые кислоты Смолы – 0, п – 30% (чаще 5 -20): (Часть мальтенов ) подразделяются на нейтральные, и кислые Твердые парафины – 0, 0 п – 30 (чаще 0, п -10) Групповой углеводородный состав нефти
Г. С. определяется классами, входящих в нефть углеводородов нефти в основном состоят из смеси углеводородных соединений трех групп: метановых, или парафиновых, УВ (алканы); нафтеновых УВ (цикланы) и ароматических, или бензольных, УВ (арены). В зависимости от преобладания той или иной группы УВ в составе нефтей последние делятся на метановые, нафтеновые и ароматические. Кроме того, выделяются промежуточные типы нефтей метано-нафтеновые, нафтенометано-ароматические, нафтено-ароматические и др. Асфальтены - 0 -20% (чаще 0, п – 2): Асфальтены и асфальтогеновые кислоты Смолы – 0, п – 30% (чаще 5 -20): (Часть мальтенов ) подразделяются на нейтральные, и кислые Твердые парафины – 0, 0 п – 30 (чаще 0, п -10) Групповой углеводородный состав нефти
 На основе распределения в нефтях реликтовых углеводородов – алканов нормального и изопреноидного строения. Выделено четыре типа нефтей: А 1, А 2, Б 1. Нефти типа А 1 относятся к метановым, А 2 – к метано-нафтеновым, Б 1 и Б 2 – к нафтеновым. Нефти типа А содержат нормальные алканы, в нефтях типа Б они отсутствуют. Нефти типов А 2 и Б 2 обладают относительно высокой концентрацией изопреноидных алканов. Наиболее важным свойством нефти типа А является ярко выраженная гомологичность углеводородного состава. Экспериментально доказано постадийное изменение нефтей (биодеградация) по следующей схеме: А 1 - А 2 - Б 1. Химическая классификация нефтей
На основе распределения в нефтях реликтовых углеводородов – алканов нормального и изопреноидного строения. Выделено четыре типа нефтей: А 1, А 2, Б 1. Нефти типа А 1 относятся к метановым, А 2 – к метано-нафтеновым, Б 1 и Б 2 – к нафтеновым. Нефти типа А содержат нормальные алканы, в нефтях типа Б они отсутствуют. Нефти типов А 2 и Б 2 обладают относительно высокой концентрацией изопреноидных алканов. Наиболее важным свойством нефти типа А является ярко выраженная гомологичность углеводородного состава. Экспериментально доказано постадийное изменение нефтей (биодеградация) по следующей схеме: А 1 - А 2 - Б 1. Химическая классификация нефтей
 МОЛЕКУЛЫ ациклических углеводородов содержат незамкнутые (открытые) цепи углеродных атомов, их называют также алифатическими или относящимися к жирному ряду; циклических углеводородов содержат замкнутые в цикл цепи углеродных атомов; карбоциклических углеводородов в замкнутых циклах содержат только атомы углерода; ароматических углеводородов содержат одно или несколько бензольных колец; алициклических углеводородов не содержат бензольные кольца; гетероциклических углеводородов в замкнутых циклах, помимо атомов углерода, содержат атомы других элементов (кислород, азот, сера) Классификация, номенклатура, изомерия и свойства углеводородов
МОЛЕКУЛЫ ациклических углеводородов содержат незамкнутые (открытые) цепи углеродных атомов, их называют также алифатическими или относящимися к жирному ряду; циклических углеводородов содержат замкнутые в цикл цепи углеродных атомов; карбоциклических углеводородов в замкнутых циклах содержат только атомы углерода; ароматических углеводородов содержат одно или несколько бензольных колец; алициклических углеводородов не содержат бензольные кольца; гетероциклических углеводородов в замкнутых циклах, помимо атомов углерода, содержат атомы других элементов (кислород, азот, сера) Классификация, номенклатура, изомерия и свойства углеводородов
 УГЛЕВОДОРОДЫ предельные (насыщенные): атомы углерода связаны только простыми связями; непредельные (ненасыщенные): атомы углерода, помимо простых связей, образуют одну или несколько кратных (двойных или тройных) связей. В составе нефтей наибольшее значение имеют следующие группы углеводородов: парафины или алканы - соединения с открытой цепью и с одинарными связями между атомами углерода - ациклические (алифатические); олефины или алкены с одной или двумя двойными связями между атомами углерода - ациклические (алифатические), нафтены или циклопарафины (циклоалканы) - алициклические; ароматические углеводороды или арены с одним или несколькими бензольными кольцами. УГЛЕВОДОРОДЫ
УГЛЕВОДОРОДЫ предельные (насыщенные): атомы углерода связаны только простыми связями; непредельные (ненасыщенные): атомы углерода, помимо простых связей, образуют одну или несколько кратных (двойных или тройных) связей. В составе нефтей наибольшее значение имеют следующие группы углеводородов: парафины или алканы - соединения с открытой цепью и с одинарными связями между атомами углерода - ациклические (алифатические); олефины или алкены с одной или двумя двойными связями между атомами углерода - ациклические (алифатические), нафтены или циклопарафины (циклоалканы) - алициклические; ароматические углеводороды или арены с одним или несколькими бензольными кольцами. УГЛЕВОДОРОДЫ
 Из ациклических углеводородов в состав нафтидов входят алканы и алкены. Парафины (алканы) Сn. Н 2 n+2 - углеводороды, в молекулах которых атомы углерода соединены в прямые или разветвленные цепи одинарными связями. В нефтях содержится около 60 парафиновых структур с прямой цепью, а теоретически возможно более миллиона разветвленных парафиновых структур. Алканы с числом атомов углерода от 1 до 4 - газы от 5 до 16 - жидкости свыше 16 - твердые вещества Парафины (алканы)
Из ациклических углеводородов в состав нафтидов входят алканы и алкены. Парафины (алканы) Сn. Н 2 n+2 - углеводороды, в молекулах которых атомы углерода соединены в прямые или разветвленные цепи одинарными связями. В нефтях содержится около 60 парафиновых структур с прямой цепью, а теоретически возможно более миллиона разветвленных парафиновых структур. Алканы с числом атомов углерода от 1 до 4 - газы от 5 до 16 - жидкости свыше 16 - твердые вещества Парафины (алканы)
 Гомологический ряд Корень Суффикс СН 4 мет = МЕТАН СН 3 - СН 3 эт = ЭТАН СН 3 - СН 2 - СН 3 проп +АН = ПРОПАН СН 3 - СН 2 - СН 3 бут = БУТАН. . Изомерия (примеры структурных изомеров) СН 3 - СН 2 - СН 3 н-пентан СН 3 | СН 3 - СН 2 - СН 3 2 -метилбутан, изопентан СН 3 | СН 3 - СН 3 2, 2 -диметилпропан, неопентан СН 3 Номенклатура
Гомологический ряд Корень Суффикс СН 4 мет = МЕТАН СН 3 - СН 3 эт = ЭТАН СН 3 - СН 2 - СН 3 проп +АН = ПРОПАН СН 3 - СН 2 - СН 3 бут = БУТАН. . Изомерия (примеры структурных изомеров) СН 3 - СН 2 - СН 3 н-пентан СН 3 | СН 3 - СН 2 - СН 3 2 -метилбутан, изопентан СН 3 | СН 3 - СН 3 2, 2 -диметилпропан, неопентан СН 3 Номенклатура
 Алкановые УВ, они же метановые, парафиновые, алифатические УВ или алканы (Al) соответствуют общей формуле Cn. H 2 n+2, где n – количество атомов углерода, которое может изменяться от одного до нескольких десятков. Их содержание в нефтях составляет от 10 до 70 %. Химическое строение простейших алканов – метана, этана и пропана – показывают их структурные формулы, из которых видно, что в алканах имеются два типа химических связей: С–С и С–Н. Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать с помощью электронных формул: Номенклатура
Алкановые УВ, они же метановые, парафиновые, алифатические УВ или алканы (Al) соответствуют общей формуле Cn. H 2 n+2, где n – количество атомов углерода, которое может изменяться от одного до нескольких десятков. Их содержание в нефтях составляет от 10 до 70 %. Химическое строение простейших алканов – метана, этана и пропана – показывают их структурные формулы, из которых видно, что в алканах имеются два типа химических связей: С–С и С–Н. Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать с помощью электронных формул: Номенклатура
 Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Каждая из четырех sp 3 -гибридных углерода образует s-связи С-Н или С-С.
Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Каждая из четырех sp 3 -гибридных углерода образует s-связи С-Н или С-С.
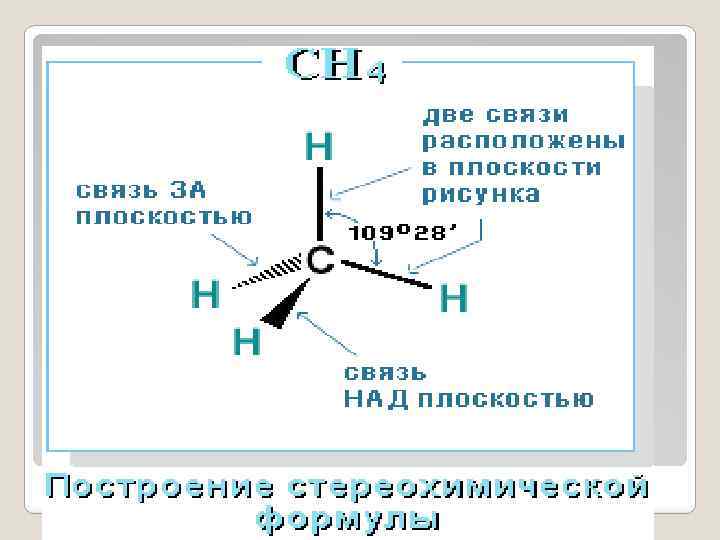
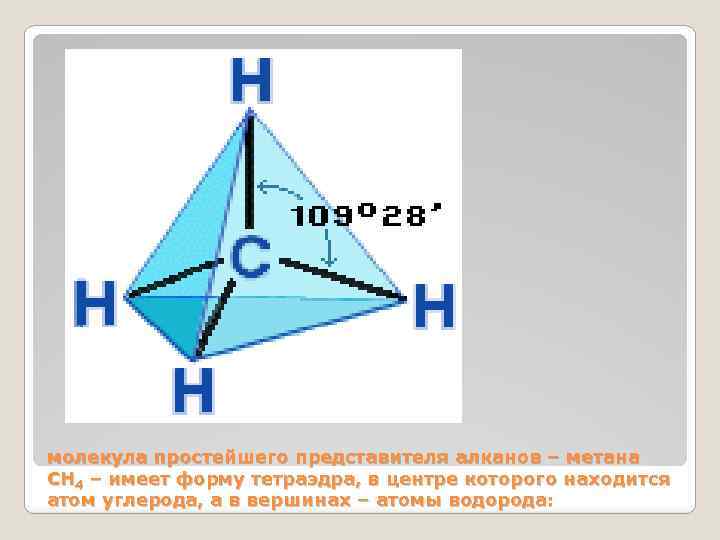 молекула простейшего представителя алканов – метана СН 4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
молекула простейшего представителя алканов – метана СН 4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
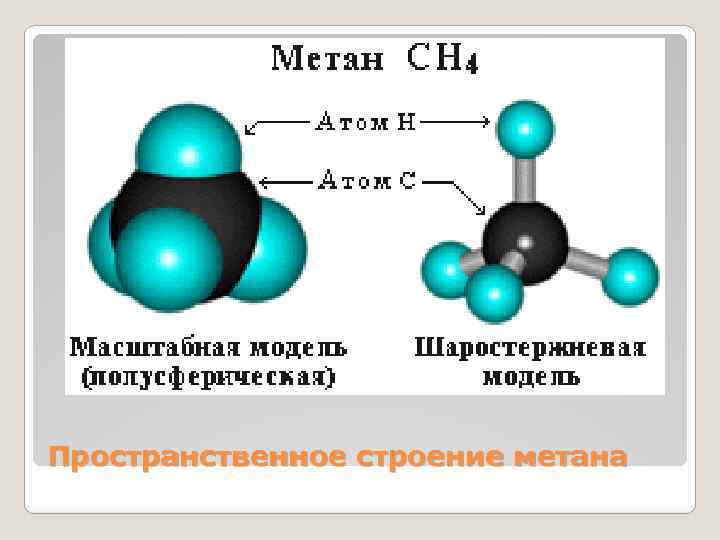 Пространственное строение метана
Пространственное строение метана
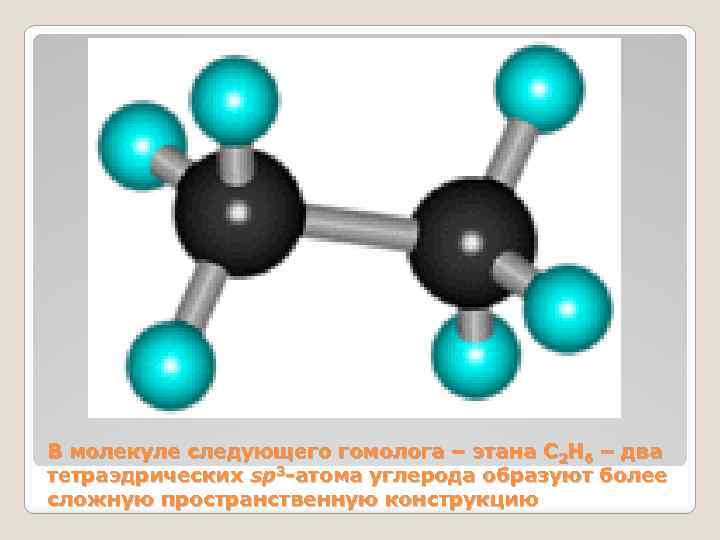 В молекуле следующего гомолога – этана С 2 Н 6 – два тетраэдрических sp 3 -атома углерода образуют более сложную пространственную конструкцию
В молекуле следующего гомолога – этана С 2 Н 6 – два тетраэдрических sp 3 -атома углерода образуют более сложную пространственную конструкцию
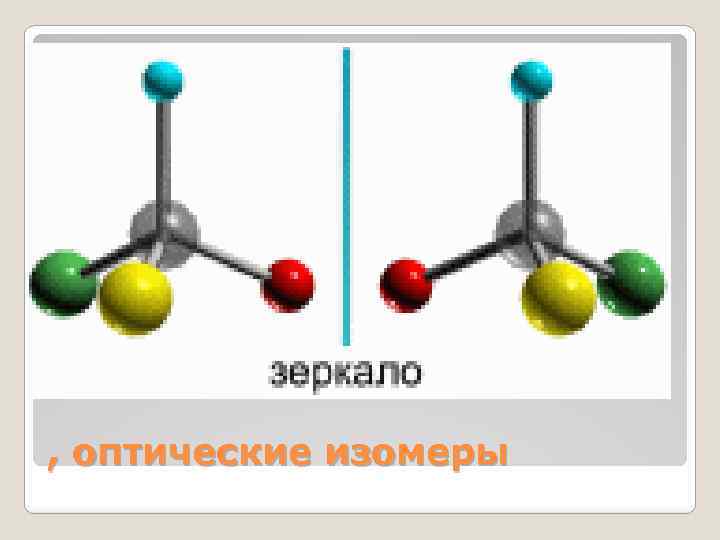 , оптические изомеры
, оптические изомеры
 Парафины с неразветвленной цепью называются нормальными парафинами, или н-парафинами (налканами), парафины с разветвленной цепью - изопарафинами или изоалканами. Число возможных изомеров (соединений с одинаковым числом атомов углерода в цепи, но обладающих боковыми цепями у различных атомов углерода) резко возрастает с увеличением числа атомов углерода. Так, для С 11 число изомеров 159, для С 13 - 802, а для С 25 - уже 36 797 588. В гомологическим ряду алканов с повышением числа атомов углерода температуры плавления и кипения возрастают. Разность в температурах кипения между алканами с n = 1 и n = 2 равна 73 С, а между алканами с n = 9 и n = 10 – 25 С, поэтому высшие алканы разделить перегонкой труднее, чем низшие. Точка кипения нормального парафина всегда несколько выше, чем любого изопарафина с тем же молекулярным весом. Алканы легче воды и не растворяются в ней, но растворяются в органических растворителях (этиловый спирт, диэтиловый эфир). Номенклатура
Парафины с неразветвленной цепью называются нормальными парафинами, или н-парафинами (налканами), парафины с разветвленной цепью - изопарафинами или изоалканами. Число возможных изомеров (соединений с одинаковым числом атомов углерода в цепи, но обладающих боковыми цепями у различных атомов углерода) резко возрастает с увеличением числа атомов углерода. Так, для С 11 число изомеров 159, для С 13 - 802, а для С 25 - уже 36 797 588. В гомологическим ряду алканов с повышением числа атомов углерода температуры плавления и кипения возрастают. Разность в температурах кипения между алканами с n = 1 и n = 2 равна 73 С, а между алканами с n = 9 и n = 10 – 25 С, поэтому высшие алканы разделить перегонкой труднее, чем низшие. Точка кипения нормального парафина всегда несколько выше, чем любого изопарафина с тем же молекулярным весом. Алканы легче воды и не растворяются в ней, но растворяются в органических растворителях (этиловый спирт, диэтиловый эфир). Номенклатура
 Олефины (алкены) Сn. H 2 n - углеводороды, молекулы которых содержат в незамкнутой углерод-углеродной цепи одну двойную связь. Алкены в небольших количествах встречаются в нефти некоторых месторождений. Многие углеводороды, которые образуются в растениях и животных, относятся к олефинам. Алкены с числом атомов углерода от 2 до 4 - газы от 5 до 15 - жидкости свыше 15 - твердые вещества Номенклатура Гомологический ряд Корень Суффикс СН 2 = СН 2 эт =ЭТЕН ЭТИЛЕН СН 3 - СН = СН 2 проп + ЕН =ПРОПЕН ПРОПИЛЕН СН 3 - СН 2 - СН = СН 2 бут =БУТЕН БУТИЛЕН
Олефины (алкены) Сn. H 2 n - углеводороды, молекулы которых содержат в незамкнутой углерод-углеродной цепи одну двойную связь. Алкены в небольших количествах встречаются в нефти некоторых месторождений. Многие углеводороды, которые образуются в растениях и животных, относятся к олефинам. Алкены с числом атомов углерода от 2 до 4 - газы от 5 до 15 - жидкости свыше 15 - твердые вещества Номенклатура Гомологический ряд Корень Суффикс СН 2 = СН 2 эт =ЭТЕН ЭТИЛЕН СН 3 - СН = СН 2 проп + ЕН =ПРОПЕН ПРОПИЛЕН СН 3 - СН 2 - СН = СН 2 бут =БУТЕН БУТИЛЕН
 СН 3 - СН 2 - СН = Н 2 бутен-1, бутилен СН 3 - С = СН 2 2 -метилпропен, изобутилен СН 3 - СН = СН - СН 3 бутен-2, ? -бутилен Алкены имеют несколько более низкие температуры плавления и кипения, чем соответствующие им алканы. Алкены обладают намного большей реакционной способностью, чем алканы. Это во многом объясняет то, что в нефти олефины встречаются лишь в виде следов. Они быстро восстанавливаются или полимеризуются с образованием парафинов. Изомерия (примеры структурных изомеров)
СН 3 - СН 2 - СН = Н 2 бутен-1, бутилен СН 3 - С = СН 2 2 -метилпропен, изобутилен СН 3 - СН = СН - СН 3 бутен-2, ? -бутилен Алкены имеют несколько более низкие температуры плавления и кипения, чем соответствующие им алканы. Алкены обладают намного большей реакционной способностью, чем алканы. Это во многом объясняет то, что в нефти олефины встречаются лишь в виде следов. Они быстро восстанавливаются или полимеризуются с образованием парафинов. Изомерия (примеры структурных изомеров)
 Алициклические Ароматические Циклоалканы Циклоалкены Из карбоциклических углеводородов в составе нафтидов распространены циклоалканы - алициклические углеводороды и ароматические углеводороды. Нафтены (циклоалканы или циклопарафины) Cn. H 2 n (моноциклические), Cn. H 2 n-2 (бициклические), Cn. H 2 n-4 (трициклические) - углеводороды, молекулы которых содержат один или несколько циклов (нафтеновых колец), состоящих из атомов углерода. Карбоциклические углеводороды
Алициклические Ароматические Циклоалканы Циклоалкены Из карбоциклических углеводородов в составе нафтидов распространены циклоалканы - алициклические углеводороды и ароматические углеводороды. Нафтены (циклоалканы или циклопарафины) Cn. H 2 n (моноциклические), Cn. H 2 n-2 (бициклические), Cn. H 2 n-4 (трициклические) - углеводороды, молекулы которых содержат один или несколько циклов (нафтеновых колец), состоящих из атомов углерода. Карбоциклические углеводороды
 Нафтеновые УВ, циклановые, циклоалкановые, циклопарафиновые, полиметиленовые УВ или нафтены (Nf) состоят из замкнутых в цикл метиленовых групп СН 2. Атомы углерода в циклоалканах, как и в алканах, находятся в sp 3– гибридизованном состоянии и все их валентности полностью насыщены. Нафтеновые УВ
Нафтеновые УВ, циклановые, циклоалкановые, циклопарафиновые, полиметиленовые УВ или нафтены (Nf) состоят из замкнутых в цикл метиленовых групп СН 2. Атомы углерода в циклоалканах, как и в алканах, находятся в sp 3– гибридизованном состоянии и все их валентности полностью насыщены. Нафтеновые УВ
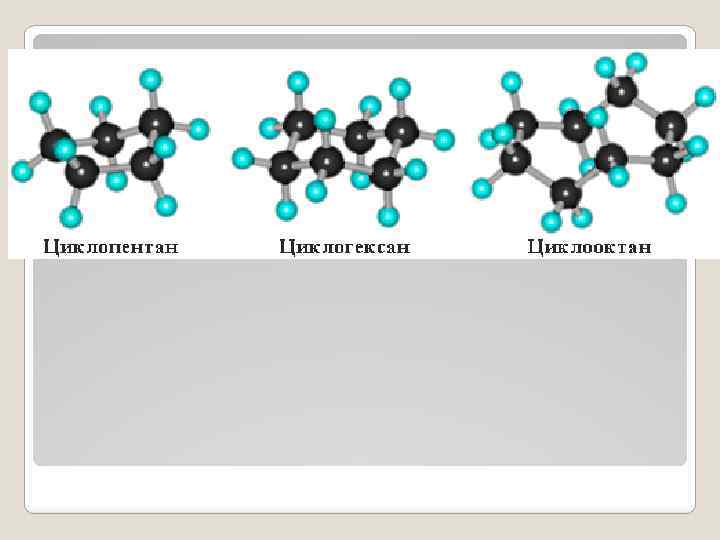
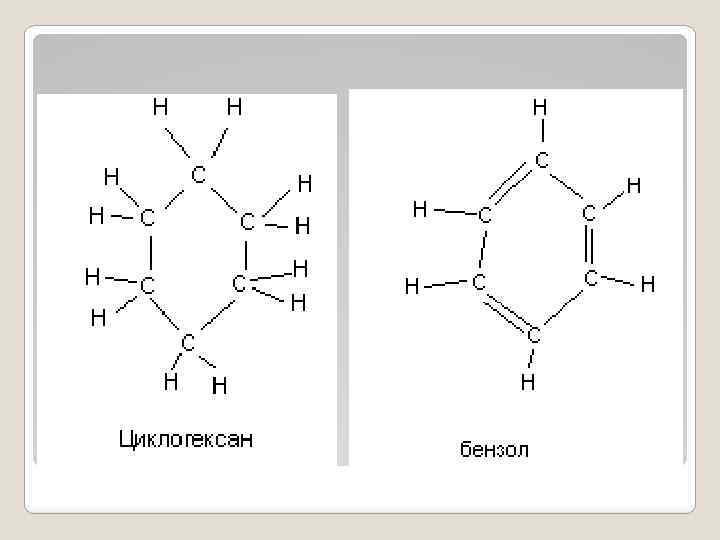
 Нафтены (циклоалканы или циклопарафины) наиболее распространены в нефтях. В среднем в составе нефти на долю нафтенов приходится до 50%. Нафтены состоят из нескольких групп -СН 2 -, соединенных в замкнутую систему. Для нефти характерны нафтены с кольцами, содержащими 5 или 6 атомов углерода. В кольце с 5 атомами все атомы С лежат в одной плоскости. Кольца с 6 углеродными атомами имеют конфигурацию складки. Как и парафины, нафтены являются насыщенными углеводородами (в них все углеродные связи насыщены водородом). Наиболее распространенные нафтены - циклопентан и циклогексан, которые обычно составляют в нефти более 2 %. Нафтены (циклоалканы циклопарафины) или
Нафтены (циклоалканы или циклопарафины) наиболее распространены в нефтях. В среднем в составе нефти на долю нафтенов приходится до 50%. Нафтены состоят из нескольких групп -СН 2 -, соединенных в замкнутую систему. Для нефти характерны нафтены с кольцами, содержащими 5 или 6 атомов углерода. В кольце с 5 атомами все атомы С лежат в одной плоскости. Кольца с 6 углеродными атомами имеют конфигурацию складки. Как и парафины, нафтены являются насыщенными углеводородами (в них все углеродные связи насыщены водородом). Наиболее распространенные нафтены - циклопентан и циклогексан, которые обычно составляют в нефти более 2 %. Нафтены (циклоалканы циклопарафины) или
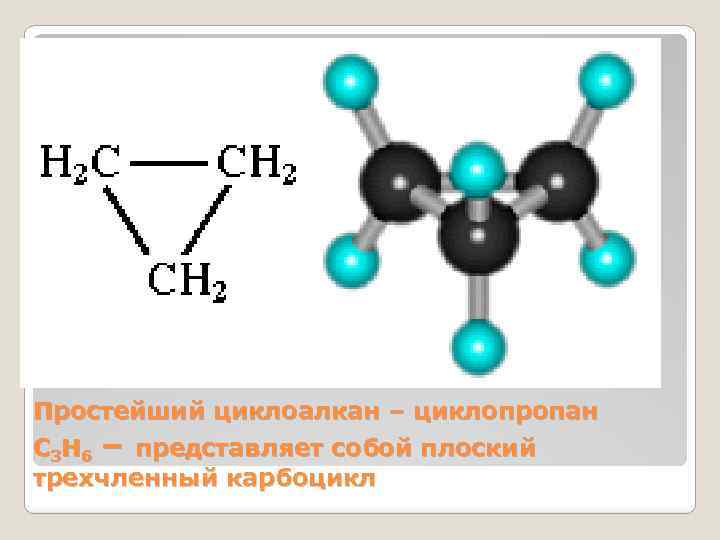 Простейший циклоалкан – циклопpопан С 3 Н 6 – представляет собой плоский трехчленный карбоцикл
Простейший циклоалкан – циклопpопан С 3 Н 6 – представляет собой плоский трехчленный карбоцикл
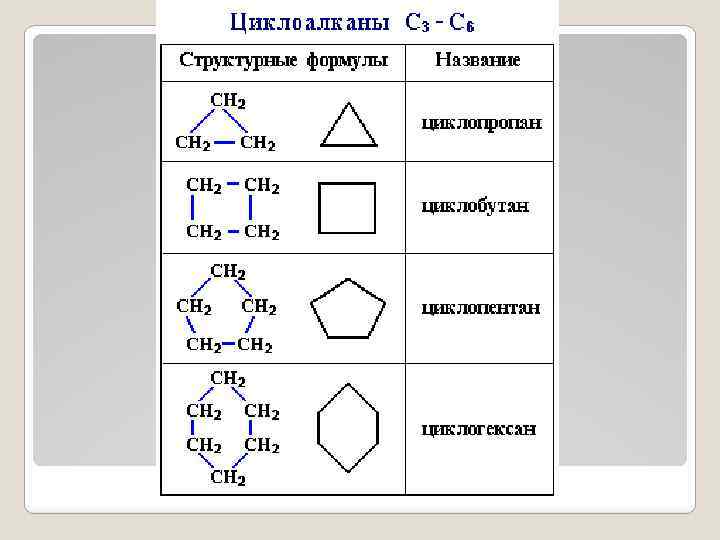
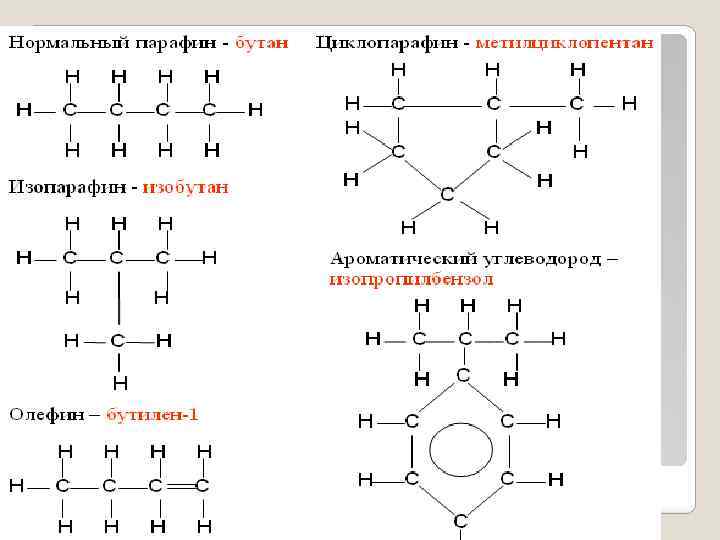
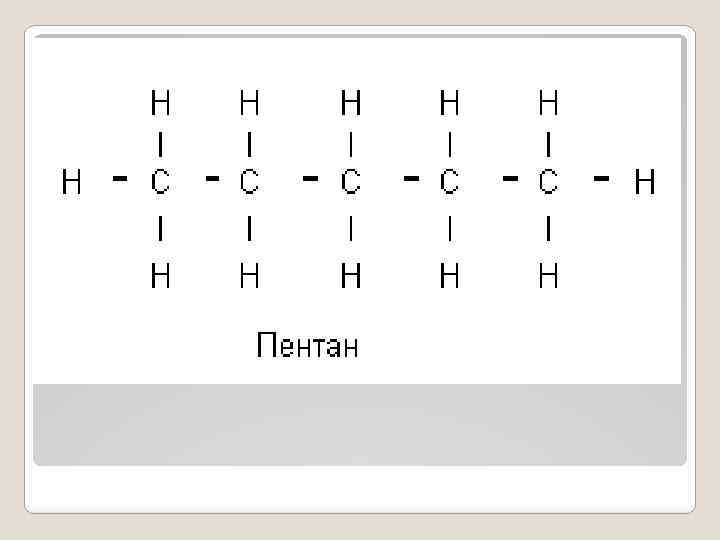
 Атом водорода в структуре может быть замещен на какой-либо углеводородный радикал - метил (СН 3), этил (С 2 Н 5) и др. В этом случае получаются производные циклопентана и циклогексана (метилциклопентан, этилциклопентан и др. ). Цикланы с числом атомов углерода от 3 до 4 - газы от 5 до 7 - жидкости свыше 8 - твердые вещества Номенклатура Гомологический ряд Префикс Корень Суффикс С 3 Н 6 проп =ЦИКЛОПРОПАН С 4 Н 8 ЦИКЛО бут + АН =ЦИКЛОБУТАН С 5 Н 10 пент =ЦИКЛОПЕНТАН. . . . Циклоалканы имеют более высокие температуры кипения и плавления, чем нециклические алканы с тем же числом атомов углерода. Они не растворяются в воде, но растворяются в неполярных органических растворителях. Цикланы
Атом водорода в структуре может быть замещен на какой-либо углеводородный радикал - метил (СН 3), этил (С 2 Н 5) и др. В этом случае получаются производные циклопентана и циклогексана (метилциклопентан, этилциклопентан и др. ). Цикланы с числом атомов углерода от 3 до 4 - газы от 5 до 7 - жидкости свыше 8 - твердые вещества Номенклатура Гомологический ряд Префикс Корень Суффикс С 3 Н 6 проп =ЦИКЛОПРОПАН С 4 Н 8 ЦИКЛО бут + АН =ЦИКЛОБУТАН С 5 Н 10 пент =ЦИКЛОПЕНТАН. . . . Циклоалканы имеют более высокие температуры кипения и плавления, чем нециклические алканы с тем же числом атомов углерода. Они не растворяются в воде, но растворяются в неполярных органических растворителях. Цикланы
 Одноядерные Многоядерные (моноциклические) (полициклические) Ароматические углеводороды (арены) Cn. H 2 n-6 (моноциклические), Cn. H 2 n-12, Cn. Н 2 n-14 (бициклические), Cn. H 2 n-16, Cn. H 2 n-18 (трициклические) - углеводороды, молекулы которых содержат одно или несколько бензольных колец. Это плоское кольцо с 6 атомами углеводорода, в котором 4 -я связь каждого атома делится на все кольцо. Ароматические углеводороды - ненасыщенные. К ароматическим относятся и гибридные углеводороды, содержащие как ароматические ядра, так и циклы. Название «ароматические» - историческое, ибо именно из природных ароматических масел впервые были выделены эти приятно пахнущие соединения, например цимол. Ароматические углеводороды
Одноядерные Многоядерные (моноциклические) (полициклические) Ароматические углеводороды (арены) Cn. H 2 n-6 (моноциклические), Cn. H 2 n-12, Cn. Н 2 n-14 (бициклические), Cn. H 2 n-16, Cn. H 2 n-18 (трициклические) - углеводороды, молекулы которых содержат одно или несколько бензольных колец. Это плоское кольцо с 6 атомами углеводорода, в котором 4 -я связь каждого атома делится на все кольцо. Ароматические углеводороды - ненасыщенные. К ароматическим относятся и гибридные углеводороды, содержащие как ароматические ядра, так и циклы. Название «ароматические» - историческое, ибо именно из природных ароматических масел впервые были выделены эти приятно пахнущие соединения, например цимол. Ароматические углеводороды
 Содержание ароматических углеводородов в «средней» нефти составляет примерно 15 %. Они концентрируются преимущественно в тяжелых фракциях нефти, где их часто более 50 %. Наиболее распространенные ароматические углеводороды в нефти - толуол и метаксилен. Ароматические углеводороды имеют высокие октановые числа, поэтому они являются ценными компонентами для бензинов. Ароматические углеводороды
Содержание ароматических углеводородов в «средней» нефти составляет примерно 15 %. Они концентрируются преимущественно в тяжелых фракциях нефти, где их часто более 50 %. Наиболее распространенные ароматические углеводороды в нефти - толуол и метаксилен. Ароматические углеводороды имеют высокие октановые числа, поэтому они являются ценными компонентами для бензинов. Ароматические углеводороды
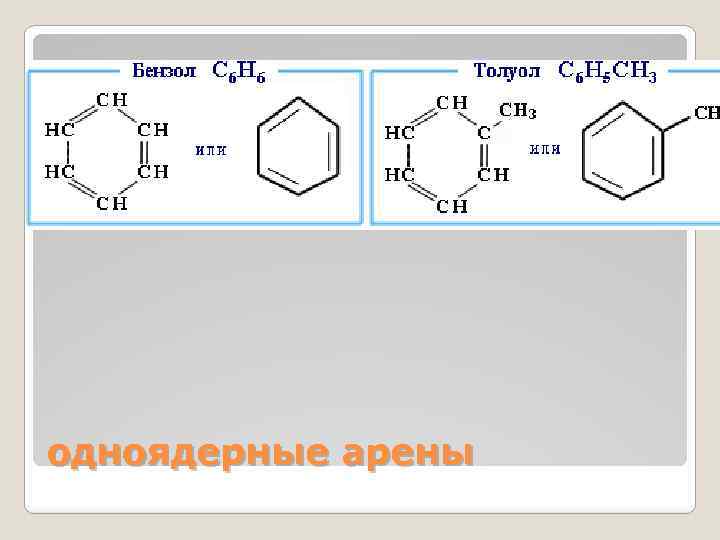 одноядерные арены
одноядерные арены
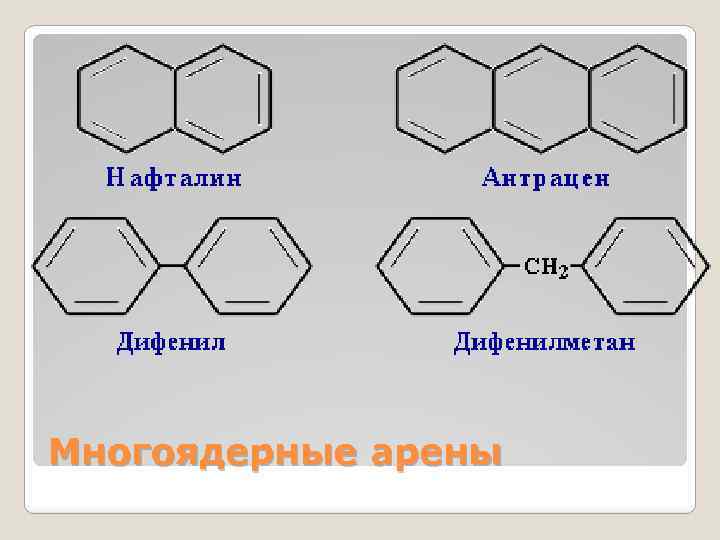 Многоядерные арены
Многоядерные арены
 Модели молекулы бензола
Модели молекулы бензола
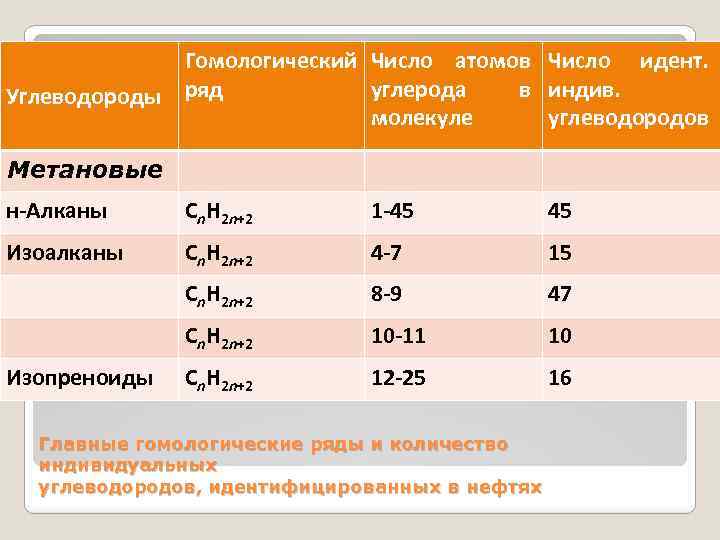 Гомологический Число атомов Число идент. углерода в индив. Углеводороды ряд молекуле углеводородов Метановые н-Алканы Сn. H 2 n+2 1 -45 45 Изоалканы Cn. H 2 n+2 4 -7 15 Cn. H 2 n+2 8 -9 47 Сn. H 2 n+2 10 -11 10 Изопреноиды Cn. H 2 n+2 12 -25 16 Главные гомологические ряды и количество индивидуальных углеводородов, идентифицированных в нефтях
Гомологический Число атомов Число идент. углерода в индив. Углеводороды ряд молекуле углеводородов Метановые н-Алканы Сn. H 2 n+2 1 -45 45 Изоалканы Cn. H 2 n+2 4 -7 15 Cn. H 2 n+2 8 -9 47 Сn. H 2 n+2 10 -11 10 Изопреноиды Cn. H 2 n+2 12 -25 16 Главные гомологические ряды и количество индивидуальных углеводородов, идентифицированных в нефтях
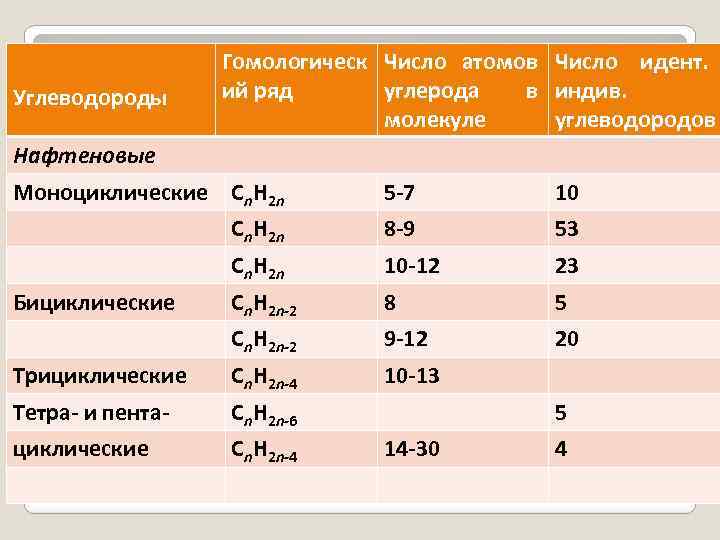 Углеводороды Гомологическ Число атомов Число идент. ий ряд углерода в индив. молекуле углеводородов Нафтеновые Моноциклические Cn. H 2 n 5 -7 10 Cn. H 2 n 8 -9 53 Cn. H 2 n 10 -12 23 Бициклические Cn. H 2 n-2 8 5 Cn. H 2 n-2 9 -12 20 Трициклические Cn. H 2 n-4 10 -13 Тетра- и пента- Cn. H 2 n-6 5 циклические Cn. H 2 n-4 14 -30 4
Углеводороды Гомологическ Число атомов Число идент. ий ряд углерода в индив. молекуле углеводородов Нафтеновые Моноциклические Cn. H 2 n 5 -7 10 Cn. H 2 n 8 -9 53 Cn. H 2 n 10 -12 23 Бициклические Cn. H 2 n-2 8 5 Cn. H 2 n-2 9 -12 20 Трициклические Cn. H 2 n-4 10 -13 Тетра- и пента- Cn. H 2 n-6 5 циклические Cn. H 2 n-4 14 -30 4
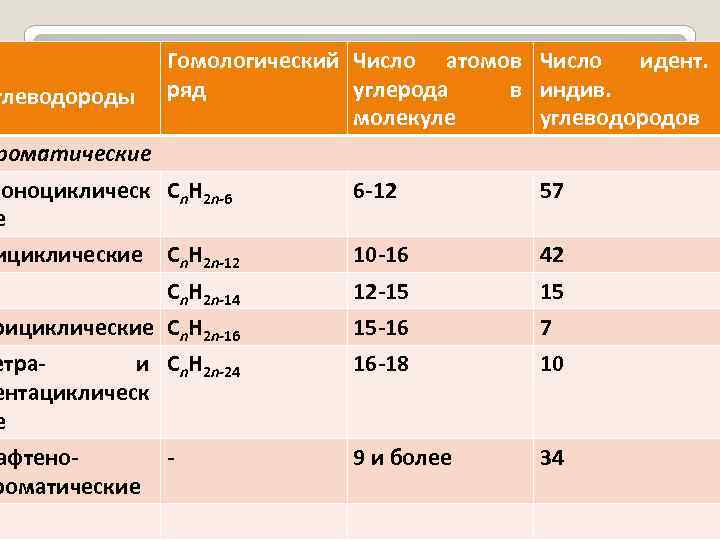 глеводороды Гомологический Число атомов Число идент. ряд углерода в индив. молекуле углеводородов роматические Моноциклическ Cn. H 2 n-6 е 6 -12 57 Cn. H 2 n-12 10 -16 42 Cn. H 2 n-14 12 -15 15 рициклические Cn. H 2 n-16 15 -16 7 етра- и Cn. H 2 n-24 ентациклическ е 16 -18 10 афтенороматические 9 и более 34 ициклические -
глеводороды Гомологический Число атомов Число идент. ряд углерода в индив. молекуле углеводородов роматические Моноциклическ Cn. H 2 n-6 е 6 -12 57 Cn. H 2 n-12 10 -16 42 Cn. H 2 n-14 12 -15 15 рициклические Cn. H 2 n-16 15 -16 7 етра- и Cn. H 2 n-24 ентациклическ е 16 -18 10 афтенороматические 9 и более 34 ициклические -
 Группа соединений, имеющая неуглеводородную природу. Количество неуглеводородных соединений, как правило, возрастает от легких нефтей к тяжелым. сложные высокомолекулярные соединения, содержащие кроме углерода и водорода такие элементы, как кислород, сера, азот и некоторые металлы. Относятся к разряду так называемых смолисто-асфальтовых компонентов нефти. конденсированные циклические структуры, в состав которых входят ароматические и нафтеновые кольца с боковыми цепями и гетероатомами (кислородом, азотом, серой и др. ). Отдельные конденсированные кольца соединяются между собой простыми цепочками или гетероатомами. К гетеросоединениям относятся порфирины - тетрациклические азотистые соединения. Генетически они связаны с пигментами живого вещества, в рассеянном органическом веществе (РОВ ) осадочных пород присутствуют в форме металлокомплексов ванадия и никеля. Азот, серо- и кислородо- содержащие соединения (гетеросоединения)
Группа соединений, имеющая неуглеводородную природу. Количество неуглеводородных соединений, как правило, возрастает от легких нефтей к тяжелым. сложные высокомолекулярные соединения, содержащие кроме углерода и водорода такие элементы, как кислород, сера, азот и некоторые металлы. Относятся к разряду так называемых смолисто-асфальтовых компонентов нефти. конденсированные циклические структуры, в состав которых входят ароматические и нафтеновые кольца с боковыми цепями и гетероатомами (кислородом, азотом, серой и др. ). Отдельные конденсированные кольца соединяются между собой простыми цепочками или гетероатомами. К гетеросоединениям относятся порфирины - тетрациклические азотистые соединения. Генетически они связаны с пигментами живого вещества, в рассеянном органическом веществе (РОВ ) осадочных пород присутствуют в форме металлокомплексов ванадия и никеля. Азот, серо- и кислородо- содержащие соединения (гетеросоединения)
 Неуглеводородные компоненты нефти производные углеводородов и разделяются на две группы. В первую группу входят гетероорганические соединения, которые описываются точной химической формулой. Называются по содержащемуся или преобладающему гетероатому представлены сернистыми, кислородными и азотистыми соединениями. Неуглеводородные компоненты
Неуглеводородные компоненты нефти производные углеводородов и разделяются на две группы. В первую группу входят гетероорганические соединения, которые описываются точной химической формулой. Называются по содержащемуся или преобладающему гетероатому представлены сернистыми, кислородными и азотистыми соединениями. Неуглеводородные компоненты
 Во вторую группу веществ входят высокомолекулярные соединения, со сложной структурой представлена смолами и асфальтенами или смолистоасфальтеновыми веществами (САВ). Смолы и асфальтены - это высокомолекулярные конденсированные циклические структуры, которые содержат гетероатомы и боковые алкильные цепи, состоящие из одновалентных радикалов: метила (СН 3), этила (С 2 Н 5), пропила (С 3 Н 7) и других. Смолы имеют молекулярную массу от 500 до 2000 единиц и обладают хорошей растворимостью в органических растворителях и УВ. Асфальтены –продукты конденсации нескольких молекул смол, поэтому они являются твердыми веществами с кристаллоподобной структурой и не растворяются в алканах. Их молекулярная масса лежит в пределах от 1000 -5000 до 10000 единиц (до сотен тысяч и даже миллионов единиц).
Во вторую группу веществ входят высокомолекулярные соединения, со сложной структурой представлена смолами и асфальтенами или смолистоасфальтеновыми веществами (САВ). Смолы и асфальтены - это высокомолекулярные конденсированные циклические структуры, которые содержат гетероатомы и боковые алкильные цепи, состоящие из одновалентных радикалов: метила (СН 3), этила (С 2 Н 5), пропила (С 3 Н 7) и других. Смолы имеют молекулярную массу от 500 до 2000 единиц и обладают хорошей растворимостью в органических растворителях и УВ. Асфальтены –продукты конденсации нескольких молекул смол, поэтому они являются твердыми веществами с кристаллоподобной структурой и не растворяются в алканах. Их молекулярная масса лежит в пределах от 1000 -5000 до 10000 единиц (до сотен тысяч и даже миллионов единиц).
 Сернистые соединения. более 250 индивидуальных органических и неорганических соединений, содержащих серу. Неорганические соединения представлены элементной серой – S и сероводородом - H 2 S. Основное количество серы, от 70 до 90 %, связано со смолами и асфальтенами. Пределы изменения концентраций серы в элементном составе нефтей очень широки: от сотых долей процента до 6 -8 %, и более. Сернистые компоненты нефтей разделяются на агрессивные и неагрессивные соединения. Присутствие агрессивных соединений весьма нежелательно, так как они активно корродируют металлы, являются сильнейшими каталитическими ядами, экологически опасны и придают нефти неприятный запах. Агрессивная сера представлена органическими и неорганическими соединениями, которые обладают кислотными свойствами. К ним относятся: элементная сера - S, сероводород - H 2 S, и меркаптаны - тиолы и тиофенолы. К неагрессивным сернистым соединениям относятся сульфиды, дисульфиды, тиофан, тиофен и тиопиран – С 5 Н 10 S. Сернистые соединения.
Сернистые соединения. более 250 индивидуальных органических и неорганических соединений, содержащих серу. Неорганические соединения представлены элементной серой – S и сероводородом - H 2 S. Основное количество серы, от 70 до 90 %, связано со смолами и асфальтенами. Пределы изменения концентраций серы в элементном составе нефтей очень широки: от сотых долей процента до 6 -8 %, и более. Сернистые компоненты нефтей разделяются на агрессивные и неагрессивные соединения. Присутствие агрессивных соединений весьма нежелательно, так как они активно корродируют металлы, являются сильнейшими каталитическими ядами, экологически опасны и придают нефти неприятный запах. Агрессивная сера представлена органическими и неорганическими соединениями, которые обладают кислотными свойствами. К ним относятся: элементная сера - S, сероводород - H 2 S, и меркаптаны - тиолы и тиофенолы. К неагрессивным сернистым соединениям относятся сульфиды, дисульфиды, тиофан, тиофен и тиопиран – С 5 Н 10 S. Сернистые соединения.
 Кислородные компоненты нефтей представлены 70 индивидуальными соединениями кислого и нейтрального характера, которые содержат кислород в виде различных функциональных групп: гидроксила (-ОН), карбоксила (СООН), карбонила (>СО), метоксила (ОСН 3), оксигрупы (=О), пероксигруппы (-О-О-) и других. Кислород содержится в нефти в элементном составе в количестве от 0, 05 до 3, 6 %, что соответствует примерно от 0, 5 до 36 % кислородных соединений. Соединения кислого характера представлены кислотами и фенолами. Кислоты имеют различное строение: алифатическое (Аl-СООН), нафтеновое (Nf. СООН или Nf-(СН 2)n-СООН), в том числе и стероидное строение, а также ароматическое и гибридное строение. Кроме фенола С 6 Н 5 ОН в нефтях присутствуют его гомологи, содержащие до шести конденсированных колец. Кислородные соединения нейтрального характера представлены спиртами, алифатическими и циклическими кетонами и пероксидами. Кислородные компоненты нефтей
Кислородные компоненты нефтей представлены 70 индивидуальными соединениями кислого и нейтрального характера, которые содержат кислород в виде различных функциональных групп: гидроксила (-ОН), карбоксила (СООН), карбонила (>СО), метоксила (ОСН 3), оксигрупы (=О), пероксигруппы (-О-О-) и других. Кислород содержится в нефти в элементном составе в количестве от 0, 05 до 3, 6 %, что соответствует примерно от 0, 5 до 36 % кислородных соединений. Соединения кислого характера представлены кислотами и фенолами. Кислоты имеют различное строение: алифатическое (Аl-СООН), нафтеновое (Nf. СООН или Nf-(СН 2)n-СООН), в том числе и стероидное строение, а также ароматическое и гибридное строение. Кроме фенола С 6 Н 5 ОН в нефтях присутствуют его гомологи, содержащие до шести конденсированных колец. Кислородные соединения нейтрального характера представлены спиртами, алифатическими и циклическими кетонами и пероксидами. Кислородные компоненты нефтей
 Азотистые компоненты нефтей составляют более 50 индивидуальных соединений, которые разделяются на три группы. Первая группа - азотистые основания, которые реагируют с кислотами, образуя органические соли, поэтому сравнительно легко выделяются из нефти. Представлены они ароматическими гетероциклами: пиридином (С 5 Н 5 N), анилином (С 6 Н 5 NН 2), хинолином (С 9 Н 7 N), акридиномом (С 13 Н 9 N) и их гомологами. Вторая группа - нейтральные соединения, которые представлены ароматическими гетероциклами: пирролом (С 4 Н 4 NН), индолом (С 8 Н 6 NН), карбазолом (С 12 Н 8 NН) бензокарбазолом (С 16 Н 10 NН), а также их гомологами и производными. Третья группа - порфирины, которые представляют собой сложные циклические металлоорганические азотсодержащие соединения. Содержание азотистых соединений обычно не превышает нескольких процентов , а концентрация азота в элементном составе нефти находится в пределах от 0, 01 до 1, 7 %. Азотистые компоненты нефтей
Азотистые компоненты нефтей составляют более 50 индивидуальных соединений, которые разделяются на три группы. Первая группа - азотистые основания, которые реагируют с кислотами, образуя органические соли, поэтому сравнительно легко выделяются из нефти. Представлены они ароматическими гетероциклами: пиридином (С 5 Н 5 N), анилином (С 6 Н 5 NН 2), хинолином (С 9 Н 7 N), акридиномом (С 13 Н 9 N) и их гомологами. Вторая группа - нейтральные соединения, которые представлены ароматическими гетероциклами: пирролом (С 4 Н 4 NН), индолом (С 8 Н 6 NН), карбазолом (С 12 Н 8 NН) бензокарбазолом (С 16 Н 10 NН), а также их гомологами и производными. Третья группа - порфирины, которые представляют собой сложные циклические металлоорганические азотсодержащие соединения. Содержание азотистых соединений обычно не превышает нескольких процентов , а концентрация азота в элементном составе нефти находится в пределах от 0, 01 до 1, 7 %. Азотистые компоненты нефтей
 Реликтовые соединения или хемофоссилии. особая группа веществ, которые одновременно присутствуют в углеводородном и в неуглеводородном составе нефтей, а также в ОВ осадочных пород. Реликтовые химические соединения по своей структуре близки к некоторым биологическим веществам или их фрагментам: стероидам, терпенам и терпеноидам, порфиринам (хлорофилл, гемоглобин крови), аминокислотам и другим. Хемофоссилии
Реликтовые соединения или хемофоссилии. особая группа веществ, которые одновременно присутствуют в углеводородном и в неуглеводородном составе нефтей, а также в ОВ осадочных пород. Реликтовые химические соединения по своей структуре близки к некоторым биологическим веществам или их фрагментам: стероидам, терпенам и терпеноидам, порфиринам (хлорофилл, гемоглобин крови), аминокислотам и другим. Хемофоссилии
 Хемофоссилии устойчивые соединения почти в неизменном виде поступают в осадки из химических остатков организмов, сохраняются при литогенезе и переходят в состав нефтей. В ходе литогенеза в строении происходит небольшая перестройка углеродной структуры молекул и потеря функциональных групп. хемофоссилии несут информацию об условиях образования и преобразования нефтематеринского ОВ и заключающих их осадков и горных пород. Из УВ к хемофоссилиям относятся высокомолекулярные нормальные и изопреноидные алканы, а также полициклические нафтены, а из неуглеводородных компонентов нефти - порфирины, амиды кислот. Хемофоссилии
Хемофоссилии устойчивые соединения почти в неизменном виде поступают в осадки из химических остатков организмов, сохраняются при литогенезе и переходят в состав нефтей. В ходе литогенеза в строении происходит небольшая перестройка углеродной структуры молекул и потеря функциональных групп. хемофоссилии несут информацию об условиях образования и преобразования нефтематеринского ОВ и заключающих их осадков и горных пород. Из УВ к хемофоссилиям относятся высокомолекулярные нормальные и изопреноидные алканы, а также полициклические нафтены, а из неуглеводородных компонентов нефти - порфирины, амиды кислот. Хемофоссилии
 Н. Б. Вассоевич и В. Н. Муратов исходя из представления о ведущей роли углерода в составе горючих ископаемых предложили новую классификацию каустобиолитов и назвали их карботенами. В этом случае генетический принцип (их происхождение) игнорируется, так к карботенам относятся органические соединения как органического, так и неорганического происхождения; они могут быть горючими и негорючими и т. д. Для природных ископаемых угольного и нефтяного рядов соответственно предложены термины карбониты и нафтониты. Нафтиды объединяют все разновидности нефтей и продукты их преобразования в природных условиях; нафтоиды представляют собой нефтеподобные вещества, не связанные генетически с нефтью и образующиеся в результате термической деструкции 0 В под влиянием высокой температуры магмы. Нафтиды включают магманафтоиды - углеводороды, которые встречаются в магме.
Н. Б. Вассоевич и В. Н. Муратов исходя из представления о ведущей роли углерода в составе горючих ископаемых предложили новую классификацию каустобиолитов и назвали их карботенами. В этом случае генетический принцип (их происхождение) игнорируется, так к карботенам относятся органические соединения как органического, так и неорганического происхождения; они могут быть горючими и негорючими и т. д. Для природных ископаемых угольного и нефтяного рядов соответственно предложены термины карбониты и нафтониты. Нафтиды объединяют все разновидности нефтей и продукты их преобразования в природных условиях; нафтоиды представляют собой нефтеподобные вещества, не связанные генетически с нефтью и образующиеся в результате термической деструкции 0 В под влиянием высокой температуры магмы. Нафтиды включают магманафтоиды - углеводороды, которые встречаются в магме.
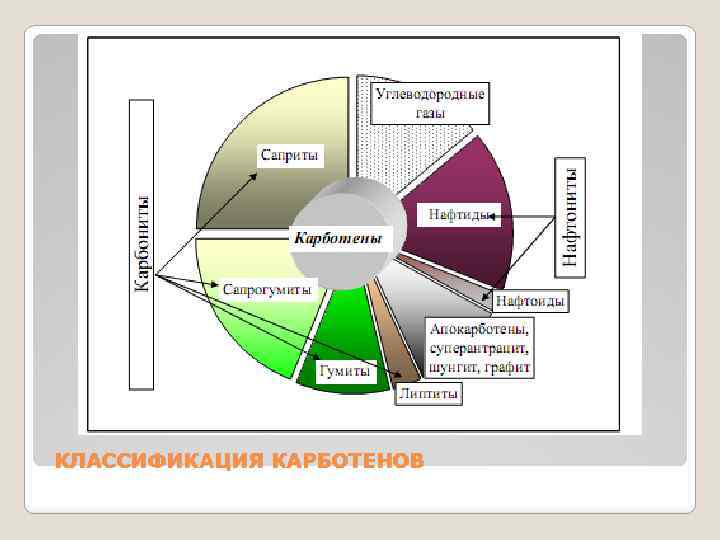 КЛАССИФИКАЦИЯ КАРБОТЕНОВ
КЛАССИФИКАЦИЯ КАРБОТЕНОВ
 Природные газы – это смеси веществ, находящиеся в нормальных условиях в газообразном состоянии и газы, выделяющиеся из состава природных систем иного агрегатного состояния, например: пластовых вод и нефтей, газовых гидратов, которые находятся в твёрдом состоянии. Среди природных газов выделяются горючие газы - это газы, способные гореть в смеси с воздухом в нормальных условиях. Горючими газами являются углеводородные газы: метан, этан, пропан, бутан, а также сероводород, окись углерода и их смеси, при суммарном содержании азота и углекислого газа менее 80 %. Кроме газообразной формы и фазового состояния природные газы, в том числе и горючие, широко распространены в земной коре в водорастворённом состоянии. В огромных объёмах они растворены в нефти и образуют твёрдые растворы с водой, так называемые газовые гидраты. Газы являются продуктом биохимических и термокаталитических преобразований ОВ, а также продуктом глубинных процессов. Часто природные газы сопровождают скопления нефти, образуя двухфазные нефтегазовые и газонефтяные залежи
Природные газы – это смеси веществ, находящиеся в нормальных условиях в газообразном состоянии и газы, выделяющиеся из состава природных систем иного агрегатного состояния, например: пластовых вод и нефтей, газовых гидратов, которые находятся в твёрдом состоянии. Среди природных газов выделяются горючие газы - это газы, способные гореть в смеси с воздухом в нормальных условиях. Горючими газами являются углеводородные газы: метан, этан, пропан, бутан, а также сероводород, окись углерода и их смеси, при суммарном содержании азота и углекислого газа менее 80 %. Кроме газообразной формы и фазового состояния природные газы, в том числе и горючие, широко распространены в земной коре в водорастворённом состоянии. В огромных объёмах они растворены в нефти и образуют твёрдые растворы с водой, так называемые газовые гидраты. Газы являются продуктом биохимических и термокаталитических преобразований ОВ, а также продуктом глубинных процессов. Часто природные газы сопровождают скопления нефти, образуя двухфазные нефтегазовые и газонефтяные залежи
 Генетические классификации природных газов. Газы образуют различные смеси, в которых определить генезис отдельных компонентов не всегда возможно. Существует много генетических классификаций газов, в которых выделяется различное количество генетических классов и типов газов. Так в наиболее краткой из них является классификация газов В. И. Ермакова и др. (1990), в которой все природные газы разделены на три большие группы: биогенную, литогенную и органолитогенную. Генетические классификации природных газов.
Генетические классификации природных газов. Газы образуют различные смеси, в которых определить генезис отдельных компонентов не всегда возможно. Существует много генетических классификаций газов, в которых выделяется различное количество генетических классов и типов газов. Так в наиболее краткой из них является классификация газов В. И. Ермакова и др. (1990), в которой все природные газы разделены на три большие группы: биогенную, литогенную и органолитогенную. Генетические классификации природных газов.
 1. Биогенные газы образуются в результате жизнедеятельности различных организмов, а также разложения и преобразования органических и минеральных веществ в биосфере. 2. Органолитогенные газы образуются при термической деструкции (углефикации) ОВ в зоне катагенеза и метагенеза, вплоть до исчерпания его продуктивности и превращения в графит. 3. Литогенные газы образуются в результате физико-химических и радиоактивные процессов в минеральном скелете водонасыщенных осадочных пород в зоне катагенеза, метагенеза и метаморфизма, а также в магматических породах земной коры и мантии. Генетические классификации природных газов
1. Биогенные газы образуются в результате жизнедеятельности различных организмов, а также разложения и преобразования органических и минеральных веществ в биосфере. 2. Органолитогенные газы образуются при термической деструкции (углефикации) ОВ в зоне катагенеза и метагенеза, вплоть до исчерпания его продуктивности и превращения в графит. 3. Литогенные газы образуются в результате физико-химических и радиоактивные процессов в минеральном скелете водонасыщенных осадочных пород в зоне катагенеза, метагенеза и метаморфизма, а также в магматических породах земной коры и мантии. Генетические классификации природных газов
 Классификации природных газов по химическому составу. По химическому составу классифицируются газы конкретных форм или условий нахождения в природе. Существует большое количество различных химических классификаций. Отличаются они широтой охвата форм газов и соответственно количеством выделенных классов газов по химическим компонентам и их количественным содержанием. Широко известна комплексная классификация природных газов, составленная в 1966 году В. А. Соколовым. В ней, по условиям нахождения газов в природе, выделено восемь типов, указан их химический состав и происхождение Классификации природных газов по химическому составу
Классификации природных газов по химическому составу. По химическому составу классифицируются газы конкретных форм или условий нахождения в природе. Существует большое количество различных химических классификаций. Отличаются они широтой охвата форм газов и соответственно количеством выделенных классов газов по химическим компонентам и их количественным содержанием. Широко известна комплексная классификация природных газов, составленная в 1966 году В. А. Соколовым. В ней, по условиям нахождения газов в природе, выделено восемь типов, указан их химический состав и происхождение Классификации природных газов по химическому составу
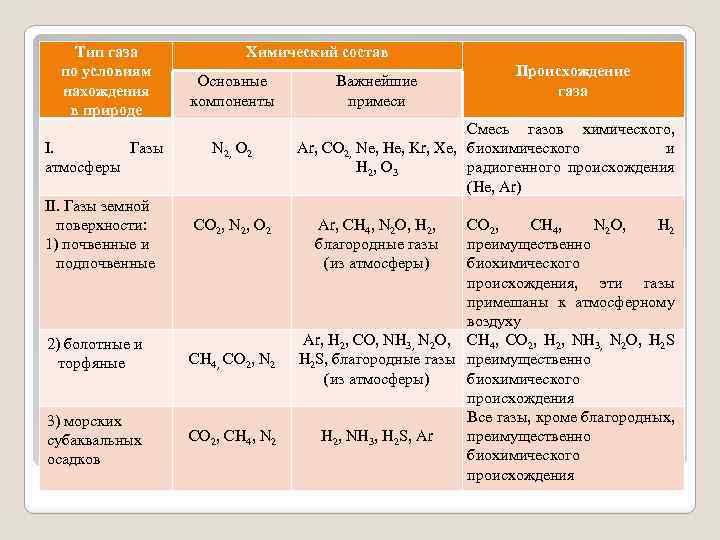 Тип газа по условиям нахождения в природе I. Газы атмосферы II. Газы земной поверхности: 1) почвенные и подпочвенные Химический состав Основные компоненты N 2, O 2 CO 2, N 2, O 2 Важнейшие примеси Происхождение газа Смесь газов химического, Ar, CO 2, Ne, He, Kr, Xe, биохимического и H 2, O 3 радиогенного происхождения (He, Ar) Ar, CH 4, N 2 O, H 2, благородные газы (из атмосферы) CO 2, CH 4, N 2 O, H 2 преимущественно биохимического происхождения, эти газы примешаны к атмосферному воздуху Ar, H 2, CO, NH 3, N 2 O, CH 4, CO 2, H 2, NH 3, N 2 O, H 2 S 2) болотные и CH 4, CO 2, N 2 H 2 S, благородные газы преимущественно торфяные (из атмосферы) биохимического происхождения Все газы, кроме благородных, 3) морских Классификация природных газов по условиям нахождения, CO 2, CH 4, N 2 H 2, NH 3, H 2 S, Ar преимущественно субаквальных химическому составу и генезису (по В. А. Соколову, 1966) биохимического осадков происхождения
Тип газа по условиям нахождения в природе I. Газы атмосферы II. Газы земной поверхности: 1) почвенные и подпочвенные Химический состав Основные компоненты N 2, O 2 CO 2, N 2, O 2 Важнейшие примеси Происхождение газа Смесь газов химического, Ar, CO 2, Ne, He, Kr, Xe, биохимического и H 2, O 3 радиогенного происхождения (He, Ar) Ar, CH 4, N 2 O, H 2, благородные газы (из атмосферы) CO 2, CH 4, N 2 O, H 2 преимущественно биохимического происхождения, эти газы примешаны к атмосферному воздуху Ar, H 2, CO, NH 3, N 2 O, CH 4, CO 2, H 2, NH 3, N 2 O, H 2 S 2) болотные и CH 4, CO 2, N 2 H 2 S, благородные газы преимущественно торфяные (из атмосферы) биохимического происхождения Все газы, кроме благородных, 3) морских Классификация природных газов по условиям нахождения, CO 2, CH 4, N 2 H 2, NH 3, H 2 S, Ar преимущественно субаквальных химическому составу и генезису (по В. А. Соколову, 1966) биохимического осадков происхождения
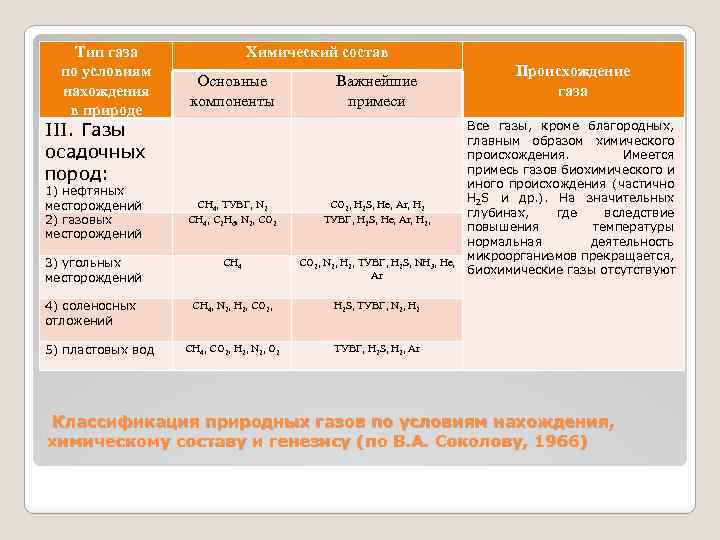 Тип газа по условиям нахождения в природе Химический состав Основные компоненты III. Газы осадочных пород: 1) нефтяных месторождений 2) газовых месторождений CH 4, ТУВГ, N 2 CH 4, C 2 H 6, N 2, CO 2 Важнейшие примеси Происхождение газа Все газы, кроме благородных, главным образом химического происхождения. Имеется примесь газов биохимического и иного происхождения (частично H 2 S и др. ). На значительных CO 2, H 2 S, He, Ar, H 2 глубинах, где вследствие ТУВГ, H 2 S, He, Ar, H 2, повышения температуры нормальная деятельность микроорганизмов прекращается, CO 2, N 2, H 2, ТУВГ, H 2 S, NH 3, He, биохимические газы отсутствуют Ar 3) угольных месторождений CH 4 4) соленосных отложений CH 4, N 2, H 2, CO 2, H 2 S, ТУВГ, N 2, H 2 CH 4, CO 2, Н 2, N 2, O 2 ТУВГ, H 2 S, H 2, Ar 5) пластовых вод Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
Тип газа по условиям нахождения в природе Химический состав Основные компоненты III. Газы осадочных пород: 1) нефтяных месторождений 2) газовых месторождений CH 4, ТУВГ, N 2 CH 4, C 2 H 6, N 2, CO 2 Важнейшие примеси Происхождение газа Все газы, кроме благородных, главным образом химического происхождения. Имеется примесь газов биохимического и иного происхождения (частично H 2 S и др. ). На значительных CO 2, H 2 S, He, Ar, H 2 глубинах, где вследствие ТУВГ, H 2 S, He, Ar, H 2, повышения температуры нормальная деятельность микроорганизмов прекращается, CO 2, N 2, H 2, ТУВГ, H 2 S, NH 3, He, биохимические газы отсутствуют Ar 3) угольных месторождений CH 4 4) соленосных отложений CH 4, N 2, H 2, CO 2, H 2 S, ТУВГ, N 2, H 2 CH 4, CO 2, Н 2, N 2, O 2 ТУВГ, H 2 S, H 2, Ar 5) пластовых вод Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
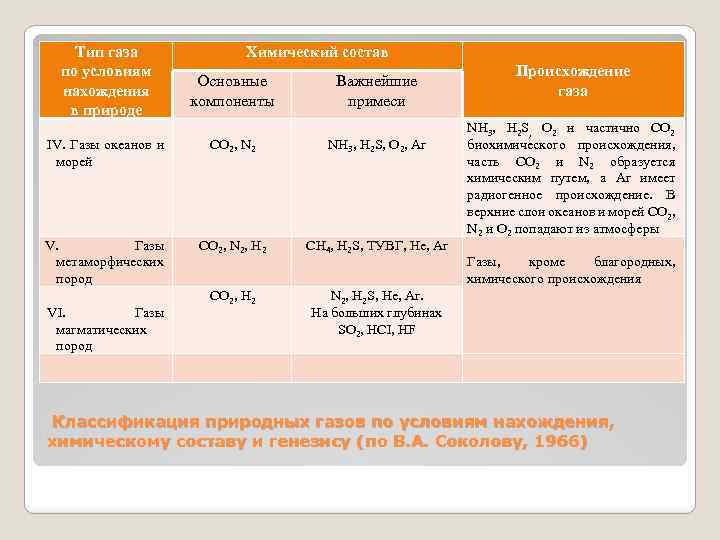 Тип газа по условиям нахождения в природе Химический состав Основные компоненты Важнейшие примеси IV. Газы океанов и морей CO 2, N 2 NH 3, H 2 S, O 2, Ar V. Газы метаморфических пород CO 2, N 2, H 2 CH 4, H 2 S, ТУВГ, He, Ar CO 2, H 2 Происхождение газа NH 3, H 2 S, O 2 и частично СО 2 биохимического происхождения, часть СО 2 и N 2 образуется химическим путем, а Аr имеет радиогенное происхождение. В верхние слои океанов и морей СО 2, N 2 и О 2 попадают из атмосферы N 2, H 2 S, He, Ar. На больших глубинах SO 2, HCI, HF VI. Газы магматических пород Газы, кроме благородных, химического происхождения Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
Тип газа по условиям нахождения в природе Химический состав Основные компоненты Важнейшие примеси IV. Газы океанов и морей CO 2, N 2 NH 3, H 2 S, O 2, Ar V. Газы метаморфических пород CO 2, N 2, H 2 CH 4, H 2 S, ТУВГ, He, Ar CO 2, H 2 Происхождение газа NH 3, H 2 S, O 2 и частично СО 2 биохимического происхождения, часть СО 2 и N 2 образуется химическим путем, а Аr имеет радиогенное происхождение. В верхние слои океанов и морей СО 2, N 2 и О 2 попадают из атмосферы N 2, H 2 S, He, Ar. На больших глубинах SO 2, HCI, HF VI. Газы магматических пород Газы, кроме благородных, химического происхождения Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
 Тип газа по условиям нахождения в природе VII. Газы вулканические: 1) высокотемператур ные (из лавовых озер и др. ) Химический состав Основные компоненты Важнейшие примеси СО 2, Н 2, SO 2, HCl, HF N 2, CO, NH 3, He, Ar 2) фумарольные (100 -300 ºС) СО 2, Н 2, H 2 S, SO 2 СО 2, SO 2 Все газы, кроме благородных, химического происхождения. Они представляют собой в той или иной степени изменённые газы, поступающие из верхней мантии с примесью газов из вышерасположенных оболочек CO, HCl, HF, N 2, NH 3, He, Ar 3) термальных источников Происхождение газа N 2, CO, NH 3, He, Ar VIII. Газы космоса H 2, H, He CO, радикалы CH, CH 2, OH и другие, ионизированные атомы элементов Ne, N, Ar Все газы являются результатом ядерных, радиационнохимических и химических реакций Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
Тип газа по условиям нахождения в природе VII. Газы вулканические: 1) высокотемператур ные (из лавовых озер и др. ) Химический состав Основные компоненты Важнейшие примеси СО 2, Н 2, SO 2, HCl, HF N 2, CO, NH 3, He, Ar 2) фумарольные (100 -300 ºС) СО 2, Н 2, H 2 S, SO 2 СО 2, SO 2 Все газы, кроме благородных, химического происхождения. Они представляют собой в той или иной степени изменённые газы, поступающие из верхней мантии с примесью газов из вышерасположенных оболочек CO, HCl, HF, N 2, NH 3, He, Ar 3) термальных источников Происхождение газа N 2, CO, NH 3, He, Ar VIII. Газы космоса H 2, H, He CO, радикалы CH, CH 2, OH и другие, ионизированные атомы элементов Ne, N, Ar Все газы являются результатом ядерных, радиационнохимических и химических реакций Классификация природных газов по условиям нахождения, химическому составу и генезису (по В. А. Соколову, 1966)
 Температура кипения углеводородных газов приблизительно до 0 ºС. Таких углеводородов всего 4. Вязкость газов возрастает с повышением температуры. Связано это с тем, что вязкость газа увеличивается при ускорении движения молекул, вызванном ростом температуры. В отличие от жидкостей более высокомолекулярные углеводороды в газовом состоянии имеют меньшую вязкость. Плотность газов зависит от входящих в него компонентов: плотность метана по воздуху – 0, 554, этана – 1, 038, пропана – 1, 522, бутанов – 2, 006. Поэтому плотность попутного газа обычно значительно больше, чем у газа газовых месторождений. Растворимость газов при небольших давлениях (до 5 МПа) подчиняется закону Генри: количество растворенного газа прямо пропорционально давлению и коэффициенту растворимости Растворимость газов зависит от температуры воды (до 100 ºС – обратная, после 100 ºС – прямая), химического состава газов (например, при 20 ºС СО 2 растворяется в 27 раз лучше, чем СН 4, и в 58 раз лучше, чем азот). Растворимость метана в природных водах и рассолах колеблется в зависимости от минерализации, в целом снижаясь с увеличением минерализации. Чем выше молекулярный вес газового углеводорода, тем лучше он растворим в жидких углеводородах и нефти. Содержание растворенного в нефти газа оценивается величиной газового фактора (ГФ) – количеством газа, выделившегося из 1 т нефти при атмосферных условиях. ГФ колеблется для разных районов и глубин от 508 до 1000– 1200 м 3/т. При ГФ = 550– 600 м 3/т пласт содержит нефть, при ГФ = 1000– 1200 м 3/т – газоконденсат. Физико-химические свойства газов
Температура кипения углеводородных газов приблизительно до 0 ºС. Таких углеводородов всего 4. Вязкость газов возрастает с повышением температуры. Связано это с тем, что вязкость газа увеличивается при ускорении движения молекул, вызванном ростом температуры. В отличие от жидкостей более высокомолекулярные углеводороды в газовом состоянии имеют меньшую вязкость. Плотность газов зависит от входящих в него компонентов: плотность метана по воздуху – 0, 554, этана – 1, 038, пропана – 1, 522, бутанов – 2, 006. Поэтому плотность попутного газа обычно значительно больше, чем у газа газовых месторождений. Растворимость газов при небольших давлениях (до 5 МПа) подчиняется закону Генри: количество растворенного газа прямо пропорционально давлению и коэффициенту растворимости Растворимость газов зависит от температуры воды (до 100 ºС – обратная, после 100 ºС – прямая), химического состава газов (например, при 20 ºС СО 2 растворяется в 27 раз лучше, чем СН 4, и в 58 раз лучше, чем азот). Растворимость метана в природных водах и рассолах колеблется в зависимости от минерализации, в целом снижаясь с увеличением минерализации. Чем выше молекулярный вес газового углеводорода, тем лучше он растворим в жидких углеводородах и нефти. Содержание растворенного в нефти газа оценивается величиной газового фактора (ГФ) – количеством газа, выделившегося из 1 т нефти при атмосферных условиях. ГФ колеблется для разных районов и глубин от 508 до 1000– 1200 м 3/т. При ГФ = 550– 600 м 3/т пласт содержит нефть, при ГФ = 1000– 1200 м 3/т – газоконденсат. Физико-химические свойства газов
 Сорбция газов происходит в атмосфере (аэрозолями), гидросфере (органическими и минеральными взвесями, живым веществом) и литосфере (минеральным и ОВ). Диффузия газа возможна практически в любой среде. Происходит диффузия одного газа в другом (атмосфера, газовая залежь), диффузия газа в твердом веществе. Именно явлением диффузии объясняется многообразие форм существования газов в оболочках Земли. Коэффициенты диффузии индивидуальных газов зависят от свойств диффундируемого газа, свойств среды, через которую происходит диффузия и термодинамических условий. С увеличением молекулярной массы газов коэффициенты диффузии снижаются, с ростом температуры – повышаются. Коэффициенты диффузии в воде для газов меняются от 1, 3 до 2, 2 см 2/с. Наибольшим коэффициентом диффузии характеризуется метан. В породах эти коэффициенты еще меньше, так как процесс диффузии осложняется сорбцией газов. Зная коэффициенты диффузии и сорбции, можно рассчитать величину диффузионного потока, идущего от скопления газа через вмещающие породы. Расчеты В. А. Соколова (1956) показали, что потребуются миллионы лет, чтобы установить стационарный диффузионный поток через 1 км толщи осадочных пород. Фильтрация газов, т. е. движение газов через пористую среду под влиянием перепада давления, имеет место только в литосфере. В естественных условиях фильтрация очень сложна, так как приходится иметь дело с двух- и многофазными жидкостями. Часто наблюдаются ретроградные явления: сжатые газы несут в себе жидкие углеводороды, которые выделяются при снижении давления в конденсаты. Физико-химические свойства газов
Сорбция газов происходит в атмосфере (аэрозолями), гидросфере (органическими и минеральными взвесями, живым веществом) и литосфере (минеральным и ОВ). Диффузия газа возможна практически в любой среде. Происходит диффузия одного газа в другом (атмосфера, газовая залежь), диффузия газа в твердом веществе. Именно явлением диффузии объясняется многообразие форм существования газов в оболочках Земли. Коэффициенты диффузии индивидуальных газов зависят от свойств диффундируемого газа, свойств среды, через которую происходит диффузия и термодинамических условий. С увеличением молекулярной массы газов коэффициенты диффузии снижаются, с ростом температуры – повышаются. Коэффициенты диффузии в воде для газов меняются от 1, 3 до 2, 2 см 2/с. Наибольшим коэффициентом диффузии характеризуется метан. В породах эти коэффициенты еще меньше, так как процесс диффузии осложняется сорбцией газов. Зная коэффициенты диффузии и сорбции, можно рассчитать величину диффузионного потока, идущего от скопления газа через вмещающие породы. Расчеты В. А. Соколова (1956) показали, что потребуются миллионы лет, чтобы установить стационарный диффузионный поток через 1 км толщи осадочных пород. Фильтрация газов, т. е. движение газов через пористую среду под влиянием перепада давления, имеет место только в литосфере. В естественных условиях фильтрация очень сложна, так как приходится иметь дело с двух- и многофазными жидкостями. Часто наблюдаются ретроградные явления: сжатые газы несут в себе жидкие углеводороды, которые выделяются при снижении давления в конденсаты. Физико-химические свойства газов
 По форме нахождения можно разделить на свободные и попутные (растворенные). природный газ является свободным, если при дебите более 10 000 м 3/сут соотношение объемов газа и жидкости более 1000. Попутный (растворенный) газ характеризуется отношением объемов газовой фазы и жидкости менее 1000. Свободные УВ газы могут находиться: 1) в чисто газовых залежах, причем в одних случаях газовые залежи перемежаются с нефтяными и газонефтяными в пределах одной нефтегазоносной зоны, в других – концентрируются в отдельные газоносные зоны; 2) в свободном состоянии в газовых шапках над нефтяными залежами. Растворенные газы могут находиться в нефтях и подземных водах. Содержание тяжелых углеводородов в попутных газах 20– 40%, иногда до 80 %. Среди гомологов метана преобладает этан (6– 20 %). В отличие от свободных в растворенных газах больше гомологов метана и меньше азота. горючие газы месторождений
По форме нахождения можно разделить на свободные и попутные (растворенные). природный газ является свободным, если при дебите более 10 000 м 3/сут соотношение объемов газа и жидкости более 1000. Попутный (растворенный) газ характеризуется отношением объемов газовой фазы и жидкости менее 1000. Свободные УВ газы могут находиться: 1) в чисто газовых залежах, причем в одних случаях газовые залежи перемежаются с нефтяными и газонефтяными в пределах одной нефтегазоносной зоны, в других – концентрируются в отдельные газоносные зоны; 2) в свободном состоянии в газовых шапках над нефтяными залежами. Растворенные газы могут находиться в нефтях и подземных водах. Содержание тяжелых углеводородов в попутных газах 20– 40%, иногда до 80 %. Среди гомологов метана преобладает этан (6– 20 %). В отличие от свободных в растворенных газах больше гомологов метана и меньше азота. горючие газы месторождений
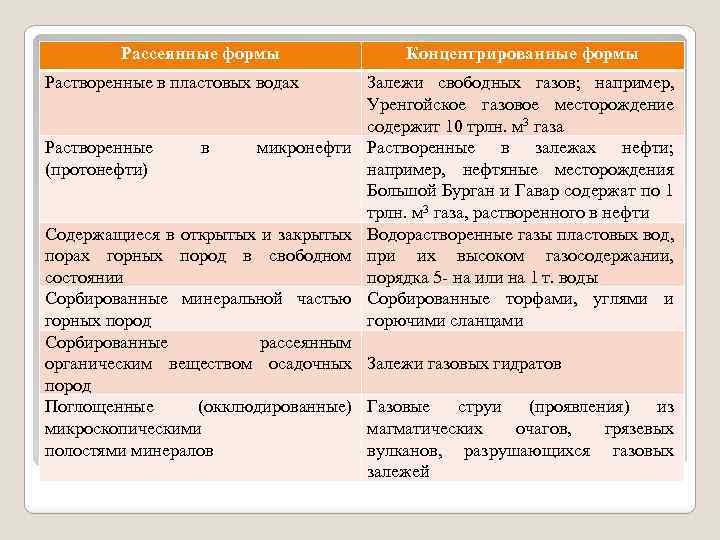 Рассеянные формы Растворенные в пластовых водах Растворенные (протонефти) в микронефти Содержащиеся в открытых и закрытых порах горных пород в свободном состоянии Сорбированные минеральной частью горных пород Сорбированные рассеянным органическим веществом осадочных пород Поглощенные (окклюдированные) микроскопическими полостями минералов Концентрированные формы Залежи свободных газов; например, Уренгойское газовое месторождение содержит 10 трлн. м 3 газа Растворенные в залежах нефти; например, нефтяные месторождения Большой Бурган и Гавар содержат по 1 трлн. м 3 газа, растворенного в нефти Водорастворенные газы пластовых вод, при их высоком газосодержании, порядка 5 - на или на 1 т. воды Сорбированные торфами, углями и горючими сланцами Залежи газовых гидратов Газовые струи (проявления) из магматических очагов, грязевых вулканов, разрушающихся газовых залежей
Рассеянные формы Растворенные в пластовых водах Растворенные (протонефти) в микронефти Содержащиеся в открытых и закрытых порах горных пород в свободном состоянии Сорбированные минеральной частью горных пород Сорбированные рассеянным органическим веществом осадочных пород Поглощенные (окклюдированные) микроскопическими полостями минералов Концентрированные формы Залежи свободных газов; например, Уренгойское газовое месторождение содержит 10 трлн. м 3 газа Растворенные в залежах нефти; например, нефтяные месторождения Большой Бурган и Гавар содержат по 1 трлн. м 3 газа, растворенного в нефти Водорастворенные газы пластовых вод, при их высоком газосодержании, порядка 5 - на или на 1 т. воды Сорбированные торфами, углями и горючими сланцами Залежи газовых гидратов Газовые струи (проявления) из магматических очагов, грязевых вулканов, разрушающихся газовых залежей
 Природные горючие газы - многокомпонентные системы состоят из предельных углеводородов – метана (CH 4), этана (C 2 H 6), пропана (C 3 H 8), бутанa (C 4 H 10), и более тяжелых гомологов метана – пентан (С 5 Н 12) и гексан (С 6 Н 14). В горючих газах месторождений могут присутствовать пары жидких углеводородов, более тяжелые, чем С 6 Н 14. Также содержатся: CO 2, N 2, H 2 S, инертные (редкие) газы, ртуть. Тяжелые гомологи метана, начиная с С 2 Н 6. Содержание тяжелых углеводородов в газах зависит от состава исходного ОВ и степени его катагенеза, условий миграции. Химический состав газов.
Природные горючие газы - многокомпонентные системы состоят из предельных углеводородов – метана (CH 4), этана (C 2 H 6), пропана (C 3 H 8), бутанa (C 4 H 10), и более тяжелых гомологов метана – пентан (С 5 Н 12) и гексан (С 6 Н 14). В горючих газах месторождений могут присутствовать пары жидких углеводородов, более тяжелые, чем С 6 Н 14. Также содержатся: CO 2, N 2, H 2 S, инертные (редкие) газы, ртуть. Тяжелые гомологи метана, начиная с С 2 Н 6. Содержание тяжелых углеводородов в газах зависит от состава исходного ОВ и степени его катагенеза, условий миграции. Химический состав газов.
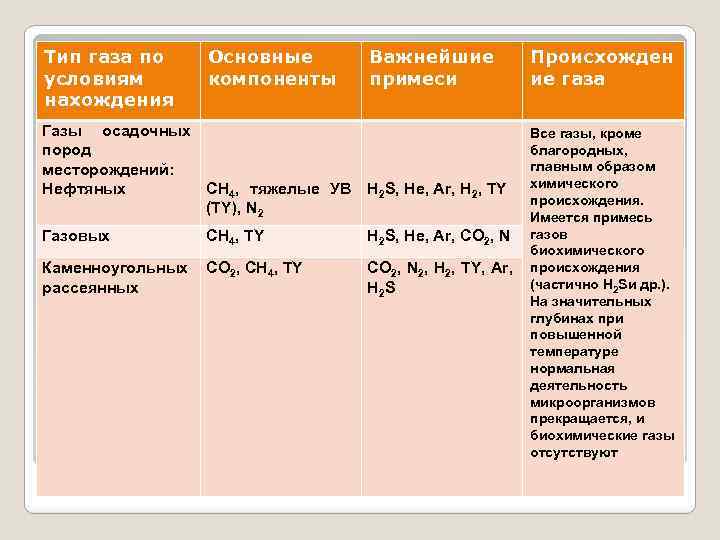 Тип газа по условиям нахождения Основные компоненты Важнейшие примеси Газы осадочных пород месторождений: Нефтяных CH 4, тяжелые УВ (TY), N 2 H 2 S, He, Ar, H 2, TY Газовых CH 4, TY Каменноугольных CO 2, CH 4, TY рассеянных Происхожден ие газа Все газы, кроме благородных, главным образом химического происхождения. Имеется примесь H 2 S, He, Ar, CO 2, N газов биохимического CO 2, N 2, H 2, TY, Ar, происхождения (частично H 2 Sи др. ). H 2 S На значительных глубинах при повышенной температуре нормальная деятельность микроорганизмов прекращается, и биохимические газы отсутствуют
Тип газа по условиям нахождения Основные компоненты Важнейшие примеси Газы осадочных пород месторождений: Нефтяных CH 4, тяжелые УВ (TY), N 2 H 2 S, He, Ar, H 2, TY Газовых CH 4, TY Каменноугольных CO 2, CH 4, TY рассеянных Происхожден ие газа Все газы, кроме благородных, главным образом химического происхождения. Имеется примесь H 2 S, He, Ar, CO 2, N газов биохимического CO 2, N 2, H 2, TY, Ar, происхождения (частично H 2 Sи др. ). H 2 S На значительных глубинах при повышенной температуре нормальная деятельность микроорганизмов прекращается, и биохимические газы отсутствуют
 Состав газовых залежей. Свободные природные газы образуют скопления, состоящие из углеводородных и неуглеводородных компонентов. Главное значение имеют углеводородные компоненты: метан СН 4, этан С 2 Н 6, пропан С 3 Н 8 и бутан С 4 Н 10, а также пары жидких УВ. Среди них преобладает метан. Среди неуглеводородных компонентов преобладают: азот, углекислый газ и сероводород. Иногда каждый из этих газов может превышать 50 % и даже достигать 100 % в составе газовых залежей. В меньших количествах в залежах присутствуют следующие газы: водород, гелий, аргон, ксенон, окись углерода, а также пары воды и ртути. Природный газ, в котором суммарное содержание углеводородных газовых компонентов превышает 50 %, называется углеводородным. Природный газ, способный гореть в смеси с воздухом при нормальных условиях называется горючим. Горючими являются газовые смеси, содержащие УВ, сероводород, водород и окись углерода. Состав газовых залежей
Состав газовых залежей. Свободные природные газы образуют скопления, состоящие из углеводородных и неуглеводородных компонентов. Главное значение имеют углеводородные компоненты: метан СН 4, этан С 2 Н 6, пропан С 3 Н 8 и бутан С 4 Н 10, а также пары жидких УВ. Среди них преобладает метан. Среди неуглеводородных компонентов преобладают: азот, углекислый газ и сероводород. Иногда каждый из этих газов может превышать 50 % и даже достигать 100 % в составе газовых залежей. В меньших количествах в залежах присутствуют следующие газы: водород, гелий, аргон, ксенон, окись углерода, а также пары воды и ртути. Природный газ, в котором суммарное содержание углеводородных газовых компонентов превышает 50 %, называется углеводородным. Природный газ, способный гореть в смеси с воздухом при нормальных условиях называется горючим. Горючими являются газовые смеси, содержащие УВ, сероводород, водород и окись углерода. Состав газовых залежей
 Качество газа, как энергоносителя, зависит от содержания метана. При содержании в газовой смеси этана и других углеводородных газов более 23 % они становятся ценным химическим сырьём, которое используется в производстве синтетического каучука, полиэтилена, пластмасс и других веществ. В зависимости от количественного соотношения метана и его гомологов углеводородные газы разделяются на сухие, тощие (полужирные) и жирные. Сухие газы состоят на 95 -99 % из метана. Сухими они называются потому, что практически не образуют конденсат. Тощие газы состоят из метана на 90 -95 % и содержат пары жидких углеводородов, которые при снижении давления образуют конденсат в количестве от 10 до 30 см 3/м 3. Жирные газы также состоят в основном из метана, но его содержание составляет менее 90 %. Содержат они и ТУВГ, а также - пары жидких высококипящих УВ, которые при снижении давления образуют конденсат в количестве боле 30 см 3/м 3. Имеются жирные газы с преобладанием неуглеводородных компонентов. Состав газовых залежей
Качество газа, как энергоносителя, зависит от содержания метана. При содержании в газовой смеси этана и других углеводородных газов более 23 % они становятся ценным химическим сырьём, которое используется в производстве синтетического каучука, полиэтилена, пластмасс и других веществ. В зависимости от количественного соотношения метана и его гомологов углеводородные газы разделяются на сухие, тощие (полужирные) и жирные. Сухие газы состоят на 95 -99 % из метана. Сухими они называются потому, что практически не образуют конденсат. Тощие газы состоят из метана на 90 -95 % и содержат пары жидких углеводородов, которые при снижении давления образуют конденсат в количестве от 10 до 30 см 3/м 3. Жирные газы также состоят в основном из метана, но его содержание составляет менее 90 %. Содержат они и ТУВГ, а также - пары жидких высококипящих УВ, которые при снижении давления образуют конденсат в количестве боле 30 см 3/м 3. Имеются жирные газы с преобладанием неуглеводородных компонентов. Состав газовых залежей
 К чисто газовым залежам относятся скопления газа, в которых при стандартных условиях отсутствует жидкая фаза или конденсат, то есть сухие газы или же скопления тощих газов, в которых содержание конденсата не достигает промышленных концентраций (25 -30 см 3/м 3). Газы с содержанием конденсата выше 25 -30 см 3/м 3 относятся к конденсатным газам или газоконденсатам. В геохимии широко используется такай показатель, как «коэффициент сухости» - это - отношение процентного содержания метана к сумме его гомологов: СН 4 /С 2 Н 6 + высшие, или применяется его обратная величина – коэффициент жирности. Состав газовых залежей
К чисто газовым залежам относятся скопления газа, в которых при стандартных условиях отсутствует жидкая фаза или конденсат, то есть сухие газы или же скопления тощих газов, в которых содержание конденсата не достигает промышленных концентраций (25 -30 см 3/м 3). Газы с содержанием конденсата выше 25 -30 см 3/м 3 относятся к конденсатным газам или газоконденсатам. В геохимии широко используется такай показатель, как «коэффициент сухости» - это - отношение процентного содержания метана к сумме его гомологов: СН 4 /С 2 Н 6 + высшие, или применяется его обратная величина – коэффициент жирности. Состав газовых залежей
 По углеводородному составу газы : «сухие» (С 2 + тяжелые гомологи 3– 15 %) «жирные» (С 2 + тяжелые гомологи 20– 60 %). Для характеристики состава газов применяется «коэффициент сухости» , т. е. отношение процентного содержания метана к сумме его гомологов (СН 4/(С 2 Н 6+высшие)), - показатель направления миграции газов. Метан обладает наибольшей подвижностью среди газообразных углеводородов, с ростом молекулярной массы скорость миграции уменьшается. Газы, прошедшие большое расстояние от источника миграции, должны быть относительно обогащены низкомолекулярными компонентами. Метан обладает низкой сорбционной способностью и наименьшей растворимостью в воде среди газообразных углеводородов. Углеводородный состав газов :
По углеводородному составу газы : «сухие» (С 2 + тяжелые гомологи 3– 15 %) «жирные» (С 2 + тяжелые гомологи 20– 60 %). Для характеристики состава газов применяется «коэффициент сухости» , т. е. отношение процентного содержания метана к сумме его гомологов (СН 4/(С 2 Н 6+высшие)), - показатель направления миграции газов. Метан обладает наибольшей подвижностью среди газообразных углеводородов, с ростом молекулярной массы скорость миграции уменьшается. Газы, прошедшие большое расстояние от источника миграции, должны быть относительно обогащены низкомолекулярными компонентами. Метан обладает низкой сорбционной способностью и наименьшей растворимостью в воде среди газообразных углеводородов. Углеводородный состав газов :
 Содержание углекислого газа варьирует от 0, 4 до 4 %, иногда до 50 % СО 2. Наибольшим количеством СО 2 характеризуются газы, растворенные в молодых нефтях. Среднее содержание азота – 0, 4– 12, 5 %. Растет от молодых месторождений к древним (в возрастном отношении). H 2 S-содержащие газы – важнейший источник получения элементарной серы. H 2 S образуется в глубокозалегающих карбонатно-эвапоритовых отложениях в присутствии углеводородов. Содержание H 2 S достигает 42, 4 %. В России сера извлекается из газов Оренбургского и Астраханского месторождений. Из инертных газов самое высокое содержание характерно для гелия. Почти 80 % газовых залежей содержат 0, 01– 0, 2 % гелия. Его максимальные концентрации (до 10 %) и фоновые значения (0, 06– 0, 15 %) фиксируются на древних платформах. Содержание аргона меняется от 0, 001 до 1 % при фоновом 0, 01– 0, 03 %. Наибольшее его содержание его – в газах протерозойских платформ. Максимальная концентрация Ar и He, как правило, характерна для одних и тех же месторождениях. Ртуть. На газовом месторождение Слохтерен (Нидерланды) содержание ртути составляет 1, 8. 10 -4 г/м 3, а ее запасы оцениваются в 340 т. Установлено кондиционное содержание ртути и на других месторождениях в Нидерландах и ФРГ. Примеси в горючих газах
Содержание углекислого газа варьирует от 0, 4 до 4 %, иногда до 50 % СО 2. Наибольшим количеством СО 2 характеризуются газы, растворенные в молодых нефтях. Среднее содержание азота – 0, 4– 12, 5 %. Растет от молодых месторождений к древним (в возрастном отношении). H 2 S-содержащие газы – важнейший источник получения элементарной серы. H 2 S образуется в глубокозалегающих карбонатно-эвапоритовых отложениях в присутствии углеводородов. Содержание H 2 S достигает 42, 4 %. В России сера извлекается из газов Оренбургского и Астраханского месторождений. Из инертных газов самое высокое содержание характерно для гелия. Почти 80 % газовых залежей содержат 0, 01– 0, 2 % гелия. Его максимальные концентрации (до 10 %) и фоновые значения (0, 06– 0, 15 %) фиксируются на древних платформах. Содержание аргона меняется от 0, 001 до 1 % при фоновом 0, 01– 0, 03 %. Наибольшее его содержание его – в газах протерозойских платформ. Максимальная концентрация Ar и He, как правило, характерна для одних и тех же месторождениях. Ртуть. На газовом месторождение Слохтерен (Нидерланды) содержание ртути составляет 1, 8. 10 -4 г/м 3, а ее запасы оцениваются в 340 т. Установлено кондиционное содержание ртути и на других месторождениях в Нидерландах и ФРГ. Примеси в горючих газах
 При низких температурах и повышенных давлениях – газы и вода образуют газогидраты - твердые скопления (клатраты), в которых молекулы газа заполняют пустоты кристаллической решетки, образованной молекулами воды с помощью водородной связи. Их общая формула М·H 2 O, где М – молекула газа-гидратообразователя. Сама по себе кристаллическая решетка этого типа, если она не заполнена определенным минимальным количеством газа, термодинамически метастабильна, т. е. в чистом виде (без газа) существовать не может. Этим она принципиально отличается от кристаллической решетки льда. По внешнему виду газогидраты напоминают снег или рыхлый лед. Природные газы обычно образуют смешанные гидраты, в которых большие полости заняты пропаном и бутаном, а малые – метаном, этаном, углекислотой и другими газами. Большинство компонентов природного газа способно образовывать гидраты. Наиболее легко переходят в гидрат сероводород и пропан, наиболее трудно – азот, аргон. Водород, гелий, бутан и более тяжелые гомологи метана не образуют гидраты и могут только захватываться гидратной решеткой как примеси. Таким образом, при процессах гидратообразования происходит фракционирование состава природного газа: гомологи метана и сероводород накапливаются в гидрате, а оставшаяся газовая фаза обогащается азотом, аргоном и гелием. При образовании гидратов один объем воды может связывать от 70 до 300 объемов газа. Соответственно и плотность газогидратов меняется в широком диапазоне – от 0, 8 до 1, 8 г/см 3. Газогидраты
При низких температурах и повышенных давлениях – газы и вода образуют газогидраты - твердые скопления (клатраты), в которых молекулы газа заполняют пустоты кристаллической решетки, образованной молекулами воды с помощью водородной связи. Их общая формула М·H 2 O, где М – молекула газа-гидратообразователя. Сама по себе кристаллическая решетка этого типа, если она не заполнена определенным минимальным количеством газа, термодинамически метастабильна, т. е. в чистом виде (без газа) существовать не может. Этим она принципиально отличается от кристаллической решетки льда. По внешнему виду газогидраты напоминают снег или рыхлый лед. Природные газы обычно образуют смешанные гидраты, в которых большие полости заняты пропаном и бутаном, а малые – метаном, этаном, углекислотой и другими газами. Большинство компонентов природного газа способно образовывать гидраты. Наиболее легко переходят в гидрат сероводород и пропан, наиболее трудно – азот, аргон. Водород, гелий, бутан и более тяжелые гомологи метана не образуют гидраты и могут только захватываться гидратной решеткой как примеси. Таким образом, при процессах гидратообразования происходит фракционирование состава природного газа: гомологи метана и сероводород накапливаются в гидрате, а оставшаяся газовая фаза обогащается азотом, аргоном и гелием. При образовании гидратов один объем воды может связывать от 70 до 300 объемов газа. Соответственно и плотность газогидратов меняется в широком диапазоне – от 0, 8 до 1, 8 г/см 3. Газогидраты
 Газоконденсаты – природная система взаиморастворенных газообразных и легкокипящих жидких нефтяных углеводородов, находящихся в термодинамических условиях земных недр в газообразном или парообразном фазовом состоянии. Охлаждение и снижение давления до атмосферного приводит к выпадению из этой системы жидкой фазы – конденсата. Газовая часть газоконденсата всегда относится к категории жирных газов. Газоконденсаты занимают значительное место в природной системе ОВ – нефть – газ и выделяются в самостоятельную группу нафтидов. Газоконденсатными называются залежи, при эксплуатации которых добывается газ и конденсат. Под конденсатностью понимают содержание жидких углеводородов в газе в пластовых условиях (см 3/м 3, г/м 3). Газоконденсатный фактор (м 3/г, м 3/м 3) – величина, обратная конденсатности. Различают сырой и стабильный конденсат. Сырой конденсат представляет собой углеводороды, находящиеся при стандартных условиях в жидком состоянии с растворенными в них газообразными компонентами (CH 4, C 2 Н 6, C 3 H 8, бутаны). Конденсат, состоящий только из жидких углеводородов (от пентана и выше) при стандартных условиях – стабильный. Стабильный конденсат получают из сырого путем его дегазации. Газоконденсаты
Газоконденсаты – природная система взаиморастворенных газообразных и легкокипящих жидких нефтяных углеводородов, находящихся в термодинамических условиях земных недр в газообразном или парообразном фазовом состоянии. Охлаждение и снижение давления до атмосферного приводит к выпадению из этой системы жидкой фазы – конденсата. Газовая часть газоконденсата всегда относится к категории жирных газов. Газоконденсаты занимают значительное место в природной системе ОВ – нефть – газ и выделяются в самостоятельную группу нафтидов. Газоконденсатными называются залежи, при эксплуатации которых добывается газ и конденсат. Под конденсатностью понимают содержание жидких углеводородов в газе в пластовых условиях (см 3/м 3, г/м 3). Газоконденсатный фактор (м 3/г, м 3/м 3) – величина, обратная конденсатности. Различают сырой и стабильный конденсат. Сырой конденсат представляет собой углеводороды, находящиеся при стандартных условиях в жидком состоянии с растворенными в них газообразными компонентами (CH 4, C 2 Н 6, C 3 H 8, бутаны). Конденсат, состоящий только из жидких углеводородов (от пентана и выше) при стандартных условиях – стабильный. Стабильный конденсат получают из сырого путем его дегазации. Газоконденсаты
 В стандартных условиях газоконденсаты - жидкости, обычно прозрачные, бесцветные или слабоокрашенные в коричневатый, иногда зеленоватый цвет. плотность конденсатов варьирует от 0, 677 до 0, 827 г/см 3, коэффициент преломления – 1, 3905– 1, 4600, молекулярная масса – 92– 158, содержание серы – 0– 1, 2%. Газоконденсаты характеризуются низкой температурой начала кипения (24– 92°С). В среднем они на 60– 80 % выкипают до 200ºС, но есть конденсаты (или нефтеконденсатные смеси), конец кипения которых лежит в пределах 350– 500ºС, содержащие не только парафины и силикагелевые смолы, но и асфальтены. Наличие высококипящих углеводородов в конденсате отличает их от выделяемых из попутных газовых бензинов, имеющих конец кипения не более 130 – 160ºС. Газоконденсаты более чем на 90 % состоят из углеводородов, нередко в них содержатся силикагелевые смолы – до 3– 7%, иногда присутствуют асфальтены в количестве 0, 02– 0, 06%, очень редко – до 0, 3%. В бензиновых фракциях конденсатов обычно преобладают метановые, реже метановые и нафтеновые углеводороды, которые содержатся примерно в равных количествах. Встречаются конденсаты, в которых преобладают ароматические и нафтеновые углеводороды. Газоконденсаты
В стандартных условиях газоконденсаты - жидкости, обычно прозрачные, бесцветные или слабоокрашенные в коричневатый, иногда зеленоватый цвет. плотность конденсатов варьирует от 0, 677 до 0, 827 г/см 3, коэффициент преломления – 1, 3905– 1, 4600, молекулярная масса – 92– 158, содержание серы – 0– 1, 2%. Газоконденсаты характеризуются низкой температурой начала кипения (24– 92°С). В среднем они на 60– 80 % выкипают до 200ºС, но есть конденсаты (или нефтеконденсатные смеси), конец кипения которых лежит в пределах 350– 500ºС, содержащие не только парафины и силикагелевые смолы, но и асфальтены. Наличие высококипящих углеводородов в конденсате отличает их от выделяемых из попутных газовых бензинов, имеющих конец кипения не более 130 – 160ºС. Газоконденсаты более чем на 90 % состоят из углеводородов, нередко в них содержатся силикагелевые смолы – до 3– 7%, иногда присутствуют асфальтены в количестве 0, 02– 0, 06%, очень редко – до 0, 3%. В бензиновых фракциях конденсатов обычно преобладают метановые, реже метановые и нафтеновые углеводороды, которые содержатся примерно в равных количествах. Встречаются конденсаты, в которых преобладают ароматические и нафтеновые углеводороды. Газоконденсаты
 С увеличением температуры и давления растворимость жидких углеводородов в газе растет, причем давление оказывает большее влияние, чем температура. При одинаковых давлениях и температурах среди углеводородов с равным числом атомов углерода в молекуле лучшей растворимостью обладают нормальные парафины, а наименьшей – ароматические. Цикланы занимают промежуточное положение. С повышением температуры и давления в недрах разница в растворимости углеводородов различных групп нивелируется. Количество и состав смол в газоконденсатах зависит прежде всего от генетического типа конденсата и наличия в газоконденсатных залежах нефтяной оторочки. Смолистые компоненты нефтей растворяются в сухих природных газах лишь при высоком давлении. Газоконденсаты
С увеличением температуры и давления растворимость жидких углеводородов в газе растет, причем давление оказывает большее влияние, чем температура. При одинаковых давлениях и температурах среди углеводородов с равным числом атомов углерода в молекуле лучшей растворимостью обладают нормальные парафины, а наименьшей – ароматические. Цикланы занимают промежуточное положение. С повышением температуры и давления в недрах разница в растворимости углеводородов различных групп нивелируется. Количество и состав смол в газоконденсатах зависит прежде всего от генетического типа конденсата и наличия в газоконденсатных залежах нефтяной оторочки. Смолистые компоненты нефтей растворяются в сухих природных газах лишь при высоком давлении. Газоконденсаты
 По соотношению отдельных индивидуальных компонентов конденсаты несколько отличаются от нефтей. Конденсаты состоят из более простых нефтяных компонентов, что обусловлено растворяющей способностью газов. В нефтях преобладают циклопентановые компоненты, в конденсатах – циклогексановые. Ароматические углеводороды в нефтях обычно сосредоточены в высококипящих фракциях, в конденсатах – в низкокипящих. Конденсаты, образовавшиеся за счет преобразования РОВ, наряду с нефтями и газами, можно считать первичными; конденсаты, являющиеся продуктами термобарических превращений, – вторичными
По соотношению отдельных индивидуальных компонентов конденсаты несколько отличаются от нефтей. Конденсаты состоят из более простых нефтяных компонентов, что обусловлено растворяющей способностью газов. В нефтях преобладают циклопентановые компоненты, в конденсатах – циклогексановые. Ароматические углеводороды в нефтях обычно сосредоточены в высококипящих фракциях, в конденсатах – в низкокипящих. Конденсаты, образовавшиеся за счет преобразования РОВ, наряду с нефтями и газами, можно считать первичными; конденсаты, являющиеся продуктами термобарических превращений, – вторичными
 Характерные особенности газоконденсатных залежей – нахождение газа и конденсата в пластовых условиях в однофазовом газообразном состоянии и подчинение их законам ретроградной конденсации. Газоконденсатные залежи отличаются от нефтяных однофазным парообразным состоянием флюида, а от чисто газовых – наличием обратного испарения жидкой фазы (конденсата), выделяющейся в результате снижения давления в системе. Газоконденсаты
Характерные особенности газоконденсатных залежей – нахождение газа и конденсата в пластовых условиях в однофазовом газообразном состоянии и подчинение их законам ретроградной конденсации. Газоконденсатные залежи отличаются от нефтяных однофазным парообразным состоянием флюида, а от чисто газовых – наличием обратного испарения жидкой фазы (конденсата), выделяющейся в результате снижения давления в системе. Газоконденсаты
 «битум» 1) понятие генетическое, включающее каустобиолиты нефтяного ряда. Обязательной чертой является эпигенетичность по отношению к вмещающей породе (миграционная природа скопления); 2) понятие аналитическое (битумоиды), охватывающее природные ОВ, извлекаемые из пород или осадков органическими растворителями. Обязательным признаком является растворимость; 3) понятие техническое, включающее природные асфальты, продукты переработки нефти и т. д. Определяющими являются технические свойства. В. А. Успенским предложено в качестве общего для всех категорий битумов наименование «битуминозные вещества» . природные битумы в генетическом аспекте - большая группа природных органических веществ, образующих с нефтью непрерывные ряды, в которых наблюдаются переходы от жидких и вязких веществ к твердым. Природные битумы
«битум» 1) понятие генетическое, включающее каустобиолиты нефтяного ряда. Обязательной чертой является эпигенетичность по отношению к вмещающей породе (миграционная природа скопления); 2) понятие аналитическое (битумоиды), охватывающее природные ОВ, извлекаемые из пород или осадков органическими растворителями. Обязательным признаком является растворимость; 3) понятие техническое, включающее природные асфальты, продукты переработки нефти и т. д. Определяющими являются технические свойства. В. А. Успенским предложено в качестве общего для всех категорий битумов наименование «битуминозные вещества» . природные битумы в генетическом аспекте - большая группа природных органических веществ, образующих с нефтью непрерывные ряды, в которых наблюдаются переходы от жидких и вязких веществ к твердым. Природные битумы
 Природные битумы классифицируются по содержанию масел и некоторым физическим свойствам Выделяются следующие классы: мальты, асфальты, асфальтиты, кериты, антраксолиты, озокериты. Выделяются еще так называемые оксикериты, представляющие собой продукт выветривания асфальтовых битумов на выходах пластов или жил асфальтов, асфальтитов и керитов, а также гуминокериты – продукт выветривания оксикеритов, элатериты – продукт особого рода превращения алифатического углеводородного материала и альгариты – продукт современной бактериальной переработки парафиновых углеводородов. Природные битумы
Природные битумы классифицируются по содержанию масел и некоторым физическим свойствам Выделяются следующие классы: мальты, асфальты, асфальтиты, кериты, антраксолиты, озокериты. Выделяются еще так называемые оксикериты, представляющие собой продукт выветривания асфальтовых битумов на выходах пластов или жил асфальтов, асфальтитов и керитов, а также гуминокериты – продукт выветривания оксикеритов, элатериты – продукт особого рода превращения алифатического углеводородного материала и альгариты – продукт современной бактериальной переработки парафиновых углеводородов. Природные битумы
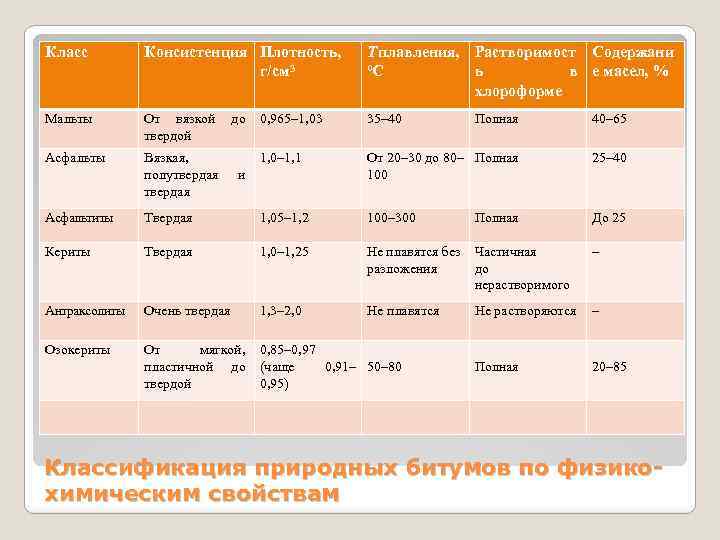 Класс Консистенция Плотность, г/см 3 Т плавления, Растворимост Содержани ºС ь в е масел, % хлороформе Мальты От вязкой до 0, 965– 1, 03 твердой 35– 40 Полная 40– 65 Асфальты Вязкая, полутвердая 1, 0– 1, 1 От 20– 30 до 80– Полная 100 25– 40 До 25 и Асфальтиты Твердая 1, 05– 1, 2 100– 300 Полная Кериты Твердая 1, 0– 1, 25 Не плавятся без Частичная разложения до нерастворимого – Антраксолиты Очень твердая 1, 3– 2, 0 Не плавятся Не растворяются – Озокериты От мягкой, 0, 85– 0, 97 пластичной до (чаще 0, 91– 50– 80 твердой 0, 95) Полная 20– 85 Классификация природных битумов по физикохимическим свойствам
Класс Консистенция Плотность, г/см 3 Т плавления, Растворимост Содержани ºС ь в е масел, % хлороформе Мальты От вязкой до 0, 965– 1, 03 твердой 35– 40 Полная 40– 65 Асфальты Вязкая, полутвердая 1, 0– 1, 1 От 20– 30 до 80– Полная 100 25– 40 До 25 и Асфальтиты Твердая 1, 05– 1, 2 100– 300 Полная Кериты Твердая 1, 0– 1, 25 Не плавятся без Частичная разложения до нерастворимого – Антраксолиты Очень твердая 1, 3– 2, 0 Не плавятся Не растворяются – Озокериты От мягкой, 0, 85– 0, 97 пластичной до (чаще 0, 91– 50– 80 твердой 0, 95) Полная 20– 85 Классификация природных битумов по физикохимическим свойствам
 «Киры» – продукты субаэрального изменения излившейся нефти. В зависимости от степени выветрелости они обладают различной консистенцией – от вязкой до твердой и относятся к классам битумов: мальты – асфальты - асфальтиты – оксикериты – гуминокериты. «Закирование» – процесс образования киров. Битумы являются природными дериватами нефти, их происхождение связано с определенными процессами изменения физико-химических свойств нефти. По запасу ресурсов природные битумы сопоставимы с нефтью. Почти в каждом нефтеносном регионе помимо основных нефтесодержащих имеются битумсодержащие горизонты. Следы ее естественных выходов служат поисковыми признаками при разведке нефти Природные битумы
«Киры» – продукты субаэрального изменения излившейся нефти. В зависимости от степени выветрелости они обладают различной консистенцией – от вязкой до твердой и относятся к классам битумов: мальты – асфальты - асфальтиты – оксикериты – гуминокериты. «Закирование» – процесс образования киров. Битумы являются природными дериватами нефти, их происхождение связано с определенными процессами изменения физико-химических свойств нефти. По запасу ресурсов природные битумы сопоставимы с нефтью. Почти в каждом нефтеносном регионе помимо основных нефтесодержащих имеются битумсодержащие горизонты. Следы ее естественных выходов служат поисковыми признаками при разведке нефти Природные битумы


