e284605c85e23f72e6529ee1d7210162.ppt
- Количество слайдов: 115
 ГЕНОМ ЧЕЛОВЕКА Часть 2: Хромосомный уровень организации
ГЕНОМ ЧЕЛОВЕКА Часть 2: Хромосомный уровень организации
 Хромосомы n Нуклеопротеидные палочковидные структуры эукариотических клеток, видимые во время деления клетки. Функции хромосом: n Информационная Транскрипционная Структурно-организационная обеспечивает точное их воспроизведение при репликации Сегрегационная Рекомбинационная n n
Хромосомы n Нуклеопротеидные палочковидные структуры эукариотических клеток, видимые во время деления клетки. Функции хромосом: n Информационная Транскрипционная Структурно-организационная обеспечивает точное их воспроизведение при репликации Сегрегационная Рекомбинационная n n
 I. Развитие представлений о хромосомах человека. Разработка методик для проведенияя анализа морфологии хромосом 70 -е годы XIX века - О. Гертвиг и В. Флемминг описали окрашиваемые нитевидные структуры в ядрах клеток эукариот 1879 г. – Дж. Арнольд (J. Arnold) – первая визуализация хромосом человека 1888 г. - В. Вальдейер (W. Waldeyer) назвал эти структуры ХРОМОСОМАМИ (chroмa –цвет; soma – тело) 1904 г. – В. Сеттон (W. Sutton) и Т. Бовери (Th. Boveri)– гипотеза о связи хромосом с элементами наследственности 1924 г - Г. А. Левитский ввел термин «кариотип» в современном его понимании. 1934 г. -А. Г. Андрес (совместно с М. С. Навашиным) – впервые в мире провели анализ тонкого морфологического строения десяти наиболее крупных хромосом человека.
I. Развитие представлений о хромосомах человека. Разработка методик для проведенияя анализа морфологии хромосом 70 -е годы XIX века - О. Гертвиг и В. Флемминг описали окрашиваемые нитевидные структуры в ядрах клеток эукариот 1879 г. – Дж. Арнольд (J. Arnold) – первая визуализация хромосом человека 1888 г. - В. Вальдейер (W. Waldeyer) назвал эти структуры ХРОМОСОМАМИ (chroмa –цвет; soma – тело) 1904 г. – В. Сеттон (W. Sutton) и Т. Бовери (Th. Boveri)– гипотеза о связи хромосом с элементами наследственности 1924 г - Г. А. Левитский ввел термин «кариотип» в современном его понимании. 1934 г. -А. Г. Андрес (совместно с М. С. Навашиным) – впервые в мире провели анализ тонкого морфологического строения десяти наиболее крупных хромосом человека.
 II этап – определение модального числа хромосом у человека и детальное описание их морфологии. Рождение цитогенетики. n 1956 г. Тио и Леван определили модальное число хромосом человека n 1959 г. – Ж. Лежен (J. Lejeune) идентифицировал трисомию по хромосоме 21 при синдроме Дауна 1960 г. – Х. Эдвардс (H. Edwards) описал синдром трисомии по хромосоме 18 1960 г. – К. Патау (K. Patau) описал синдром трисомии по хромосоме 13 n n
II этап – определение модального числа хромосом у человека и детальное описание их морфологии. Рождение цитогенетики. n 1956 г. Тио и Леван определили модальное число хромосом человека n 1959 г. – Ж. Лежен (J. Lejeune) идентифицировал трисомию по хромосоме 21 при синдроме Дауна 1960 г. – Х. Эдвардс (H. Edwards) описал синдром трисомии по хромосоме 18 1960 г. – К. Патау (K. Patau) описал синдром трисомии по хромосоме 13 n n
 III этап – появление методов идентификации хромосом и их отдельных районов (конец 60 -х – начало 70 -х годов XX в. ) n n 1968 г. – Т. Касперсон (T. Caspersson) применил для исследования метафазных хромосом метод дифференциальной Q-окраски 1971 г. – М. Дретс (M. Drets) и М. Шау (M. Shaw) использовали GTG-метод дифференциальной окраски хромосом
III этап – появление методов идентификации хромосом и их отдельных районов (конец 60 -х – начало 70 -х годов XX в. ) n n 1968 г. – Т. Касперсон (T. Caspersson) применил для исследования метафазных хромосом метод дифференциальной Q-окраски 1971 г. – М. Дретс (M. Drets) и М. Шау (M. Shaw) использовали GTG-метод дифференциальной окраски хромосом
 IV этап – внедрение и широкое использование молекулярноцитогенетических методов (с 1986 г. ) n 1986 г. - первые молекулярноцитогенетические эксперименты на хромосомах человека – FISH-метод 1992 г. - разработка метода сравнительной геномной гибриидзации (CGH) n A. Kallionieme D. Pinkel
IV этап – внедрение и широкое использование молекулярноцитогенетических методов (с 1986 г. ) n 1986 г. - первые молекулярноцитогенетические эксперименты на хромосомах человека – FISH-метод 1992 г. - разработка метода сравнительной геномной гибриидзации (CGH) n A. Kallionieme D. Pinkel
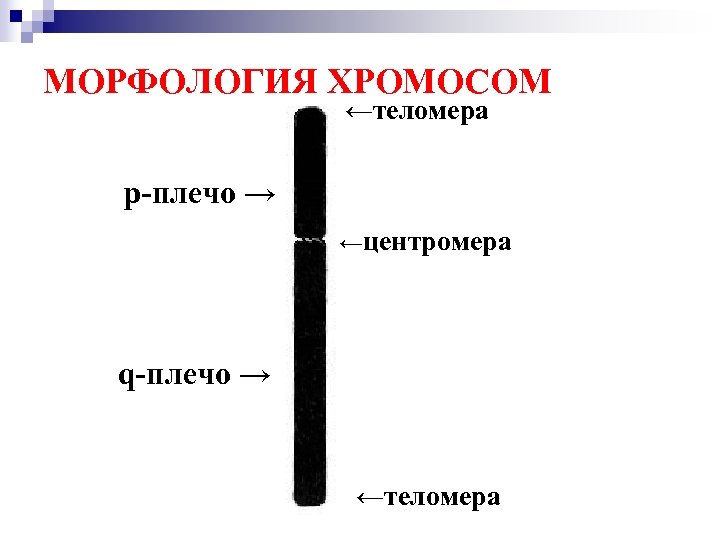 МОРФОЛОГИЯ ХРОМОСОМ ←теломера p-плечо → ←центромера q-плечо → ←теломера
МОРФОЛОГИЯ ХРОМОСОМ ←теломера p-плечо → ←центромера q-плечо → ←теломера
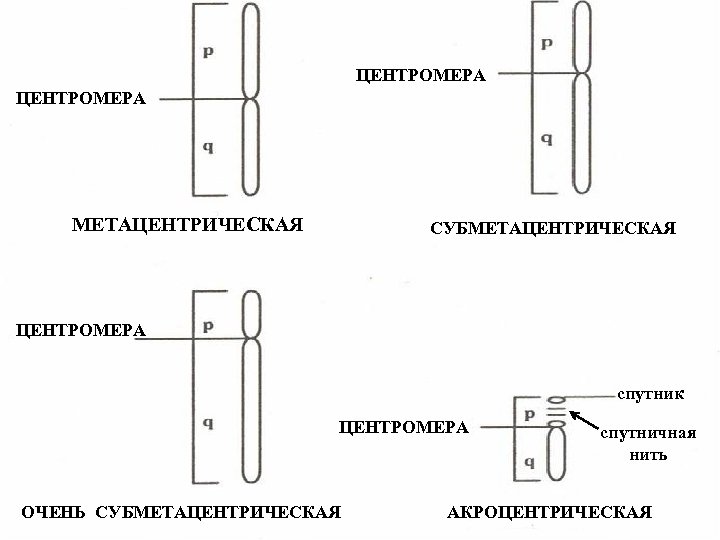 ЦЕНТРОМЕРА МЕТАЦЕНТРИЧЕСКАЯ СУБМЕТАЦЕНТРИЧЕСКАЯ ЦЕНТРОМЕРА спутник ЦЕНТРОМЕРА ОЧЕНЬ СУБМЕТАЦЕНТРИЧЕСКАЯ спутничная нить АКРОЦЕНТРИЧЕСКАЯ
ЦЕНТРОМЕРА МЕТАЦЕНТРИЧЕСКАЯ СУБМЕТАЦЕНТРИЧЕСКАЯ ЦЕНТРОМЕРА спутник ЦЕНТРОМЕРА ОЧЕНЬ СУБМЕТАЦЕНТРИЧЕСКАЯ спутничная нить АКРОЦЕНТРИЧЕСКАЯ
 II. Структурно-функциональная организация хромосом Хромосома содержит одну длинную ТЕЛОМЕРА Белки кинетохора ЦЕНТРОМЕРА ТЕЛОМЕРА (несколько см) линейную молекулу ДНК типы ДНК- последовательностей: 1. Уникальная или неповторяющаяся (гены) 2. Умеренно повторяющаяся 3. Высоко повторяющаяся • Гены локализованы между центромерным и теломерными районами (от нескольких сотен до нескольких тысяч) Ø Повторяющиеся последовательности в основном локализованы в центромерных и теломерных районах, но могут быть диспергированы в других районах хромосом Гены Повторяющиеся последовательности
II. Структурно-функциональная организация хромосом Хромосома содержит одну длинную ТЕЛОМЕРА Белки кинетохора ЦЕНТРОМЕРА ТЕЛОМЕРА (несколько см) линейную молекулу ДНК типы ДНК- последовательностей: 1. Уникальная или неповторяющаяся (гены) 2. Умеренно повторяющаяся 3. Высоко повторяющаяся • Гены локализованы между центромерным и теломерными районами (от нескольких сотен до нескольких тысяч) Ø Повторяющиеся последовательности в основном локализованы в центромерных и теломерных районах, но могут быть диспергированы в других районах хромосом Гены Повторяющиеся последовательности
 ГЕТЕРОХРОМАТИН vs ЭУХРОМАТИН n n Эухроматин n Менее конденсированные районы хромосом n Транскрипционно активен Гетерохроматин n Плотные, компактные (конденсированные) районы хромосом, интенсивно окрашивается. n Обычно выявляются в зоне первичной перетяжки (центромера) n Транскрипционно неактивен (в целом) n Поздно реплицируется в S-фазе митоза (асинхронно с эухроматином)
ГЕТЕРОХРОМАТИН vs ЭУХРОМАТИН n n Эухроматин n Менее конденсированные районы хромосом n Транскрипционно активен Гетерохроматин n Плотные, компактные (конденсированные) районы хромосом, интенсивно окрашивается. n Обычно выявляются в зоне первичной перетяжки (центромера) n Транскрипционно неактивен (в целом) n Поздно реплицируется в S-фазе митоза (асинхронно с эухроматином)
 Виды гетерохроматина • I. Структурный (конституциональный) гетерохроматин • II. Гетерохроматизированные эухроматические районы (факультативный гетерохроматин)
Виды гетерохроматина • I. Структурный (конституциональный) гетерохроматин • II. Гетерохроматизированные эухроматические районы (факультативный гетерохроматин)
 I. Структурный (конституциональный) гетерохроматин n n Стабильно выявляется в хромосомах Генетически инертный (не содержит активно транскрибируемых генов)
I. Структурный (конституциональный) гетерохроматин n n Стабильно выявляется в хромосомах Генетически инертный (не содержит активно транскрибируемых генов)
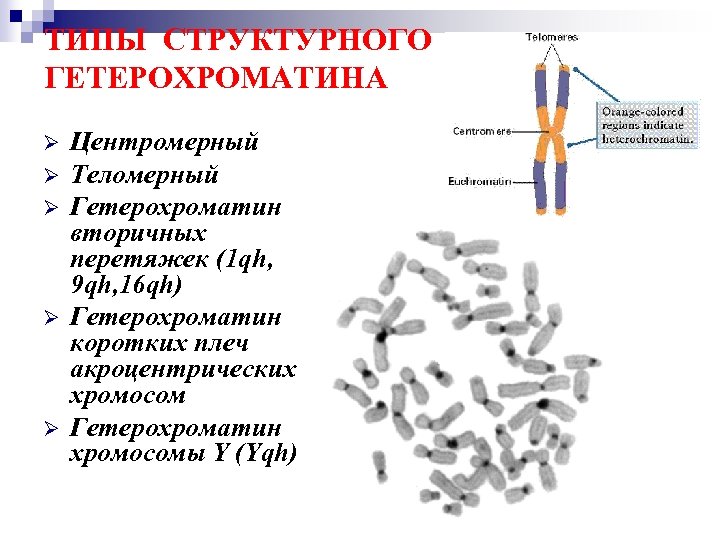 ТИПЫ СТРУКТУРНОГО ГЕТЕРОХРОМАТИНА Ø Ø Ø Центромерный Теломерный Гетерохроматин вторичных перетяжек (1 qh, 9 qh, 16 qh) Гетерохроматин коротких плеч акроцентрических хромосом Гетерохроматин хромосомы Y (Yqh)
ТИПЫ СТРУКТУРНОГО ГЕТЕРОХРОМАТИНА Ø Ø Ø Центромерный Теломерный Гетерохроматин вторичных перетяжек (1 qh, 9 qh, 16 qh) Гетерохроматин коротких плеч акроцентрических хромосом Гетерохроматин хромосомы Y (Yqh)
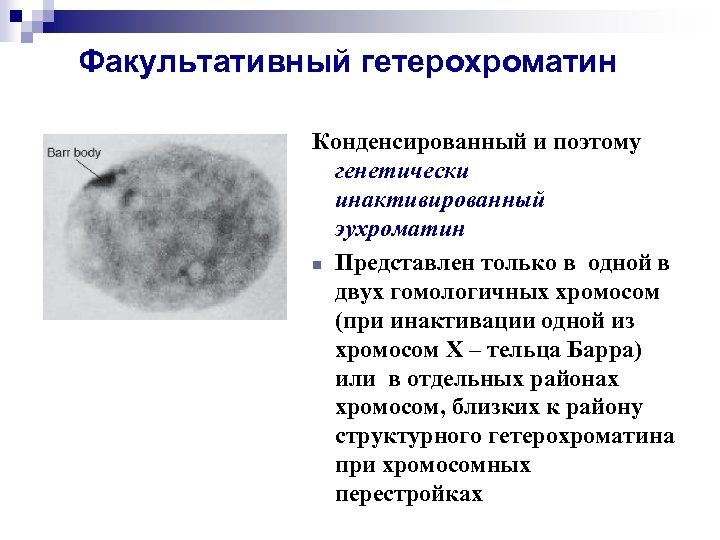 Факультативный гетерохроматин Конденсированный и поэтому генетически инактивированный эухроматин n Представлен только в одной в двух гомологичных хромосом (при инактивации одной из хромосом X – тельца Барра) или в отдельных районах хромосом, близких к району структурного гетерохроматина при хромосомных перестройках
Факультативный гетерохроматин Конденсированный и поэтому генетически инактивированный эухроматин n Представлен только в одной в двух гомологичных хромосом (при инактивации одной из хромосом X – тельца Барра) или в отдельных районах хромосом, близких к району структурного гетерохроматина при хромосомных перестройках
 n ХРОМОСОМЫ ЛОКАЛИЗОВАНЫ В ЯДРЕ КЛЕТКИ n должна быть высокая степень компактизации нити ДНК, которая обеспечивается при ее связывании с различными белками ДНК + БЕЛКИ ХРОМОСОМ = ХРОМАТИН
n ХРОМОСОМЫ ЛОКАЛИЗОВАНЫ В ЯДРЕ КЛЕТКИ n должна быть высокая степень компактизации нити ДНК, которая обеспечивается при ее связывании с различными белками ДНК + БЕЛКИ ХРОМОСОМ = ХРОМАТИН
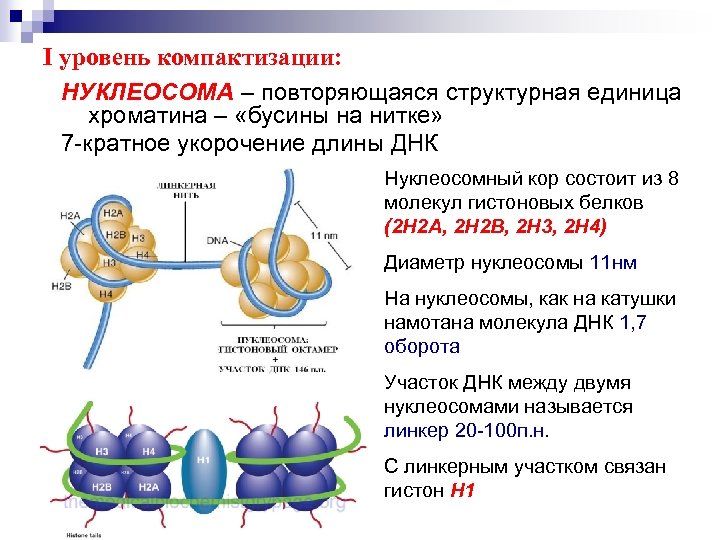 I уровень компактизации: НУКЛЕОСОМА – повторяющаяся структурная единица хроматина – «бусины на нитке» 7 -кратное укорочение длины ДНК Нуклеосомный кор состоит из 8 молекул гистоновых белков (2 H 2 A, 2 H 2 B, 2 H 3, 2 H 4) Диаметр нуклеосомы 11 нм На нуклеосомы, как на катушки намотана молекула ДНК 1, 7 оборота Участок ДНК между двумя нуклеосомами называется линкер 20 -100 п. н. С линкерным участком связан гистон Н 1
I уровень компактизации: НУКЛЕОСОМА – повторяющаяся структурная единица хроматина – «бусины на нитке» 7 -кратное укорочение длины ДНК Нуклеосомный кор состоит из 8 молекул гистоновых белков (2 H 2 A, 2 H 2 B, 2 H 3, 2 H 4) Диаметр нуклеосомы 11 нм На нуклеосомы, как на катушки намотана молекула ДНК 1, 7 оборота Участок ДНК между двумя нуклеосомами называется линкер 20 -100 п. н. С линкерным участком связан гистон Н 1
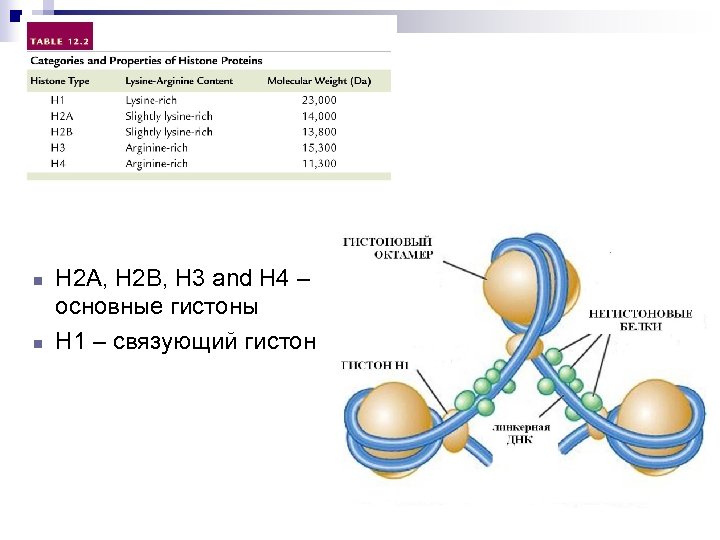 n n H 2 A, H 2 B, H 3 and H 4 – основные гистоны H 1 – связующий гистон
n n H 2 A, H 2 B, H 3 and H 4 – основные гистоны H 1 – связующий гистон
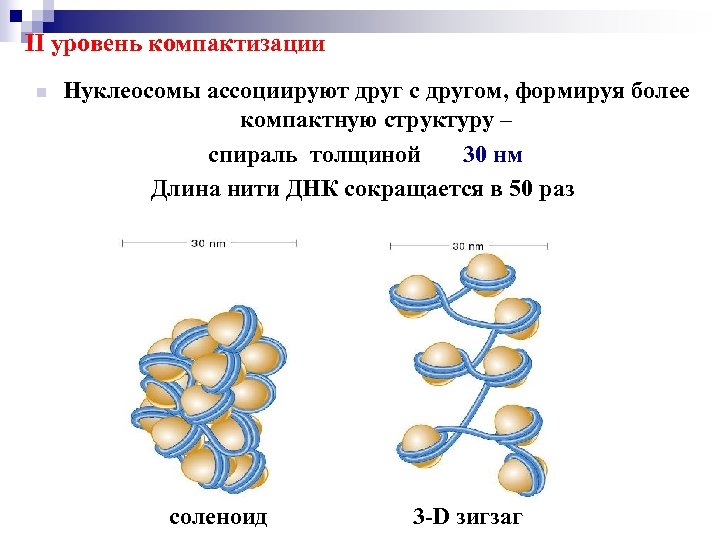 II уровень компактизации n Нуклеосомы ассоциируют друг с другом, формируя более компактную структуру – спираль толщиной 30 нм Длина нити ДНК сокращается в 50 раз соленоид 3 -D зигзаг
II уровень компактизации n Нуклеосомы ассоциируют друг с другом, формируя более компактную структуру – спираль толщиной 30 нм Длина нити ДНК сокращается в 50 раз соленоид 3 -D зигзаг
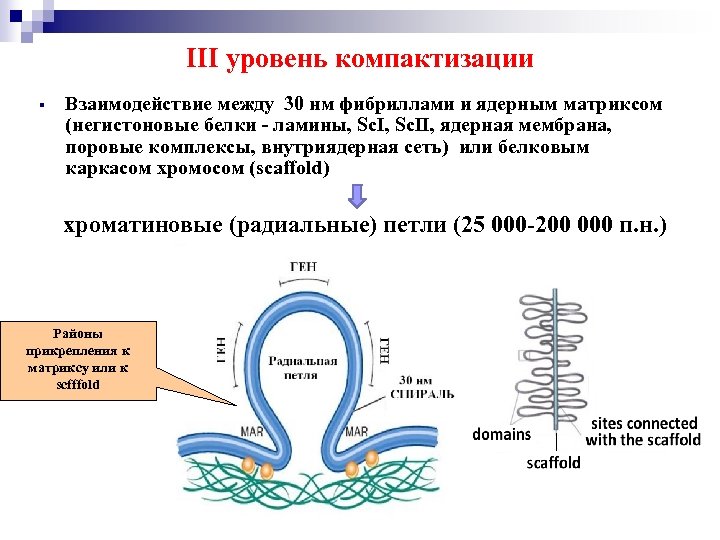 III уровень компактизации Взаимодействие между 30 нм фибриллами и ядерным матриксом (негистоновые белки - ламины, Sc. II, ядерная мембрана, поровые комплексы, внутриядерная сеть) или белковым каркасом хромосом (scaffold) § хроматиновые (радиальные) петли (25 000 -200 000 п. н. ) Районы прикрепления к матриксу или к scfffold
III уровень компактизации Взаимодействие между 30 нм фибриллами и ядерным матриксом (негистоновые белки - ламины, Sc. II, ядерная мембрана, поровые комплексы, внутриядерная сеть) или белковым каркасом хромосом (scaffold) § хроматиновые (радиальные) петли (25 000 -200 000 п. н. ) Районы прикрепления к матриксу или к scfffold
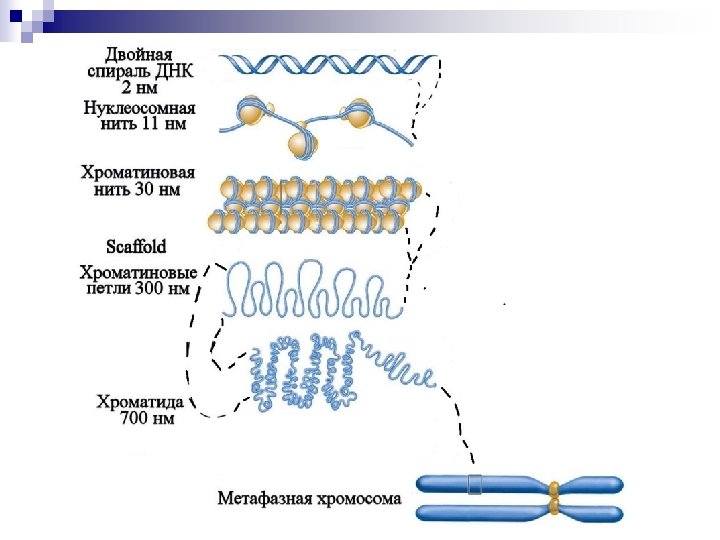
 ЦЕНТРОМЕРНЫЙ РАЙОН ХРОМОСОМЫ Центромера - это структура, обеспечивающая удержание хромосом, правильность выстраивания хромосом в метафазной пластинке и их прикрепление к веретену; участок, ответственный за контроль наступления анафазы Центромера включает: 1. Кинетохор Белки кинетохора ЦЕНТРОМЕРА 2. Центромерный хроматин 3. Центромерный район (район, включающий различные домены, расположенные рядом с центромерным локусом)
ЦЕНТРОМЕРНЫЙ РАЙОН ХРОМОСОМЫ Центромера - это структура, обеспечивающая удержание хромосом, правильность выстраивания хромосом в метафазной пластинке и их прикрепление к веретену; участок, ответственный за контроль наступления анафазы Центромера включает: 1. Кинетохор Белки кинетохора ЦЕНТРОМЕРА 2. Центромерный хроматин 3. Центромерный район (район, включающий различные домены, расположенные рядом с центромерным локусом)
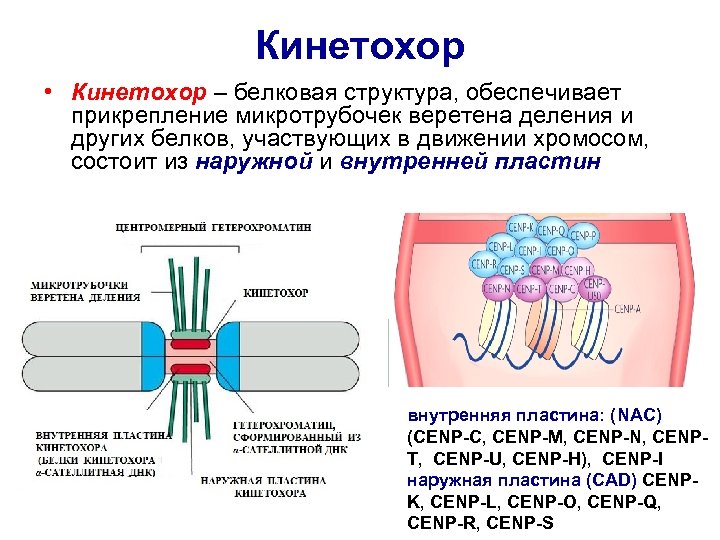 Кинетохор • Кинетохор – белковая структура, обеспечивает прикрепление микротрубочек веретена деления и других белков, участвующих в движении хромосом, состоит из наружной и внутренней пластин внутренняя пластина: (NAC) (CENP-С, CENP-М, CENP-N, CENPT, CENP-U, CENP-H), CENP-I наружная пластина (CAD) CENPK, CENP-L, CENP-O, CENP-Q, CENP-R, CENP-S
Кинетохор • Кинетохор – белковая структура, обеспечивает прикрепление микротрубочек веретена деления и других белков, участвующих в движении хромосом, состоит из наружной и внутренней пластин внутренняя пластина: (NAC) (CENP-С, CENP-М, CENP-N, CENPT, CENP-U, CENP-H), CENP-I наружная пластина (CAD) CENPK, CENP-L, CENP-O, CENP-Q, CENP-R, CENP-S
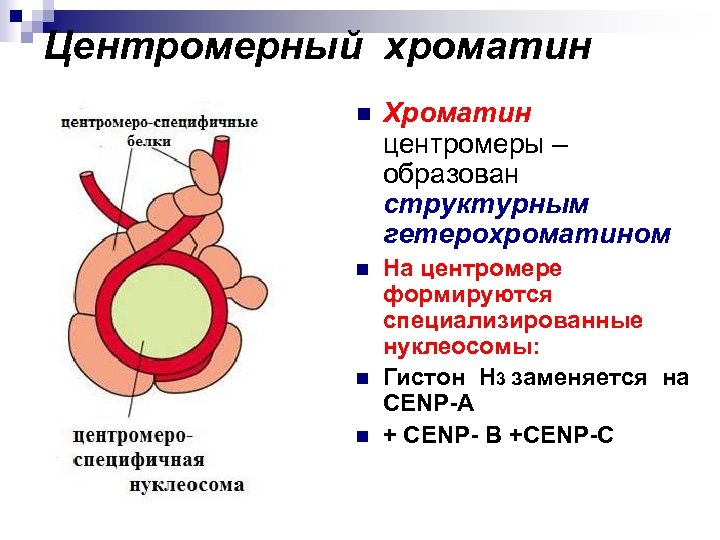 Центромерный хроматин n Хроматин центромеры – образован структурным гетерохроматином n На центромере формируются специализированные нуклеосомы: Гистон Н 3 заменяется на CENP-A + CENP- B +CENP-C n n
Центромерный хроматин n Хроматин центромеры – образован структурным гетерохроматином n На центромере формируются специализированные нуклеосомы: Гистон Н 3 заменяется на CENP-A + CENP- B +CENP-C n n
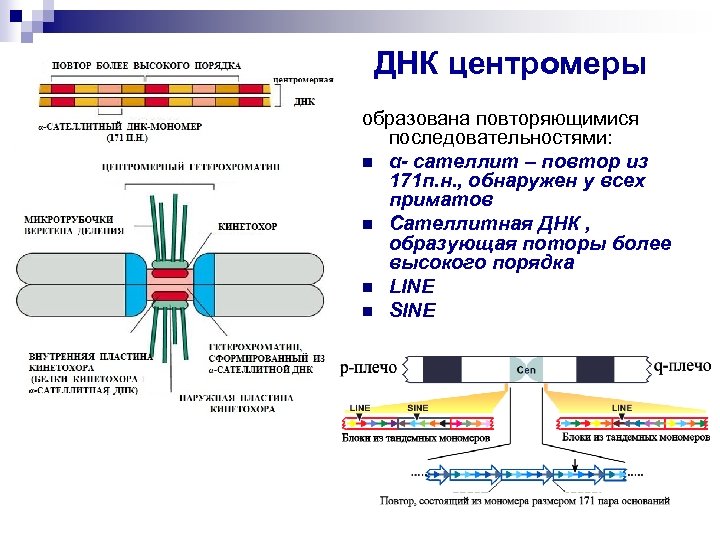 ДНК центромеры образована повторяющимися последовательностями: n α- сателлит – повтор из 171 п. н. , обнаружен у всех приматов n Сателлитная ДНК , образующая поторы более высокого порядка n LINE n SINE
ДНК центромеры образована повторяющимися последовательностями: n α- сателлит – повтор из 171 п. н. , обнаружен у всех приматов n Сателлитная ДНК , образующая поторы более высокого порядка n LINE n SINE
 ТЕЛОМЕРЫ • Теломеры представляют собой в основном двунитевые некодирующие повторы (TTAGGG)n, заканчивающиеся 3’однонитевым участком • Размер двунитевого участка варьирует от 3 до 20 т. п. н. , однонитевого – от 100 до 200 пар оснований Основной функцией теломер является сохранение целостности хромосомы и обеспечение ее полной репликации.
ТЕЛОМЕРЫ • Теломеры представляют собой в основном двунитевые некодирующие повторы (TTAGGG)n, заканчивающиеся 3’однонитевым участком • Размер двунитевого участка варьирует от 3 до 20 т. п. н. , однонитевого – от 100 до 200 пар оснований Основной функцией теломер является сохранение целостности хромосомы и обеспечение ее полной репликации.
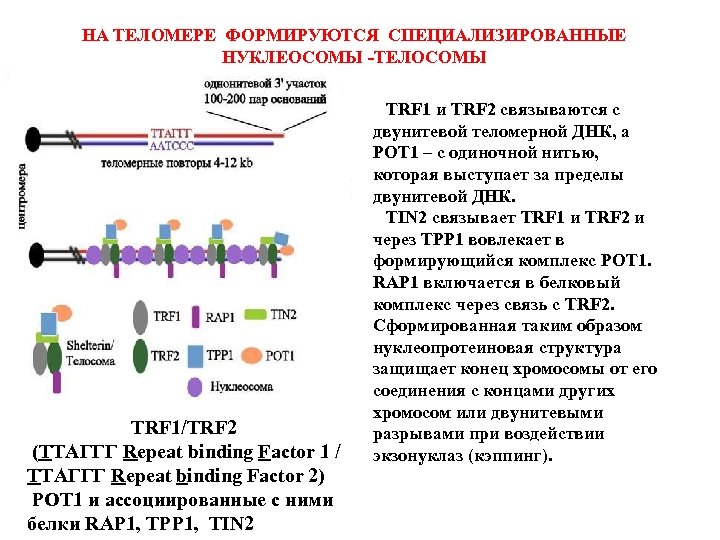 НА ТЕЛОМЕРЕ ФОРМИРУЮТСЯ СПЕЦИАЛИЗИРОВАННЫЕ НУКЛЕОСОМЫ -ТЕЛОСОМЫ TRF 1/TRF 2 (ТТАГГГ Repeat binding Factor 1 / ТТАГГГ Repeat binding Factor 2) POT 1 и ассоциированные с ними белки RAP 1, TPP 1, TIN 2 TRF 1 и TRF 2 связываются с двунитевой теломерной ДНК, а РОТ 1 – с одиночной нитью, которая выступает за пределы двунитевой ДНК. TIN 2 связывает TRF 1 и TRF 2 и через TPP 1 вовлекает в формирующийся комплекс POT 1. RAP 1 включается в белковый комплекс через связь с TRF 2. Сформированная таким образом нуклеопротеиновая структура защищает конец хромосомы от его соединения с концами других хромосом или двунитевыми разрывами при воздействии экзонуклаз (кэппинг).
НА ТЕЛОМЕРЕ ФОРМИРУЮТСЯ СПЕЦИАЛИЗИРОВАННЫЕ НУКЛЕОСОМЫ -ТЕЛОСОМЫ TRF 1/TRF 2 (ТТАГГГ Repeat binding Factor 1 / ТТАГГГ Repeat binding Factor 2) POT 1 и ассоциированные с ними белки RAP 1, TPP 1, TIN 2 TRF 1 и TRF 2 связываются с двунитевой теломерной ДНК, а РОТ 1 – с одиночной нитью, которая выступает за пределы двунитевой ДНК. TIN 2 связывает TRF 1 и TRF 2 и через TPP 1 вовлекает в формирующийся комплекс POT 1. RAP 1 включается в белковый комплекс через связь с TRF 2. Сформированная таким образом нуклеопротеиновая структура защищает конец хромосомы от его соединения с концами других хромосом или двунитевыми разрывами при воздействии экзонуклаз (кэппинг).
 Теломераза • Фермент теломераза обеспечивает репликацию теломерной днк • Резкое уменьшение активности теломеразы и укорочение теломер обычно сопутствует клеточной дифференцировке Ø Часто наблюдается зависимость размера теломеры от возраста человека (возраст-зависимое прогрессивное укорочение теломер) • Феномен репликативного старения клеток, вызванного концевой недорепликацией ДНК, был предсказан А. Оловниковым в 1971 г. За биохимическое доказательство его идеи Э. Блэкберн (E. Blackburn), К. Грейдер (C. Greider) и Д. Шостак (J. Szostak) были удостоены в 2009 г. Нобелевской премии по физиологии и медицине. Ø Нарушение организации теломерных районов приводит к хромосомным перестройкам
Теломераза • Фермент теломераза обеспечивает репликацию теломерной днк • Резкое уменьшение активности теломеразы и укорочение теломер обычно сопутствует клеточной дифференцировке Ø Часто наблюдается зависимость размера теломеры от возраста человека (возраст-зависимое прогрессивное укорочение теломер) • Феномен репликативного старения клеток, вызванного концевой недорепликацией ДНК, был предсказан А. Оловниковым в 1971 г. За биохимическое доказательство его идеи Э. Блэкберн (E. Blackburn), К. Грейдер (C. Greider) и Д. Шостак (J. Szostak) были удостоены в 2009 г. Нобелевской премии по физиологии и медицине. Ø Нарушение организации теломерных районов приводит к хромосомным перестройкам
 Ядрышко-образующие районы хромосом Окраска азотнокислым серебром (Ag-NOR) • Короткие плечи акроцентрических хромосом человека (13, 14, 15, 21 и 22 пары) содержат ядрышкообразующие районы (ЯОР) • На препаратах метафазных хромосом активные ЯО-районы выявляются как вторичные перетяжки и окрашиваются азотнокислым серебром
Ядрышко-образующие районы хромосом Окраска азотнокислым серебром (Ag-NOR) • Короткие плечи акроцентрических хромосом человека (13, 14, 15, 21 и 22 пары) содержат ядрышкообразующие районы (ЯОР) • На препаратах метафазных хромосом активные ЯО-районы выявляются как вторичные перетяжки и окрашиваются азотнокислым серебром
 • ЯОР всех пяти пар хромосом в интерфазе участвуют в образовании ядрышка
• ЯОР всех пяти пар хромосом в интерфазе участвуют в образовании ядрышка
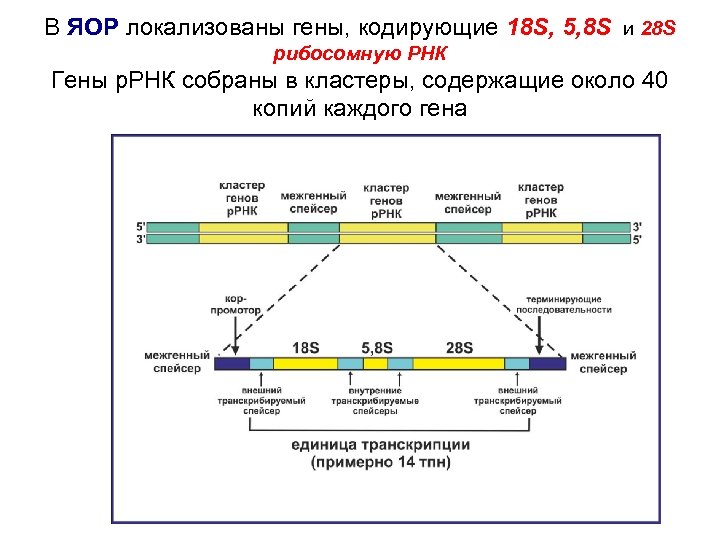 В ЯОР локализованы гены, кодирующие 18 S, 5, 8 S и 28 S рибосомную РНК Гены р. РНК собраны в кластеры, содержащие около 40 копий каждого гена
В ЯОР локализованы гены, кодирующие 18 S, 5, 8 S и 28 S рибосомную РНК Гены р. РНК собраны в кластеры, содержащие около 40 копий каждого гена
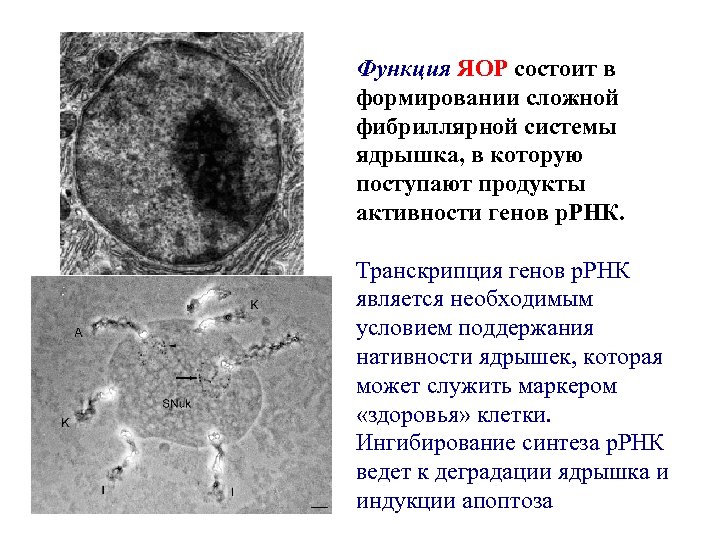 Функция ЯОР состоит в формировании сложной фибриллярной системы ядрышка, в которую поступают продукты активности генов р. РНК. Транскрипция генов р. РНК является необходимым условием поддержания нативности ядрышек, которая может служить маркером «здоровья» клетки. Ингибирование синтеза р. РНК ведет к деградации ядрышка и индукции апоптоза
Функция ЯОР состоит в формировании сложной фибриллярной системы ядрышка, в которую поступают продукты активности генов р. РНК. Транскрипция генов р. РНК является необходимым условием поддержания нативности ядрышек, которая может служить маркером «здоровья» клетки. Ингибирование синтеза р. РНК ведет к деградации ядрышка и индукции апоптоза
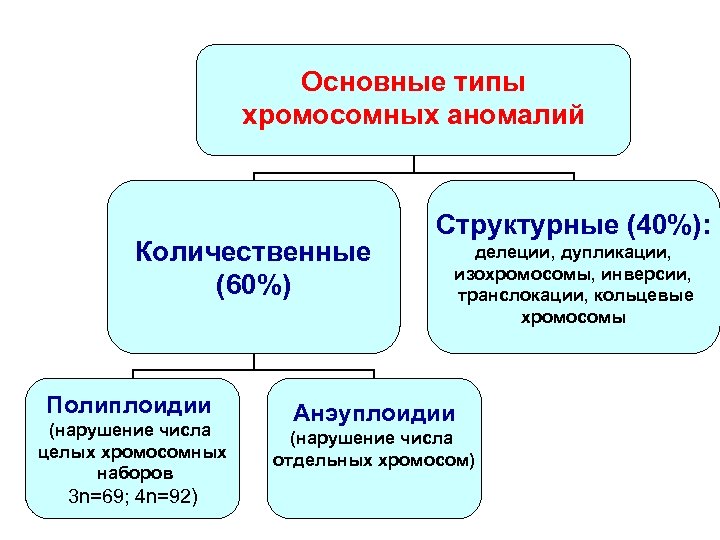 Основные типы хромосомных аномалий Количественные (60%) Полиплоидии (нарушение числа целых хромосомных наборов 3 n=69; 4 n=92) Структурные (40%): делеции, дупликации, изохромосомы, инверсии, транслокации, кольцевые хромосомы Анэуплоидии (нарушение числа отдельных хромосом)
Основные типы хромосомных аномалий Количественные (60%) Полиплоидии (нарушение числа целых хромосомных наборов 3 n=69; 4 n=92) Структурные (40%): делеции, дупликации, изохромосомы, инверсии, транслокации, кольцевые хромосомы Анэуплоидии (нарушение числа отдельных хромосом)
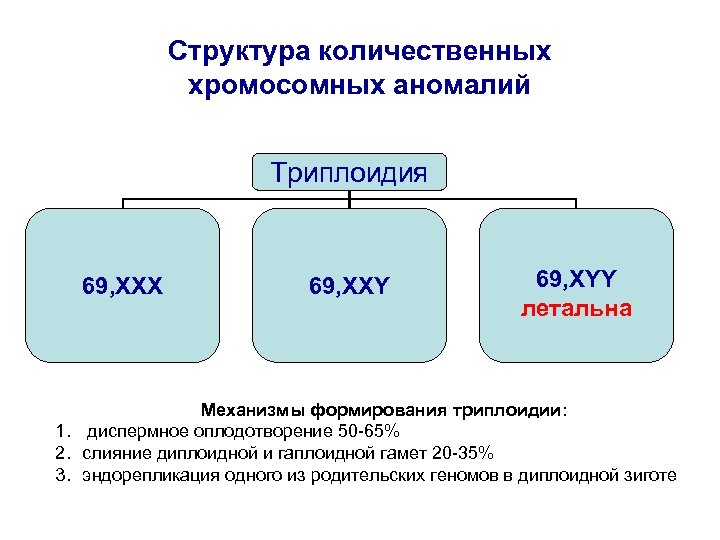 Структура количественных хромосомных аномалий Триплоидия 69, XXX 69, XXY 69, XYY летальна Механизмы формирования триплоидии: 1. диспермное оплодотворение 50 -65% 2. слияние диплоидной и гаплоидной гамет 20 -35% 3. эндорепликация одного из родительских геномов в диплоидной зиготе
Структура количественных хромосомных аномалий Триплоидия 69, XXX 69, XXY 69, XYY летальна Механизмы формирования триплоидии: 1. диспермное оплодотворение 50 -65% 2. слияние диплоидной и гаплоидной гамет 20 -35% 3. эндорепликация одного из родительских геномов в диплоидной зиготе
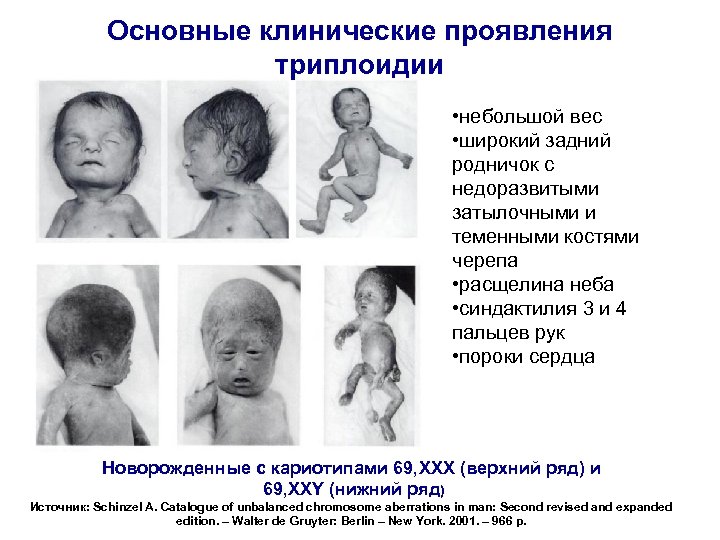 Основные клинические проявления триплоидии • небольшой вес • широкий задний родничок с недоразвитыми затылочными и теменными костями черепа • расщелина неба • синдактилия 3 и 4 пальцев рук • пороки сердца Новорожденные с кариотипами 69, XXX (верхний ряд) и 69, XXY (нижний ряд) Источник: Schinzel A. Catalogue of unbalanced chromosome aberrations in man: Second revised and expanded edition. – Walter de Gruyter: Berlin – New York. 2001. – 966 p.
Основные клинические проявления триплоидии • небольшой вес • широкий задний родничок с недоразвитыми затылочными и теменными костями черепа • расщелина неба • синдактилия 3 и 4 пальцев рук • пороки сердца Новорожденные с кариотипами 69, XXX (верхний ряд) и 69, XXY (нижний ряд) Источник: Schinzel A. Catalogue of unbalanced chromosome aberrations in man: Second revised and expanded edition. – Walter de Gruyter: Berlin – New York. 2001. – 966 p.
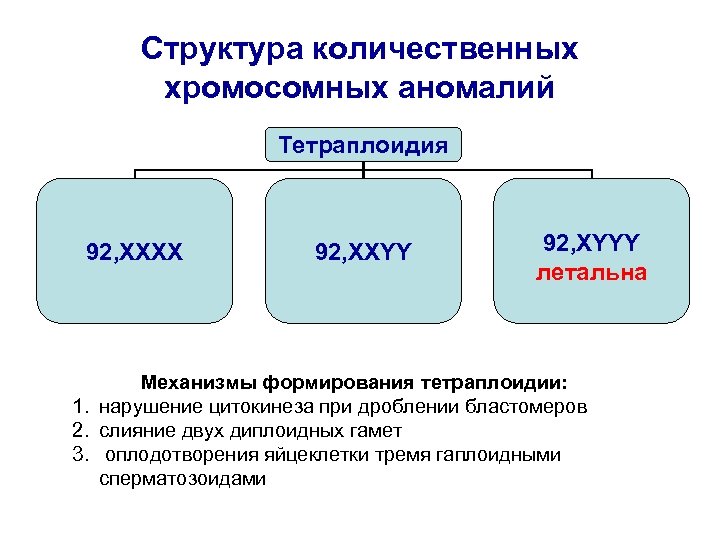 Структура количественных хромосомных аномалий Тетраплоидия 92, XXXX 92, XXYY 92, XYYY летальна Механизмы формирования тетраплоидии: 1. нарушение цитокинеза при дроблении бластомеров 2. слияние двух диплоидных гамет 3. оплодотворения яйцеклетки тремя гаплоидными сперматозоидами
Структура количественных хромосомных аномалий Тетраплоидия 92, XXXX 92, XXYY 92, XYYY летальна Механизмы формирования тетраплоидии: 1. нарушение цитокинеза при дроблении бластомеров 2. слияние двух диплоидных гамет 3. оплодотворения яйцеклетки тремя гаплоидными сперматозоидами
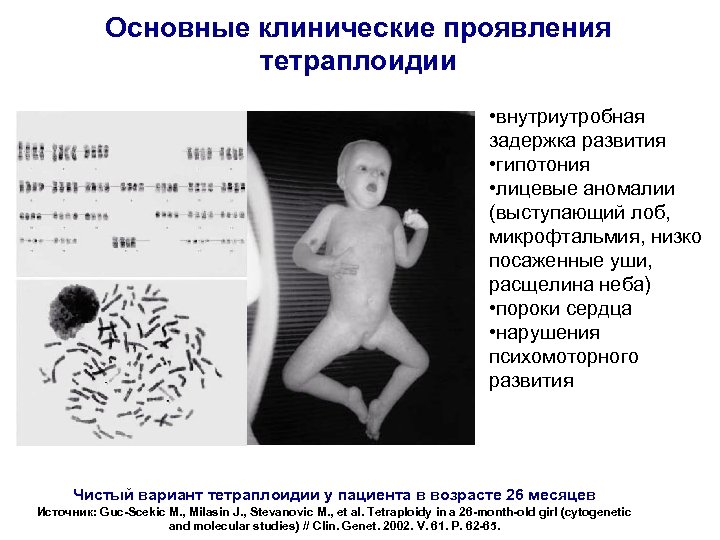 Основные клинические проявления тетраплоидии • внутриутробная задержка развития • гипотония • лицевые аномалии (выступающий лоб, микрофтальмия, низко посаженные уши, расщелина неба) • пороки сердца • нарушения психомоторного развития Чистый вариант тетраплоидии у пациента в возрасте 26 месяцев Источник: Guc-Scekic M. , Milasin J. , Stevanovic M. , et al. Tetraploidy in a 26 -month-old girl (cytogenetic and molecular studies) // Clin. Genet. 2002. V. 61. P. 62 -65.
Основные клинические проявления тетраплоидии • внутриутробная задержка развития • гипотония • лицевые аномалии (выступающий лоб, микрофтальмия, низко посаженные уши, расщелина неба) • пороки сердца • нарушения психомоторного развития Чистый вариант тетраплоидии у пациента в возрасте 26 месяцев Источник: Guc-Scekic M. , Milasin J. , Stevanovic M. , et al. Tetraploidy in a 26 -month-old girl (cytogenetic and molecular studies) // Clin. Genet. 2002. V. 61. P. 62 -65.
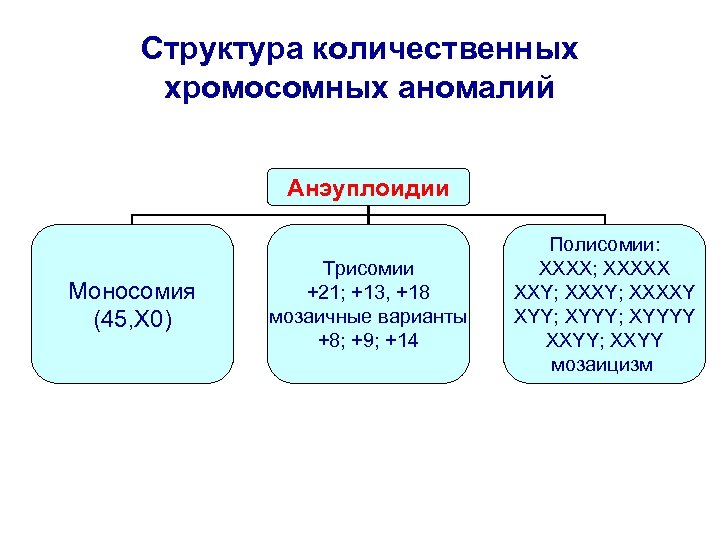 Структура количественных хромосомных аномалий Анэуплоидии Моносомия (45, X 0) Трисомии +21; +13, +18 мозаичные варианты +8; +9; +14 Полисомии: XXXX; XXXXX XXY; XXXXY XYY; XYYYY XXYY; XXYY мозаицизм
Структура количественных хромосомных аномалий Анэуплоидии Моносомия (45, X 0) Трисомии +21; +13, +18 мозаичные варианты +8; +9; +14 Полисомии: XXXX; XXXXX XXY; XXXXY XYY; XYYYY XXYY; XXYY мозаицизм
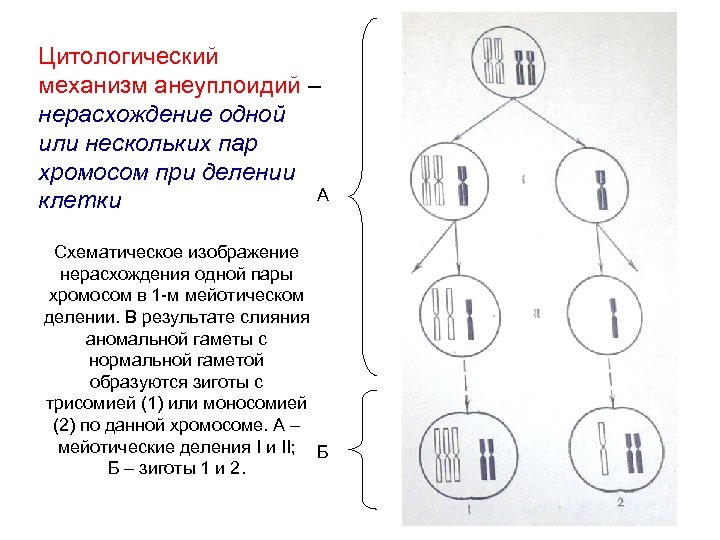 Цитологический механизм анеуплоидий – нерасхождение одной или нескольких пар хромосом при делении А клетки Схематическое изображение нерасхождения одной пары хромосом в 1 -м мейотическом делении. В результате слияния аномальной гаметы с нормальной гаметой образуются зиготы с трисомией (1) или моносомией (2) по данной хромосоме. А – мейотические деления I и II; Б Б – зиготы 1 и 2.
Цитологический механизм анеуплоидий – нерасхождение одной или нескольких пар хромосом при делении А клетки Схематическое изображение нерасхождения одной пары хромосом в 1 -м мейотическом делении. В результате слияния аномальной гаметы с нормальной гаметой образуются зиготы с трисомией (1) или моносомией (2) по данной хромосоме. А – мейотические деления I и II; Б Б – зиготы 1 и 2.
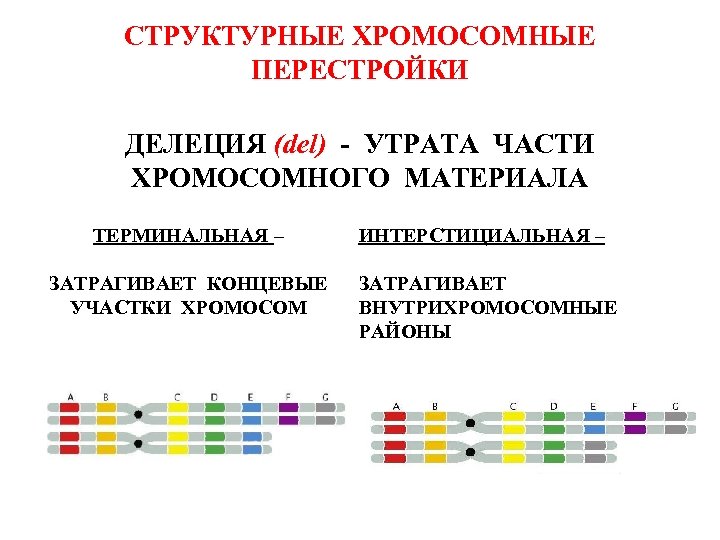 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ДЕЛЕЦИЯ (del) - УТРАТА ЧАСТИ ХРОМОСОМНОГО МАТЕРИАЛА ТЕРМИНАЛЬНАЯ – ЗАТРАГИВАЕТ КОНЦЕВЫЕ УЧАСТКИ ХРОМОСОМ ИНТЕРСТИЦИАЛЬНАЯ – ЗАТРАГИВАЕТ ВНУТРИХРОМОСОМНЫЕ РАЙОНЫ
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ДЕЛЕЦИЯ (del) - УТРАТА ЧАСТИ ХРОМОСОМНОГО МАТЕРИАЛА ТЕРМИНАЛЬНАЯ – ЗАТРАГИВАЕТ КОНЦЕВЫЕ УЧАСТКИ ХРОМОСОМ ИНТЕРСТИЦИАЛЬНАЯ – ЗАТРАГИВАЕТ ВНУТРИХРОМОСОМНЫЕ РАЙОНЫ
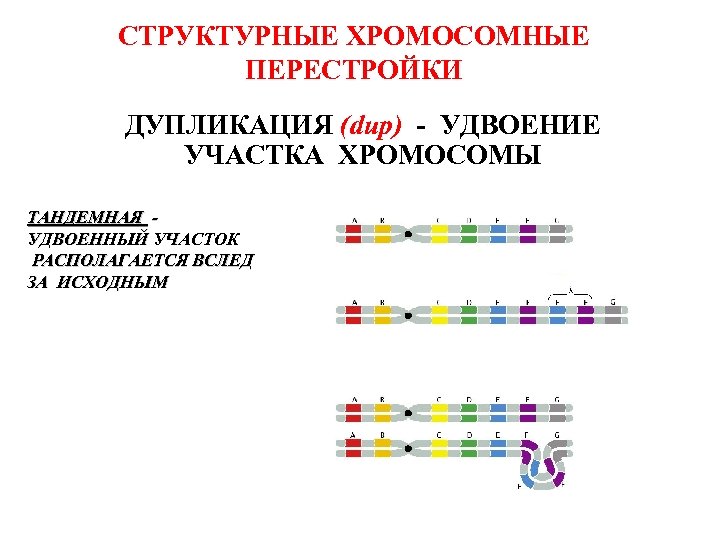 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ДУПЛИКАЦИЯ (dup) - УДВОЕНИЕ УЧАСТКА ХРОМОСОМЫ ТАНДЕМНАЯ УДВОЕННЫЙ УЧАСТОК РАСПОЛАГАЕТСЯ ВСЛЕД ЗА ИСХОДНЫМ
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ДУПЛИКАЦИЯ (dup) - УДВОЕНИЕ УЧАСТКА ХРОМОСОМЫ ТАНДЕМНАЯ УДВОЕННЫЙ УЧАСТОК РАСПОЛАГАЕТСЯ ВСЛЕД ЗА ИСХОДНЫМ
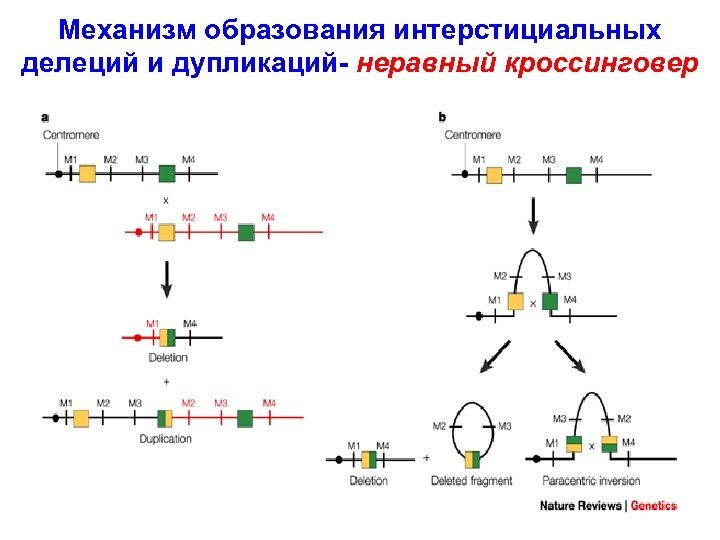 Механизм образования интерстициальных делеций и дупликаций- неравный кроссинговер
Механизм образования интерстициальных делеций и дупликаций- неравный кроссинговер
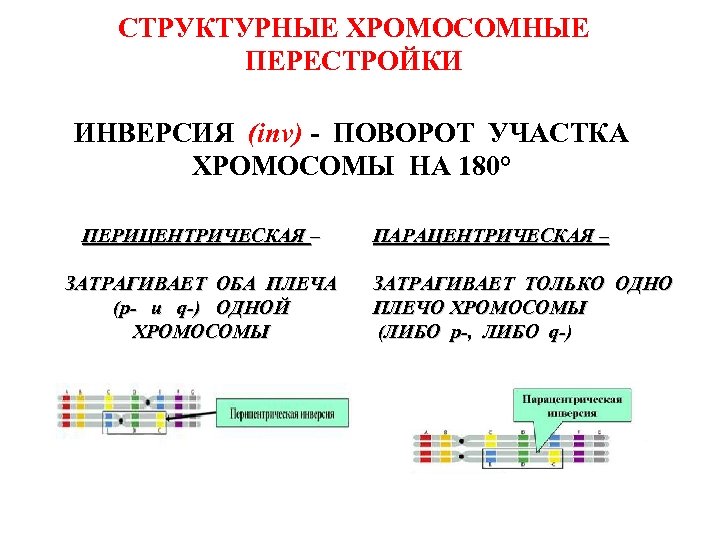 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИНВЕРСИЯ (inv) - ПОВОРОТ УЧАСТКА ХРОМОСОМЫ НА 180° ПЕРИЦЕНТРИЧЕСКАЯ – ЗАТРАГИВАЕТ ОБА ПЛЕЧА (p- и q-) ОДНОЙ ХРОМОСОМЫ ПАРАЦЕНТРИЧЕСКАЯ – ЗАТРАГИВАЕТ ТОЛЬКО ОДНО ПЛЕЧО ХРОМОСОМЫ (ЛИБО p-, ЛИБО q-)
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИНВЕРСИЯ (inv) - ПОВОРОТ УЧАСТКА ХРОМОСОМЫ НА 180° ПЕРИЦЕНТРИЧЕСКАЯ – ЗАТРАГИВАЕТ ОБА ПЛЕЧА (p- и q-) ОДНОЙ ХРОМОСОМЫ ПАРАЦЕНТРИЧЕСКАЯ – ЗАТРАГИВАЕТ ТОЛЬКО ОДНО ПЛЕЧО ХРОМОСОМЫ (ЛИБО p-, ЛИБО q-)
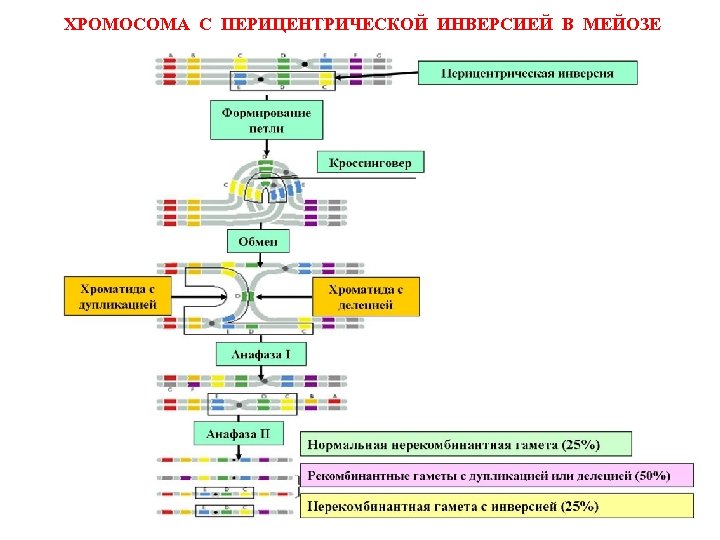 ХРОМОСОМА С ПЕРИЦЕНТРИЧЕСКОЙ ИНВЕРСИЕЙ В МЕЙОЗЕ
ХРОМОСОМА С ПЕРИЦЕНТРИЧЕСКОЙ ИНВЕРСИЕЙ В МЕЙОЗЕ
 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИНСЕРЦИЯ (ins)- ВСТАВКА ФРАГМЕНТА ХРОМОСОМЫ ИНТРАХРОМОСОМНАЯ (внутрихромосомная) – ИНТЕРХРОМОСОМНАЯ (межхромосомная) – вставка фрагмента одной вставка фрагмента хромосомы в другой район одной хромосомы в другой той же самой хромосомы район другой негомологичной хромосмоы
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИНСЕРЦИЯ (ins)- ВСТАВКА ФРАГМЕНТА ХРОМОСОМЫ ИНТРАХРОМОСОМНАЯ (внутрихромосомная) – ИНТЕРХРОМОСОМНАЯ (межхромосомная) – вставка фрагмента одной вставка фрагмента хромосомы в другой район одной хромосомы в другой той же самой хромосомы район другой негомологичной хромосмоы
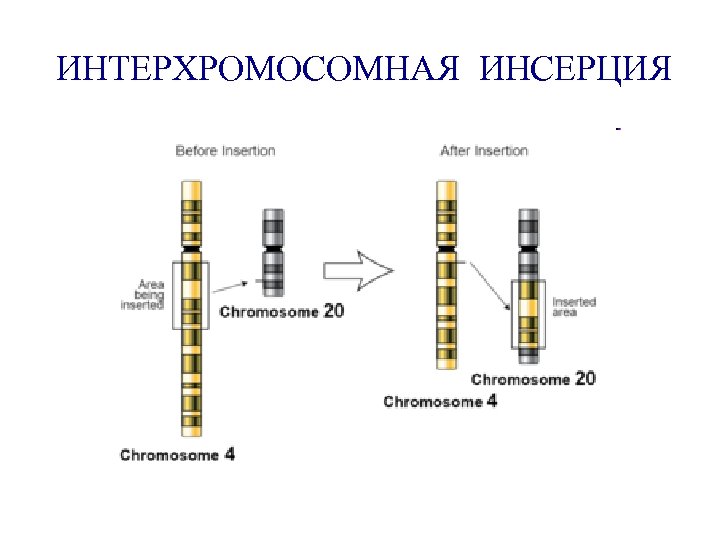 ИНТЕРХРОМОСОМНАЯ ИНСЕРЦИЯ
ИНТЕРХРОМОСОМНАЯ ИНСЕРЦИЯ
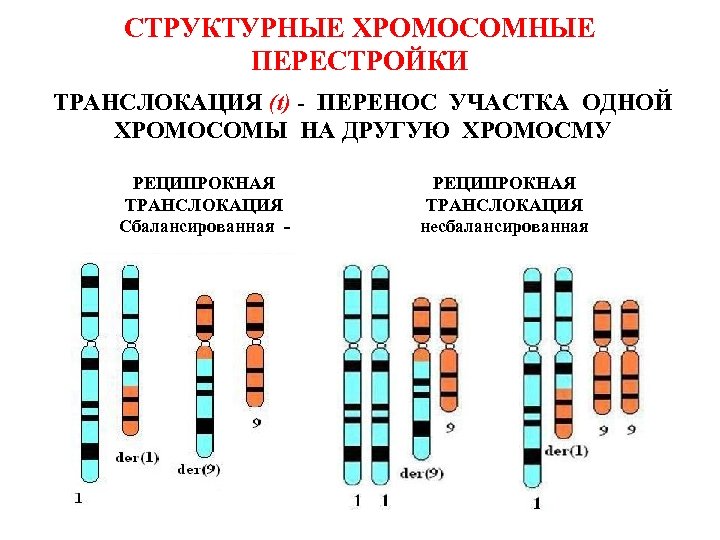 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ТРАНСЛОКАЦИЯ (t) - ПЕРЕНОС УЧАСТКА ОДНОЙ ХРОМОСОМЫ НА ДРУГУЮ ХРОМОСМУ РЕЦИПРОКНАЯ ТРАНСЛОКАЦИЯ Сбалансированная - РЕЦИПРОКНАЯ ТРАНСЛОКАЦИЯ несбалансированная
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ТРАНСЛОКАЦИЯ (t) - ПЕРЕНОС УЧАСТКА ОДНОЙ ХРОМОСОМЫ НА ДРУГУЮ ХРОМОСМУ РЕЦИПРОКНАЯ ТРАНСЛОКАЦИЯ Сбалансированная - РЕЦИПРОКНАЯ ТРАНСЛОКАЦИЯ несбалансированная
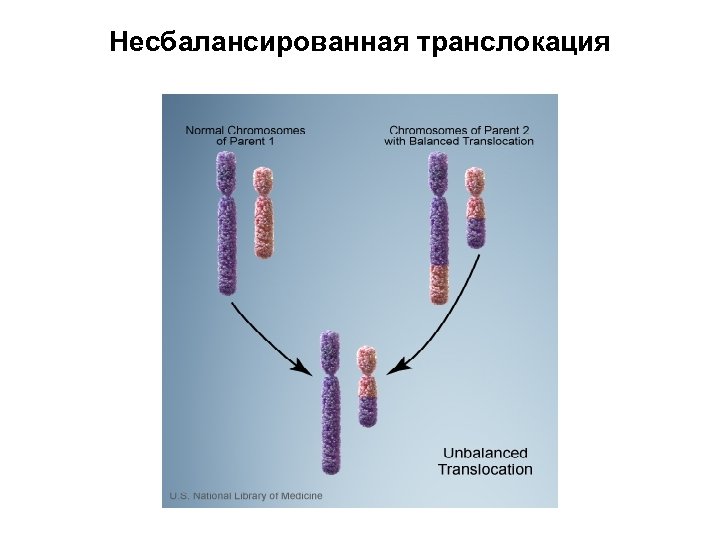 Несбалансированная транслокация
Несбалансированная транслокация
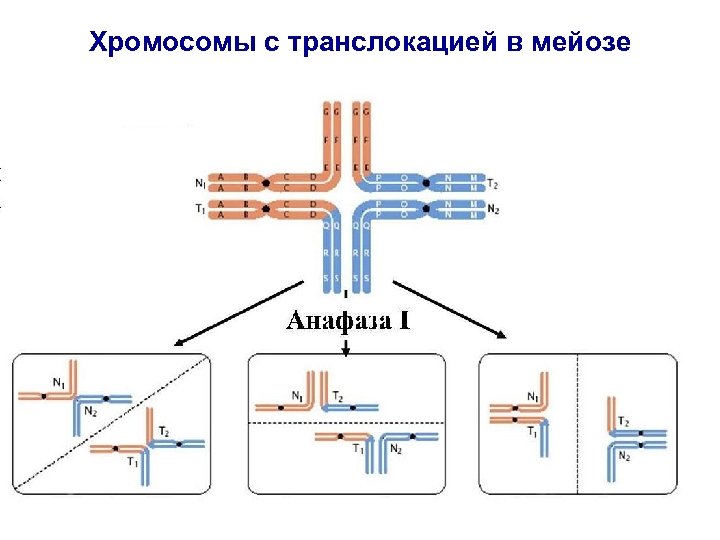 Хромосомы с транслокацией в мейозе
Хромосомы с транслокацией в мейозе
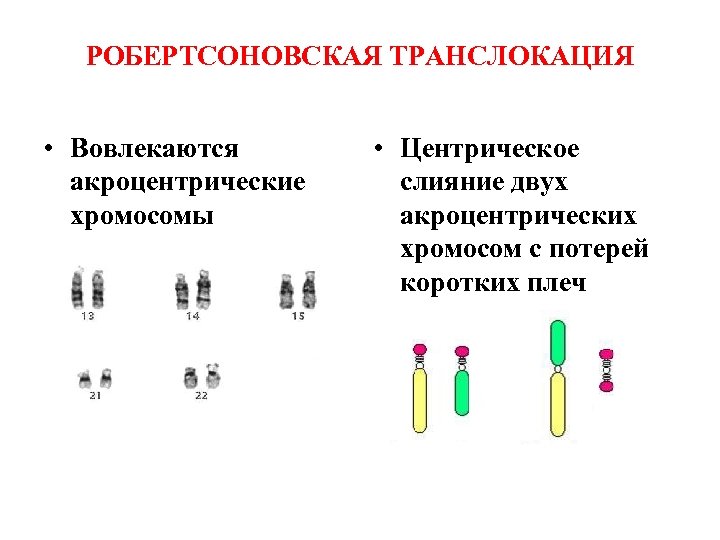 РОБЕРТСОНОВСКАЯ ТРАНСЛОКАЦИЯ • Вовлекаются акроцентрические хромосомы • Центрическое слияние двух акроцентрических хромосом с потерей коротких плеч
РОБЕРТСОНОВСКАЯ ТРАНСЛОКАЦИЯ • Вовлекаются акроцентрические хромосомы • Центрическое слияние двух акроцентрических хромосом с потерей коротких плеч
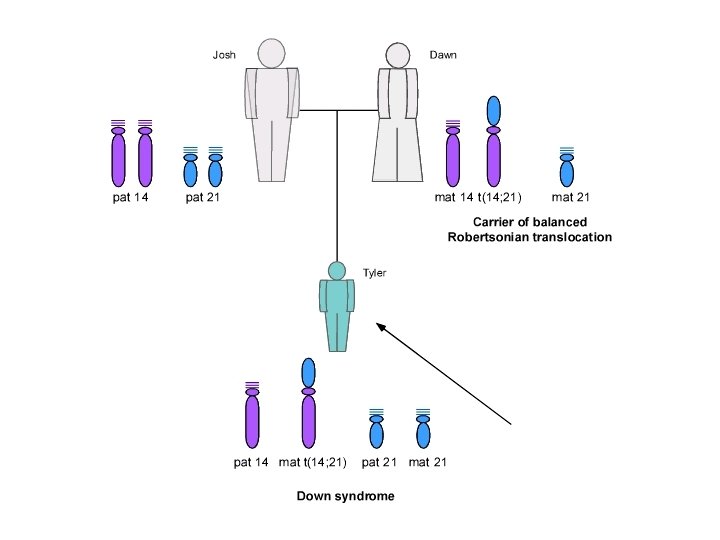
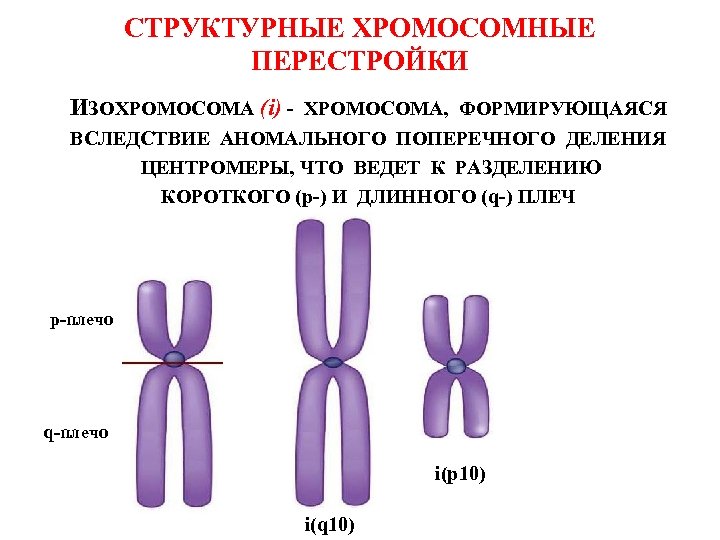 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИЗОХРОМОСОМА (i) - ХРОМОСОМА, ФОРМИРУЮЩАЯСЯ ВСЛЕДСТВИЕ АНОМАЛЬНОГО ПОПЕРЕЧНОГО ДЕЛЕНИЯ ЦЕНТРОМЕРЫ, ЧТО ВЕДЕТ К РАЗДЕЛЕНИЮ КОРОТКОГО (p-) И ДЛИННОГО (q-) ПЛЕЧ p-плечо q-плечо i(p 10) i(q 10)
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ ИЗОХРОМОСОМА (i) - ХРОМОСОМА, ФОРМИРУЮЩАЯСЯ ВСЛЕДСТВИЕ АНОМАЛЬНОГО ПОПЕРЕЧНОГО ДЕЛЕНИЯ ЦЕНТРОМЕРЫ, ЧТО ВЕДЕТ К РАЗДЕЛЕНИЮ КОРОТКОГО (p-) И ДЛИННОГО (q-) ПЛЕЧ p-плечо q-плечо i(p 10) i(q 10)
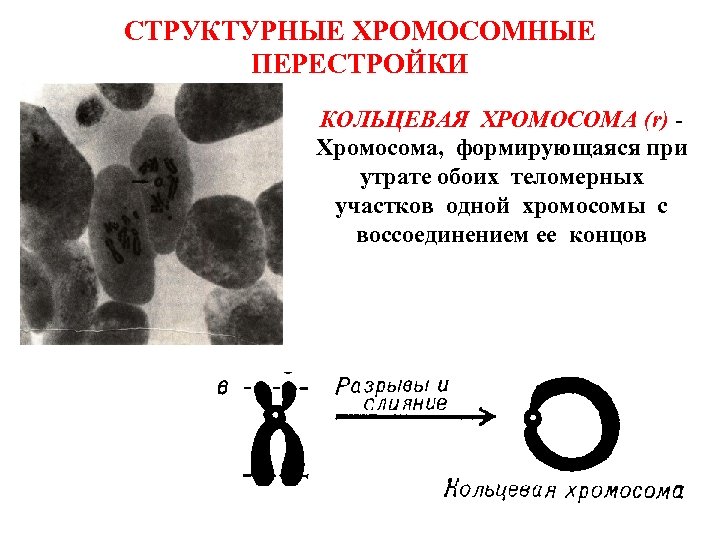 СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ КОЛЬЦЕВАЯ ХРОМОСОМА (r) - Хромосома, формирующаяся при утрате обоих теломерных участков одной хромосомы с воссоединением ее концов
СТРУКТУРНЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ КОЛЬЦЕВАЯ ХРОМОСОМА (r) - Хромосома, формирующаяся при утрате обоих теломерных участков одной хромосомы с воссоединением ее концов
 Хромосомные болезни – это большая группа клинически многообразных состояний, характеризующихся множественными врожденными пороками развития, этиология которых связана с количественными или структурными изменениями кариотипа
Хромосомные болезни – это большая группа клинически многообразных состояний, характеризующихся множественными врожденными пороками развития, этиология которых связана с количественными или структурными изменениями кариотипа
 КЛАССИФИКАЦИЯ ХРОМОСОМНЫХ БОЛЕЗНЕЙ • Этиология – характеристика типа мутации • Тип клеток, в которых возникла мутация – ü гаметические ü соматические • Поколение, в котором возникла мутация ü унаследованные ü cпорадические случаи (de novo)
КЛАССИФИКАЦИЯ ХРОМОСОМНЫХ БОЛЕЗНЕЙ • Этиология – характеристика типа мутации • Тип клеток, в которых возникла мутация – ü гаметические ü соматические • Поколение, в котором возникла мутация ü унаследованные ü cпорадические случаи (de novo)
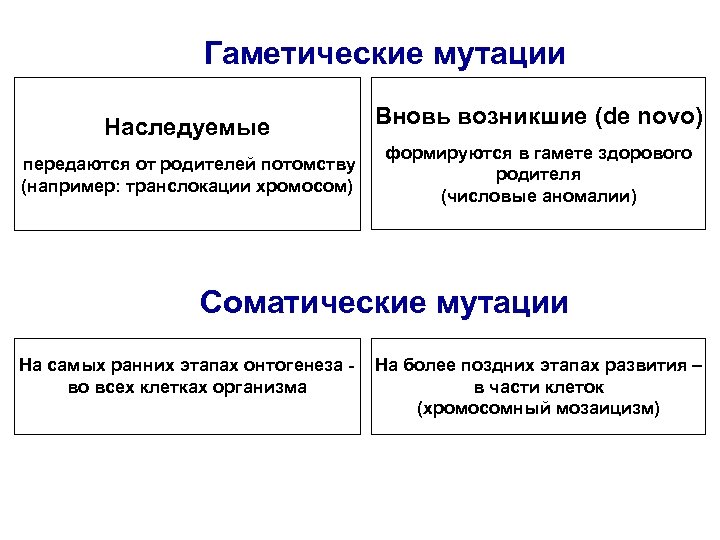 Гаметические мутации Наследуемые передаются от родителей потомству (например: транслокации хромосом) Вновь возникшие (de novo) формируются в гамете здорового родителя (числовые аномалии) Соматические мутации На самых ранних этапах онтогенеза во всех клетках организма На более поздних этапах развития – в части клеток (хромосомный мозаицизм)
Гаметические мутации Наследуемые передаются от родителей потомству (например: транслокации хромосом) Вновь возникшие (de novo) формируются в гамете здорового родителя (числовые аномалии) Соматические мутации На самых ранних этапах онтогенеза во всех клетках организма На более поздних этапах развития – в части клеток (хромосомный мозаицизм)
 ХРОМОСОМНЫЕ БОЛЕЗНИ ГРУППЫ ЧАСТОТА ХРОМОСОМНЫХ АНОМАЛИЙ Ранние доимплантационные потери около 50% Спонтанные выкидыши В среднем около 30% 5 -7% Младенческая и детская смертность Врожденные пороки развития 4 -8% Врожденные пороки сердца 13% Умственная отсталость средней и тяжелой степени 15 -20% Мужское бесплодие Привычное невынашивание 2% (до 15% в группе с азооспермией) 2 -5%
ХРОМОСОМНЫЕ БОЛЕЗНИ ГРУППЫ ЧАСТОТА ХРОМОСОМНЫХ АНОМАЛИЙ Ранние доимплантационные потери около 50% Спонтанные выкидыши В среднем около 30% 5 -7% Младенческая и детская смертность Врожденные пороки развития 4 -8% Врожденные пороки сердца 13% Умственная отсталость средней и тяжелой степени 15 -20% Мужское бесплодие Привычное невынашивание 2% (до 15% в группе с азооспермией) 2 -5%
 Частота хромосомных аномалий в зависимости от срока прерывания беременности • • • до 2 недель – 100% до 4 недель – 75% до 14 недели – 50% до 24 недели – 25 -35% у новорожденных – 3 -5%
Частота хромосомных аномалий в зависимости от срока прерывания беременности • • • до 2 недель – 100% до 4 недель – 75% до 14 недели – 50% до 24 недели – 25 -35% у новорожденных – 3 -5%
 Фенотипические проявления хромосомных болезней • Нарушение бластогенеза с аномальной имплантацией или с невозможностью имплантации бластоцисты • Нарушение эмбриогенеза со спонтанным прерыванием беременности обычно в I триместре беременности • Нарушения внутриутробного морфогенеза, приводящие к мертворождению или ранней неонатальной гибели • Нарушения внутриутробного морфогенеза различной степени тяжести у жизнеспособного индивидуума • Минимальные или отсутствующие фенотипические проявления хромосомного дисбаланса
Фенотипические проявления хромосомных болезней • Нарушение бластогенеза с аномальной имплантацией или с невозможностью имплантации бластоцисты • Нарушение эмбриогенеза со спонтанным прерыванием беременности обычно в I триместре беременности • Нарушения внутриутробного морфогенеза, приводящие к мертворождению или ранней неонатальной гибели • Нарушения внутриутробного морфогенеза различной степени тяжести у жизнеспособного индивидуума • Минимальные или отсутствующие фенотипические проявления хромосомного дисбаланса
 Клинические признаки хромосомных заболеваний • Низкая масса тела при рождении (доношенная беременность) • Изменение формы и размеров черепа ( микроцефалия, долихоцефалия, гидроцефалия, краниостеноз • Изменение вида и пропорций лица • Аномалии лба (низкий, выступающий, килевидный и т. д. ) • Аномалии глаз (монголоидный или антимонголоидный разрез, гипертелоризм, косоглазие, эпикант и т. д. • Аномалии подбородка • Аномалии носа (седловидный, массивный, деформированные ноздри) • Аномалии ушных раковин (низкое расположение, деформации) • Челюстные аномалии (микроретрогнатия) • Высокое (готическое) нёбо, расщелины нёба
Клинические признаки хромосомных заболеваний • Низкая масса тела при рождении (доношенная беременность) • Изменение формы и размеров черепа ( микроцефалия, долихоцефалия, гидроцефалия, краниостеноз • Изменение вида и пропорций лица • Аномалии лба (низкий, выступающий, килевидный и т. д. ) • Аномалии глаз (монголоидный или антимонголоидный разрез, гипертелоризм, косоглазие, эпикант и т. д. • Аномалии подбородка • Аномалии носа (седловидный, массивный, деформированные ноздри) • Аномалии ушных раковин (низкое расположение, деформации) • Челюстные аномалии (микроретрогнатия) • Высокое (готическое) нёбо, расщелины нёба
 Клинические признаки хромосомных заболеваний (продолжение) • Короткая шея • Аномалии пальцев (клинодактилия, камптодиктилия, синдактилия) • Косолапость, косорукость (искривление стоп и кистей) • Аномалии наружных гениталий (крипторхизм, гипоспадия, гипоплазия) • Пороки развития сердца и других внутренних органов • Отставание в умственном и физическом развитии
Клинические признаки хромосомных заболеваний (продолжение) • Короткая шея • Аномалии пальцев (клинодактилия, камптодиктилия, синдактилия) • Косолапость, косорукость (искривление стоп и кистей) • Аномалии наружных гениталий (крипторхизм, гипоспадия, гипоплазия) • Пороки развития сердца и других внутренних органов • Отставание в умственном и физическом развитии
 Диагностика хромосомных аномалий Цитогенетические методы • Кариотипирование • Метод FISH Молекулярно-генетические методы • Микросателлитный анализ • Блоттинг-гибридизация • RT-PCR • Анализ микрочипов
Диагностика хромосомных аномалий Цитогенетические методы • Кариотипирование • Метод FISH Молекулярно-генетические методы • Микросателлитный анализ • Блоттинг-гибридизация • RT-PCR • Анализ микрочипов
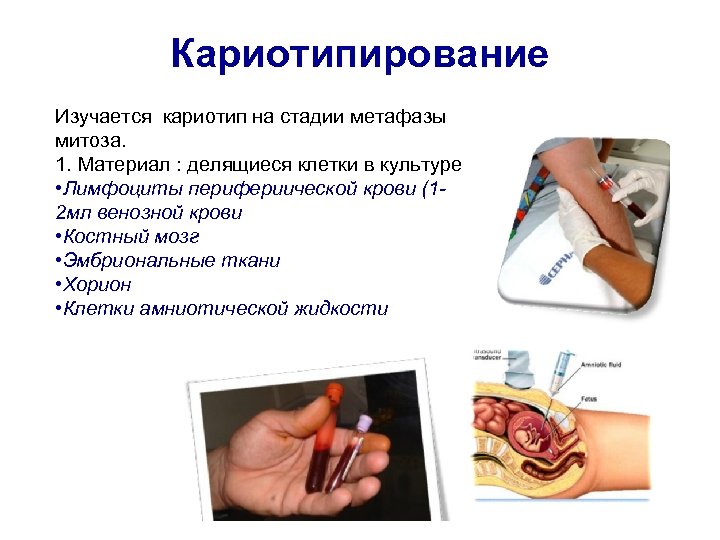 Кариотипирование Изучается кариотип на стадии метафазы митоза. 1. Материал : делящиеся клетки в культуре • Лимфоциты перифериической крови (12 мл венозной крови • Костный мозг • Эмбриональные ткани • Хорион • Клетки амниотической жидкости
Кариотипирование Изучается кариотип на стадии метафазы митоза. 1. Материал : делящиеся клетки в культуре • Лимфоциты перифериической крови (12 мл венозной крови • Костный мозг • Эмбриональные ткани • Хорион • Клетки амниотической жидкости
 Кариотипирование 2. Посев на питательную среду с митогеном (фитогемагглютинин) 3. Культивируют 2 -3 суток 4. Останавливают деление, добавляя колхицин за 2 -3 часа до окончания культивирования (повышается митотический индекс) 5. Обработка гипотоническим раствором КСl (разрушается ядерная оболочка, хромосомы отделяются друг от друга 6. Фиксация смесью этанола и уксусной кислоты 7. центрифугирование
Кариотипирование 2. Посев на питательную среду с митогеном (фитогемагглютинин) 3. Культивируют 2 -3 суток 4. Останавливают деление, добавляя колхицин за 2 -3 часа до окончания культивирования (повышается митотический индекс) 5. Обработка гипотоническим раствором КСl (разрушается ядерная оболочка, хромосомы отделяются друг от друга 6. Фиксация смесью этанола и уксусной кислоты 7. центрифугирование
 Кариотипирование 8. Готовят микропрепарат, окрашивают его 9. Находят клетки на стадии метафазы (метафазная пластинка) 10. Фотографируют 11. Составляют кариограмму и анализируют ее
Кариотипирование 8. Готовят микропрепарат, окрашивают его 9. Находят клетки на стадии метафазы (метафазная пластинка) 10. Фотографируют 11. Составляют кариограмму и анализируют ее
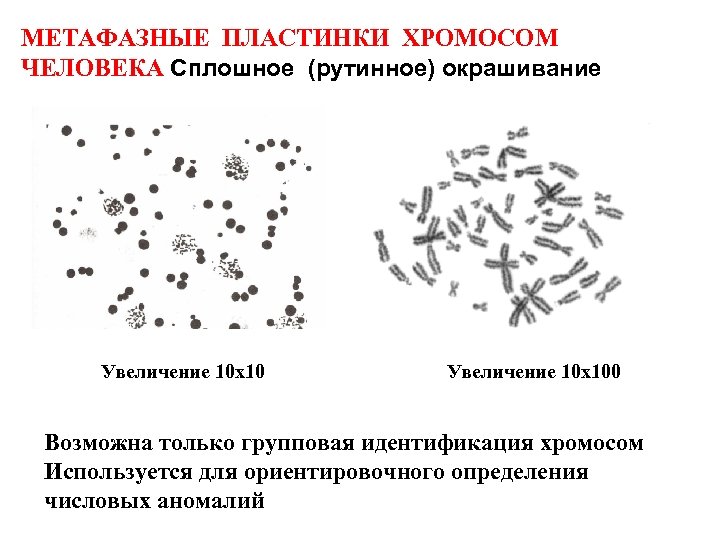 МЕТАФАЗНЫЕ ПЛАСТИНКИ ХРОМОСОМ ЧЕЛОВЕКА Сплошное (рутинное) окрашивание Увеличение 10 х100 Возможна только групповая идентификация хромосом Используется для ориентировочного определения числовых аномалий
МЕТАФАЗНЫЕ ПЛАСТИНКИ ХРОМОСОМ ЧЕЛОВЕКА Сплошное (рутинное) окрашивание Увеличение 10 х100 Возможна только групповая идентификация хромосом Используется для ориентировочного определения числовых аномалий
 НОМЕНКЛАТУРА ХРОМОСОМ ЧЕЛОВЕКА • Денверская конференция (1960 г. ) – предложена система описания хромосом Лондонская конференция (1963 г. ) – официально введено разделение хромосом на 7 морфологических групп (A, B, C, D, E, F, G), учитывая размеры и положение центромеры
НОМЕНКЛАТУРА ХРОМОСОМ ЧЕЛОВЕКА • Денверская конференция (1960 г. ) – предложена система описания хромосом Лондонская конференция (1963 г. ) – официально введено разделение хромосом на 7 морфологических групп (A, B, C, D, E, F, G), учитывая размеры и положение центромеры
 Группа A Хромосомы 1– 3 Описание Большие, метацентрические, равноплечие B 4, 5 Большие, субметацентрические, плечи сильно отличются по размеру C 6– 12, X Среднего размера; субметацентрические D 13– 15 Среднего размера; акроцентрические, со спутниками E 16– 18 Маленькие; 16 хромосома - метацентрческая, хромосомы 17 и 18 - субметацентрические F 19, 20 Маленькие; метацентрические G 21, 22, Y Маленькие; акроцентрические, со спутниками Маленькая; акроцентрическая, без спутников Аутосомы нумеруются от больших к меньшим, кроме хромосомы 21, которая меньше чем хромосома 22.
Группа A Хромосомы 1– 3 Описание Большие, метацентрические, равноплечие B 4, 5 Большие, субметацентрические, плечи сильно отличются по размеру C 6– 12, X Среднего размера; субметацентрические D 13– 15 Среднего размера; акроцентрические, со спутниками E 16– 18 Маленькие; 16 хромосома - метацентрческая, хромосомы 17 и 18 - субметацентрические F 19, 20 Маленькие; метацентрические G 21, 22, Y Маленькие; акроцентрические, со спутниками Маленькая; акроцентрическая, без спутников Аутосомы нумеруются от больших к меньшим, кроме хромосомы 21, которая меньше чем хромосома 22.
 Дифференциальное окрашивание хромосом - методы выявляющие поперечную исчерченность хромосом (чередование светлых и темных полос), специфичную для каждой хромосомы - • GTG-окраска 1968 г. – Т. Касперсон (T. Caspersson) применил для исследования метафазных хромосом метод дифференциальной Qокраски 1971 г. – М. Дретс (M. Drets) и М. Шау (M. Shaw) использовали GTG-метод дифференциальной окраски хромосом
Дифференциальное окрашивание хромосом - методы выявляющие поперечную исчерченность хромосом (чередование светлых и темных полос), специфичную для каждой хромосомы - • GTG-окраска 1968 г. – Т. Касперсон (T. Caspersson) применил для исследования метафазных хромосом метод дифференциальной Qокраски 1971 г. – М. Дретс (M. Drets) и М. Шау (M. Shaw) использовали GTG-метод дифференциальной окраски хромосом
 • V Международный конгресс по генетике человека (Мехико, 1972 г. ) – появление первой официальной номенклатуры хромосом человека - «An International System for Human Cytogenetic Nomenclature» (ISCN, 1978)
• V Международный конгресс по генетике человека (Мехико, 1972 г. ) – появление первой официальной номенклатуры хромосом человека - «An International System for Human Cytogenetic Nomenclature» (ISCN, 1978)
 ХРОМОСОМНЫЕ БЭНДЫ (BANDS) Бэнд - участок хромосомы, отличающийся от соседних по интенсивности окраски, при использовании соответствующего метода дифференциального окрашивания. Молекулярной основой дифференциального окрашивания хромосом является нуклеотидный и белковый состав и функциональная организация соответствующих бэндам участков генома.
ХРОМОСОМНЫЕ БЭНДЫ (BANDS) Бэнд - участок хромосомы, отличающийся от соседних по интенсивности окраски, при использовании соответствующего метода дифференциального окрашивания. Молекулярной основой дифференциального окрашивания хромосом является нуклеотидный и белковый состав и функциональная организация соответствующих бэндам участков генома.
 Бэнды представляют собой крупные структуры размером 510 Mb, которые могут включать сотни генов. «… Бэнды отражают структурно-функциональную организацию генома, обусловливающую регуляцию репликации ДНК, репарацию, транскрипцию и генетическую рекомбинацию. G-позитивные бэнды (R-негативные) содержат АТбогатую, поздно реплицирующуюся ДНК, бедную генами G-негативные бэнды (R-позитивные) GC–богаты, обогащены генами, их ДНК рано реплицируется» . ISCN, 2009
Бэнды представляют собой крупные структуры размером 510 Mb, которые могут включать сотни генов. «… Бэнды отражают структурно-функциональную организацию генома, обусловливающую регуляцию репликации ДНК, репарацию, транскрипцию и генетическую рекомбинацию. G-позитивные бэнды (R-негативные) содержат АТбогатую, поздно реплицирующуюся ДНК, бедную генами G-негативные бэнды (R-позитивные) GC–богаты, обогащены генами, их ДНК рано реплицируется» . ISCN, 2009
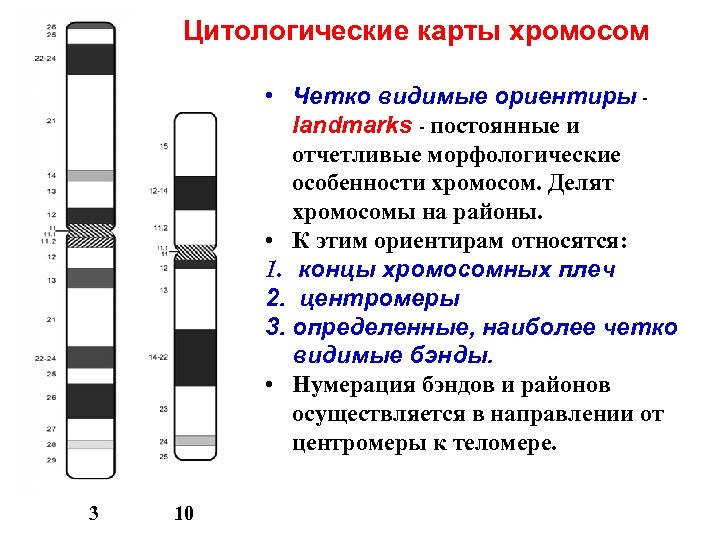 Цитологические карты хромосом • Четко видимые ориентиры - landmarks - постоянные и отчетливые морфологические особенности хромосом. Делят хромосомы на районы. • К этим ориентирам относятся: 1. концы хромосомных плеч 2. центромеры 3. определенные, наиболее четко видимые бэнды. • Нумерация бэндов и районов осуществляется в направлении от центромеры к теломере. 3 10
Цитологические карты хромосом • Четко видимые ориентиры - landmarks - постоянные и отчетливые морфологические особенности хромосом. Делят хромосомы на районы. • К этим ориентирам относятся: 1. концы хромосомных плеч 2. центромеры 3. определенные, наиболее четко видимые бэнды. • Нумерация бэндов и районов осуществляется в направлении от центромеры к теломере. 3 10
 Цитологические карты хромосом • p - короткое плечо хромосомы • q - длинное плечо • Центромера обозначается символом «cen» , однако для обозначения части центромеры, прилежащей к р-плечу используется символ р10, а части центромеры, прилежащий к qплечу - символ q 10. • Район хромосомного плеча, ближайший к центромере, обозначается цифрой 1, следующий район – цифрой 2 и т. д. • h - Центромерный гетерохроматин • s - спутник • stk - спутничные нити
Цитологические карты хромосом • p - короткое плечо хромосомы • q - длинное плечо • Центромера обозначается символом «cen» , однако для обозначения части центромеры, прилежащей к р-плечу используется символ р10, а части центромеры, прилежащий к qплечу - символ q 10. • Район хромосомного плеча, ближайший к центромере, обозначается цифрой 1, следующий район – цифрой 2 и т. д. • h - Центромерный гетерохроматин • s - спутник • stk - спутничные нити
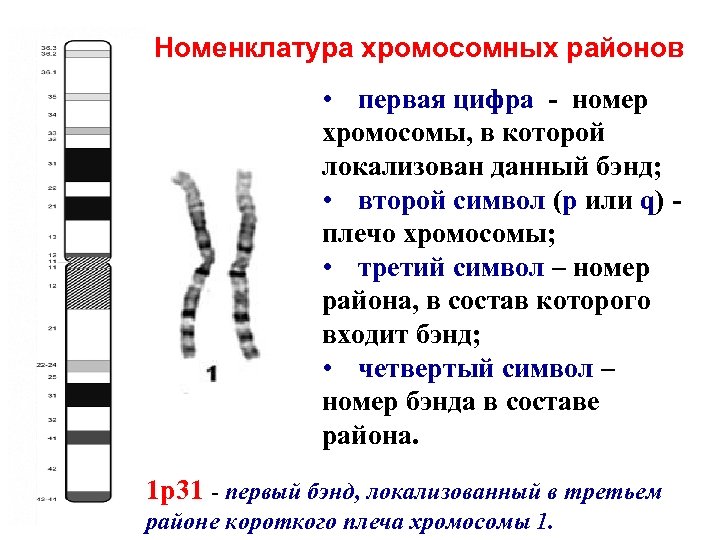 Номенклатура хромосомных районов • первая цифра - номер хромосомы, в которой локализован данный бэнд; • второй символ (p или q) - плечо хромосомы; • третий символ – номер района, в состав которого входит бэнд; • четвертый символ – номер бэнда в составе района. 1 р31 - первый бэнд, локализованный в третьем районе короткого плеча хромосомы 1.
Номенклатура хромосомных районов • первая цифра - номер хромосомы, в которой локализован данный бэнд; • второй символ (p или q) - плечо хромосомы; • третий символ – номер района, в состав которого входит бэнд; • четвертый символ – номер бэнда в составе района. 1 р31 - первый бэнд, локализованный в третьем районе короткого плеча хромосомы 1.
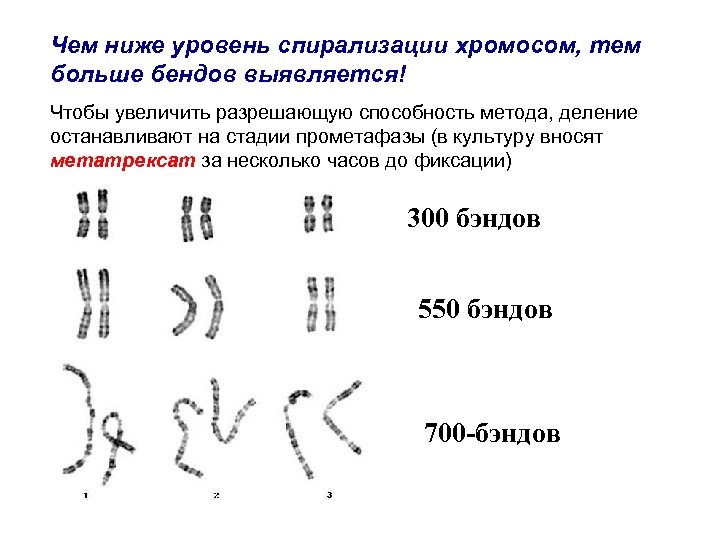 Чем ниже уровень спирализации хромосом, тем больше бендов выявляется! Чтобы увеличить разрешающую способность метода, деление останавливают на стадии прометафазы (в культуру вносят метатрексат за несколько часов до фиксации) 300 бэндов 550 бэндов 700 -бэндов
Чем ниже уровень спирализации хромосом, тем больше бендов выявляется! Чтобы увеличить разрешающую способность метода, деление останавливают на стадии прометафазы (в культуру вносят метатрексат за несколько часов до фиксации) 300 бэндов 550 бэндов 700 -бэндов
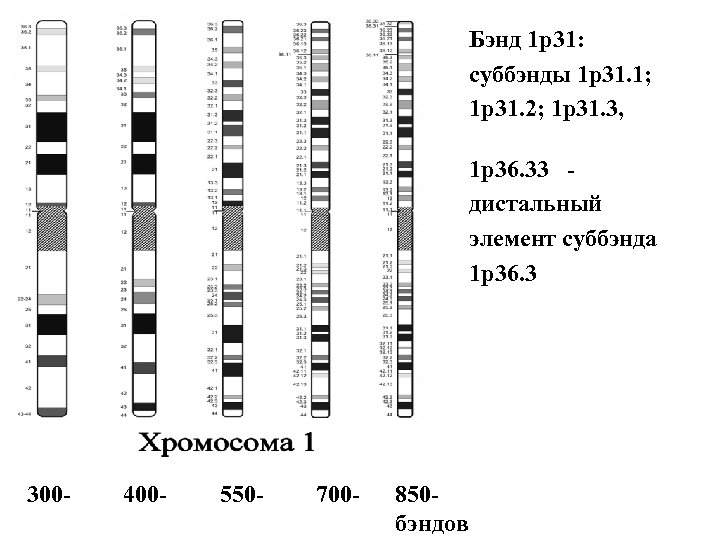 Бэнд 1 р31: суббэнды 1 р31. 1; 1 р31. 2; 1 р31. 3, 1 р36. 33 - дистальный элемент суббэнда 1 р36. 3 300 - 400 - 550 - 700 - 850 - бэндов
Бэнд 1 р31: суббэнды 1 р31. 1; 1 р31. 2; 1 р31. 3, 1 р36. 33 - дистальный элемент суббэнда 1 р36. 3 300 - 400 - 550 - 700 - 850 - бэндов
 ИДИОГРАММЫ ПЯТИ УРОВНЕЙ РАЗРЕШЕНИЯ, СООТВЕТСТВУЮЩИХ 300 -, 400 -, 550 -, 700 - и 850 –ЭЛЕМЕНТОВ В ГАПЛОИДНОМ НАБОРЕ ХРОМОСОМ
ИДИОГРАММЫ ПЯТИ УРОВНЕЙ РАЗРЕШЕНИЯ, СООТВЕТСТВУЮЩИХ 300 -, 400 -, 550 -, 700 - и 850 –ЭЛЕМЕНТОВ В ГАПЛОИДНОМ НАБОРЕ ХРОМОСОМ
 НОМЕНКЛАТУРА ВАРИАНТОВ ХРОМОСОМ Варибельность длины (размеров) 16 qh+ увеличение длины гетерохроматического района длинного плеча хромосомы 16 Yqh+ увеличение гетерохроматического района длинного плеча хромосомы Y. увеличение размеров спутников на коротком плече 21 рs+ хромосомы 21 увеличение длины спутничной нити на коротком 22 рstk+ плече хромосомы 22. увеличение азмера ентромерного етерохроматина р ц г 13 cenh+mat хромосомы 13, унаследованное от матери 9 qh+, 15 cenh+ 21 ps+ увеличение длины гетерохроматического района длинного плеча хромосомы 9, увеличение центромерного гетерохроматина в хромосоме 15 и большие спутники на коротком плече хромосомы 21. Центромерный гетерохроматин (h), спутничные нити (stk) спутник (s)
НОМЕНКЛАТУРА ВАРИАНТОВ ХРОМОСОМ Варибельность длины (размеров) 16 qh+ увеличение длины гетерохроматического района длинного плеча хромосомы 16 Yqh+ увеличение гетерохроматического района длинного плеча хромосомы Y. увеличение размеров спутников на коротком плече 21 рs+ хромосомы 21 увеличение длины спутничной нити на коротком 22 рstk+ плече хромосомы 22. увеличение азмера ентромерного етерохроматина р ц г 13 cenh+mat хромосомы 13, унаследованное от матери 9 qh+, 15 cenh+ 21 ps+ увеличение длины гетерохроматического района длинного плеча хромосомы 9, увеличение центромерного гетерохроматина в хромосоме 15 и большие спутники на коротком плече хромосомы 21. Центромерный гетерохроматин (h), спутничные нити (stk) спутник (s)
 Виды дифференциального окрашивания хромосом QF QFQ QFH GT GTG GTW GAG CB CBG RF RFA RH RHG Q- флуоресцентное окрашивание Q-флуоресцентное окрашивание с акрихином Q-флуоресцентное окрашивание с Hoechst 33258 G-окрашивание с красителем Гимза (Giemsa) G-окрашивание с трипсином и красителем Гимза G-окрашивание с трипсином и красителем Райта (Wright) G-окрашивание с солями уксусной кислоты и красителем Гимза С-окрашивание с гидроксидом бария и красителем Гимза R- флуоресцентное окрашивание R-флуоресцентное окрашивание с акридином оранжевым R-окрашивание при нагревании с красителем Гимза
Виды дифференциального окрашивания хромосом QF QFQ QFH GT GTG GTW GAG CB CBG RF RFA RH RHG Q- флуоресцентное окрашивание Q-флуоресцентное окрашивание с акрихином Q-флуоресцентное окрашивание с Hoechst 33258 G-окрашивание с красителем Гимза (Giemsa) G-окрашивание с трипсином и красителем Гимза G-окрашивание с трипсином и красителем Райта (Wright) G-окрашивание с солями уксусной кислоты и красителем Гимза С-окрашивание с гидроксидом бария и красителем Гимза R- флуоресцентное окрашивание R-флуоресцентное окрашивание с акридином оранжевым R-окрашивание при нагревании с красителем Гимза
 GTG –окраска -окрашивание с трипсином и красителем Гимза
GTG –окраска -окрашивание с трипсином и красителем Гимза
 G-banding темные полосы – геторохроматиновые, поздно реплицирующиеся, богатые А-Т, светлые полосы – эухроматиновые, рано реплицирующиеся , богатые Г-Ц R-banding -обратный G-banding Темные участки – эухроматиновые, светлые участки - гетерохроматиновые
G-banding темные полосы – геторохроматиновые, поздно реплицирующиеся, богатые А-Т, светлые полосы – эухроматиновые, рано реплицирующиеся , богатые Г-Ц R-banding -обратный G-banding Темные участки – эухроматиновые, светлые участки - гетерохроматиновые
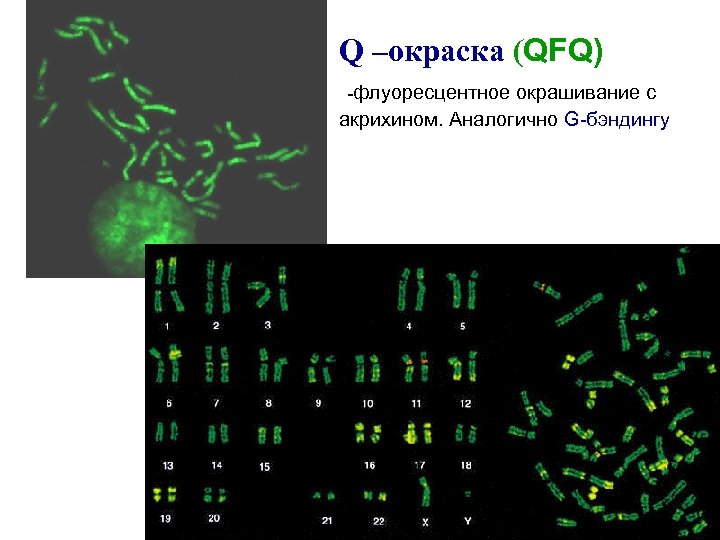 Q –окраска (QFQ) -флуоресцентное окрашивание с акрихином. Аналогично G-бэндингу
Q –окраска (QFQ) -флуоресцентное окрашивание с акрихином. Аналогично G-бэндингу
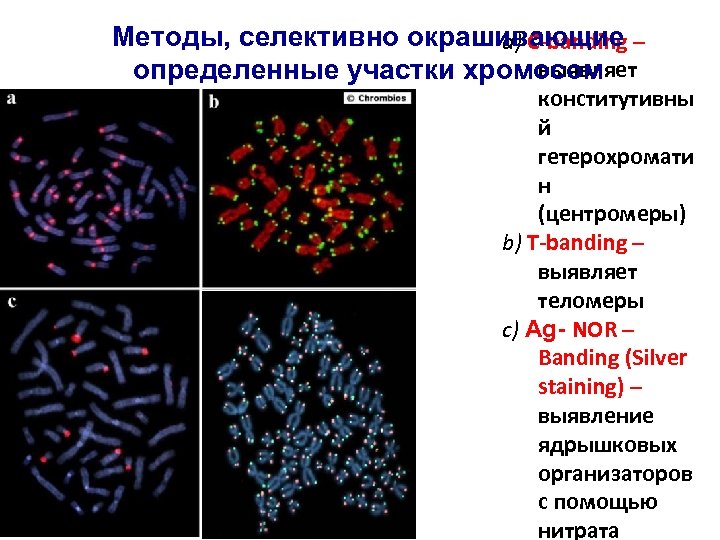 Методы, селективно окрашивающие – a) C-banding выявляет определенные участки хромосом конститутивны й гетерохромати н (центромеры) b) T-banding – выявляет теломеры c) Ag- NOR – Banding (Silver staining) – выявление ядрышковых организаторов с помощью нитрата
Методы, селективно окрашивающие – a) C-banding выявляет определенные участки хромосом конститутивны й гетерохромати н (центромеры) b) T-banding – выявляет теломеры c) Ag- NOR – Banding (Silver staining) – выявление ядрышковых организаторов с помощью нитрата
 Флуоресцентная гибридизация in situ Fluorescent In Situ Hybridisation FISH - цитогенетический метод, который применяют для детекции и определения положения специфической последовательности ДНК на метафазных хромосомах или в интерфазных ядрах in situ
Флуоресцентная гибридизация in situ Fluorescent In Situ Hybridisation FISH - цитогенетический метод, который применяют для детекции и определения положения специфической последовательности ДНК на метафазных хромосомах или в интерфазных ядрах in situ
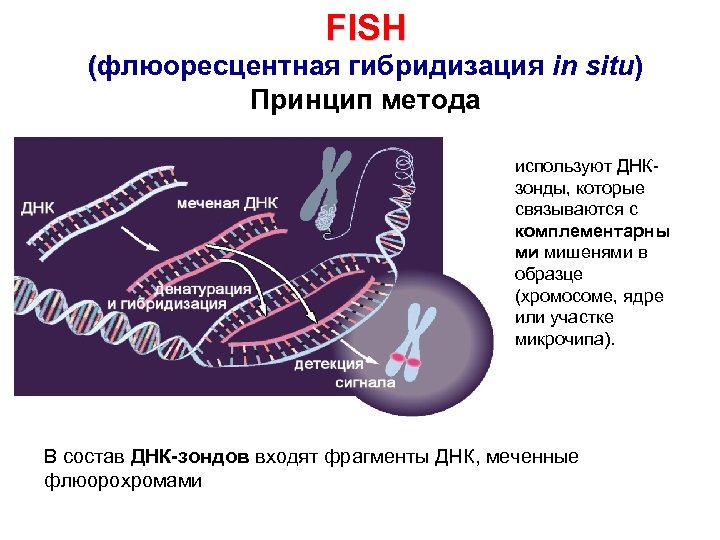 FISH (флюоресцентная гибридизация in situ) Принцип метода используют ДНКзонды, которые связываются с комплементарны ми мишенями в образце (хромосоме, ядре или участке микрочипа). В состав ДНК-зондов входят фрагменты ДНК, меченные флюорохромами
FISH (флюоресцентная гибридизация in situ) Принцип метода используют ДНКзонды, которые связываются с комплементарны ми мишенями в образце (хромосоме, ядре или участке микрочипа). В состав ДНК-зондов входят фрагменты ДНК, меченные флюорохромами
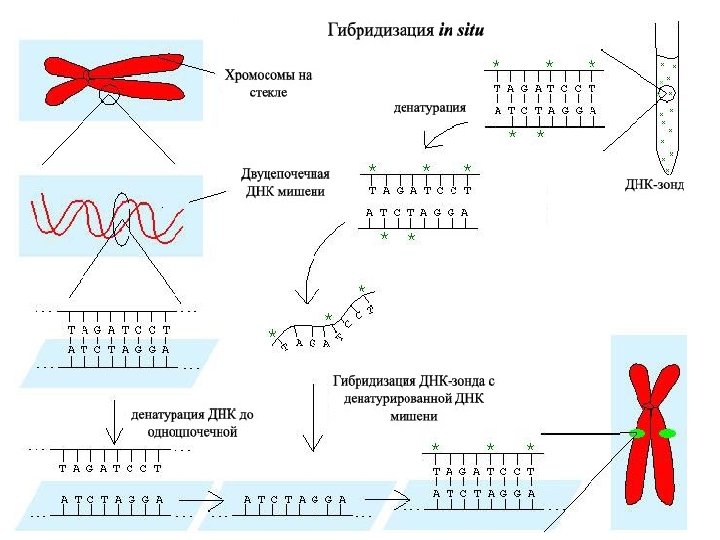
 ДНК-зонды: 1. Специфические для маркирования определенного района (уникальные гены, центромерные или субтеломерные последовательности), плеча или всей хромосомы. 2. Маркерные для всех теломерных , центромерных или ядрашкоорганизующих районов. 3. Геномные, специфичные для генома индивида определенного вида
ДНК-зонды: 1. Специфические для маркирования определенного района (уникальные гены, центромерные или субтеломерные последовательности), плеча или всей хромосомы. 2. Маркерные для всех теломерных , центромерных или ядрашкоорганизующих районов. 3. Геномные, специфичные для генома индивида определенного вида
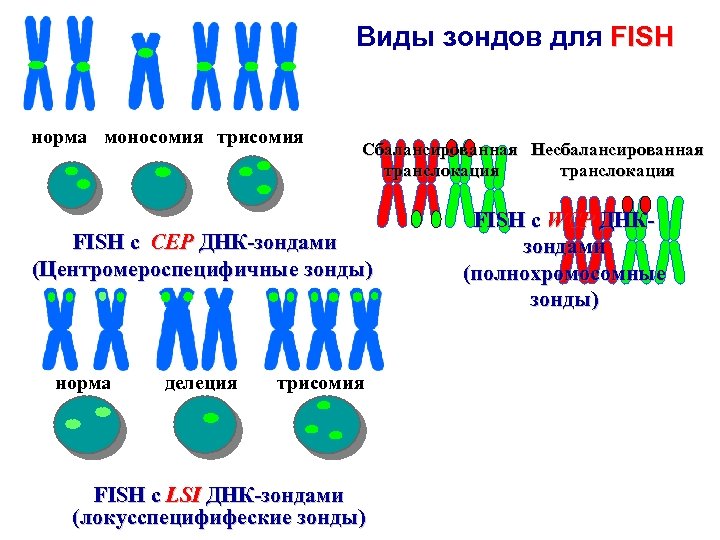 Виды зондов для FISH норма моносомия трисомия Сбалансированная Несбалансированная транслокация FISH c CEP ДНК-зондами (Центромероспецифичные зонды) норма делеция трисомия FISH с LSI ДНК-зондами (локусспецифифеские зонды) FISH c WCP ДНКзондами (полнохромосомные зонды)
Виды зондов для FISH норма моносомия трисомия Сбалансированная Несбалансированная транслокация FISH c CEP ДНК-зондами (Центромероспецифичные зонды) норма делеция трисомия FISH с LSI ДНК-зондами (локусспецифифеские зонды) FISH c WCP ДНКзондами (полнохромосомные зонды)
 Применение FISH в цитогенетическом анализе 1. Для выявления анеуплоидий , мозаицизма и сверчисленных хромосом используют зонды, специфичные к центромерам CEP (Chromosome Enuveration Probes) 2. Для выявления микроделеций, амплификаций, исследования сложных хромосомных перестроек и дополнительных маркерных хромосом используют локус специфические зонды LSI (Locus Specific Identification)
Применение FISH в цитогенетическом анализе 1. Для выявления анеуплоидий , мозаицизма и сверчисленных хромосом используют зонды, специфичные к центромерам CEP (Chromosome Enuveration Probes) 2. Для выявления микроделеций, амплификаций, исследования сложных хромосомных перестроек и дополнительных маркерных хромосом используют локус специфические зонды LSI (Locus Specific Identification)
 FISH-метод • Пренатальная или предимплантационная диагностика наиболее частых анеуплоидий (интерфазная FISH) • Диагностика скрытого и/или низко-уровневого мозаицизма по гоносомам (интерфазная FISH) • Диагностика известных микроделеционных синдромов • Уточнение цитогенетического диагноза • Идентификация сверхчисленных маркерных хромосом • Диагностика сложных комплексных хромосомных аберраций
FISH-метод • Пренатальная или предимплантационная диагностика наиболее частых анеуплоидий (интерфазная FISH) • Диагностика скрытого и/или низко-уровневого мозаицизма по гоносомам (интерфазная FISH) • Диагностика известных микроделеционных синдромов • Уточнение цитогенетического диагноза • Идентификация сверхчисленных маркерных хромосом • Диагностика сложных комплексных хромосомных аберраций
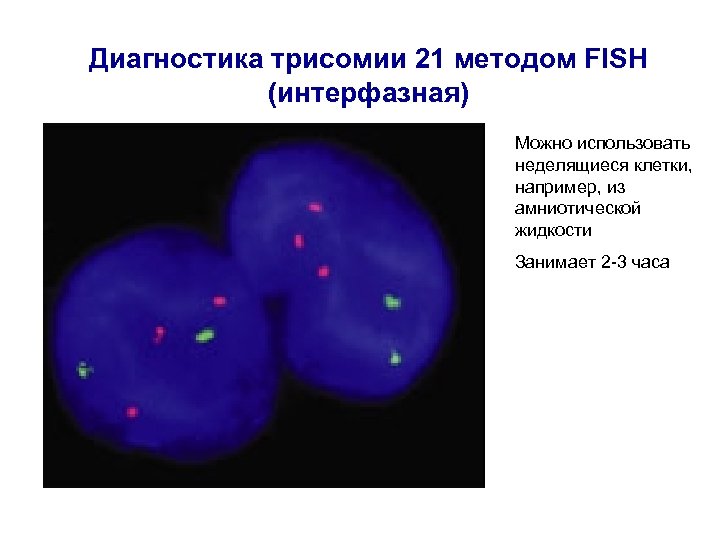 Диагностика трисомии 21 методом FISH (интерфазная) Можно использовать неделящиеся клетки, например, из амниотической жидкости Занимает 2 -3 часа
Диагностика трисомии 21 методом FISH (интерфазная) Можно использовать неделящиеся клетки, например, из амниотической жидкости Занимает 2 -3 часа
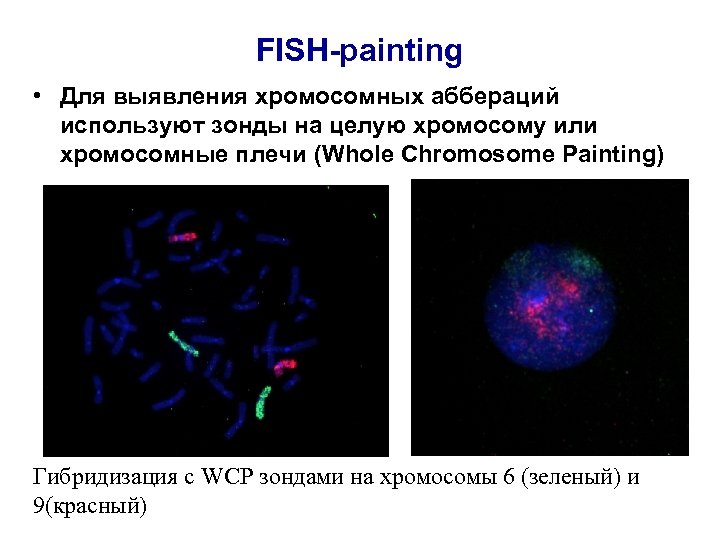 FISH-painting • Для выявления хромосомных аббераций используют зонды на целую хромосому или хромосомные плечи (Whole Chromosome Painting) Гибридизация с WCP зондами на хромосомы 6 (зеленый) и 9(красный)
FISH-painting • Для выявления хромосомных аббераций используют зонды на целую хромосому или хромосомные плечи (Whole Chromosome Painting) Гибридизация с WCP зондами на хромосомы 6 (зеленый) и 9(красный)
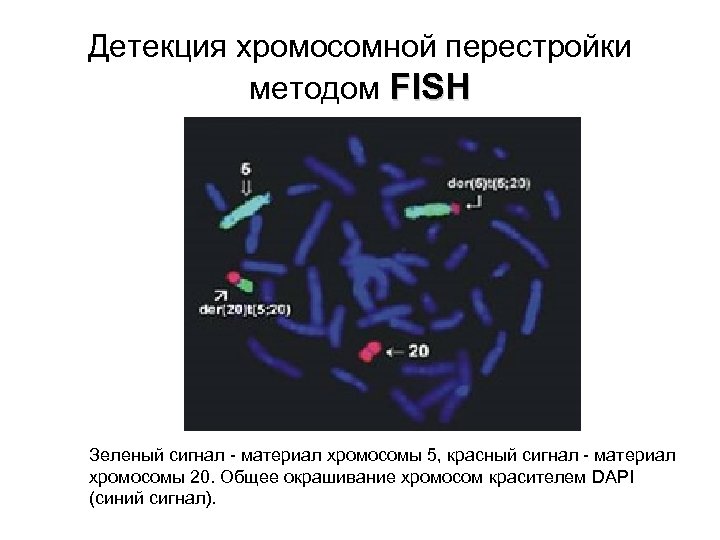 Детекция хромосомной перестройки методом FISH Зеленый сигнал - материал хромосомы 5, красный сигнал - материал хромосомы 20. Общее окрашивание хромосом красителем DAPI (синий сигнал).
Детекция хромосомной перестройки методом FISH Зеленый сигнал - материал хромосомы 5, красный сигнал - материал хромосомы 20. Общее окрашивание хромосом красителем DAPI (синий сигнал).
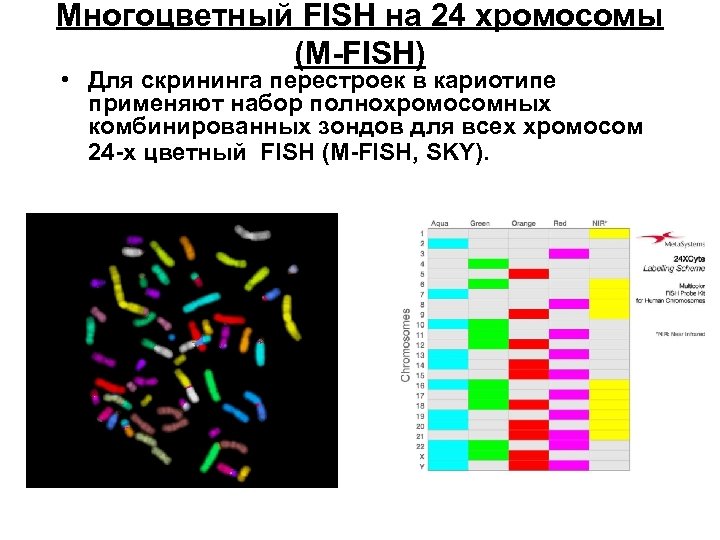 Многоцветный FISH на 24 хромосомы (М-FISH) • Для скрининга перестроек в кариотипе применяют набор полнохромосомных комбинированных зондов для всех хромосом 24 -х цветный FISH (M-FISH, SKY).
Многоцветный FISH на 24 хромосомы (М-FISH) • Для скрининга перестроек в кариотипе применяют набор полнохромосомных комбинированных зондов для всех хромосом 24 -х цветный FISH (M-FISH, SKY).
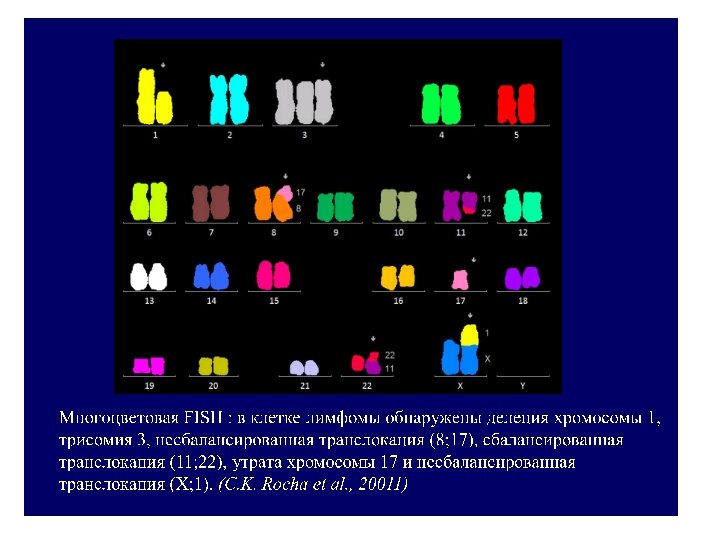
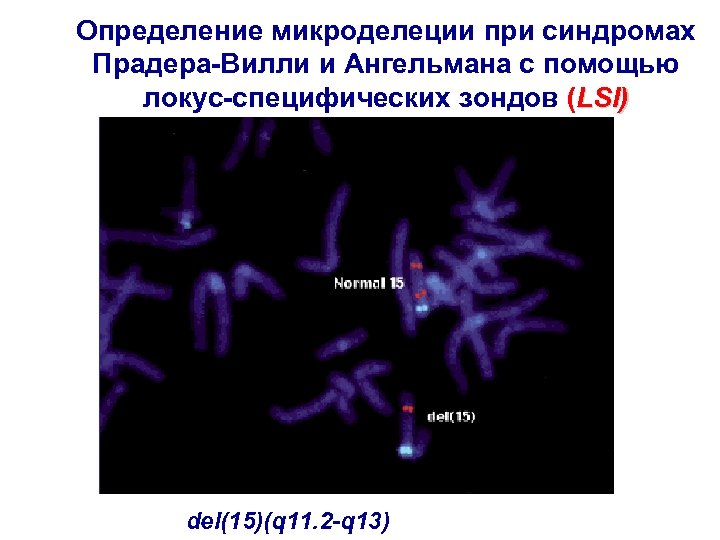 Определение микроделеции при синдромах Прадера-Вилли и Ангельмана с помощью локус-специфических зондов (LSI) del(15)(q 11. 2 -q 13)
Определение микроделеции при синдромах Прадера-Вилли и Ангельмана с помощью локус-специфических зондов (LSI) del(15)(q 11. 2 -q 13)
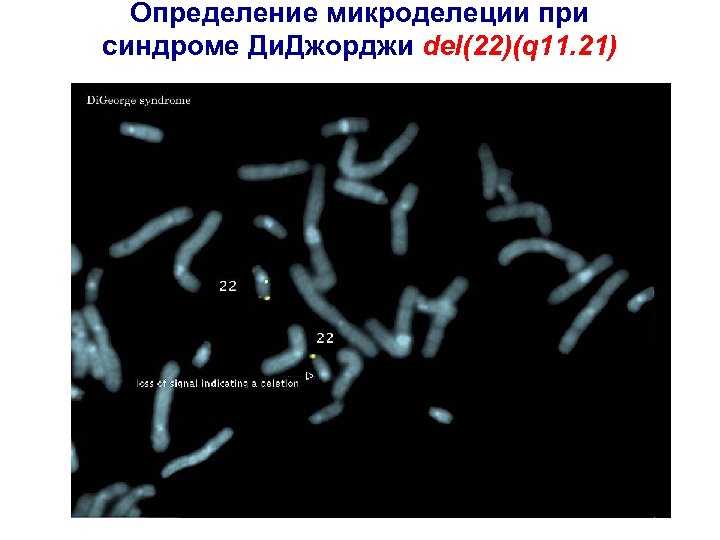 Определение микроделеции при синдроме Ди. Джорджи del(22)(q 11. 21)
Определение микроделеции при синдроме Ди. Джорджи del(22)(q 11. 21)
 Многоцветный бэндинг хромосом (multicolor banding – MCB, m. BAND)
Многоцветный бэндинг хромосом (multicolor banding – MCB, m. BAND)
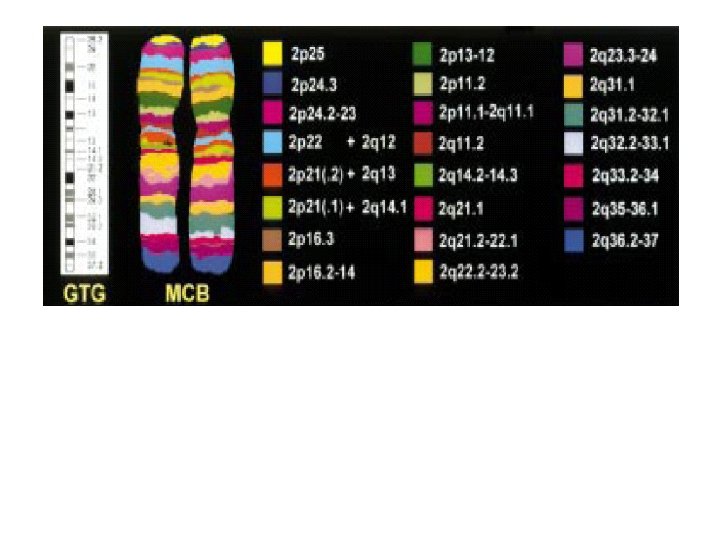 Многоцветовое окрашивание хромосомы 2 (MCB). Слева – схема расположения полос при окрашивании на G-полосы (A. Weise et al. , 2002).
Многоцветовое окрашивание хромосомы 2 (MCB). Слева – схема расположения полос при окрашивании на G-полосы (A. Weise et al. , 2002).
 Сравнительная геномная гибридизация Comparative Genomic Hybridization CGH • Метод сравнительной геномной гибридизации (Comparative Genomic Hybridization или CGH) - молекулярная цитогенетическая технология, объединившая стандартную цитогенетическую методику кариотипирования и FISH-анализ. Преимуществом метода CGH является возможность проведения полного анализа структурных хромосомных аномалий всего генома в пределах одного эксперимента.
Сравнительная геномная гибридизация Comparative Genomic Hybridization CGH • Метод сравнительной геномной гибридизации (Comparative Genomic Hybridization или CGH) - молекулярная цитогенетическая технология, объединившая стандартную цитогенетическую методику кариотипирования и FISH-анализ. Преимуществом метода CGH является возможность проведения полного анализа структурных хромосомных аномалий всего генома в пределах одного эксперимента.
 CGH • CGH основана на сравнении тестируемой и контрольной ДНК, меченных разными флуорохромами, которые смешиваются в соотношении 1: 1 и гибридизуются на метафазных хромосомах кариотипически здорового человека. Затем снимается серия изображений одного и того же поля зрения с использованием разных фильтров (например, DAPI, FITC, TRITC). После проведения выделения хромосом программа автоматически рассчитывает значение флуоресцентного отношения для каждой точки хромосомы и, исходя из полученных данных, строит цветокодированное изображение – ФО изображение.
CGH • CGH основана на сравнении тестируемой и контрольной ДНК, меченных разными флуорохромами, которые смешиваются в соотношении 1: 1 и гибридизуются на метафазных хромосомах кариотипически здорового человека. Затем снимается серия изображений одного и того же поля зрения с использованием разных фильтров (например, DAPI, FITC, TRITC). После проведения выделения хромосом программа автоматически рассчитывает значение флуоресцентного отношения для каждой точки хромосомы и, исходя из полученных данных, строит цветокодированное изображение – ФО изображение.
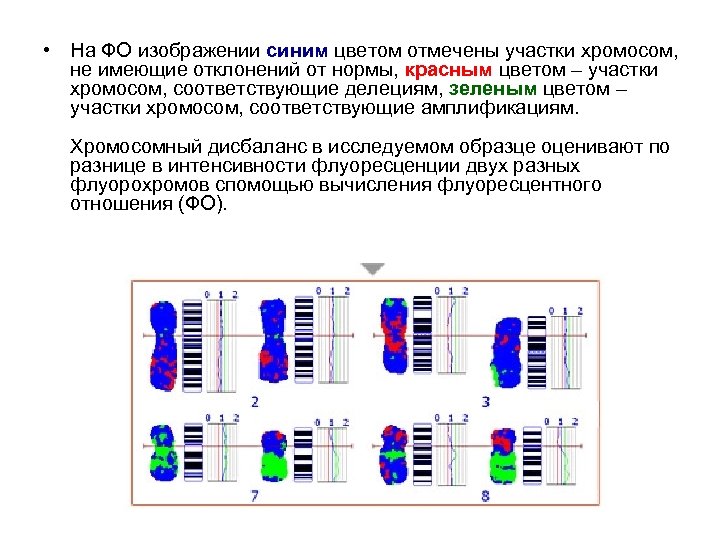 • На ФО изображении синим цветом отмечены участки хромосом, не имеющие отклонений от нормы, красным цветом – участки хромосом, соответствующие делециям, зеленым цветом – участки хромосом, соответствующие амплификациям. Хромосомный дисбаланс в исследуемом образце оценивают по разнице в интенсивности флуоресценции двух разных флуорохромов спомощью вычисления флуоресцентного отношения (ФО).
• На ФО изображении синим цветом отмечены участки хромосом, не имеющие отклонений от нормы, красным цветом – участки хромосом, соответствующие делециям, зеленым цветом – участки хромосом, соответствующие амплификациям. Хромосомный дисбаланс в исследуемом образце оценивают по разнице в интенсивности флуоресценции двух разных флуорохромов спомощью вычисления флуоресцентного отношения (ФО).
 Преимущества CGH • не зависит от источника исследуемого материала, и может быть успешно проведен с малым количеством тестируемой ДНК, включая архивный материал. • позволяет получить детальную информацию о потерях или увеличении числа копий генетического материала по всему геному в одном эксперименте. • не зависит от процесса культивирования клеток и связанных с ним артефактов.
Преимущества CGH • не зависит от источника исследуемого материала, и может быть успешно проведен с малым количеством тестируемой ДНК, включая архивный материал. • позволяет получить детальную информацию о потерях или увеличении числа копий генетического материала по всему геному в одном эксперименте. • не зависит от процесса культивирования клеток и связанных с ним артефактов.
 Cравнительная геномная гибридизация на микрочипах – array Comparative Genomic Hybridization (array –CGH или a-CGH) 1 -2: ДНК пациента (опытная) и ДНК здорового индивидуума (контрольная) метятся различными флуорохромами (Cy 3 и Cy 5) и наносятся на микрочип 3: Конкурентная гибридизация опытной и контрольной ДНК с ДНК -зондами на микрочипе 4: Измерение флуоресцентного сигнала (соотношение интенсивности флуресценции Сy 3/Cy 5) с использованием сканнера для микрочипов 5: Анализ полученных данных с использованием компьютерной программы и получение графического изображения
Cравнительная геномная гибридизация на микрочипах – array Comparative Genomic Hybridization (array –CGH или a-CGH) 1 -2: ДНК пациента (опытная) и ДНК здорового индивидуума (контрольная) метятся различными флуорохромами (Cy 3 и Cy 5) и наносятся на микрочип 3: Конкурентная гибридизация опытной и контрольной ДНК с ДНК -зондами на микрочипе 4: Измерение флуоресцентного сигнала (соотношение интенсивности флуресценции Сy 3/Cy 5) с использованием сканнера для микрочипов 5: Анализ полученных данных с использованием компьютерной программы и получение графического изображения
 array-CGH Ø Возможность одновременной детекции ануплоидий, делеций, дупликаций и/или амплификации любого локуса, представленного на микрочипе 1 анализ array CGH эквивалентен 1000 FISH-анализам! Ø Мощный инструмент детекции субмикроскопических хромосомных аномалий у пациентов с идиопатической умственной отсталостью и множественными врожденными пороками развития Ø Обеспечивает более детальный, автоматизированный и менее субъективный анализ аномального количества копий ДНК по сравнению со стандартным цитогенетическим исследованием Ø Может быть использован при исследовании архивного материала и тканей с неделящимися клетками
array-CGH Ø Возможность одновременной детекции ануплоидий, делеций, дупликаций и/или амплификации любого локуса, представленного на микрочипе 1 анализ array CGH эквивалентен 1000 FISH-анализам! Ø Мощный инструмент детекции субмикроскопических хромосомных аномалий у пациентов с идиопатической умственной отсталостью и множественными врожденными пороками развития Ø Обеспечивает более детальный, автоматизированный и менее субъективный анализ аномального количества копий ДНК по сравнению со стандартным цитогенетическим исследованием Ø Может быть использован при исследовании архивного материала и тканей с неделящимися клетками
 Выявляемость хромосомных аномалий у пациентов с умственной отсталостью средней и тяжелой степени и МВПР при использовании различных методов Ø Стандартное цитогенетическое исследование (GTG-дифференциальное окрашивание) 5 -10% Ø Субтеломерный FISH-скрининг при нормальном кариотипе Ø 4 -7% ØArray- CGH при нормальном кариотипе 10 -15%
Выявляемость хромосомных аномалий у пациентов с умственной отсталостью средней и тяжелой степени и МВПР при использовании различных методов Ø Стандартное цитогенетическое исследование (GTG-дифференциальное окрашивание) 5 -10% Ø Субтеломерный FISH-скрининг при нормальном кариотипе Ø 4 -7% ØArray- CGH при нормальном кариотипе 10 -15%
 Ограничения array CGH Ø Не выявляет сбалансированные хромосомные перестройки Ø Сложности интерпретации CNVs ( клинически значимые или нейтральный полиморфизм? ) Ø Не выявляет изменения количества копий в регионах генома, ДНК которых не присутствуют на микрочипе
Ограничения array CGH Ø Не выявляет сбалансированные хромосомные перестройки Ø Сложности интерпретации CNVs ( клинически значимые или нейтральный полиморфизм? ) Ø Не выявляет изменения количества копий в регионах генома, ДНК которых не присутствуют на микрочипе
 Нозологические формы, сопровождающиеся микрохромосомными аномалиями. с-м Вольфа-Хиршхорна del(4)(p 16). с-м “кошачьего крика” del(5)(p 15. 5). с-м Вильямса del(7)(q 11. 2). с-мы Лангера-Гидиона и ТРФС-I del(8)(q 24. 1). с-мы WAGR и Денниса-Драша del(11)(p 13). с-м Видеманна-Беквита dup(11)(p 15. 3). с-м DEFECT 11 del(11)(p 12). с-м Прадера-Вилли del(15)(q 11. 2 -q 13). с-м Ангельмана del(15)(q 11. 2 -q 13 с-м Рубинштейна-Тейби del(16)(p 13). с-м Смита-Магениса del(17)(p 11. 2). с-м Миллера-Дикера del(17)(p 13. 3). с-м Алладжила-Уотсона del(20)(p 11. 2). с-мы Ди. Джорджи и вело-кардио-фациальный del(22)(q 11. 21) Ретинобластома и остеосаркома del(13)(q 14. 1). Нейрофиброматоз, тип I del(17)(q 11. 2)
Нозологические формы, сопровождающиеся микрохромосомными аномалиями. с-м Вольфа-Хиршхорна del(4)(p 16). с-м “кошачьего крика” del(5)(p 15. 5). с-м Вильямса del(7)(q 11. 2). с-мы Лангера-Гидиона и ТРФС-I del(8)(q 24. 1). с-мы WAGR и Денниса-Драша del(11)(p 13). с-м Видеманна-Беквита dup(11)(p 15. 3). с-м DEFECT 11 del(11)(p 12). с-м Прадера-Вилли del(15)(q 11. 2 -q 13). с-м Ангельмана del(15)(q 11. 2 -q 13 с-м Рубинштейна-Тейби del(16)(p 13). с-м Смита-Магениса del(17)(p 11. 2). с-м Миллера-Дикера del(17)(p 13. 3). с-м Алладжила-Уотсона del(20)(p 11. 2). с-мы Ди. Джорджи и вело-кардио-фациальный del(22)(q 11. 21) Ретинобластома и остеосаркома del(13)(q 14. 1). Нейрофиброматоз, тип I del(17)(q 11. 2)
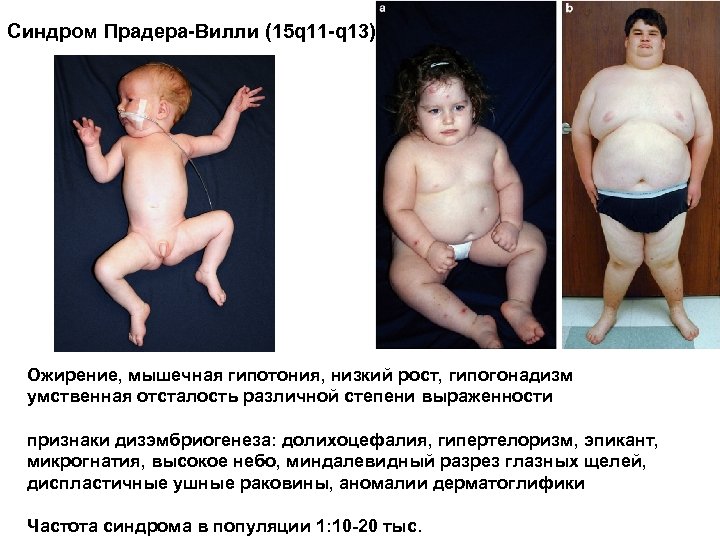 Синдром Прадера-Вилли (15 q 11 -q 13) Ожирение, мышечная гипотония, низкий рост, гипогонадизм умственная отсталость различной степени выраженности признаки дизэмбриогенеза: долихоцефалия, гипертелоризм, эпикант, микрогнатия, высокое небо, миндалевидный разрез глазных щелей, диспластичные ушные раковины, аномалии дерматоглифики Частота синдрома в популяции 1: 10 -20 тыс.
Синдром Прадера-Вилли (15 q 11 -q 13) Ожирение, мышечная гипотония, низкий рост, гипогонадизм умственная отсталость различной степени выраженности признаки дизэмбриогенеза: долихоцефалия, гипертелоризм, эпикант, микрогнатия, высокое небо, миндалевидный разрез глазных щелей, диспластичные ушные раковины, аномалии дерматоглифики Частота синдрома в популяции 1: 10 -20 тыс.
 Синдром Ангельмана (15 q 11 -q 13) - гипотония, неврологические проявления: тяжелая задержка умственного и моторного развития, атаксия, судорожная готовность, гиперрефлексия и гиперкинезия, приступы неконтролируемого смеха, хлопанье в ладоши. - микробрахицефалия с уплощенным затылком, большая нижняя челюсть, приоткрытый рот с выступающим языком, макростомия, редко растущие зубы, - гипопигментация Частота синдрома в популяции составляет 1: 20000
Синдром Ангельмана (15 q 11 -q 13) - гипотония, неврологические проявления: тяжелая задержка умственного и моторного развития, атаксия, судорожная готовность, гиперрефлексия и гиперкинезия, приступы неконтролируемого смеха, хлопанье в ладоши. - микробрахицефалия с уплощенным затылком, большая нижняя челюсть, приоткрытый рот с выступающим языком, макростомия, редко растущие зубы, - гипопигментация Частота синдрома в популяции составляет 1: 20000
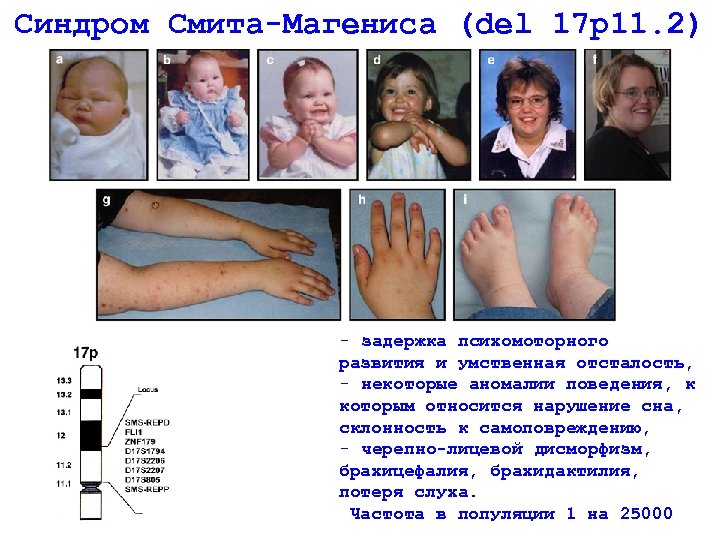 Синдром Смита-Магениса (del 17 р11. 2) - задержка психомоторного развития и умственная отсталость, - некоторые аномалии поведения, к которым относится нарушение сна, склонность к самоповреждению, - черепно-лицевой дисморфизм, брахицефалия, брахидактилия, потеря слуха. Частота в популяции 1 на 25000
Синдром Смита-Магениса (del 17 р11. 2) - задержка психомоторного развития и умственная отсталость, - некоторые аномалии поведения, к которым относится нарушение сна, склонность к самоповреждению, - черепно-лицевой дисморфизм, брахицефалия, брахидактилия, потеря слуха. Частота в популяции 1 на 25000
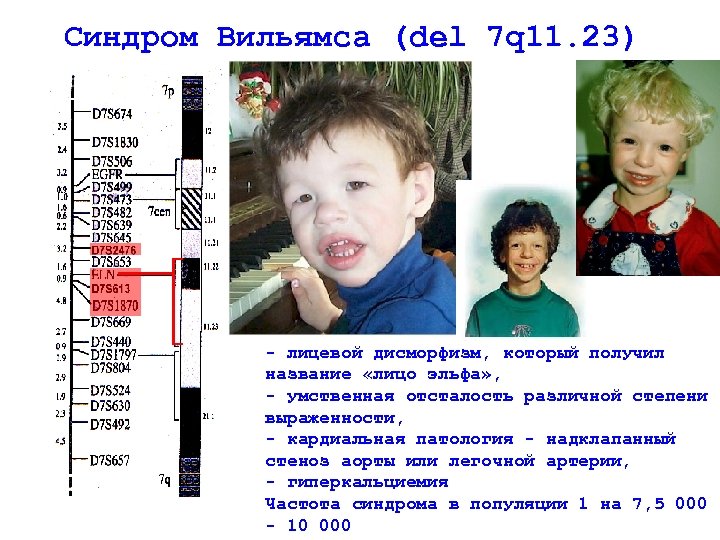 Синдром Вильямса (del 7 q 11. 23) - лицевой дисморфизм, который получил название «лицо эльфа» , - умственная отсталость различной степени выраженности, - кардиальная патология - надклапанный стеноз аорты или легочной артерии, - гиперкальциемия Частота синдрома в популяции 1 на 7, 5 000 - 10 000
Синдром Вильямса (del 7 q 11. 23) - лицевой дисморфизм, который получил название «лицо эльфа» , - умственная отсталость различной степени выраженности, - кардиальная патология - надклапанный стеноз аорты или легочной артерии, - гиперкальциемия Частота синдрома в популяции 1 на 7, 5 000 - 10 000
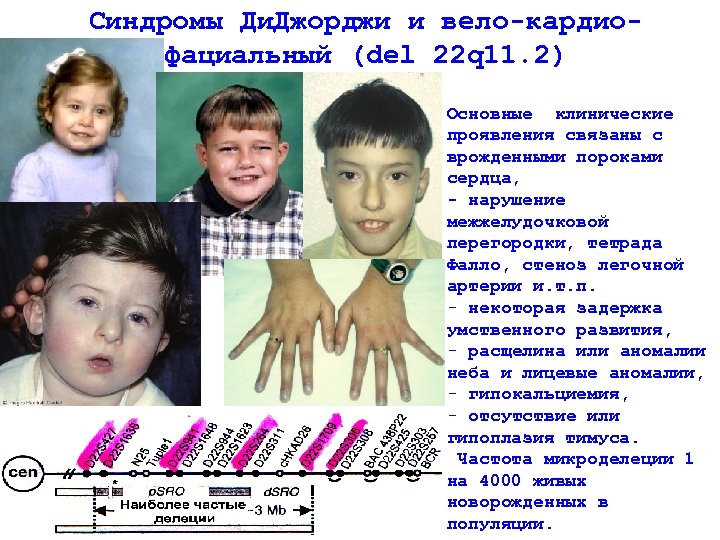 Синдромы Ди. Джорджи и вело-кардиофациальный (del 22 q 11. 2) Основные клинические проявления связаны с врожденными пороками сердца, - нарушение межжелудочковой перегородки, тетрада Фалло, стеноз легочной артерии и. т. п. - некоторая задержка умственного развития, - расщелина или аномалии неба и лицевые аномалии, - гипокальциемия, - отсутствие или гипоплазия тимуса. Частота микроделеции 1 на 4000 живых новорожденных в популяции.
Синдромы Ди. Джорджи и вело-кардиофациальный (del 22 q 11. 2) Основные клинические проявления связаны с врожденными пороками сердца, - нарушение межжелудочковой перегородки, тетрада Фалло, стеноз легочной артерии и. т. п. - некоторая задержка умственного развития, - расщелина или аномалии неба и лицевые аномалии, - гипокальциемия, - отсутствие или гипоплазия тимуса. Частота микроделеции 1 на 4000 живых новорожденных в популяции.
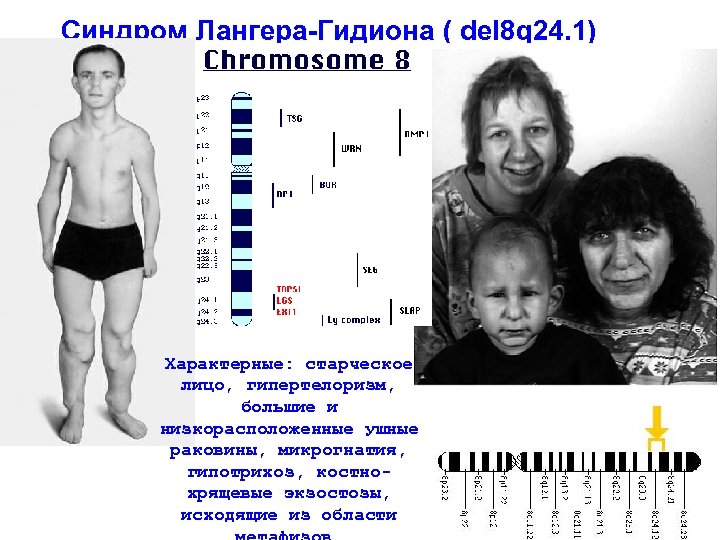 Синдром Лангера-Гидиона ( del 8 q 24. 1) Характерные: старческое лицо, гипертелоризм, большие и низкорасположенные ушные раковины, микрогнатия, гипотрихоз, костнохрящевые экзостозы, исходящие из области
Синдром Лангера-Гидиона ( del 8 q 24. 1) Характерные: старческое лицо, гипертелоризм, большие и низкорасположенные ушные раковины, микрогнатия, гипотрихоз, костнохрящевые экзостозы, исходящие из области
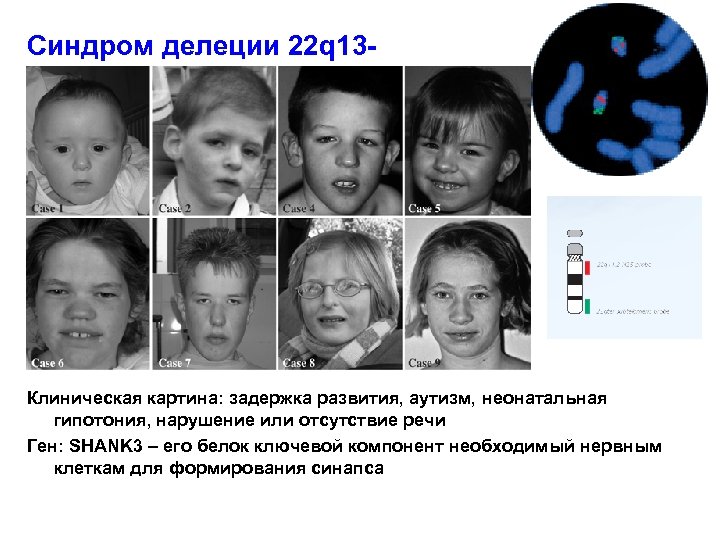 Синдром делеции 22 q 13 - Клиническая картина: задержка развития, аутизм, неонатальная гипотония, нарушение или отсутствие речи Ген: SHANK 3 – его белок ключевой компонент необходимый нервным клеткам для формирования синапса
Синдром делеции 22 q 13 - Клиническая картина: задержка развития, аутизм, неонатальная гипотония, нарушение или отсутствие речи Ген: SHANK 3 – его белок ключевой компонент необходимый нервным клеткам для формирования синапса


