Генодиагностика, принципы нанодиагностики профессор Т. А. Бажукова


Генодиагностика, принципы нанодиагностики профессор Т. А. Бажукова зав. каф. микробиологии, вирусологии и иммунологии

Генодиагностика Ø Важнейшими особенностями современной клинической медицины являются широкое использование высокоинформативных лабораторно-диагностических технологий и стремительное внедрение в практику здравоохранения новых лабораторных методов. Ø Внедренные в клиническую практику в рациональных и обоснованных комбинациях, такие технологии значительно расширили, а в ряде случаев существенно изменили представления об этиологии и патогенезе многих известных заболеваний инфекционной, аутоиммунной и опухолевой природы.

Генодиагностика Современная система доказательной медицины выдвигает для врача-клинициста несколько задач: Ø постановка диагноза на основе полученных лабораторных или других диагностически значимых методов (скрининг); Ø контроль за лечением (мониторинг); Ø определение степени резистентности к схеме лечения; Ø контроль излеченности пациента и формирование прогноза. Эти задачи на всех этапах призваны решать современные наукоемкие технологии, к которым принадлежит арсенал методов иммуно- и генодиагностики.

Методы клинической генодиагностики Ø Методы молекулярной диагностики. Ø ПЦР-детекция нуклеотидного материала микроорганизмов путем многократного увеличения числа копий консервативных участков их генома. Ø Среди основных нозологических категорий, входящих в сферу применения этих методов, - Ø заболевания инфекционной природы, Ø наследственные и Ø опухолевые формы патологии и др.

Методы иммуногенодиагностики в клинической практике Ø Чтобы правильно разработать алгоритм обследования больного и интерпретировать результаты лабораторных исследований, необходимо иметь представление об основных принципах методик, их преимуществах и недостатках. Главные характеристики любого лабораторного метода - чувствительность и специфичность. Очевидно, что в идеале оба эти показателя должны приближаться к 100%. Показатели чувствительности и специфичности методов лабораторной диагностики ИППП Ø ПЦР - 80 -95%, Ø ИФА - 45 -75%, Ø РИФ - 20 -70%.

Методы иммуногенодиагностики в клинической практике Ø На что должен обращать внимание врач? Ø Выбор объекта исследования Ø Выбор метода и сроков исследования

Выбор объекта исследования Ø Клетки крови служат резервуаром для многих вирусов и внутриклеточных микроорганизмов, но их концентрация здесь нередко бывает значительно меньше, чем в основном очаге, и может оказаться ниже предела чувствительности лабораторного метода. Ø Хламидии персистируют в моноцитах, определение в этих клетках ДНК данного микроорганизма не является приемлемым маркером острого респираторного хламидиоза. В то же время исследование бронхоальвеолярного лаважа оказывается весьма информативным.

Выбор объекта исследования Ø При нейроинфекциях в качестве объекта исследования целесообразно использовать спинномозговую жидкость. Ø В ряде случаев при урогенитальной патологии, особенно у женщин с вторичным бесплодием, хламидии могут персистировать в маточных трубах, в спайках, но при этом в соскобах их нижних отделов урогенитального тракта они не обнаруживаются. Ø По некоторым данным, частота выявления C. trachomatis методом ПЦР у женщин составляет 22, 5% при исследовании материала из цервикального канала, 29% - из влагалища и 14% - из уретры, поэтому для диагностики урогенитальных инфекций желательно брать материал из нескольких точек.

Выбор объекта исследования Ø Большое значение имеет техника забора материала. Ø Неправильная техника забора биоматериала может привести к тому, что инфицированные клетки не попадут в исследуемую пробу либо избыточное количество посторонних примесей (гноя, крови и др. ) затруднит дальнейшее исследование. Ø Неправильные транспортировка и хранение образца также негативно сказывается на результате анализа. Так гемолиз приводит к ингибированию ПЦР, а при повторных многократных замораживаниях и размораживаниях образцов снижается уровень специфических антител, что влияет на качество метода ИФА.

Выбор метода и сроков исследования Ø Применительно к инфекционной патологии лабораторные исследования можно разделить на методы прямой детекции патогена (РИФ, ПЦР, иногда ИФА) и косвенные, при которых определяется уровень специфических антител к возбудителю (ИФА, реже - РИФ). Ø Как правило, серологическими методами целесообразно пользоваться: Ø при наличии распространенных инфекционно- воспалительных процессов; Ø при послеродовых осложнениях, когда массивная антигенная нагрузка обеспечивает выработку достаточного количества антител; Ø для диагностики внутриутробных инфекций (в режиме исследования парных сывороток матери и плода)

Выбор метода и сроков исследования Ø Молекулярно-генетические методы пригодны как для диагностики манифестированных форм инфекции, так и для латентных, субклинических форм, когда отмечается длительная персистенция возбудителя. Ø Обнаружение генетического материала возбудителя служит лишь свидетельством инфицирования, а не инфекционного заболевания. Ø Эти методы не являются безусловным доказательством этиологической значимости выявленного возбудителя в патологическом процессе.

Выбор метода и сроков исследования Ø Весьма перспективно применение молекулярно- генетических технологий для ранней диагностики онкологической патологии и заболеваний, предшествующих стадии онкогенеза. Ø За последние десятилетия отмечается неуклонный рост этой патологии, а количество картированных и клонированых генов, вовлеченных в канцерогенез, увеличивается с каждым днем. Ø Поэтому молекулярно-биологические исследования в онкологии являются самостоятельным направлением в геномике человека и на сегодняшний день составляют в большей степени фундаментальную проблему, разрешения которой требует клиническая практика.

Выбор метода и сроков исследования Молекулярная диагностика в онкологии сегодня – выделяет основные направления: Ø диагностика наследственных форм рака; Ø поиск и диагностика молекулярных маркеров неблагоприятного прогноза при онкологических заболеваниях; Ø поиск маркеров и диагностика микрометастазов; Ø диагностика полиморфных ДНК-маркеров, предрасполагающих к онкогенезу.

Выбор метода и сроков исследования Ø Доказана связь генов: Ø с диабетом, Ø аутоиммунным тиреоидитом, Ø ревматоидным артритом, Ø рассеянным склерозом, Ø злокачественными опухолями и Ø некоторыми другими заболеваниями. Ø Выявлено более 20 заболеваний, ассоциированных с генами, в том числе с локусами HLA. Сюда можно отнести мышечную дистрофию Дюшенна (МДД), которая является наиболее распространенным наследственным нервно-мышечным заболеванием человека. Его частота - около 1: 5000 новорожденных мальчиков. Ø Наследственные формы рака молочной железы составляют около 5% всех карцином молочной железы.

Выбор метода и сроков исследования Поиск прогностически ценных молекулярных маркеров при Ø раке молочной железы, Ø предстательной железы, Ø колоректальных опухолях, Ø меланомах, Ø нейробластоме - одно из наиболее разрабатываемых направлений исследований в сфере клинической генодиагностики соматических заболеваний. Ø Методами ПЦР-анализа и блоттинга установлено, что экспрессия и гиперэкспрессия ряда генов - неблагоприятные признаки развития заболевания.

Выбор метода и сроков исследования Ø Диагностика микрометастазов в крови, лимфатических узлах и костном мозге при высокоинвазивных опухолях, для контроля эффективности лечения и мониторинга в периоды ремиссий. Ø Молекулярные методы позволяют определить 1 -2 клетки среди 1 -5 млн. лимфоцитов. Основным методическим подходом для такой диагностики считается ПЦР на обратнотранскрибированной м. РНК (RT-PCR), выделенной из анализируемого образца. Ø Экспрессия опухолеспецифических генов, характерная для метастатической клетки, позволяет идентифицировать ее среди сотен тысяч неизмененных клеток. Ø Определение круга генов, экспрессирующихся в опухоли. Для ряда опухолей (меланома, метастазирующая нейробластома, микрометастазы рака молочной железы и др. ) такие маркеры уже найдены.

Генодиагностика в неврологии Ø ДНК-диагностика чрезвычайно затруднена. При проведении косвенной ДНК-диагностики могут использоваться как маркеры, сцепленные с геном болезни. Ø В качестве примеров заболеваний с установленными генами, при которых с успехом применяют косвенную ДНК-диагностику, можно назвать атаксию- телеангиэктазию, гепатолентикулярную дегенерацию, различные формы аутосомно-рецессивных прогрессирующих мышечных дистрофий и др. Ø Косвенный ДНК-анализ можно применять в качестве дополнительного диагностического метода у лиц из группы риска при отрицательных результатах традиционного мутационного скрининга.

Генодиагностика в неврологии Ø Например, у больных с миопатией Дюшенна— Беккера при невозможности обнаружения конкретных нуклеотидных изменений в гигантском гене дистрофина косвенная ДНК-диагностика с вне- или внутригенными маркерами позволяет с высокой вероятностью определять генетический статус лиц из групп риска (родственники пробанда мужского пола) или плода (при проведении пренатальной диагностики у женщин-носителей мутантного гена), Ø а также проводить диагностику гетерозиготного носительства мутантной хромосомы у женщин в семьях высокого риска.

Генодиагностика в неврологии Классификация Ø Идентификация генов и разработка разнообразных методов ДНК-диагностики нейрогередитарных заболеваний способствовали внедрению наиболее совершенного геномного подхода к их классификации. Это позволило на качественно новом уровне решить одну из наиболее сложных проблем нейрогенетики — построение четкой и упорядоченной современной номенклатуры наследственных заболеваний нервной системы. Ø Существовавшие ранее классификации отдельных групп заболеваний базировались главным образом на клинико-морфологическом подходе, что приводило к серьезным затруднениям при определении нозологической принадлежности отдельных синдромов ввиду выраженного меж- и внутрисемейного полиморфизма наследственных болезней нервной системы, существования ряда так называемых переходных, стертых форм и т. д.

Генодиагностика в неврологии Ø Современная геномная классификация основана на определении прямой взаимосвязи между конкретной нозологической формой и повреждением определенного гена. Ярким примером может служить группа аутосомно-доминантных атаксий, систематизация которых до недавнего времени была чрезвычайно затруднена. Ø В самые последние годы было убедительно продемонстрировано, что вариабельность клинико- анатомической картины аутосомно-доминантных атаксий обусловлена генетической гетерогенностью данной группы заболеваний. Ø На сегодняшний день устанолено существование как минимум 14 различных генов, локализованных на отдельных хромосомах, мутации которых в виде экспансии тринуклеотидных CAG-повторов обусловливают развитие доминантных атактических синдромов.

Генодиагностика в неврологии Ø Стала возможной предельно четкая и объективная молекулярно-генетическая классификация доминантных атаксий на основе прямой ДНК- диагностики: в зависимости от того, в каком из исследуемых генов обнаруживается динамическая мутация, соответствующий клинический синдром обозначается как спиноцеребеллярная атаксия 1 -го (2 - го, 3 -го, 4 -го и т. д. ) типа. Ø Аналогичным образом строится в настоящее время классификация наследственных невропатий (идентифицировано 13 генов демиелинизируюших и аксональных моторно-сенсорных невропатий), аутосомных форм конечностно-поясной прогрессирующей мышечной дистрофии (свыше 10 генов) и других групп наследственных неврологических заболеваний. Ø Вопрос геномной классификации наследственных болезней имеет ярко выраженную практическую направленность.

Генодиагностика атеросклероза и сердечно-сосудистых заболеваний Ø В крупных городах России ежегодно регистрируется 300 случаев инфаркта на каждые 100 тысяч жителей. Совсем недавно он считался болезнью пожилых, но за последние годы наметилась тревожная тенденция - инфаркт быстро "молодеет". Ø Причин для этого много: Ø стресс, Ø нарушение питания, Ø курение, Ø недостаточная физическая активность.

Генодиагностика атеросклероза и сердечно-сосудистых заболеваний Ø Но существует еще одна, очень весомая причина развития ишемической болезни сердца, следствием которой бывает инфаркт, - генетическая предрасположенность. Ø Будущее медицины принадлежит генетике. Именно она станет основой профилактики и лечения заболеваний, в том числе ишемии сердца и инфаркта. Ø Одно из важных преимуществ генетики заключается в том, что она дает возможность выявить риск развития заболевания задолго до его клинических проявлений.

Генодиагностика атеросклероза и сердечно-сосудистых заболеваний Ø Во многих случаях причиной сердечно- сосудистой патологии становятся атеросклеротические нарушения в сосудах сердца, приводящие к ухудшению снабжения его кровью, из-за чего развивается ишемия. Атеросклеротическая бляшка может оторваться от стенки сосуда и закупорить его. В результате происходит кровоизлияние, то есть инфаркт миокарда. Ø Атеросклероз, естественный процесс, происходящий в организме любого человека. Первые признаки атеросклероза сосудов наблюдаются уже у новорожденных. С возрастом этот процесс прогрессирует, но у разных людей с разной интенсивностью, что связано с генетическими факторами.

Генодиагностика атеросклероза и сердечно-сосудистых заболеваний Ø Курение, неправильное питание, стресс, инфекция способствуют более быстрому развитию атеросклероза. Ø Вероятность развития угрожающих жизни осложнений после инфаркта миокарда также обусловлена генетически. Ø Диагностика по генам позволяет заранее определить склонность к тому или иному заболеванию и вовремя принять профилактические меры, предотвратив его развитие или облегчив его течение.

Генодиагностика атеросклероза и сердечно-сосудистых заболеваний Ø В известной степени решением проблемы определения этиологии заболевания может стать модификация ПЦР в режиме реального времени (real-time PCR), которая соединила в себе достоинства традиционной ПЦР - высокую чувствительность и специфичность, с одной стороны, и количественного ИФА - с другой, что позволяет не только идентифицировать микроорганизм, но и определять количество возбудителя в пробе. Ø Это особенно актуально для мониторинга течения и эффективности терапии таких социально значимых заболеваний как ВИЧ-инфекция туберкулез и вирусные гепатиты.

Генотипирование по одному гену Ø К этой группе относятся методы, основанные на амплификации определенного гена с помощью ПЦР и дальнейшей идентификации ампликона. Ø Способы идентификации: Ø гель-электрофорез (специфический ампликон должен иметь определенную длину и соответствующую электрофоретическую подвижность); Ø рестрикционный анализ (ампликон подвергается действию ферментов-рестриктаз, нарезающих его на характерное число фрагментов определенной длины); ПЦР с иммуноферментным детектированием (аналог ИФА при котором ампликон связывается со специфическим зондом); и другие.

Генотипирование по одному гену Ø Экспресс-методы способны обнаружить лишь ограниченное число вариаций гена, но ампликон можно характеризовать полностью путем его дальнейшего прямого секвенирования. Любые методики, работающие только с одним геном, упускают потенциально существенную информацию и, следовательно, недостаточно пригодны для классификации бактерий и филогенетических исследований. Ø ПЦР-технологии для идентификации серогруппы менингококка являются технологиями генотипирования по одному гену. Поскольку антигенные свойства белков наружной мембраны класса 1 и классов 2/3, характеризующие серотип и серосубтип менингококка, также определяются соответствующими генами, возможно серотипирование и серосубтипирование на основе ПЦР-технологий.

Генотипирование по всему геному Ø К этой группе относятся гель-электрофорез в пульсирующем поле (ППГЭ), ПЦР-амплификация со случайными праймерами или праймерами, комплементарными повторяющимся последовательностям. Ø При ППГЭ весь геном бактерии подвергается действию набора ферментов-рестриктаз, а затем фрагменты характеризуются путем электрофореза в меняющемся во времени и пространстве электрическом поле; в результате каждый фрагмент занимает в геле позицию, зависящую от его длины. Ø Случайные праймеры или праймеры, комплементарные повторяющимся последовательностям, - это короткие праймеры, связывающиеся с большим количеством участков бактериального генома. В результате амплификации получается большое количество ампликонов, число и длина которых определяется числом и позицией потенциальных мест связывания праймеров в бактериальном геноме. Ø Затем фрагменты характеризуются по подвижности в гель- электрофорезе.
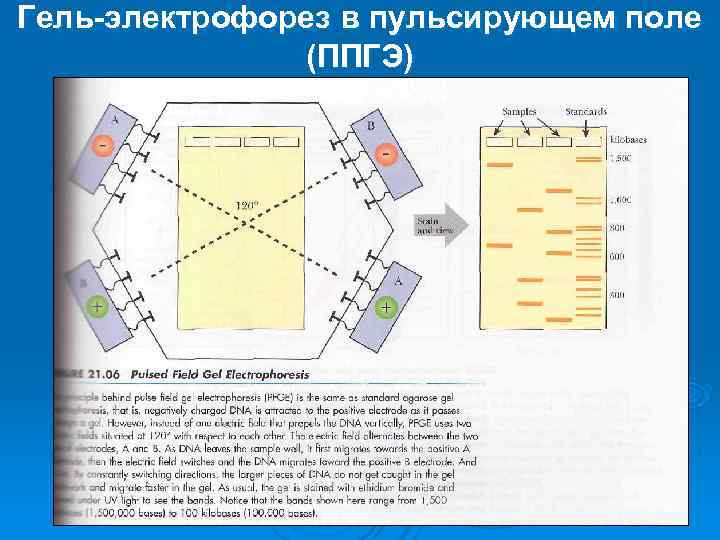
Гель-электрофорез в пульсирующем поле (ППГЭ)

Гель-электрофорез в пульсирующем поле (ППГЭ) Ø Электрофоретическая картина-паттерн, т. е. специфический набор полос на электрофореграмме препарата ДНК штамма. Паттерн практически уникален, то есть если при сравнении двух штаммов получаются одинаковые паттерны - это указывает на их идентичность.
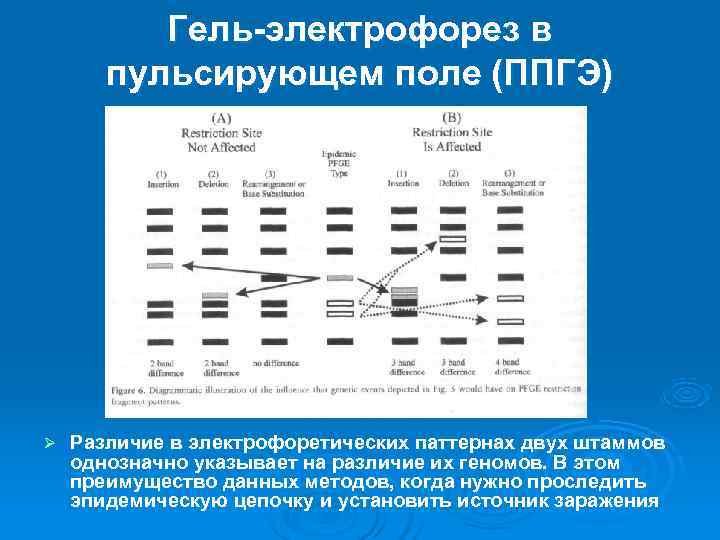
Гель-электрофорез в пульсирующем поле (ППГЭ) Ø Различие в электрофоретических паттернах двух штаммов однозначно указывает на различие их геномов. В этом преимущество данных методов, когда нужно проследить эпидемическую цепочку и установить источник заражения

Генотипирование по всему геному Ø Ограничение данных методов в том, что различие в электрофоретических паттернах непосредственно не раскрывает природы, локализации и биологического смысла различия, требующего исследования иными методами. Ø «Молчащая" мутация, не приводящая к замене аминокислоты и изменению свойств белка, вполне может привести к изменениям, выявляемым методами ППГЭ или ПЦР со случайными праймерами.

Мультилокусное секвенирование- типирование (МЛСТ) Основные принципы МЛСТ 1. Выбирается ограниченное количество (от 6 до 10) бактериальных генов, предпочтительно "нейтральных", не кодирующих известные факторы вирулентности или патогенности, но являющихся маркерами филогенетического родства. В исследуемой популяции каждый ген должен встречаться в достаточном числе аллелей (более десяти). Желательно, чтобы вариации в данных генах накапливались медленно, а обладание тем или иным аллелем маркерного гена само по себе не обуславливало явных эволюционных преимуществ штамма. Этому условию соответствуют гены цитоплазматических ферментов, отвечающих за внутриклеточный метаболизм.

Мультилокусное секвенирование- типирование (МЛСТ) 2. Для каждого исследуемого штамма нуклеотидные последовательности выбранных генов (или их участков) определяются методом прямого секвенирования. Каждая уникальная последовательность определяет аллель локуса. Набор аллелей исследуемых локусов конкретного штамма определяет его сиквенс-тип (СТ). Эволюционные взаимосвязи различных СТ и генетическое расстояние между ними оценивается с помощью существующего специализированного программного обеспечения.

Мультилокусное секвенирование- типирование (МЛСТ) 3. В Интернете поддерживаются общедоступные веб-сайты, содержащие базы данных об известных уникальных последовательностях и соответствующих им СТ. Ø В общемировой базе хранятся в стандартизованной форме индивидуальные сведения о каждом штамме, включающие СТ и, если известно, данные о типировании другими методами (серологическими и пр. ) и эпидемиологические данные (страна выделения, источник изолята - например, СМЖ - и пр. ). Таким образом, со временем проясняется взаимосвязь между МЛСТ и традиционными методами типирования.

Мультилокусное секвенирование- типирование (МЛСТ) 4. В силу специфики методов получения и хранения информации о СТ, данные, получаемые различными лабораториями, абсолютно сопоставимы. В перспективе это позволит провести глобальный эпидемиологический анализ распространения штаммов в разное время, на различных территориях, среди пациентов с различными патологиями, и т. д. и т. п.

• Дендрограмма генетического родства (на основе матрицы попарных различий аллельных профилей), построенная по методу UPGMA, объединяет эти СТ в несколько больших кластеров (Рис. 2).

МЛСТ 4. На дендрограмме родства по МЛСТ в первую очередь четко отличаются менингококки серогруппы А от менингококков серогрупп В и С. Ø Это подтверждает современные представления о том, что для популяции менингококков группы А характерна клональная структура, в то время как среди менингококков групп В и С имеет место интенсивный процесс рекомбинаций и горизонтального переноса, в том числе и генов, ответственных за синтез капсулы В или С, что приводит к достаточно быстрому размыванию клональной структуры.

МЛСТ 5. На дендрограмме родства по МЛСТ могут быть четко выделены так называемые гипервирулентные подгруппы (субгруппы I, III и IV менингококков серогруппы А, а также ET-5 и ET-37 комплексы, А 4 кластер и "ветвь 3" менингококков серогрупп В и С. Выделяется также ряд устойчивых субгруппы А, имеющих меньшее эпидемическое значение (субгруппы V, VI, X и др. )

Мультилокусное секвенирование- типирование (МЛСТ) 6. Результаты генотипирования методом МЛСТ и методом ПЦР-амплификация со случайными праймерами в принципе совпадают, хотя последний метод более подвержен влиянию "шумов", вызванных несущественными мутациями. Также результаты генотипирования методом МЛСТ совпадают с результатами, полученными с помощью популярного ранее за рубежом, но чрезвычайно трудоемкого и доростоящего метода мультилокусного энзимоэлектрофореза.
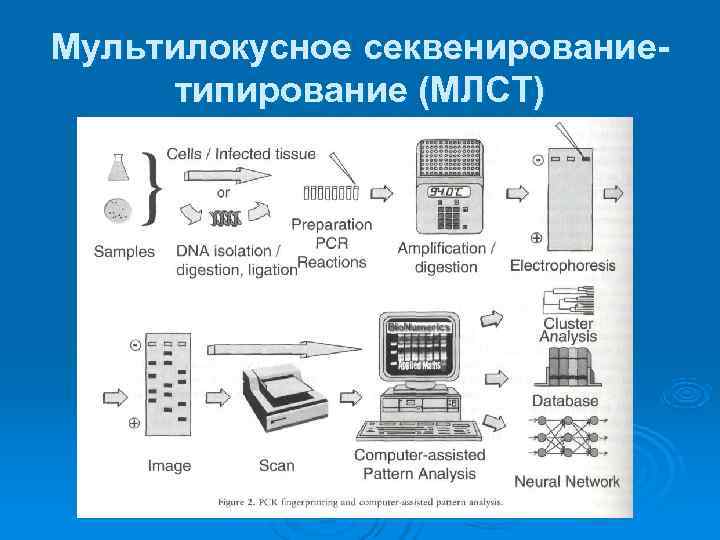
Мультилокусное секвенирование- типирование (МЛСТ)

Современные методы генодиагностики Ø Полимеразно-цепная реакция (ПЦР) Ø Секвенирование ДНК Ø Саузернблоттинг Ø Нозернблоттинг Ø ДНК-гибридизация Ø Риботипирование Ø Рестрикционный анализ

Полимеразная цепная реакция (ПЦР) Ø ПЦР заключается в амплификации, т. е. увеличении количества копий специфического (маркерного) гена возбудителя. Ø Выделенную из исследуемого материала ДНК, «расплетают» при нагревании около 90 °С (денатурируют) Ø Достраивают к расплетенным нитям ДНК новые комплементарные нити, снижая температуру до 50 °С ( «отжиг» ). Достраивание (при 70 °С) новых комплементарных нитей ДНК происходит при добавлении к искомым генам праймеров (затравки из коротких однонитевых ДНК, комплементарных 3'-концам ДНК искомого гена), ДНК-полимеразы и нуклеотидов. Ø 3'-концы праймеров достраиваются добавлением термостабильной полимеразы ( «Taq-полимеразы» ). В результате достраивания комплементарных нитей ДНК из одного гена образуются два. Ø Этот цикл копирования генов, состоящий из денатурации, ренатурации и элонгации многократно повторяется при заданных температурных режимах. Ø Продукты ПЦР отделяют с помощью гель-электрофореза и выявляют с помощью добавления этидия бромида, который флюоресцирует при освещении ультрафиолетом.
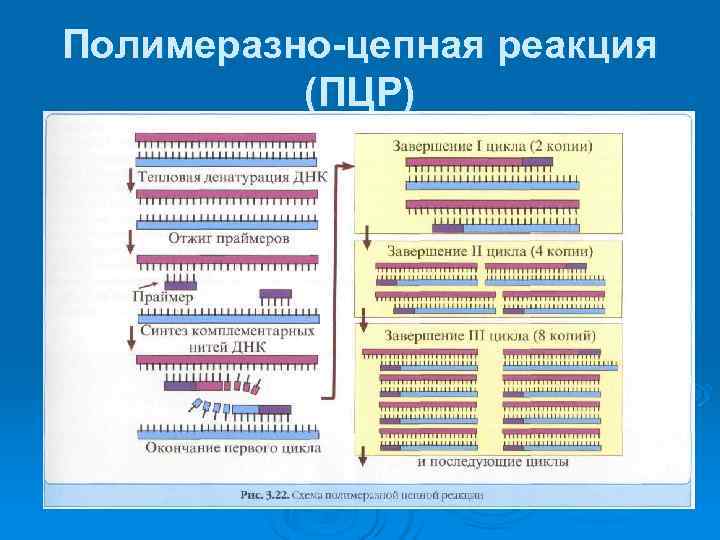
Полимеразно-цепная реакция (ПЦР)
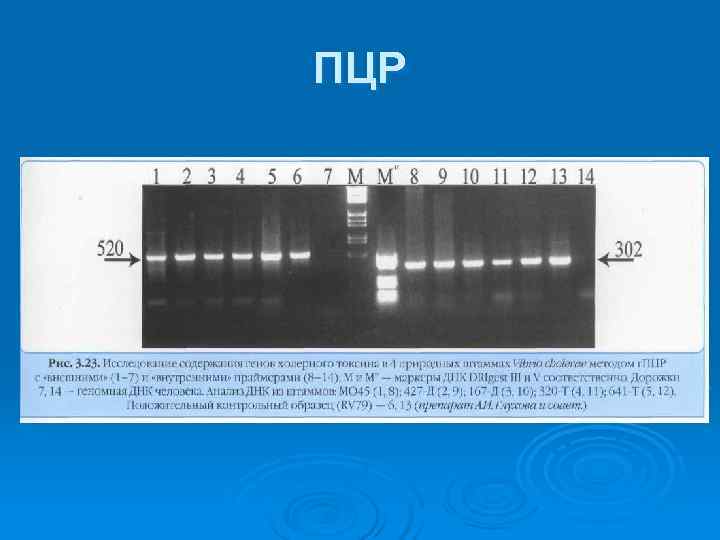
ПЦР
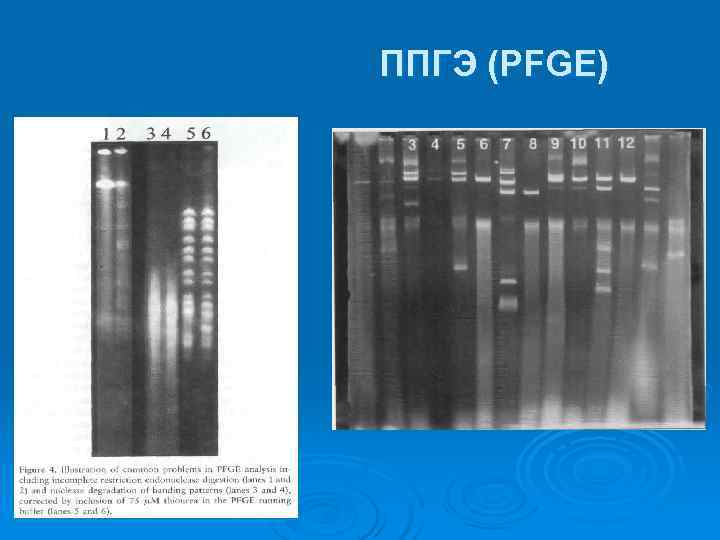
ППГЭ (PFGE)

Секвенирование ДНК Ø При идентификации микроорганизмов используют секвенирование ДНК для чего экстрагируют нуклеиновую кислоту, амплифицируют специфическую последовательность нуклеотидов методом ПЦР, определяют ее и проводят компьютерный подбор соответствующего «сиквенса» в базе данных. Обычно для секвенирования используют ДНК-копию гена 16 S р. РНК — наиболее стабильный компонент бактерий и ген белка теплового шока (HSP 65).
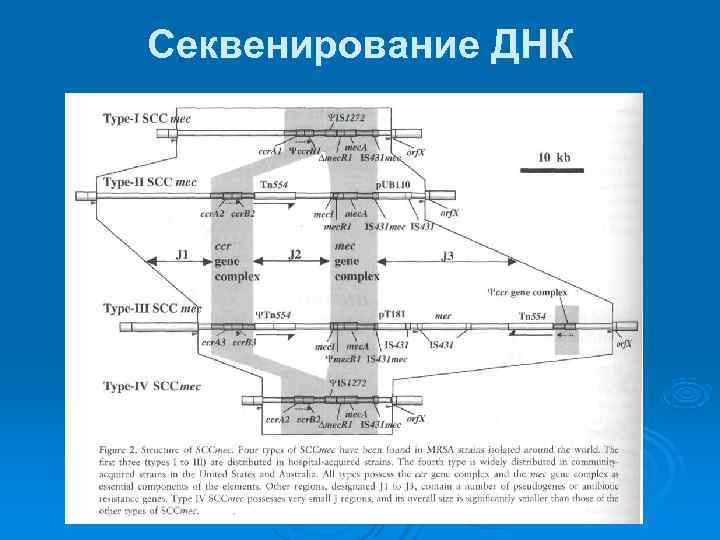
Секвенирование ДНК

Секвенирование ДНК

ДНК-гибридизация Ø Денатурация, т. е. разделениу двунитевой ДНК на отдельные нити в щелочной среде (90°С) Ø Восстановление (отжиг) двунитевой структуры с комплементарной меченой нитью ДНК (молекулярным зондом) (10 -37°С). Ø Гибридизацию проводят на фильтрах (блот- гибридизация) или in situ. Молекулярный зонд с присоединенным биотином гибридизируется на ДНК мишени. Ø После отжига и промывки на образец наносят антибиотиновый конъюгат (стрептавидин, соединенный со щелочной фосфатазой) и проводят специфическое окрашивание клеток. Ø Стрептавидин с меткой избирательно связывается с биотином, что выявляется при микроскопии. Так выявляют локализацию микробов в ткани, хромосомные аномалии в клетках и т. д.

Методы ДНК гибридизации

Саузернблоттинг Ø Разделение фрагментов ДНК (гель-электрофорез) Ø Перенос в щелочной раствор для получения однонитевых фрагментов ДНК. Ø Перенос на нитроцеллюлозную или нейлоновую мембрану Ø Гибридизация со специфической меченой пробой ДНК Ø Выявление полос меченого зонда ДНК путем экспонирования фильтра с рентгеновской пленкой (ауторадиография), Ø Зонды, меченые флюорохро- мом, выявляют при помощи люминесцентной микроскопии.

Саузернблотинг

Нозернблоттинг Ø Применяют для выявления и гибридизации РНК (фрагментов РНК). Ø Размер и количество специфических молекул и. РНК определяется после обработки общей РНК или поли (А) РНК. Ø Молекулы РНК выделяют гель-электрофорезом и переносят на иммобилизованную мембрану. Ø Искомые последовательности РНК определяют гибридизацией с меченой пробой.

Риботипирование Выявление количественных различий по рибосомным оперонам и нуклеотидным последовательностям. Ø Проводят гидролиз ДНК, которую разделяют в агарозном геле и затем гибридизируют с ДНК-зондами на один или более генов, кодирующих 16 S-, 23 S-, 5 S-рибосомные РНК. Ø Бактерии можно типировать по серотипу, фаготипу и по риботипу. Методически сходно с риботипированием S-типирование: проводят сравнительный анализ числа копий S-элементов и рестрикционного разнообразия нуклеотидных последовательностей различных штаммов микробов.
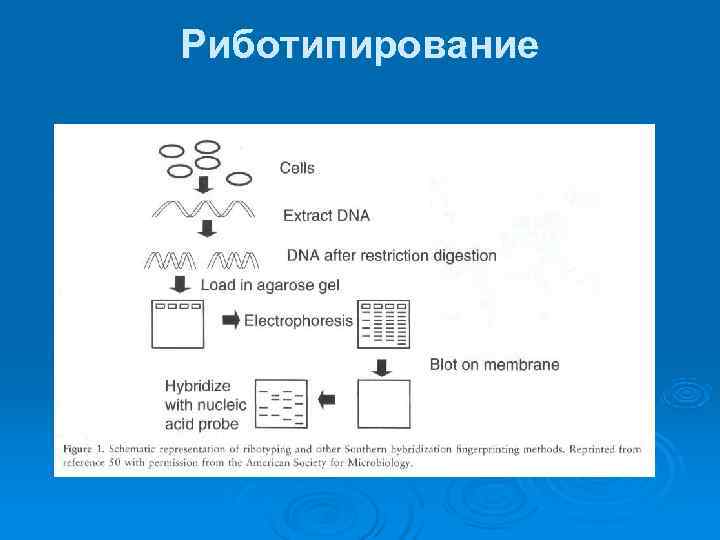
Риботипирование
Риботипирование

Рестрикционный анализ Ø ДНК расщепляют с помощью рестриктаз (бактериальных эндонуклеаз) Ø Отдельные рестриктазы способствуют выделению строго определенных фрагментов ДНК. Размер полученных фрагментов ДНК можно определить путем электрофореза в агарозном или полиакриламидном геле. Ø После электрофореза каждый фрагмент ДНК располагается в определенном участке геля в виде дискретной полосы. Фрагменты ДНК выявляют путем обработки геля бромидом этидия, который связывается с ДНК. Ø Такие фрагменты ДНК высвечиваются при ультрафиолетовом облучении в красной области спектра. Длину каждого фрагмента можно выявить, сравнивая расстояние, пройденное фрагментом ДНК при электрофорезе, с расстоянием, пройденным стандартным фрагментом ДНК известного размера.

Наномедицина: применение макромолекул и наночастиц для диагностики и лечения болезней, а также репарации поврежденных тканей (National Institutes of Health, USA) Н а н о ш к а л а 10 -12 m 10 -9 m 10 -7 m 10 -6 m 10 -3 m 1 m (pm) (nm) (mm) Атомы (0, 1 -0, 5 nm) Белки, ДНК Бактерии (0, 1 -10 mm) Многоклеточные РНК, антитела, Эритроциты (10 mm) организмы (1 mm >) вирусы (1 -100 nm) Яйцеклетка человека (100 mm) Рентгеновское Ультрафиолет (100 nm) Видимый свет (1 mm) Микроволны (1 sm) излучение (0, 1 -10 nm) Инфракрасные Лучи (10 mm)
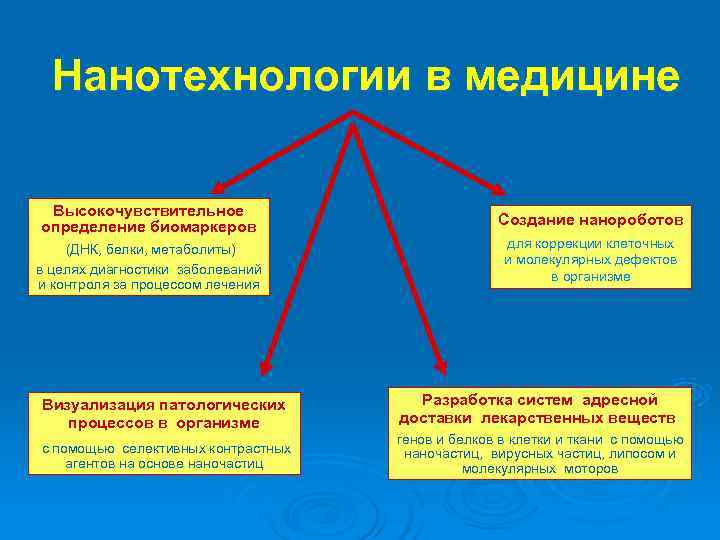
Нанотехнологии в медицине Высокочувствительное определение биомаркеров Создание нанороботов (ДНК, белки, метаболиты) для коррекции клеточных и молекулярных дефектов в целях диагностики заболеваний в организме и контроля за процессом лечения Визуализация патологических Разработка систем адресной процессов в организме доставки лекарственных веществ, генов и белков в клетки и ткани с помощью селективных контрастных наночастиц, вирусных частиц, липосом и агентов на основе наночастиц молекулярных моторов

Наночастицы Ø Что такое наночастицы? Ø Прежде всего, приставка нано- указывает на размер: один нанометр (нм) – это одна миллиардная метра. Отсюда название целого направления работ - нанотехнологии, т. е. технологии, имеющие дело с частицами любого вещества размером порядка нанометров. Ø Согласно наиболее распространенной классификации различают кластеры (частицы размером 1 -10 нм) и собственно наночастицы (размером от 10 до 50 нм). Известно, что физические и химические свойства вещества в этой области размеров отличаются как от свойств отдельных атомов и ионов, так и от свойств массивного вещества.

Наночастицы Ø Например, для многих металлов при переходе в наносостояние существенно изменяются механические, электрические, магнитные, оптические и химические свойства. Это позволяет усиливать или ослаблять известные свойства металлов, а также создавать совершенно новые металлические или металлсодержащие материалы с необычными, до сих пор неизвестными свойствами. Ø Особые, часто весьма замечательные свойства вещества в наносостоянии и прекрасные перспективы применения наноматериалов во многих областях жизни – вот главные причины столь высокого интереса к нанотехнологиям.
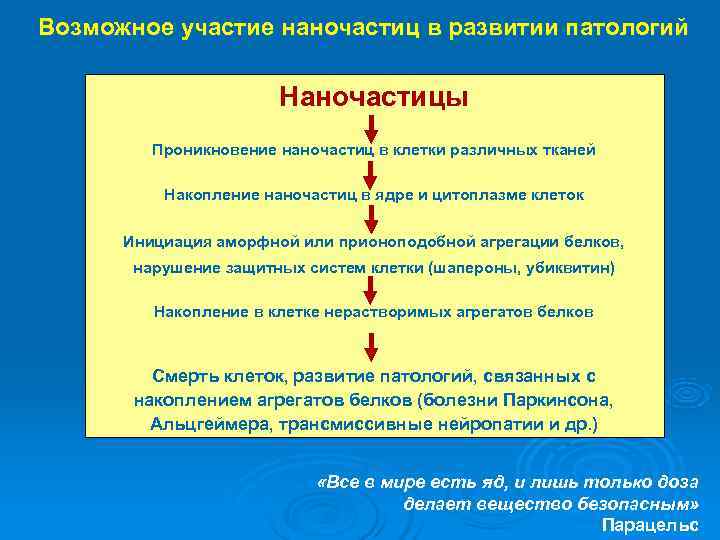
Возможное участие наночастиц в развитии патологий Наночастицы Проникновение наночастиц в клетки различных тканей Накопление наночастиц в ядре и цитоплазме клеток Инициация аморфной или прионоподобной агрегации белков, нарушение защитных систем клетки (шапероны, убиквитин) Накопление в клетке нерастворимых агрегатов белков Смерть клеток, развитие патологий, связанных с накоплением агрегатов белков (болезни Паркинсона, Альцгеймера, трансмиссивные нейропатии и др. ) «Все в мире есть яд, и лишь только доза делает вещество безопасным» Парацельс

Нанотехнология Ø НАНО - приставка, означающая десять в минус девятой степени, или одну миллиардную долю метра. Ø Нанотехнология позволит создавать абсолютно любые объекты манипулируя отдельными атомами вещества. Она, заменив другие технологии, позволит не только победить старение и болезни, дав нам Бессмертие и время Вечной молодости, но и обеспечит человечество фантастическими материальными богатствами, позволит освоить космическое пространство.

Нанотехнология Ø Нанотехнология - отрасль молекулярной технологии, ориентированная на получение устройств, роботов, веществ с наперед заданной молекулярной структурой, производя их атом за атомом.

Задачи нанотехнологий Нанотехнология решает следующие задачи: Ø Создание твердых тел и поверхностей (материалов и пленок) с измененной молекулярной структурой. На практике это даст сверхпрочные металлы, ткани, пластмассы; самовосстанавливающиеся материалы. Ø Создание новых химических веществ посредством составления молекул (без химических реакций). Это даст массу новых лекарств (в ближайшие 10 -20 лет, потом они будут не нужны), которые врачи будут "конструировать" исходя из болезни. Также создание биологически совместимых полимеров, в основном на базе углерода. Это потребуется для наномедицины. Нанороботы должны приниматься организмом как "свои" и не провоцировать "атаки" антител.

Задачи нанотехнологий Ø Создание сверхпроводников нового типа, т. н. сверххолодных. Также - коммуникационных линий: нанотрубки, ДНК 4 G. (ДНК 4 G – обыкновенная ДНК, в которой гуаниновые основания заменены на проводящие или непроводящие участки, что позволит получить структуру с различной электропроводимостью). Ø Создание нанокомпьютера. Дальнейшая миниатюризация и радикальное повышение вычислительной мощности.

Задачи нанотехнологий Ø Разработка самореплицирующихся (саморазмножающихся) систем на базе биоаналогов – бактерий, вирусов, простейших. Ø Проектирование и испытание моделей наномашин (нанодвигателей). Ø Создание прецизионных (точных) наноманипуляторов и многое другое

Наномедицина Ø А что же такое Наномедицина? Ø По каноническому определению ведущего учёного в данной области Р. Фрейтаса это: "слежение, исправление, конструирование и контроль над биологическими системами человека на молекулярном уровне, используя разработанные наноустройства и наноструктуры". Ø В действительности наномедицины пока еще не существует, существуют лишь нанопроекты, воплощение которых в медицину, в конечном итоге, и даст результат. Ø Но научное проектирование и прогнозирование тоже очень важная и нужная вещь. Через несколько десятков лет, когда уже будет работан первый наноробот-сборщик, знания, накопленные наномедициной, воплотятся в жизнь.

Что такое наномедицина? США: NIH Roadmap Initiative Европа: Наномедицина : применение Наномедицина: применение нанотехнологии для диагностики, нанотехнологии в здравоохранении лечения и контроля состояния пациента В США в 2005 -2006 гг. создано 8 центров Создается европейская развития наномедицины : технологическая платформа в области 1. Центр исследования белковых наномедицины и сформулированы машин клеточного ядра стратегические направления 2. Phi 29 ДНК-упаковывающий мотор исследований: для наномедицины 3. Центр системного контроля 1. Нанодиагностика, включая регуляторных сетей клеток визуализацию 4. Центр оптического контроля биологических функций 2. Направленная доставка и 5. Центр изучения механизмов контролируемое высвобождение сворачивания белков лекарственных веществ 6. Национальный центр разработки биомиметических нанопроводников 3. Регенеративная медицина 7. Разработка систем клеточного контроля: искусственные сигнальные и двигательные системы. 8. Наномедицинский центр исследования механики в регенеративной медицине

Наномедицина Ø Нанороботы будут способны ремонтировать клетки. Снабжённые полным описанием человеческого тела с точностью до атома они смогут вернуть даже очень старого человека в то состояние, в котором он был в молодости. Ø От операций на органах мы перейдём к операциям на молекулах и станем практически бессмертными. Ø Замороженные при помощи крионики найдут свое воскрешение – миллионы роботов смогут поклеточно восстановить их разрушенные в процессе замораживания клетки.

Научные направления Ø Мультифакторная терапия старения организма человека культурами аутологичных стволовых клеток (предшественники нервных клеток, кардиомиоцитов, миобластов, Клеточная терапия соматических опухолей (трансфузия транспортной системы из аутологичных СД 34+ клеток предшественников с приклепленными липосомами, содержащими химиотерапевтический препарат. Клеточная терапия нейроглиом (трансфузия транспортной системы аутологичных СД 34+стволовых клеток с предшественниками 5 - фторурацила с интраселективным получением 5 -фторурацила в зоне опухоли мозга). Ø Применение аутологичных гемопоэтических стволовых клеток и транспортных иммунолипосомных наноконтейнеров с радиоизотопным (J 125) и противоопухолевым препаратом ("Иринотекан"тм) для диагностики и химиотерапии глиобластом головного мозга.

Научные направления Ø Клеточная терапия инсультов (трансфузии и трансплантации аутологичных мобилизованных стволовых клеток, эндотелиоцитов в геронтологической практике. Ø Тканевая инженерия в стоматологии и челюстно - лицевой хирургии (биотехнологические продукты: трансплантат биоинженерного искусственного зуба из аутологичных стволовых клеток и костного матрикса на имплантируемом штифте, протез биоинженерной аутологичной костной ткани челюсти). Ø Интрамедулярная имплантация регенераторного матрикса при травме спинного мозга. Ø Тяжелая травма головного мозга (ушибы мозга и их последствия).

Научные направления Ø Травма спинного мозга (частичная и с полным перерывом). Ø Острые ишемические и геморрагические инсульты и их последствия. Ø Дисциркуляторные энцефалопатии 3 стадии и сосудистые деменции (слабоумие). Ø Токсические поражения мозга (токсическая энцефалопатия) с психоорганическим синдромом. Ø Хронические вегетативные состояния (посттравматические, постгипоксические). Ø Дегенеративные заболевания нервной системы (болезнь Паркинсона, хорея Геттингтона). Ø Последствия перенесенных нейроинфекции (клещевого энцефалита, цитомегаловируса, герпетические и т. д. ). Ø Рассеянный склероз и рассеянный энцефаломиелит.

Научные направления Ø Протезирование вторично-сморщенной почки при хронической почечной недостаточности 2 -3 стадии (моделирование искусственной ткани почки биодеградируемым матриксом "Сферогель" и аутологичными мезенхимальными стволовыми клетками и эндотелиоцитами). Ø Лечение детского церебрального паралича с применением трансфузий аутологичных клеток предшественников костного мозга. Ø Моделирование и имплантация искусственной клеточно-биополимерной нейроэндопротезной системы для пластики дефектов и повреждений головного и спинного мозга при реконструктивных операциях.

ТКАНЕВАЯ ИНЖЕНЕРИЯ Ø Значительный прорыв в тканевой инженерии за последние 5 лет был достигнут благодаря расширению возможностей управления регенерацией и ангиогенезом ткани, малоинвазивным биоконструированием формы тканевых протезов из новейших биополимерных материалов четвертого поколения, являющихся питательной средой для стволовых клеток. Ø Биополимерам 4 -го поколения могут быть заданы определенные свойства и время биодеградации, к ним могут быть добавлены ростовые и питательные факторы, заданы свойства объема трехмерной структуры. Ø Применение аутологичных эндотелиоцитов и факторов роста сосудов и новых биополимерных каркасов открыл не ограниченные возможности васкуляризации "восстановленной" ткани.

ТКАНЕВАЯ ИНЖЕНЕРИЯ Ø Сегодня разработаны биодеградирующие материалы не только твердых форм, но и жидкие и гелевые консистенции полимеров. Тканевое окружение является определяющим в дифференциации стволовых клеток. Ø Нервные стволовые клетки (neural stem cell), попадая в организме в соответствующее окружение, специализируются в нейроны и формируют синапсы нужного типа. Ø Angelo L. Vesconi из Итальянского неврологического института в Милане доказал, что нервные стволовые клетки в костном мозгу превращались в клетки крови.

ТКАНЕВАЯ ИНЖЕНЕРИЯ Ø Возможность применения аутологичных гемопоэтических стволовых (СD 34+) клеток и транспортных иммуннолипосомальных наноконтейнеров с противоопухолевыми химиопрепаратами для терапии глиальных опухолей мозга, а также разработать претаргетинг целенаводяших бинарных наноиммунолипосомальных систем для диагностики и лечения опухолей головного и спинного мозга. Ø Новые биоинженерные технологии, трансплантация гемопоэтических стволовых клеток, так и на биополимерные конструкции - матриксы для стволовых клеток "Сферогель", позволяющие формировать в поврежденном мозге "искусственную нервную ткань".

РЕГЕНЕРАТИВНАЯ МЕДИЦИНА Ø Решение проблем доставки препаратов в регенеративной медицине. Наночастицы позволят врачам доставлять лекарство точно к месту болезни, увеличивая эффективность и минимизируя побочные эффекты. Ø Наночастицы также могут стимулировать врожденные механизмы регенерации. Основное внимание здесь сосредоточено на искусственной активации и управлении взрослыми стволовыми клетками. Ø Одним из направлений быстрого внедрения достижений медицинских нанотехнологий является интеграция их с новыми клеточными технологиями.

РЕГЕНЕРАТИВНАЯ МЕДИЦИНА Ø Дальнейшее развитие существующих стратегий клеточной медицины практически невозможно без дальнейшего привлечения нанотехнологий Ø Заместительная стратегия клеточной медицины (восстановление анатомической структуры поврежденной ткани органа) также планирует свое развитие с использованием нанотехнологических подходов молекулярной стыков атомарной сварки, осаждения биологических молекул из газовой среды, создание нанороботов и т. д. Ø Индукционная стратегия клеточной медицины (активация процессов местной регенерации) также будет развиваться с использованием нанозондов и наноструктур

Нанотехнологии в практике Ø Сегодня для врачей и фармакологов очевидна аксиома, что лекарства, упакованные в липосомы, становятся более эффективными и безопасными, точно попадают к органам- мишеням и позволяют снизить дозу препаратов. Применение наноконтейнеров в медицине открывает перед ней новые возможности и новые перспективы манипуляций с минидозами препаратов. Ø Зачем медицине нанотехнологии? "Поскольку основной объект воздействия современной медицины - это клетка, а зачастую - макромолекулы, - то и инструменты для их починки должны быть того же порядка, что и объект, то есть нанометрового диапазона".

ЛЕКАРСТВЕННЫЕ НАНОКОНТЕЙНЕРЫ Ø Лекарственные нанопрепараты. Ø Лекарства, молекулы которых упакованы в наноконтейнеры - например, липосомы. В таком "упакованном" виде они поступают в организм, достигают органов и клеток-мишеней, высвобождают лекарство и распадаются на безопасные части, которые организм покидают. Ø В липосомном виде увеличивается растворимость многих лекарственных веществ, что крайне важно для их действия. Уменьшается токсичность, поскольку действующее вещество защищено липосомной оболочкой. Ø Поэтому лекарство действует только тогда, когда достигает клетки-мишени, никак не раньше, и по пути не деградирует, а доходит в активной форме.

ЛЕКАРСТВЕННЫЕ НАНОПРЕПАРАТЫ "КОНТЕЙНЕРЫ Ø Все это позволяет снизить эффективную дозу лекарства, что особенно существенно, например, для онкологических больных, получающих химиотерапию. Ø В основе прицельной доставки нанопрепаратов к мишеням лежат два основных механизма: Ø Они обладают свойством пассивного нацеливания. В районе воспаления в капиллярах расширяются поры, и липосомы проходят как раз через эти поры, то есть, попадают именно туда, куда нужно. Ø Но можно организовать еще и активный транспорт, присоединяя к наночастице "молекулярный адрес" к рецепторам на мембранах клеток-мишеней. .
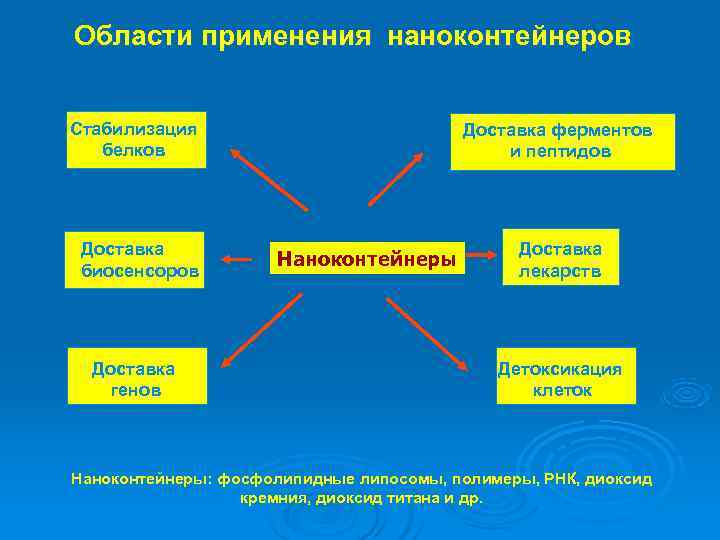
Области применения наноконтейнеров Стабилизация Доставка ферментов белков и пептидов Доставка Наноконтейнеры биосенсоров лекарств Доставка Детоксикация генов клеток Наноконтейнеры: фосфолипидные липосомы, полимеры, РНК, диоксид кремния, диоксид титана и др.
1 ПЦР лаборатория и генодиагностика интерны.ppt
- Количество слайдов: 85

