Генные мутации.ppt
- Количество слайдов: 11
 Генные мутации
Генные мутации
 Генные мутации ДНК является носителем наследственной информации. В основе морфологических и функциональных изменений лежат изменения генетические. Наследственная информация, заключенная в нуклеотидной последовательности ДНК, сохраняется неизменной благодаря действию сложных метаболических процессов, механизмов, обеспечивающих процесс репликации. Ошибки на любом этапе этих процессов приводят к изменению наследственного материала – мутациям. Генные мутации связаны с изменением главного носителя наследственной информации – ДНК, т. е. изменения в нуклеотидной последовательности.
Генные мутации ДНК является носителем наследственной информации. В основе морфологических и функциональных изменений лежат изменения генетические. Наследственная информация, заключенная в нуклеотидной последовательности ДНК, сохраняется неизменной благодаря действию сложных метаболических процессов, механизмов, обеспечивающих процесс репликации. Ошибки на любом этапе этих процессов приводят к изменению наследственного материала – мутациям. Генные мутации связаны с изменением главного носителя наследственной информации – ДНК, т. е. изменения в нуклеотидной последовательности.
 Генные мутации можно разделить на два больших класса: 1. Замена оснований, составляют более 20 % спонтанных мутаций. Замены могут быть двух существенно различных типов: транзиции – замена одного пурина на другой или одного пиримидина на другой. Возможны 4 типа транзиций А Г; Т Ц. В результате происходит взаимозамена пар: АТ которая не нарушает, не изменяет ориентации; ГЦ, ТА ЦГ, - трансверсии – замена пурина на пиримидин и наоборот. Это приводит к замене пар нуклеотидов АТ ЦГ, АТ ТА, ГЦ ЦГ, ГЦ ТА, т. е. такая замена пар изменяет ориентацию. Механизм возникновения трансверсии менее понятен.
Генные мутации можно разделить на два больших класса: 1. Замена оснований, составляют более 20 % спонтанных мутаций. Замены могут быть двух существенно различных типов: транзиции – замена одного пурина на другой или одного пиримидина на другой. Возможны 4 типа транзиций А Г; Т Ц. В результате происходит взаимозамена пар: АТ которая не нарушает, не изменяет ориентации; ГЦ, ТА ЦГ, - трансверсии – замена пурина на пиримидин и наоборот. Это приводит к замене пар нуклеотидов АТ ЦГ, АТ ТА, ГЦ ЦГ, ГЦ ТА, т. е. такая замена пар изменяет ориентацию. Механизм возникновения трансверсии менее понятен.
 Генные мутации В структурных генах большинство замен оснований приводит к возникновению мутаций с изменением смысла (mis sens), при которых одна аминокислота заменяется другой. Поскольку код вырожден, мутация в кодоне не всегда приводит к замене одной аминокислоты на другую. В результате миссенс мутаций образуется либо менее активный фермент, либо меньшее количество нормального фермента.
Генные мутации В структурных генах большинство замен оснований приводит к возникновению мутаций с изменением смысла (mis sens), при которых одна аминокислота заменяется другой. Поскольку код вырожден, мутация в кодоне не всегда приводит к замене одной аминокислоты на другую. В результате миссенс мутаций образуется либо менее активный фермент, либо меньшее количество нормального фермента.
 Генные мутации Замена оснований может превратить кодон в какой либо из трех нонсес триплетов, которые не кодируют никаких аминокислот (нонсес мутации) – это УАГ (amber), УАА (ochre), УГА (opal), которые не транслируются и приводят к преждевременной терминации растущей полипептидной цепи. Так, если в кодоне УГГ, кодирующий триптофан, происходит транзиция во втором положении Г А, то кодон УГГ изменяется и образуется amber л триплет УАГ. Нонсес мутации дают более выраженный эффект, чем мутации и поэтому легче выявляются. миссенс Терминация цепи приводит к нарушению функции фермента, нонсес мутации проявляются обычно как аморфы (функция нормального гена полностью утрачена – ген w (white в серии локуса white).
Генные мутации Замена оснований может превратить кодон в какой либо из трех нонсес триплетов, которые не кодируют никаких аминокислот (нонсес мутации) – это УАГ (amber), УАА (ochre), УГА (opal), которые не транслируются и приводят к преждевременной терминации растущей полипептидной цепи. Так, если в кодоне УГГ, кодирующий триптофан, происходит транзиция во втором положении Г А, то кодон УГГ изменяется и образуется amber л триплет УАГ. Нонсес мутации дают более выраженный эффект, чем мутации и поэтому легче выявляются. миссенс Терминация цепи приводит к нарушению функции фермента, нонсес мутации проявляются обычно как аморфы (функция нормального гена полностью утрачена – ген w (white в серии локуса white).
 Генные мутации 2. Делеции или вставки одного или нескольких нуклеотидов: мутации со сдвигом рамки считывания. Делеция одного или нескольких триплетов влечет за собой утрату одной или нескольких аминокислот из соответствующего полипептида. Фенотипическое проявление зависит от значения утраченных аминокислот для функционирования данного белка. Если выпадает одно или два основания в триплете, то все аминокислоты в цепи, начиная с «усеченного» триплета, оказались бы «ошибочными» . Такой «сдвиг рамки» (frameshift) получается при любой делеции или вставке оснований за исключением тех случаев, когда их число кратно трем. Мутации со сдвигом рамки считывания возникают как спонтанно, так и под влиянием мутагенов. Инсерции и делеции вызывают изменение всех последующих за мутантным сай том триплетов и появление терминирующих кодонов (UАА, UАG и UGA), которые прерывают трансляцию. Поэтому последствия таких мутаций довольно серьезны.
Генные мутации 2. Делеции или вставки одного или нескольких нуклеотидов: мутации со сдвигом рамки считывания. Делеция одного или нескольких триплетов влечет за собой утрату одной или нескольких аминокислот из соответствующего полипептида. Фенотипическое проявление зависит от значения утраченных аминокислот для функционирования данного белка. Если выпадает одно или два основания в триплете, то все аминокислоты в цепи, начиная с «усеченного» триплета, оказались бы «ошибочными» . Такой «сдвиг рамки» (frameshift) получается при любой делеции или вставке оснований за исключением тех случаев, когда их число кратно трем. Мутации со сдвигом рамки считывания возникают как спонтанно, так и под влиянием мутагенов. Инсерции и делеции вызывают изменение всех последующих за мутантным сай том триплетов и появление терминирующих кодонов (UАА, UАG и UGA), которые прерывают трансляцию. Поэтому последствия таких мутаций довольно серьезны.
 Генные мутации 1. Из за вырожденности генетического кода замена нуклеотида не всегда приводит к замене аминокислоты. 2. Даже при замене аминокислоты она может быть локализована в области, нейтральной для функции белка. 3. Если аминокислотная замена происходит в критической для функции белка области, то она не обязательно влияет на его функции, поскольку может иметь свойства, сходные с соответствующей аминокислотой немутантного гена, компенсирующие замену. В результате, однонуклеотидные замены иногда не влияют на функции белка или только снижают его функциональную активность. По мере роста числа секвенированных генов проясняются и представления о вкладе мутаций в развитии заболевания.
Генные мутации 1. Из за вырожденности генетического кода замена нуклеотида не всегда приводит к замене аминокислоты. 2. Даже при замене аминокислоты она может быть локализована в области, нейтральной для функции белка. 3. Если аминокислотная замена происходит в критической для функции белка области, то она не обязательно влияет на его функции, поскольку может иметь свойства, сходные с соответствующей аминокислотой немутантного гена, компенсирующие замену. В результате, однонуклеотидные замены иногда не влияют на функции белка или только снижают его функциональную активность. По мере роста числа секвенированных генов проясняются и представления о вкладе мутаций в развитии заболевания.
 Генные мутации. Примеры мутаций у человека О различных превращениях нуклеотидов и мутациях сдвига рамки стало известно, в основном, благодаря анализу аминокислотных последовательностей в молекулах разнообразных белков. Это разнообразие белков у представителей каждого вида возникло в ходе эволюции и отражает изменения генетического кода, обусловленные замещением, инсерциями или делециями нуклеотидов в генах. Методы быстрого и точного секвенирования ДНК значительно расширили наши представления о структуре генов.
Генные мутации. Примеры мутаций у человека О различных превращениях нуклеотидов и мутациях сдвига рамки стало известно, в основном, благодаря анализу аминокислотных последовательностей в молекулах разнообразных белков. Это разнообразие белков у представителей каждого вида возникло в ходе эволюции и отражает изменения генетического кода, обусловленные замещением, инсерциями или делециями нуклеотидов в генах. Методы быстрого и точного секвенирования ДНК значительно расширили наши представления о структуре генов.
 Мышечная дистрофия Характерна прогрессирующая дегенерация мышечной ткани, или миопатия, которая приводит к относительно ранней смерти больных рецессивное Х сцепленное заболевание, — больные мужчины умирают (1 на 3500), не достигнув репродуктивного возраста, а женщины поражаются значительно реже. Миодистрофия Дюшенна (DMD) встречается чаще другой аллельной формы миодистрофии Беккера (ВМD). Мутантный ген дистрофина содержит более 2 миллионов пар нуклеотидов. У здоровых людей транскрипция этой последовательности на м. РНК длиной 14 т. п. н. и последующая трансляция приводит к образованию белка дистрофина, содержащего 3685 аминокислот. Этот белок часто обнаруживается и у больных с более или менее выраженными симптомами ВМD, но крайне редко — у больных DMD. Поэтому предположили, что большинство мутаций, вызывающих ВМD, не изменяет рамки считывания. Однако, мутации, определяющие DMD, приводят к изменению рамки, появлению стоп-кодона и трансляции дефектного дистрофина. Это предположение согласуется различной тяжестью разных форм миодистрофии.
Мышечная дистрофия Характерна прогрессирующая дегенерация мышечной ткани, или миопатия, которая приводит к относительно ранней смерти больных рецессивное Х сцепленное заболевание, — больные мужчины умирают (1 на 3500), не достигнув репродуктивного возраста, а женщины поражаются значительно реже. Миодистрофия Дюшенна (DMD) встречается чаще другой аллельной формы миодистрофии Беккера (ВМD). Мутантный ген дистрофина содержит более 2 миллионов пар нуклеотидов. У здоровых людей транскрипция этой последовательности на м. РНК длиной 14 т. п. н. и последующая трансляция приводит к образованию белка дистрофина, содержащего 3685 аминокислот. Этот белок часто обнаруживается и у больных с более или менее выраженными симптомами ВМD, но крайне редко — у больных DMD. Поэтому предположили, что большинство мутаций, вызывающих ВМD, не изменяет рамки считывания. Однако, мутации, определяющие DMD, приводят к изменению рамки, появлению стоп-кодона и трансляции дефектного дистрофина. Это предположение согласуется различной тяжестью разных форм миодистрофии.
 Тринуклеотидные повторы В мутантных генах происходит экспансия (распространение) тринуклеотидных повторов, которые представлены в генах здоровых людей немногими копиями (обычно от нескольких до 15). Экспансия таких повторов была обнаружена и в генах, ответственных за развитие двух аутосомно доминантных заболеваний: — миотонической дистрофии и хореи Гентингтона, — Х сцепленного доминантного заболевания синдрома ломкой Х хромосомы. Миотоническая дистрофия от слабой миопатии до катаракты, мышечной дистрофии, умственной отсталости, вплоть до ранней смерти. Тяжесть этих симптомов коррелирует с длиной повторяющейся тринуклеотидной последовательности Эти повторы выявлены в генах здоровых людей, однако в гораздо меньшем количестве.
Тринуклеотидные повторы В мутантных генах происходит экспансия (распространение) тринуклеотидных повторов, которые представлены в генах здоровых людей немногими копиями (обычно от нескольких до 15). Экспансия таких повторов была обнаружена и в генах, ответственных за развитие двух аутосомно доминантных заболеваний: — миотонической дистрофии и хореи Гентингтона, — Х сцепленного доминантного заболевания синдрома ломкой Х хромосомы. Миотоническая дистрофия от слабой миопатии до катаракты, мышечной дистрофии, умственной отсталости, вплоть до ранней смерти. Тяжесть этих симптомов коррелирует с длиной повторяющейся тринуклеотидной последовательности Эти повторы выявлены в генах здоровых людей, однако в гораздо меньшем количестве.
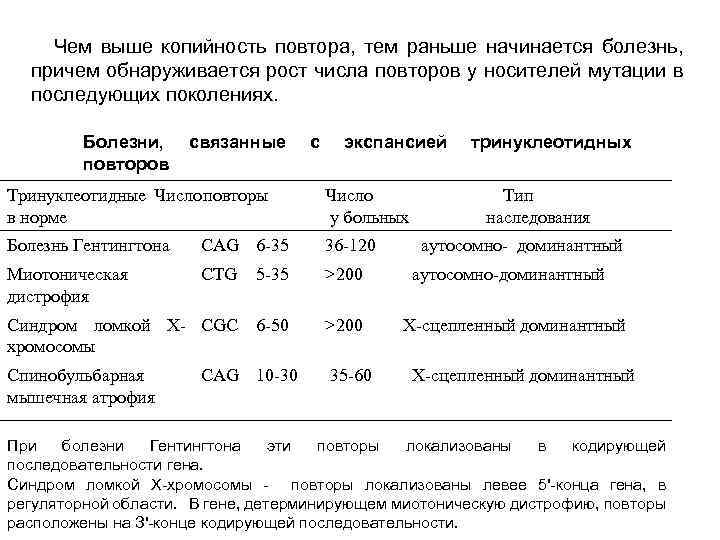 Чем выше копийность повтора, тем раньше начинается болезнь, причем обнаруживается рост числа повторов у носителей мутации в последующих поколениях. Болезни, повторов связанные с экспансией Тринуклеотидные Число повторы в норме Число у больных Болезнь Гентингтона САG 6 -35 36 -120 Миотоническая дистрофия СТG 5 -35 >200 Синдром ломкой Х- СGС 6 -50 хромосомы >200 Спинобульбарная мышечная атрофия 35 -60 САG 10 -30 тринуклеотидных Тип наследования аутосомно- доминантный аутосомно-доминантный Х-сцепленный доминантный При болезни Гентингтона эти повторы локализованы в кодирующей последовательности гена. Синдром ломкой Х хромосомы повторы локализованы левее 5' конца гена, в регуляторной области. В гене, детерминирующем миотоническую дистрофию, повторы расположены на З' конце кодирующей последовательности.
Чем выше копийность повтора, тем раньше начинается болезнь, причем обнаруживается рост числа повторов у носителей мутации в последующих поколениях. Болезни, повторов связанные с экспансией Тринуклеотидные Число повторы в норме Число у больных Болезнь Гентингтона САG 6 -35 36 -120 Миотоническая дистрофия СТG 5 -35 >200 Синдром ломкой Х- СGС 6 -50 хромосомы >200 Спинобульбарная мышечная атрофия 35 -60 САG 10 -30 тринуклеотидных Тип наследования аутосомно- доминантный аутосомно-доминантный Х-сцепленный доминантный При болезни Гентингтона эти повторы локализованы в кодирующей последовательности гена. Синдром ломкой Х хромосомы повторы локализованы левее 5' конца гена, в регуляторной области. В гене, детерминирующем миотоническую дистрофию, повторы расположены на З' конце кодирующей последовательности.


