Нарушения обмена веществ. Генные болезни.ppt
- Количество слайдов: 58

Генные болезни. В основе лежит генетически детерминированные нарушения ферментов, наступившие в результате генных мутаций. Или ферментопатии Или «болезни накопления» Или тезаурисмозы

Дефицит белка-фермента ↓ Нарушение определенной биохимической реакции ↓ Избыток субстрата ↓ Накопление субстрата в тканях и выведение его из организма. ↓ Клиническая симптоматика, обусловленная накоплением субстрата или вовлечением его в альтернативный обмен с образованием токсических продуктов.

Классификация По типу передачи наследственного признака: аутосомно-рецессивные сцепленные с Х-хромосомой. 2. Органный и системный принципы (наследственные болезни нервно-мышечные, печеночные, лизосомальные, эндокринные и др. ) 3. Этиологический принцип: с выясненным биохимическим дефектом с невыясненным биохимическим дефектом. 4. По преимущественному нарушению вида обмена: нарушения обмена углеводов нарушения обмена аминокислот нарушения обмена липидов нарушения обмена витаминов нарушения обмена гормонов нарушения обмена пуринов и пиримидинов 1. -

Общие признаки, позволяющие заподозрить наследственное заболевание Задержка умственного развития Атетозы, атаксия Судорожный синдром Повторные коматозные состояния Рецидивы кетоацидоза Специфический запах мочи и тела Миопатии Аномалии скелета Изменения волос и кожи Катаракта Увеличение печени и селезенки Синдром мальабсорбции Необъяснимая смерть сибсов

Наследственные (первичные) аминоацидопатии Требуют специального лабораторного обследования дети с: Сочетанием умственной отсталости и патологии зрения Сочетанием умственной отсталости и судорожного синдрома Наличием изменения запаха или цвета мочи Поражением печени и ЦНС Сочетанием умственной отсталости и поражением кожи

Классификация Наследственные нарушения обмена аминокислот, сопровождающиеся повышением их концентрации в крови и моче (ФКУ, триптофанурия, гистидинемия, гиперлизинемия) Наследственные нарушения обмена аминокислот, сопровождающиеся повышением их выделения с мочой без изменения содержания в крови (гомоцистинурия). В этой группе не нарастает концентрация аминокислот в крови, т. к. блокирована реабсорбция в почках а/к, метаболизм которых нарушен. Наследственные нарушения системы транспорта а/к (цистинурия, гиперлизинурия). Развитие этих болезней обусловлено снижением реабсорбции определенных а/к в почках и кишечнике. Вторичные гипераминоацидурии, возникающие, чаще всего, как результат вторичных тубулярных нарушений.
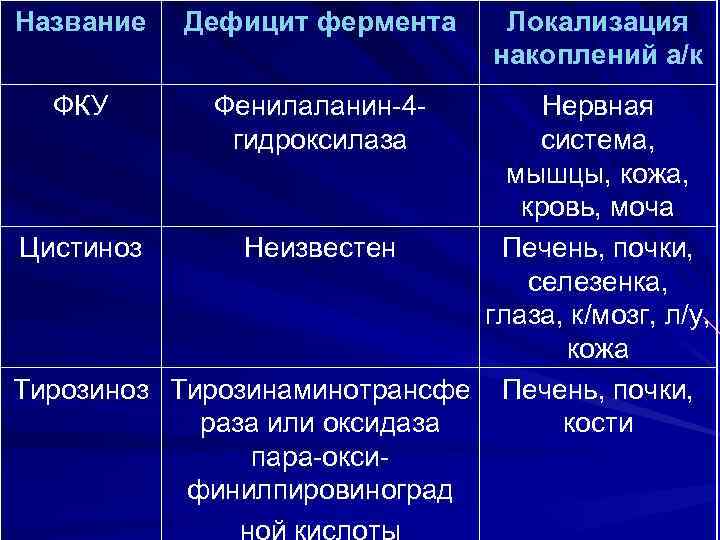
Название Дефицит фермента ФКУ Фенилаланин-4 гидроксилаза Локализация накоплений а/к Нервная система, мышцы, кожа, кровь, моча Цистиноз Неизвестен Печень, почки, селезенка, глаза, к/мозг, л/у, кожа Тирозиноз Тирозинаминотрансфе Печень, почки, раза или оксидаза кости пара-оксифинилпировиноград ной кислоты

Фенилаланин А ↓ фенилпируват ↓ ↓ фенил- глутамин лактат А – фенилкетонурия В – тирозиноз С - алкаптонурия Тирозин ДОФА (диоксифенилаланин) ↓D ↓Е тироксин меланин ↓ оксифенилпируват ↓ В гомогентизиновая кислота ↓ С малеилацетилацетат ↓ фумарат + ацетилацетат D - кретинизм Е - альбинизм

Фенилкетонурия Дефект: фенилаланингидроксилаза. Наследование: аутсомно-рецессивное Частота: 1 : 8 – 10 тыс. Не болеют евреи ашкенази и афроамериканцы. ♀ : ♂ = 1: 1. Впервые описана в 1934 г Феллингом (в моче обнаружена фенилпировиноградная кислота, котороя давала зеленое окрашивание при взаимодействии с Fe. Cl 3.

Клиника фенилкетонурии. С рождения трудности вскармливания, рвота, часто сочетается с пилоростенозом. Повышенная возбудимость и двигательная гиперактивность Запах плесени от мочи и пота До 3 – 5 мес нет ЗПМР. С 3 – 6 мес – вялость, отсутствие интереса к окружающим, раздражительность, беспокойство, повторные рвоты, экзематозные изменения кожи, судороги. Формируется ЗПМР. Отставание в развитии связано с нарушением формирования миелиновой оболочки вокруг аксонов в ЦНС. В дальнейшем: физическое развитие снижено, светлые (деколорированные) волосы, голубые глаза, «мышиный запах» мочи (фенилацетат), эпилептические припадки, экзема, дерматит.

Биохимические нарушения Фенилаланингидроксилаза имеется в печени, почках и поджелудочное железе. Накопление фенилаланина, выведение с мочой фенилпировиноградной кислоты и молочной кислоты. Снижение тирозина в плазме крови. А также торможение транспорта других а/к и нарушения синтеза белка и нейромедиаторов в ЦНС.

Повышения уровня фенилаланина в крови >4 мг/дл – не всегда ФКУ. Встречается при транзиторной задержке развития системы окисления тирозина у недоношенных детей и детей с низкой массой тела при рождении. Если к 3 нед жизни уровень фенилаланина >15 мл/дл не зависимо от наличия его метаболитов в моче, прибегают к ограничению фенилаланина в пище.

Диагностика Скрининг новорожденных – на 4 - 5 д. ж. (у недоношенных на 7 -й) – определение уровня фенилаланина в крови. Норма до 2. 2 мг/дл. Если 20 – 30 мг/дл – диагноз ФКУ. Если 4 – 5 мг/дл, повторные исследования крови, осмотр в МГЦ + постановка на учет (не диагноз). В возрасте старше 4 - 6 недель продукт распада фенилаланина можно выявить в моче больного ребенка. В это время проводят мочевой скрининг-тест на фенилкетонурию, причем детям из семей, где имеется больной фенилкетонурией, его следует регулярно повторять в течение первого года жизни. Реакция Феллинга – качественное определение фенилпировиноградной кислоты в моче (2 -3 мл мочи + 1 мл 10% Fe. Cl 3 + несколько капель 5% НCL зеленое окрашивание). Тест не строго специфичен, м/б (+) при 17 вариантах аминоацидопатий. Молекулярно-генетическое пренатальное обследование – исследование лимфоцитов, амниоцитов, клеток хориона). Для подтверждение диагноза проводится определение генотипа ребенка (12 хромосома).

Лечение Диета с ограничением фенилаланина при концентрации фенилаланина >20 мг/дл. Длительность диеты от 7 до 10 лет. Уровень фенилаланина не должен опускаться ниже 3 мг/дл, чтобы дефицит а/к не вызывал задержку роста. Замена животного белка на искусственные а/к композиции без фенилаланина. Используемые молочные смеси: «Афенилак» для младших детей; «Тетрафен» , «Фенил-фри» , «Лофенак» для старших.

Последствия Минимальные неблагоприятные последствия (сохранность интеллекта) при назначении диеты с 3 -х недельного возраста. С 8 -ми мес возраста последствия необратимы. Женщины, леченные диетой вновь прибегают к ней перед зачатием. Допустимая норма фенилаланина 4060 мг/дл. При геперфенилаланинемии у беременной происходит интоксикация плода фенилаланином матери – тяжелые органические поражения ЦНС.

Алкаптонурия (Гомогентизинурия). Дефект: оксидаза гомогентизиновой кислоты. Наследование: аутосомно-рецессивное. Проявления практически с рождения: моча ребенка окрашивается в черный цвет за счет окисления гомогентизиновой кислоты на воздухе и превращения ее в меланиноподобное соединение. Развивается охраноз – накопление гомогентизиновой кислоты и ее полимеров в хрящевой ткани – серо-голубое окрашивание ушного и носового хрящей, окрашивание одежды в местах наибольшей потливости кожи (подмышечные впадины). Сероватый оттенок кожи и глаз (особенно выражена пигментация скул, подмышечных впадин и гениталий. Артропатии к 30 – 40 годам, чаще поражаются крупные суставы, позвоночник.

Биохимические нарушения. Накопление гомогентизиновой кислоты вследствие дефекта ее оксидазы. Нет образования малеилатацетата и продуктов его распада – фумарата и ацетата, участвующих в цикле трикарбоновых кислот. Избыток гомогентизиновой кислоты хорошо секретируется в просвет канальцев почек, мало накапливается в плазме. Нет избытка тирозина т. к. он используется в синтезе белка и нейромедиаторов.

Диагностика § § Скрининг – визуальный осмотр мочи (черного цвета). Но, такое окрашивание могут давать желчь, порфирины, миоглобин и гемоглобин. Качественные реакции: добавление к моче щелочи вызывает ее потеменение, реакция Бенедикта – коричневое окрашивание мочи с выпадением оранжевого осадка Реакция с хлоридом железа приводит к появлению пурпурно-черной окраски. Для выявления гомогентизиновой кислоты в плавзме крови проводят тонкослойную хроматографию или ферментативное определение. Рентгенологические изменения у взрослых: в поясничном отделе позвоночника межпозвонковые диски дегенерированы, плотные с отложением солей кальция, межпозвонковые пространства сужены.

Лечение Большие дозы витамина С. Ранняя диетотерапия с ограничением поступления фенилаланина и тирозина до 200 – 500 мг/день. Прогноз для жизни благоприятный.

Альбинизм Частота: 1: 5 000 – 1: 25 000 Наиболее распространенная форма: глазо-кожный тирозиназонегативный альбинизм, имеющий аутосомно-рецессивный тип наследования. Клинически: отсутствие меланина в клетках кожи (молочно-белый цвет), очень светлые волосы, светло-серая или светло-голубая радужка, красный зрачок, повышенная чувствительность к УФоблучению (вызывает воспалительные заболевания кожи). Нет пигментных пятен на коже, снижена острота зрения. Диагностика – осмотр ребенка.

Наследственная тирозинемия Тип наследования аутосомно-рецессивный Частота: 1: 100 тыс. Дефект: в зависимости от типа тирозинемии: - I тип (гепаторенальная тирозинемия) – недостаточность фумарилацетоацетазы. -II тип недостаточность тирозин-аминотрансферазы. -III тип – недостаточность 4 -гидроксифенилпируват гидроксилазы. Возможна пренатальная диагностика – определение сукцинил ацетона в амниотической жидкости или активности ферментов.

Клиника тирозинемии - - - Острая форма: Протекает злокачественно Первые симптомы в первые 6 мес жизни 90% летальных исходов от печеночной недостаточности Гипотрофия, иктеричность кожи и склер, гепатомегалия, кровоточивость различной выраженности Рвота, особый запах (метиониновый, напоминает запах капусты), диарея Асцит, лихорадка, гипогликемия, дыхательные нарушения. - - - Поздняя форма: Медленно прогрессирующая гипотрофия Выраженный узелковый цирроз печени Синдром Фанкони Склонность к гипогликемии, лейкопении, тромбоцитопении, образованию гематом.

Лабораторная диагностика Положительная реакция Бенедикта (на метаболиты метионина) Положительные тесты с хлоридом железа и нитрозонафтоном В анализах мочи – тирозинурия, преимущественно за счет гидроксифенилпировиноградной кислоты.

I тип– недостаточность фумарилацетоацетазы. Клинические проявления в период новорожденности – гепаторенальный синдром, поражение нервной системы. Отставание в физическом и нервно-психическом развитии, чередование общего возбуждения и сомнолентности, периферические невропатии и параличи, слабость мышц, кровоточивость, гипогликемия, иктеричность кожи и склер, развитие цирроза печени, синдром Фанкони. Лабораторно: тирозинемия, тирозинурия, аминоацидурия, метионинемия и метионинурия, недостаточность фермента определяется в биоптатах печени, увеличение сукцинил-ацетона в крови, гипогликемия, гипофосфатемия,

II тип недостаточность тирозинаминотрансферазы. Клинические проявления в ранне возрасте: задержка умственного и физического развития, изъязвления роговицы, кератоз ладоней и стоп. Лабораторно: недостаточность фермента в биоптатах печени, тирозинемия, тирозинурия, аминоацидурия, метионинемия и метионинурия

III тип (хауксинурия)– недостаточность 4 гидроксифенилпируват гидроксилазы. Клинически: отставание в развитии, эпизоды атаксии, метаболический ацидоз. Лабораторно: повышена экскреция хауксина, тирозина, 4 -гидроксифенилпирувата, 4 гидроксифениллактата, анизоцитоз, сфероцитоз, тнедостаточность фермента в биоптатах печени.

Гистидинемия Дефект: гистидаза =>повышение уровня гистидина в плазме крови Наследование: аутосомно-рецессивное Частота: 1: 10 тыс – 1: 110 тыс. Возможна пренатальная диагностика. Подтверждение диагноза – проведение нагрузочной пробы. Диетотерапия? Т. к. нет данных о клиническом улучшении элиминационной диеты, а также неизвестны последствия дефицита гистидина.

Клиника Вариабельность клинических проявлений Диагностика к концу первого года жизни и позже Самое типичное нарушение: дефект речи, умственная отсталость у 2/3 детей, нарушение слуха. Частые ОРВИ, низкорослость, судороги и изменения ЭЭГ Могут быть только поведенческие нарушения: эмоциональная лабильность, трудности в учебе.

Диагностика Проба с хлоридом железа дает зеленый цвет за счет имидаралпировиноградной кислоте (при уровне гистидинемии более 0. 5 м. М), но не является диагностическим в периоде новорожденности. У новорожденных определяют уровень гистидинурии. В норме: 0. 4 – 1. 0 мг/дл, при гистидинемии 2 – 27 мг/дл.

Лечение Диета с низким содержание фенилаланина и тирозина. Смеси аминокислот, белковые гидролизаты: «Альбумайд» , «Цимогран» , безбелковый хлеб.

Гомоцистинурия Наследование: аутосомно-рецессивное Возможна пренатальная диагностика Частота: 1: 50 тыс – 1: 250 тыс Дефект: цистатионин-β-синтетаза Диагностика: определение уровня гомоцистеина в моче и плазме крови, снижение активности фермента. 2 формы: пиридоксинзависимая и пиридоксинрезистентная. Противопоказаны плановые операции, ангиография в связи с риском в/сосудистой коагуляции.

Клиника Беременность и период новорожденности без особенностей. До 2 -х лет симптомы могут отсутствовать. Поражение: глаз, скелета, сосудов, г/мозга. Эктопия хрусталиков проявляется от 3 до 10 лет, иногда этому предшествует «дрожание» радужек при быстрых движениях головой. Может быть вывих или подвывих хрусталика, миопия, катаракта, глаукома. Остеопороз на втором десятилетии жизни, кифосколиозы, вальгусные искривления голеней, плоскостопие. Высокий рост, длинные конечности, арахнодактилия, деформации грудной клетки. Умственная отсталость в 50%, медленно прогрессирующая ЗПМР, судороги у 10 – 15%. Склонность к тромбоэмболии – частая причина смерти. «Пылающие» скулы, эритематозные высыпания на конечностях, могут быть телеангиэктазии.

Лечение При пиридоксинзависимой форме: пиридоксальфосфат (В 6) в дозе 250 – 500 мгдень + фолиевая кислота 5 мг/день. Большие дозы В 6 оказывают активирующее влияние на цистатионсинтетазу. Пиридоксинрезистентная форма: назначается диета со сниженным содержанием метионина.

Клинический случай Мальчик 1 г 8 мес, от 2 беременности без особенностей, при рождении масса=3450 г, длина=52 см. С рождения абсансы типа «замирания» , «кивков» более 100/сут. ПМР: практически не держит голову, не сидит, не стоит, не говорит. М=9200 г, длина=98 см. Наблюдался с диагшнозом синдром Веста, получал конвулекс, суксилеп, фенобарбитал без эффекта. При осмотре: длинные конечности, арахнодактилия, воронкообразная деформация грудной клетки, миатонический синдром. В моче: повышенное содержание метионина и гомоцистина, снижение цистина и таурина.

Диагноз: гомоцистинурия, метаболическая энцефалопатия с симптоматической эпилепсией, грубая ЗПМР. Лечение: диета с ограничением продуктов, содержащих метионин; витамин В 6 200 мг/сут, фолиевая кислота в возрастной дозе. → количество абсансов 20 – 40 в день. → добавлены аминокислотные препараты, через 2 нед: улучшился сон и аппетит, начал гулить, произносить отдельные слова, зрительное сосредоточение, абсансов до 15/день. Через 4 нед: абсансы 1 – 2 р/день; 5 нед: хорошо удерживает голову; 8 нед: стоит с поддержкой за руки. Через 3 мес: хорошо сидит, держит голову, стоит держась за одну руку, +2 кг, говорит слова, абсансы 1 – 2 р/нед.

Цистинурия Наследование: аутосомно-рецессивное Типично нарушение функции проксимальных отделов почечных канальцев Характерно: повышенная экскреция с мочой цистина, лизина и аргинина; образование мочевых камней Лечение: диета не содержащая метионина, отщелачивающие мочу средства и другая профилактика камнеобразования

Нарушение обмена триптофана Болезнь Хартнапа Аутосомно-рецессивное, связанное с нарушением активного транспорта триптофана в слизистой кишечника и проксимальных отделах канальцев почек. Нарушено всасывание триптофана, лизина, метионина, глицина. Пеллагроподобный дерматит, фотодерматоз, неврологические нарушения (спонтанный нистагм, интенционный тремор, прирамидная симптоматика, мозжечковая атаксия). Повышена экскреция индоловых соединений, генерализованная аминоацидурия, отсутствие в моче триптофана. Лечение: диета с ограничением белка, обогащение фруктами, витамины группы В, предохранение кожи от воздействия солнечных лучей.

Нарушение обмена триптофана Синдром Кнаппа-Комровера. Наследственная пиридоксинзависимая ксануренурия: Повышенная ферментативная активность триптофанпирролазы Наследование: аутосомно-рецессивное Экзема, уртикарная сыпь, бронхиальная астма, психоневрологические нарушения (повышенная возбудимость, судорожный синдром, особенности поведения). Лабораторно: положительный триптофановый тест (повышенная экскреция с мочой кинуреина, кинуреновой, ксантуреновой кислот). Лечение: высокие дозы витамина В 6 (60 – 120 мг/сут).

Лейциноз или болезнь мочи с запахом кленового сиропа. Наследование: аутосомно-рецессивное Частота: 1: 120 тыс – 1: 300 тыс Чаще встречается у франкоязычного населения Канады. Дефицит дегидрогеназы кетокислот с разветвленной цепью, обеспечивающей окислительное декарбоксилирование лейцина, изолейцина и валина. Накопление: α-кетопромежуточных соединений, дефицит нейтральных аминокислот – аланина, глицина, глутамина и др. Важную роль в патогенезе неврологических расстройств играют развивающиеся нарушения функции митохондриальной дыхательной цепи и окислительного фосфорилирования.

Клиника Известны 4 клинических варианта болезни: классический, интермиттирующий, промежуточный и тиаминзависимый. Классический вариант: первые симптомы на 1 -й неделе жизни ребенка: генерализованные судороги, повышенная возбудимость, резкий крик, отказ от пищи, упорная рвота, мышечная гипертония (до опистотонуса). В дальнейшем присоединяются признаки обезвоживания, развивается вялость, угнетение ЦНС (до комы), чередование мышечного гипертонуса и гипотонии, эритематозные высыпания на коже. Нередко смерть от отека г/мозга. Если выживает: резкое отставание в ПМР, мышечная дистония, пирамидные нарушения, судорожный синдром, иммунодефицит, характерен ацидоз с высоким содержанием молочной кислоты в крови, склонность к гипогликемии.

Лабораторно: повышение содержания в крови и моче а/к с разветвленной цепью (лейцин, изолейцин, валин), снижение содержания аланина, глицина. Экскреция с мочой 2 -кетоизовалерьяновой, 2 гидроксиизокапроновой, 2 -гидрокси-3 -метил-nвалериановой, 2 -кетоизокапроновой и других оргпнических кислот. Необычный запах мочи, напоминающий кленовый сироп, пивную закваску, мясной суп, жженый сахар, а также изменение запаха всех секретов за счет фуранового производного – сотолона. Положительный тест мочи с хлоридом железа. Активность дегидрогеназы кетокислот составляет менее 2% от нормы МРТ г/м: признаки диффузного отека мозговой ткани (особенно в острый период), изменение всего белого вещества.

Интермиттирующая форма: Приступообразное течение, обострения провоцируются интеркуррентными заболеваниями, хирургическими вмешательствами, приемом больших количеств белка и др. В межприступный период без симптоматики. Лабораторно: активность дегидрогеназы кетокислот 5 – 20% от нормы. Промежуточная форма: Менее злокачественное течение без приступов. Отставание в ПМР, судороги, мышечная гипотония, ацидоз, может быть характерный запах мочи. Активность дегидрогеназы 3 – 30% от нормы.

Тиаминзависимая форма: По клинике сходна с интермиттирующим или промежуточным вариантом, хотя встречается реже. Манифестация после неонатального периода. Лабораторно: Коэффициент лейцин/аланин составляет 1. 3 – 12. 4, что в 2 – 20 раз выше нормы (0. 1 – 0. 5) Изменения спектра аминокислот и органических кислот в биологических жидкостях Дефицит дегидрогеназы кетокислот в лейкоцитах и фибробластах.

Лечение Первые 3 варианта: малобелковая элиминационная диета – исключение из рациона продуктов, содержащих белки животного происхождения, ограничение растительных белков с учетом минимальной суточной потребности ребенка в лейцине, изолейцине, валине, применение полусинтетических лечебных продуктов на основе гидролизатов белки или смесей а/к. Экстренная терапия: гемосорбция, гемодиализ, заменное переливание крови, перитонеальный диализ. Возможна трансплантация печени – дает возможность расширить пищевой рацион ребенка. Тиаминзависимая форма поддается терапии высокими дозами витамина В 1 (более 100 мг/сут).

Критерии эффективности терапии Основной критерий адекватности лечебного питания – уровень лейцина в крови 100 – 300 мкмоль/л (норма 50 – 160 мкмоль/л) Уровень изолейцина 200 – 400 мкмоль/л (норма 30 – 90) Уровень валина 275 – 450 мкмоль/л (норма 80 – 290). Низкий уровень этих а/к свидетельствует о дефиците белка, что ведет к снижению аппетита, сонливости, энтеропатии, эритематозному дерматиту, задержке физического развития.

Изовалерьяновая ацидурия Синдром с запахом «потных ног» Обусловлена недостаточностью дегидрогеназы изовалерьяновой кислоты Накапливается изовалерил-Со. А, который гидролизуется с образованием изовалерата и выделяется в составе мочи и пота (отсюда характерный запах). Проявления с раннего детского возраста: ацидоз, характерный запах. В дальнейшем отмечается задержка умственного развития.

Лабораторно: Повышение изовалерьяновой кислоты в крови и моче Высокий уровень глицина в моче Снижение уровня дегидрогеназы изовалерьяновой кислоты Лечение: Диета со сниженным содержанием изовалерьяновой кислоты в продуктах питания.

Ферментопатии, обусловленные нарушением синтеза мочевины. Аргининянтарная ацидурия – недостаточность фермента аргининсукциназы, катализирующей образование аргинина и фумарата из аргининянтарной кислоты. Мутантный ген на 7 -й хромосоме. Частота: 1: 60 тыс. 2 клинические формы: неонатальная и подострая (поздняя).

При неонатальной форме: гипераммониемия развивается в течение первых нескольких дней жизни на фоне отказа от пищи, анорексии, рвоты, гепатомегалии, респираторных расстройств, мышечной гипотонии, судорог. После – новорожденные становятся сонливыми, отмечаются ризнаки угнетения ЦНС. Итог: кома и смерть от апноэ и остановки сердца.

Поздняя форма Первые клинические проявления могут возникать в раннем детском возрасте. Характерны неврологические нарушения: судороги, транзиторная атаксия, задержка психомоторного развития (до умственной отсталости). Также отмечаются рвота, гепатомегалия, повышенная ломкость и сухость волос.

Диагностика и лечение Лабораторно: Увеличение концентрации аргининянтарной кислоты в моче, крови и спинномозговой жидкости Умеренное повышение активности печеночных ферментов Повышение аргининянтарной кислоты в амниотической жидкости Лечение: Ограничение белка в пище Применение аргинина

Цитруллинемия Это дефицит синтеза аргининянтарной кислоты вследствие недостаточности аргининсукцинатсинтетазы =>повышение цитруллина в плазме и моче. Встречается редко. Клинически: от бессимптомных форм до тяжелых с летальным исходом. Тяжелая форма (тип 1) – манифестация с рождения, ранняя смерть (до 1 мес). На фоне кормления грудным молоком в первые дни заторможенность, гипотония, судороги, кома. При морфологическом исследовании г/мозга нейрогенная дегенерация и нарушения миелинизации. Тип 2 развивается позднее, активность фермента снижена только в печени. Характерна умственная отсталость и неврологическая симптоматика.

Диагностика Повышение в плазме цитруллина Снижение активности аргининсукцинатсинтетазы в лейкоцитах, фибробластах, клетках печени Гипераммониемия у новорожденных с цитруллинемией обнаруживается не всегда. Клинические симптомы не коррелируют с концентрацией аммиака в плазме крови Пренатальная диагностика – снижение активности аргининсукцинатсинтетазы в амниотической жидкости. Лечение Малобелковая диета (1. 2 – 1. 5 г/кг/сут с добавлением аргинина (0. 4 – 0. 7 г/кг), сначала вводят 1/3 – ½ дозы, затем при хорошей переносимости увеличивают.

Нарушения углеводного обмена Патофизиология синдрома диареи: недостаточность дисахаридазы щеточной каймы эпителия или системы транспорта моносахаридов ↓ сахар накапливается в просвете кишечника ↓ повышение осмолярности кишечного сока, «притягивание» воды, увеличение объема кишечного содержимого ↓ рястяжение кишечника, его спазматическое сокращение ↓ боли в животе, диарея.

Синдромы нарушенного всасывания углеводов 1. 2. 3. 4. 5. 6. 7. 8. 9. Диарея, вздутие живота и боли после приема с пищей определенного сахара. Исчезновение симптомов после исключения определенного сахара из пищи. Кислая реакция кала (р. Н<6). Положительная реакция кала с сульфатом меди (кал развести водой в отношении 1: 2, отцентрифугировать, к 15 кап надосадочной жидкости добавить 1 таб Cu. SO 4 ). Отставание в росте. Раздражительность. Меллитурия. Отсутствие повышения уровня сахара крови после нагрузки определенным сахаром. Отсутствие определенного фермента или транспортной системы в слизистой оболочке кишечника.

Синдром первичного нарушения всасывания глюкозы и галактозы. Встречается редко После первого кормления у ребенка возникает профузная водная диарея, быстро приводящая к дегидратации и ацидозу. Аппетит может быть нормальным. Причина синдрома – врожденное отсутствие транспортной системы кишечника, общей для глюкозы и галактозы. Способность транспортировать глюкозу менее 10% от нормы. Всасывание фруктозы не страдает т. к. опосредованно другой системой переносчика. С возрастом тяжесть клинических симптомов спонтанно уменьшается.

Врожденная недостаточность лактазы (1) Новорожденный получает 50 – 60 г лактозы с молоком. Вскоре после начала кормления при лактазной недостаточности возникают клинические симптомы: стойкая диарея и гмпотрофия. При нагрузке лактозой уровень сахара в крови не повышается. Кал имеет кислый р. Н и содержит лактозу. Дифференциальный диагноз с приобретенной лактазной недостаточностью при инфекционном энтерите, спру, гипотрофии, воспалительных заболеваниях толстого кишечника. В отличие от приобретенного врожденный дефицит проявляется с первых дней жизни.

Врожденная недостаточность лактазы (2) Диагностика: положительная реакция на безлактозную диету. Современный способ диагностики – тест с выдыханием водорода: известно, что количество Н 2, образующегося в толстом кишечнике нечетко коррелирует с Н 2, экскретируемым легкими. В норме вся лактоза расщепляется в верхних отделах тонкого кишечника. При недостаточности лактозы, лактаза достигает толстого кишечника и там под действием микроорганизмов из лактазы вырабатывается Н 2.
Нарушения обмена веществ. Генные болезни.ppt