ген_терапия_2010.ppt
- Количество слайдов: 45
 Генная терапия – лечение, основанное на введении в клетки организма ДНК или РНК Зародышевые клетки (гаметы, зиготы или эмбрион на ранних стадиях развития) Соматические клетки Добавление гена Замена гена Направленное подавление экспрессии гена Направленная элиминация клеток Фармацевтические препараты для генной терапии – клонированный ген, синтезированные РНК или ДНК
Генная терапия – лечение, основанное на введении в клетки организма ДНК или РНК Зародышевые клетки (гаметы, зиготы или эмбрион на ранних стадиях развития) Соматические клетки Добавление гена Замена гена Направленное подавление экспрессии гена Направленная элиминация клеток Фармацевтические препараты для генной терапии – клонированный ген, синтезированные РНК или ДНК
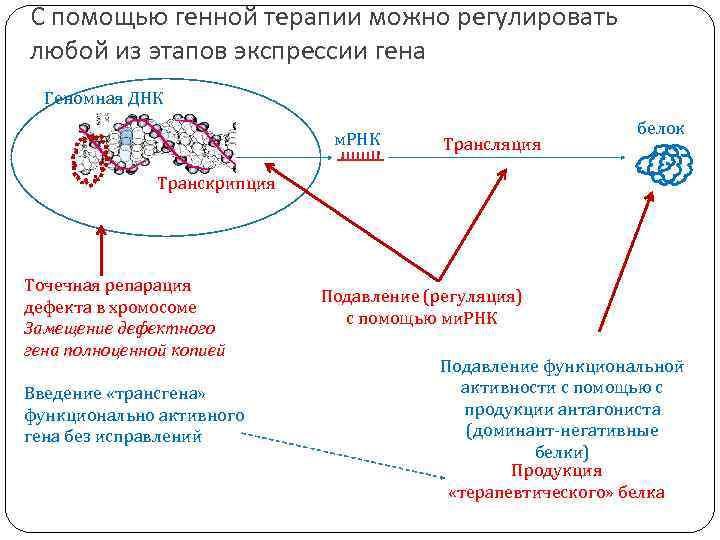 С помощью генной терапии можно регулировать любой из этапов экспрессии гена Геномная ДНК м. РНК Трансляция белок Транскрипция Точечная репарация дефекта в хромосоме Замещение дефектного гена полноценной копией Введение «трансгена» функционально активного гена без исправлений Подавление (регуляция) с помощью ми. РНК Подавление функциональной активности с помощью с продукции антагониста (доминант-негативные белки) Продукция «терапевтического» белка
С помощью генной терапии можно регулировать любой из этапов экспрессии гена Геномная ДНК м. РНК Трансляция белок Транскрипция Точечная репарация дефекта в хромосоме Замещение дефектного гена полноценной копией Введение «трансгена» функционально активного гена без исправлений Подавление (регуляция) с помощью ми. РНК Подавление функциональной активности с помощью с продукции антагониста (доминант-негативные белки) Продукция «терапевтического» белка
 Что используют для генной терапии: Олигонуклеотиды Короткие РНК (si. RNA, mi. RNA) Рибозимы Аптамерные олигонуклеотиды Плазмидные векторы Миникольца Искусственные хромосомы Репликативно-дефицитные вирусы Ретровирусы Лентивирусы Адено-ассоциированные вирусы Аденовирусы
Что используют для генной терапии: Олигонуклеотиды Короткие РНК (si. RNA, mi. RNA) Рибозимы Аптамерные олигонуклеотиды Плазмидные векторы Миникольца Искусственные хромосомы Репликативно-дефицитные вирусы Ретровирусы Лентивирусы Адено-ассоциированные вирусы Аденовирусы
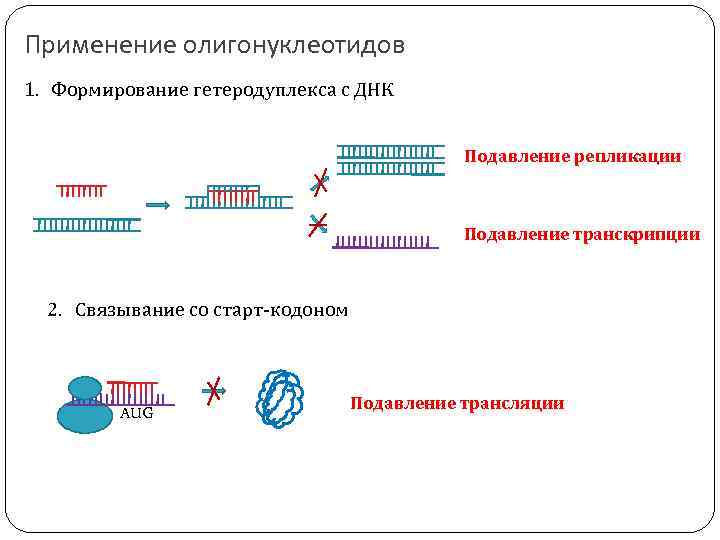 Применение олигонуклеотидов 1. Формирование гетеродуплекса с ДНК Подавление репликации Подавление транскрипции 2. Связывание со старт-кодоном AUG Подавление трансляции
Применение олигонуклеотидов 1. Формирование гетеродуплекса с ДНК Подавление репликации Подавление транскрипции 2. Связывание со старт-кодоном AUG Подавление трансляции
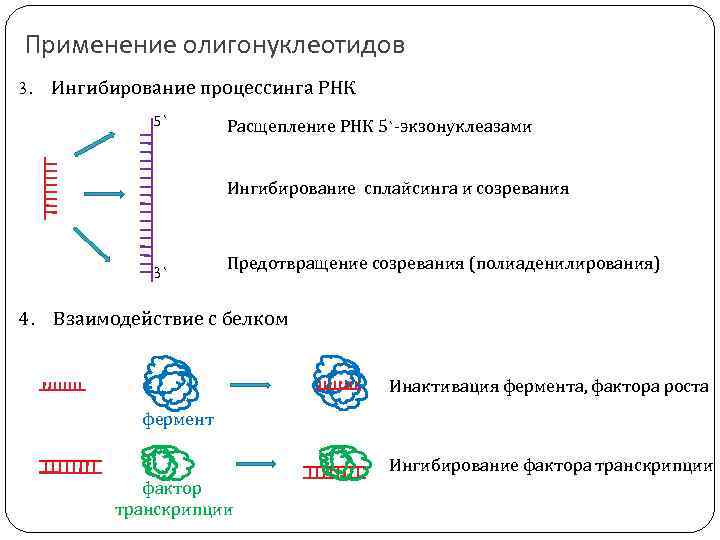 Применение олигонуклеотидов 3. Ингибирование процессинга РНК 5` Расщепление РНК 5`-экзонуклеазами Ингибирование сплайсинга и созревания 3` Предотвращение созревания (полиаденилирования) 4. Взаимодействие с белком Инактивация фермента, фактора роста фермент Ингибирование фактора транскрипции фактор транскрипции
Применение олигонуклеотидов 3. Ингибирование процессинга РНК 5` Расщепление РНК 5`-экзонуклеазами Ингибирование сплайсинга и созревания 3` Предотвращение созревания (полиаденилирования) 4. Взаимодействие с белком Инактивация фермента, фактора роста фермент Ингибирование фактора транскрипции фактор транскрипции
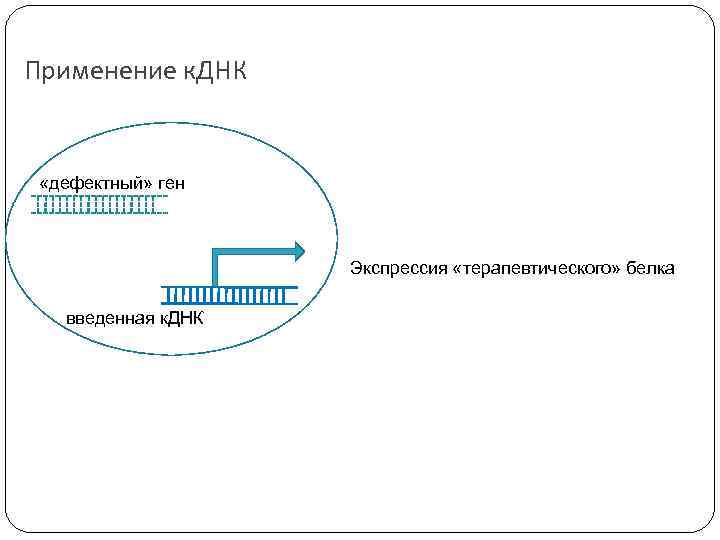 Применение к. ДНК «дефектный» ген Экспрессия «терапевтического» белка введенная к. ДНК
Применение к. ДНК «дефектный» ген Экспрессия «терапевтического» белка введенная к. ДНК
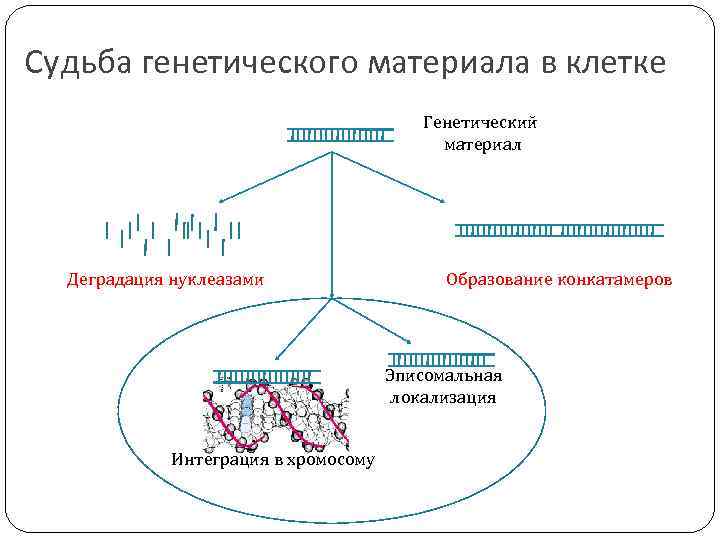 Судьба генетического материала в клетке Генетический материал Деградация нуклеазами Образование конкатамеров Эписомальная локализация Интеграция в хромосому
Судьба генетического материала в клетке Генетический материал Деградация нуклеазами Образование конкатамеров Эписомальная локализация Интеграция в хромосому
 Вектор – инструмент для переноса генетического материала в клетки Вектор для клонирования (cloning vector) – используется для наращивания фрагмента ДНК Вектор для экспрессии (expression vector) – используется для экспрессии к. ДНК НЕВИРУСНЫЕ ВЕКТОРЫ Плазмидные векторы Векторы на основе бактериофага лямбда Космидные векторы Миникольца Искусственные хромосомы ВИРУСНЫЕ ВЕКТОРЫ Ретровирусы Лентивирусы Адено-ассоциированные вирусы Аденовирусы
Вектор – инструмент для переноса генетического материала в клетки Вектор для клонирования (cloning vector) – используется для наращивания фрагмента ДНК Вектор для экспрессии (expression vector) – используется для экспрессии к. ДНК НЕВИРУСНЫЕ ВЕКТОРЫ Плазмидные векторы Векторы на основе бактериофага лямбда Космидные векторы Миникольца Искусственные хромосомы ВИРУСНЫЕ ВЕКТОРЫ Ретровирусы Лентивирусы Адено-ассоциированные вирусы Аденовирусы
 Назначение векторов Доставка генетического материала Адресная доставка Экспрессия трансгена Регулируемая Долговременная Для экспрессии трансгена вектор должен содержать участок для вставки к. ДНК промотор
Назначение векторов Доставка генетического материала Адресная доставка Экспрессия трансгена Регулируемая Долговременная Для экспрессии трансгена вектор должен содержать участок для вставки к. ДНК промотор
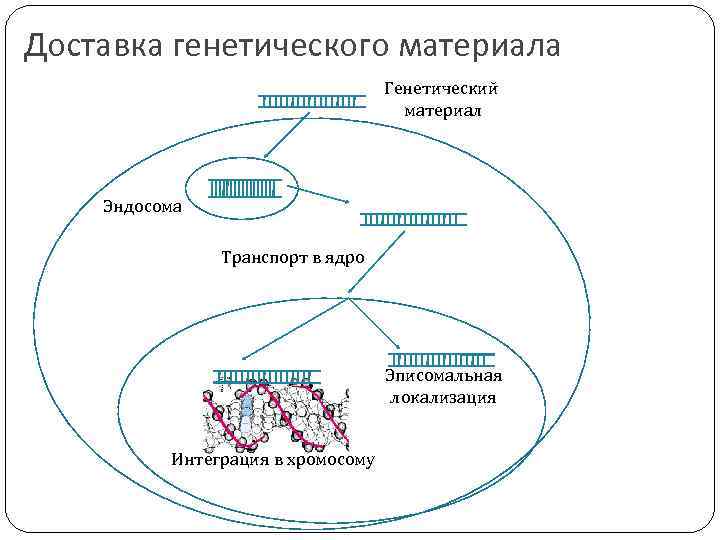 Доставка генетического материала Генетический материал Эндосома Транспорт в ядро Эписомальная локализация Интеграция в хромосому
Доставка генетического материала Генетический материал Эндосома Транспорт в ядро Эписомальная локализация Интеграция в хромосому
 «Идеальная» система доставки генетического материала: Совместима с системами транспорта организма Биосовместима (иммуногенность, стабильность) Обеспечивает специфичность взаимодействия с клеткой- мишенью Обеспечивает подавление (избегание) эндосомальной деградации Обеспечивает ядерную локализацию Обеспечивает эффективную работу генетической конструкции
«Идеальная» система доставки генетического материала: Совместима с системами транспорта организма Биосовместима (иммуногенность, стабильность) Обеспечивает специфичность взаимодействия с клеткой- мишенью Обеспечивает подавление (избегание) эндосомальной деградации Обеспечивает ядерную локализацию Обеспечивает эффективную работу генетической конструкции
 Репликативно-дефицитные вирусы В геноме вирусов отсутствуют участки, кодирующие элементы, необходимые для репликации вируса и сборки вирусных частиц Распознаются рецепторами клеточной поверхности (эффективная и прицельная доставка, но активация иммунной системы) Для наращивания необходимы клетки- упаковщики (сложно нарастить в больших объемах)
Репликативно-дефицитные вирусы В геноме вирусов отсутствуют участки, кодирующие элементы, необходимые для репликации вируса и сборки вирусных частиц Распознаются рецепторами клеточной поверхности (эффективная и прицельная доставка, но активация иммунной системы) Для наращивания необходимы клетки- упаковщики (сложно нарастить в больших объемах)
 Особенности вирусных векторов Упаковка Компактизация ДНК вирусной частицы обеспечивает совместимость с системами транспорта Распознаются рецепторами клеточной поверхности Обеспечивает специфичность взаимодействия с клеткой-мишенью Подвергаются эндоцитозу и умеют избежать деградации Закисление внутриэндосомальной среды Транспорт в ядро Используют активный транспорт в ядро благодаря сигналу ядерной локализации Организация генома Биосовместимость Сделаны из природных материалов: иммуногенны, но стабильны
Особенности вирусных векторов Упаковка Компактизация ДНК вирусной частицы обеспечивает совместимость с системами транспорта Распознаются рецепторами клеточной поверхности Обеспечивает специфичность взаимодействия с клеткой-мишенью Подвергаются эндоцитозу и умеют избежать деградации Закисление внутриэндосомальной среды Транспорт в ядро Используют активный транспорт в ядро благодаря сигналу ядерной локализации Организация генома Биосовместимость Сделаны из природных материалов: иммуногенны, но стабильны
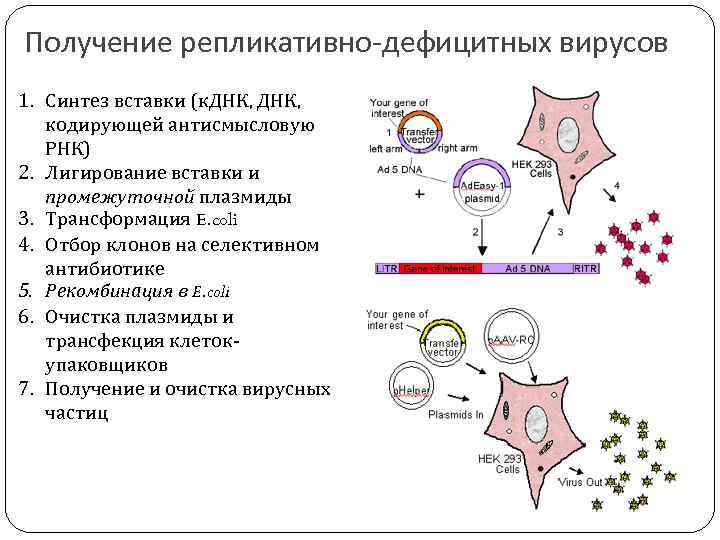 Получение репликативно-дефицитных вирусов 1. Синтез вставки (к. ДНК, кодирующей антисмысловую РНК) 2. Лигирование вставки и промежуточной плазмиды 3. Трансформация E. coli 4. Отбор клонов на селективном антибиотике 5. Рекомбинация в E. coli 6. Очистка плазмиды и трансфекция клетокупаковщиков 7. Получение и очистка вирусных частиц
Получение репликативно-дефицитных вирусов 1. Синтез вставки (к. ДНК, кодирующей антисмысловую РНК) 2. Лигирование вставки и промежуточной плазмиды 3. Трансформация E. coli 4. Отбор клонов на селективном антибиотике 5. Рекомбинация в E. coli 6. Очистка плазмиды и трансфекция клетокупаковщиков 7. Получение и очистка вирусных частиц
 Преимущества и недостатки репликативнодефицитных вирусов Эффективная доставка Встраивание в геном (перманентное присутствие в геноме реципиента) Вирусный геном быстро инактивируется клеткой Активация иммунной системы Трудоемкий процесс производства
Преимущества и недостатки репликативнодефицитных вирусов Эффективная доставка Встраивание в геном (перманентное присутствие в геноме реципиента) Вирусный геном быстро инактивируется клеткой Активация иммунной системы Трудоемкий процесс производства
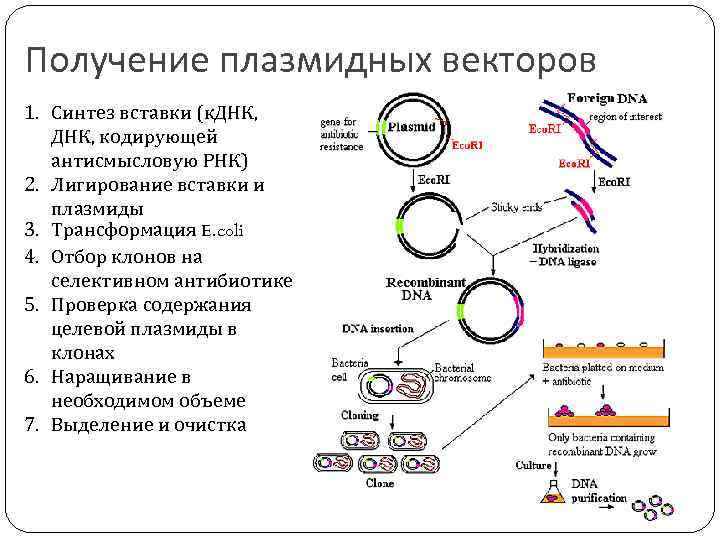 Получение плазмидных векторов 1. Синтез вставки (к. ДНК, кодирующей антисмысловую РНК) 2. Лигирование вставки и плазмиды 3. Трансформация E. coli 4. Отбор клонов на селективном антибиотике 5. Проверка содержания целевой плазмиды в клонах 6. Наращивание в необходимом объеме 7. Выделение и очистка
Получение плазмидных векторов 1. Синтез вставки (к. ДНК, кодирующей антисмысловую РНК) 2. Лигирование вставки и плазмиды 3. Трансформация E. coli 4. Отбор клонов на селективном антибиотике 5. Проверка содержания целевой плазмиды в клонах 6. Наращивание в необходимом объеме 7. Выделение и очистка
 Преимущества и недостатки плазмидных конструкций Можно внести много копий в клетки-мишени (высокий уровень экспрессии трансгена) Можно нарастить в больших объемах при низкой себестоимости Не происходит встраивания в геном Достаточно быстро инактивируются клеткой (метилирование вирусного промотора) Производство связано с культурами бактерий (необходима очистка от эндотоксинов)
Преимущества и недостатки плазмидных конструкций Можно внести много копий в клетки-мишени (высокий уровень экспрессии трансгена) Можно нарастить в больших объемах при низкой себестоимости Не происходит встраивания в геном Достаточно быстро инактивируются клеткой (метилирование вирусного промотора) Производство связано с культурами бактерий (необходима очистка от эндотоксинов)
 Искусственные хромосомы Конструкции, собранные из фрагментов ДНК de novo (содержат теломеру и центромеру) Модифицированные существующие хромосомы (14 и 21 хромосомы человека)
Искусственные хромосомы Конструкции, собранные из фрагментов ДНК de novo (содержат теломеру и центромеру) Модифицированные существующие хромосомы (14 и 21 хромосомы человека)
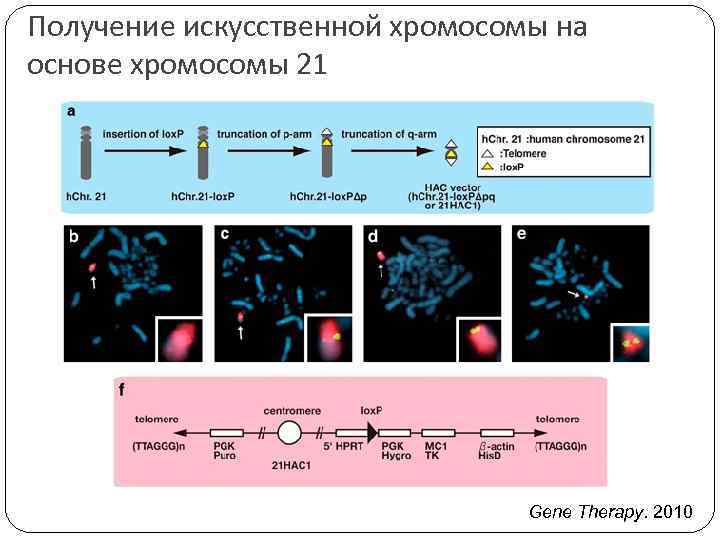 Получение искусственной хромосомы на основе хромосомы 21 Gene Therapy. 2010
Получение искусственной хромосомы на основе хромосомы 21 Gene Therapy. 2010
 Искусственные хромосомы Встраивание в геном в качестве самостоятельной хромосомы(реплицируются в клеточном цикле) Перенос трансгенов большого размера Эффективная доставка достигается с помощью вирусных ампликонов
Искусственные хромосомы Встраивание в геном в качестве самостоятельной хромосомы(реплицируются в клеточном цикле) Перенос трансгенов большого размера Эффективная доставка достигается с помощью вирусных ампликонов
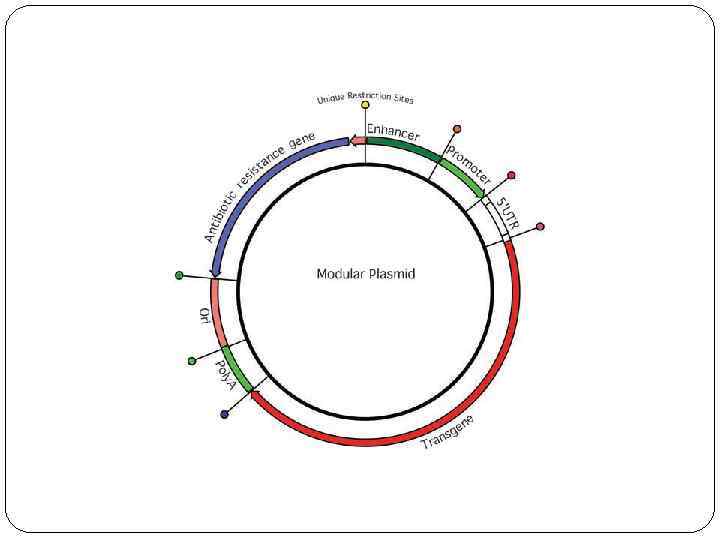
 Препараты для генной терапии: производство и доставка
Препараты для генной терапии: производство и доставка
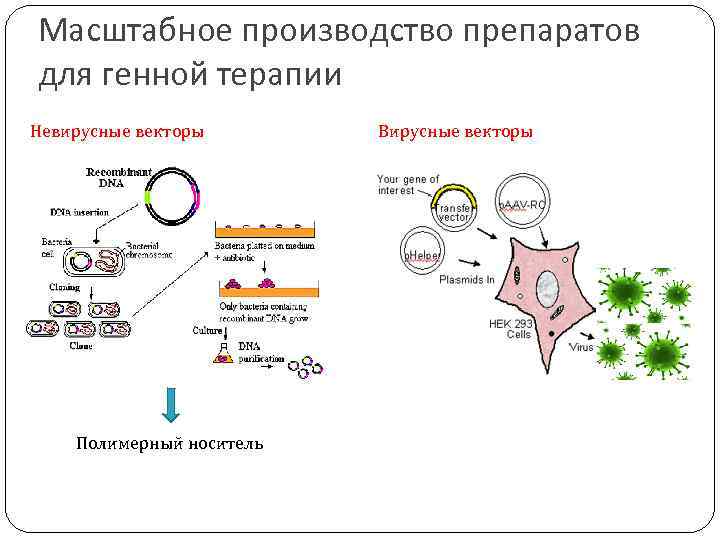 Масштабное производство препаратов для генной терапии Невирусные векторы Полимерный носитель Вирусные векторы
Масштабное производство препаратов для генной терапии Невирусные векторы Полимерный носитель Вирусные векторы
 Требования к препаратам для генной терапии Чистота и гомогенность Удаление примесей продуцирующих систем Стабильность при хранении и применении (сохранение интактной структуры, сохранение дискретности в физиологических средах) Лиофильная сушка Добавление стабилизирующих полимеров (ПЭГ) Использование меньшего давления при введении Соотношение терапевтическая ДНК : носитель < 1: 1 Адресность Использование конъюгатов с лигандами к поверхностным рецепторам
Требования к препаратам для генной терапии Чистота и гомогенность Удаление примесей продуцирующих систем Стабильность при хранении и применении (сохранение интактной структуры, сохранение дискретности в физиологических средах) Лиофильная сушка Добавление стабилизирующих полимеров (ПЭГ) Использование меньшего давления при введении Соотношение терапевтическая ДНК : носитель < 1: 1 Адресность Использование конъюгатов с лигандами к поверхностным рецепторам
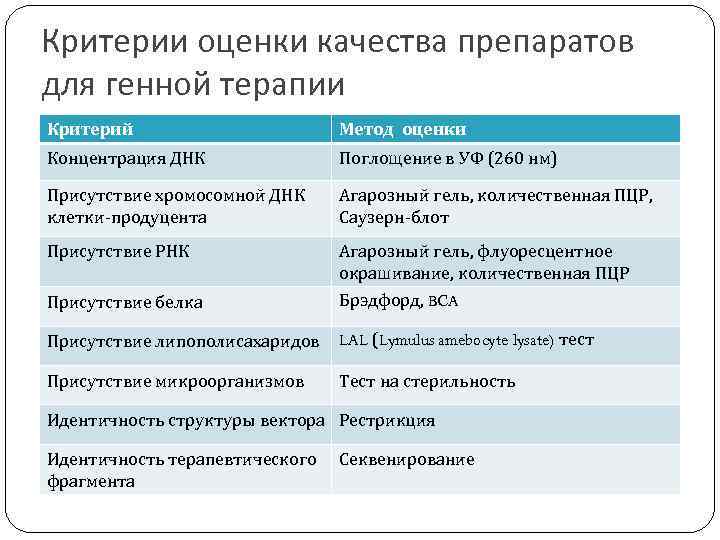 Критерии оценки качества препаратов для генной терапии Критерий Метод оценки Концентрация ДНК Поглощение в УФ (260 нм) Присутствие хромосомной ДНК клетки-продуцента Агарозный гель, количественная ПЦР, Саузерн-блот Присутствие РНК Присутствие белка Агарозный гель, флуоресцентное окрашивание, количественная ПЦР Брэдфорд, BCA Присутствие липополисахаридов LAL (Lymulus amebocyte lysate) тест Присутствие микроорганизмов Тест на стерильность Идентичность структуры вектора Рестрикция Идентичность терапевтического фрагмента Секвенирование
Критерии оценки качества препаратов для генной терапии Критерий Метод оценки Концентрация ДНК Поглощение в УФ (260 нм) Присутствие хромосомной ДНК клетки-продуцента Агарозный гель, количественная ПЦР, Саузерн-блот Присутствие РНК Присутствие белка Агарозный гель, флуоресцентное окрашивание, количественная ПЦР Брэдфорд, BCA Присутствие липополисахаридов LAL (Lymulus amebocyte lysate) тест Присутствие микроорганизмов Тест на стерильность Идентичность структуры вектора Рестрикция Идентичность терапевтического фрагмента Секвенирование
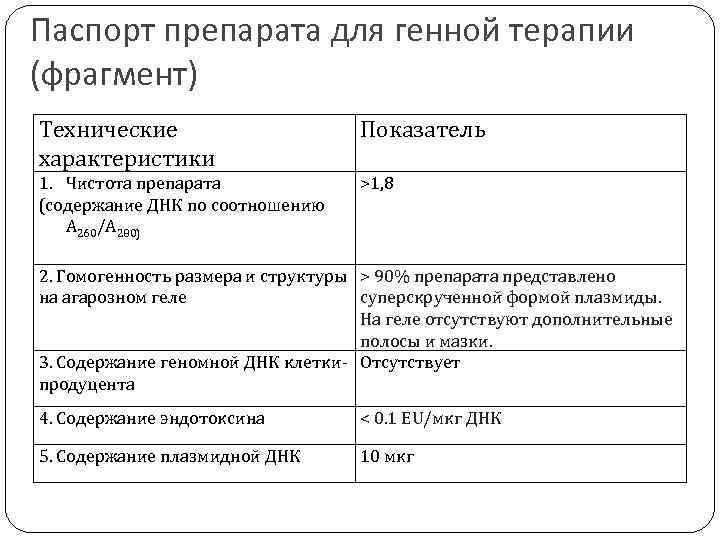 Паспорт препарата для генной терапии (фрагмент) Технические характеристики Показатель 1. Чистота препарата (содержание ДНК по соотношению А 260/А 280) >1, 8 2. Гомогенность размера и структуры > 90% препарата представлено на агарозном геле суперскрученной формой плазмиды. На геле отсутствуют дополнительные полосы и мазки. 3. Содержание геномной ДНК клетки- Отсутствует продуцента 4. Содержание эндотоксина < 0. 1 EU/мкг ДНК 5. Содержание плазмидной ДНК 10 мкг
Паспорт препарата для генной терапии (фрагмент) Технические характеристики Показатель 1. Чистота препарата (содержание ДНК по соотношению А 260/А 280) >1, 8 2. Гомогенность размера и структуры > 90% препарата представлено на агарозном геле суперскрученной формой плазмиды. На геле отсутствуют дополнительные полосы и мазки. 3. Содержание геномной ДНК клетки- Отсутствует продуцента 4. Содержание эндотоксина < 0. 1 EU/мкг ДНК 5. Содержание плазмидной ДНК 10 мкг
 Компактизация ДНК в искусственном векторе Взаимодействие с поликатионами Липосомы Искусственные полимеры Природные полимеры Поликатионы обеспечивают неспецифическое связывание вектора с поверхностью клетки
Компактизация ДНК в искусственном векторе Взаимодействие с поликатионами Липосомы Искусственные полимеры Природные полимеры Поликатионы обеспечивают неспецифическое связывание вектора с поверхностью клетки
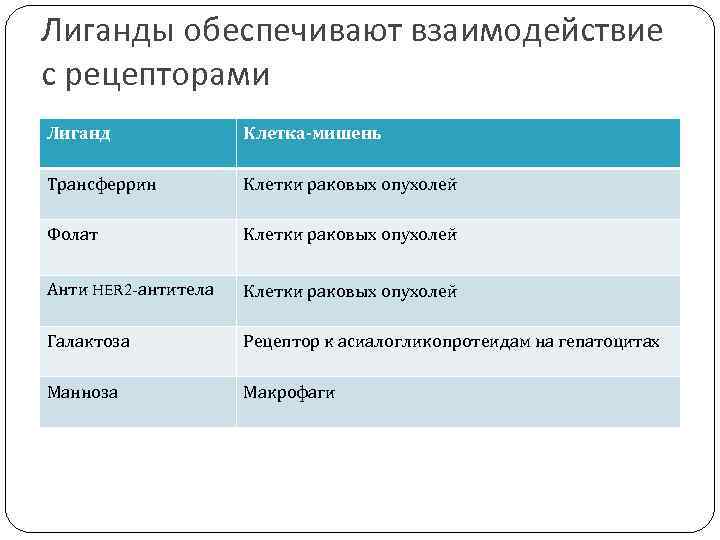 Лиганды обеспечивают взаимодействие с рецепторами Лиганд Клетка-мишень Трансферрин Клетки раковых опухолей Фолат Клетки раковых опухолей Анти HER 2 -антитела Клетки раковых опухолей Галактоза Рецептор к асиалогликопротеидам на гепатоцитах Манноза Макрофаги
Лиганды обеспечивают взаимодействие с рецепторами Лиганд Клетка-мишень Трансферрин Клетки раковых опухолей Фолат Клетки раковых опухолей Анти HER 2 -антитела Клетки раковых опухолей Галактоза Рецептор к асиалогликопротеидам на гепатоцитах Манноза Макрофаги
 Предотвращение деградации в эндосомах Субъединица 2 гемагглютинина вируса гриппа Меллитин Производные полиакриловой кислоты Полиэтиленимин (протоновая губка) Полиамидоаминные дендримеры
Предотвращение деградации в эндосомах Субъединица 2 гемагглютинина вируса гриппа Меллитин Производные полиакриловой кислоты Полиэтиленимин (протоновая губка) Полиамидоаминные дендримеры
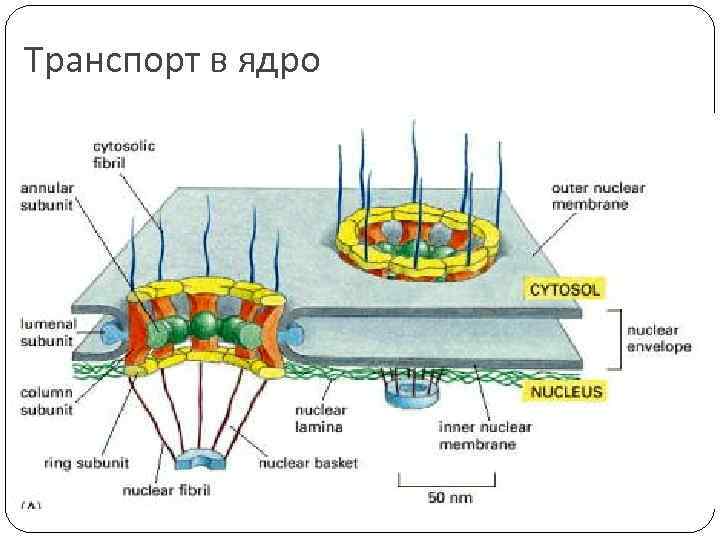 Транспорт в ядро
Транспорт в ядро
 Модификация векторной «основы» Удаление или энзиматическая модификация Cp. G- последовательностей Снижение активации иммунной системы Часто содержится в промоторной области Удаление всех «второстепенных» элементов, уменьшение размера векторной «основы» Возрастает соотношение терапевтическая ДНК : вес вектора Возникает место для добавления дополнительных элементов Может приводить к снижению репликации или продукции трансгена Использование селективных антибиотиков, редко применяемых в клинической практике
Модификация векторной «основы» Удаление или энзиматическая модификация Cp. G- последовательностей Снижение активации иммунной системы Часто содержится в промоторной области Удаление всех «второстепенных» элементов, уменьшение размера векторной «основы» Возрастает соотношение терапевтическая ДНК : вес вектора Возникает место для добавления дополнительных элементов Может приводить к снижению репликации или продукции трансгена Использование селективных антибиотиков, редко применяемых в клинической практике
 Биосовместимость искусственных систем доставки Удаление или энзиматическая модификация Cp. G- последовательностей ПЭГилирование Присоединение производных полиакриловой кислоты N-(2 -гидроксипропил)метакриламид
Биосовместимость искусственных систем доставки Удаление или энзиматическая модификация Cp. G- последовательностей ПЭГилирование Присоединение производных полиакриловой кислоты N-(2 -гидроксипропил)метакриламид
 Этапы направленной доставки Этап локализации Процесс Место введения - тканьмишень Накопление в ткани-мишени Ткань мишень – клеткамишень Накопление или связывание с клеткамимишенями Поверхность клетки – внутриклеточная локализация Интернализация клеткой и заданная внутриклеточная локализация Ядерная локализация – хромосомная интеграция Сайт-специфичная интеграция, а не хаотичная
Этапы направленной доставки Этап локализации Процесс Место введения - тканьмишень Накопление в ткани-мишени Ткань мишень – клеткамишень Накопление или связывание с клеткамимишенями Поверхность клетки – внутриклеточная локализация Интернализация клеткой и заданная внутриклеточная локализация Ядерная локализация – хромосомная интеграция Сайт-специфичная интеграция, а не хаотичная
 Методы адресной доставки и контроля Биологические Конъюгация с лигандами Последовательности внутриклеточной локализации Сайт-специфичная интеграция в геном Физические Сила гравитации Магнитное поле Гидродинамическая сила В составе аэрозоля На крупном носителе В составе инъецируемого носителя Электрическое поле Ультразвук
Методы адресной доставки и контроля Биологические Конъюгация с лигандами Последовательности внутриклеточной локализации Сайт-специфичная интеграция в геном Физические Сила гравитации Магнитное поле Гидродинамическая сила В составе аэрозоля На крупном носителе В составе инъецируемого носителя Электрическое поле Ультразвук
 Магнетофекция ПРИНЦИП: магнитные наночастицы смешивают с НК или векторами в буфере, помещают на клетки, которые помещают на магнит IN VIVO: трансфекция сегментов кровеносных сосудов и ЖКТ ОГРАНИЧЕНИЯ: противодействия гидродинамики тока крови; накопление магнитных наночастиц
Магнетофекция ПРИНЦИП: магнитные наночастицы смешивают с НК или векторами в буфере, помещают на клетки, которые помещают на магнит IN VIVO: трансфекция сегментов кровеносных сосудов и ЖКТ ОГРАНИЧЕНИЯ: противодействия гидродинамики тока крови; накопление магнитных наночастиц
 Гидродинамический метод доставки ПРИНЦИП: быстрое внутривенное введение больших объемов растворов ДНК IN VIVO: трансфекция гепатоцитов ОГРАНИЧЕНИЯ: оседает именно в печени, сложно добиться трансфекции иных тканей
Гидродинамический метод доставки ПРИНЦИП: быстрое внутривенное введение больших объемов растворов ДНК IN VIVO: трансфекция гепатоцитов ОГРАНИЧЕНИЯ: оседает именно в печени, сложно добиться трансфекции иных тканей
 Местная имплантация вектора ПРИНЦИП: коллагеновая или фибриновая губка инфильтрируется раствором вектора и подвергается сушке-замораживанию, при помещении в ткань (на раневую поверхность) клетки, заселяющие губку, поглощают генетический материал IN VIVO: заживление ран, восстановление дефектов хрящей и костей, стенты
Местная имплантация вектора ПРИНЦИП: коллагеновая или фибриновая губка инфильтрируется раствором вектора и подвергается сушке-замораживанию, при помещении в ткань (на раневую поверхность) клетки, заселяющие губку, поглощают генетический материал IN VIVO: заживление ран, восстановление дефектов хрящей и костей, стенты
 Инъецируемые имплантаты ПРИНЦИП: смешивание ДНК с полимерами (дендримерами), на основе поли(лактид-когликолид) и гликофурола, образование нано или микрочастиц IN VIVO: различные ткани ОГРАНИЧЕНИЯ: проникает в клетки, связывающие эти полимеры
Инъецируемые имплантаты ПРИНЦИП: смешивание ДНК с полимерами (дендримерами), на основе поли(лактид-когликолид) и гликофурола, образование нано или микрочастиц IN VIVO: различные ткани ОГРАНИЧЕНИЯ: проникает в клетки, связывающие эти полимеры
 Аэрозольная доставка ПРИНЦИП: смешивание ДНК или векторов с полиэтиленимином, смешивание с компонентами для аэрозольного распыления IN VIVO: легкие ОГРАНИЧЕНИЯ: полиэтиленимин высокотоксичен
Аэрозольная доставка ПРИНЦИП: смешивание ДНК или векторов с полиэтиленимином, смешивание с компонентами для аэрозольного распыления IN VIVO: легкие ОГРАНИЧЕНИЯ: полиэтиленимин высокотоксичен
 Доставка с помощью ультразвука ПРИНЦИП: ДНК доставляется в составе микропузырьков или липосом, ультразвук вызывает высвобождение ДНК из носителя IN VIVO: различные ткани ОГРАНИЧЕНИЯ: сложно обеспечить локализацию суспензии ДНК
Доставка с помощью ультразвука ПРИНЦИП: ДНК доставляется в составе микропузырьков или липосом, ультразвук вызывает высвобождение ДНК из носителя IN VIVO: различные ткани ОГРАНИЧЕНИЯ: сложно обеспечить локализацию суспензии ДНК
 Доставка с помощью электрического поля ПРИНЦИП: приложение электрического разряда вызывает деполяризацию мембран и повышает их проницаемость IN VIVO: ткани, доступные для приложения разряда (мышцы, сосуды) ОГРАНИЧЕНИЯ: доступность тканей для приложения разряда
Доставка с помощью электрического поля ПРИНЦИП: приложение электрического разряда вызывает деполяризацию мембран и повышает их проницаемость IN VIVO: ткани, доступные для приложения разряда (мышцы, сосуды) ОГРАНИЧЕНИЯ: доступность тканей для приложения разряда
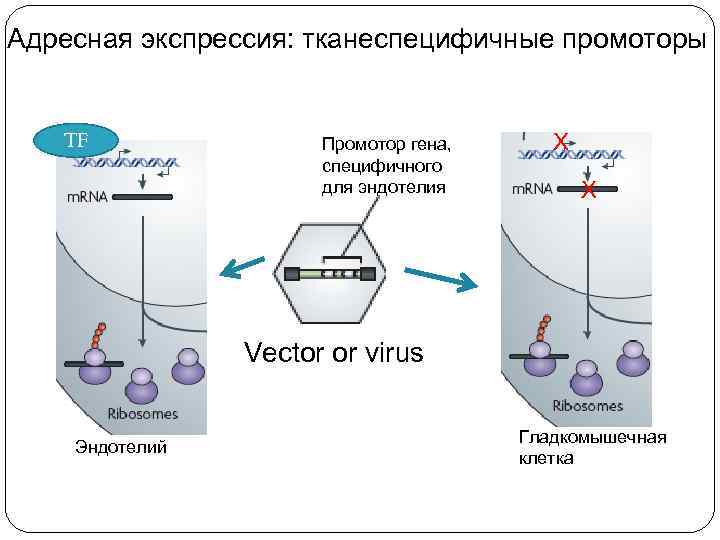 Адресная экспрессия: тканеспецифичные промоторы TF Промотор гена, специфичного для эндотелия Х Х Vector or virus Эндотелий Гладкомышечная клетка
Адресная экспрессия: тканеспецифичные промоторы TF Промотор гена, специфичного для эндотелия Х Х Vector or virus Эндотелий Гладкомышечная клетка
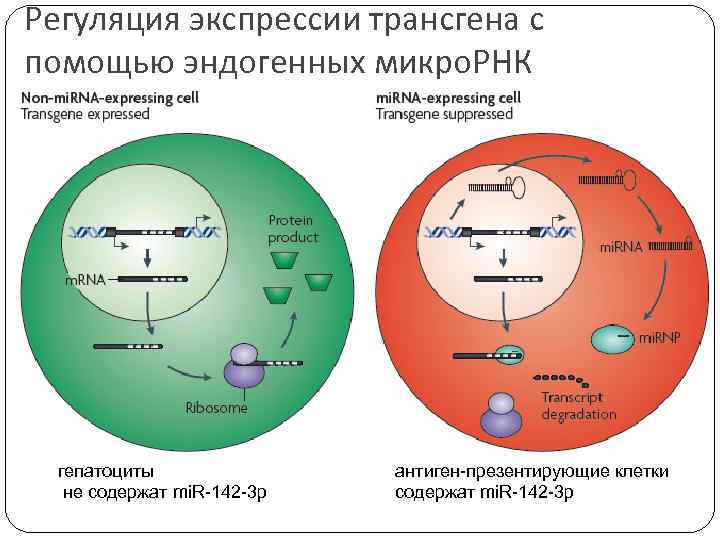 Регуляция экспрессии трансгена с помощью эндогенных микро. РНК гепатоциты не содержат mi. R-142 -3 p антиген-презентирующие клетки содержат mi. R-142 -3 p
Регуляция экспрессии трансгена с помощью эндогенных микро. РНК гепатоциты не содержат mi. R-142 -3 p антиген-презентирующие клетки содержат mi. R-142 -3 p

 Генная терапия: Вирусные и невирусные векторы используют для доставки к. ДНК или РНК в клетки и ткани Применяют для восполнения функции поврежденных генов продукции «терапевтических» белков подавления продукции нежелательного белка избирательной элиминации клеток
Генная терапия: Вирусные и невирусные векторы используют для доставки к. ДНК или РНК в клетки и ткани Применяют для восполнения функции поврежденных генов продукции «терапевтических» белков подавления продукции нежелательного белка избирательной элиминации клеток


