през био генная.ppt
- Количество слайдов: 32

ГЕННАЯ ИНЖЕНЕРИЯ В БИОТЕХНОЛОГИИ 1. История развития генной инженерии. Методы генной инженерии и способы получения генов 2. Степень безопасности трансгенных продуктов. 3. Практические аспекты генной инженерии

Вопрос 1. История развития генной инженерии Генная инженерия (технология рекомбинантных ДНК, молекулярное клонирование) - это совокупность экспериментальных процедур, позволяющих осуществлять перенос генетического материала из одного организма в другой. Генная инженерия - конструирование in vitro функционально активных генетических структур (рекомбинантных ДНК), или как создание искусственных генетических программ. Генная инженерия – управление генетической основой организмов посредством внедрения или удаления специфических генов, с использованием техники современной молекулярной биологии. Задача конструировать рекомбинантные ДНК, которые могли бы придать клеткам-реципиентам полезные для человека свойства (синтезировать пищевой и кормовой белок).

Этапы развития генной инженерии: Первый этап - работы касаются получения гибридов между различными плазмидами и фагами, иначе говоря, конструированием так называемых векторных молекул. Плазмиды – автономно реплицирующиеся небольшие, чаще кольцевые молекулы ДНК, содержащие сразу несколько сайтов рестрикции для разных рестрикционных ферментов. Фаг – вирусная ДНК, паразитирующая в клетках микроорганизмов. 2. Второй этап связан с началом работ по получению рекомбинатных молекул ДНК между хромосомными генами прокариот и различными плазмидами, доказательством их стабильности и жизнеспособности. 3. Третий этап связан с началом работ по включению в векторные молекулы ДНК генов эукариот, главным образом, растений и животных.

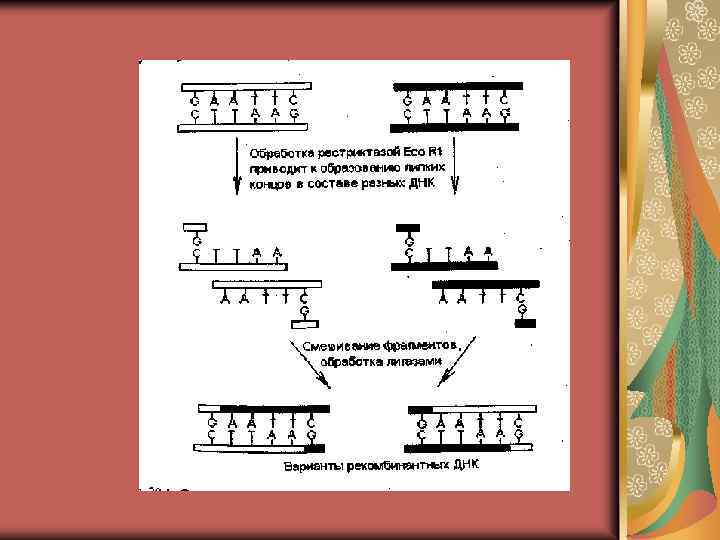
Методы генной инженерии и способы получения генов. 1. Метод рекомбинантных ДНК. Ферменты, которые в настоящее время применяются для конструирования рекомбинантных ДНК, можно разделить на следующие группы: • Ферменты, осуществляющие фрагментацию ДНК (рестриктазы). • Фермент, синтезирующий фрагменты ДНК на матрице РНК: РНК-зависимая ДНК-полимераза (обратная транскриптаза). • Ферменты, сшивающие фрагменты ДНК: ДНК-лигаза (полинуклеотидлигаза). • Ферменты, позволяющие осуществлять изменение структуры концов фрагментов ДНК: нуклеаза. • Ферменты, применяемые для приготовления гибридизационных проб: ДНК-полимераза.

2. МЕТОД. Секвенирование ДНК определение последовательности нуклеотидов в ее молекулах. 2. 1. Секвенирование обрыва цепи 2. 2. Секвенирование химическим расщеплением 3. МЕТОД. химического и химикоэнзиматического синтеза дезоксиполинуклеотидов.
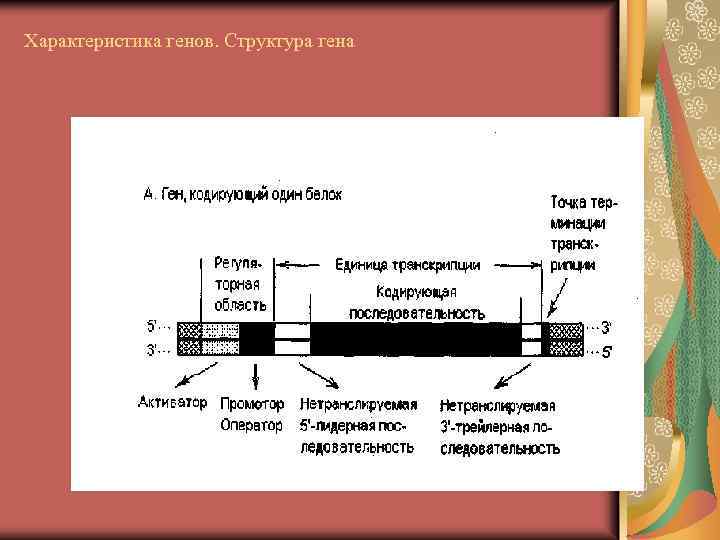
Характеристика генов. Структура гена

СПОСОБЫ ПОЛУЧЕНИЯ ГЕНОВ: 1. Выделение из ДНК

2. Химико-ферментативный синтез генов а) матрица ДНК и с помощью полинуклеотидфосфорилаз, б) матрица м. РНК с затравкой с 3' конца для комплементарной цепи ДНК. 3. Ферментативный синтез

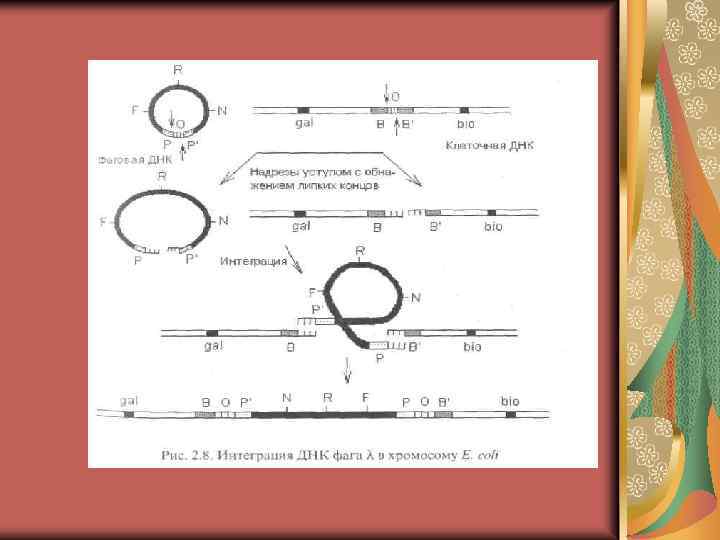
Пути переноса генов: 1. Получение фрагментов ДНК (генов). 2. Создание рекомбинантной генетической конструкции. На этом этапе производится встраивание нужного фрагмента ДНК (вставки) в другую молекулу ДНК (вектор). Для выделения, анализа и конструирования генов используют клетки прокариот. 3. Введение ДНК в клетку-хозяина. Получившуюся молекулу рекомбинантной ДНК вводят в клетку-хозяина (реципиент), где она реплицируется (размножается) либо самостоятельно, либо интегрируется в хромосому и передается потомкам.

4. Идентификация и отбор клеток, несущих рекомбинантную ДНК. Производится на селективной среде, на которой могут вырасти только трансформированные клетки. 5. Анализ экспрессии (встраивания)перенесенного гена в ДНКклетку хозяина. Получение специфического белкового продукта, синтезирующегося клетками-хозяевами, служит подтверждением их трансгенной природы. С момента введения рекомбинантной ДНК в клетку начинается молекулярное клонирование, т. е. получение потомков созданной рекомбинантной ДНК.

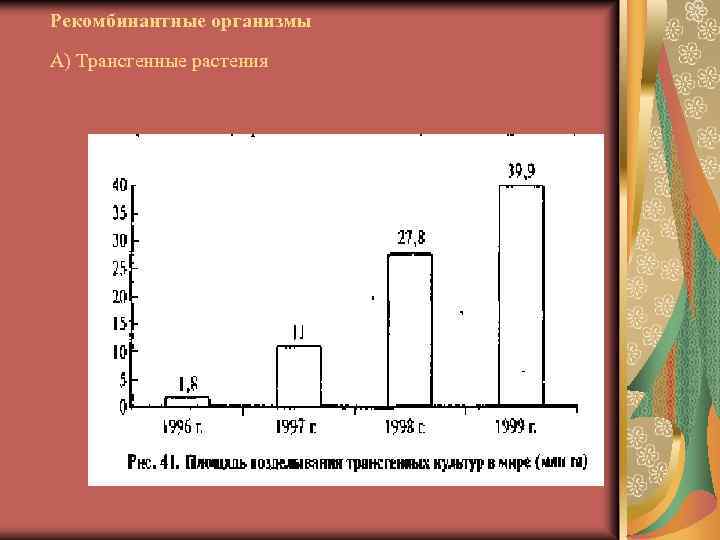
Рекомбинантные организмы А) Трансгенные растения
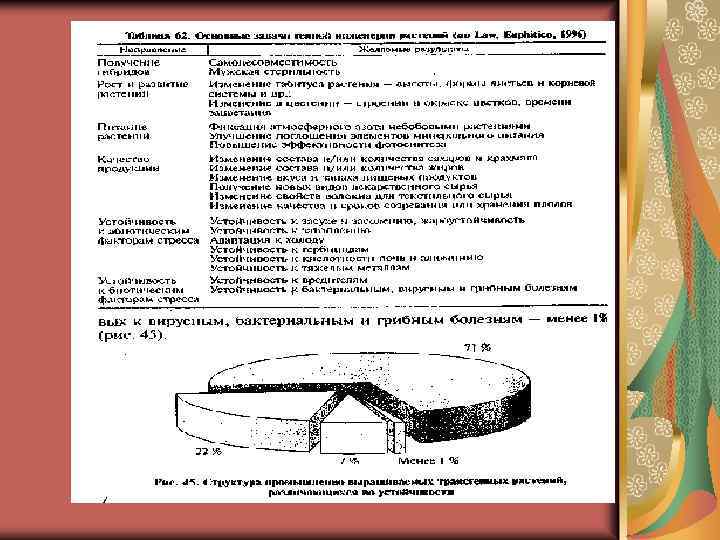


Признаки, контролируемые перенесенными генами в растения Устойчивость к гербецидам. Устойчивость к насекомым вредителям. Устойчивость к гербицидам и насекомым. Устойчивость к вирусам. Устойчивость к грибным болезням. Устойчивость одновременно к бактериальной и грибной инфекции. Устойчивость к абиотическим факторам. Создание трансгенных растений для фармакологической промышленности. Выращивание растений с определенным аминокислотным составом. Создание трансгенных растений, несущих гены, кодирующие синтез вакцин, против многих болезней. Применение трансгенных растений для фитомедиации – очистки почв, вод от чужеродных загрязнений.
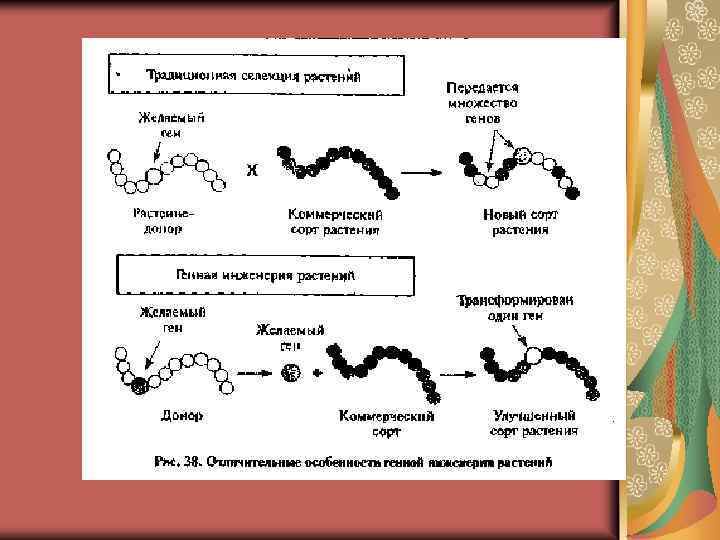


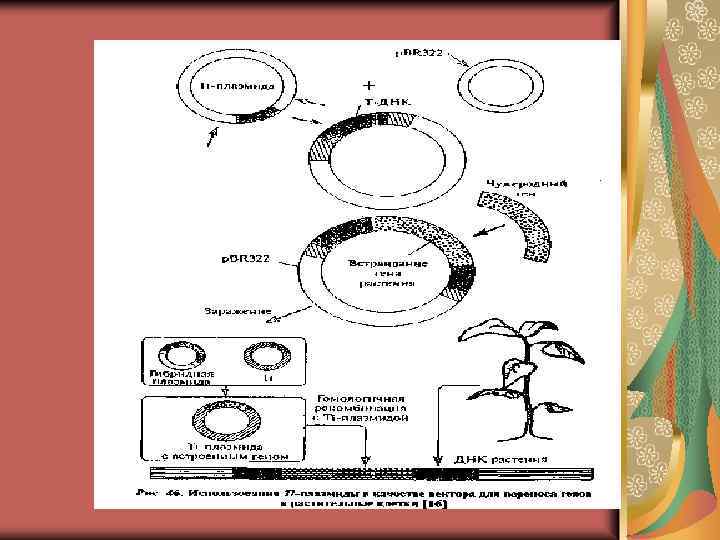
Этапы переноса генов в клетки растений. 1. Рестриктазы (рестрикционными эндонуклеазами) узнают определенную последовательность своей ДНК и расщепляют чужую на мелкие фрагменты. 2. Сшивка фрагментов идет тремя методами в зависимости от видов концов. А) Сшивка по одноименным «липким» концам – любые два фрагмента могут слипаться за счет образования водородных связей между однонитевыми участками комплементарных нуклеотидов. Б) Сшивка по «тупым» концам – реже используется. В) Сшивка фрагментов с разноименными «липкими» концами проводят с использование «переходников» - линкеров. Линкеры – химически синтезированные олигонуклеотиды, представляющие собой сайты рестрикции (места расщипления) или их комбинацию. 3. Сшитую ДНК в пробирке вносят в живую клетку при помощи векторов разными способами. Векторы (векторные молекулы) – молекулы ДНК, способные акцептировать чужеродную ДНК и обеспечивающие ее репликацию и даже экспрессию. Экспрессия гена – проявление генетической информации, записанной в гене, в форме РНК, белка и фенотипического признака. В качестве векторов используют плазмиды (кольцевые внехромосомные ДНК, автономно реплицирующиеся) и бактериофаги – вирусы, инфицирующие бактерии. 3. 1. Использование промежуточного вектора 3. 2. Метод биологической баллистики для трансформации однодольных.

Б) ТРАНСГЕННЫЕ ЖИВОТНЫЕ Методы введения чужеродной ДНК в животные клетки: физическими методами (микроинъекция, электропорация, слияние липосом), либо при помощи вирусных векторов. Стратегия получения трансгенных животных состоит в следующем: 1. Клонированный ген в составе вектора вводят в ядро оплодотворенной яйцеклетки. 2. Инокулированные оплодотворенные яйцеклетки имплантируют в реципиентную женскую особь. 3. Отбирают потомков, которые содержат клонированный ген во всех клетках. 4. Скрещивают животных, которые несут клонированный ген в клетках зародышевой линии, и получают новую генетическую линию. Основные схемы получения трансгенных животных. 1. Вектором на основе ретровируса животных инфицируют восьмимиклеточный эмбрион, который потом имплантируется в самку. Этот способ трансформации считается наиболее эффективным. 2. Трансгенную конструкцию вводят путем микроинъекции в мужской пронуклеус оплодотворенной яйцеклетки, которая затем переносится в «суррогатную мать» . 3. Стволовые клетки модифицируются в культуре, после чего их вводят в эмбрион на стадии бластоцисты. 4. Перенос гена осуществляют при помощи дрожжевых хромосом (YAC), что позволяет переносить несколько генов вместе с их собственными регуляторными последовательностями.
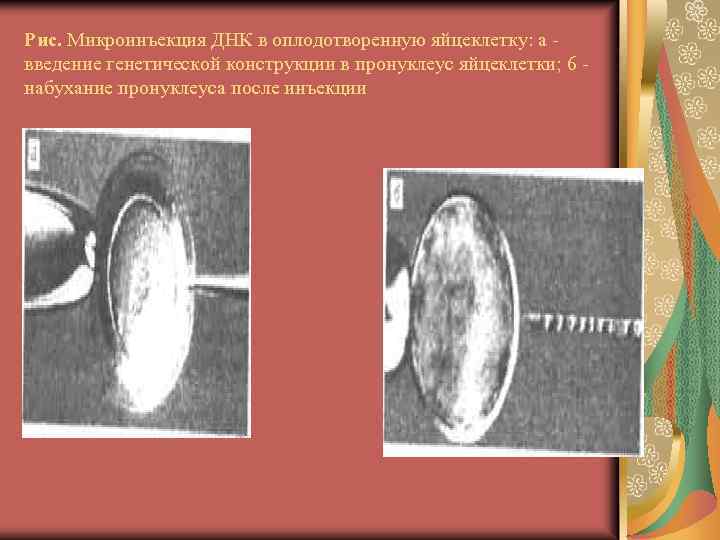
Рис. Микроинъекция ДНК в оплодотворенную яйцеклетку: а введение генетической конструкции в пронуклеус яйцеклетки; 6 набухание пронуклеуса после инъекции

5. Степень безопасности трансгенных продуктов Оценка генно-модифицированного организма по критериям безопасности складывается из 2 направлений: исследование биобезопасности организмов. определение пищевой безопасности трансгенных организмов.


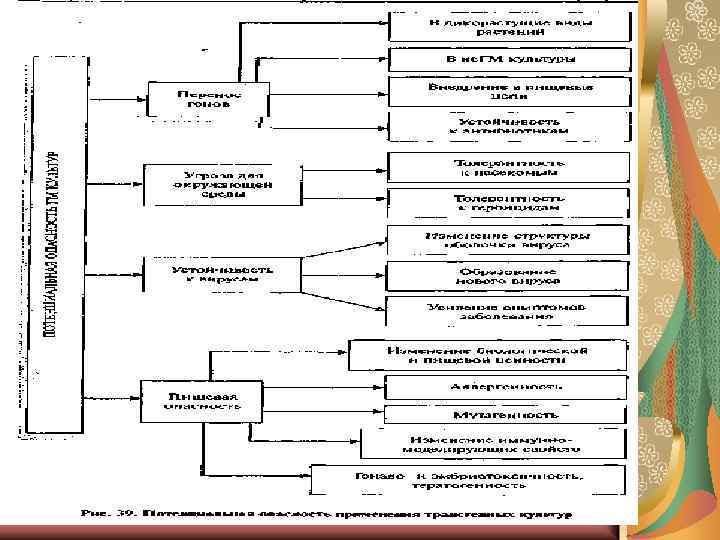
1. Биобезопасность генно-модифицированных продуктов – оценка потенциальной опасности трансгенных организмов для окружающей среды и для человека связана с возможными отрицательными последствиями: вытеснением природных организмов из их экологических ниш с последующим нарушением экологического равновесия, уменьшение биоразнообразия, бесконтрольный перенос чужеродных генов из трансгенных организмов в природные, что может привести к активации ранее известных или образованию новых патогенов.

Этапы исследований на биобезопасность трансгенных микроорганизмов: 1. Лабораторные испытания, подтверждающие отсутствие опасности штамма. 2. Исследование поведения микроорганизма в изолированной теплице или изолированном водоеме. 3. Проведение мелкоделяночных полевых испытаний. Крупномасштабные полевые испытания. Крупномасштабная интродукция трансгенного организма.

2. Пищевая токсиколого-гигиеническая оценка трансгенных культур Оценка пищевых свойств включает изучение: пищевой ценности продукта, норм потребления, способов использования в питании, поступления отдельных нутриентов (если ожидаемое поступление нутриента превышает 15% от его суточной потребности), влияние на микрофлору кишечника (если содержит живые организмы).

Токсикологическая характеристика предусматривает определение следующих показателей: токсикокинетика, генотоксичность, потенциальная аллергенность, потенциальная колонизация в желудочнокишечном тракте (в случае содержания живых организмов), результаты субхронического (90 суток) токсикологического эксперимента на лабораторных животных и исследований на добровольцах.

Медико-генетическая оценка – включает экспертизу структуры рекомбинантной ДНК, внедренной в растительный геном, в том числе маркерных генов, промоторов, оценку регуляторных последовательностей, определение стабильности генетически модифицированных организмов на протяжении нескольких поколений с учетом уровня выраженности генов. Медико-биологическая оценка – определение санитарнохимических показателей качества и безопасности, проведения токсикологических исследований на лабораторных животных, оценки аллергенных свойств, возможных мутагенных и канцерогенных эффектов продукта, изучения влияния на функцию воспроизводства, наблюдений на добровольцах и эпидемиологических исследований. Исследования технологических свойств – определение ее органолептических и физико-химических свойств, изучения сохранности и влияния генетической модификации на технологические параметры продукции.
през био генная.ppt