Генна терапія Генна терапія – сукупність генно-інженерних і


























34644-bt15_genna_terapiya.ppt
- Количество слайдов: 35
 Генна терапія
Генна терапія
 Генна терапія – сукупність генно-інженерних і медичних методів, скерованих на внесення змін в генетичний апарат соматичних клітин людини з метою лікування захворювань. За допомогою генної терапії можна виправляти: Соматичні мутацій Зміни, зумовлені появою чужорідного генетичного матеріалу, наприклад, внаслідок інфекції.
Генна терапія – сукупність генно-інженерних і медичних методів, скерованих на внесення змін в генетичний апарат соматичних клітин людини з метою лікування захворювань. За допомогою генної терапії можна виправляти: Соматичні мутацій Зміни, зумовлені появою чужорідного генетичного матеріалу, наприклад, внаслідок інфекції.
 У генній терапії використовують два основних підходи, що відрізняються природою клітин-мішеней: * Фетальна генотерапія, при якій чужорідну ДНК вводять у зиготу або ембріон на ранній стадії розвитку, при цьому очікується, що введений матеріал потрапить в усі клітини реципієнта (і навіть у статеві клітини, забезпечивши тим самим передачу наступному поколінню). Для лікування захворювань людини не використовується !!! * Соматична генотерапія, при якій генетичний матеріал вводять тільки в соматичні клітини, він не передається по спадковості.
У генній терапії використовують два основних підходи, що відрізняються природою клітин-мішеней: * Фетальна генотерапія, при якій чужорідну ДНК вводять у зиготу або ембріон на ранній стадії розвитку, при цьому очікується, що введений матеріал потрапить в усі клітини реципієнта (і навіть у статеві клітини, забезпечивши тим самим передачу наступному поколінню). Для лікування захворювань людини не використовується !!! * Соматична генотерапія, при якій генетичний матеріал вводять тільки в соматичні клітини, він не передається по спадковості.
 Стратегії генної терапії: У тих випадках, коли клітини втратили функцію певного гена і це є причиною хвороби, треба цю функцію відновити – внести в клітину ген, здатний її забезпечити (поповнююча (замісна) терапія) Коли хвороби є наслідком надлишкової активності гена, не властивої нормальній клітині – цю активність треба пригнічувати (інгібіторна терапія) Клітини модифікують так, щоб посилити імунну відповідь організму на появу інфекційного агента або утворення пухлини, або елімінують Стратегії генної терапії не передбачають використання генеративних клітин і тому генетичні зміни, що виникли як результат генної терапії, НЕ ПЕРЕДАЮТЬСЯ НАЩАДКАМ
Стратегії генної терапії: У тих випадках, коли клітини втратили функцію певного гена і це є причиною хвороби, треба цю функцію відновити – внести в клітину ген, здатний її забезпечити (поповнююча (замісна) терапія) Коли хвороби є наслідком надлишкової активності гена, не властивої нормальній клітині – цю активність треба пригнічувати (інгібіторна терапія) Клітини модифікують так, щоб посилити імунну відповідь організму на появу інфекційного агента або утворення пухлини, або елімінують Стратегії генної терапії не передбачають використання генеративних клітин і тому генетичні зміни, що виникли як результат генної терапії, НЕ ПЕРЕДАЮТЬСЯ НАЩАДКАМ
 1. Замісна генна терапія в організм поряд з існуючим “хворим” геном вводять додатковий “здоровий” ген , який збільшує кількість недостатнього продукту. При такому способі відбувається нецілеспрямоване введення гена метод генетичної корекції: забирається хворий ген або більша його частина і замінюється здоровим. Такі процедури здійснюються щляхом таргетинга – або метода введення генів в строго визначений тип клітин, визначене місце геному із забезпеченням їх експресії. Недолік – низька ефективність гомологічної рекомбінації. Застосовується для лікування моногенних захворювань
1. Замісна генна терапія в організм поряд з існуючим “хворим” геном вводять додатковий “здоровий” ген , який збільшує кількість недостатнього продукту. При такому способі відбувається нецілеспрямоване введення гена метод генетичної корекції: забирається хворий ген або більша його частина і замінюється здоровим. Такі процедури здійснюються щляхом таргетинга – або метода введення генів в строго визначений тип клітин, визначене місце геному із забезпеченням їх експресії. Недолік – низька ефективність гомологічної рекомбінації. Застосовується для лікування моногенних захворювань
 2. Інгібіторна терапія Лікування захворювань, зумовлених надмірною функцією гена. В цій стратегії виділяють основні підходи: внутрішньоклітинна імунізація (застосування внутрішньоклітинних одноланцюгових антитіл – SFv); застосування антизмістовних РНК; застосування рибозимів; застосування антисенс-олігонуклеотидів (проти будь-якої РНК –вірусної, онкогенної, мутантної і т.д.) . РНК-інтерференція (РНКі); домінант-негативні протеїни; РНК-капкани.
2. Інгібіторна терапія Лікування захворювань, зумовлених надмірною функцією гена. В цій стратегії виділяють основні підходи: внутрішньоклітинна імунізація (застосування внутрішньоклітинних одноланцюгових антитіл – SFv); застосування антизмістовних РНК; застосування рибозимів; застосування антисенс-олігонуклеотидів (проти будь-якої РНК –вірусної, онкогенної, мутантної і т.д.) . РНК-інтерференція (РНКі); домінант-негативні протеїни; РНК-капкани.
 Внутрішньоклітинна імунізація Введення в клітини експресуючих конструкцій, продукти яких взаємодіють з продуктами експресії небажаного гена та нейтралізують їх шкідливий ефект (введення генів, які програмують синтез антитіл до небажаного білка). Такі антитіла називаються “інтрабоді” (intra-body). Домінант-негативні протеїни Вводиться ген (або викликається мутація в гені), що експресує мутантну одну з субодиниць олігомерного протеїну. Такий домінант-негативний протеїн, взаємодіючи з нормальними субодиницями протеїну, утворює функціонально неактивний комплекс.
Внутрішньоклітинна імунізація Введення в клітини експресуючих конструкцій, продукти яких взаємодіють з продуктами експресії небажаного гена та нейтралізують їх шкідливий ефект (введення генів, які програмують синтез антитіл до небажаного білка). Такі антитіла називаються “інтрабоді” (intra-body). Домінант-негативні протеїни Вводиться ген (або викликається мутація в гені), що експресує мутантну одну з субодиниць олігомерного протеїну. Такий домінант-негативний протеїн, взаємодіючи з нормальними субодиницями протеїну, утворює функціонально неактивний комплекс.
 Застосування рибозимів Рибозими (каталітичні РНК)– ферменти рибонуклеїнової природи, які розщеплюють РНК. Сучасні методи дозволяють отримувати рибозими, які специфічно будуть розщеплювати задану мРНК. В 2009 р. опубліковано результати клінічних випробувань лікування ВІЛ-інфекції методом генної терапії на 74 добровольцях. В стовбурові клітини ВІЛ-інфікованих вбудовували ген, що кодує синтез “каталітичної РНК” (рибозиму – OZ). Передбачалось, що оснащені рибозимом стовбурові клітини дадуть початок новому поколінню гемопоетичних клітин, які будуть невразливі до ВІЛ-інфекції. “Каталітична РНК” цих клітин буде розщеплювати РНК ВІЛ. Протягом 100 тижнів у пацієнтів знижувалось вірусне навантаження та зростало число CD4-лімфоцитів – клітин, основних мішеней вірусу імунодефіциту. Однак з часом число генетично модифікованих клітин у крові пацієнтів зменшувалось (до 7%). Генна терапія не викликала у хворих побічних ефектів.
Застосування рибозимів Рибозими (каталітичні РНК)– ферменти рибонуклеїнової природи, які розщеплюють РНК. Сучасні методи дозволяють отримувати рибозими, які специфічно будуть розщеплювати задану мРНК. В 2009 р. опубліковано результати клінічних випробувань лікування ВІЛ-інфекції методом генної терапії на 74 добровольцях. В стовбурові клітини ВІЛ-інфікованих вбудовували ген, що кодує синтез “каталітичної РНК” (рибозиму – OZ). Передбачалось, що оснащені рибозимом стовбурові клітини дадуть початок новому поколінню гемопоетичних клітин, які будуть невразливі до ВІЛ-інфекції. “Каталітична РНК” цих клітин буде розщеплювати РНК ВІЛ. Протягом 100 тижнів у пацієнтів знижувалось вірусне навантаження та зростало число CD4-лімфоцитів – клітин, основних мішеней вірусу імунодефіциту. Однак з часом число генетично модифікованих клітин у крові пацієнтів зменшувалось (до 7%). Генна терапія не викликала у хворих побічних ефектів.
 Антисенс-олігонуклеотиди Олігонуклеотид проникає в клітину і зв’язується з мРНК, в результаті чого трансляція специфічно інгібується. Можливе інгібування будь-якої РНК – вірусної, онкогенної, мутантної і т.д.) . Недоліки: Постійне введення олігонуклеотида для досягнення ефекту. Погане проникнення через плазматичну мембрану. Недостатня стабільність. Неспецифічне зв’язування.
Антисенс-олігонуклеотиди Олігонуклеотид проникає в клітину і зв’язується з мРНК, в результаті чого трансляція специфічно інгібується. Можливе інгібування будь-якої РНК – вірусної, онкогенної, мутантної і т.д.) . Недоліки: Постійне введення олігонуклеотида для досягнення ефекту. Погане проникнення через плазматичну мембрану. Недостатня стабільність. Неспецифічне зв’язування.
 РНК-інтерференція Малі інтерферуючі РНК (міРНК – siRNA) є дволанцюговими РНК послідовностями, що містять приблизно 22 пари основ у довжину, зв’язуються з клітинними РНК по специфічних послідовностях та розщеплюють їх по центрах комплементарних ділянок. РНК-капкани блокування зворотної транскрипції. Молекули малих РНК містять незамінні цис-взаємодіючі елементи, які зв’язують транс-взаємодіючі протеїни. Тому транс-взаємодіючі протеїни не звязуються з їх справжніми мішенями-послідовностями. При значному рівні експресії їх може бути цілком достатньо для цис-взаємодіючих послідовностей віруса, які є абсолютно необхідними для реплікації віруса.
РНК-інтерференція Малі інтерферуючі РНК (міРНК – siRNA) є дволанцюговими РНК послідовностями, що містять приблизно 22 пари основ у довжину, зв’язуються з клітинними РНК по специфічних послідовностях та розщеплюють їх по центрах комплементарних ділянок. РНК-капкани блокування зворотної транскрипції. Молекули малих РНК містять незамінні цис-взаємодіючі елементи, які зв’язують транс-взаємодіючі протеїни. Тому транс-взаємодіючі протеїни не звязуються з їх справжніми мішенями-послідовностями. При значному рівні експресії їх може бути цілком достатньо для цис-взаємодіючих послідовностей віруса, які є абсолютно необхідними для реплікації віруса.
 3. Елімінація певних клітин Знищення певної популяції клітин, наприклад, трансформованих. Стратегія включає: утворення в клітині токсичного продукту; експресія ензиму, що перетворює нетоксичний лікарський засіб у токсичний продукт; специфічне мічення клітин для їх елімінації імунною системою; модифікація геному клітин імунної системи з метою більш ефективного впізнання і знищення небезпечних клітин.
3. Елімінація певних клітин Знищення певної популяції клітин, наприклад, трансформованих. Стратегія включає: утворення в клітині токсичного продукту; експресія ензиму, що перетворює нетоксичний лікарський засіб у токсичний продукт; специфічне мічення клітин для їх елімінації імунною системою; модифікація геному клітин імунної системи з метою більш ефективного впізнання і знищення небезпечних клітин.
 Введення генів в клітини Трансфекція (в широкому розумінні) та трансдукція (при використанні вірусних векторів). Трансфекція може проводитися з використанням: чистої (“голої” – naked) ДНК, яка вбудована у відповідну плазміду; комплексованої ДНК (плазмідна ДНК, поєднана з солями, білками (трансферин), органічним полімерами (DEAE-декстран, полілізин, ліпосоми, частинки золота); ДНК в складі вірусних частинок, попередньо позбавлених здатності до реплікації. Методи введення генів: фізичні, хімічні, біологічні.
Введення генів в клітини Трансфекція (в широкому розумінні) та трансдукція (при використанні вірусних векторів). Трансфекція може проводитися з використанням: чистої (“голої” – naked) ДНК, яка вбудована у відповідну плазміду; комплексованої ДНК (плазмідна ДНК, поєднана з солями, білками (трансферин), органічним полімерами (DEAE-декстран, полілізин, ліпосоми, частинки золота); ДНК в складі вірусних частинок, попередньо позбавлених здатності до реплікації. Методи введення генів: фізичні, хімічні, біологічні.
 1. Фізичні методи перенесення генів (пряма ін’єкція гена в тканину, ін’єкція струменем, електропорація, аерозольне введення, біолістика, перенесення з допомогою ліпосом, заморожування-відтаювання) недоліки переваги Ці методи вважають найменш ефективними, оскільки лізосоми розщеплюють чужорідну ДНК і лише в деяких клітинах потрібні генетичні конструкції вбудовуються в геном.
1. Фізичні методи перенесення генів (пряма ін’єкція гена в тканину, ін’єкція струменем, електропорація, аерозольне введення, біолістика, перенесення з допомогою ліпосом, заморожування-відтаювання) недоліки переваги Ці методи вважають найменш ефективними, оскільки лізосоми розщеплюють чужорідну ДНК і лише в деяких клітинах потрібні генетичні конструкції вбудовуються в геном.
 2. Хімічні методи введення генів (кальцій-фосфатна преципітація, декстрановий метод). Обробка хімічними сполуками сприяє полегшеному проникненню ДНК в клітини шляхом ендоцитозу.
2. Хімічні методи введення генів (кальцій-фосфатна преципітація, декстрановий метод). Обробка хімічними сполуками сприяє полегшеному проникненню ДНК в клітини шляхом ендоцитозу.
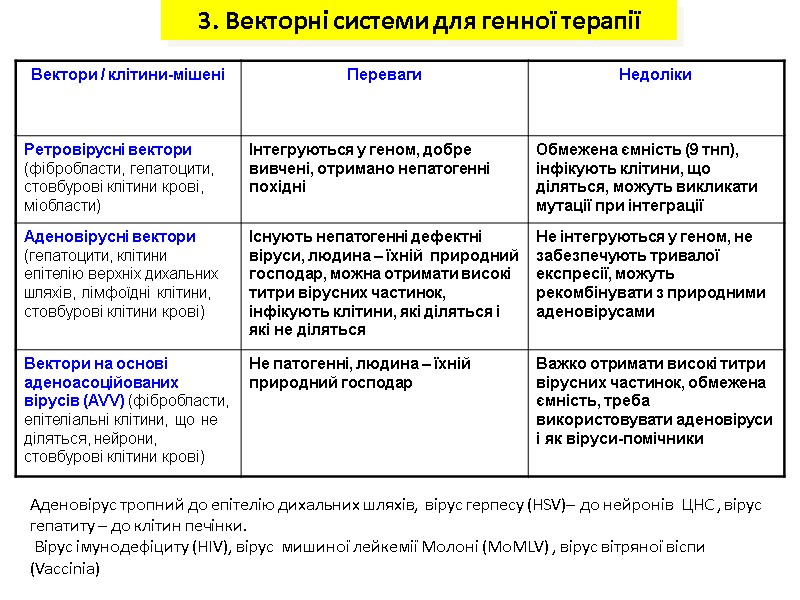
 3. Векторні системи для генної терапії Аденовірус тропний до епітелію дихальних шляхів, вірус герпесу (HSV)– до нейронів ЦНС , вірус гепатиту – до клітин печінки. Вірус імунодефіциту (HIV), вірус мишиної лейкемії Молоні (MoMLV) , вірус вітряної віспи (Vaccinia)
3. Векторні системи для генної терапії Аденовірус тропний до епітелію дихальних шляхів, вірус герпесу (HSV)– до нейронів ЦНС , вірус гепатиту – до клітин печінки. Вірус імунодефіциту (HIV), вірус мишиної лейкемії Молоні (MoMLV) , вірус вітряної віспи (Vaccinia)
 Інші біологічні методи трансфекції (невірусної природи): Ліпофекція - використання ліпосом, які мають виражені фузогенні властивості. При застосуванні ліпосом досягається ефективний внутрішньоклітинний транспорт і захист від деградації лізосомальними ферментами. Рецепторопосередкований траспорт - поєднання біологічних (напр., аденовірусів) та фізико-хімічних підходів. ДНК вводять в комплекс з полікатіоном (напр., полілізином), лігандом для зв’язування з клітиною і ендоцитозу (таким лігандом може бути антитіло, специфічне до якогось поверхневого білку клітини) і спеціальним агентом, який полегшує вивільнення ДНК з цьог о комплексу і ендосом в цитоплазмі. Такими агентами можуть бути реплікаційно-дефектні аденовірусні частинки, які включаються в комплекс. Ліганд визначає клітинну специфічність доставки ДНК. Системи невірусної доставки мають недоліки: низька ефективність і небезпека їх використання.
Інші біологічні методи трансфекції (невірусної природи): Ліпофекція - використання ліпосом, які мають виражені фузогенні властивості. При застосуванні ліпосом досягається ефективний внутрішньоклітинний транспорт і захист від деградації лізосомальними ферментами. Рецепторопосередкований траспорт - поєднання біологічних (напр., аденовірусів) та фізико-хімічних підходів. ДНК вводять в комплекс з полікатіоном (напр., полілізином), лігандом для зв’язування з клітиною і ендоцитозу (таким лігандом може бути антитіло, специфічне до якогось поверхневого білку клітини) і спеціальним агентом, який полегшує вивільнення ДНК з цьог о комплексу і ендосом в цитоплазмі. Такими агентами можуть бути реплікаційно-дефектні аденовірусні частинки, які включаються в комплекс. Ліганд визначає клітинну специфічність доставки ДНК. Системи невірусної доставки мають недоліки: низька ефективність і небезпека їх використання.
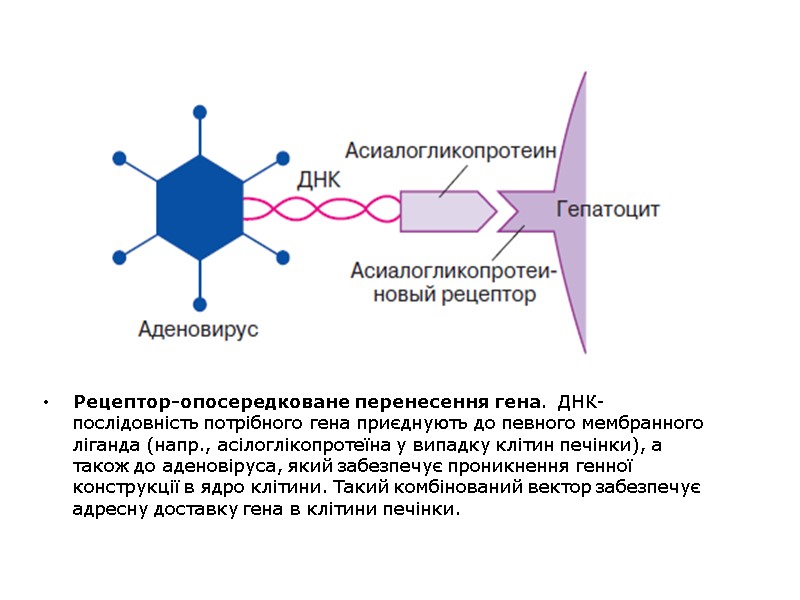
 Рецептор-опосередковане перенесення гена. ДНК-послідовність потрібного гена приєднують до певного мембранного ліганда (напр., асілоглікопротеїна у випадку клітин печінки), а також до аденовіруса, який забезпечує проникнення генної конструкції в ядро клітини. Такий комбінований вектор забезпечує адресну доставку гена в клітини печінки.
Рецептор-опосередковане перенесення гена. ДНК-послідовність потрібного гена приєднують до певного мембранного ліганда (напр., асілоглікопротеїна у випадку клітин печінки), а також до аденовіруса, який забезпечує проникнення генної конструкції в ядро клітини. Такий комбінований вектор забезпечує адресну доставку гена в клітини печінки.
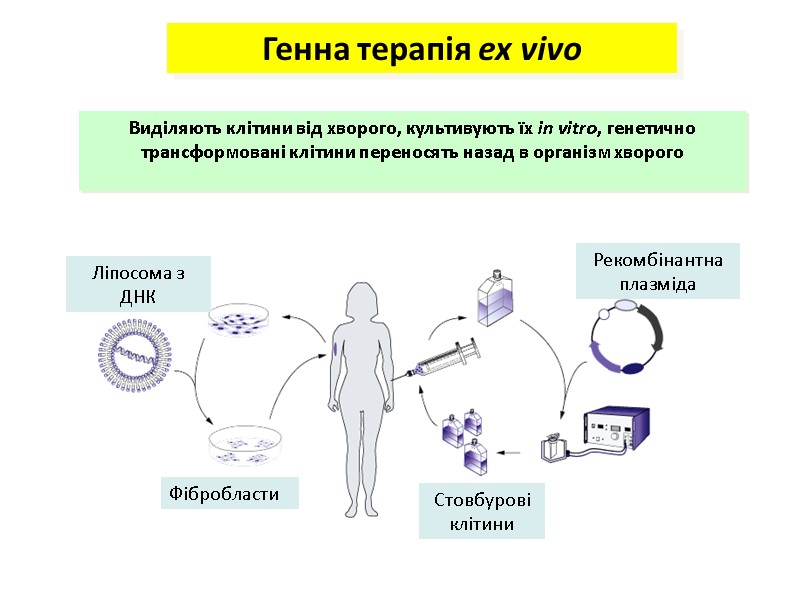
 Генна терапія ex vivo Виділяють клітини від хворого, культивують їх in vitro, генетично трансформовані клітини переносять назад в організм хворого
Генна терапія ex vivo Виділяють клітини від хворого, культивують їх in vitro, генетично трансформовані клітини переносять назад в організм хворого
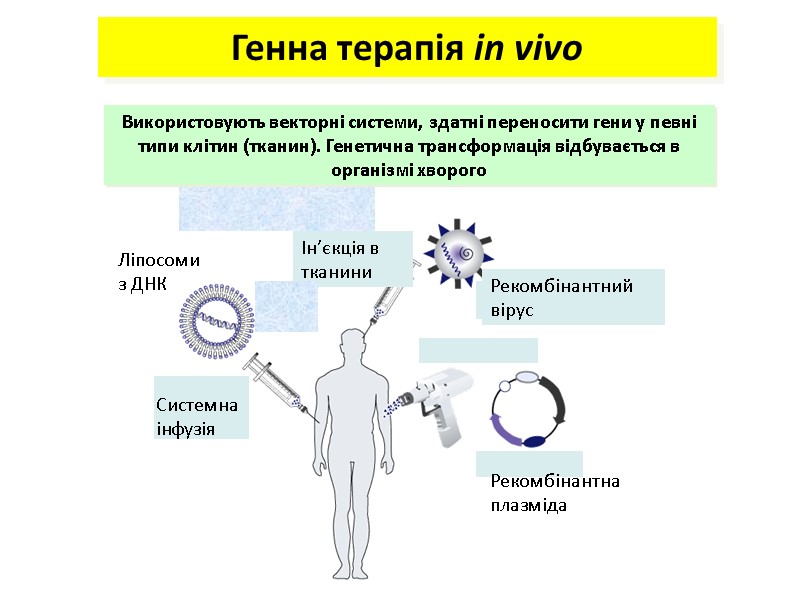
 Використовують векторні системи, здатні переносити гени у певні типи клітин (тканин). Генетична трансформація відбувається в організмі хворого Генна терапія in vivo
Використовують векторні системи, здатні переносити гени у певні типи клітин (тканин). Генетична трансформація відбувається в організмі хворого Генна терапія in vivo
 Захворювання, для яких розроблені технології генної терапії
Захворювання, для яких розроблені технології генної терапії
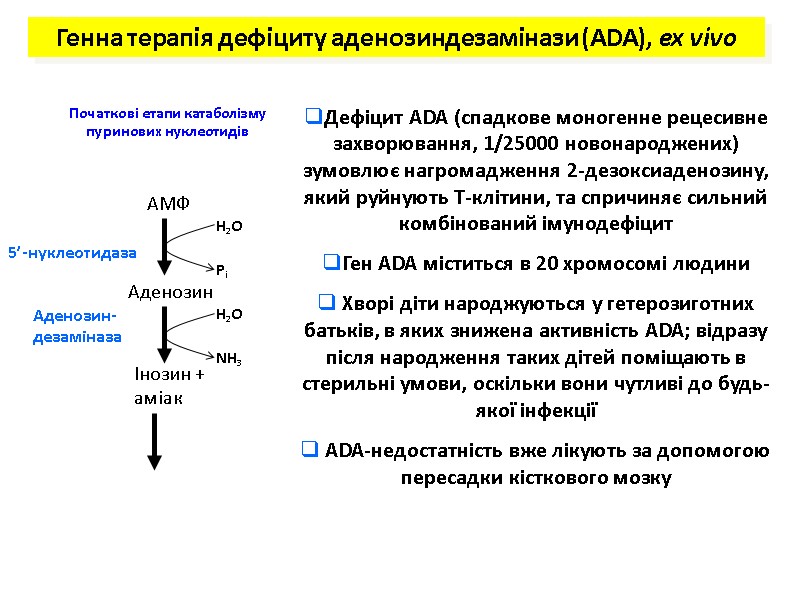
 Початкові етапи катаболізму пуринових нуклеотидів Генна терапія дефіциту аденозиндезамінази (ADA), ex vivo Дефіцит ADA (спадкове моногенне рецесивне захворювання, 1/25000 новонароджених) зумовлює нагромадження 2-дезоксиаденозину, який руйнують Т-клітини, та спричиняє сильний комбінований імунодефіцит Ген ADA міститься в 20 хромосомі людини Хворі діти народжуються у гетерозиготних батьків, в яких знижена активність ADA; відразу після народження таких дітей поміщають в стерильні умови, оскільки вони чутливі до будь-якої інфекції ADA-недостатність вже лікують за допомогою пересадки кісткового мозку
Початкові етапи катаболізму пуринових нуклеотидів Генна терапія дефіциту аденозиндезамінази (ADA), ex vivo Дефіцит ADA (спадкове моногенне рецесивне захворювання, 1/25000 новонароджених) зумовлює нагромадження 2-дезоксиаденозину, який руйнують Т-клітини, та спричиняє сильний комбінований імунодефіцит Ген ADA міститься в 20 хромосомі людини Хворі діти народжуються у гетерозиготних батьків, в яких знижена активність ADA; відразу після народження таких дітей поміщають в стерильні умови, оскільки вони чутливі до будь-якої інфекції ADA-недостатність вже лікують за допомогою пересадки кісткового мозку
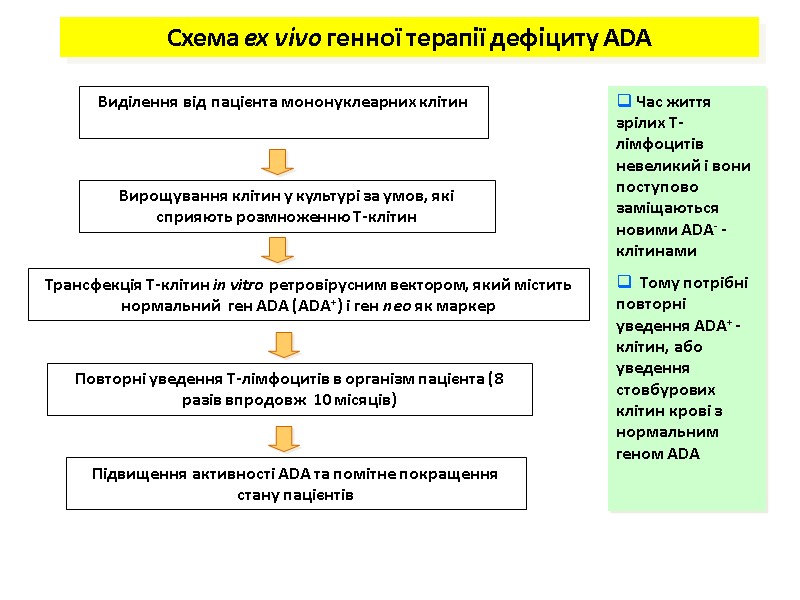
 Виділення від пацієнта мононуклеарних клітин Вирощування клітин у культурі за умов, які сприяють розмноженню Т-клітин Повторні уведення Т-лімфоцитів в організм пацієнта (8 разів впродовж 10 місяців) Підвищення активності ADA та помітне покращення стану пацієнтів Трансфекція Т-клітин in vitro ретровірусним вектором, який містить нормальний ген ADA (ADA+) і ген neo як маркер Схема ex vivo генної терапії дефіциту ADA Час життя зрілих Т-лімфоцитів невеликий і вони поступово заміщаються новими ADA- - клітинами Тому потрібні повторні уведення ADA+ - клітин, або уведення стовбурових клітин крові з нормальним геном ADA
Виділення від пацієнта мононуклеарних клітин Вирощування клітин у культурі за умов, які сприяють розмноженню Т-клітин Повторні уведення Т-лімфоцитів в організм пацієнта (8 разів впродовж 10 місяців) Підвищення активності ADA та помітне покращення стану пацієнтів Трансфекція Т-клітин in vitro ретровірусним вектором, який містить нормальний ген ADA (ADA+) і ген neo як маркер Схема ex vivo генної терапії дефіциту ADA Час життя зрілих Т-лімфоцитів невеликий і вони поступово заміщаються новими ADA- - клітинами Тому потрібні повторні уведення ADA+ - клітин, або уведення стовбурових клітин крові з нормальним геном ADA
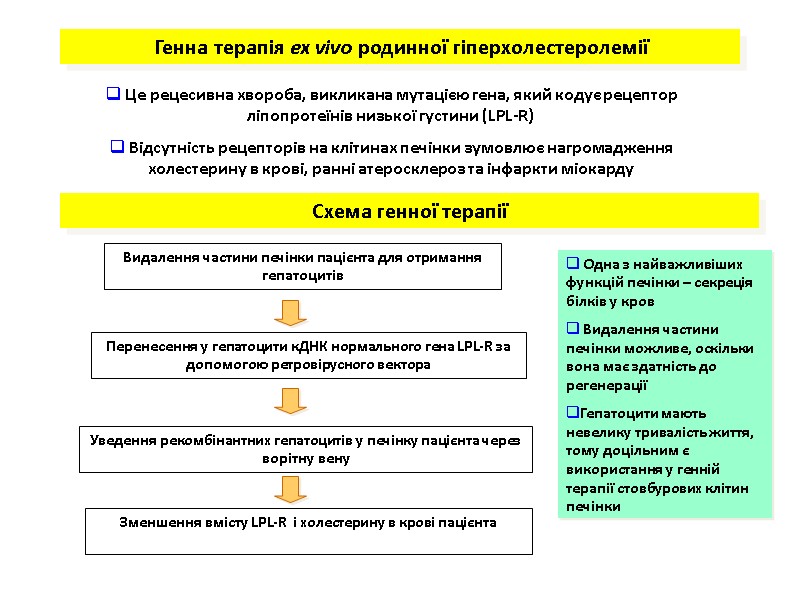
 Генна терапія ex vivo родинної гіперхолестеролемії Це рецесивна хвороба, викликана мутацією гена, який кодує рецептор ліпопротеїнів низької густини (LPL-R) Відсутність рецепторів на клітинах печінки зумовлює нагромадження холестерину в крові, ранні атеросклероз та інфаркти міокарду Видалення частини печінки пацієнта для отримання гепатоцитів Перенесення у гепатоцити кДНК нормального гена LPL-R за допомогою ретровірусного вектора Уведення рекомбінантних гепатоцитів у печінку пацієнта через ворітну вену Зменшення вмісту LPL-R і холестерину в крові пацієнта Схема генної терапії Одна з найважливіших функцій печінки – секреція білків у кров Видалення частини печінки можливе, оскільки вона має здатність до регенерації Гепатоцити мають невелику тривалість життя, тому доцільним є використання у генній терапії стовбурових клітин печінки
Генна терапія ex vivo родинної гіперхолестеролемії Це рецесивна хвороба, викликана мутацією гена, який кодує рецептор ліпопротеїнів низької густини (LPL-R) Відсутність рецепторів на клітинах печінки зумовлює нагромадження холестерину в крові, ранні атеросклероз та інфаркти міокарду Видалення частини печінки пацієнта для отримання гепатоцитів Перенесення у гепатоцити кДНК нормального гена LPL-R за допомогою ретровірусного вектора Уведення рекомбінантних гепатоцитів у печінку пацієнта через ворітну вену Зменшення вмісту LPL-R і холестерину в крові пацієнта Схема генної терапії Одна з найважливіших функцій печінки – секреція білків у кров Видалення частини печінки можливе, оскільки вона має здатність до регенерації Гепатоцити мають невелику тривалість життя, тому доцільним є використання у генній терапії стовбурових клітин печінки
 Муковісцидоз – аутосомно-рецесивне захворювання, зумовлене мутаціями в гені CFTR, який кодує трансмембранний білок хлоридного каналу Ген CFTR локалізований в середині довгого плеча 7-ї хромосоми. В Європі частота захворювання становить 1:2000, 1:2500 новонароджених. Частота гетерозигот за геном CFTR ≈ 2 – 5% Хворі в країнах Зах. Європи доживають до 40 років. Лікування: Симптоматичне (включає ферментотерапію – спрямовану на корекцію порушень екзокринних залоз) Антибіотикотерапія (респіраторних інфекцій) Дієтотерапія, фізіотерапія і т.д. Приклади генної терапії in vivo
Муковісцидоз – аутосомно-рецесивне захворювання, зумовлене мутаціями в гені CFTR, який кодує трансмембранний білок хлоридного каналу Ген CFTR локалізований в середині довгого плеча 7-ї хромосоми. В Європі частота захворювання становить 1:2000, 1:2500 новонароджених. Частота гетерозигот за геном CFTR ≈ 2 – 5% Хворі в країнах Зах. Європи доживають до 40 років. Лікування: Симптоматичне (включає ферментотерапію – спрямовану на корекцію порушень екзокринних залоз) Антибіотикотерапія (респіраторних інфекцій) Дієтотерапія, фізіотерапія і т.д. Приклади генної терапії in vivo
 Аденовірусним вектором з нормальним геном CFTR інфікують клітини епітелію носової порожнини хворого Показано, що 5%-й рівень нормальної експресії гена CFTR, призводить до виправлення на 50% транспорту іонів. Схема in vivo генної терапії муковісцидозу
Аденовірусним вектором з нормальним геном CFTR інфікують клітини епітелію носової порожнини хворого Показано, що 5%-й рівень нормальної експресії гена CFTR, призводить до виправлення на 50% транспорту іонів. Схема in vivo генної терапії муковісцидозу
 Приклади генної терапії in vivo Гемофілія В зумовлена недостатністю фактора IX, який виділяють у кров клітини печінки Рекомбінантні молекули з кДНК гена фактора ІХ, сконструйовану на основі аденовірусного вектора, уводять в печінку через ворітну вену Аденовіруси здатні інфікувати гепатоцити (немає потреби проводити гепатектомію) Спостерігається зростання концентрації фактора ІХ в крові та нормальне зсідання крові
Приклади генної терапії in vivo Гемофілія В зумовлена недостатністю фактора IX, який виділяють у кров клітини печінки Рекомбінантні молекули з кДНК гена фактора ІХ, сконструйовану на основі аденовірусного вектора, уводять в печінку через ворітну вену Аденовіруси здатні інфікувати гепатоцити (немає потреби проводити гепатектомію) Спостерігається зростання концентрації фактора ІХ в крові та нормальне зсідання крові
 М’язева дистрофія Дюшена зумовлена мутаціями гена дистрофіну. Для нормального функціонування м’язів, принаймні, 10% міобластів повинні нести нормальний ген дистрофіну Аденовіруси здатні інфікувати міобласти В аденовірусний вектор клонують вкорочений, але функціональний ген дистрофіну- мініген (повний ген занадто великий для такого вектора) та вводять його у міобласти Від 5 до 50% таких міобластів експресували мінідистрофін Приклади генної терапії in vivo
М’язева дистрофія Дюшена зумовлена мутаціями гена дистрофіну. Для нормального функціонування м’язів, принаймні, 10% міобластів повинні нести нормальний ген дистрофіну Аденовіруси здатні інфікувати міобласти В аденовірусний вектор клонують вкорочений, але функціональний ген дистрофіну- мініген (повний ген занадто великий для такого вектора) та вводять його у міобласти Від 5 до 50% таких міобластів експресували мінідистрофін Приклади генної терапії in vivo
 Підходи до генної терапії раку збільшення імуногенності пухлинних клітин (шляхом введення генів, які кодують чужий для цих клітин антиген (цитокінових генів, генів ГКГ і т.д)); суїцидна генотерапія (введення в пухлинні клітини генів-убивць, які синтезують продукт, який в певних умов приводить до загибелі ракових клітин); блокування експресії онкогенів з допомогою внутрішньоклітинної імунізації (використання антизмістовних РНК або антитіл до онкобілків); введення генів-супресорів пухлинного росту або інших генів, які сповільнюють проліферацію клітин (гена p53, інтерлейкінів, апоптозу, інгібіторів росту); технологія “мовчазних” генів (сайленсинг генів); введення в здорові клітини (напр., клітини кісткового мозку) генів, які забезпечують стійкість до протипухлинних засобів, для проведення більш активної хіміотерапії.
Підходи до генної терапії раку збільшення імуногенності пухлинних клітин (шляхом введення генів, які кодують чужий для цих клітин антиген (цитокінових генів, генів ГКГ і т.д)); суїцидна генотерапія (введення в пухлинні клітини генів-убивць, які синтезують продукт, який в певних умов приводить до загибелі ракових клітин); блокування експресії онкогенів з допомогою внутрішньоклітинної імунізації (використання антизмістовних РНК або антитіл до онкобілків); введення генів-супресорів пухлинного росту або інших генів, які сповільнюють проліферацію клітин (гена p53, інтерлейкінів, апоптозу, інгібіторів росту); технологія “мовчазних” генів (сайленсинг генів); введення в здорові клітини (напр., клітини кісткового мозку) генів, які забезпечують стійкість до протипухлинних засобів, для проведення більш активної хіміотерапії.
 Для досягнення позитивного ефекту необхідно вводити генотерапевтичний вектор безпосередньо всередину пухлини. Злоякісні пухлини містять як ракові клітини, так і здорові клітини, що перешкоджає вірусному інфікуванню всіх ракових клітин. Повноцінному функціонуванню і розмноженню вірусів в пухлинах перешкоджає гіпоксія. Обмеження генної терапії раку:
Для досягнення позитивного ефекту необхідно вводити генотерапевтичний вектор безпосередньо всередину пухлини. Злоякісні пухлини містять як ракові клітини, так і здорові клітини, що перешкоджає вірусному інфікуванню всіх ракових клітин. Повноцінному функціонуванню і розмноженню вірусів в пухлинах перешкоджає гіпоксія. Обмеження генної терапії раку:
 Генна терапія проти алкоголізму Чілійським вченим вдалося на 50% знизити вживання алкоголю у щурів з вродженою схильністю до алкоголізму. Етанол етиловий альдегід оцтова кислота 1 – алкогольдегідрогеназа 2 – ацетальдегіддегідрогеназа В сучасному лікуванні використовують препарати, які блокують дію ацетальдегіддегідрогенази. Вчені використали аденовірус з антизмістовним геном ацетальдегіддегідрогенази. Одноразове введення знижувало активність ферменту в печінці щурів на 80%.
Генна терапія проти алкоголізму Чілійським вченим вдалося на 50% знизити вживання алкоголю у щурів з вродженою схильністю до алкоголізму. Етанол етиловий альдегід оцтова кислота 1 – алкогольдегідрогеназа 2 – ацетальдегіддегідрогеназа В сучасному лікуванні використовують препарати, які блокують дію ацетальдегіддегідрогенази. Вчені використали аденовірус з антизмістовним геном ацетальдегіддегідрогенази. Одноразове введення знижувало активність ферменту в печінці щурів на 80%.
 При розробці генотерапії слід враховувати питання: 1) які клітини необхідно використовувати? 2) яку частину клітин необхідно вилікувати, щоб зменшити або зупинити прогресування хвороби? 3) чи буде небезпечна надекспресія введеного гена? 4) чи є безпечним потрапляння реконструйованого гена в інші тканини? 5) як довго буде функціонувати змінена клітина? 6) чи будуть атаковані нові клітини імунною системою?
При розробці генотерапії слід враховувати питання: 1) які клітини необхідно використовувати? 2) яку частину клітин необхідно вилікувати, щоб зменшити або зупинити прогресування хвороби? 3) чи буде небезпечна надекспресія введеного гена? 4) чи є безпечним потрапляння реконструйованого гена в інші тканини? 5) як довго буде функціонувати змінена клітина? 6) чи будуть атаковані нові клітини імунною системою?
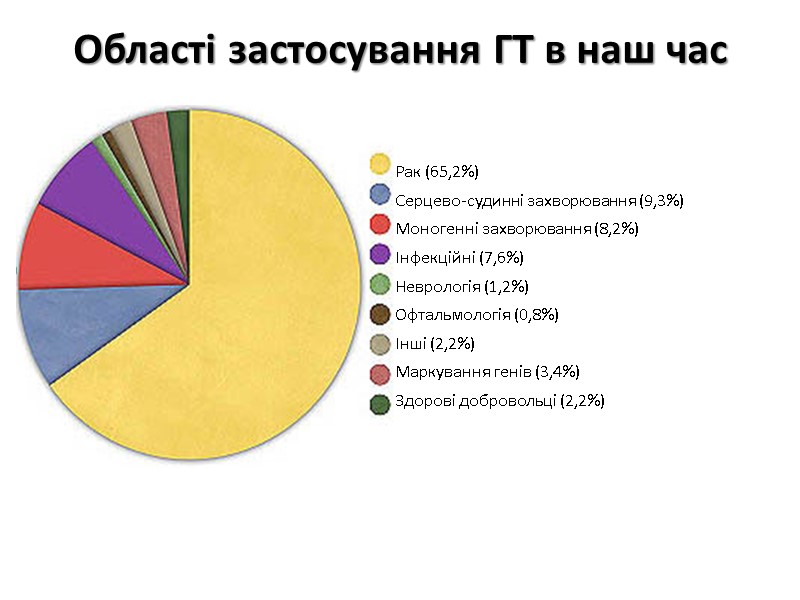
 Області застосування ГТ в наш час Рак (65,2%) Серцево-судинні захворювання (9,3%) Моногенні захворювання (8,2%) Інфекційні (7,6%) Неврологія (1,2%) Офтальмологія (0,8%) Інші (2,2%) Маркування генів (3,4%) Здорові добровольці (2,2%)
Області застосування ГТ в наш час Рак (65,2%) Серцево-судинні захворювання (9,3%) Моногенні захворювання (8,2%) Інфекційні (7,6%) Неврологія (1,2%) Офтальмологія (0,8%) Інші (2,2%) Маркування генів (3,4%) Здорові добровольці (2,2%)
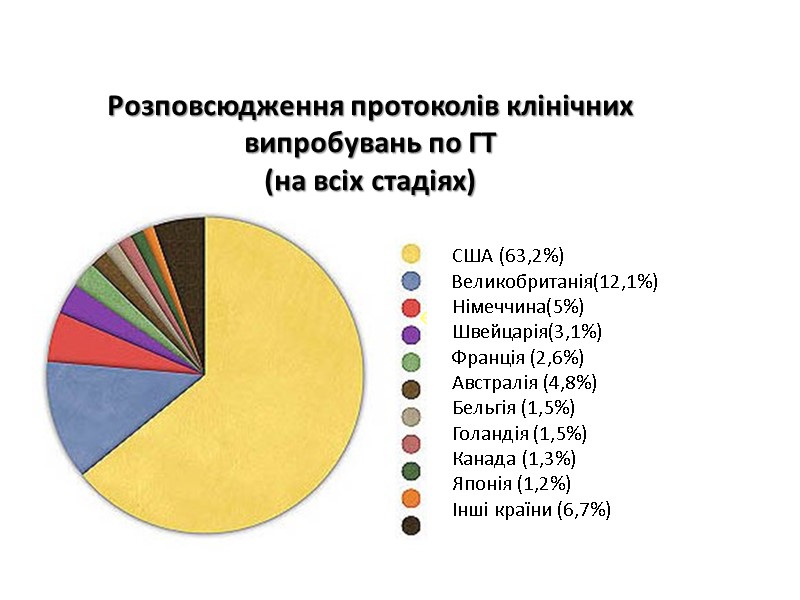
 Розповсюдження протоколів клінічних випробувань по ГТ (на всіх стадіях) США (63,2%) Великобританія(12,1%) Німеччина(5%) Швейцарія(3,1%) Франція (2,6%) Австралія (4,8%) Бельгія (1,5%) Голандія (1,5%) Канада (1,3%) Японія (1,2%) Інші країни (6,7%)
Розповсюдження протоколів клінічних випробувань по ГТ (на всіх стадіях) США (63,2%) Великобританія(12,1%) Німеччина(5%) Швейцарія(3,1%) Франція (2,6%) Австралія (4,8%) Бельгія (1,5%) Голандія (1,5%) Канада (1,3%) Японія (1,2%) Інші країни (6,7%)
 Етичні проблеми генної терапії Правовий захист унікальної генетичної інформації кожної людини Інформація про геном кожної конкретної людини повинна охоронятися Не можна допускати дискримінації людини через її генетичні особливості Правовий статус ембріона людини
Етичні проблеми генної терапії Правовий захист унікальної генетичної інформації кожної людини Інформація про геном кожної конкретної людини повинна охоронятися Не можна допускати дискримінації людини через її генетичні особливості Правовий статус ембріона людини
 Дякую за увагу!
Дякую за увагу!

