Эпигенетика_медики_2014.ppt
- Количество слайдов: 99
 «Генетика предполагает, а эпигенетика располагает» P. Medawar & J. Medawar Эпигенетика Геномный импринтинг Тихонов Андрей Владимирович ФГБУ НИИ акушерства и гинекологии им. Д. О. Отта СЗО РАМН лаборатория пренатальной диагностики наследственных заболеваний человека
«Генетика предполагает, а эпигенетика располагает» P. Medawar & J. Medawar Эпигенетика Геномный импринтинг Тихонов Андрей Владимирович ФГБУ НИИ акушерства и гинекологии им. Д. О. Отта СЗО РАМН лаборатория пренатальной диагностики наследственных заболеваний человека
 Центральная догма молекулярной биологии: ДНК ------- РНК ------- БЕЛОК Генотип -------- Фенотип ДНК ответственна за хранение, передачу и реализацию наследственной информации 2
Центральная догма молекулярной биологии: ДНК ------- РНК ------- БЕЛОК Генотип -------- Фенотип ДНК ответственна за хранение, передачу и реализацию наследственной информации 2
 Доимплантационное развитие человека День 1. Стадия зиготы День 2. Эмбрион в стадии дробления 4 бластомера День 3. Эмбрион на стадии дробления 8 клеток. День 4. Морула. 3 День 5. Бластоциста 3
Доимплантационное развитие человека День 1. Стадия зиготы День 2. Эмбрион в стадии дробления 4 бластомера День 3. Эмбрион на стадии дробления 8 клеток. День 4. Морула. 3 День 5. Бластоциста 3
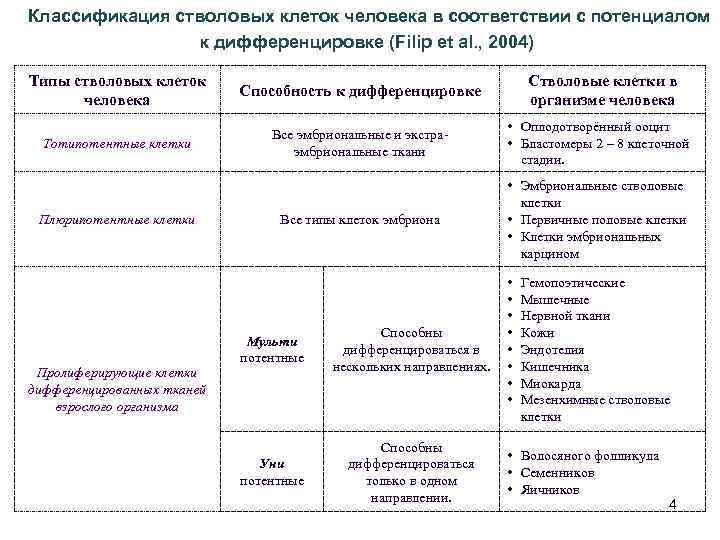 Классификация стволовых клеток человека в соответствии с потенциалом к дифференцировке (Filip et al. , 2004) Типы стволовых клеток человека Способность к дифференцировке Тотипотентные клетки Все эмбриональные и экстраэмбриональные ткани • Оплодотворённый ооцит • Бластомеры 2 – 8 клеточной стадии. Все типы клеток эмбриона • Эмбриональные стволовые клетки • Первичные половые клетки • Клетки эмбриональных карцином Плюрипотентные клетки Пролиферирующие клетки дифференцированных тканей взрослого организма Мульти потентные Способны дифференцироваться в нескольких направлениях. Уни потентные Способны дифференцироваться только в одном направлении. Стволовые клетки в организме человека • • Гемопоэтические Мышечные Нервной ткани Кожи Эндотелия Кишечника Миокарда Мезенхимные стволовые клетки • Волосяного фолликула • Семенников • Яичников 4
Классификация стволовых клеток человека в соответствии с потенциалом к дифференцировке (Filip et al. , 2004) Типы стволовых клеток человека Способность к дифференцировке Тотипотентные клетки Все эмбриональные и экстраэмбриональные ткани • Оплодотворённый ооцит • Бластомеры 2 – 8 клеточной стадии. Все типы клеток эмбриона • Эмбриональные стволовые клетки • Первичные половые клетки • Клетки эмбриональных карцином Плюрипотентные клетки Пролиферирующие клетки дифференцированных тканей взрослого организма Мульти потентные Способны дифференцироваться в нескольких направлениях. Уни потентные Способны дифференцироваться только в одном направлении. Стволовые клетки в организме человека • • Гемопоэтические Мышечные Нервной ткани Кожи Эндотелия Кишечника Миокарда Мезенхимные стволовые клетки • Волосяного фолликула • Семенников • Яичников 4
 Разные судьбы, функции, морфология, «способности» клеток при одинаковом генотипе 5
Разные судьбы, функции, морфология, «способности» клеток при одинаковом генотипе 5
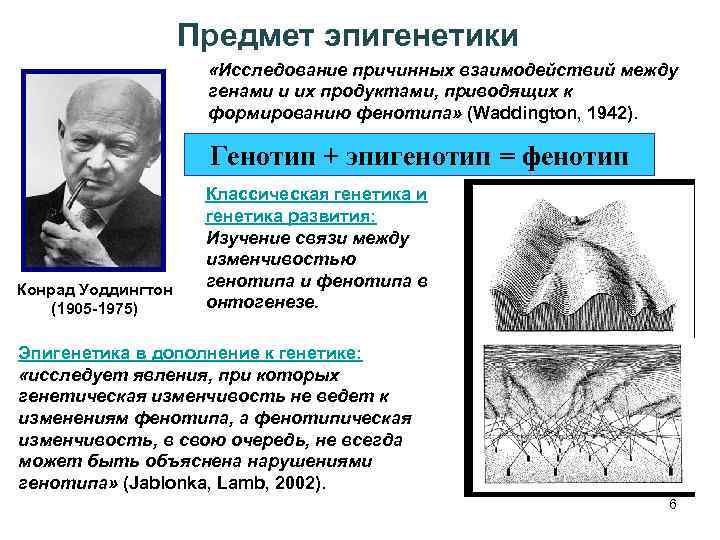 Предмет эпигенетики «Исследование причинных взаимодействий между генами и их продуктами, приводящих к формированию фенотипа» (Waddington, 1942). Генотип + эпигенотип = фенотип Конрад Уоддингтон (1905 -1975) Классическая генетика и генетика развития: Изучение связи между изменчивостью генотипа и фенотипа в онтогенезе. Эпигенетика в дополнение к генетике: «исследует явления, при которых генетическая изменчивость не ведет к изменениям фенотипа, а фенотипическая изменчивость, в свою очередь, не всегда может быть объяснена нарушениями генотипа» (Jablonka, Lamb, 2002). 6
Предмет эпигенетики «Исследование причинных взаимодействий между генами и их продуктами, приводящих к формированию фенотипа» (Waddington, 1942). Генотип + эпигенотип = фенотип Конрад Уоддингтон (1905 -1975) Классическая генетика и генетика развития: Изучение связи между изменчивостью генотипа и фенотипа в онтогенезе. Эпигенетика в дополнение к генетике: «исследует явления, при которых генетическая изменчивость не ведет к изменениям фенотипа, а фенотипическая изменчивость, в свою очередь, не всегда может быть объяснена нарушениями генотипа» (Jablonka, Lamb, 2002). 6
 Эпигенетическое наследование В более общем смысле, предметом эпигенетики являются явления, связанные с развитием различных фенотипов клеток или организмов на основе одного генотипа. В более узком смысле эпигенетика – раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток. Эпигенетическое наследование – это наследование паттерна экспрессии генов. 7
Эпигенетическое наследование В более общем смысле, предметом эпигенетики являются явления, связанные с развитием различных фенотипов клеток или организмов на основе одного генотипа. В более узком смысле эпигенетика – раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток. Эпигенетическое наследование – это наследование паттерна экспрессии генов. 7
 Эпигенетическая регуляция - наследственные и ненаследственные изменения в экспрессии конкретного гена без каких-либо соответствующих структурных изменений в его нуклеотидной последовательности. Эпигенетические явления: • импринтинг, • эффект положения, • особенности структурно-функциональной организации хроматина определенных хромосомных локусов, влияющие на экспрессию генов, • интерференция РНК. 8
Эпигенетическая регуляция - наследственные и ненаследственные изменения в экспрессии конкретного гена без каких-либо соответствующих структурных изменений в его нуклеотидной последовательности. Эпигенетические явления: • импринтинг, • эффект положения, • особенности структурно-функциональной организации хроматина определенных хромосомных локусов, влияющие на экспрессию генов, • интерференция РНК. 8
 ДВА ВИДА ИНФОРМАЦИИ В ГЕНОМЕ Генетическая – закодированная в ДНК программа создания живого организма Эпигенетическая (динамическая) – как, где и когда должна быть реализована генетическая информация. Каждый вид информации обеспечен своими системами: • кодирования • хранения • передачи 9
ДВА ВИДА ИНФОРМАЦИИ В ГЕНОМЕ Генетическая – закодированная в ДНК программа создания живого организма Эпигенетическая (динамическая) – как, где и когда должна быть реализована генетическая информация. Каждый вид информации обеспечен своими системами: • кодирования • хранения • передачи 9
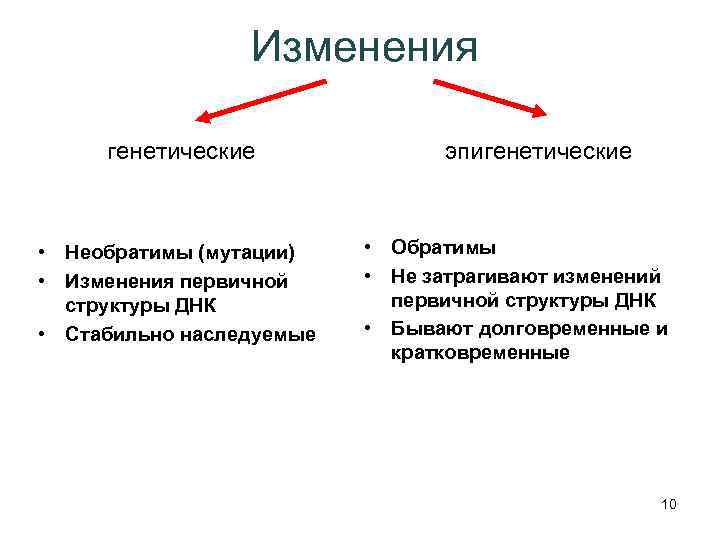 Изменения генетические • Необратимы (мутации) • Изменения первичной структуры ДНК • Стабильно наследуемые эпигенетические • Обратимы • Не затрагивают изменений первичной структуры ДНК • Бывают долговременные и кратковременные 10
Изменения генетические • Необратимы (мутации) • Изменения первичной структуры ДНК • Стабильно наследуемые эпигенетические • Обратимы • Не затрагивают изменений первичной структуры ДНК • Бывают долговременные и кратковременные 10
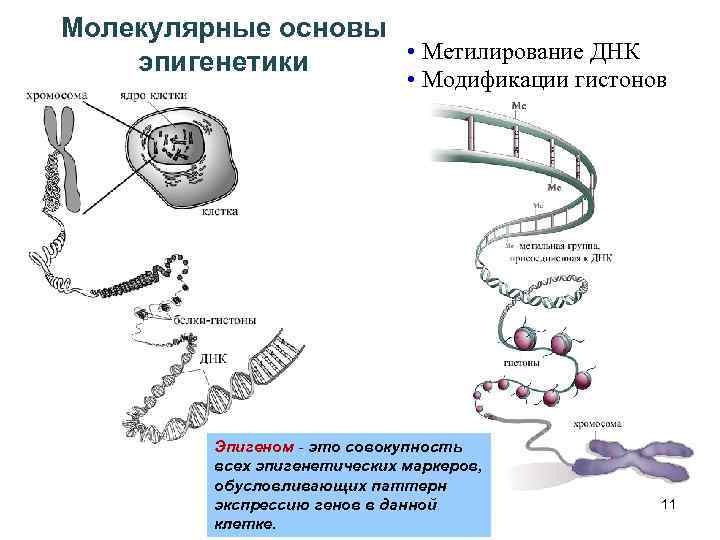 Молекулярные основы • Метилирование ДНК эпигенетики • Модификации гистонов Эпигеном - это совокупность всех эпигенетических маркеров, обусловливающих паттерн экспрессию генов в данной клетке. 11
Молекулярные основы • Метилирование ДНК эпигенетики • Модификации гистонов Эпигеном - это совокупность всех эпигенетических маркеров, обусловливающих паттерн экспрессию генов в данной клетке. 11
 Посттрансляционные модификации гистонов 12
Посттрансляционные модификации гистонов 12
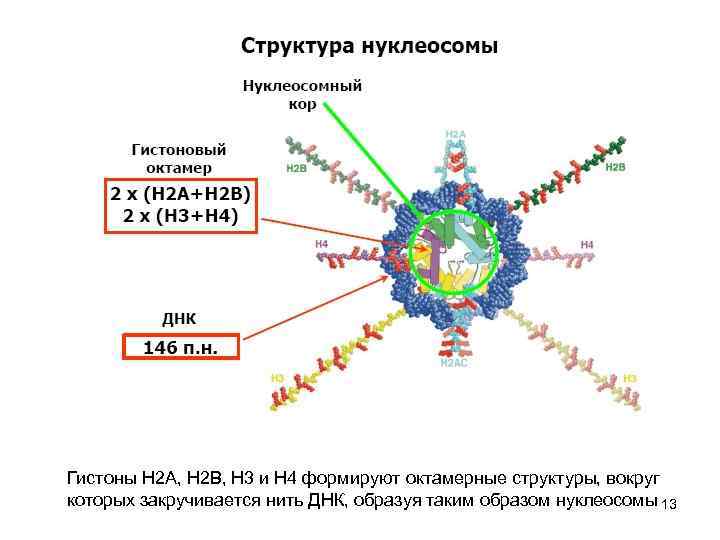 Гистоны Н 2 А, Н 2 В, Н 3 и Н 4 формируют октамерные структуры, вокруг которых закручивается нить ДНК, образуя таким образом нуклеосомы 13
Гистоны Н 2 А, Н 2 В, Н 3 и Н 4 формируют октамерные структуры, вокруг которых закручивается нить ДНК, образуя таким образом нуклеосомы 13
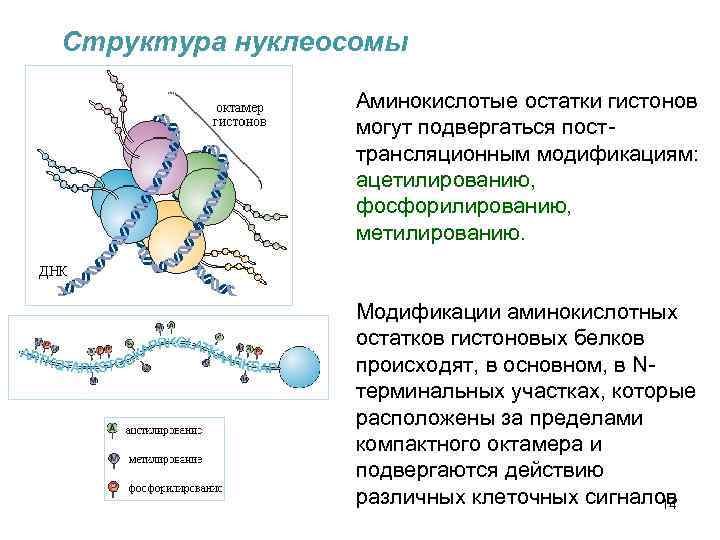 Структура нуклеосомы Аминокислотые остатки гистонов могут подвергаться посттрансляционным модификациям: ацетилированию, фосфорилированию, метилированию. Модификации аминокислотных остатков гистоновых белков происходят, в основном, в Nтерминальных участках, которые расположены за пределами компактного октамера и подвергаются действию различных клеточных сигналов 14
Структура нуклеосомы Аминокислотые остатки гистонов могут подвергаться посттрансляционным модификациям: ацетилированию, фосфорилированию, метилированию. Модификации аминокислотных остатков гистоновых белков происходят, в основном, в Nтерминальных участках, которые расположены за пределами компактного октамера и подвергаются действию различных клеточных сигналов 14
 В зависимости от типа и сайта модификаций аминокислотных остатков, каждая нуклеосома имеет свой «гистоновый код» , регулирующий активность транскрипции 15
В зависимости от типа и сайта модификаций аминокислотных остатков, каждая нуклеосома имеет свой «гистоновый код» , регулирующий активность транскрипции 15
 Ацетилирование и деацетилирование гистонов • ацетилирование связано с активацией транскрипции • белки, осуществляющие ацетилирование - гистоновые ацетилтрансферазы (НАТ); донор ацетильной группы – ацетил ко. А • белки, осуществляющие деацетилирование – гистоновые деацетилазы (HDAC) Модель модификации гистонов: ДНК-связывающиеся активаторы привлекают НАТ для ацетилирования нуклеосомных гистонов, а репрессоры привлекают HDAC для деацетилирования гистонов. Эти события приводят к изменению структуры нуклеосом и активации или репрессии транскрипции соответственно. 16
Ацетилирование и деацетилирование гистонов • ацетилирование связано с активацией транскрипции • белки, осуществляющие ацетилирование - гистоновые ацетилтрансферазы (НАТ); донор ацетильной группы – ацетил ко. А • белки, осуществляющие деацетилирование – гистоновые деацетилазы (HDAC) Модель модификации гистонов: ДНК-связывающиеся активаторы привлекают НАТ для ацетилирования нуклеосомных гистонов, а репрессоры привлекают HDAC для деацетилирования гистонов. Эти события приводят к изменению структуры нуклеосом и активации или репрессии транскрипции соответственно. 16
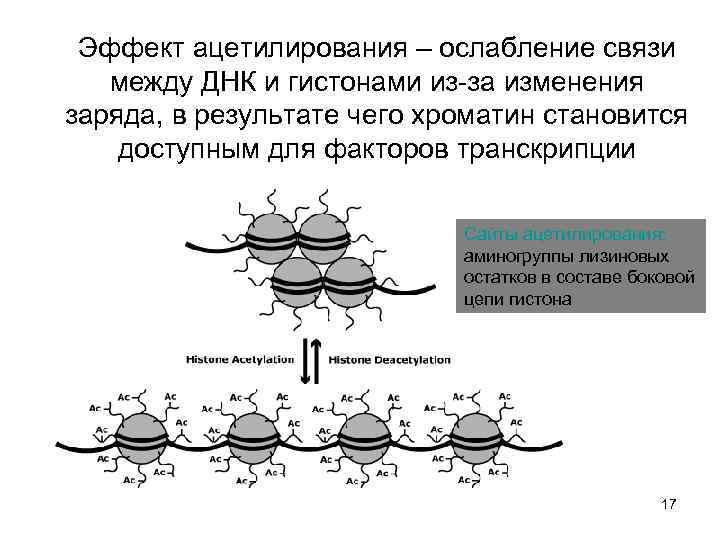 Эффект ацетилирования – ослабление связи между ДНК и гистонами из-за изменения заряда, в результате чего хроматин становится доступным для факторов транскрипции Сайты ацетилирования: аминогруппы лизиновых остатков в составе боковой цепи гистона 17
Эффект ацетилирования – ослабление связи между ДНК и гистонами из-за изменения заряда, в результате чего хроматин становится доступным для факторов транскрипции Сайты ацетилирования: аминогруппы лизиновых остатков в составе боковой цепи гистона 17
 Фосфорилирование и дефосфорилирование гистонов • фосфорилирование связано с активацией транскрипции • белки, осуществляющие фосфорилирование – протеинкиназами; донор фосфата – АТФ • белки, осуществляющие дефосфорилирование – фосфатазы Сайты фосфорилирования: гидроксильные группы серина, треонина и тирозина. В результате фосфорилирования увеличивается негативный заряд. 18
Фосфорилирование и дефосфорилирование гистонов • фосфорилирование связано с активацией транскрипции • белки, осуществляющие фосфорилирование – протеинкиназами; донор фосфата – АТФ • белки, осуществляющие дефосфорилирование – фосфатазы Сайты фосфорилирования: гидроксильные группы серина, треонина и тирозина. В результате фосфорилирования увеличивается негативный заряд. 18
 Метилирование гистонов Метилируются - Лизин (моно-, ди- и триметилирование) - Агринин (моно- и диметилирование) Метилирование не приводит к изменению заряда модифицируемого остатка Эффекты метилирования в зависимости от сайта модификации и количества метильных групп: - Репрессия транскрипции - Активация транскрипции Регуляция транскрипции через молекулы-эффекторы 19
Метилирование гистонов Метилируются - Лизин (моно-, ди- и триметилирование) - Агринин (моно- и диметилирование) Метилирование не приводит к изменению заряда модифицируемого остатка Эффекты метилирования в зависимости от сайта модификации и количества метильных групп: - Репрессия транскрипции - Активация транскрипции Регуляция транскрипции через молекулы-эффекторы 19
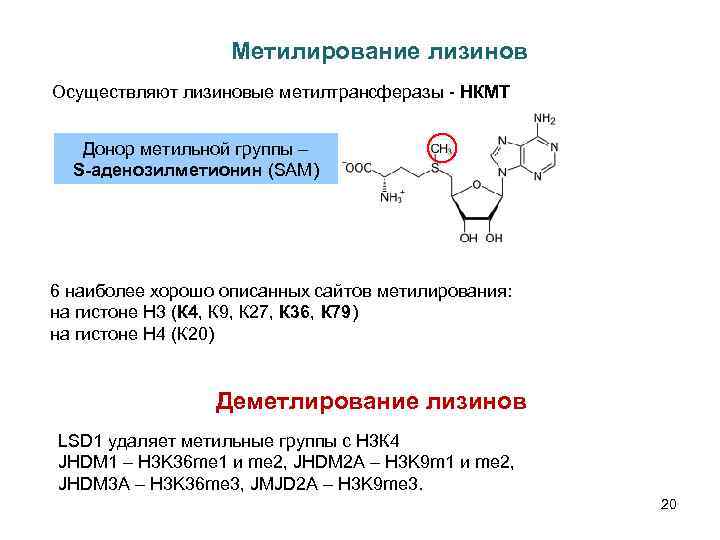 Метилирование лизинов Осуществляют лизиновые метилтрансферазы - НКМТ Донор метильной группы – S-аденозилметионин (SAM) 6 наиболее хорошо описанных сайтов метилирования: на гистоне Н 3 (К 4, К 9, К 27, К 36, К 79) на гистоне Н 4 (К 20) Деметлирование лизинов LSD 1 удаляет метильные группы с Н 3 К 4 JHDM 1 – H 3 K 36 me 1 и me 2, JHDM 2 A – H 3 K 9 m 1 и me 2, JHDM 3 A – H 3 K 36 me 3, JMJD 2 A – H 3 K 9 me 3. 20
Метилирование лизинов Осуществляют лизиновые метилтрансферазы - НКМТ Донор метильной группы – S-аденозилметионин (SAM) 6 наиболее хорошо описанных сайтов метилирования: на гистоне Н 3 (К 4, К 9, К 27, К 36, К 79) на гистоне Н 4 (К 20) Деметлирование лизинов LSD 1 удаляет метильные группы с Н 3 К 4 JHDM 1 – H 3 K 36 me 1 и me 2, JHDM 2 A – H 3 K 9 m 1 и me 2, JHDM 3 A – H 3 K 36 me 3, JMJD 2 A – H 3 K 9 me 3. 20
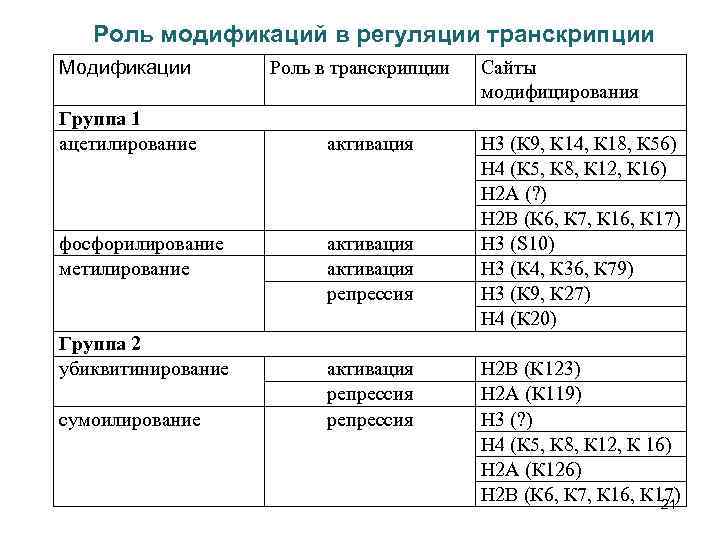 Роль модификаций в регуляции транскрипции Модификации Группа 1 ацетилирование фосфорилирование метилирование Группа 2 убиквитинирование сумоилирование Роль в транскрипции активация репрессия Сайты модифицирования Н 3 (К 9, К 14, К 18, К 56) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (? ) Н 2 В (К 6, К 7, К 16, К 17) Н 3 (S 10) Н 3 (К 4, К 36, К 79) Н 3 (К 9, К 27) Н 4 (К 20) Н 2 В (К 123) Н 2 А (К 119) Н 3 (? ) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (К 126) Н 2 В (К 6, К 7, К 16, К 17) 21
Роль модификаций в регуляции транскрипции Модификации Группа 1 ацетилирование фосфорилирование метилирование Группа 2 убиквитинирование сумоилирование Роль в транскрипции активация репрессия Сайты модифицирования Н 3 (К 9, К 14, К 18, К 56) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (? ) Н 2 В (К 6, К 7, К 16, К 17) Н 3 (S 10) Н 3 (К 4, К 36, К 79) Н 3 (К 9, К 27) Н 4 (К 20) Н 2 В (К 123) Н 2 А (К 119) Н 3 (? ) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (К 126) Н 2 В (К 6, К 7, К 16, К 17) 21
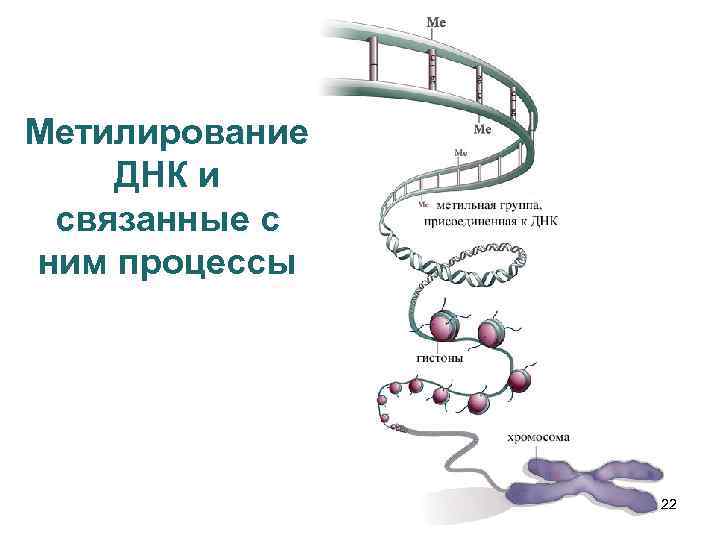 Метилирование ДНК и связанные с ним процессы 22
Метилирование ДНК и связанные с ним процессы 22
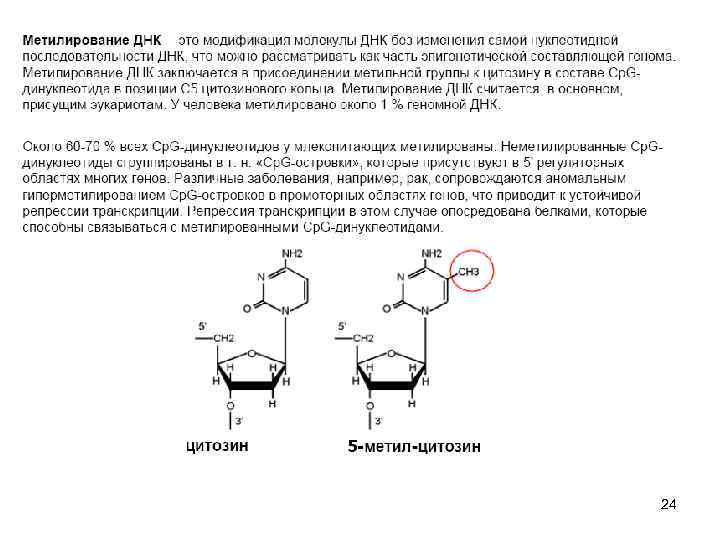
 Молекулярные основы эпигенетики H H N CH 3 4 3 5 6 N 1 Б. Ф. Ванюшин Впервые определил природу метилируемых последовательностей ДНК у разных видов организмов (1959 г. ) N 2 O Robin Holliday Обосновал роль метилирования ДНК в регуляции работы гена. Предложил термин «эпимутация» (1987 г. ) 23
Молекулярные основы эпигенетики H H N CH 3 4 3 5 6 N 1 Б. Ф. Ванюшин Впервые определил природу метилируемых последовательностей ДНК у разных видов организмов (1959 г. ) N 2 O Robin Holliday Обосновал роль метилирования ДНК в регуляции работы гена. Предложил термин «эпимутация» (1987 г. ) 23
 24
24
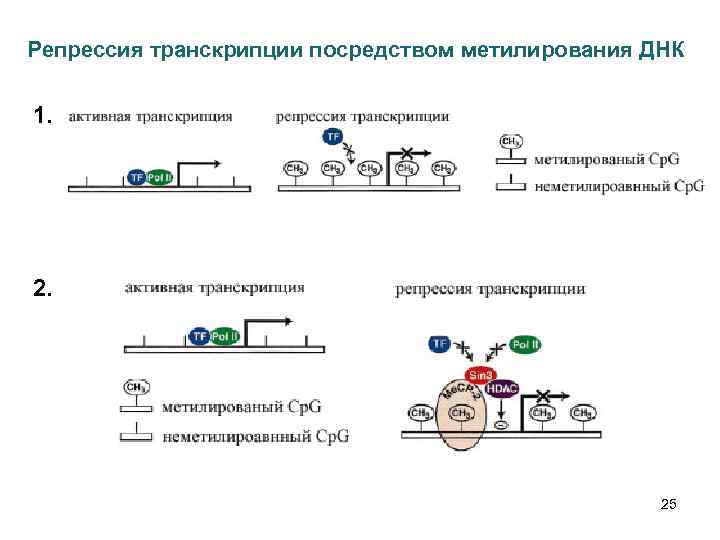 Репрессия транскрипции посредством метилирования ДНК 1. 25
Репрессия транскрипции посредством метилирования ДНК 1. 25
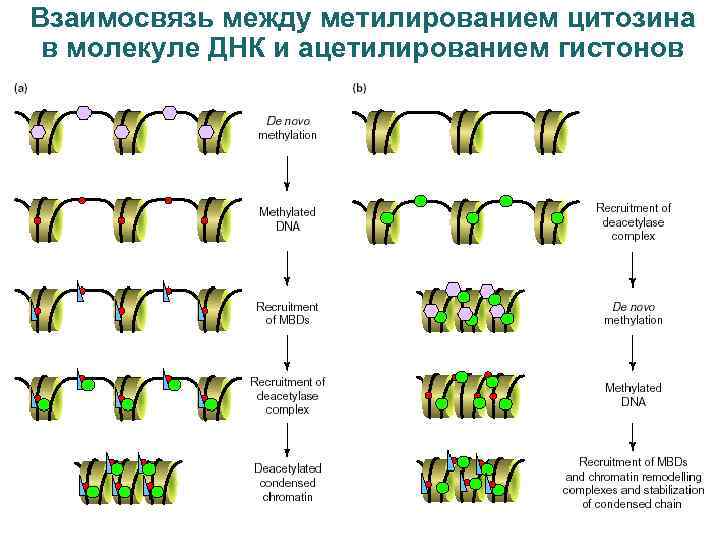 Взаимосвязь между метилированием цитозина в молекуле ДНК и ацетилированием гистонов
Взаимосвязь между метилированием цитозина в молекуле ДНК и ацетилированием гистонов
 Механизмы инактивации гена в результате метилирования промоторной области 1. Метильные группы нарушают ДНК-белковые взаимодействия, выступая в большую бороздку ДНК и препятствуя связыванию специфических транскрипционных факторов. 2. Метилированные районы ДНК специфически связывают транскрипционные репрессоры. 3. Метилирование ДНК влияет на структуру хроматина. 27
Механизмы инактивации гена в результате метилирования промоторной области 1. Метильные группы нарушают ДНК-белковые взаимодействия, выступая в большую бороздку ДНК и препятствуя связыванию специфических транскрипционных факторов. 2. Метилированные районы ДНК специфически связывают транскрипционные репрессоры. 3. Метилирование ДНК влияет на структуру хроматина. 27
 Метилирование ДНК в клетке контролирует все (!) генетические процессы, в том числе такие как: • Транскрипция (клеточная дифференцировка) • Репликация • Рекомбинация • Репарация • Транспозиция генов • Инактивация Х-хромосомы 28
Метилирование ДНК в клетке контролирует все (!) генетические процессы, в том числе такие как: • Транскрипция (клеточная дифференцировка) • Репликация • Рекомбинация • Репарация • Транспозиция генов • Инактивация Х-хромосомы 28
 Биологическая специфичность метилирования ДНК: • • • Видовая (штаммовая) Тканевая (клеточная) Органоидная (ядро, митохондрии, пластиды) Внутримолекулярная (островки метилирования, повторы) Возрастная Резкое искажение метилирования ДНК: • отсутствие метильных доноров рак • суперметилирование ДНК рак • полное выключение (knockout) ДНК-метилазного гена остановка развития, апоптоз, смерть (без метилирования ДНК жизни нет!) 29
Биологическая специфичность метилирования ДНК: • • • Видовая (штаммовая) Тканевая (клеточная) Органоидная (ядро, митохондрии, пластиды) Внутримолекулярная (островки метилирования, повторы) Возрастная Резкое искажение метилирования ДНК: • отсутствие метильных доноров рак • суперметилирование ДНК рак • полное выключение (knockout) ДНК-метилазного гена остановка развития, апоптоз, смерть (без метилирования ДНК жизни нет!) 29
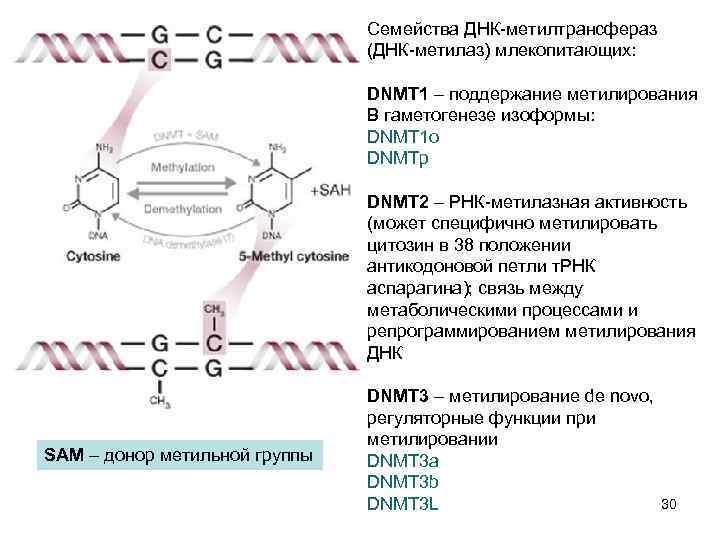 Семейства ДНК-метилтрансфераз (ДНК-метилаз) млекопитающих: DNMT 1 – поддержание метилирования В гаметогенезе изоформы: DNMT 1 o DNMTp DNMT 2 – РНК-метилазная активность (может специфично метилировать цитозин в 38 положении антикодоновой петли т. РНК аспарагина); связь между метаболическими процессами и репрограммированием метилирования ДНК SAM – донор метильной группы DNMT 3 – метилирование de novo, регуляторные функции при метилировании DNMT 3 a DNMT 3 b 30 DNMT 3 L
Семейства ДНК-метилтрансфераз (ДНК-метилаз) млекопитающих: DNMT 1 – поддержание метилирования В гаметогенезе изоформы: DNMT 1 o DNMTp DNMT 2 – РНК-метилазная активность (может специфично метилировать цитозин в 38 положении антикодоновой петли т. РНК аспарагина); связь между метаболическими процессами и репрограммированием метилирования ДНК SAM – донор метильной группы DNMT 3 – метилирование de novo, регуляторные функции при метилировании DNMT 3 a DNMT 3 b 30 DNMT 3 L
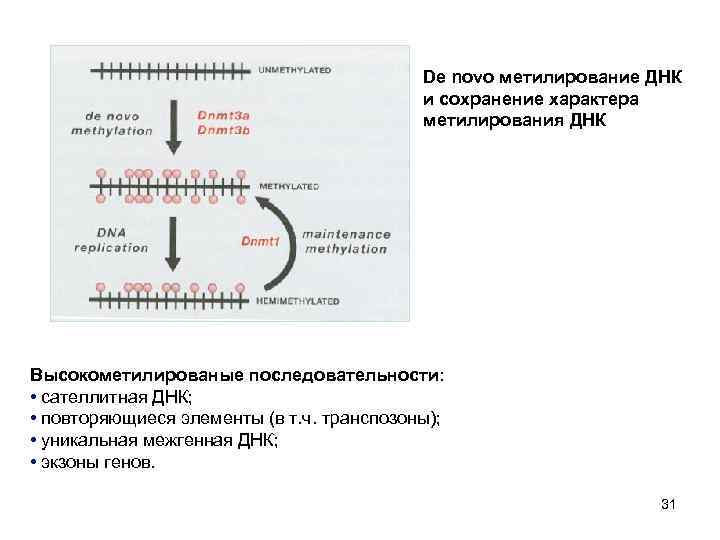 De novo метилирование ДНК и сохранение характера метилирования ДНК Высокометилированые последовательности: • сателлитная ДНК; • повторяющиеся элементы (в т. ч. транспозоны); • уникальная межгенная ДНК; • экзоны генов. 31
De novo метилирование ДНК и сохранение характера метилирования ДНК Высокометилированые последовательности: • сателлитная ДНК; • повторяющиеся элементы (в т. ч. транспозоны); • уникальная межгенная ДНК; • экзоны генов. 31
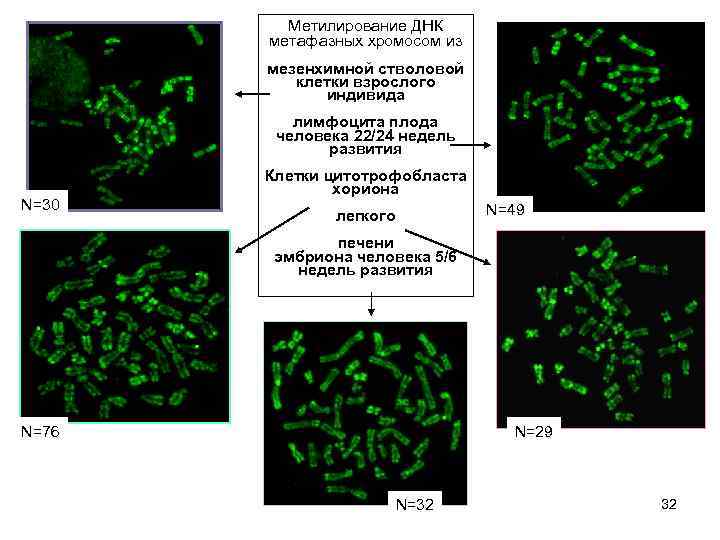 Метилирование ДНК метафазных хромосом из мезенхимной стволовой клетки взрослого индивида лимфоцита плода человека 22/24 недель развития N=30 Клетки цитотрофобласта хориона легкого N=49 печени эмбриона человека 5/6 недель развития N=76 N=29 N=32 32
Метилирование ДНК метафазных хромосом из мезенхимной стволовой клетки взрослого индивида лимфоцита плода человека 22/24 недель развития N=30 Клетки цитотрофобласта хориона легкого N=49 печени эмбриона человека 5/6 недель развития N=76 N=29 N=32 32
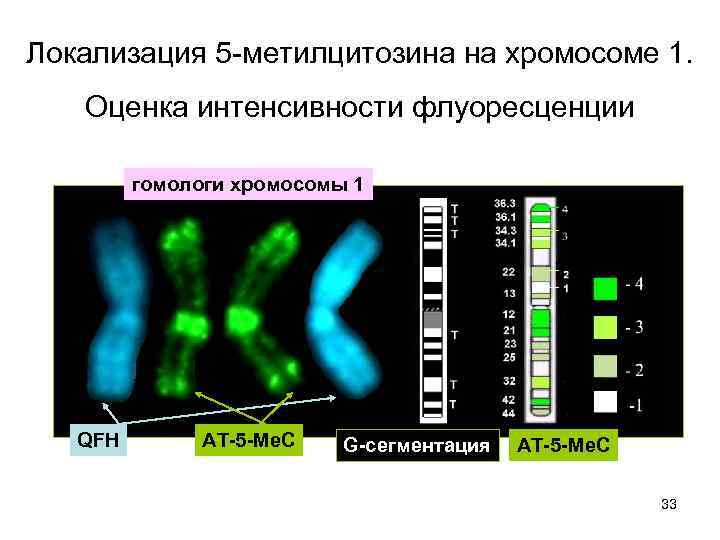 Локализация 5 -метилцитозина на хромосоме 1. Оценка интенсивности флуоресценции гомологи хромосомы 1 QFH АТ-5 -Ме. С G-сегментация АТ-5 -Ме. С 33
Локализация 5 -метилцитозина на хромосоме 1. Оценка интенсивности флуоресценции гомологи хромосомы 1 QFH АТ-5 -Ме. С G-сегментация АТ-5 -Ме. С 33
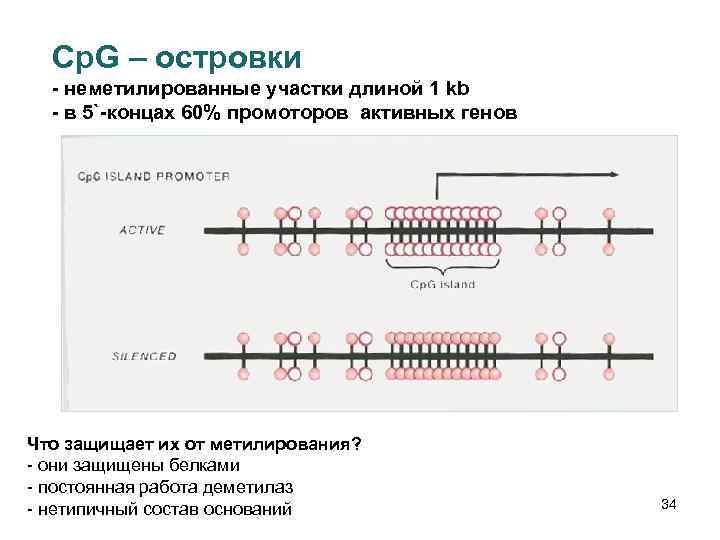 Cp. G – островки - неметилированные участки длиной 1 kb - в 5`-концах 60% промоторов активных генов Что защищает их от метилирования? - они защищены белками - постоянная работа деметилаз - нетипичный состав оснований 34
Cp. G – островки - неметилированные участки длиной 1 kb - в 5`-концах 60% промоторов активных генов Что защищает их от метилирования? - они защищены белками - постоянная работа деметилаз - нетипичный состав оснований 34
 Деметилирование – удаление метильных групп из ДНК Пассивное деметилирование – реализуется после репликации ДНК, за счет отсутствия метилазной активности. Новосинтезированная нить ДНК не метилируется по образцу старой, и образуется полуметилированная (гемиметилированная) ДНК. Активное деметилирование – задействована ферментативная система, превращающая 5 -метилцитозин в цитозин независимо от репликации Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК оставались неизвестными! 35
Деметилирование – удаление метильных групп из ДНК Пассивное деметилирование – реализуется после репликации ДНК, за счет отсутствия метилазной активности. Новосинтезированная нить ДНК не метилируется по образцу старой, и образуется полуметилированная (гемиметилированная) ДНК. Активное деметилирование – задействована ферментативная система, превращающая 5 -метилцитозин в цитозин независимо от репликации Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК оставались неизвестными! 35
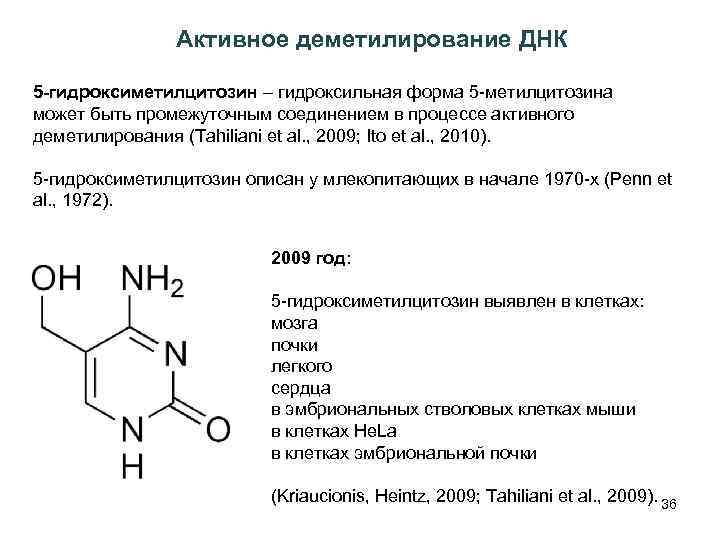 Активное деметилирование ДНК 5 -гидроксиметилцитозин – гидроксильная форма 5 -метилцитозина может быть промежуточным соединением в процессе активного деметилирования (Tahiliani et al. , 2009; Ito et al. , 2010). 5 -гидроксиметилцитозин описан у млекопитающих в начале 1970 -х (Penn et al. , 1972). 2009 год: 5 -гидроксиметилцитозин выявлен в клетках: мозга почки легкого сердца в эмбриональных стволовых клетках мыши в клетках He. La в клетках эмбриональной почки (Kriaucionis, Heintz, 2009; Tahiliani et al. , 2009). 36
Активное деметилирование ДНК 5 -гидроксиметилцитозин – гидроксильная форма 5 -метилцитозина может быть промежуточным соединением в процессе активного деметилирования (Tahiliani et al. , 2009; Ito et al. , 2010). 5 -гидроксиметилцитозин описан у млекопитающих в начале 1970 -х (Penn et al. , 1972). 2009 год: 5 -гидроксиметилцитозин выявлен в клетках: мозга почки легкого сердца в эмбриональных стволовых клетках мыши в клетках He. La в клетках эмбриональной почки (Kriaucionis, Heintz, 2009; Tahiliani et al. , 2009). 36
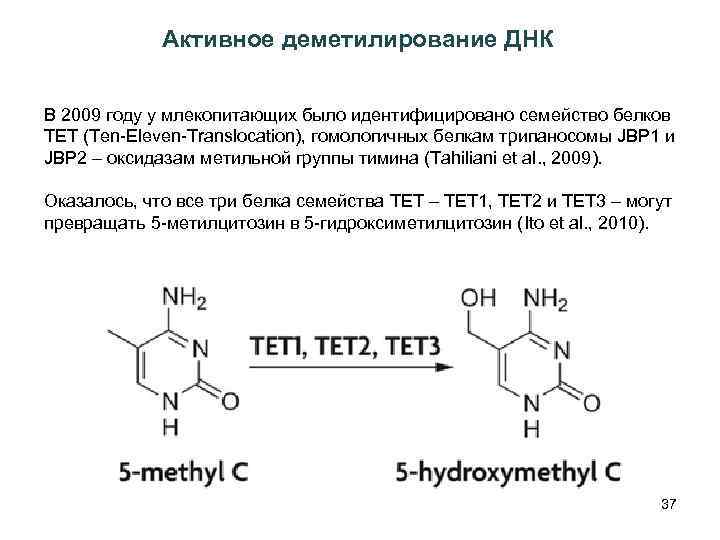 Активное деметилирование ДНК В 2009 году у млекопитающих было идентифицировано семейство белков TET (Ten-Eleven-Translocation), гомологичных белкам трипаносомы JBP 1 и JBP 2 – оксидазам метильной группы тимина (Tahiliani et al. , 2009). Оказалось, что все три белка семейства TET – TET 1, TET 2 и TET 3 – могут превращать 5 -метилцитозин в 5 -гидроксиметилцитозин (Ito et al. , 2010). 37
Активное деметилирование ДНК В 2009 году у млекопитающих было идентифицировано семейство белков TET (Ten-Eleven-Translocation), гомологичных белкам трипаносомы JBP 1 и JBP 2 – оксидазам метильной группы тимина (Tahiliani et al. , 2009). Оказалось, что все три белка семейства TET – TET 1, TET 2 и TET 3 – могут превращать 5 -метилцитозин в 5 -гидроксиметилцитозин (Ito et al. , 2010). 37
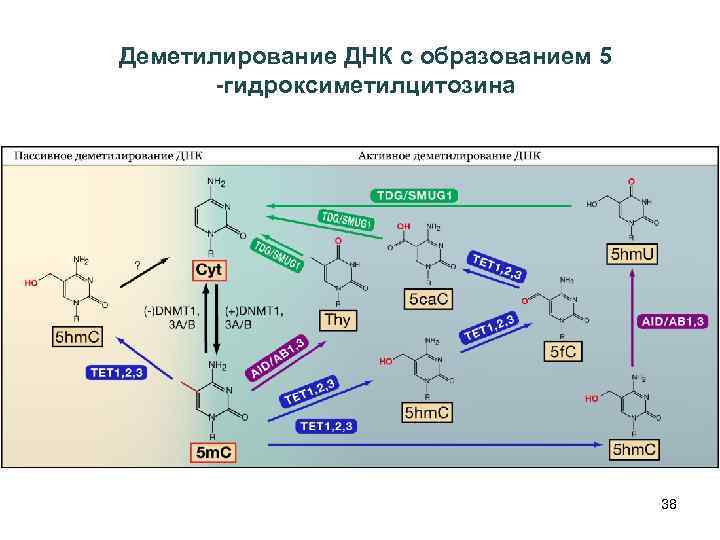 Деметилирование ДНК с образованием 5 -гидроксиметилцитозина 38
Деметилирование ДНК с образованием 5 -гидроксиметилцитозина 38
 «В последние годы … установлен особый класс заболеваний человека, обусловленный дефектами структуры и модификаций хроматина – так называемые «хроматиновые болезни» . С. Назаренко, 2005 г. 39
«В последние годы … установлен особый класс заболеваний человека, обусловленный дефектами структуры и модификаций хроматина – так называемые «хроматиновые болезни» . С. Назаренко, 2005 г. 39
 Синдром Ретта (OMIM 312750) Частота 1 на 10000 -15000 детей женского пола Впервые описан Реттом в 1966 г. (Rett, 1966), повторно в 1983 Хогбергом (Hagberg, 1993). Мутация в гене Me. CP 2 (Me. C binding protein), расположенном на Xq 28 http: //www. mississippichallenge. or g/rettsyndrome. html http: //www. rodim. ru/conference/in dex. php? s=0 b 8265 fee 36 f 1322 b 6 da b 8 dae 8 f 038 a 7&showtopic=83503& pid=4926083&st=765&#entry 49260 83 • регрессия развития • аутизм • стереотипные движения рук 40 http: //swimpig. blogspot. com/200 7_02_01_archive. html
Синдром Ретта (OMIM 312750) Частота 1 на 10000 -15000 детей женского пола Впервые описан Реттом в 1966 г. (Rett, 1966), повторно в 1983 Хогбергом (Hagberg, 1993). Мутация в гене Me. CP 2 (Me. C binding protein), расположенном на Xq 28 http: //www. mississippichallenge. or g/rettsyndrome. html http: //www. rodim. ru/conference/in dex. php? s=0 b 8265 fee 36 f 1322 b 6 da b 8 dae 8 f 038 a 7&showtopic=83503& pid=4926083&st=765&#entry 49260 83 • регрессия развития • аутизм • стереотипные движения рук 40 http: //swimpig. blogspot. com/200 7_02_01_archive. html
 Синдром ICF (OMIM 242860) (Immunodeficiency, Centromere instability and Facial anomalies syndrome ) Luciani et al. , 2005 Мутации в гене DNMT 3 B (DNA metiltransferase), расположенном на хромосоме 20 q 11. 2 Синдром ICF (иммунодефицит, хромосомная нестабильность, аномалии лицевого черепа) Гетерохроматиновые районы хромосом 1, 9 и 16 неметелированы, вследствие чего растянуты и имеют ветвистую структуру Впервые синдром описан в 1978 году 41 (Hulten, 1978)
Синдром ICF (OMIM 242860) (Immunodeficiency, Centromere instability and Facial anomalies syndrome ) Luciani et al. , 2005 Мутации в гене DNMT 3 B (DNA metiltransferase), расположенном на хромосоме 20 q 11. 2 Синдром ICF (иммунодефицит, хромосомная нестабильность, аномалии лицевого черепа) Гетерохроматиновые районы хромосом 1, 9 и 16 неметелированы, вследствие чего растянуты и имеют ветвистую структуру Впервые синдром описан в 1978 году 41 (Hulten, 1978)
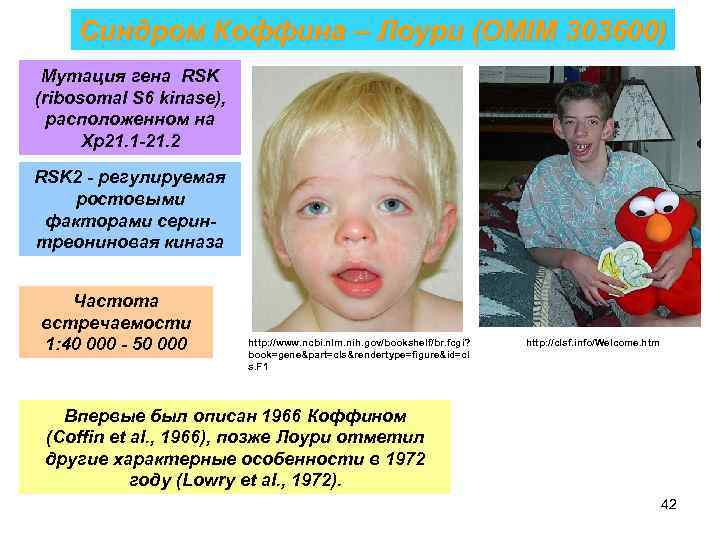 Синдром Коффина – Лоури (OMIM 303600) Мутация гена RSK (ribosomal S 6 kinase), расположенном на Хp 21. 1 -21. 2 RSK 2 - регулируемая ростовыми факторами серинтреониновая киназа Частота встречаемости 1: 40 000 - 50 000 http: //www. ncbi. nlm. nih. gov/bookshelf/br. fcgi? book=gene&part=cls&rendertype=figure&id=cl s. F 1 http: //clsf. info/Welcome. htm Впервые был описан 1966 Коффином (Coffin et al. , 1966), позже Лоури отметил другие характерные особенности в 1972 году (Lowry et al. , 1972). 42
Синдром Коффина – Лоури (OMIM 303600) Мутация гена RSK (ribosomal S 6 kinase), расположенном на Хp 21. 1 -21. 2 RSK 2 - регулируемая ростовыми факторами серинтреониновая киназа Частота встречаемости 1: 40 000 - 50 000 http: //www. ncbi. nlm. nih. gov/bookshelf/br. fcgi? book=gene&part=cls&rendertype=figure&id=cl s. F 1 http: //clsf. info/Welcome. htm Впервые был описан 1966 Коффином (Coffin et al. , 1966), позже Лоури отметил другие характерные особенности в 1972 году (Lowry et al. , 1972). 42
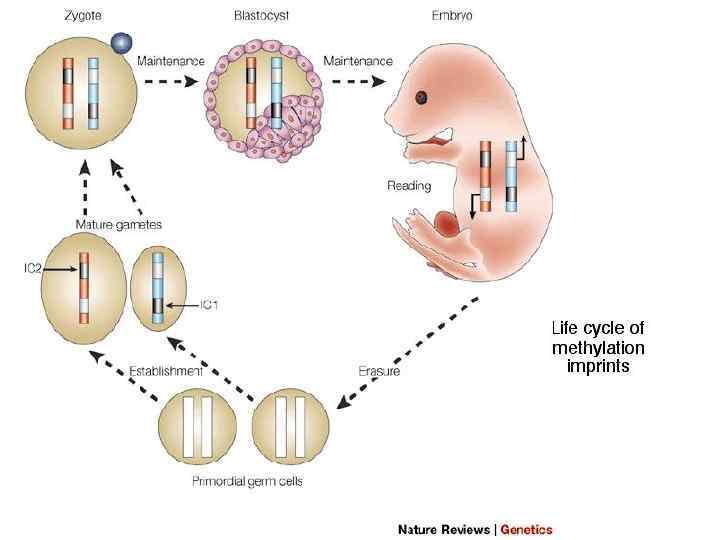
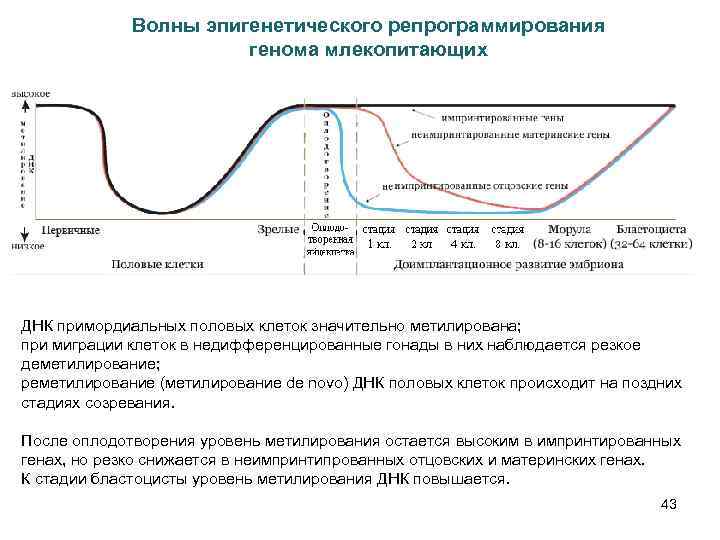 Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается. 43
Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается. 43
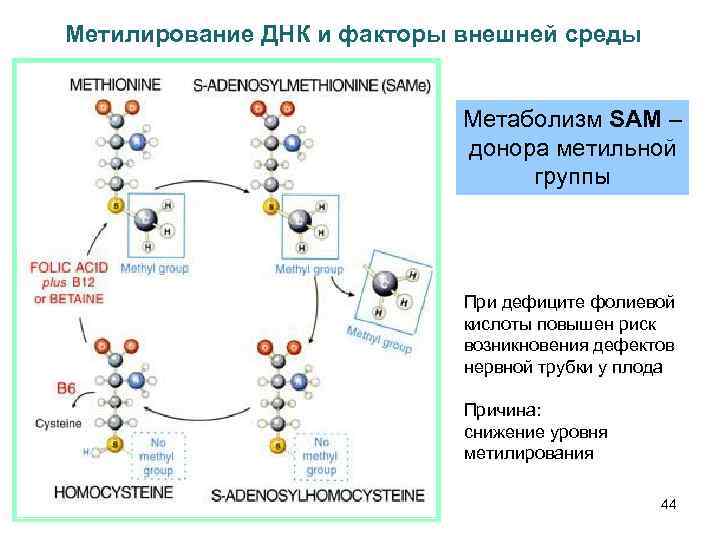 Метилирование ДНК и факторы внешней среды Метаболизм SAM – донора метильной группы При дефиците фолиевой кислоты повышен риск возникновения дефектов нервной трубки у плода Причина: снижение уровня метилирования 44
Метилирование ДНК и факторы внешней среды Метаболизм SAM – донора метильной группы При дефиците фолиевой кислоты повышен риск возникновения дефектов нервной трубки у плода Причина: снижение уровня метилирования 44
 Метилирование ДНК и факторы внешней среды Доказано влияние на метилирование ДНК металлов – никеля, кадмия, мышьяка, а также хрома, ртути, трихлорэтилена, дихлоруксусной и трихлоруксусной кислоты, бензола, бисфенола. Металлы способствуют образованию в клетке активных форм кислорода, вызывающих повреждения ДНК, которые затрудняют или делают невозможной работу ДНК метилтрансфераз. В 1992 году Баркером была выдвинута гипотеза FEBAD (fetal basis of adult disease). В пользу гипотезы свидетельствует обнаруженная взаимосвязь между воздействием на плод экзогенных и эндогенных факторов и риском последующего развития сердечно-сосудистых заболеваний, сахарного диабета второго типа, остеопороза и некоторых видов рака. 45
Метилирование ДНК и факторы внешней среды Доказано влияние на метилирование ДНК металлов – никеля, кадмия, мышьяка, а также хрома, ртути, трихлорэтилена, дихлоруксусной и трихлоруксусной кислоты, бензола, бисфенола. Металлы способствуют образованию в клетке активных форм кислорода, вызывающих повреждения ДНК, которые затрудняют или делают невозможной работу ДНК метилтрансфераз. В 1992 году Баркером была выдвинута гипотеза FEBAD (fetal basis of adult disease). В пользу гипотезы свидетельствует обнаруженная взаимосвязь между воздействием на плод экзогенных и эндогенных факторов и риском последующего развития сердечно-сосудистых заболеваний, сахарного диабета второго типа, остеопороза и некоторых видов рака. 45
 Внешние факторы, действующие на женщину в период беременности, могут изменять характер метилирования ДНК в ее клетках, модифицировать формирующиеся эпигенетические паттерны плода, а также влиять на процесс репрограммирования в формирующихся половых 46 клетках плода!
Внешние факторы, действующие на женщину в период беременности, могут изменять характер метилирования ДНК в ее клетках, модифицировать формирующиеся эпигенетические паттерны плода, а также влиять на процесс репрограммирования в формирующихся половых 46 клетках плода!
 Метилирование ДНК является обратимой реакцией и в значительной степени подвержено воздействию эндогенных и экзогенных факторов. Эти особенности, с одной стороны, увеличивают риск возникновения ошибок из-за влияния негативных факторов, но с другой – дают возможность проводить коррекцию эпигенетической регуляции генома за счет определенных внешних воздействий, в том числе лекарственных средств, гормонов и диеты. 47
Метилирование ДНК является обратимой реакцией и в значительной степени подвержено воздействию эндогенных и экзогенных факторов. Эти особенности, с одной стороны, увеличивают риск возникновения ошибок из-за влияния негативных факторов, но с другой – дают возможность проводить коррекцию эпигенетической регуляции генома за счет определенных внешних воздействий, в том числе лекарственных средств, гормонов и диеты. 47
 ПЕРЕНОС ЯДРА СОМАТИЧЕСКОЙ КЛЕТКИ В ЭНУКЛЕИРОВАННЫЙ ООЦИТ ЛЯГУШКИ Проверка гипотезы: «По мере дифференцировки клетки претерпевают необратимую утрату / репрессию генетического материала» . Эксперименты проводились в конце 1950 -х в течение 15 лет. 48
ПЕРЕНОС ЯДРА СОМАТИЧЕСКОЙ КЛЕТКИ В ЭНУКЛЕИРОВАННЫЙ ООЦИТ ЛЯГУШКИ Проверка гипотезы: «По мере дифференцировки клетки претерпевают необратимую утрату / репрессию генетического материала» . Эксперименты проводились в конце 1950 -х в течение 15 лет. 48
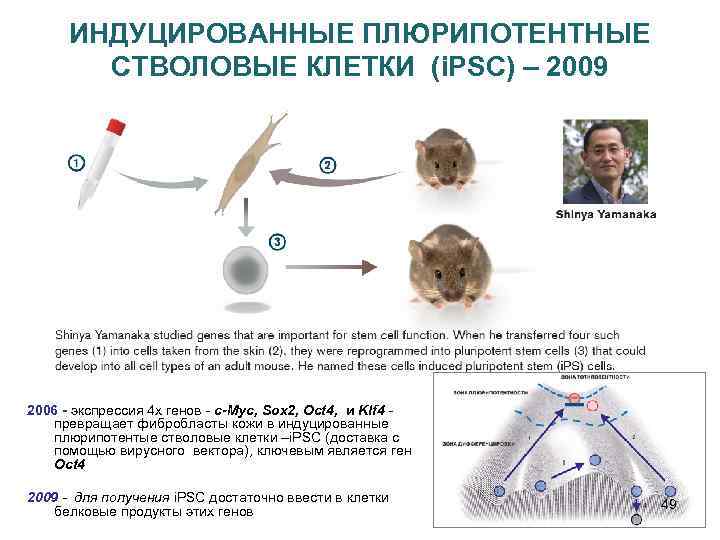 ИНДУЦИРОВАННЫЕ ПЛЮРИПОТЕНТНЫЕ СТВОЛОВЫЕ КЛЕТКИ (i. PSC) – 2009 2006 - экспрессия 4 х генов - c-Myc, Sox 2, Oct 4, и Klf 4 - превращает фибробласты кожи в индуцированные плюрипотентые стволовые клетки –i. PSC (доставка с помощью вирусного вектора), ключевым является ген Oct 4 2009 - для получения i. PSC достаточно ввести в клетки белковые продукты этих генов 49
ИНДУЦИРОВАННЫЕ ПЛЮРИПОТЕНТНЫЕ СТВОЛОВЫЕ КЛЕТКИ (i. PSC) – 2009 2006 - экспрессия 4 х генов - c-Myc, Sox 2, Oct 4, и Klf 4 - превращает фибробласты кожи в индуцированные плюрипотентые стволовые клетки –i. PSC (доставка с помощью вирусного вектора), ключевым является ген Oct 4 2009 - для получения i. PSC достаточно ввести в клетки белковые продукты этих генов 49
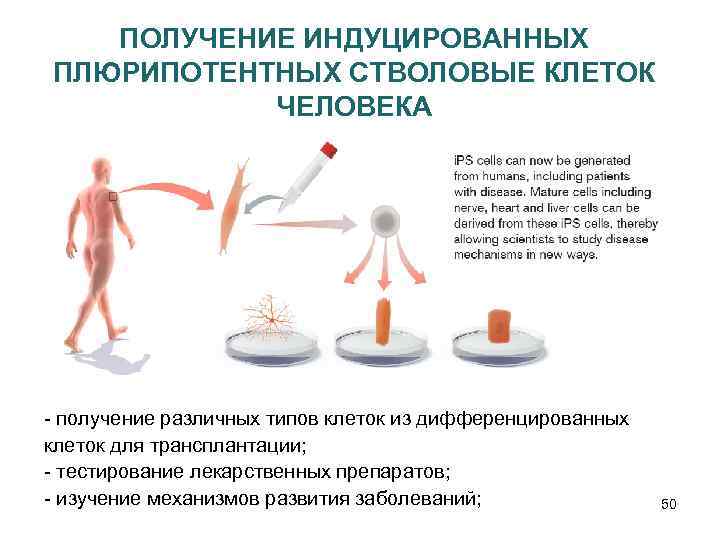 ПОЛУЧЕНИЕ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ СТВОЛОВЫЕ КЛЕТОК ЧЕЛОВЕКА - получение различных типов клеток из дифференцированных клеток для трансплантации; - тестирование лекарственных препаратов; - изучение механизмов развития заболеваний; 50
ПОЛУЧЕНИЕ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ СТВОЛОВЫЕ КЛЕТОК ЧЕЛОВЕКА - получение различных типов клеток из дифференцированных клеток для трансплантации; - тестирование лекарственных препаратов; - изучение механизмов развития заболеваний; 50
 The Nobel Assembly at Karolinska Institutet has decided to award The Nobel Prize in Physiology or Medicine 2012 jointly to John B. Gurdon and Shinya Yamanaka for the discovery that mature cells can be reprogrammed to become pluripotent John B. Gurdon Shinya Yamanaka 51
The Nobel Assembly at Karolinska Institutet has decided to award The Nobel Prize in Physiology or Medicine 2012 jointly to John B. Gurdon and Shinya Yamanaka for the discovery that mature cells can be reprogrammed to become pluripotent John B. Gurdon Shinya Yamanaka 51
 Август 2011: у мышей получено жизнеспособное фертильное потомство из индуцированных сперматозоидов. 52
Август 2011: у мышей получено жизнеспособное фертильное потомство из индуцированных сперматозоидов. 52
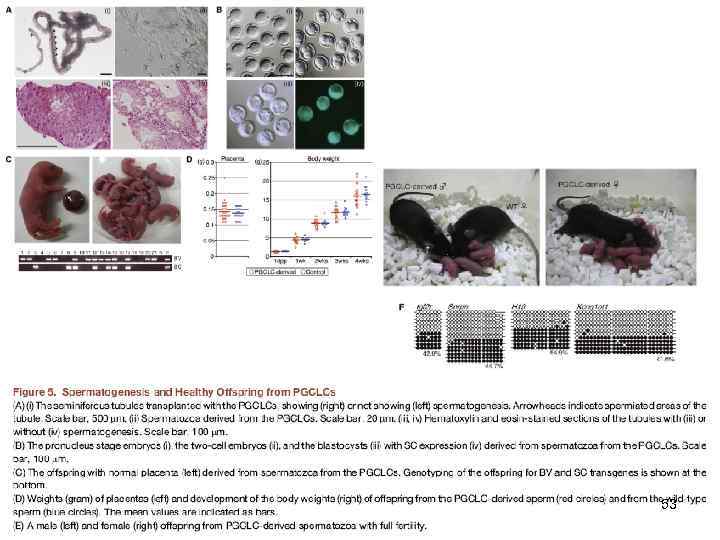 53
53
 Октябрь 2012: у мышей получено жизнеспособное фертильное потомство из индуцированных ооцитов. 54
Октябрь 2012: у мышей получено жизнеспособное фертильное потомство из индуцированных ооцитов. 54
 Геномный импринтинг 55
Геномный импринтинг 55
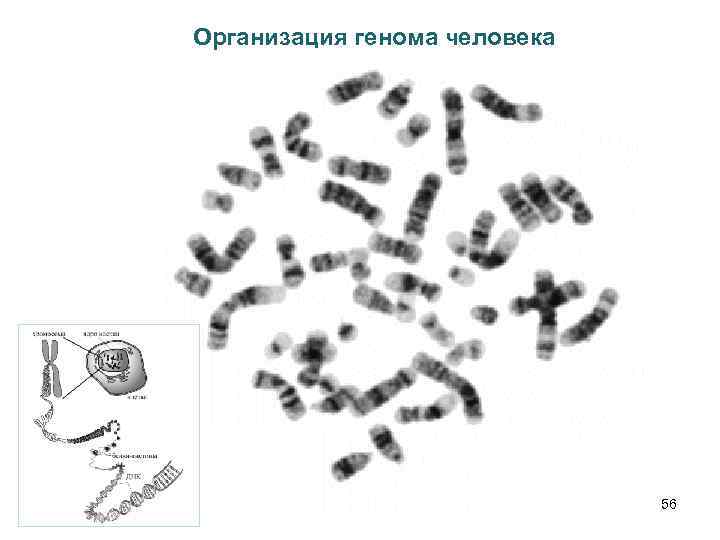 Организация генома человека 56
Организация генома человека 56
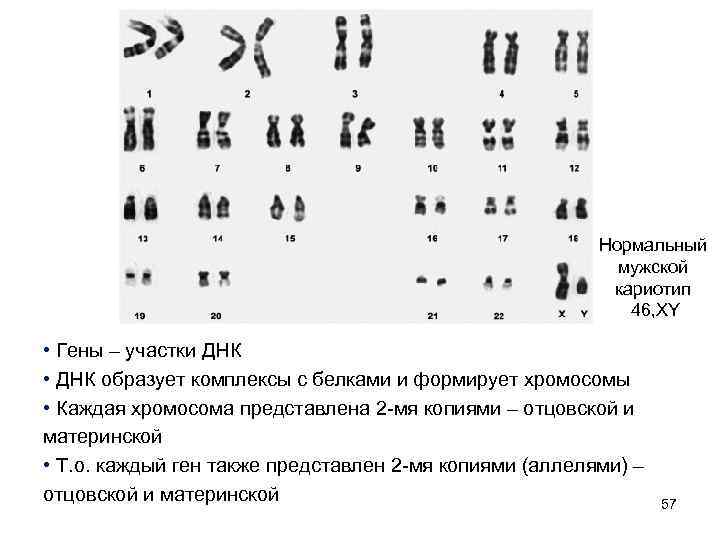 Нормальный мужской кариотип 46, XY • Гены – участки ДНК • ДНК образует комплексы с белками и формирует хромосомы • Каждая хромосома представлена 2 -мя копиями – отцовской и материнской • Т. о. каждый ген также представлен 2 -мя копиями (аллелями) – отцовской и материнской 57
Нормальный мужской кариотип 46, XY • Гены – участки ДНК • ДНК образует комплексы с белками и формирует хромосомы • Каждая хромосома представлена 2 -мя копиями – отцовской и материнской • Т. о. каждый ген также представлен 2 -мя копиями (аллелями) – отцовской и материнской 57
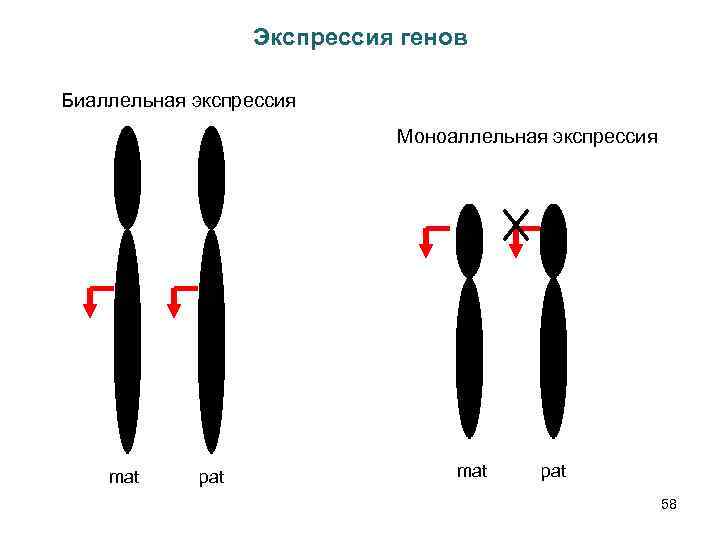 Экспрессия генов Биаллельная экспрессия Моноаллельная экспрессия mat pat 58
Экспрессия генов Биаллельная экспрессия Моноаллельная экспрессия mat pat 58
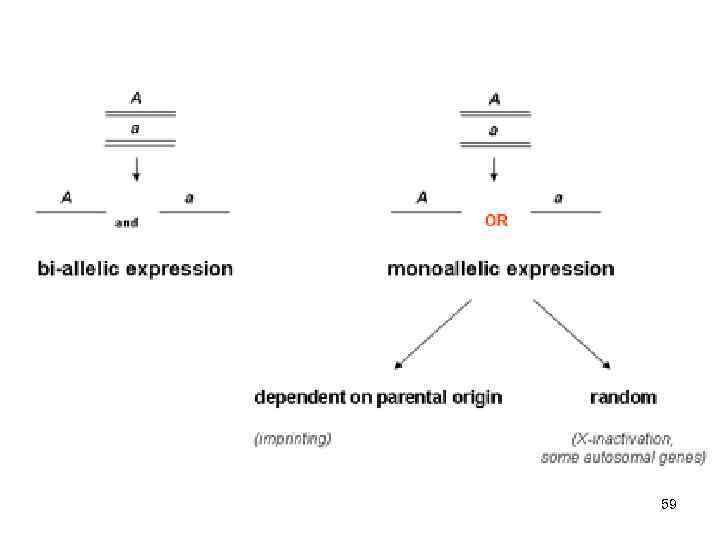 59
59
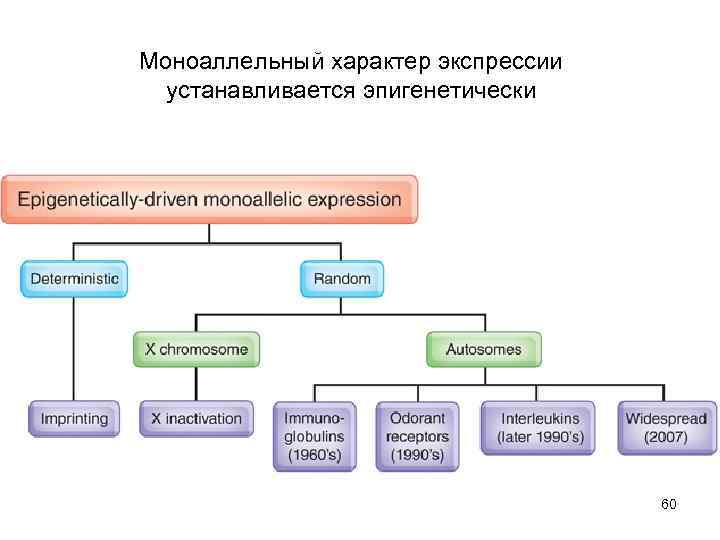 Моноаллельный характер экспрессии устанавливается эпигенетически 60
Моноаллельный характер экспрессии устанавливается эпигенетически 60
 Черепаховый окрас кошек - результат случайной инактивации хромосомы Х 61
Черепаховый окрас кошек - результат случайной инактивации хромосомы Х 61
 Геномный импринтинг (ГИ) – дифференциальная модификация отцовского и материнского генетического материала в процессе созревания гамет, следствием чего являются различия в экспрессии родительских аллелей как в процессе раннего эмбриогенеза, так и у взрослых особей 62
Геномный импринтинг (ГИ) – дифференциальная модификация отцовского и материнского генетического материала в процессе созревания гамет, следствием чего являются различия в экспрессии родительских аллелей как в процессе раннего эмбриогенеза, так и у взрослых особей 62
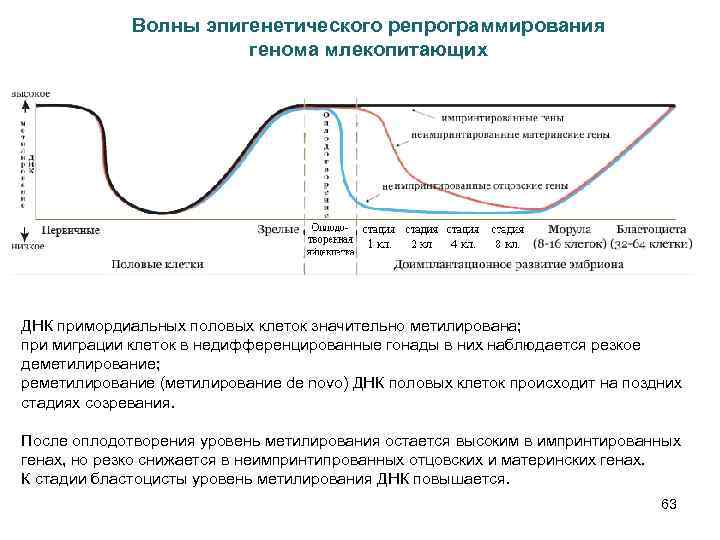 Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается. 63
Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается. 63
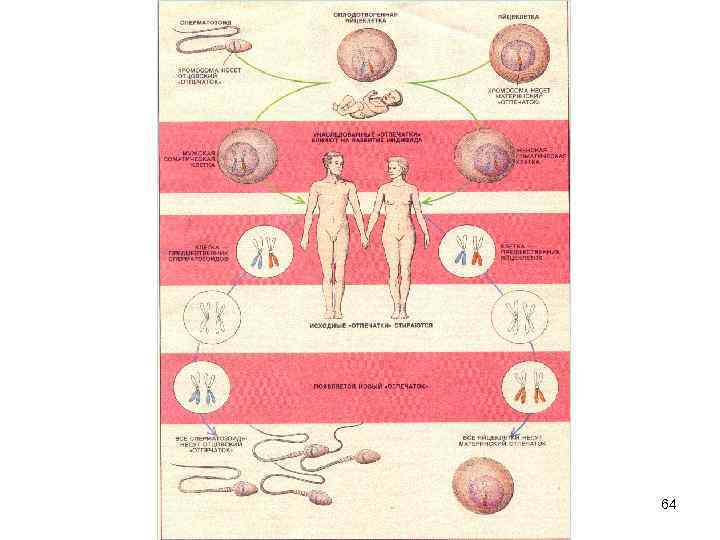 64
64
 65
65
 Импринтированный ген – ген, который дифференциально экспрессируется в зависимости от материнского или отцовского происхождения. Импринтированные гены в диплоидной клетке млекопитающих обычно экспрессируются только с одного аллеля. mat pat Пример: Материнская аллель экспрессируется, отцовская – нет (она импринтирована) Эпигенотип (импринт) – совокупность модификаций, которые по-разному маркируют родительские аллели и обеспечивают моноаллельный характер экспрессии импринтированных генов на хромосомах отцовского или 66 материнского происхождения.
Импринтированный ген – ген, который дифференциально экспрессируется в зависимости от материнского или отцовского происхождения. Импринтированные гены в диплоидной клетке млекопитающих обычно экспрессируются только с одного аллеля. mat pat Пример: Материнская аллель экспрессируется, отцовская – нет (она импринтирована) Эпигенотип (импринт) – совокупность модификаций, которые по-разному маркируют родительские аллели и обеспечивают моноаллельный характер экспрессии импринтированных генов на хромосомах отцовского или 66 материнского происхождения.
 Сколько импринтированных генов в геноме человека? Предполагают: около 200. Известно: около 100. http: //www. geneimprint. com 67
Сколько импринтированных генов в геноме человека? Предполагают: около 200. Известно: около 100. http: //www. geneimprint. com 67
 Характерные черты импринтированных генов: 1. Кластеризация Общие черты кластеров: 1) находятся на достаточно большом расстоянии; 2) наличие в кластере генов, экспрессирующихся только с отцовской или материнской хромосомы; 3) наличие генов, которые продуцируют нетранслируемую РНК. 2. Консервативность импринтинга Характер импринтинга генов H 19, IGF 2, p 57 KIP и SNRPN идентичен у человека и мыши. 3. Асинхронность репликации ДНК импринтированных генов Импринтированные гены имеют асинхронную репликацию, показанную в кластерах импринтированных генов с использованием гибридизации in situ. 68
Характерные черты импринтированных генов: 1. Кластеризация Общие черты кластеров: 1) находятся на достаточно большом расстоянии; 2) наличие в кластере генов, экспрессирующихся только с отцовской или материнской хромосомы; 3) наличие генов, которые продуцируют нетранслируемую РНК. 2. Консервативность импринтинга Характер импринтинга генов H 19, IGF 2, p 57 KIP и SNRPN идентичен у человека и мыши. 3. Асинхронность репликации ДНК импринтированных генов Импринтированные гены имеют асинхронную репликацию, показанную в кластерах импринтированных генов с использованием гибридизации in situ. 68
 4. Онтогенетическая и тканевая регуляция импринтинга. Kv. LQT 1 экспрессируется с материнской аллели во всех тканях кроме сердца; E 6 -AP - экспрессируется биаллельно во всех тканях, а в мозге - только с материнской аллели; IGF 2 имеет отцовскую экспрессию в большинстве тканей, но обе аллели экспрессируются в определенных структурах в течение развития мозга и в зрелом состоянии. Кроме того, IGF 2 в процессе развития экспрессируется с трех различных промоторов. 5. Импринтированные гены кодируют как белки, так и нетранслируемые РНК. H 19 кодирует РНК, аккумулирующуюся в больших количествах в течение развития фетальных тканей мезодермального и эндодермального происхождения. XIST. Транскрипция гена с инактивированной отцовской Ххромосомы в экстраэмбриональных тканях заставляет предполагать регуляторную роль импринтированной РНК. IPW, PAR-SN, PAR 1 и PAR 5 экспрессируются с отцовской хромосомы и их продуктом является нетранслируемая РНК. 69
4. Онтогенетическая и тканевая регуляция импринтинга. Kv. LQT 1 экспрессируется с материнской аллели во всех тканях кроме сердца; E 6 -AP - экспрессируется биаллельно во всех тканях, а в мозге - только с материнской аллели; IGF 2 имеет отцовскую экспрессию в большинстве тканей, но обе аллели экспрессируются в определенных структурах в течение развития мозга и в зрелом состоянии. Кроме того, IGF 2 в процессе развития экспрессируется с трех различных промоторов. 5. Импринтированные гены кодируют как белки, так и нетранслируемые РНК. H 19 кодирует РНК, аккумулирующуюся в больших количествах в течение развития фетальных тканей мезодермального и эндодермального происхождения. XIST. Транскрипция гена с инактивированной отцовской Ххромосомы в экстраэмбриональных тканях заставляет предполагать регуляторную роль импринтированной РНК. IPW, PAR-SN, PAR 1 и PAR 5 экспрессируются с отцовской хромосомы и их продуктом является нетранслируемая РНК. 69
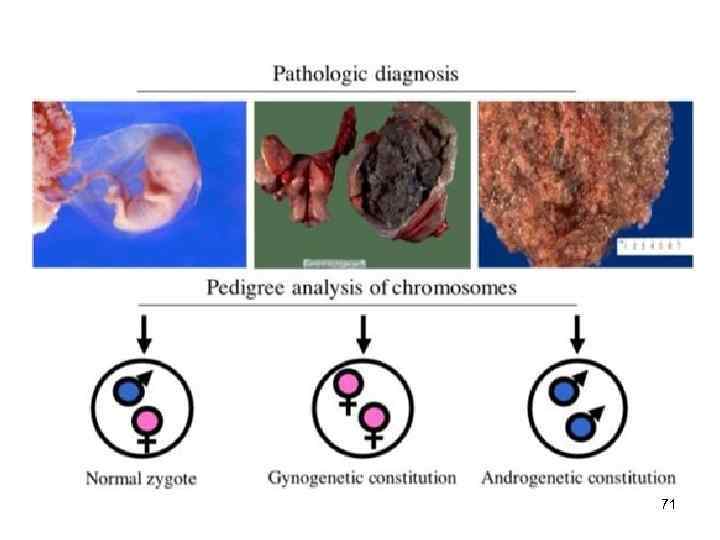
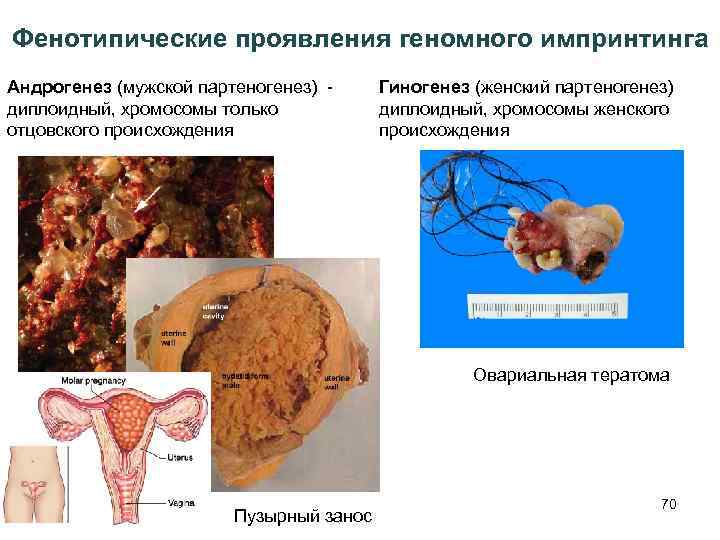 Фенотипические проявления геномного импринтинга Андрогенез (мужской партеногенез) - диплоидный, хромосомы только отцовского происхождения Гиногенез (женский партеногенез) диплоидный, хромосомы женского происхождения Овариальная тератома Пузырный занос 70
Фенотипические проявления геномного импринтинга Андрогенез (мужской партеногенез) - диплоидный, хромосомы только отцовского происхождения Гиногенез (женский партеногенез) диплоидный, хромосомы женского происхождения Овариальная тератома Пузырный занос 70
 71
71
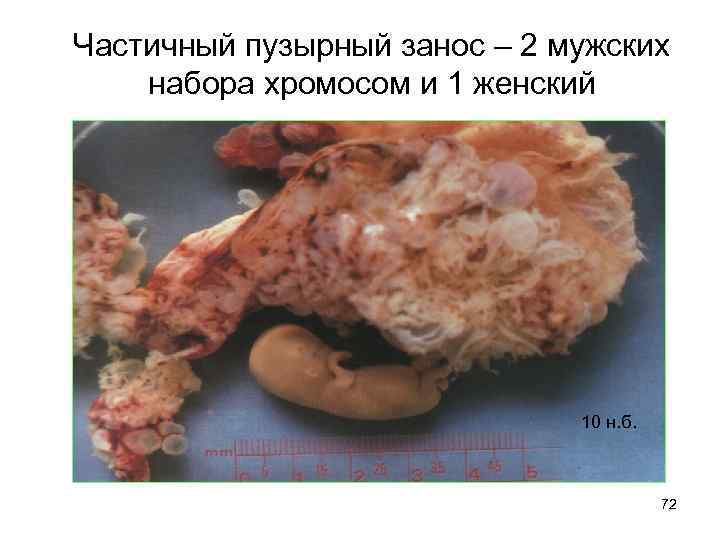 Частичный пузырный занос – 2 мужских набора хромосом и 1 женский 10 н. б. 72
Частичный пузырный занос – 2 мужских набора хромосом и 1 женский 10 н. б. 72
 Однородительская дисомия (ОРД=UPD) – наличие у потомков в кариотипе фрагментов или целых хромосом одного (материнского или отцовского) происхождения 47 типов ОРД: - 44 типа ОРД по 22 аутосомам материнская (mat) и отцовская (pat) - 3 типа по половым хромосомам UPDХmat, UPDXpat, UPDXYpat Гетеродисомия – наследование потомком двух разных гомологов от одного родителя Изодисомия – наследование двух репликационных копий одной из хромосом 73
Однородительская дисомия (ОРД=UPD) – наличие у потомков в кариотипе фрагментов или целых хромосом одного (материнского или отцовского) происхождения 47 типов ОРД: - 44 типа ОРД по 22 аутосомам материнская (mat) и отцовская (pat) - 3 типа по половым хромосомам UPDХmat, UPDXpat, UPDXYpat Гетеродисомия – наследование потомком двух разных гомологов от одного родителя Изодисомия – наследование двух репликационных копий одной из хромосом 73
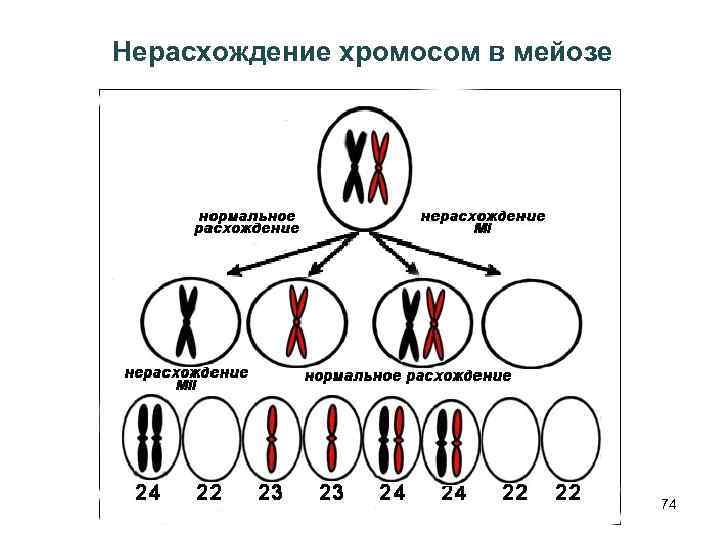 Нерасхождение хромосом в мейозе 74
Нерасхождение хромосом в мейозе 74
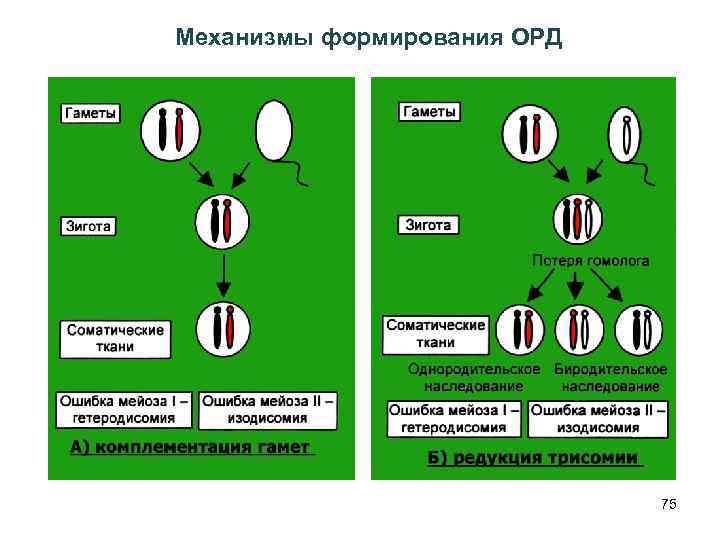 Механизмы формирования ОРД 75
Механизмы формирования ОРД 75
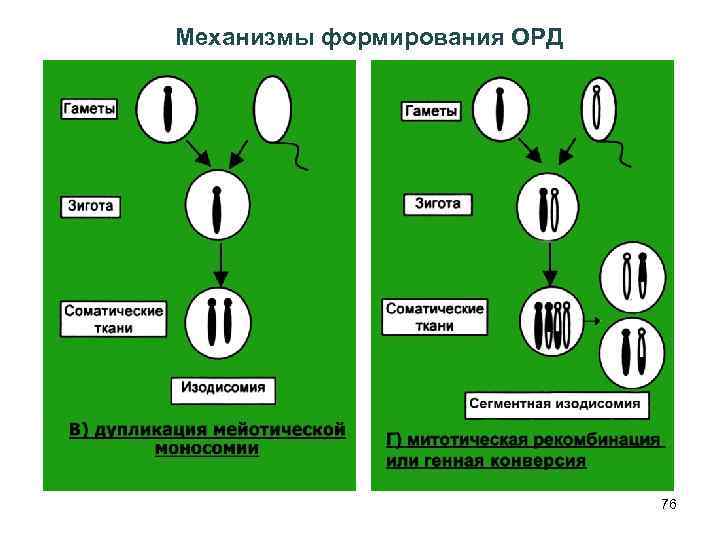 Механизмы формирования ОРД 76
Механизмы формирования ОРД 76
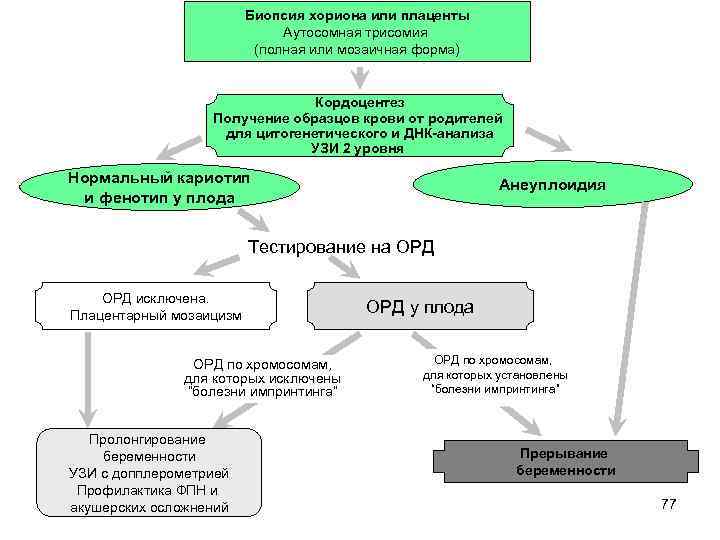 Биопсия хориона или плаценты Аутосомная трисомия (полная или мозаичная форма) Кордоцентез Получение образцов крови от родителей для цитогенетического и ДНК-анализа УЗИ 2 уровня Нормальный кариотип и фенотип у плода Анеуплоидия Тестирование на ОРД исключена. Плацентарный мозаицизм ОРД по хромосомам, для которых исключены “болезни импринтинга” Пролонгирование беременности УЗИ с допплерометрией Профилактика ФПН и акушерских осложнений ОРД у плода ОРД по хромосомам, для которых установлены “болезни импринтинга” Прерывание беременности 77
Биопсия хориона или плаценты Аутосомная трисомия (полная или мозаичная форма) Кордоцентез Получение образцов крови от родителей для цитогенетического и ДНК-анализа УЗИ 2 уровня Нормальный кариотип и фенотип у плода Анеуплоидия Тестирование на ОРД исключена. Плацентарный мозаицизм ОРД по хромосомам, для которых исключены “болезни импринтинга” Пролонгирование беременности УЗИ с допплерометрией Профилактика ФПН и акушерских осложнений ОРД у плода ОРД по хромосомам, для которых установлены “болезни импринтинга” Прерывание беременности 77
 Группы риска ОРД • носители структурно аномальных хромосом, включая семейные сбалансированные реципрокные и робертсоновские транслокации, изохромосомы, инверсии, маркерные хромосомы • носители мозаичных трисомий • плоды с пренатально подтвержденным диагнозом ограниченного плацентарного мозаицизма • больные с моногенным рецессивным заболеванием или гетерозиготным носительством мутантного гена у одного из родителей 78
Группы риска ОРД • носители структурно аномальных хромосом, включая семейные сбалансированные реципрокные и робертсоновские транслокации, изохромосомы, инверсии, маркерные хромосомы • носители мозаичных трисомий • плоды с пренатально подтвержденным диагнозом ограниченного плацентарного мозаицизма • больные с моногенным рецессивным заболеванием или гетерозиготным носительством мутантного гена у одного из родителей 78
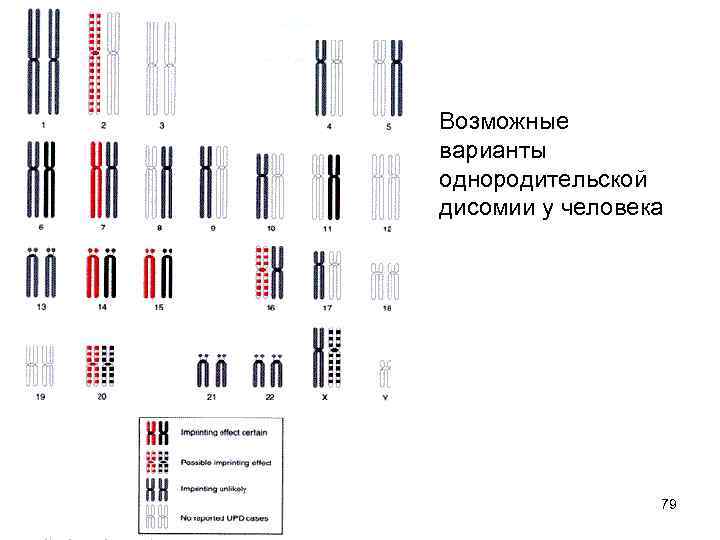 Возможные варианты однородительской дисомии у человека 79
Возможные варианты однородительской дисомии у человека 79
 ОРД по целым хромосомам или их фрагментам выявлены при анализе наследственной патологии и у человека материнская ОРД по хромосоме 2 => признаки дисэмбриогенеза и отставание в развитии; отцовская ОРД по длинному плечу хромосомы 6 (q 23 - q 24) => неонатальный диабет; материнская ОРД по короткому плечу хромосомы 7 (GRB 10) => синдром Сильвера–Рассела; материнская ОРД по хромосоме 14 => гипотония, черепно-лицевые аномалии, акромикрия, сколиоз, задержка физического, моторного и умственного развития; отцовская ОРД по хромосоме 14 => сильная умственная отсталость и скелетно мышечные аномалии; материнская ОРД по хромосоме 16 => малый вес при рождении и врожденные аномалии; отцовская ОРД по длинному плечу хромосомы 20 (GNAS 1) => псевдогипопаратироидизм Залетаев Д. В. 80
ОРД по целым хромосомам или их фрагментам выявлены при анализе наследственной патологии и у человека материнская ОРД по хромосоме 2 => признаки дисэмбриогенеза и отставание в развитии; отцовская ОРД по длинному плечу хромосомы 6 (q 23 - q 24) => неонатальный диабет; материнская ОРД по короткому плечу хромосомы 7 (GRB 10) => синдром Сильвера–Рассела; материнская ОРД по хромосоме 14 => гипотония, черепно-лицевые аномалии, акромикрия, сколиоз, задержка физического, моторного и умственного развития; отцовская ОРД по хромосоме 14 => сильная умственная отсталость и скелетно мышечные аномалии; материнская ОРД по хромосоме 16 => малый вес при рождении и врожденные аномалии; отцовская ОРД по длинному плечу хромосомы 20 (GNAS 1) => псевдогипопаратироидизм Залетаев Д. В. 80
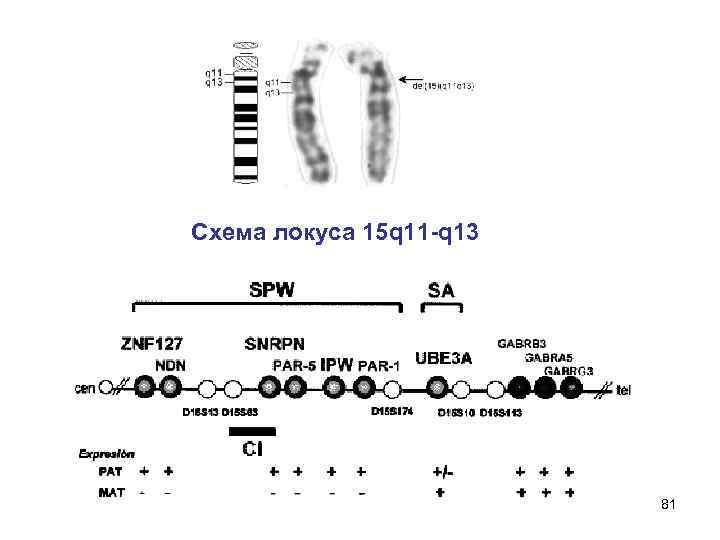 Схема локуса 15 q 11 -q 13 81
Схема локуса 15 q 11 -q 13 81
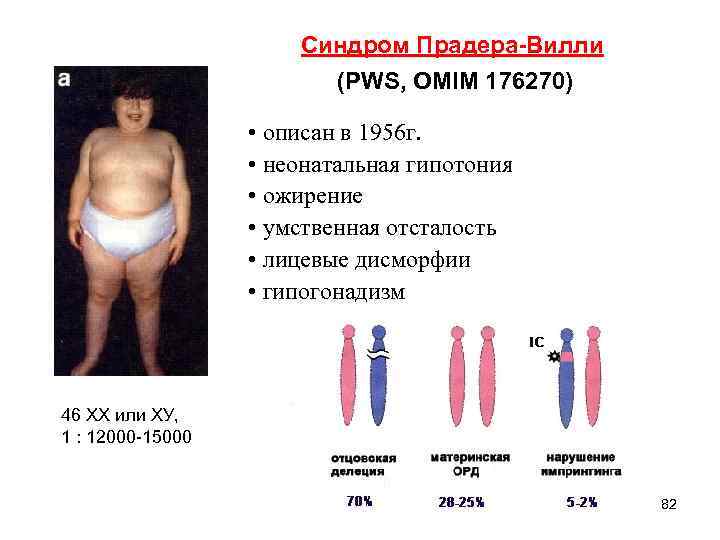 Синдром Прадера-Вилли (PWS, OMIM 176270) • описан в 1956 г. • неонатальная гипотония • ожирение • умственная отсталость • лицевые дисморфии • гипогонадизм 46 XX или ХУ, 1 : 12000 -15000 82
Синдром Прадера-Вилли (PWS, OMIM 176270) • описан в 1956 г. • неонатальная гипотония • ожирение • умственная отсталость • лицевые дисморфии • гипогонадизм 46 XX или ХУ, 1 : 12000 -15000 82
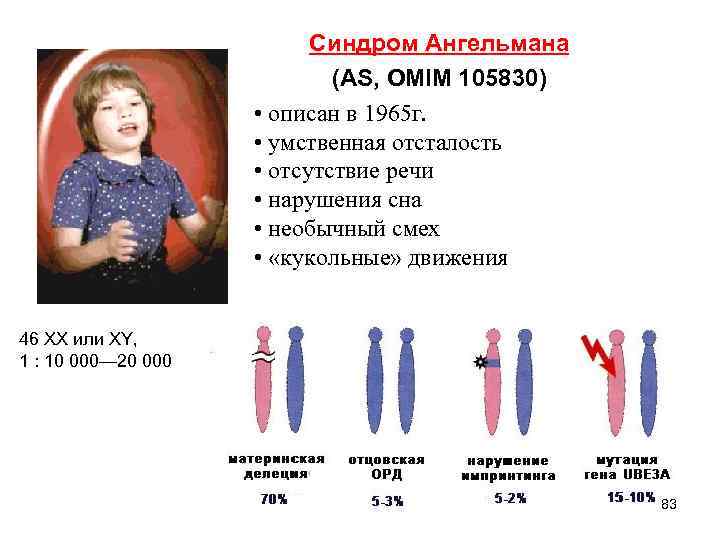 Синдром Ангельмана (AS, OMIM 105830) • описан в 1965 г. • умственная отсталость • отсутствие речи • нарушения сна • необычный смех • «кукольные» движения 46 XX или XY, 1 : 10 000— 20 000 83
Синдром Ангельмана (AS, OMIM 105830) • описан в 1965 г. • умственная отсталость • отсутствие речи • нарушения сна • необычный смех • «кукольные» движения 46 XX или XY, 1 : 10 000— 20 000 83
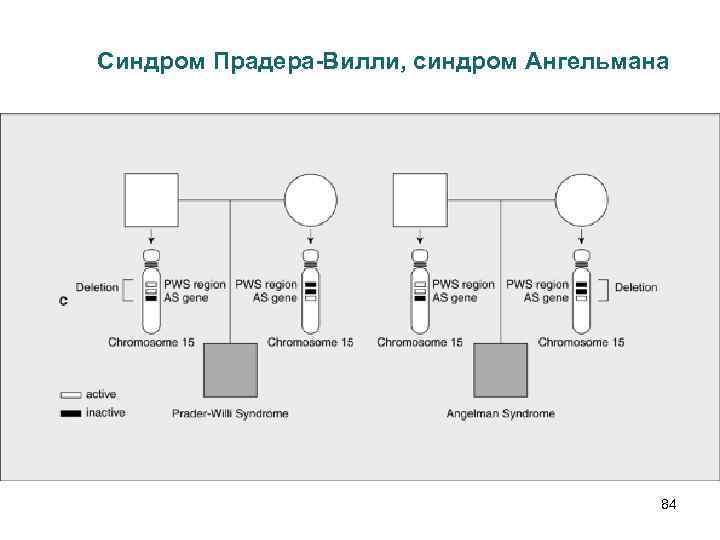 Синдром Прадера-Вилли, синдром Ангельмана 84
Синдром Прадера-Вилли, синдром Ангельмана 84

 Интерференция РНК (RNAi) и регуляция экспрессии генов
Интерференция РНК (RNAi) и регуляция экспрессии генов
 Нобелевская премия по физиологии и медицине 2006 год "RNA interference – gene silencing by double-stranded RNA" Andrew Z. Fire Craig C. Mello 87
Нобелевская премия по физиологии и медицине 2006 год "RNA interference – gene silencing by double-stranded RNA" Andrew Z. Fire Craig C. Mello 87
 Предположение Fire & Mello: Двуцепочечные РНК (ds. RNA) – запускающий механизм (триггер) системы интерференции РНК. 88
Предположение Fire & Mello: Двуцепочечные РНК (ds. RNA) – запускающий механизм (триггер) системы интерференции РНК. 88
 Интерференция РНК – это замолкание (сайленсинг) генов, обеспечиваемое двуцепочечными молекулами РНК (ds. РНК). Явление интерференции РНК открыто в 1998 г. у Nematoda (Fire et al. , 1998) 89
Интерференция РНК – это замолкание (сайленсинг) генов, обеспечиваемое двуцепочечными молекулами РНК (ds. РНК). Явление интерференции РНК открыто в 1998 г. у Nematoda (Fire et al. , 1998) 89
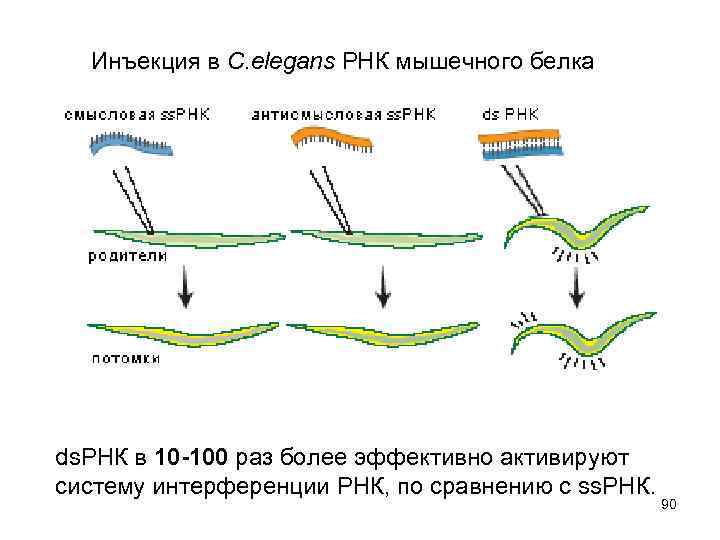 Инъекция в C. elegans РНК мышечного белка ds. РНК в 10 -100 раз более эффективно активируют систему интерференции РНК, по сравнению с ss. РНК. 90
Инъекция в C. elegans РНК мышечного белка ds. РНК в 10 -100 раз более эффективно активируют систему интерференции РНК, по сравнению с ss. РНК. 90
 Fire A. , Xu S. Q. , Montgomery M. K. , Kostas S. A. , Driver S. E. , Mello C. C. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature 391, 806– 811 (1998). Эффект генетического сайленсинга посредством интерференции РНК: распространяется в тканях организма (!) наследуется (!!!) 91
Fire A. , Xu S. Q. , Montgomery M. K. , Kostas S. A. , Driver S. E. , Mello C. C. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature 391, 806– 811 (1998). Эффект генетического сайленсинга посредством интерференции РНК: распространяется в тканях организма (!) наследуется (!!!) 91
 Механизм интерференции РНК • при исследовании интерференции РНК у растений обнаружены короткие молекулы РНК, маркирующие ген, подверженный сайленсингу; • в условиях in vitro воспроизведены биохимические реакции интерференции РНК. Малые интерферирующие РНК (si. RNAs – short interfering RNAs) – класс 21 -22 нуклеотидных двуцепочечных РНК, образующихся из более длинных двуцепочечных РНК. 92
Механизм интерференции РНК • при исследовании интерференции РНК у растений обнаружены короткие молекулы РНК, маркирующие ген, подверженный сайленсингу; • в условиях in vitro воспроизведены биохимические реакции интерференции РНК. Малые интерферирующие РНК (si. RNAs – short interfering RNAs) – класс 21 -22 нуклеотидных двуцепочечных РНК, образующихся из более длинных двуцепочечных РНК. 92
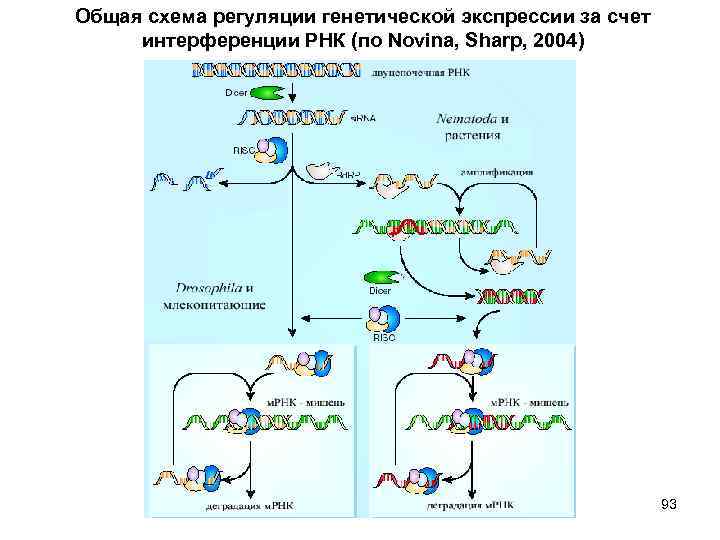 Общая схема регуляции генетической экспрессии за счет интерференции РНК (по Novina, Sharp, 2004) 93
Общая схема регуляции генетической экспрессии за счет интерференции РНК (по Novina, Sharp, 2004) 93
 Функции si. РНК 1. Сайленсинг мобильных генетических элементов; 2. Сайленсинг гетерохроматиновых повторов; 3. Сайленсинг генетического материала вирусного происхождения; 4. Ограничение степени экспрессии гена в определенных тканях. 94
Функции si. РНК 1. Сайленсинг мобильных генетических элементов; 2. Сайленсинг гетерохроматиновых повторов; 3. Сайленсинг генетического материала вирусного происхождения; 4. Ограничение степени экспрессии гена в определенных тканях. 94
 При выделение фракций коротких РНК (19 -25 нуклеотидов) из различных организмов обнаружен еще один класс малых РНК – микро. РНК. Микро. РНК (mi. RNAs - micro RNAs) – класс 19 -25 нуклеотидных одноцепочечных РНК, закодированных в уникальных генах геномов многоклеточных организмов. 95
При выделение фракций коротких РНК (19 -25 нуклеотидов) из различных организмов обнаружен еще один класс малых РНК – микро. РНК. Микро. РНК (mi. RNAs - micro RNAs) – класс 19 -25 нуклеотидных одноцепочечных РНК, закодированных в уникальных генах геномов многоклеточных организмов. 95
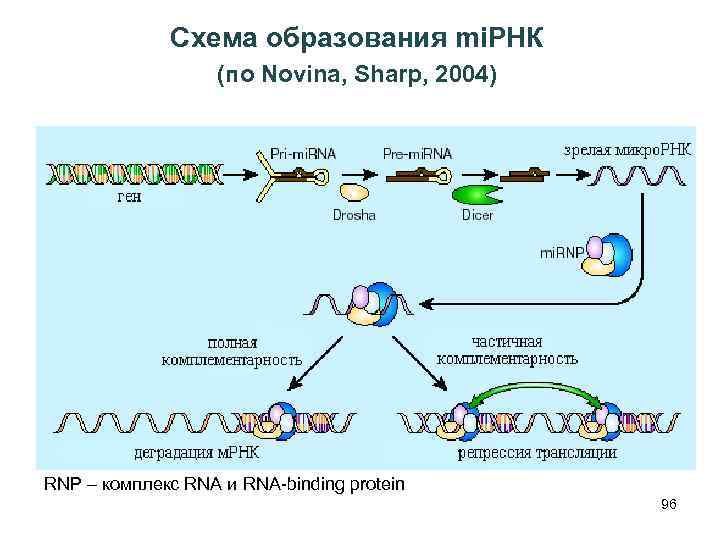 Схема образования mi. РНК (по Novina, Sharp, 2004) RNP – комплекс RNA и RNA-binding protein 96
Схема образования mi. РНК (по Novina, Sharp, 2004) RNP – комплекс RNA и RNA-binding protein 96
 Функция mi. РНК Обеспечивают сайленсинг различных генов, обычно, за счет частично комплементарного связывания с м. РНК, в результате которого блокируется ее трансляция. • один тип mi. РНК может регулировать трансляцию м. РНК более 100 различных генов; • степень ингибирования зависит от количества связывающихся mi. РНК (в 3’UTR м. РНК содержится несколько сайтов связывания). 97
Функция mi. РНК Обеспечивают сайленсинг различных генов, обычно, за счет частично комплементарного связывания с м. РНК, в результате которого блокируется ее трансляция. • один тип mi. РНК может регулировать трансляцию м. РНК более 100 различных генов; • степень ингибирования зависит от количества связывающихся mi. РНК (в 3’UTR м. РНК содержится несколько сайтов связывания). 97
 Отличия mi. РНК и si. РНК mi. РНК si. РНК • Продукт ds. РНК, закодированных в уникальных генах геномов многоклеточных организмов (>1% от всех генов у человека); • Продукт ds. РНК, образующихся в результате транскрипции транспозонов, гетерохроматиновых повторов или генетического материала вирусного происхождения ; • м. РНК может не разрушаться; • Один тип mi. РНК регулирует разные гены. • м. РНК разрушается; • Один тип si. РНК обычно регулирует только один тип м. РНК. 98
Отличия mi. РНК и si. РНК mi. РНК si. РНК • Продукт ds. РНК, закодированных в уникальных генах геномов многоклеточных организмов (>1% от всех генов у человека); • Продукт ds. РНК, образующихся в результате транскрипции транспозонов, гетерохроматиновых повторов или генетического материала вирусного происхождения ; • м. РНК может не разрушаться; • Один тип mi. РНК регулирует разные гены. • м. РНК разрушается; • Один тип si. РНК обычно регулирует только один тип м. РНК. 98
 • созданы библиотеки коротких РНК и ДНК- векторов, кодирующих короткие РНК, мишенями которых является около 8000 генов генома человека; • внедряется в практику терапевтическое применение синтетических коротких РНК для целенаправленного подавления генетической экспрессии при некоторых заболеваниях. 99
• созданы библиотеки коротких РНК и ДНК- векторов, кодирующих короткие РНК, мишенями которых является около 8000 генов генома человека; • внедряется в практику терапевтическое применение синтетических коротких РНК для целенаправленного подавления генетической экспрессии при некоторых заболеваниях. 99


