Генетика микроорганизмов и микробиологическая промышленность

Генетика микроорганизмов и микробиологическая промышленность

Понятие «микробиологическая промышленность» относится к крупному индустриальному производству, целиком основанному на деятельности микроорганизмов, и не охватывает всех случаев использования микроорганизмов в хозяйственной деятельности людей. На микробиологических процессах основаны виноделие, пивоварение, хлебопечение, сыроварение, производство пищевого уксуса, известные с глубокой древности и в настоящее время являющиеся важными отраслями пищевой промышленности. Традиционно эти технологии не относятся к микробиологическому производству.

Рождение специализированной микробиологической промышленности следует отнести к середине 40 х годов нашего века, когда было реализовано крупномасштабное производство антибиотиков. В течение 50 70 х годов микробиологическая промышленность сделала заметные успехи. Выросла номенклатура и масштабы производства антибиотиков для медицинских сельскохозяйственных целей. Было организовано производство кормового белка, аминокислот, витаминов, ферментных препаратов, биологических средств защиты растений, органических кислот и растворителей, полисахаридов, трансформации стероидов и алкалоидов, стимуляторов роста растений, микроорганизмов фиксаторов атмосферного азота и ряда других биологически активных препаратов. Табл. 1 иллюстрирует масштабы мирового производства некоторых продуктов микробиологического синтеза.

Со второй половины 70 х годов в связи с нарастающим исчерпанием природных ресурсов, загрязнением окружающей среды, ростом народонаселения, с одной стороны, и революционными открытиями в биологии — с другой, все большее внимание ученых, хозяйственных руководителей и правительств привлекает биотехнология, которая потенциально способна внести крупный вклад в решение перечисленных выше глобальных проблем. Микробиологическая индустрия, являющаяся существенной частью биотехнологии, вступает в 'настоящее время в новую фазу своего развития, характеризующуюся расширением масштаба производства, расширением сферы деятельности и увеличением влияния науки на производство.

В СССР микробиологическая промышленность была выделена в отдельную отрасль в 1966 г. (Главное управление микробиологической промышленности при Совете Министров СССР — Главмикробиопром) главным образом в связи с созданием крупного производства кормовых дрожжей на базе н парафинов нефти. В настоящее время очевидна своевременность и целесообразность этого шага. На предприятиях Главмикробиопрома сегодня сосредоточено все микробиологическое производство, за исключением производства медицинских антибиотиков и некоторых специальных медицинских препаратов.

В настоящее время отечественная микробиологическая промышленность производит сотни тысяч тонн кормовых дрожжей, тысячи тонн незаменимой аминокислоты — лизина, тысячи тонн биологических средств защиты растений, антибиотики для сельскохозяйственных животных, витамины, органические растворители, этиловый спирт и много других видов продукции. В течение длительного времени темпы роста микробиологической промышленности существенно выше, чем промышленности в целом. Особенно важно, что Главмикробиопром обладает сетью отраслевых научно исследовательских к проектных организаций, способных адаптировать достижения современной науки для развития производства.

Генетика — наука о законах на следственности и изменчивости организмов — является фундаментом биологических наук, одной из первых количественных наук в биологии. Бурное развитие генетики микроорганизмов началось с 40 х годов нашего века и почти совпадает по времени с возникновением современной микробиологической промышленности. Роль генетики микроорганизмов особенно велика в расшифровке процессов жизнедеятельности на молекулярном уровне, т. е. в решении фундаментальных вопросов биологии.
Достаточно вспомнить, что доказательство того, что ДНК (дезоксирибонуклеиновая кислота) служит материальным носителем наследственной информации было получено американскими исследователями Эйвери, Мак Лео дом и Маккарти в 1944 г. при изучении бактерий рода пневмококков.

Преимуществом микроорганизмов (как для организации промышленного производства на их основе, так и для изучения генетических закономерностей) является их уникальная способность к быстрому размножению. Для различных видов бактерий период деления (смены поколений) составляет при оптимальных условиях роста от 30 мин до 1— 2 ч. Другой особенностью, также важной и в теоретическом и в практическом аспекте, является способность микроорганизмов к росту на очень простых питательных средах. Минимальные среды включают минеральные соли один источник углерода, например, глюкозу, или уксусную кислоту, или н парафин и т. д.
Вследствие скудности морфологических признаков, отсутствия у большинства микроорганизмов видимых в световом микроскопе хромосом до конца 40 х годов бытовало мнение, что на микроорганизмы не распространяются генетические закономерности, хорошо к этому времени выявленные для высших организмов.

Положение изменилось коренным образом в результате исследований Лурия и Дельбрюка, показавших, что бактерии подчиняются обычным мутационным закономерностям. Важнейшей посылкой развития генетики микроорганизмов явился также принцип клонального анализа, последовательно разработанного американским исследователем Ледербергом. Суть метода заключается в рассеве бактерий на твердую питательную среду таким образом, чтобы отдельные бактерии были удалены друг от друга и после периода роста, возникшие колонии представляли потомство единичной клетки.

В течение 50 х годов был открыт и введен в практику научных исследований ряд методов генетического обмена у микроорганизмов: трансформация (поглощение клеткой ДНК из внешней среды), конъюгация — половой процесс, осуществляемый при непосредственном контакте донорной и реципиентной клеток, трансдукция — обмен с помощью бактериофагов (вирусов бактерий). Следует отметить, что развитие генетики микроорганизмов осуществлялось главным образом на модельном объекте — бактерии кишечной палочке (Е. coli) и ее бактериофагах. Сосредоточение усилий многих исследователей на одном объекте дало впечатляющие фундаментальные результаты. Были открыты принципы регуляции активности генов у бактерий, изучены механизмы репликации ДНК, транскрипции, трансляции, расшифрован генетический код, открыты и изучены готазмиды и мигрирующие генетические элементы — транспозоны.

Все перечисленные открытия имеют общебиологическое значение и вместе с успехами биохимии послужили основанием для развития молекулярной биологии, молекулярной генетики и в последние годы новой мощной методологии — генной инженерии. Вместе с тем арсенал современной генетики микроорганизмов до последнего времени не применялся в полном объеме для целей создания высокоактивных промышленных штаммов.

Основная причина этого обстоятельства — недостаточная генетическая изученность микроорганизмов, традиционно используемых промышленностью, отсутствие у многих из них известных методов генетического обмена, отсутствие знаний о метаболических путях биосинтеза целевых продуктов. В силу перечисленных обстоятельств основным методом повышения активности промышленных штаммов с 50 х годов до нашего времени остается индуцированный мутагенез и ступенчатый отбор. В этом случае популяцию клеток обрабатывают мутагеном (чаще всего специальным химическим веществом или ультрафиолетовым светом), рассевают на питательную среду и анализируют популяции, возникшие при размножении отдельных клеток (клональный анализ).
Отобрав более продуктивный клон, процедуру повторяют (ступенчатый отбор). Метод чрезвычайно трудоемок. Мутагенез не специфичен, большинство мутаций вредно или летально для клетки, следовательно, нужная мутация (или набор мутаций) возникает крайне редко.

Преимуществом метода является то, что можно ничего не знать о путях биосинтеза целевого продукта, не знать генетики селектируемого микроорганизма. Достаточно знать, что химические и физические мутагены оказывают свое действие. Недостаток (кроме трудоемкости) непредсказуемость результатов. Тем не менее этот метод дал замечательные результаты, например, в селекции продуцентов антибиотиков (табл. 2). Существует ряд приемов, которые значительно упрощают и ускоряют селекцию. Так, мощным методом является селекция на устойчивость микробной клетки к структурному аналогу целевого продукта.

Все синтезы метаболитов в микробной клетке обычно находятся под негативным контролем продукта, т. е. повышение внутриклеточной концентрации того или иного метаболита снижает или прекращает его синтез. Такая обратная связь может выражаться в подавлении активности ферментов, участвующих в биосинтезе (аллостерическое регулирование) и в прекращении синтеза этих ферментов. Мутационным путем можно получить такое изменение фермента, чтобы он, сохраняя активность, терял способность к аллостерической регуляции.

Можно изменить и регуляторные сайты генов так, что избыток продукта не будет влиять на интенсивность их синтеза. Структурные аналоги это вещества, близкородственные целевому метаболиту, которые клетка «путает» с метаболитом. В присутствии аналога в среде рост нормальной клетки тормозится или прекращается, так как аналог выключает синтез метаболита по приведенным схемам, но не может заменить метаболита функционально. В присутствии аналога в среде выживают лишь те клетки, которые тем или иным путем преодолели барьеры негативной регуляции. Как правело, штамм прдуцент должен нести в своем геноме несколько необходимых для сверхпродукции мутаций. Стратегия ступенчатого отбора предполагает последовательное введение мутаций Любой метод генетического обмена может устранить из потомств вредные мутации и собрать в одной клетке нужные.

Одним из важнейших приемов генетики микроорганизмов сегодня является метод слияния протопластов, который применим ко многим организмам, в том числе и к низшим грибам и актиномицетам продуцентам антибиотиков. Метод заключается в удалении оболочек клеток ферментативным методом, слиянии образовавшихся сферопластов и последующей регенерации оболочек. В качестве положительного практического примера можно указать на работу Хэмлина и Болла, которым путем слияния протопластов удалось получить рекомбинант, производящий на 40% больше антибиотика (цефалоспорина), чем лучший из родительских штаммов.
В настоящее время перспективы применения генетических и генно инженерных методов для улучшения промышленных штаммов или для конструирования штаммов для новых производств более чем обнадеживающие. Такое заключение имеет основанием бурное развитие генетики промышленных» микроорганизмов бацилл, актиномицетов, дрожжей, псевдомонад и т. д. , наблюдаемое в последние десять лет.

Другая важная предпосылка-это возможность создания штаммов продуцентов на базе хорошо изученных микроорганизмов, таких, как E. coli или В ас. subtil is (табл. 3). Основными направлениями применения генетики микроорганизмов в микробиологической промышленности в перспективе можно считать следующие:

1. Ускорение традиционной селекционной работы, что является наиболее эффективным методом интенсификации действующих производств, так как не требует значительных капиталовложений. 2. Подбор продуцентов для действующих производств, относящихся к другим видам микроорганизмов. Новый вид микроорганизма может обладать более быстрым метаболизмом, усваивать новые субстраты. . Этот путь может повысить объем производства и расширить сырьевую базу промышленности.

3. Генная инженерия и (или) межвидовое скрещивание позволяют думать о производстве новых продуктов на базе уже освоенных промышленностью видов микроорганизмов. Например, можно представить себе перенос генов термостабильных протеаз или амилаз из термофилов в промышленные штаммы бацилл. 4. Генная инженерия в сочетании с генетическими приемами стабилизации штаммов может привести к созданию микроорганизмов с измененным (улучшенным) аминокислотным составом белков, что важно для таких кормовых добавок, как дрожжи.

5. Генетика микроорганизмов и генная инженерия создадут штаммы для новых производств-заменителей сахара (сладких белков и пептидов), белков человека и сельскохозяйственных животных, используемых в медицине и ветеринарии, - инсулина, интерферона, вакцин, гормонов и т. д. Приведенными сведениями, конечно, не исчерпываются возможности генетики и генной инженерии в интенсификации и расширении сферы деятельности микробиологической промышленности. Стремительное развитие современной генетики и быстрый рост промышленности несомненно вызовут появление новых направлений практического использования достижений науки в производстве.
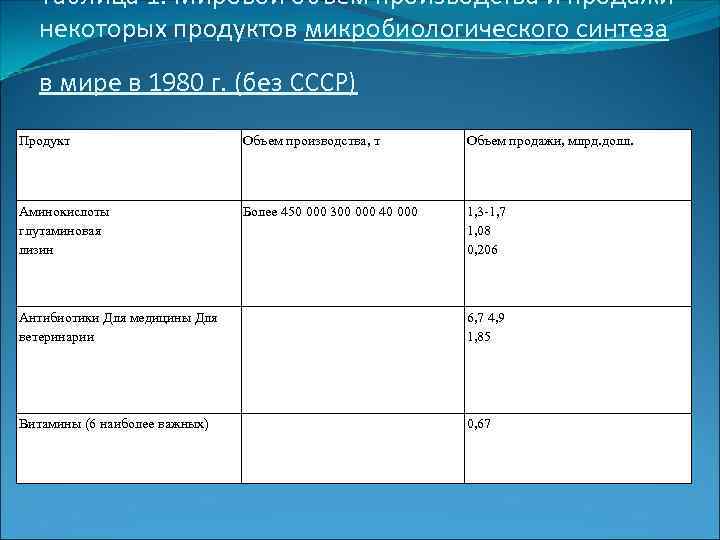
Таблица 1. Мировой объем производства и продажи некоторых продуктов микробиологического синтеза в мире в 1980 г. (без СССР) Продукт Объем производства, т Объем продажи, млрд. долл. Аминокислоты Более 450 000 300 000 40 000 1, 3 -1, 7 глутаминовая 1, 08 лизин 0, 206 Антибиотики Для медицины Для 6, 7 4, 9 ветеринарии 1, 85 Витамины (6 наиболее важных) 0, 67
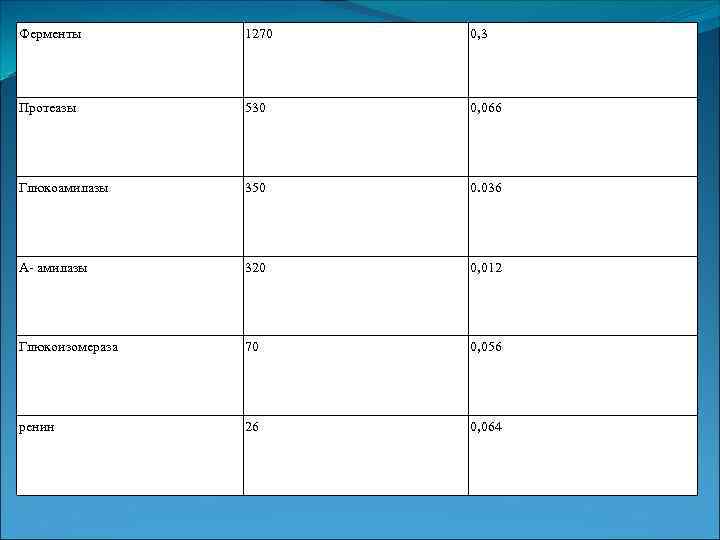
Ферменты 1270 0, 3 Протеазы 530 0, 066 Глюкоамилазы 350 0. 036 А- амилазы 320 0, 012 Глюкоизомераза 70 0, 056 ренин 26 0, 064
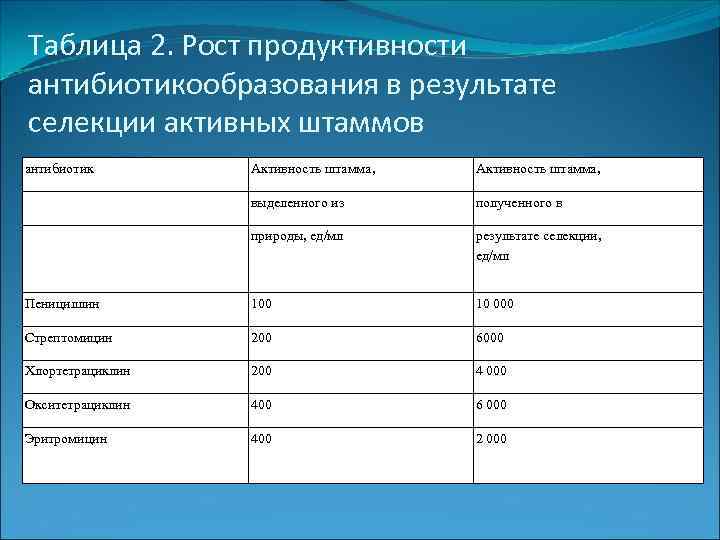
Таблица 2. Рост продуктивности антибиотикообразования в результате селекции активных штаммов антибиотик Активность штамма, выделенного из полученного в природы, ед/мл результате селекции, ед/мл Пенициллин 100 10 000 Стрептомицин 200 6000 Хлортетрациклин 200 4 000 Окситетрациклин 400 6 000 Эритромицин 400 2 000

Таблица 3. Создание штаммов-продуцентов аминокислот на базе Е. Coli Продукт Этапы конструирования Показатели биосинтеза L-треонин L- 1. Селекция с аналогами и получение 30 г/л за 40 ч ферментации пролин мутаций, снимающих подавление синтеза на среде с глюкозой избытком треонина и препятствующих 27 г/л за 48 ч ферментации деградации треонина в клетке на среде с глюкозой 2. Введение мутации, обеспечивающей общеклеточную положительную регуляцию сверсинтеза аминокислот 3. Амплификация генов (трех) треонинового оперона на многокопийной плазмиде 4. Введение (конъюнгация) генов, ответственных за способность использовать сахарозу как источник углерода 1. Получение штамма сверхпродукта глутаминовой кислоты (предшественник пролина) 2. Мутация, препятствующая деградации L- пролина 3. Клонирование трех генов, биосинтез и объединение их на одной многокопийной плазмиде (амплефикация)
Показатели продуктивности этих штаммов значительно выше, чем у штаммов, полученных классическими методами селекции с аналогами промышленного микроорганизма С. glutamicum.
Генетика микроорганизмов.ppt
- Количество слайдов: 29

