Короткий курс генетики КЦ 16.ppt
- Количество слайдов: 142

Генетика клеточного цикла Электронно-лекционный курс Выборка к зачету 2016
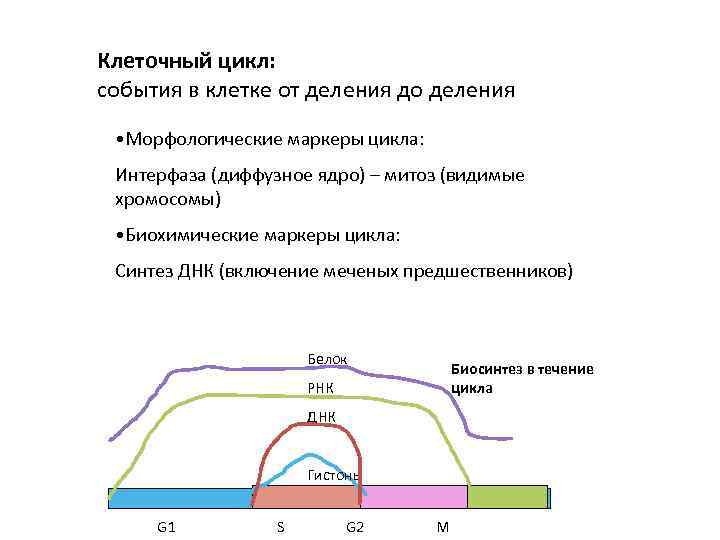
Клеточный цикл: события в клетке от деления до деления • Морфологические маркеры цикла: Интерфаза (диффузное ядро) – митоз (видимые хромосомы) • Биохимические маркеры цикла: Синтез ДНК (включение меченых предшественников) Белок Биосинтез в течение цикла РНК ДНК Гистоны G 1 S G 2 M
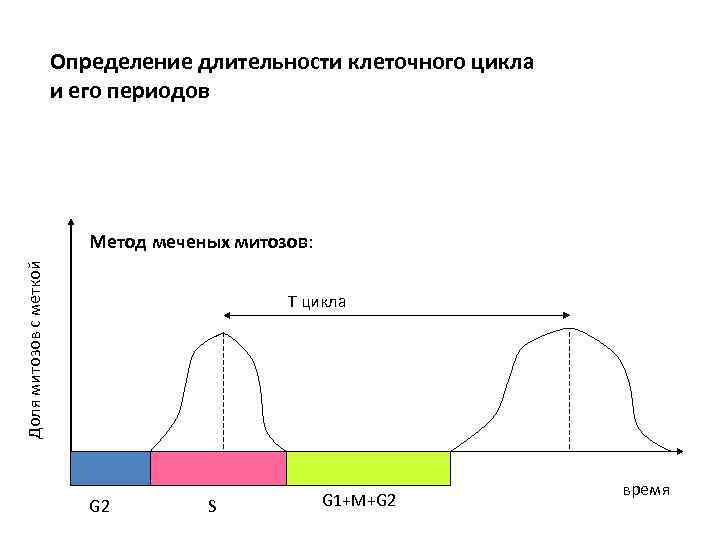
Определение длительности клеточного цикла и его периодов Доля митозов с меткой Метод меченых митозов: Т цикла G 2 S G 1+M+G 2 время
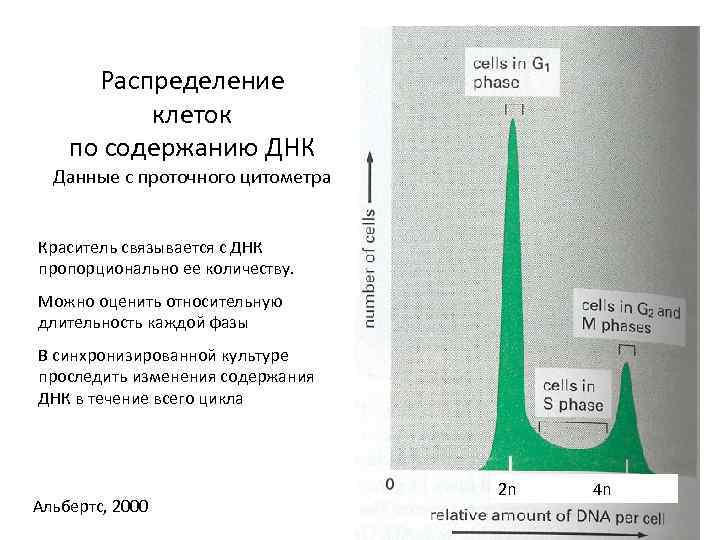
Распределение клеток по содержанию ДНК Данные с проточного цитометра Краситель связывается с ДНК пропорционально ее количеству. Можно оценить относительную длительность каждой фазы В синхронизированной культуре проследить изменения содержания ДНК в течение всего цикла Альбертс, 2000 2 n 4 n

Периоды клеточного цикла Варианты длительности клеточных циклов: • Клетки делящиеся Длительность периодов • Клетки эмбриональные клеточного цикла делящейся • Клетки в состоянии покоя клетки млекопитающего

Разработаны методы культивирования клеток Как синхронизировать циклы клеток? Синхронизация индукционная: обработка агентом, блокирующим (обратимо или нет) специфический этап в клетке G 1 - гидроксимочевина блокируют репликацию -остановка в - колхицин, винбластин, колцемид – блокируют веретено деления - остановка в метафазе Синхронизация селекционная: отбирают субпопуляцию клеток по их принадлежности к какой-либо фазе цикла. и G 2 -центрифугирование по массе – разделяют популяции G 1 -смывают плохо прикрепленные митотические клетки – получают популяцию в начале G 1 Синхронизация естественная: деления дробления у амфибий и некоторых беспозвоночных
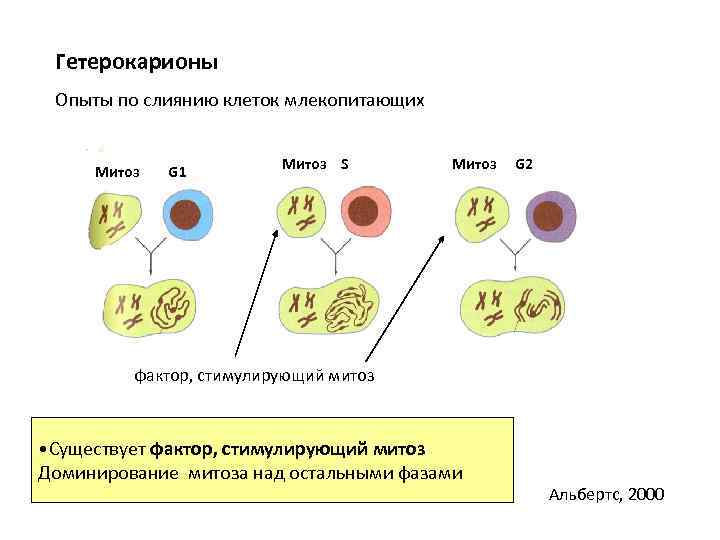
Гетерокарионы Опыты по слиянию клеток млекопитающих Митоз G 1 Митоз S Митоз G 2 фактор, стимулирующий митоз • Существует фактор, стимулирующий митоз Доминирование митоза над остальными фазами Альбертс, 2000
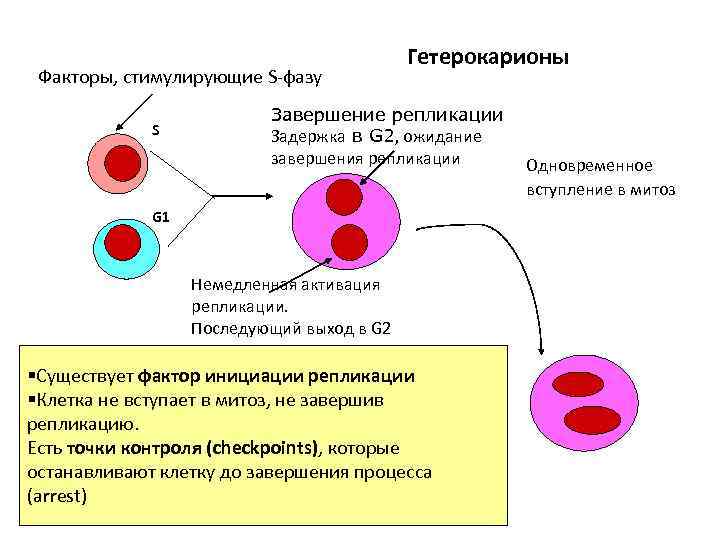
Факторы, стимулирующие S-фазу S Гетерокарионы Завершение репликации Задержка в G 2, ожидание завершения репликации G 1 Немедленная активация репликации. Последующий выход в G 2 §Существует фактор инициации репликации §Клетка не вступает в митоз, не завершив репликацию. Есть точки контроля (checkpoints), которые останавливают клетку до завершения процесса (arrest) Одновременное вступление в митоз
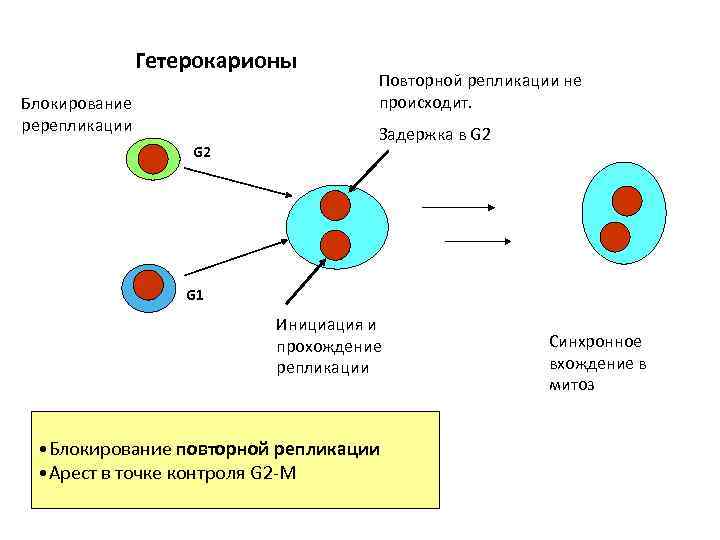
Гетерокарионы Блокирование ререпликации G 2 Повторной репликации не происходит. Задержка в G 2 G 1 Инициация и прохождение репликации • Блокирование повторной репликации • Арест в точке контроля G 2 -M Синхронное вхождение в митоз
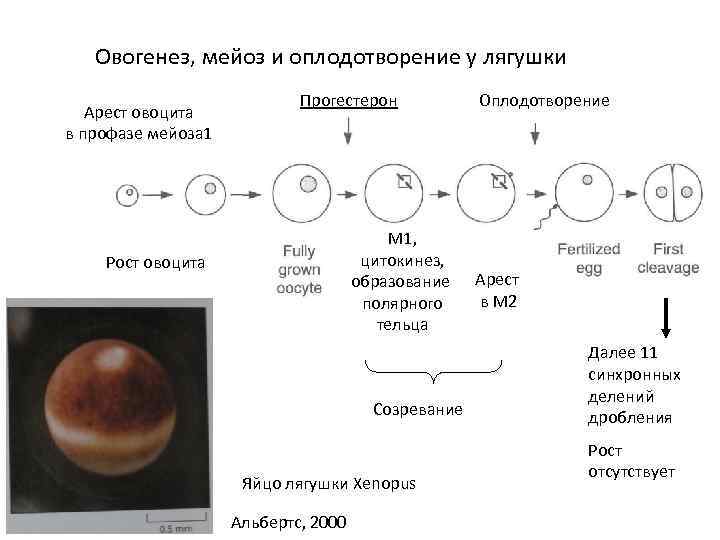
Овогенез, мейоз и оплодотворение у лягушки Арест овоцита в профазе мейоза 1 Прогестерон M 1, цитокинез, образование полярного тельца Рост овоцита Созревание Яйцо лягушки Xenopus Альбертс, 2000 Оплодотворение Арест в М 2 Далее 11 синхронных делений дробления Рост отсутствует
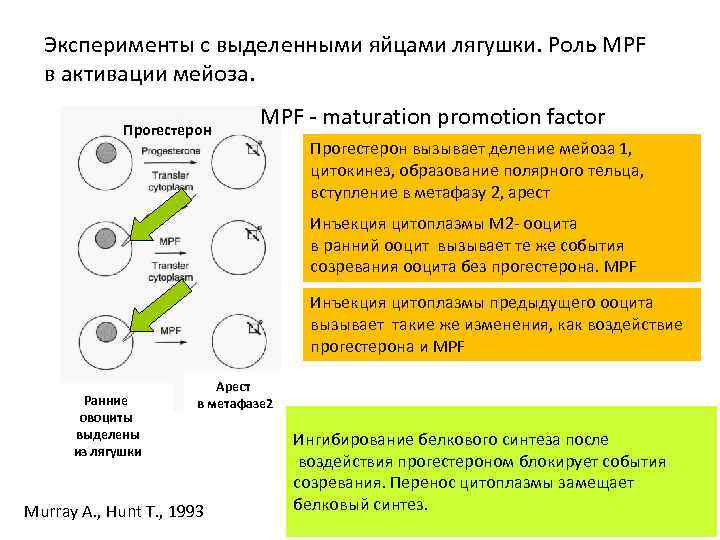
Эксперименты с выделенными яйцами лягушки. Роль MPF в активации мейоза. Прогестерон MPF - maturation promotion factor Прогестерон вызывает деление мейоза 1, цитокинез, образование полярного тельца, вступление в метафазу 2, арест Инъекция цитоплазмы М 2 - ооцита в ранний ооцит вызывает те же события созревания ооцита без прогестерона. MPF Инъекция цитоплазмы предыдущего ооцита вызывает такие же изменения, как воздействие прогестерона и MPF Ранние овоциты выделены из лягушки Арест в метафазе 2 Murray A. , Hunt T. , 1993 Ингибирование белкового синтеза после воздействия прогестероном блокирует события созревания. Перенос цитоплазмы замещает белковый синтез.
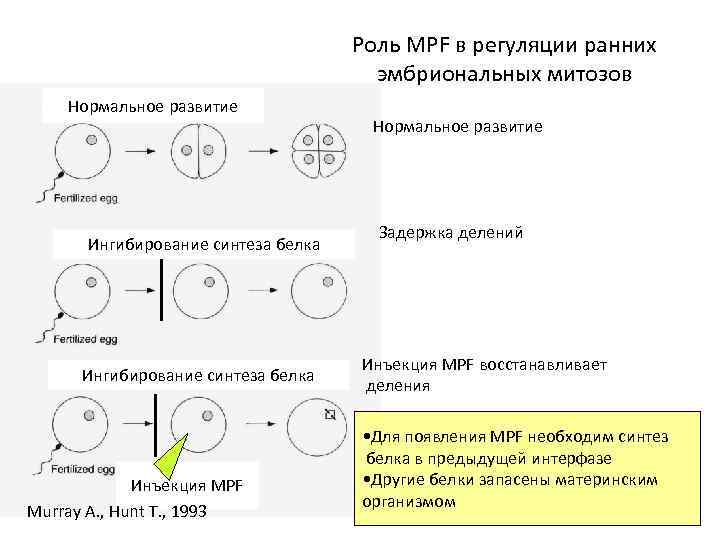
Роль MPF в регуляции ранних эмбриональных митозов Нормальное развитие Ингибирование синтеза белка Инъекция MPF Murray A. , Hunt T. , 1993 Нормальное развитие Задержка делений Инъекция MPF восстанавливает деления • Для появления MPF необходим синтез белка в предыдущей интерфазе • Другие белки запасены материнским организмом
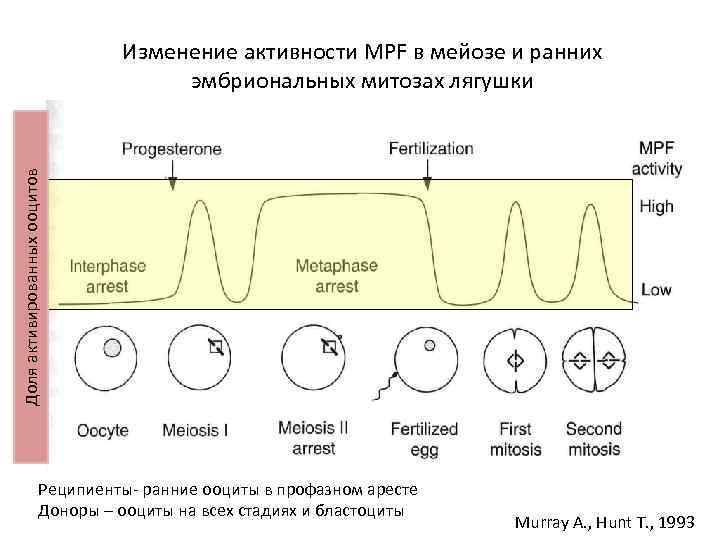
Доля активированных ооцитов Изменение активности MPF в мейозе и ранних эмбриональных митозах лягушки Реципиенты- ранние ооциты в профазном аресте Доноры – ооциты на всех стадиях и бластоциты Murray A. , Hunt T. , 1993
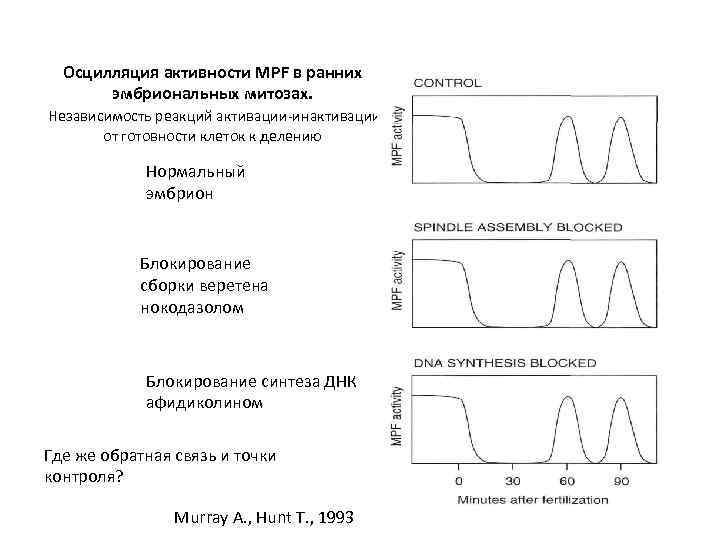
Осцилляция активности MPF в ранних эмбриональных митозах. Независимость реакций активации-инактивации от готовности клеток к делению Нормальный эмбрион Блокирование сборки веретена нокодазолом Блокирование синтеза ДНК афидиколином Где же обратная связь и точки контроля? Murray A. , Hunt T. , 1993

Мейоз и ранние эмбриональные митозы Косвенные данные о существовании MPF – по видимым изменениям, происходящим в клетке Появлению MPF всегда предшествует белковый синтез – поиск белка, синтезируемого к метафазе. В остальном «машина» клеточного цикла работает автономно Блокирование репликации и разрушение ядра не останавливает остальных событий цикла – это не типично для большинства клеток
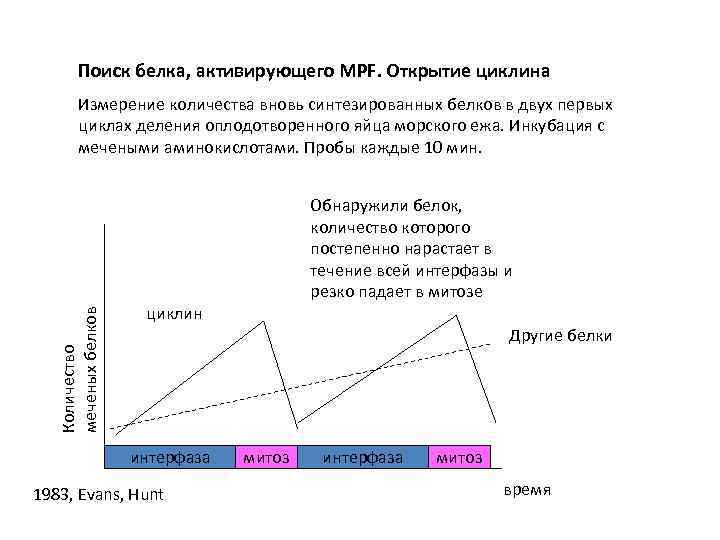
Поиск белка, активирующего MPF. Открытие циклина Количество меченых белков Измерение количества вновь синтезированных белков в двух первых циклах деления оплодотворенного яйца морского ежа. Инкубация с мечеными аминокислотами. Пробы каждые 10 мин. Обнаружили белок, количество которого постепенно нарастает в течение всей интерфазы и резко падает в митозе циклин Другие белки интерфаза 1983, Evans, Hunt митоз интерфаза митоз время

Циклины нашли у всех эукариот: дрожжей, кольчатых червей, насекомых, моллюсков, иглокожих, амфибий, млекопитающих и растений Первая простая модель активации MPF: Аккумуляция циклина активирует MPF и митоз: циклин- часть MPF? Активный MPF вызывает деградацию циклина и выход из митоза? Деградация циклина инактивирует MPF? Как соотносятся циклин и MPF? Противоречивость фактов, полученных при изучении клеточных культур млекопитающих и цикла ранних эмбриональных делений. Необходимость нового объекта
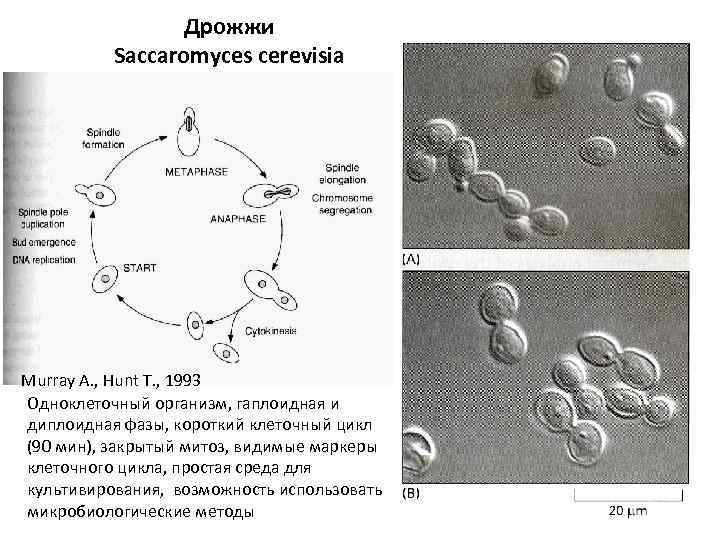
Дрожжи Saccaromyces cerevisia Murray A. , Hunt T. , 1993 Одноклеточный организм, гаплоидная и диплоидная фазы, короткий клеточный цикл (90 мин), закрытый митоз, видимые маркеры клеточного цикла, простая среда для культивирования, возможность использовать микробиологические методы
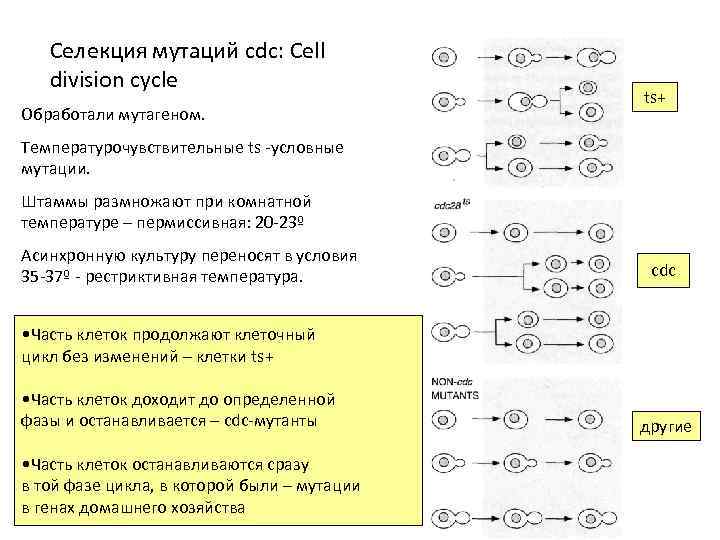
Селекция мутаций cdc: Cell division cycle Обработали мутагеном. ts+ Температурочувствительные ts -условные мутации. Штаммы размножают при комнатной температуре – пермиссивная: 20 -23º Асинхронную культуру переносят в условия 35 -37º - рестриктивная температура. cdc • Часть клеток продолжают клеточный цикл без изменений – клетки ts+ • Часть клеток доходит до определенной фазы и останавливается – cdc-мутанты • Часть клеток останавливаются сразу в той фазе цикла, в которой были – мутации в генах домашнего хозяйства другие
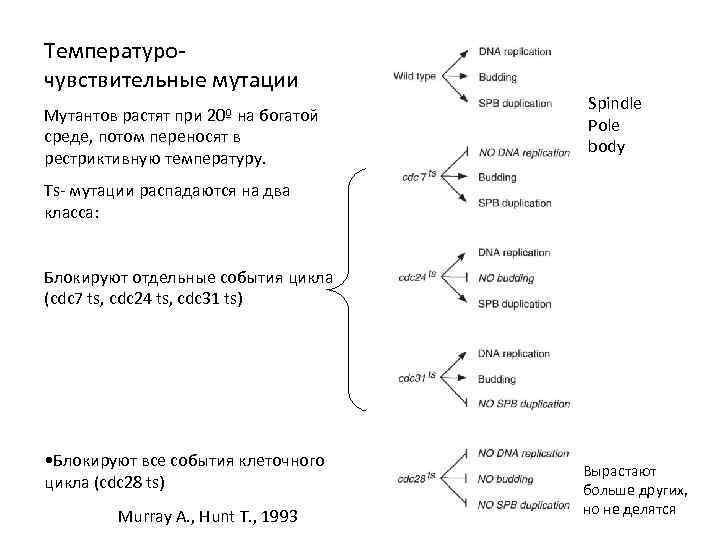
Температурочувствительные мутации Мутантов растят при 20º на богатой среде, потом переносят в рестриктивную температуру. Spindle Pole body Ts- мутации распадаются на два класса: Блокируют отдельные события цикла (cdc 7 ts, cdc 24 ts, cdc 31 ts) • Блокируют все события клеточного цикла (cdc 28 ts) Murray A. , Hunt T. , 1993 Вырастают больше других, но не делятся
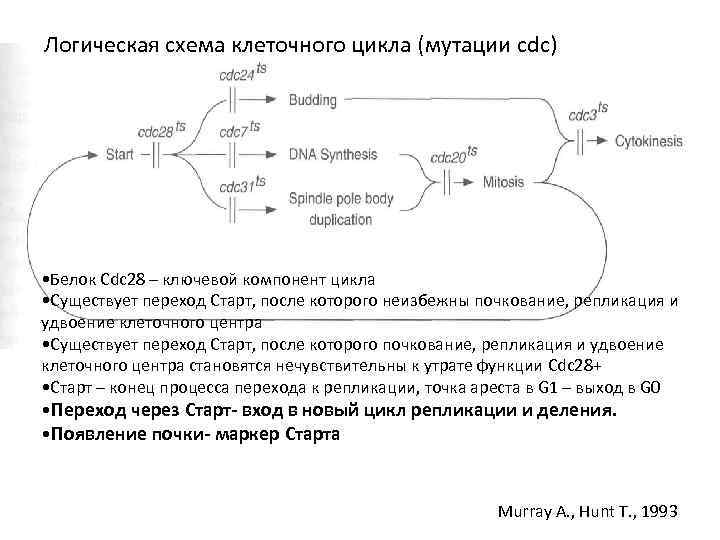
Логическая схема клеточного цикла (мутации cdc) • Белок Сdc 28 – ключевой компонент цикла • Существует переход Старт, после которого неизбежны почкование, репликация и удвоение клеточного центра • Существует переход Старт, после которого почкование, репликация и удвоение клеточного центра становятся нечувствительны к утрате функции Cdc 28+ • Старт – конец процесса перехода к репликации, точка ареста в G 1 – выход в G 0 • Переход через Старт- вход в новый цикл репликации и деления. • Появление почки- маркер Старта Murray A. , Hunt T. , 1993
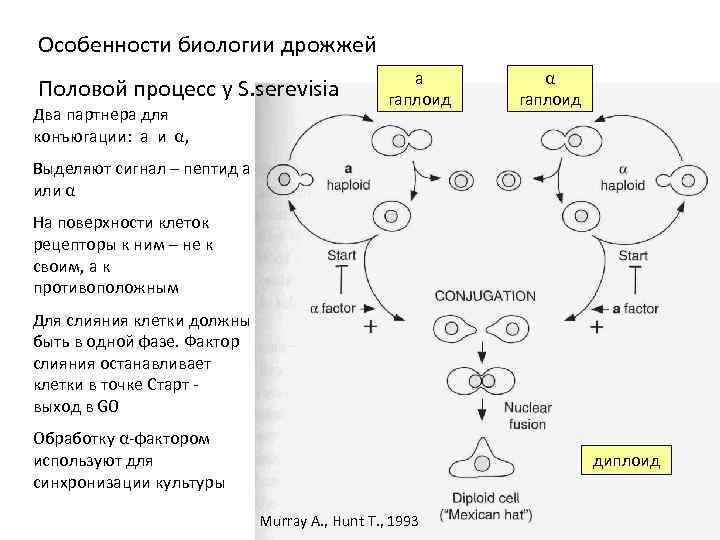
Особенности биологии дрожжей Половой процесс у S. serevisia Два партнера для конъюгации: a и α, a гаплоид α гаплоид Выделяют сигнал – пептид а или α На поверхности клеток рецепторы к ним – не к своим, а к противоположным Для слияния клетки должны быть в одной фазе. Фактор слияния останавливает клетки в точке Старт выход в G 0 Обработку α-фактором используют для синхронизации культуры диплоид Murray A. , Hunt T. , 1993
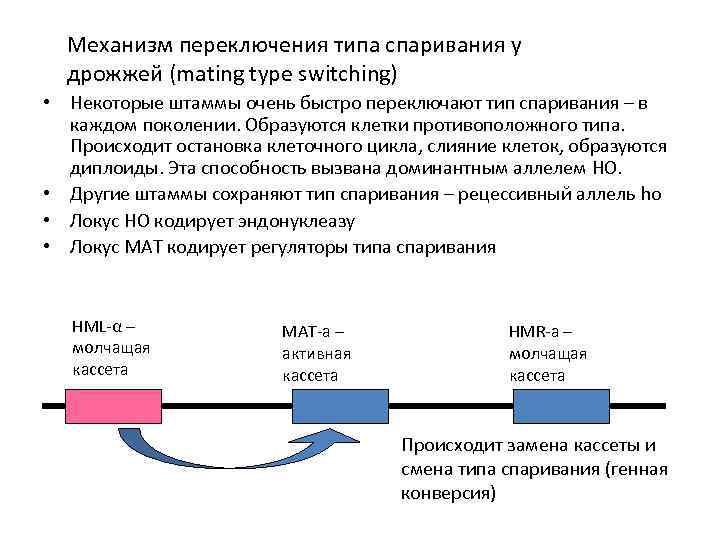
Механизм переключения типа спаривания у дрожжей (mating type switching) • Некоторые штаммы очень быстро переключают тип спаривания – в каждом поколении. Образуются клетки противоположного типа. Происходит остановка клеточного цикла, слияние клеток, образуются диплоиды. Эта способность вызвана доминантным аллелем HO. • Другие штаммы сохраняют тип спаривания – рецессивный аллель ho • Локус HO кодирует эндонуклеазу • Локус МАТ кодирует регуляторы типа спаривания HML-α – молчащая кассета MAT-a – активная кассета HMR-a – молчащая кассета Происходит замена кассеты и смена типа спаривания (генная конверсия)
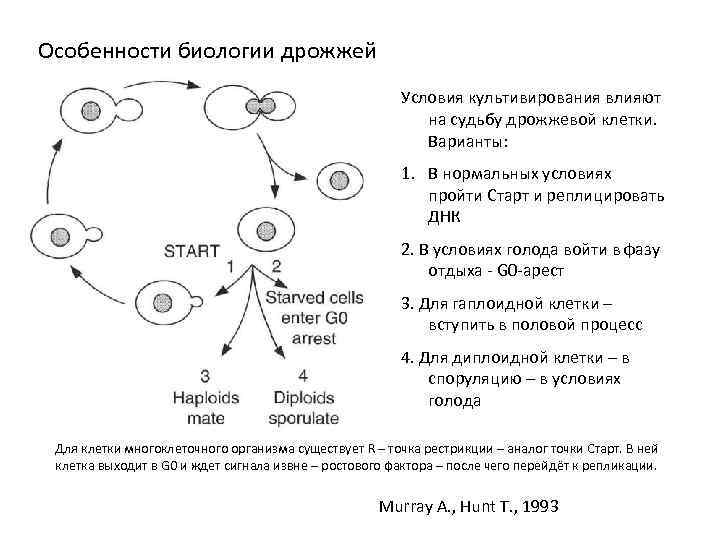
Особенности биологии дрожжей Условия культивирования влияют на судьбу дрожжевой клетки. Варианты: 1. В нормальных условиях пройти Старт и реплицировать ДНК 2. В условиях голода войти в фазу отдыха - G 0 -арест 3. Для гаплоидной клетки – вступить в половой процесс 4. Для диплоидной клетки – в споруляцию – в условиях голода Для клетки многоклеточного организма существует R – точка рестрикции – аналог точки Старт. В ней клетка выходит в G 0 и ждет сигнала извне – ростового фактора – после чего перейдёт к репликации. Murray A. , Hunt T. , 1993
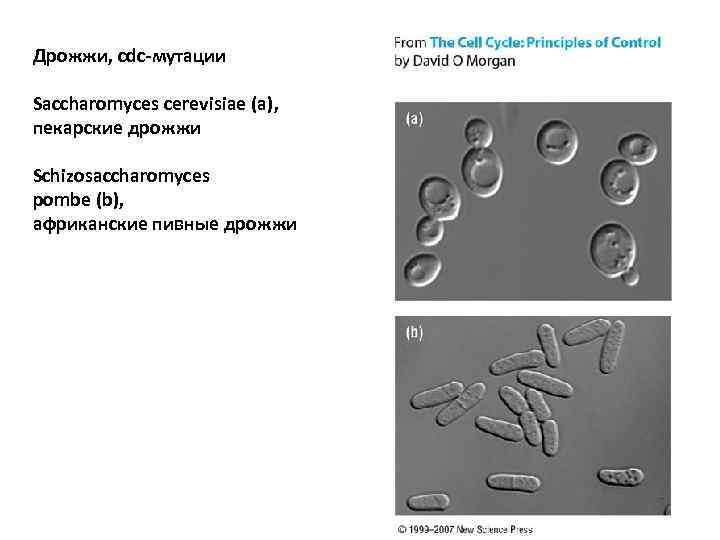
Дрожжи, cdc-мутации Saccharomyces cerevisiae (a), пекарские дрожжи Schizosaccharomyces pombe (b), африканские пивные дрожжи
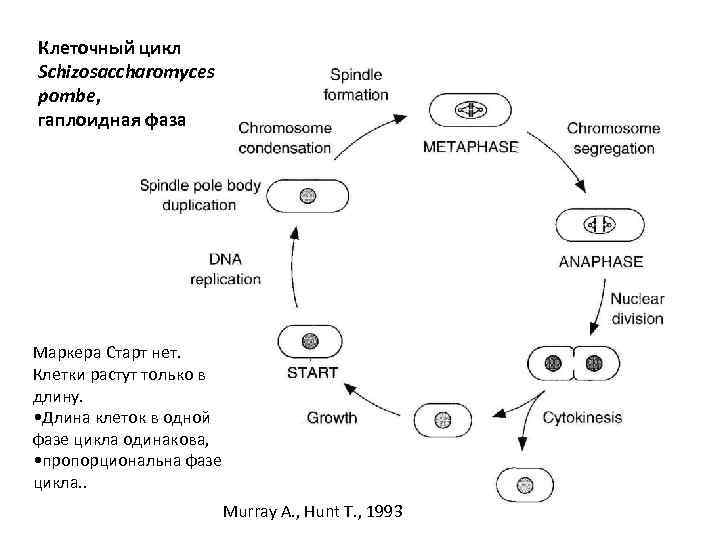
Клеточный цикл Schizosaccharomyces pombe, гаплоидная фаза Маркера Старт нет. Клетки растут только в длину. • Длина клеток в одной фазе цикла одинакова, • пропорциональна фазе цикла. . Murray A. , Hunt T. , 1993
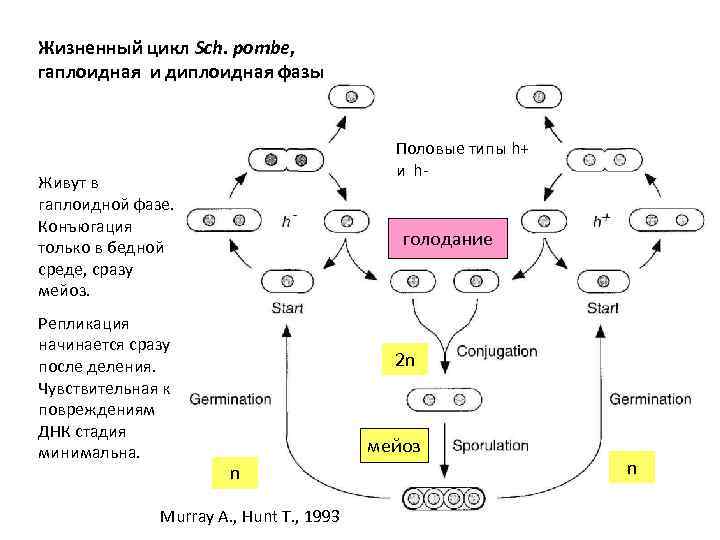
Жизненный цикл Sch. pombe, гаплоидная и диплоидная фазы Половые типы h+ и h- Живут в гаплоидной фазе. Конъюгация только в бедной среде, сразу мейоз. Репликация начинается сразу после деления. Чувствительная к повреждениям ДНК стадия минимальна. голодание 2 n мейоз n Murray A. , Hunt T. , 1993 n
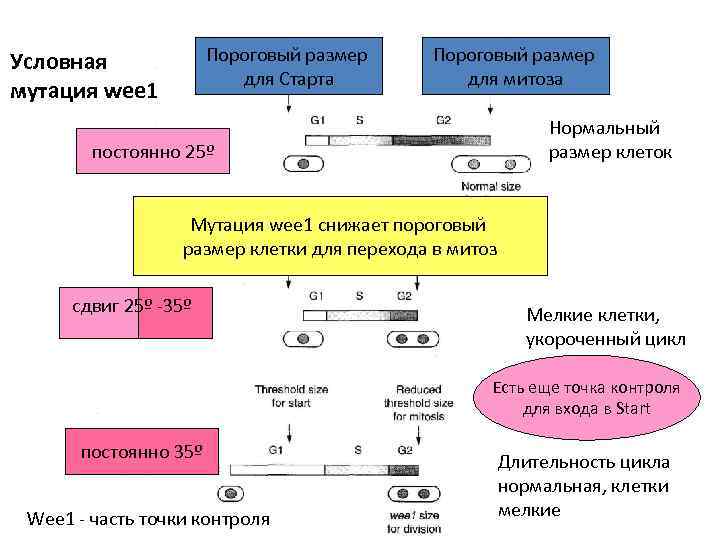
Пороговый размер для Старта Условная мутация wee 1 Пороговый размер для митоза Нормальный размер клеток постоянно 25º Мутация wee 1 снижает пороговый размер клетки для перехода в митоз сдвиг 25º -35º Мелкие клетки, укороченный цикл Есть еще точка контроля для входа в Start постоянно 35º Wee 1 - часть точки контроля Длительность цикла нормальная, клетки мелкие
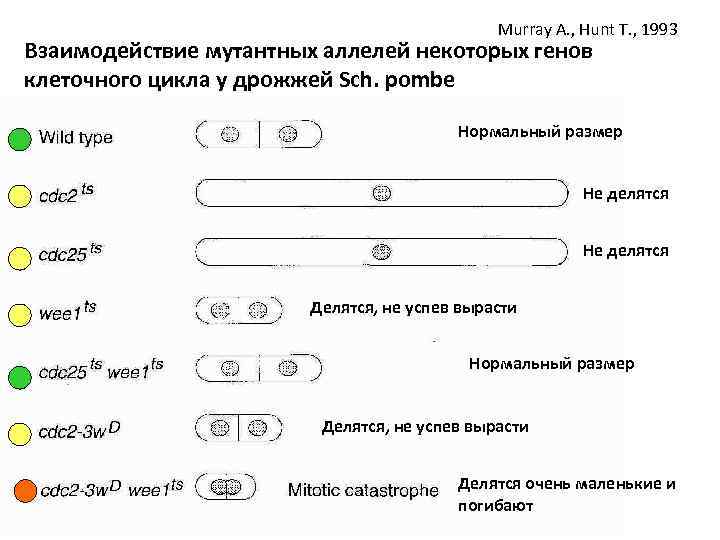
Murray A. , Hunt T. , 1993 Взаимодействие мутантных аллелей некоторых генов клеточного цикла у дрожжей Sch. pombe Нормальный размер Не делятся Делятся, не успев вырасти Нормальный размер Делятся, не успев вырасти Делятся очень маленькие и погибают
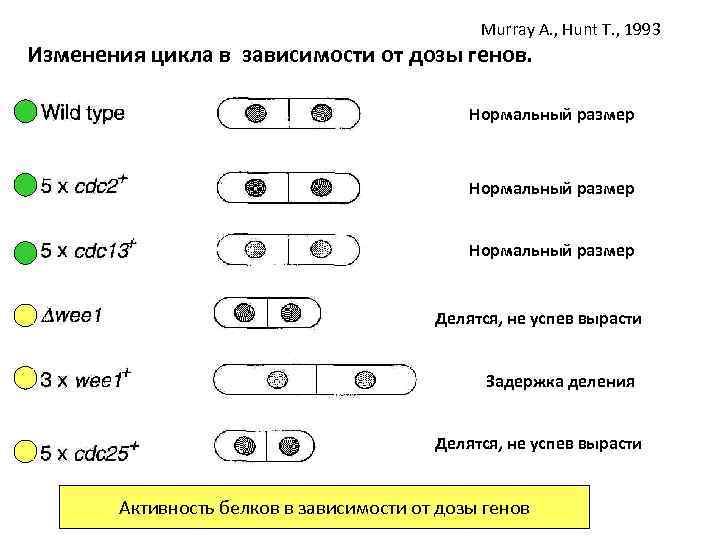
Murray A. , Hunt T. , 1993 Изменения цикла в зависимости от дозы генов. Нормальный размер Делятся, не успев вырасти Задержка деления Делятся, не успев вырасти Активность белков в зависимости от дозы генов

Проанализировав взаимодействия, пришли к выводам: • Cdc 2 -главный индуктор митоза • Wee 1 – ингибирует Cdc 2 • Cdc 25 – активирует Cdc 2 регуляторы
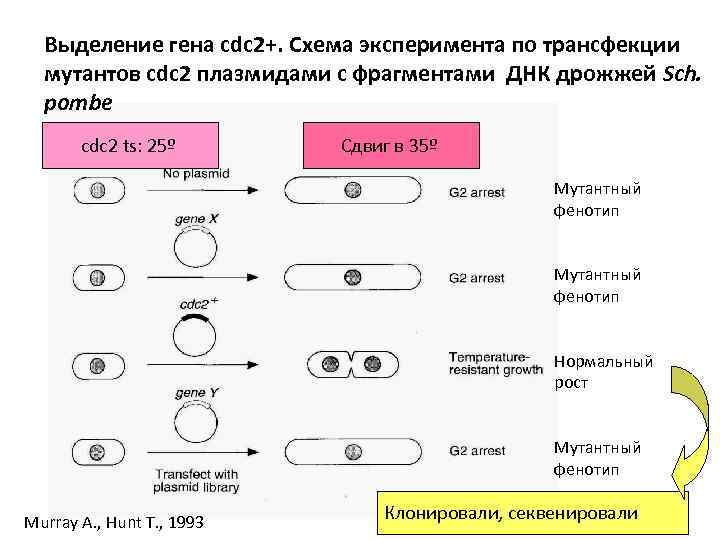
Выделение гена cdc 2+. Схема эксперимента по трансфекции мутантов cdc 2 плазмидами с фрагментами ДНК дрожжей Sch. pombe cdc 2 ts: 25º Сдвиг в 35º Мутантный фенотип Нормальный рост Мутантный фенотип Murray A. , Hunt T. , 1993 Клонировали, секвенировали
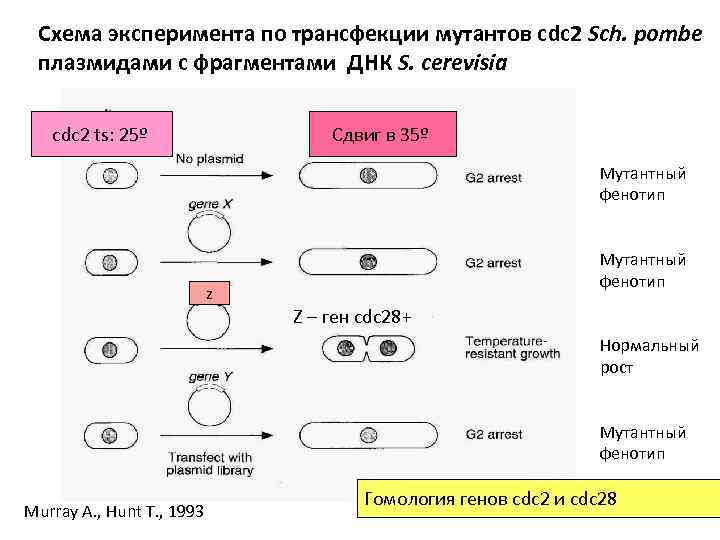
Схема эксперимента по трансфекции мутантов cdc 2 Sch. pombe плазмидами с фрагментами ДНК S. cerevisia cdc 2 ts: 25º Сдвиг в 35º Мутантный фенотип z Z – ген cdc 28+ Нормальный рост Мутантный фенотип Murray A. , Hunt T. , 1993 Гомология генов сdc 2 и cdc 28

Клонировали и секвенировали гены -аналоги сdc 2 (Sch. pombe) и cdc 28 (S. cerevisia) - 60 % гомологии. Играют ключевую роль в регуляции цикла. Продукт гена – полипептид длиной 297 ак (34 к. Да). Протеинкиназа: Серин-треонинкиназа p 34 cdc 2 Аналогичным способом получили ген cdc 2+ человека в культуре cdc 2 ts при рестриктивной температуре. Таким же способом получили и клонировали гены cdc 13+, cdc 25+, wee 1+. cdc 13+ - продукт длиной 482 ак оказался гомологичен уже известным циклинам группы В. cdc 25+ - фосфатаза wee 1+ - протеинкиназа

К 1988 г: • генетики показали, что цикл регулируется киназами Cdc 2/Cdc 28 у всех видов, • биохимики и физиологи – что MPF универсален для митоза и мейоза, • количество циклина меняется в клеточном цикле, какова его роль? Из 1 литра лягушачьих яиц выделили 1 мкг MPF: • антитела на циклин дрожжей выявили субъединицу 46 к. Да. • антитела на Cdc 2 дрожжей выявили субъединицу 34 к. Да. Выявили киназную активность – по фосфорилированию гистона Н 1 Свойства MPF изучали в бесклеточной системе

Получение бесклеточного экстракта • Яйца лягушки стимулируют электрошоком, имитируя оплодотворение. В цитоплазме повышается содержание Са 2+, завершается М 2 Желток и липиды • Яйца центрифугируют, цитоплазму отделяют от желтка и липидов Цитоплазма • Добавляют спермии и АТФ • Ядра спермиев набухают и проходят циклы репликации- митоза за 40 -60 мин ядра В бесклеточной системе происходит репликация ДНК, сборка веретена, расхождение сестринских хроматид, анафазное движение
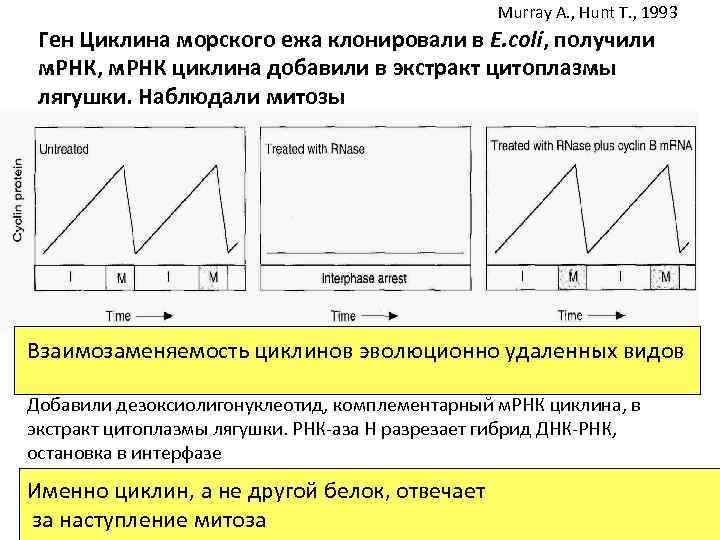
Murray A. , Hunt T. , 1993 Ген Циклина морского ежа клонировали в E. coli, получили м. РНК, м. РНК циклина добавили в экстракт цитоплазмы лягушки. Наблюдали митозы Взаимозаменяемость циклинов эволюционно удаленных видов Добавили дезоксиолигонуклеотид, комплементарный м. РНК циклина, в экстракт цитоплазмы лягушки. РНК-аза Н разрезает гибрид ДНК-РНК, остановка в интерфазе Именно циклин, а не другой белок, отвечает за наступление митоза

Проверка гипотезы: для инактивации MPF нужна деградация циклина. Отсутствие деградации должно остановить цикл в митозе. Мутантная форма циклина: в белке отсутствует концевой фрагмент из 90 ак. Добавили в бесклеточный экстракт, деления остановились За деградацию циклина отвечает концевой фрагмент
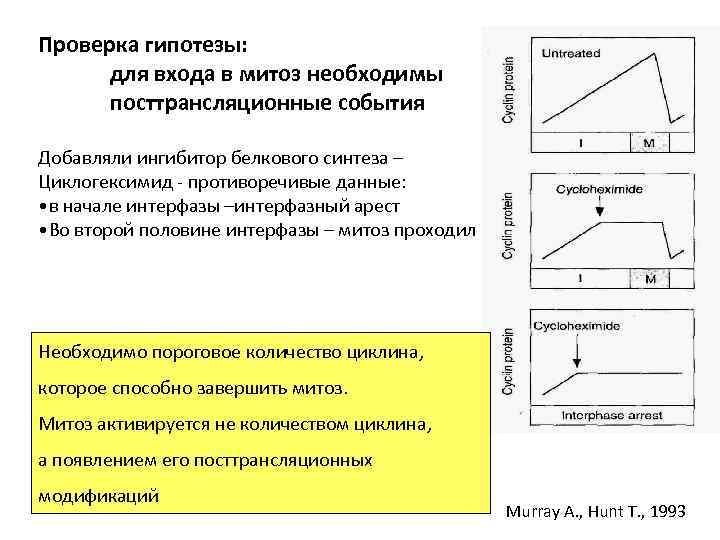
Проверка гипотезы: для входа в митоз необходимы посттрансляционные события Добавляли ингибитор белкового синтеза – Циклогексимид - противоречивые данные: • в начале интерфазы –интерфазный арест • Во второй половине интерфазы – митоз проходил Необходимо пороговое количество циклина, которое способно завершить митоз. Митоз активируется не количеством циклина, а появлением его посттрансляционных модификаций Murray A. , Hunt T. , 1993
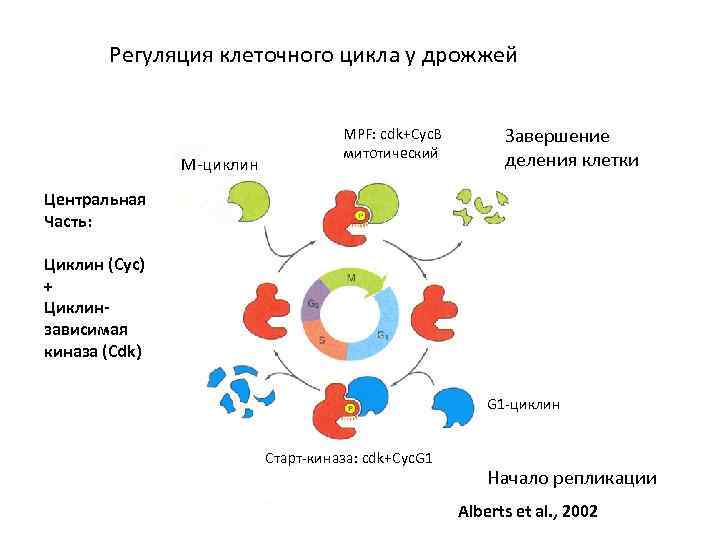
Регуляция клеточного цикла у дрожжей М-циклин MPF: cdk+Cyc. B митотический Завершение деления клетки Центральная Часть: Циклин (Cyc) + Циклинзависимая киназа (Cdk) G 1 -циклин Старт-киназа: cdk+Cyc. G 1 Начало репликации Alberts et al. , 2002
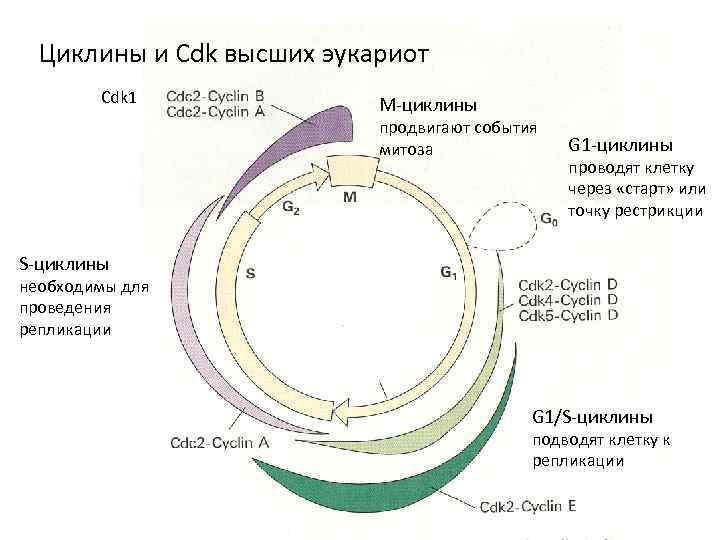
Циклины и Cdk высших эукариот Cdk 1 М-циклины продвигают события митоза G 1 -циклины проводят клетку через «старт» или точку рестрикции S-циклины необходимы для проведения репликации G 1/S-циклины подводят клетку к репликации

CDK-каталитическая субъединица MPF, циклин - активаторная • В настоящее время известно восемь циклинов, обозначаемых латинскими буквами от А до Н. Все циклины имеют общую последовательность длиной 100150 аминокислотных остатков - консервативный циклиновый бокс, который необходим для связывания с CDK. На основании анализа кристаллической структуры циклин А 1 состоит из двух компактных центральных доменов, каждый из которых представлен пятью спиралями, и двух дополнительных спиралей у Си N-конца. • • CDK 1 ассоциируется с циклинами A и B и участвуют в переходе G 2 -M. CDK 2 может связываться с циклинами A , E , D 2 и D 3 (но не D 1) и является одной из основных киназ, регулирующих переход G 1 -S и прохождение через Sпериод. CDK 3 экспрессируется в большинстве линий на незначительном уровне, и ее функция пока не выяснена, хотя предполагается, что она, подобно CDK 2, участвует в переходе G 1 -S. Данные о роли CDK 5 и о взаимодействующих с ней циклинах противоречивы. СDK 4 и CDK 6 участвуют в регуляции перехода G 1 -S. Они являются основными каталитическими партнерами циклинов D -типа, образуя с ними функциональные комплексы, обладающие субстратной специфичностью к белку Rb. • •
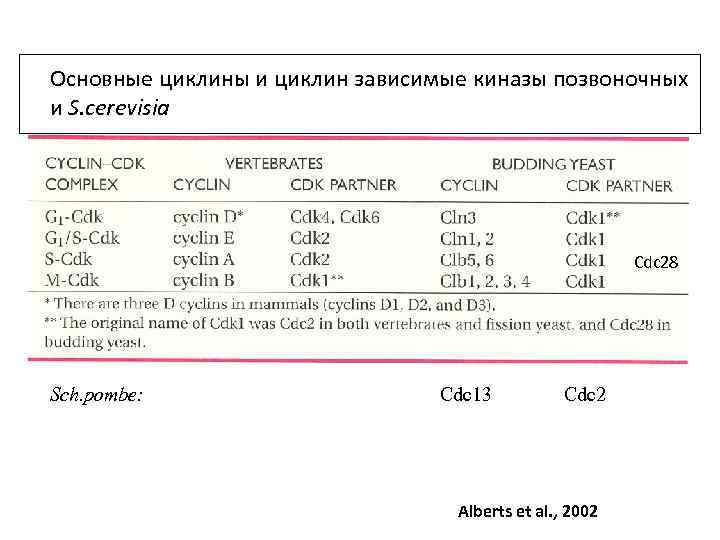
Основные циклины и циклин зависимые киназы позвоночных и S. cerevisia Cdc 28 Sch. pombe: Cdc 13 Cdc 2 Alberts et al. , 2002
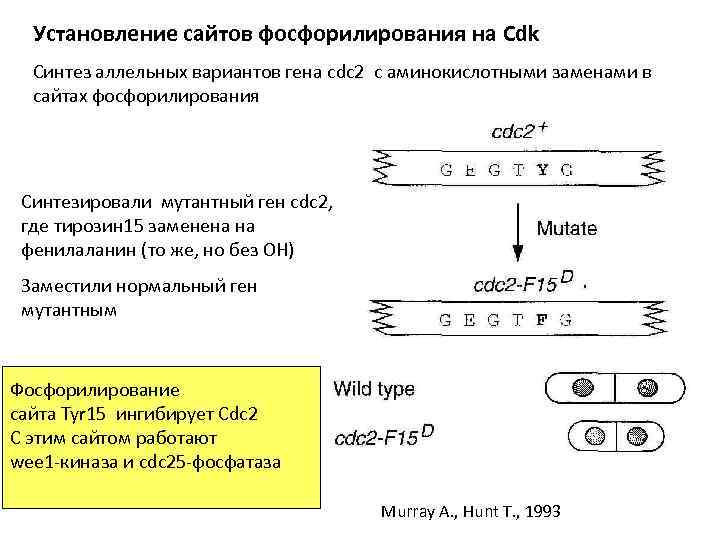
Установление сайтов фосфорилирования на Cdk Синтез аллельных вариантов гена cdc 2 с аминокислотными заменами в сайтах фосфорилирования Синтезировали мутантный ген cdc 2, где тирозин 15 заменена на фенилаланин (то же, но без ОН) Заместили нормальный ген мутантным Фосфорилирование сайта Tyr 15 ингибирует Cdc 2 С этим сайтом работают wee 1 -киназа и cdc 25 -фосфатаза Murray A. , Hunt T. , 1993
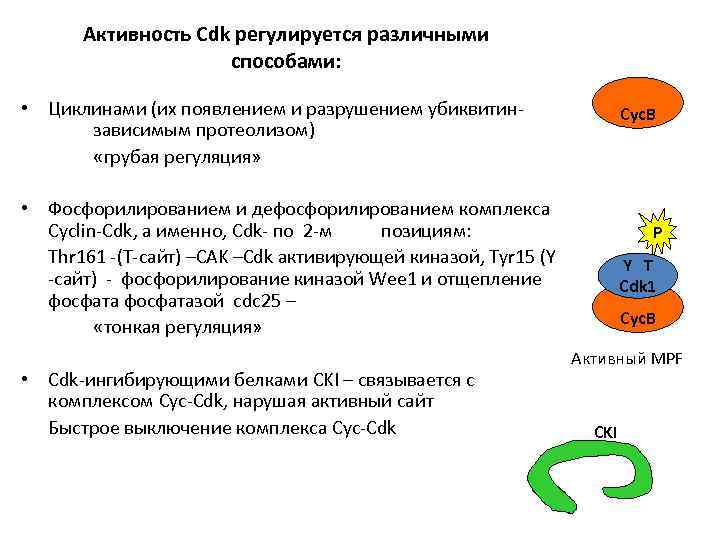
Активность Cdk регулируется различными способами: • Циклинами (их появлением и разрушением убиквитинзависимым протеолизом) «грубая регуляция» Cyc. B • Фосфорилированием и дефосфорилированием комплекса Cyclin-Cdk, а именно, Cdk- по 2 -м позициям: Thr 161 -(T-сайт) –CAK –Cdk активирующей киназой, Tyr 15 (Y -сайт) - фосфорилирование киназой Wee 1 и отщепление фосфатазой cdc 25 – «тонкая регуляция» • Cdk-ингибирующими белками CKI – связывается с комплексом Cyc-Cdk, нарушая активный сайт Быстрое выключение комплекса Cyc-Cdk P Y T Cdk 1 Cyc. B Активный MPF CKI
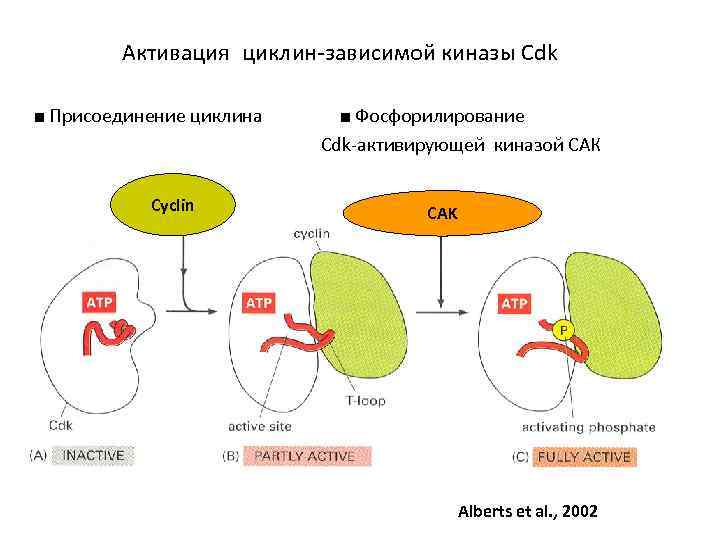
Активация циклин-зависимой киназы Cdk ■ Присоединение циклина Cyclin ■ Фосфорилирование Cdk-активирующей киназой САК CAK Alberts et al. , 2002
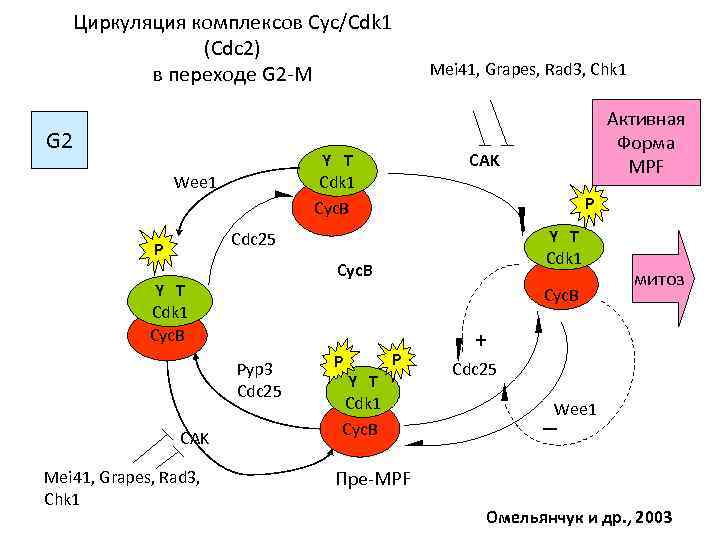
Циркуляция комплексов Cyc/Cdk 1 (Cdc 2) в переходе G 2 -M G 2 P Y T Cdk 1 Cdc 25 P Cyc. B Y T Cdk 1 Cyc. B Pyp 3 Cdc 25 CAK Mei 41, Grapes, Rad 3, Chk 1 Активная Форма MPF CAK Y T Cdk 1 Cyc. B Wee 1 Mei 41, Grapes, Rad 3, Chk 1 P Y T Cdk 1 Cyc. B P митоз + Cdc 25 Wee 1 ─ Пре-MPF Омельянчук и др. , 2003
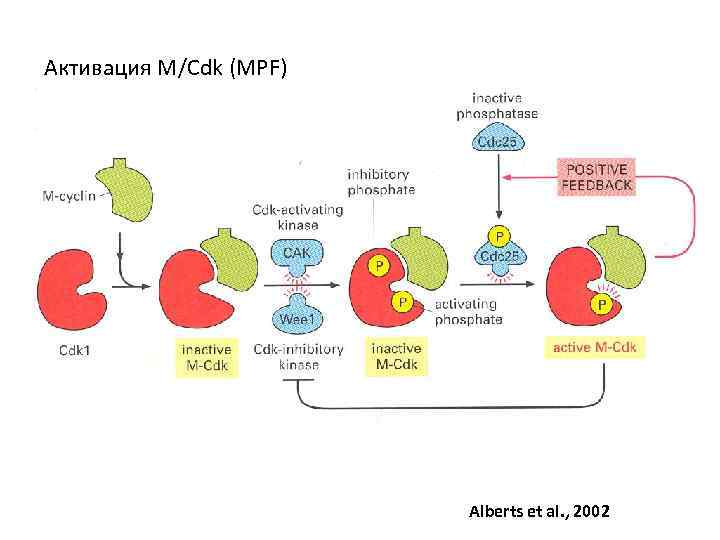
Активация M/Cdk (MPF) Alberts et al. , 2002
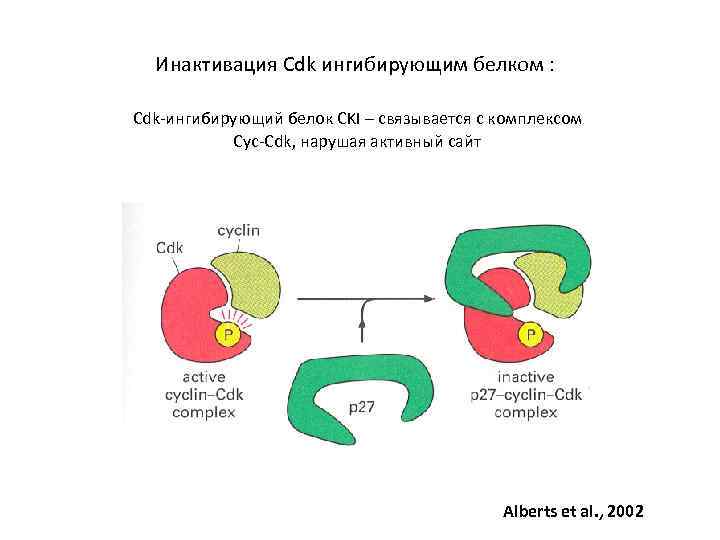
Инактивация Cdk ингибирующим белком : Cdk-ингибирующий белок CKI – связывается с комплексом Cyc-Cdk, нарушая активный сайт Alberts et al. , 2002
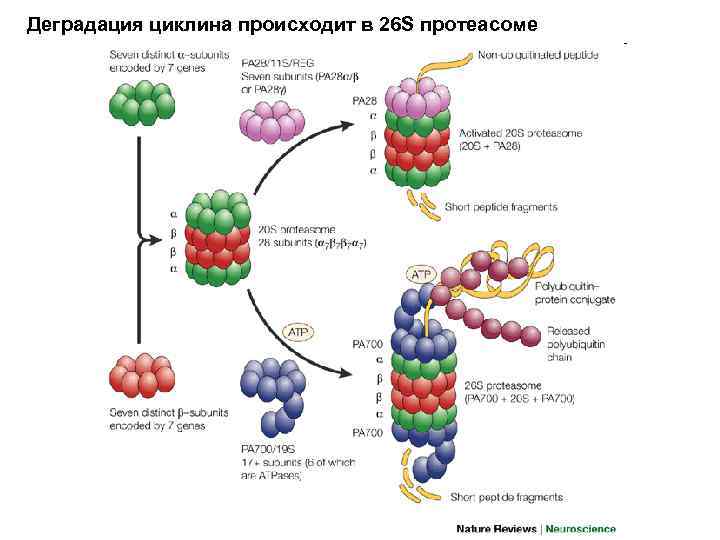
Деградация циклина происходит в 26 S протеасоме
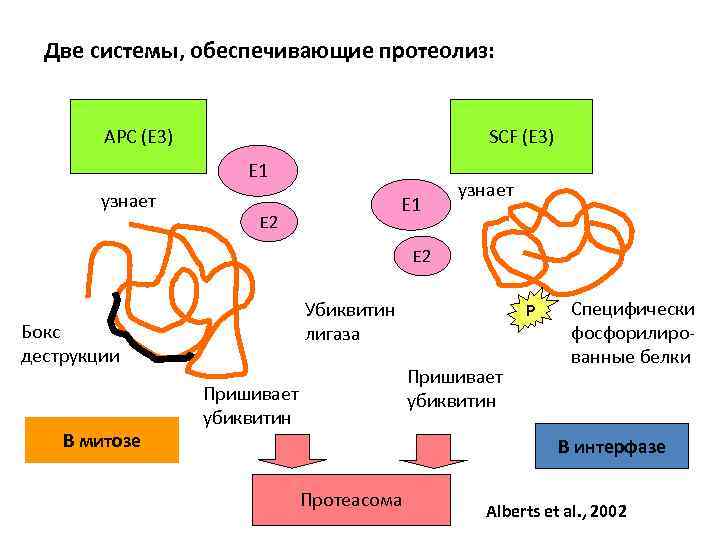
Две системы, обеспечивающие протеолиз: APC (Е 3) SCF (Е 3) E 1 узнает E 1 E 2 узнает E 2 Убиквитин лигаза Бокс деструкции В митозе P Пришивает убиквитин Специфически фосфорилированные белки В интерфазе Протеасома Alberts et al. , 2002
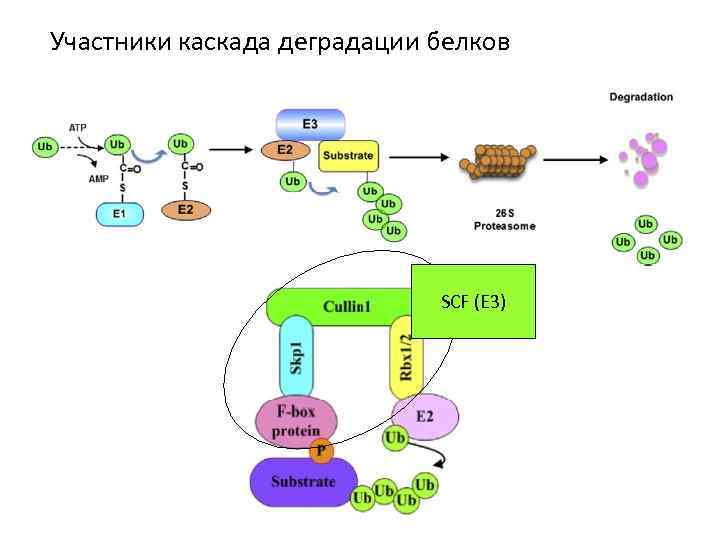
Участники каскада деградации белков SCF (Е 3)
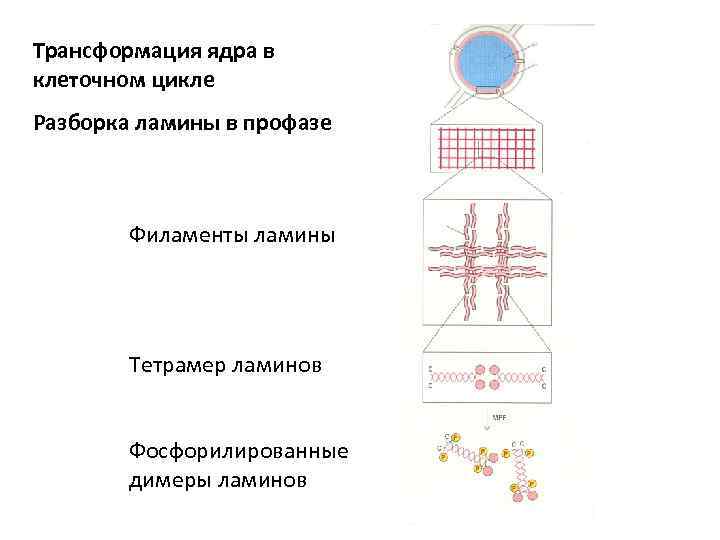
Трансформация ядра в клеточном цикле Разборка ламины в профазе Филаменты ламины Тетрамер ламинов Фосфорилированные димеры ламинов
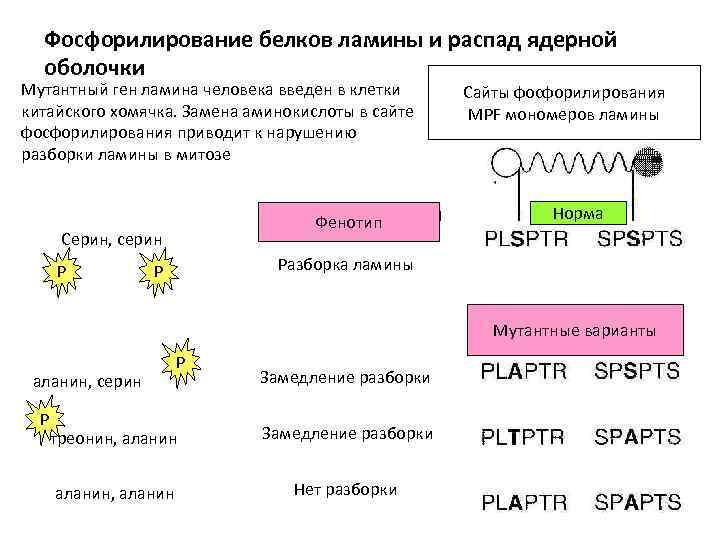
Фосфорилирование белков ламины и распад ядерной оболочки Мутантный ген ламина человека введен в клетки китайского хомячка. Замена аминокислоты в сайте фосфорилирования приводит к нарушению разборки ламины в митозе Фенотип Серин, серин P Сайты фосфорилирования MPF мономеров ламины Норма Разборка ламины P Мутантные варианты аланин, серин P P треонин, аланин, аланин Замедление разборки Нет разборки
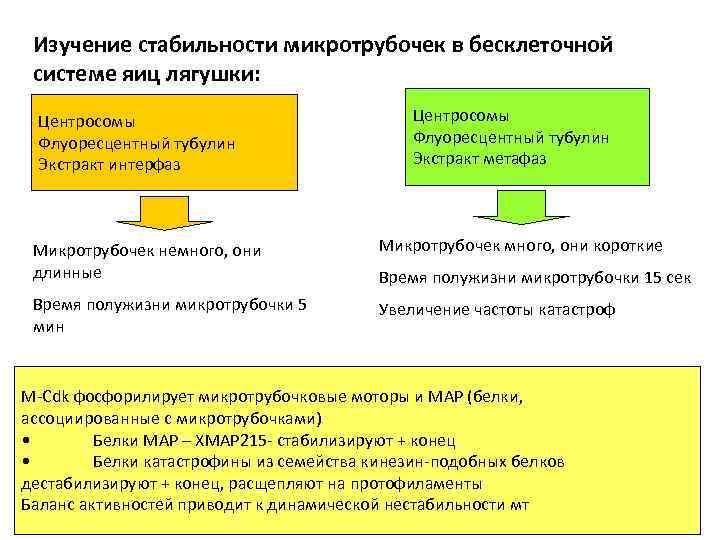
Изучение стабильности микротрубочек в бесклеточной системе яиц лягушки: Центросомы Флуоресцентный тубулин Экстракт интерфаз Центросомы Флуоресцентный тубулин Экстракт метафаз Микротрубочек немного, они длинные Микротрубочек много, они короткие Время полужизни микротрубочки 5 мин Увеличение частоты катастроф Время полужизни микротрубочки 15 сек M-Cdk фосфорилирует микротрубочковые моторы и МАР (белки, ассоциированные с микротрубочками) • Белки МАР – ХМАР 215 - стабилизируют + конец • Белки катастрофины из семейства кинезин-подобных белков дестабилизируют + конец, расщепляют на протофиламенты Баланс активностей приводит к динамической нестабильности мт
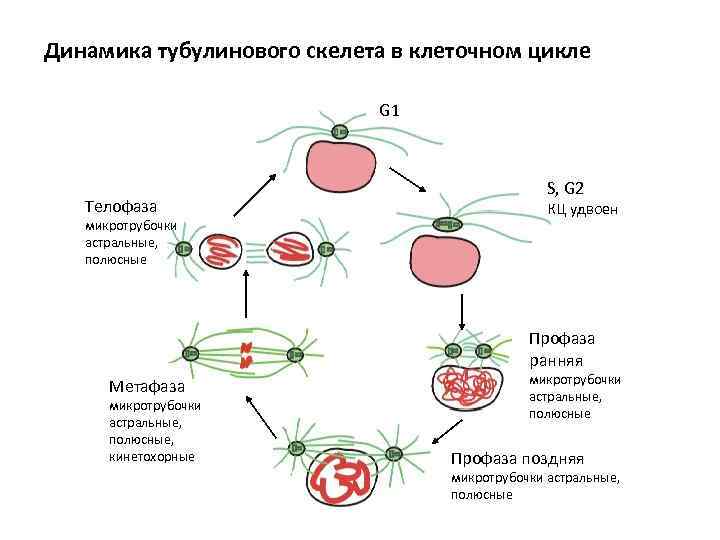
Динамика тубулинового скелета в клеточном цикле G 1 Телофаза микротрубочки астральные, полюсные S, G 2 КЦ удвоен Профаза ранняя Метафаза микротрубочки астральные, полюсные, кинетохорные микротрубочки астральные, полюсные Профаза поздняя микротрубочки астральные, полюсные
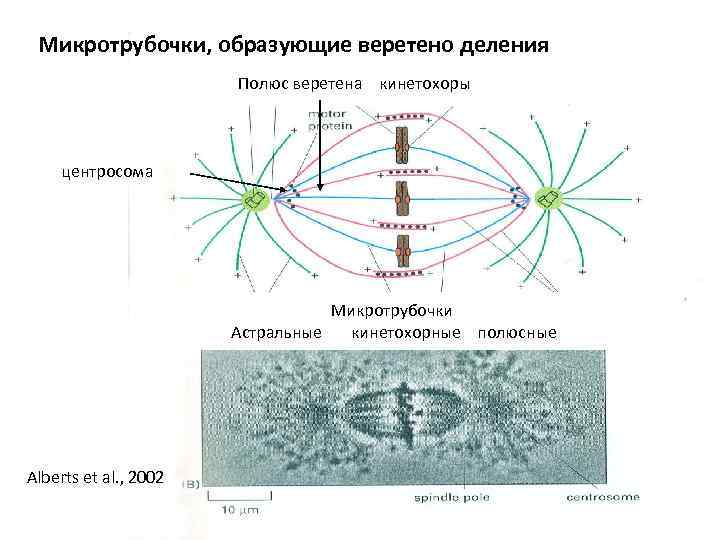
Микротрубочки, образующие веретено деления Полюс веретена кинетохоры центросома Микротрубочки Астральные кинетохорные полюсные Alberts et al. , 2002
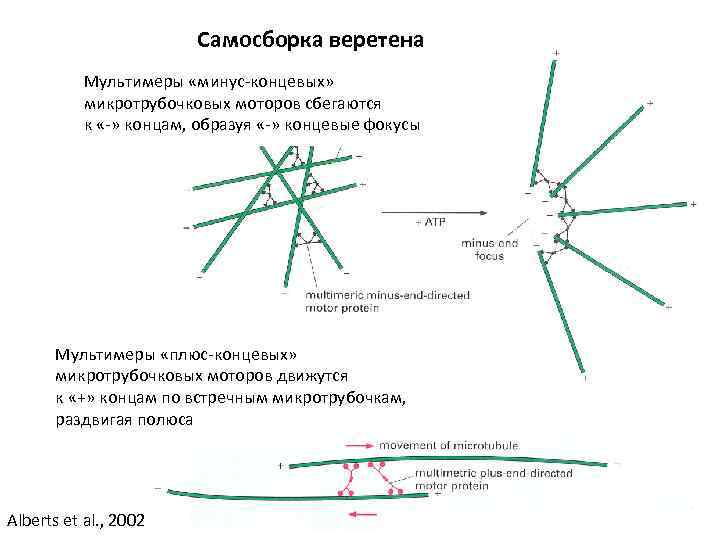
Самосборка веретена Мультимеры «минус-концевых» микротрубочковых моторов сбегаются к «-» концам, образуя «-» концевые фокусы Мультимеры «плюс-концевых» микротрубочковых моторов движутся к «+» концам по встречным микротрубочкам, раздвигая полюса Alberts et al. , 2002
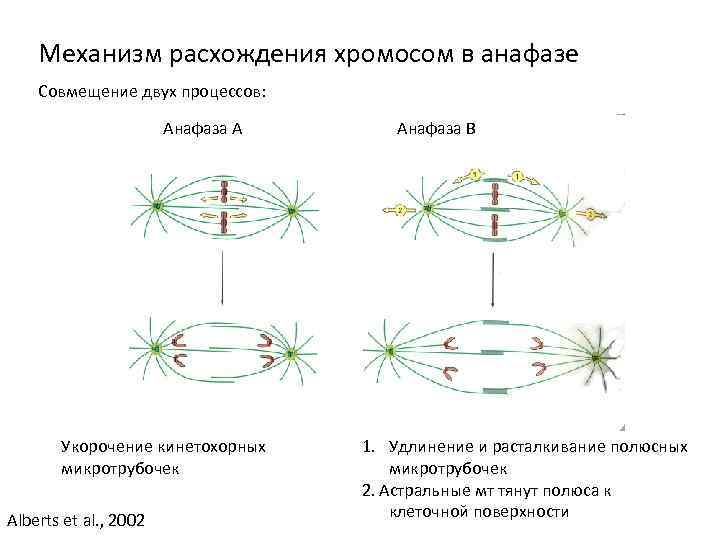
Механизм расхождения хромосом в анафазе Совмещение двух процессов: Анафаза А Укорочение кинетохорных микротрубочек Alberts et al. , 2002 Анафаза В 1. Удлинение и расталкивание полюсных микротрубочек 2. Астральные мт тянут полюса к клеточной поверхности
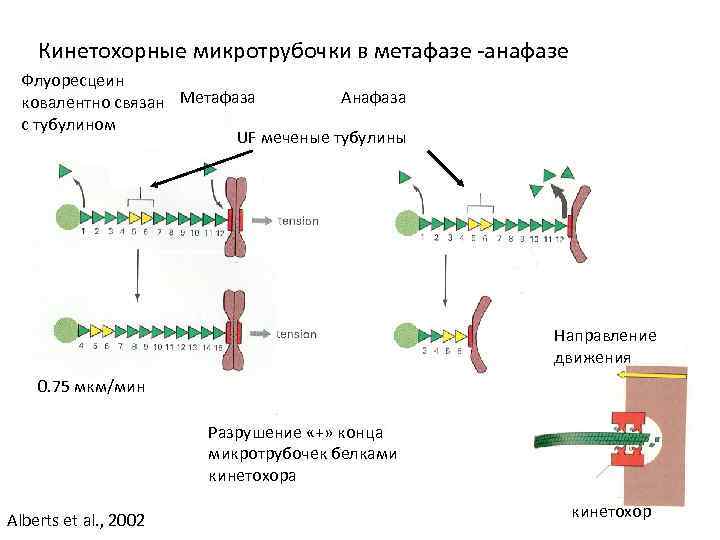
Кинетохорные микротрубочки в метафазе -анафазе Флуоресцеин Анафаза ковалентно связан Метафаза с тубулином UF меченые тубулины Направление движения 0. 75 мкм/мин Разрушение «+» конца микротрубочек белками кинетохора Alberts et al. , 2002 кинетохор

Центромера и кинетохор Центромера- участок хромосомы, имеющий возможность прикрепляться к микротрубочкам. У высших организмов формируется сложная структуракинетохор. Генетический скрининг проводили на клетках дрожжей, изучалась стабильность передачи минихромосомы в клеточных поколениях. chl – chromosome loss, msm- minichromosome maintenance, stf - chromosome transmission fidelity, ndc – nonedisjunction cin – chromosome instability dis – defective in sister chromatid disjoining mis - minichromosome instability
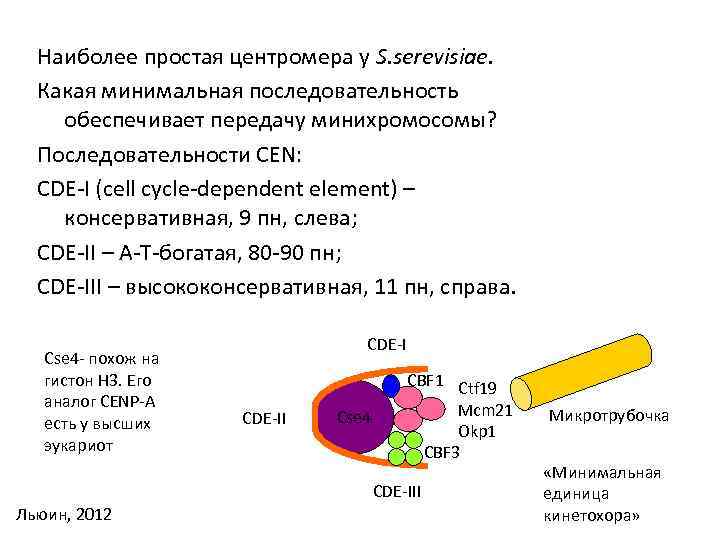
Наиболее простая центромера у S. serevisiae. Какая минимальная последовательность обеспечивает передачу минихромосомы? Последовательности CEN: CDE-I (cell cycle-dependent element) – консервативная, 9 пн, слева; CDE-II – А-Т-богатая, 80 -90 пн; CDE-III – высококонсервативная, 11 пн, справа. Cse 4 - похож на гистон H 3. Его аналог CENP-A есть у высших эукариот CDE-II Cse 4 CBF 1 Ctf 19 Mcm 21 Okp 1 CBF 3 CDE-III Льюин, 2012 Микротрубочка «Минимальная единица кинетохора»
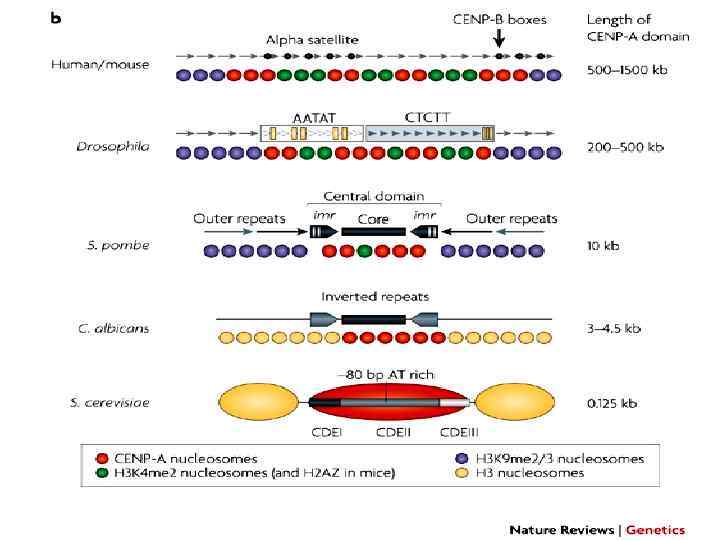
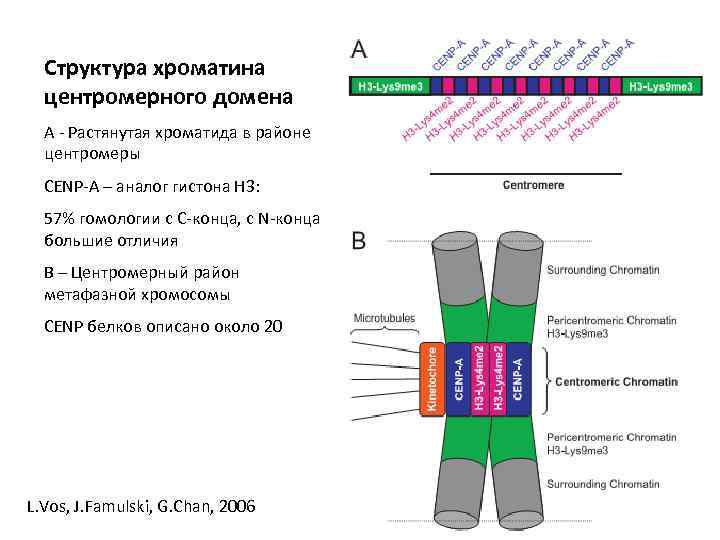
Структура хроматина центромерного домена А - Растянутая хроматида в районе центромеры CENP-A – аналог гистона Н 3: 57% гомологии с С-конца, с N-конца большие отличия В – Центромерный район метафазной хромосомы CENP белков описано около 20 L. Vos, J. Famulski, G. Chan, 2006
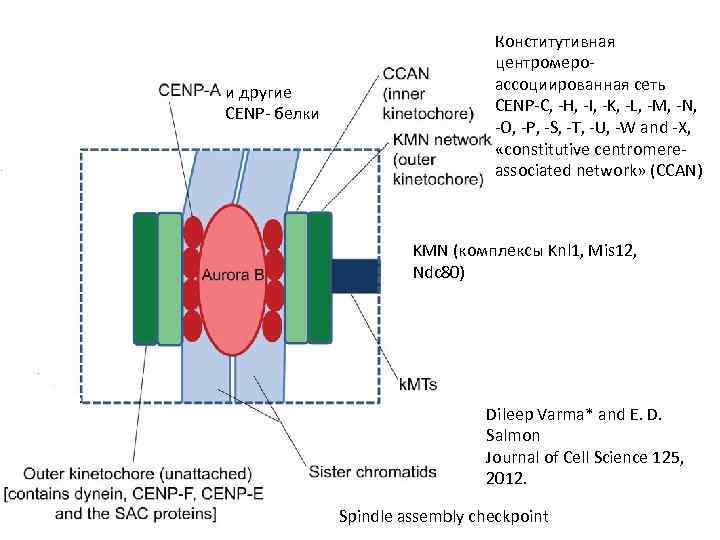
и другие CENP- белки Конститутивная центромероассоциированная сеть CENP-C, -H, -I, -K, -L, -M, -N, -O, -P, -S, -T, -U, -W and -X, «constitutive centromereassociated network» (CCAN) KMN (комплексы Knl 1, Mis 12, Ndc 80) Dileep Varma* and E. D. Salmon Journal of Cell Science 125, 2012. Spindle assembly checkpoint
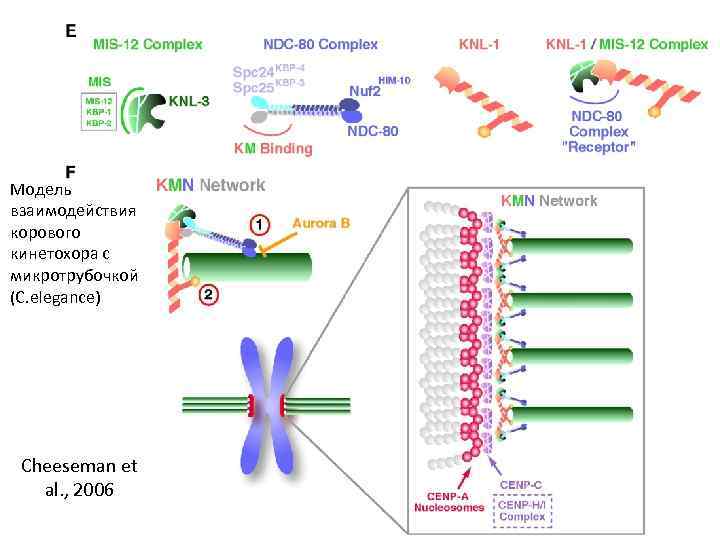
Модель взаимодействия корового кинетохора с микротрубочкой (C. elegance) Cheeseman et al. , 2006
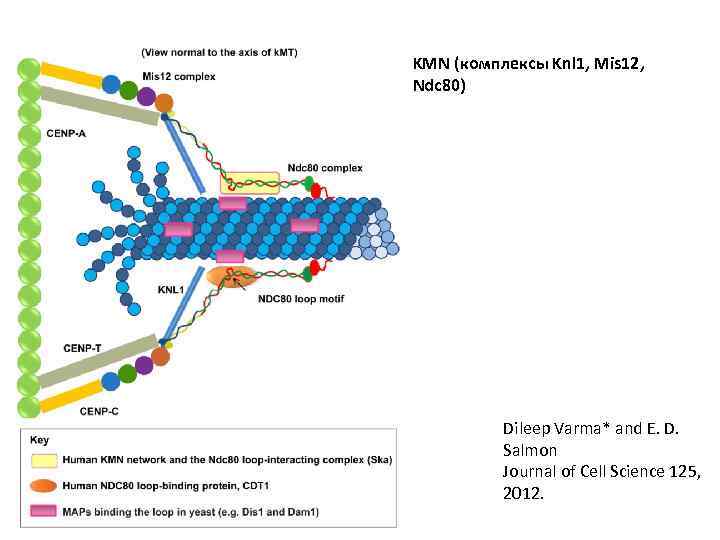
KMN (комплексы Knl 1, Mis 12, Ndc 80) Dileep Varma* and E. D. Salmon Journal of Cell Science 125, 2012.
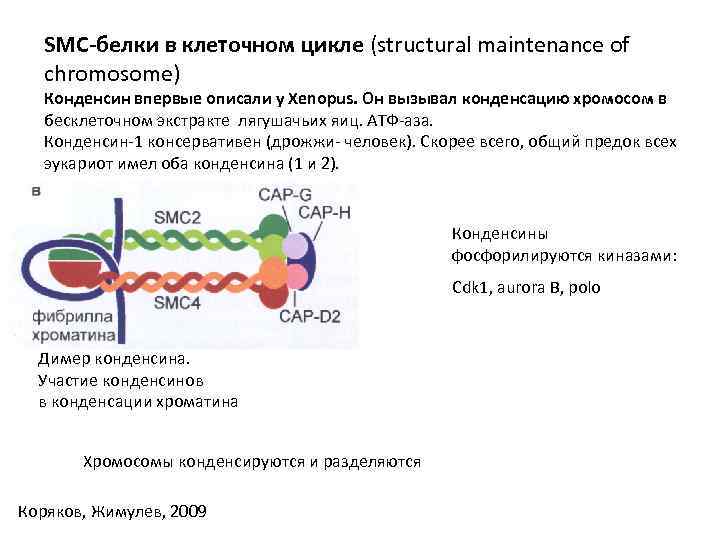
SMC-белки в клеточном цикле (structural maintenance of chromosome) Конденсин впервые описали у Xenopus. Он вызывал конденсацию хромосом в бесклеточном экстракте лягушачьих яиц. АТФ-аза. Конденсин-1 консервативен (дрожжи- человек). Скорее всего, общий предок всех эукариот имел оба конденсина (1 и 2). Конденсины фосфорилируются киназами: Cdk 1, aurora B, polo Димер конденсина. Участие конденсинов в конденсации хроматина Хромосомы конденсируются и разделяются Коряков, Жимулев, 2009
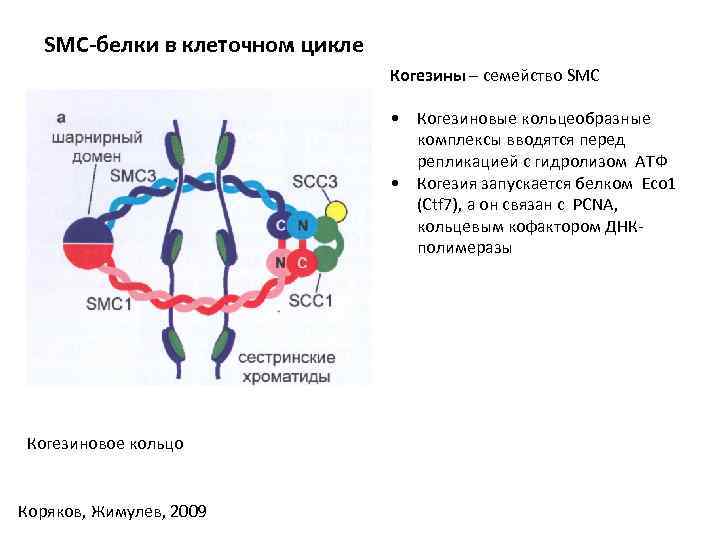
SMC-белки в клеточном цикле Когезины – семейство SMC • Когезиновые кольцеобразные комплексы вводятся перед репликацией с гидролизом АТФ • Когезия запускается белком Eco 1 (Ctf 7), а он связан с PCNA, кольцевым кофактором ДНКполимеразы Когезиновое кольцо Коряков, Жимулев, 2009
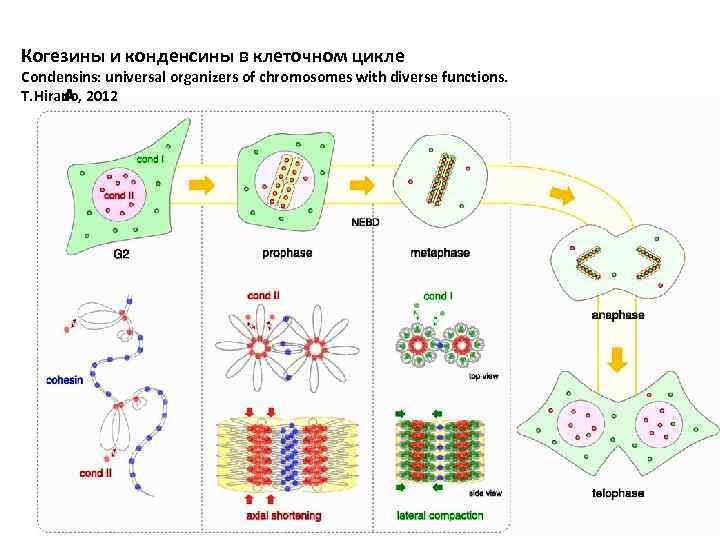
Когезины и конденсины в клеточном цикле Condensins: universal organizers of chromosomes with diverse functions. T. Hirano, 2012

Когезины и конденсины в клеточном цикле. Морфология хроматина в зависимости от соотношения конденсинов 1 и 2 Condensins: universal organizers of chromosomes with diverse functions. T. Hirano, 2012 Культуры клеток млекопитающих, курицы, бесклеточный экстракт яиц Xenopus
Активация M-Cdk: Индуцирует сборку веретена вызывает конденсацию хромосом растворение ядерной оболочки перестройку тубулинового цитоскелета Фосфорилирование белков этих структур или их регулирующих реорганизацию аппарата Гольджи и ЭПС Инактивация M-Cdk: Те же события разворачиваются в обратном направлении дефосфорилирование Не понятно, что вызывает сегрегацию хромосом и цитокинез?
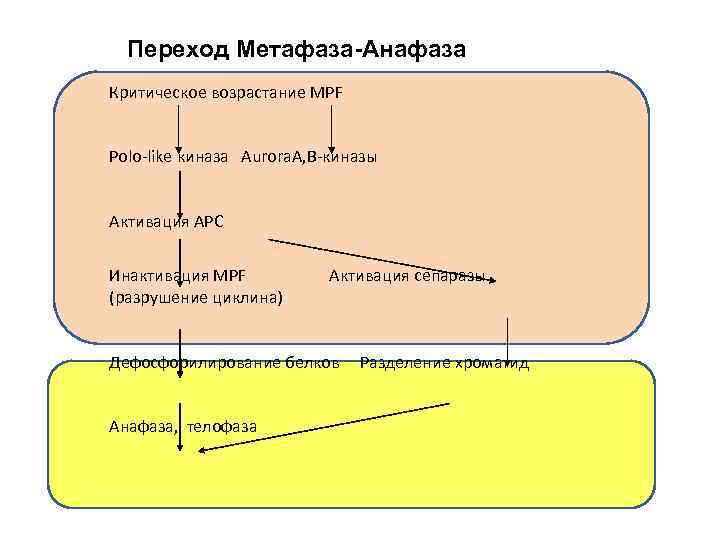
Переход Метафаза-Анафаза Критическое возрастание MPF Polo-like киназа Aurora. A, В-киназы Активация APC Инактивация MPF (разрушение циклина) Активация сепаразы Дефосфорилирование белков Анафаза, телофаза Разделение хроматид
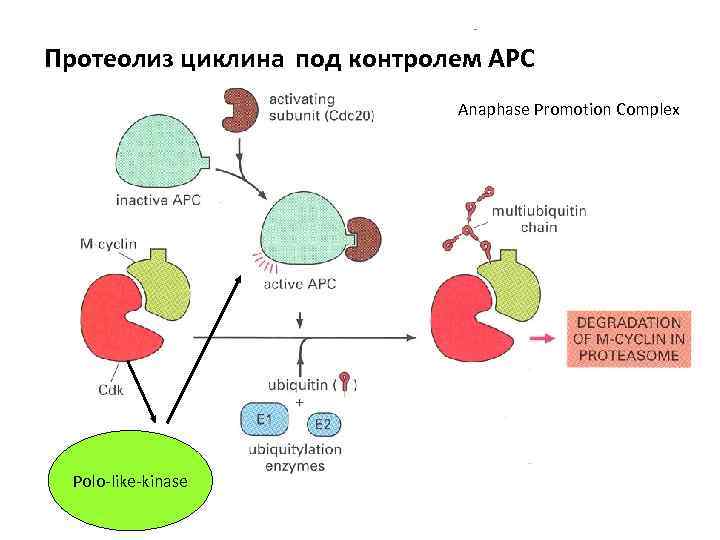
Протеолиз циклина под контролем АРС Anaphase Promotion Complex Polo-like-kinase
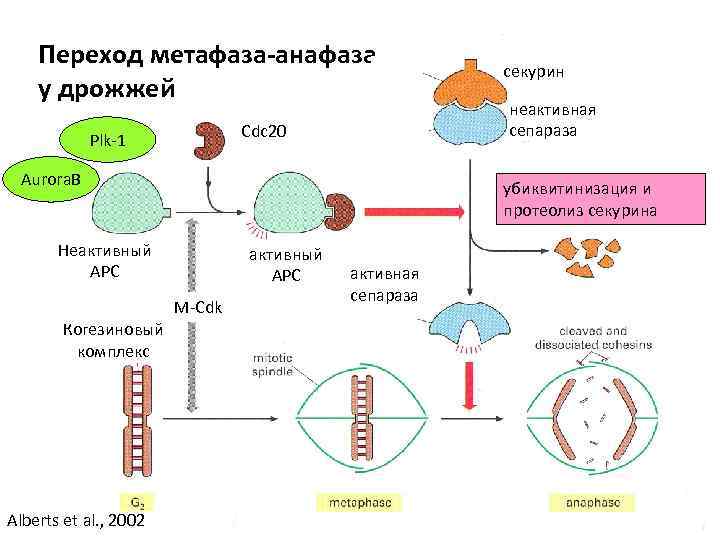
Переход метафаза-анафаза у дрожжей Cdc 20 Plk-1 Aurora. B Alberts et al. , 2002 неактивная сепараза убиквитинизация и протеолиз секурина Неактивный АРС Когезиновый комплекс секурин активный АРС M-Cdk активная сепараза

Переход метафаза- анафаза у дрожжей Основные участники: • APC - anaphase promotion complex – при добавлении субъединиц Е 1 и Е 2 служит убиквитин лигазой • Cdc 20 - белок, активирующий APC • Сепараза – протеаза, разрезающая один из когезинов (Rad 21, Scc 1) • Секурин- белок, инактивирующий протеазу • Polo-like – киназа 1 – активирует АРС (Plk-1)

Разделение сестринских хроматид в митозе Дрожжи: Сепараза разрезает когезины по всей длине хромосом в переходе М-А Позвоночные (человек, He. La): 1. Профаза-прометафаза: • Polo-подобная киназа и Aurora- киназа фосфорилируют и удаляют когезины по плечам хромосом в течение профазы. Обособление сестринских хроматид • Белок шугошин препятствует отделению когезинов в центромерном районе (присоединяет фосфатазу). • Количество конденсинов нарастает 2. Переход М-А: Сепараза разрезает когезины в центромерном районе

СРС- chromosomal passenger complex Aurora киназа В - каталитическая субъединица СРС Survivin Borealin регуляторный кор комплекса – INCENP регулирует активность Aurora TD-60 киназы В CSC-1 Aurora серин-треонин киназа- у дрожжей (А), у дрозофилы (А и В), у человека (А, В, С). Aurora киназа-В фосфорилирует: Н 3 -гистон, CENP-A, кинетохоро-специфичный вариант гистона Н 3 INCENP- внутренний центромерный белок (между хроматидами) Миозина II регуляторную лёгкую цепь Топоизомеразу II α Виментин Десмин MCAK (митотический центромерно-ассоциированный кинезин) Survivin
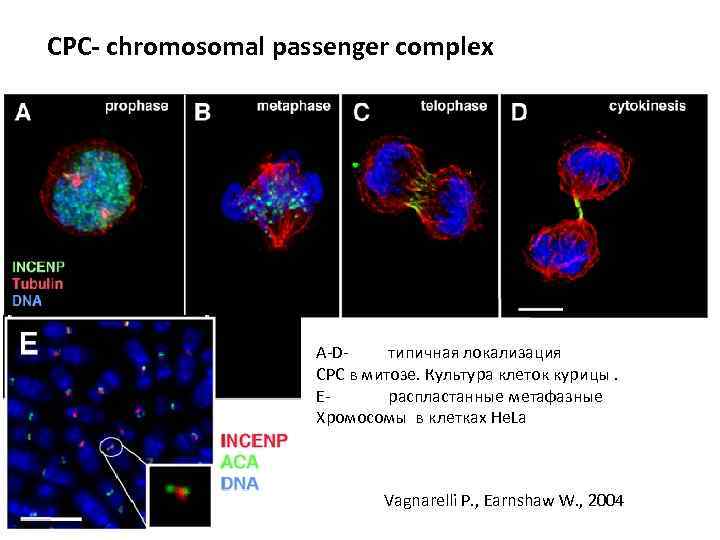
СРС- chromosomal passenger complex A-Dтипичная локализация СРС в митозе. Культура клеток курицы. Ераспластанные метафазные Хромосомы в клетках He. La Vagnarelli P. , Earnshaw W. , 2004

СРС- chromosomal passenger complex CPC, хромосомные пассажиры: белки, локализованные в специфических районах: • в G 2 – внутриядерно, • в профазе митоза – вдоль конденсирующихся хромосом, • в метафазе – в центромерных районах хромосом, • в анафазе – в центральном веретене, • в телофазе- в остаточном тельце веретена Комплекс работает в митозе и мейозе, контролирует: – Хромосомную модификацию (фосфорилирование гистона Н 3) – Хромосомную конгрессию (построение) – Прикрепление кинетохоров к микротрубочкам, коррекция – Формирование стабильного биполярного веретена – Участвует в митотической точке контроля
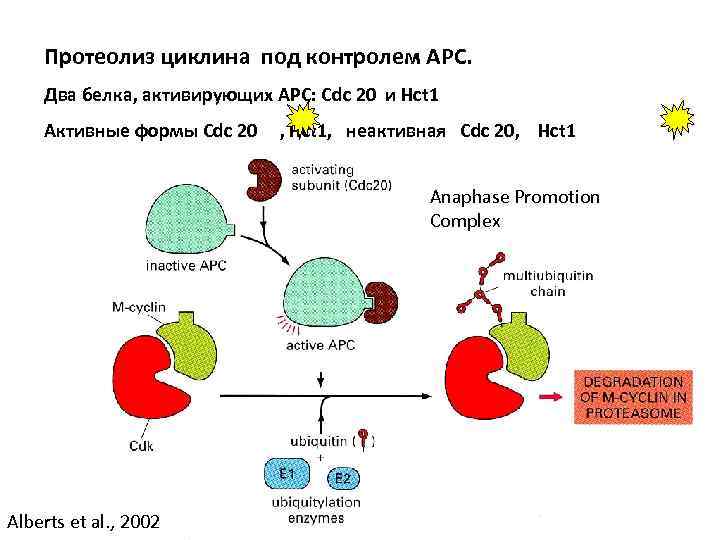
Протеолиз циклина под контролем АРС. Два белка, активирующих АРС: Cdc 20 и Hct 1 Активные формы Cdc 20 , Hct 1, неактивная Cdc 20, Hct 1 Anaphase Promotion Complex Alberts et al. , 2002
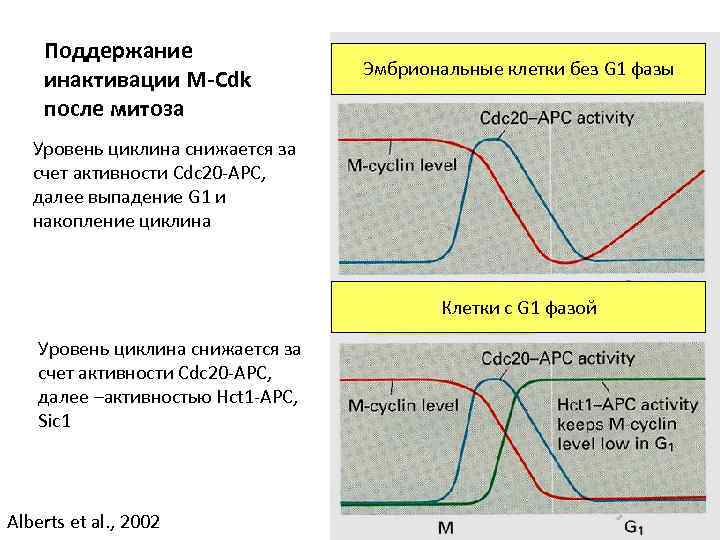
Поддержание инактивации M-Cdk после митоза Эмбриональные клетки без G 1 фазы Уровень циклина снижается за счет активности Cdc 20 -APC, далее выпадение G 1 и накопление циклина Клетки с G 1 фазой Уровень циклина снижается за счет активности Cdc 20 -APC, далее –активностью Hct 1 -APC, Sic 1 Alberts et al. , 2002
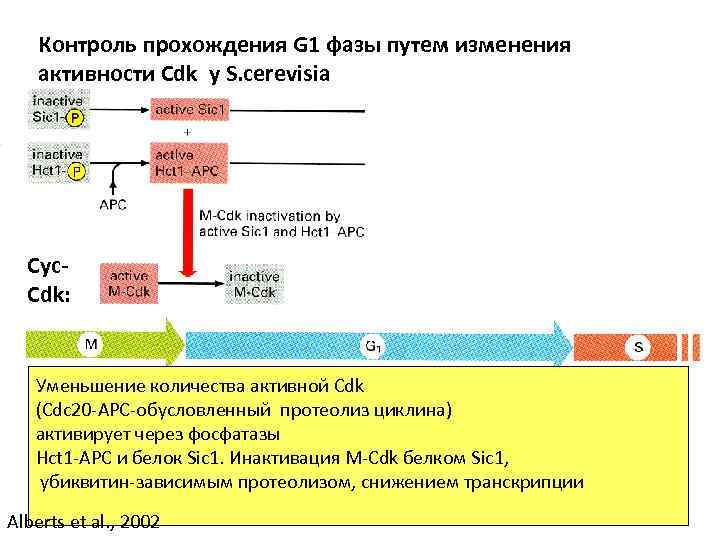
Контроль прохождения G 1 фазы путем изменения активности Cdk у S. cerevisia Cyc. Cdk: Уменьшение количества активной Cdk (Cdc 20 -APC-обусловленный протеолиз циклина) активирует через фосфатазы Hct 1 -APC и белок Sic 1. Инактивация M-Cdk белком Sic 1, убиквитин-зависимым протеолизом, снижением транскрипции Alberts et al. , 2002
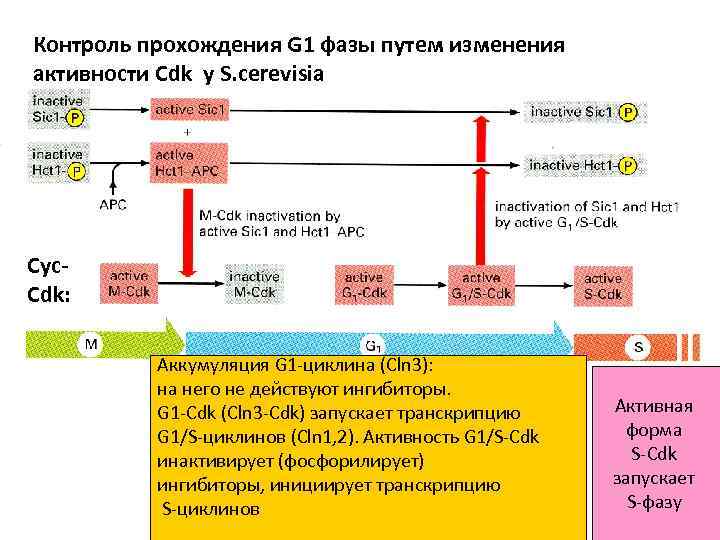
Контроль прохождения G 1 фазы путем изменения активности Cdk у S. cerevisia Cyc. Cdk: Аккумуляция G 1 -циклина (Cln 3): на него не действуют ингибиторы. G 1 -Cdk (Cln 3 -Cdk) запускает транскрипцию G 1/S-циклинов (Cln 1, 2). Активность G 1/S-Cdk инактивирует (фосфорилирует) ингибиторы, инициирует транскрипцию S-циклинов Активная форма S-Cdk запускает S-фазу
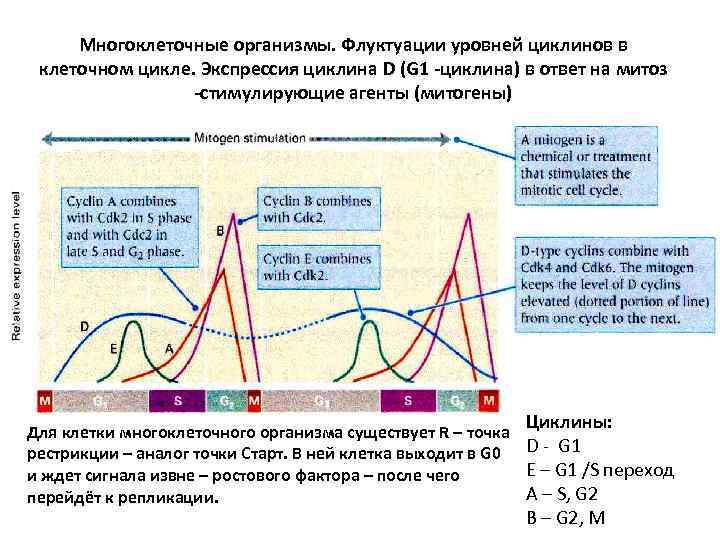
Многоклеточные организмы. Флуктуации уровней циклинов в клеточном цикле. Экспрессия циклина D (G 1 -циклина) в ответ на митоз -стимулирующие агенты (митогены) Циклины: Для клетки многоклеточного организма существует R – точка рестрикции – аналог точки Старт. В ней клетка выходит в G 0 D - G 1 E – G 1 /S переход и ждет сигнала извне – ростового фактора – после чего A – S, G 2 перейдёт к репликации. B – G 2, M
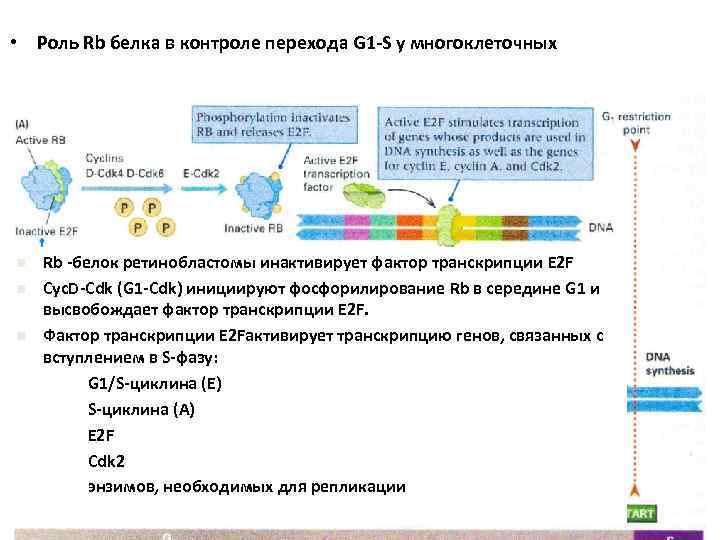
• Роль Rb белка в контроле перехода G 1 -S у многоклеточных n n n Rb -белок ретинобластомы инактивирует фактор транскрипции E 2 F Cyc. D-Cdk (G 1 -Cdk) инициируют фосфорилирование Rb в середине G 1 и высвобождает фактор транскрипции E 2 F. Фактор транскрипции E 2 Fактивирует транскрипцию генов, связанных с вступлением в S-фазу: G 1/S-циклина (Е) S-циклина (А) E 2 F Cdk 2 энзимов, необходимых для репликации
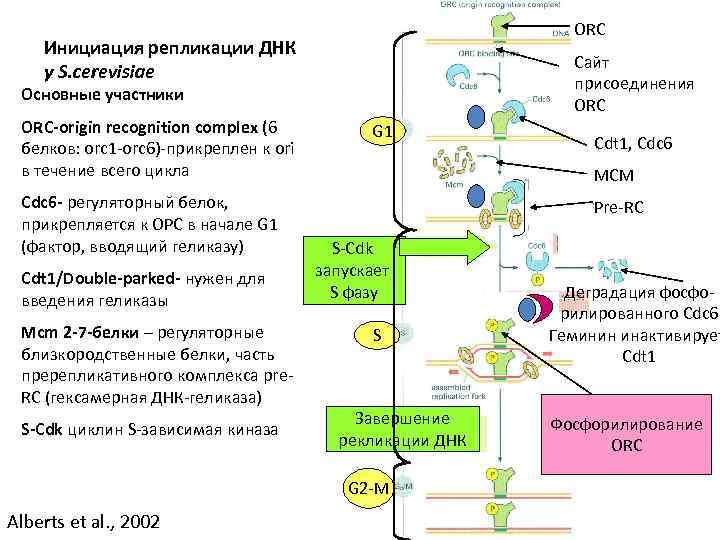
ORC Инициация репликации ДНК у S. cerevisiae Сайт присоединения ORC Основные участники ОRС-origin recognition complex (6 белков: orc 1 -orc 6)-прикреплен к ori в течение всего цикла Сdc 6 - регуляторный белок, прикрепляется к ОРС в начале G 1 (фактор, вводящий геликазу) Cdt 1/Double-parked- нужен для введения геликазы Mcm 2 -7 -белки – регуляторные близкородственные белки, часть пререпликативного комплекса pre. RC (гексамерная ДНК-геликаза) S-Cdk циклин S-зависимая киназа G 1 MCM Pre-RC S-Cdk запускает S фазу S Завершение рекликации ДНК G 2 -M Alberts et al. , 2002 Cdt 1, Cdc 6 Деградация фосфорилированного Cdc 6 Геминин инактивирует Cdt 1 Фосфорилирование ORC

Предотвращение повторной репликации S-Cdk: • -запускает репликацию ДНК • -фосфорилирует Сdc 6, он отделяется от ОRС- предотвращение репликации с этого ori. Фосфорилированный Сdc 6 узнается комплексом SCF, убиквитинизируется. • -фосфорилирует Mcm-белки , это вызывает их экспорт из ядра – гарантия того, что комплекс Mcm больше не соберется • -фосфорилирует Cdt 1 Geminin у многоклеточных накапливается в S, G 2, M Связывается - инактивирует Cdt 1 и препятствует повторной сборке пререпликативного сомплекса -лицензированию репликации • RESET: в конце митоза активность всех Cdk падает до нуля. • Сdc 6 и Mcm-белки и Cdt 1 дефосфорилируются, . • Геминин и все циклины Е, А и В разрушаются с помощью APC. • pre-ORC может собираться снова
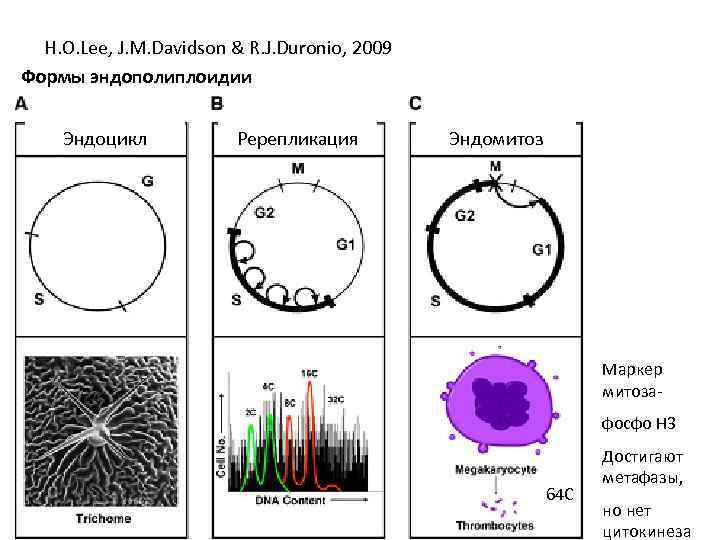
H. O. Lee, J. M. Davidson & R. J. Duronio, 2009 Формы эндополиплоидии Эндоцикл Ререпликация Эндомитоз Маркер митозафосфо Н 3 64 С Достигают метафазы, но нет цитокинеза
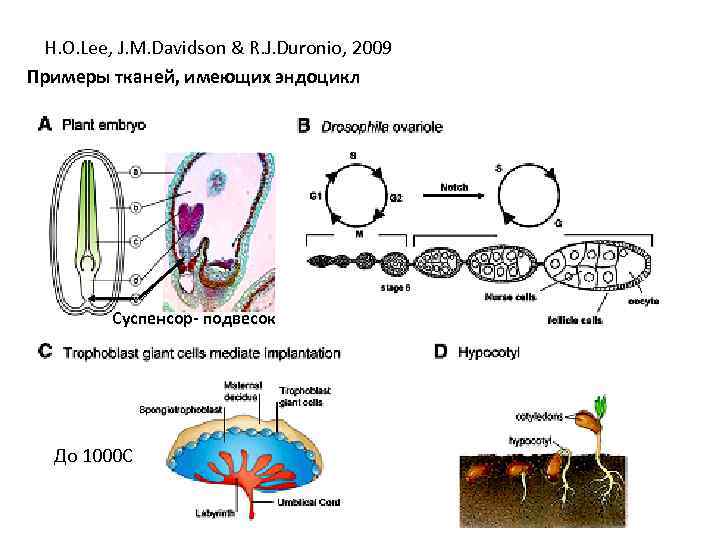
H. O. Lee, J. M. Davidson & R. J. Duronio, 2009 Примеры тканей, имеющих эндоцикл Суспенсор- подвесок До 1000 С
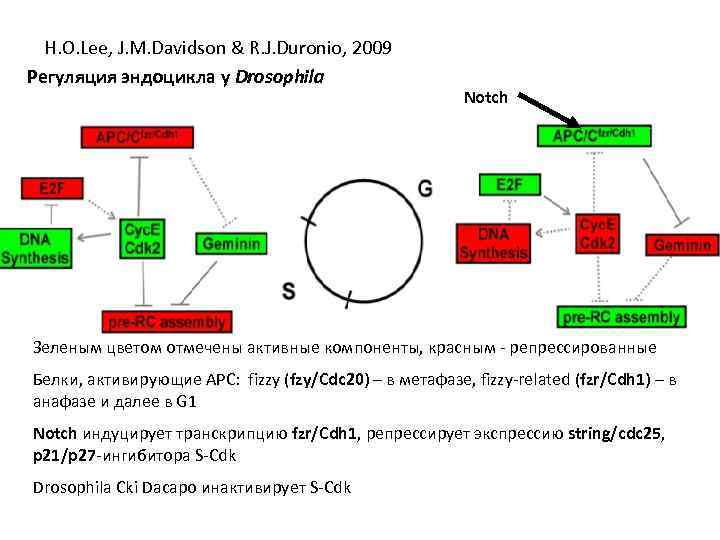
H. O. Lee, J. M. Davidson & R. J. Duronio, 2009 Регуляция эндоцикла у Drosophila Notch Зеленым цветом отмечены активные компоненты, красным - репрессированные Белки, активирующие АРС: fizzy (fzy/Cdc 20) – в метафазе, fizzy-related (fzr/Cdh 1) – в анафазе и далее в G 1 Notch индуцирует транскрипцию fzr/Cdh 1, репрессирует экспрессию string/cdc 25, p 21/p 27 -ингибитора S-Cdk Drosophila Cki Dacapo инактивирует S-Cdk
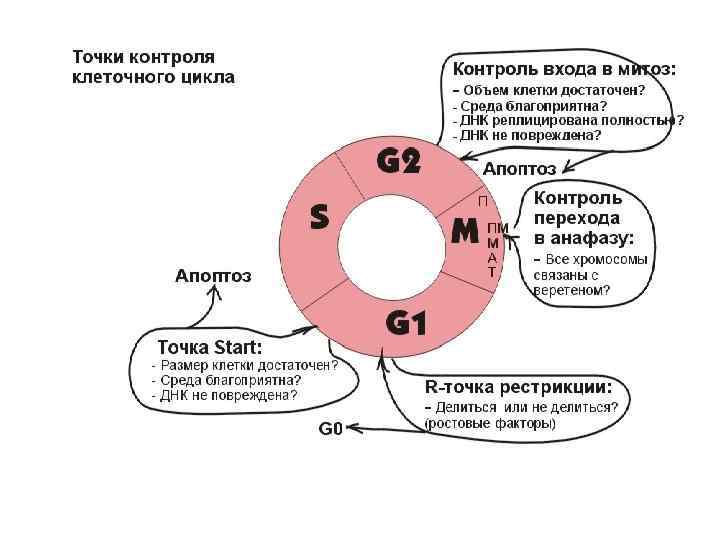
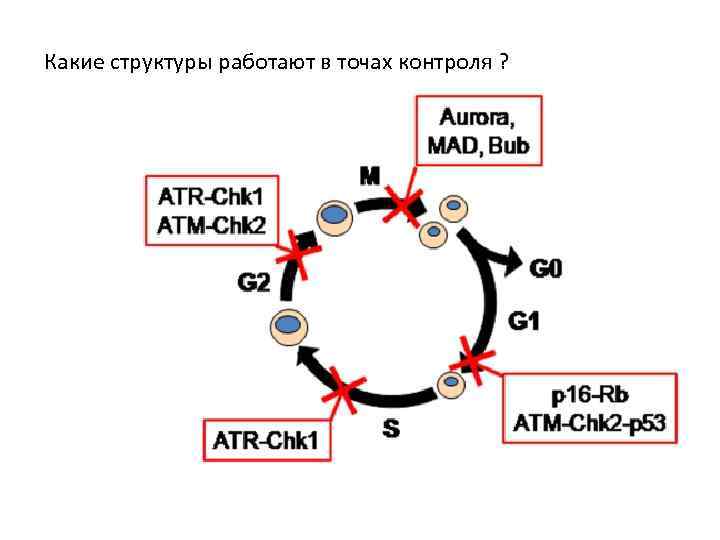
Какие структуры работают в точах контроля ?

Изучение точек контроля у дрожжей: Получение условных мутагенчувствительных мутаций • Обработка слабой дозой радиации (мутации rad) • веществами, блокирующими репликацию (гидроксимочевина) (мутации hus) • веществами, блокирующими сборку веретена деления (мутации mad - mitotic arrest deficient, мутации bub - budding uninhibited by benzimadazole) Селекция мутантов с неправильной реакцией на обработку (не останавливали клеточный цикл)

Точки контроля клеточного цикла. Переход М-А -дефект веретена -дефект полюсов (в т. ч. нереплицированная центросома) -дефект кинетохоров К неприкрепленному кинетохору присоединяется белок Mad 2, ингибирует Cdc 20 -APC Мутации: mad- metaphase arrest deficient, bub – budding uninhibited Benzimadazole Кинетохорный белок Bub 1 (киназа): запускает сборку компонентов кинетохора (Bub. R 1, CENP-F), Контролирует правильное формирование кинетохора.
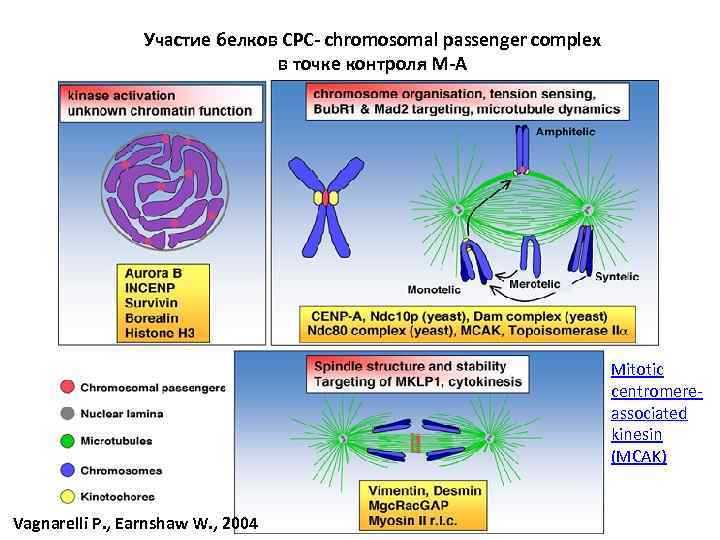
Участие белков СРС- chromosomal passenger complex в точке контроля М-А Mitotic centromereassociated kinesin (MCAK) Vagnarelli P. , Earnshaw W. , 2004
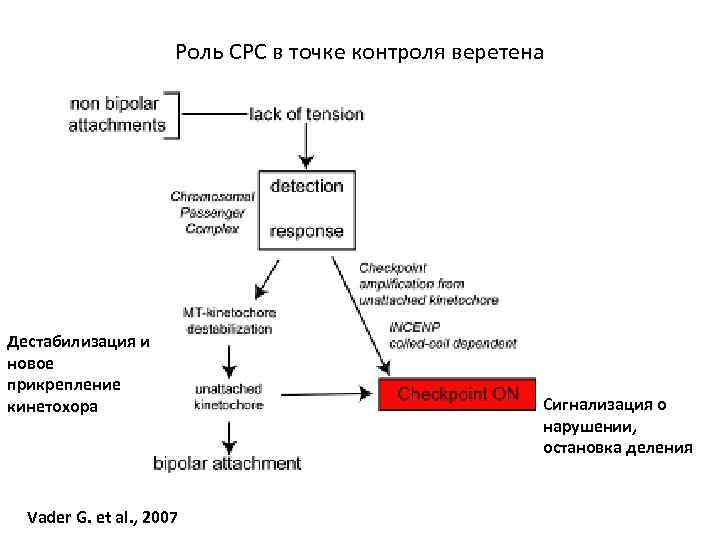
Роль СРС в точке контроля веретена Дестабилизация и новое прикрепление кинетохора Vader G. et al. , 2007 Сигнализация о нарушении, остановка деления
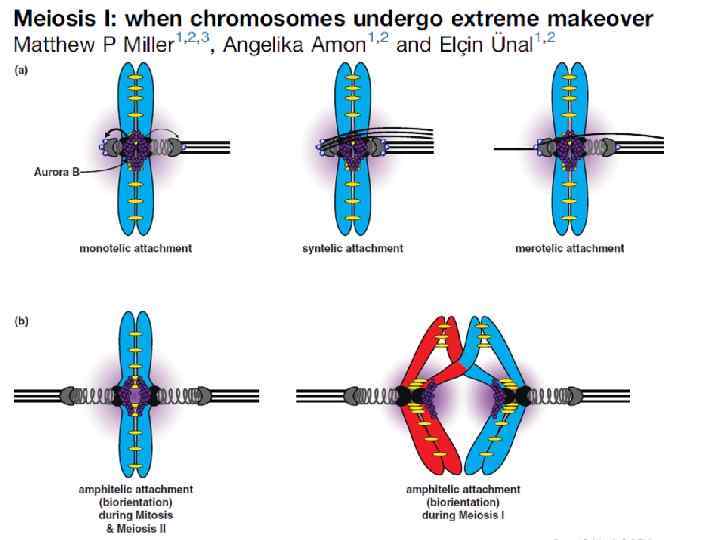

Точка контроля клеточного цикла. G 1 контроль размера клетки перед Стартом Сln 3 у дрожжей G 1 контроль повреждения ДНК. Поврежденная ДНК – активация р53 – CKI Блок активации G 1/S-Cdk, S-Cdk Повышенная стимуляция митогеном. Активация р53 – CKI - апоптоз Блок активации G 1/S-Cdk, S-Cdk

Точки контроля клеточного цикла: Повреждения ДНК • Болезнь «атаксия телангиэктазия» - синдром Луи-Бара – дефект одной из протеинкиназ, фосфорилирующих р53 в ответ на облучение - ATМкиназа (ATM – ataxia telangiectasia mutated) (ответ на двунитевые разрывы) • ATR – ATM and Rad 3 related – ответ на многие формы повреждения ДНК (генотоксический стресс ) • киназы фосфатидилинозитол 3 -подобные. Центральные компоненты ответа на повреждения ДНК • Белок RPA взаимодействует с однонитевыми разрывами ДНК (остановленные вилки репликации, двунитевые разрывы ДНК, сайты репарации эксцизионные, мисматч) • привлекает ATR-киназу и белок ATRIP (ATR-interacting protein) – Rad 17 - подобен репликативному фактору С – Rad 9 – кольцевой белковый комплекс, подобный PCNA • ATM и ATR активируют серин-треонин-киназы точки контроля Chk 1 и Chk 2 • Chk 1 и Chk 2 ингибируют фосфорилированием Cdc 25 фосфатазу, предотвращая вступление в митоз, фосфорилируют р53.
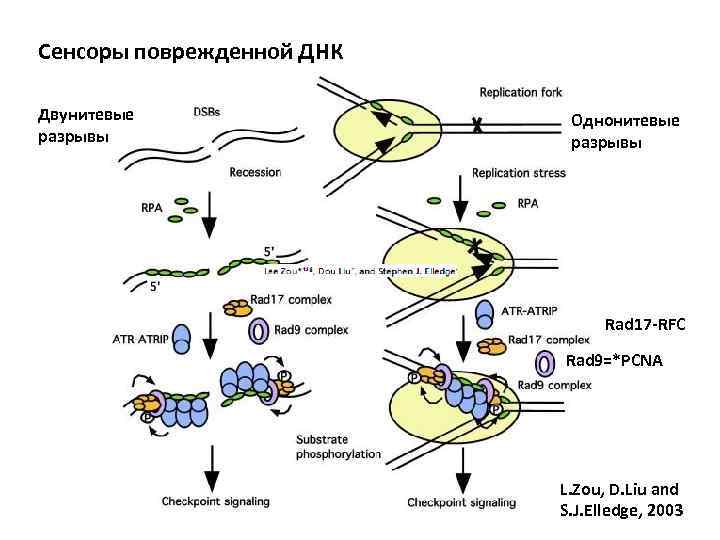
Cенсоры поврежденной ДНК Двунитевые разрывы Однонитевые разрывы Rad 17 -RFC Rad 9=*PCNA L. Zou, D. Liu and S. J. Elledge, 2003
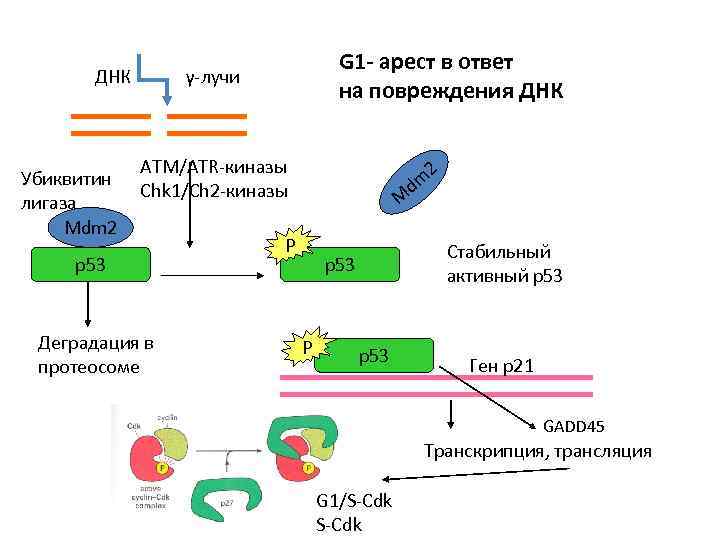
ДНК Убиквитин лигаза Mdm 2 G 1 - арест в ответ на повреждения ДНК γ-лучи ATМ/ATR-киназы Chk 1/Ch 2 -киназы p 53 Деградация в протеосоме dm 2 M P Стабильный активный р53 p 53 P p 53 Ген р21 GADD 45 Транскрипция, трансляция G 1/S-Cdk

Сенсоры повреждения ДНК: RPA – ATR - амплификация сигнала ATRIP Передача сигнала: Активация Chk 1, 2 киназ Эффекторная часть: Фосфорилирование Cdc 25 – остановка входа в митоз Фосфорилирование р53 – транскрипция гена белка CKI – ингибитора комплекса cdk-cyclin
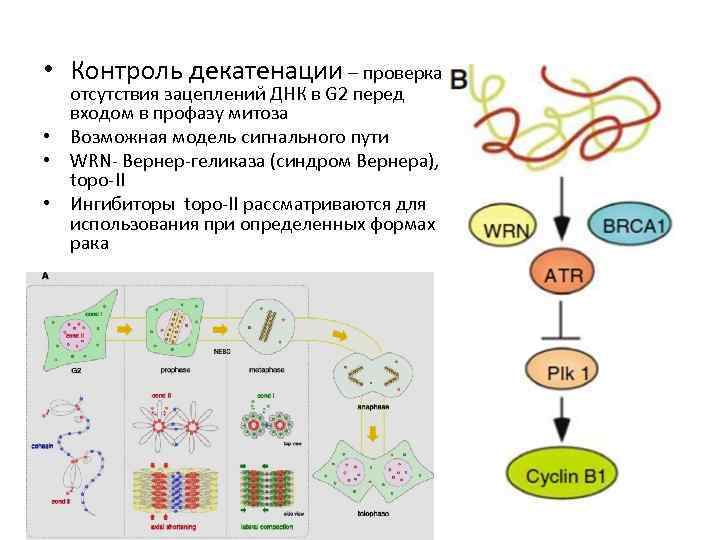
• Контроль декатенации – проверка отсутствия зацеплений ДНК в G 2 перед входом в профазу митоза • Возможная модель сигнального пути • WRN- Вернер-геликаза (синдром Вернера), topo-II • Ингибиторы topo-II рассматриваются для использования при определенных формах рака

• Antephase checkpoint. • Точка контроля в Антефазе отлична от контроля декатенации. • Клетки откладывают вступление в профазу митоза (конденсацию хроматина) при обработке Х-лучами, микротрубочковыми ядами (колхицином), низкой температурой. Клетки, вступившие в профазу, деконденсируют свой хроматин (в нейробластах саранчи после облучения уменьшилось число клеток в профазе) • Короткий промежуток в конце G 2 Ключевой белок – CHFR – неканоническая убиквитин-лигаза. Убиквитинизирует polo-like (Plk) киназу, тем самым воздействуя на Cdk-1, откладывая вхождение в митоз. P 38 – киназа играет роль в ответе на UV-облучение, осмотический стресс
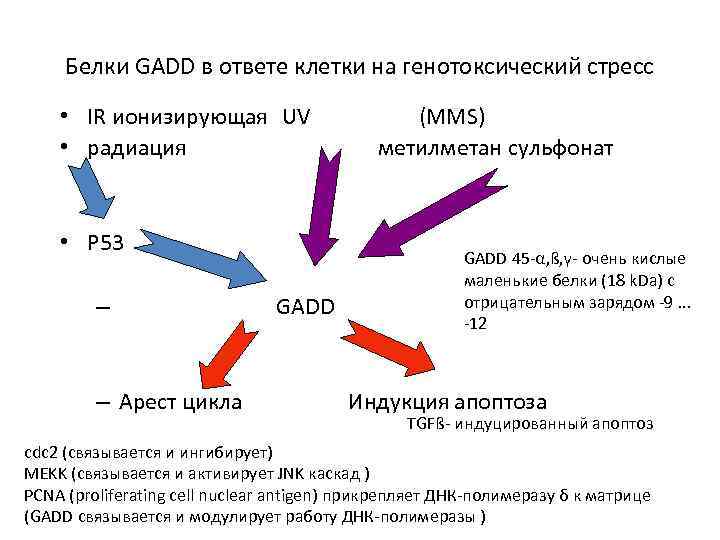
Белки GADD в ответе клетки на генотоксический стресс • IR ионизирующая UV • радиация • P 53 – – Арест цикла GADD (MMS) метилметан сульфонат GADD 45 -α, ß, γ- очень кислые маленькие белки (18 k. Da) с отрицательным зарядом -9. . . -12 Индукция апоптоза TGFß- индуцированный апоптоз cdc 2 (связывается и ингибирует) MEKK (связывается и активирует JNK каскад ) PCNA (proliferating cell nuclear antigen) прикрепляет ДНК-полимеразу δ к матрице (GADD связывается и модулирует работу ДНК-полимеразы )
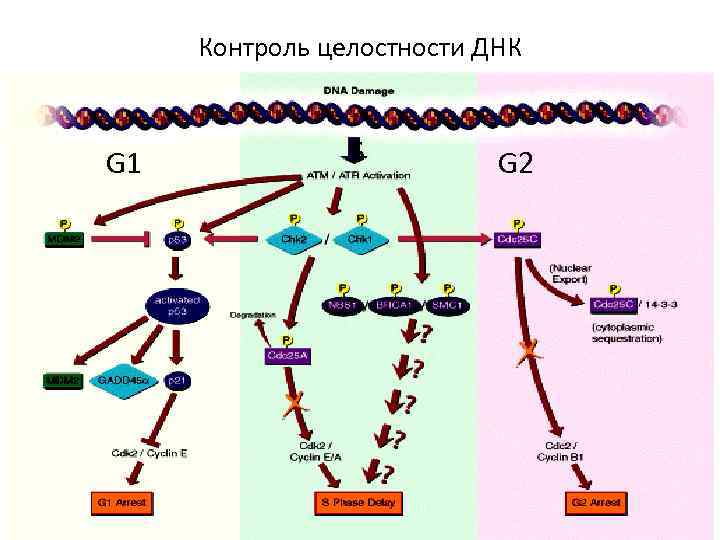
Контроль целостности ДНК G 1 S G 2
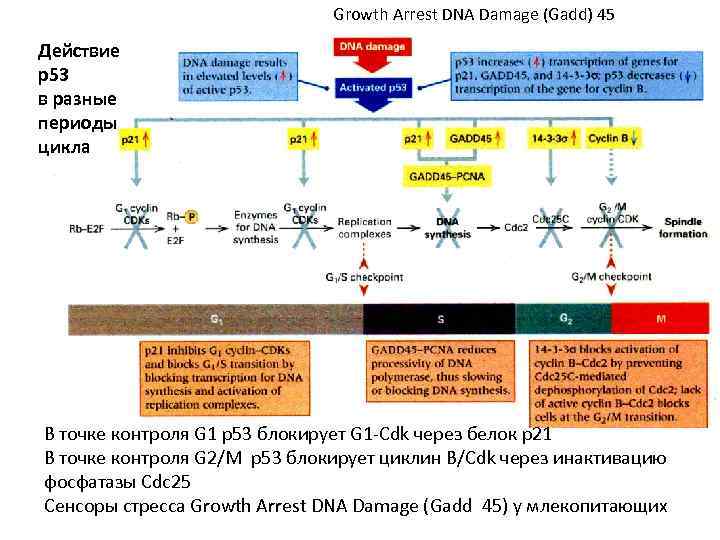
Growth Arrest DNA Damage (Gadd) 45 Действие р53 в разные периоды цикла В точке контроля G 1 р53 блокирует G 1 -Cdk через белок р21 В точке контроля G 2/М р53 блокирует циклин В/Cdk через инактивацию фосфатазы Cdc 25 Сенсоры стресса Growth Arrest DNA Damage (Gadd 45) у млекопитающих
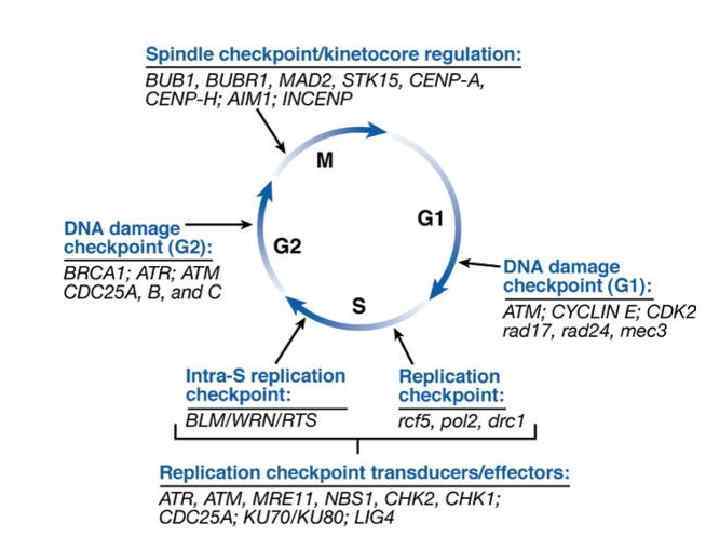

Надклеточный контроль клеточного деления, роста и апоптоза Размер организма и органа зависит от числа клеток и их массы. Число клеток определяется их рождением и гибелью Экстраклеточные сигналы, регулирующие эти процессы, часто называют «факторы роста» в широком смысле. Для точного выражения следует различать: 1. Митогены – стимулируют клеточные деления, снимая внутриклеточный блок с продвижения по циклу. 2. Ростовые факторы – стимулируют увеличение массы клетки, вызывая синтез макромолекул и ингибируя их деградацию 3. Факторы выживания – супрессируют апоптоз

Апоптоз, морфологические изменения: • Конденсация хроматина, фрагментация и разрушение ядра. • Цитоскелет сжимается. • Клеточная мембрана вспухает. • Клетки фрагментируются, образуются «апоптозные тела» . Молекулярные изменения: • Возрастает концентрация Са 2+ • Активируются протеазы-каспазы • Разрушение ламины. • Разрезание белка, инактивирующего эндонуклеазу. • ДНК режется на фрагменты • Клеточная поверхность меняется- теряется сиаловая кислота на гликопротеинах и гликолипидах-, что вызывает быстрый фагоцитоз клетки макрофагами или соседями • На мембране появляются рецепторы витронектина, притягивающие макрофаги, фосфатидилсерин появляется на внешнем мембранном слое,
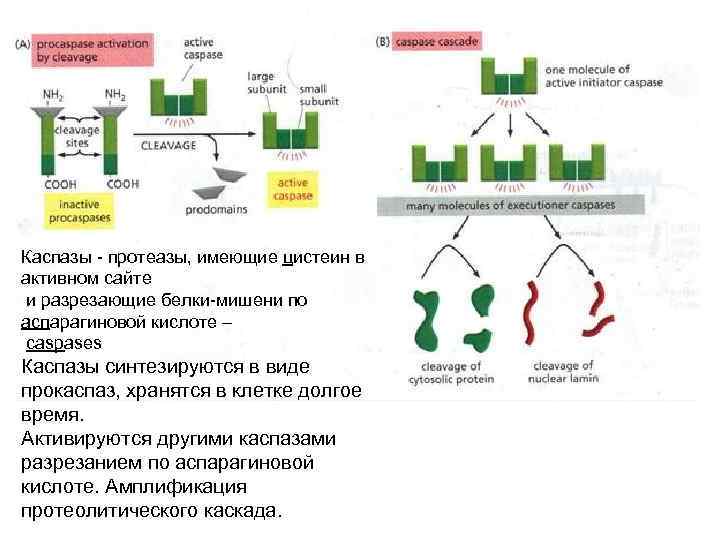
Каспазы - протеазы, имеющие цистеин в активном сайте и разрезающие белки-мишени по аспарагиновой кислоте – caspases Каспазы синтезируются в виде прокаспаз, хранятся в клетке долгое время. Активируются другими каспазами разрезанием по аспарагиновой кислоте. Амплификация протеолитического каскада.
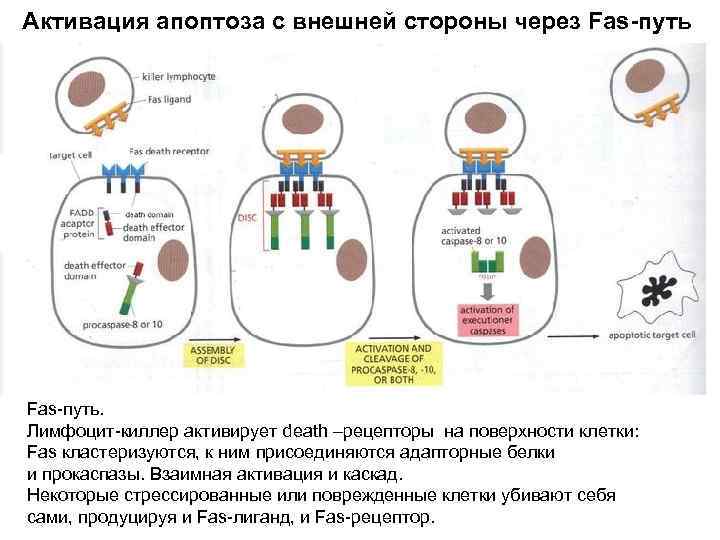
Активация апоптоза с внешней стороны через Fas-путь. Лимфоцит-киллер активирует death –рецепторы на поверхности клетки: Fas кластеризуются, к ним присоединяются адапторные белки и прокаспазы. Взаимная активация и каскад. Некоторые стрессированные или поврежденные клетки убивают себя сами, продуцируя и Fas-лиганд, и Fas-рецептор.
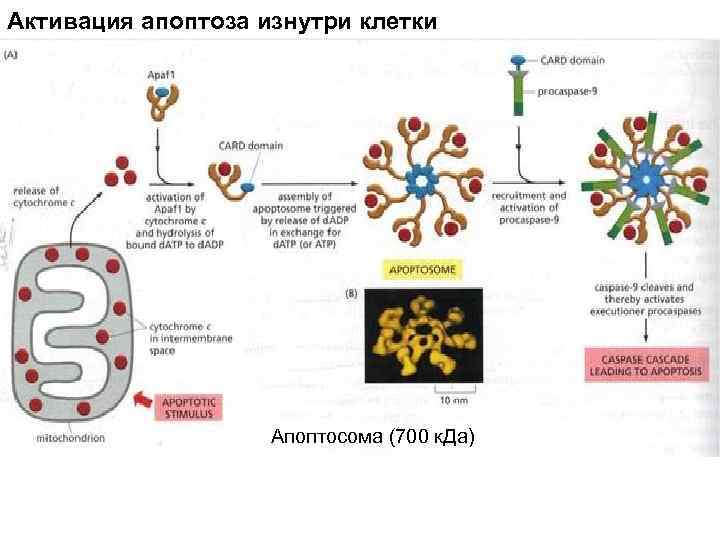
Активация апоптоза изнутри клетки Апоптосома (700 к. Да)
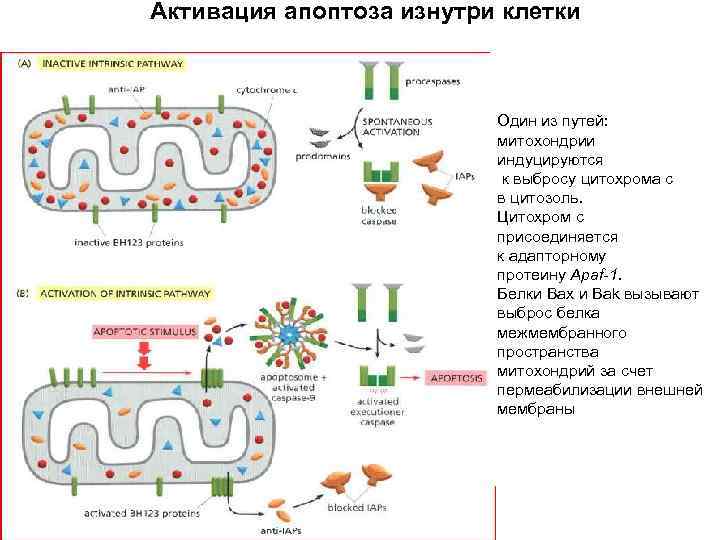
Активация апоптоза изнутри клетки Прокаспаза-3 Один из путей: митохондрии индуцируются к выбросу цитохрома с в цитозоль. Цитохром с присоединяется к адапторному протеину Apaf-1. Белки Bax и Bak вызывают выброс белка межмембранного пространства митохондрий за счет пермеабилизации внешней мембраны

Митогены (более 50 белков) Фактор роста тромбоцитов PDGF –platelet-derived grows factor Клетки фибробластов в культуре делились с добавлением сыворотки крови и не делились в плазме. Плазма – забирают жидкую часть крови без образования сгустка. Сыворотка – то же после образования сгустка. Клетки делились при добавлении экстракта фибробластов В организме тромбоциты стимулируют деление клеток при заживлении ран. EGF –epidermal growth factor PDGF (фибробласты, гладкие мышечные, нейроглиальные) и EGF – широкого спектра дейстия Эритропоэтин – только для эритроцитов TGF-β – трансформирующий фактор роста – одни клетки стимулирует, другие ингибирует
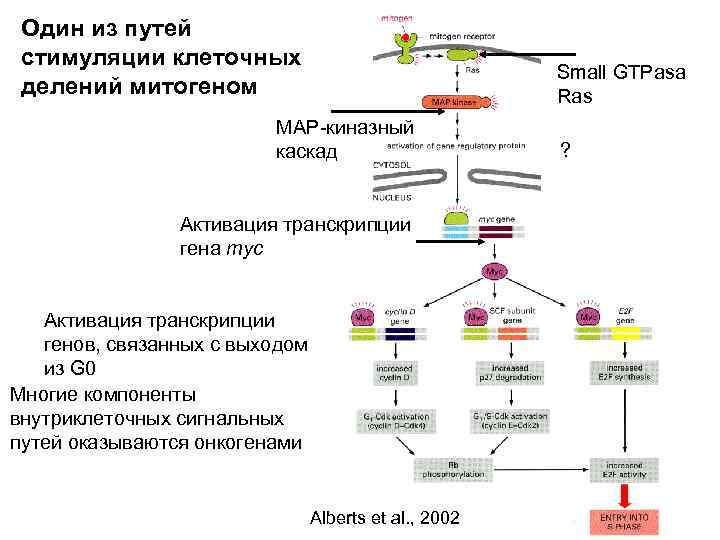
Один из путей стимуляции клеточных делений митогеном Small GTPasa Ras MAP-киназный каскад Активация транскрипции гена myc Активация транскрипции генов, связанных с выходом из G 0 Многие компоненты внутриклеточных сигнальных путей оказываются онкогенами Alberts et al. , 2002 ?
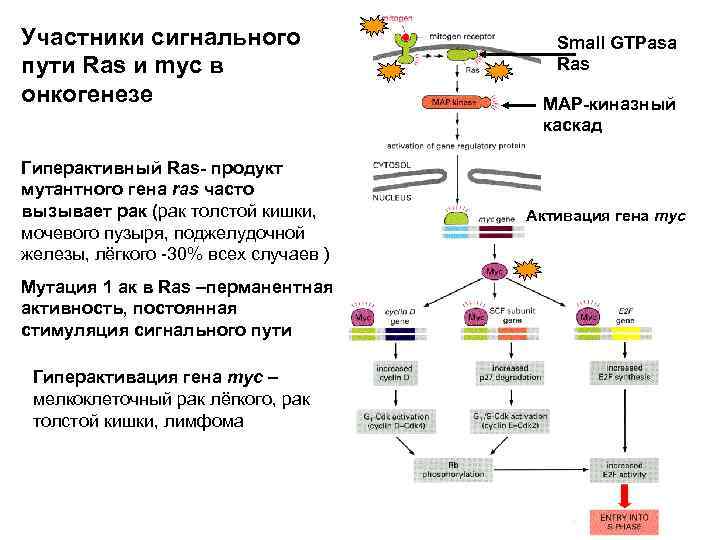
Участники сигнального пути Ras и myc в онкогенезе Гиперактивный Ras- продукт мутантного гена ras часто вызывает рак (рак толстой кишки, мочевого пузыря, поджелудочной железы, лёгкого -30% всех случаев ) Мутация 1 ак в Ras –перманентная активность, постоянная стимуляция сигнального пути Гиперактивация гена myc – мелкоклеточный рак лёгкого, рак толстой кишки, лимфома Small GTPasa Ras MAP-киназный каскад Активация гена myc
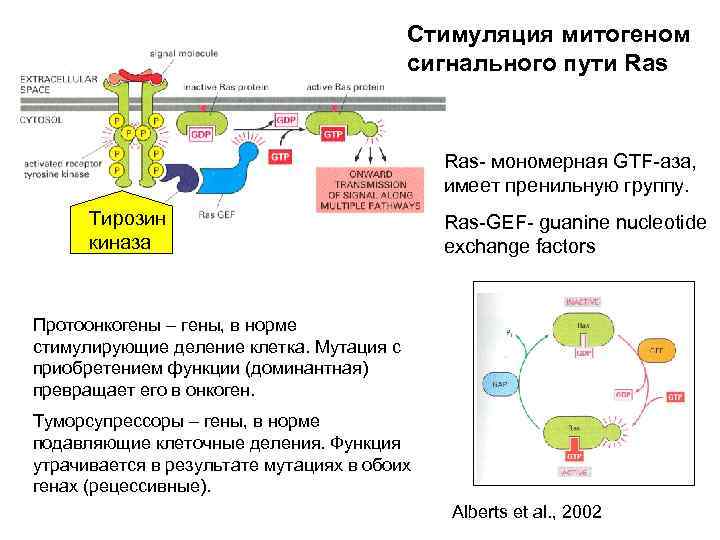
Стимуляция митогеном сигнального пути Ras- мономерная GTF-аза, имеет пренильную группу. Тирозин киназа Ras-GEF- guanine nucleotide exchange factors Протоонкогены – гены, в норме стимулирующие деление клетка. Мутация с приобретением функции (доминантная) превращает его в онкоген. Туморсупрессоры – гены, в норме подавляющие клеточные деления. Функция утрачивается в результате мутациях в обоих генах (рецессивные). Alberts et al. , 2002
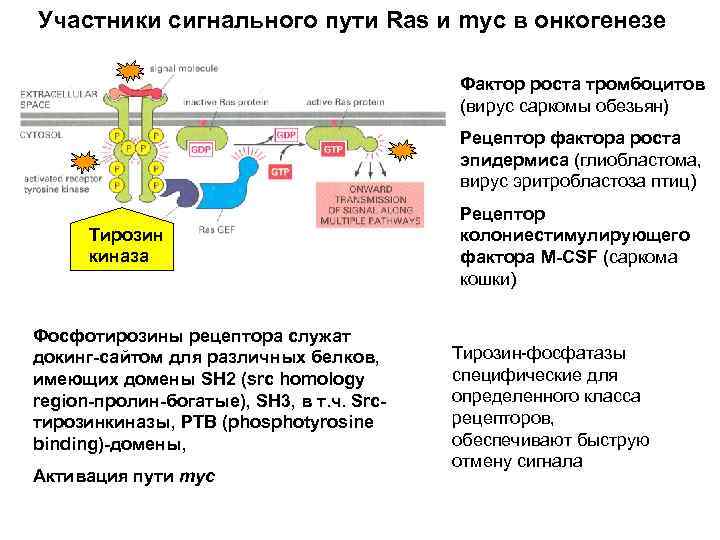
Участники сигнального пути Ras и myc в онкогенезе Фактор роста тромбоцитов (вирус саркомы обезьян) Рецептор фактора роста эпидермиса (глиобластома, вирус эритробластоза птиц) Тирозин киназа Фосфотирозины рецептора служат докинг-сайтом для различных белков, имеющих домены SH 2 (src homology region-пролин-богатые), SH 3, в т. ч. Srcтирозинкиназы, PTB (phosphotyrosine binding)-домены, Активация пути myc Рецептор колониестимулирующего фактора M-CSF (саркома кошки) Тирозин-фосфатазы специфические для определенного класса рецепторов, обеспечивают быструю отмену сигнала
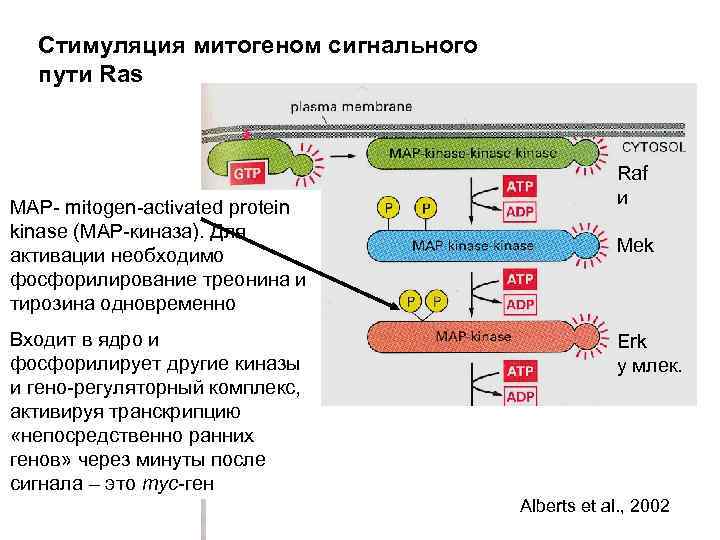
Стимуляция митогеном сигнального пути Ras MAP- mitogen-activated protein kinase (MAP-киназа). Для активации необходимо фосфорилирование треонина и тирозина одновременно Входит в ядро и фосфорилирует другие киназы и гено-регуляторный комплекс, активируя транскрипцию «непосредственно ранних генов» через минуты после сигнала – это myc-ген Raf и Mek Erk у млек. Alberts et al. , 2002
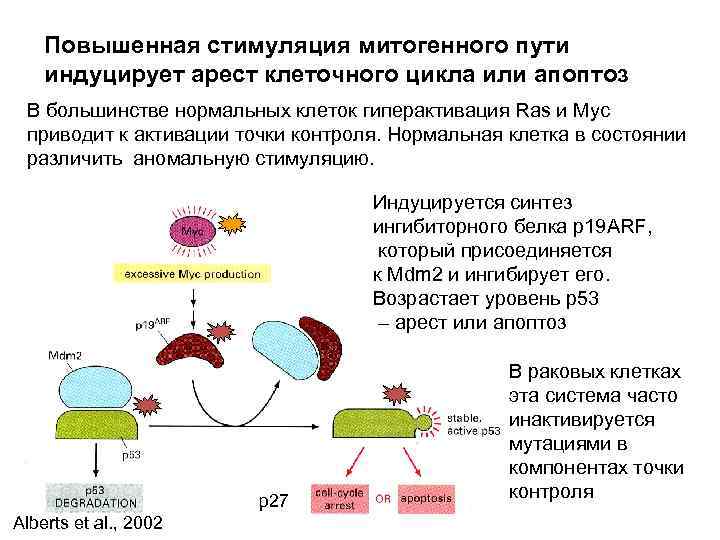
Повышенная стимуляция митогенного пути индуцирует арест клеточного цикла или апоптоз В большинстве нормальных клеток гиперактивация Ras и Myc приводит к активации точки контроля. Нормальная клетка в состоянии различить аномальную стимуляцию. Индуцируется синтез ингибиторного белка р19 ARF, который присоединяется к Mdm 2 и ингибирует его. Возрастает уровень р53 – арест или апоптоз р27 Alberts et al. , 2002 В раковых клетках эта система часто инактивируется мутациями в компонентах точки контроля

Другие способы регуляции митогенной активности Репликативное старение клеток, связанное с теломерами. У фибробластов через 25 -50 делений в среде с митогенами наступает арест клеточного цикла. Активация пути р53 в ответ на повреждения теломер. • У грызунов теломераза активна. Контроль над делениями осуществляется механизмом p 19 ARF. Мутации в нем могут приводить к «бессмертию» культуры клеток • Количество белка CKI p 27 прогрессивно нарастает в клетках, которые делятся определенное число раз, прежде чем войдут в перманентный арест при терминальной дифференцировке. • У мышей, дефицитных по р27, общее число клеток увеличено
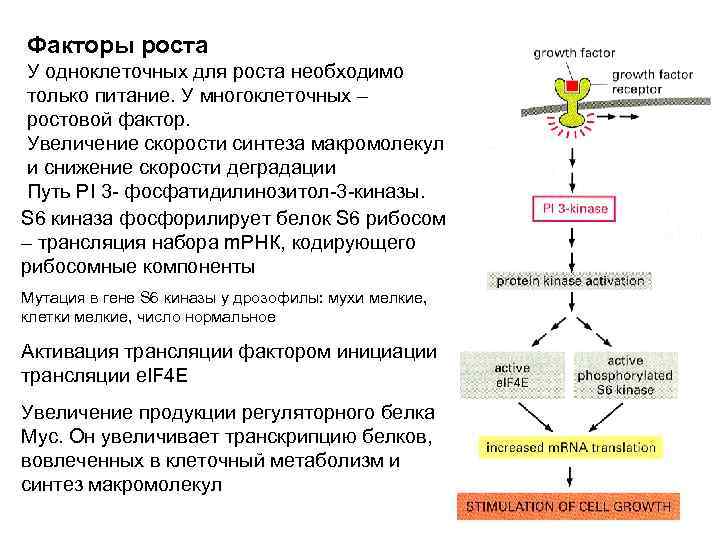
Факторы роста У одноклеточных для роста необходимо только питание. У многоклеточных – ростовой фактор. Увеличение скорости синтеза макромолекул и снижение скорости деградации Путь PI 3 - фосфатидилинозитол-3 -киназы. S 6 киназа фосфорилирует белок S 6 рибосом – трансляция набора m. РНК, кодирующего рибосомные компоненты Мутация в гене S 6 киназы у дрозофилы: мухи мелкие, клетки мелкие, число нормальное Активация трансляции фактором инициации трансляции e. IF 4 E Увеличение продукции регуляторного белка Myc. Он увеличивает транскрипцию белков, вовлеченных в клеточный метаболизм и синтез макромолекул
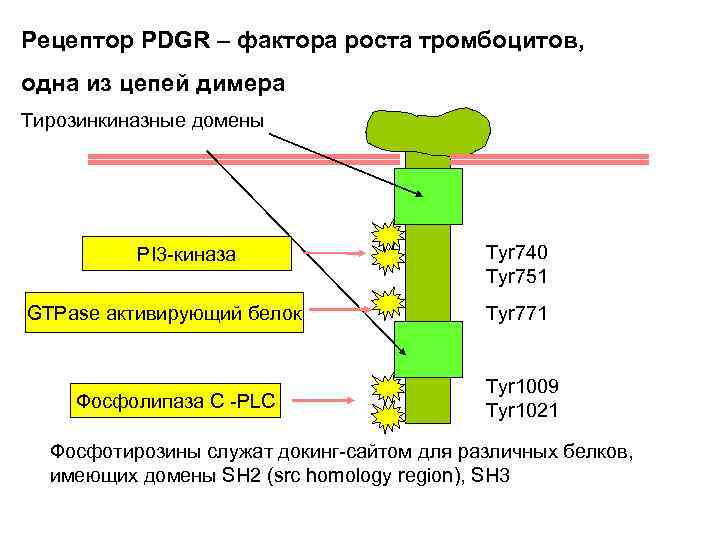
Рецептор PDGR – фактора роста тромбоцитов, одна из цепей димера Тирозинкиназные домены PI 3 -киназа GTPase активирующий белок Фосфолипаза С -PLC Tyr 740 Tyr 751 Tyr 771 Tyr 1009 Tyr 1021 Фосфотирозины служат докинг-сайтом для различных белков, имеющих домены SH 2 (src homology region), SH 3
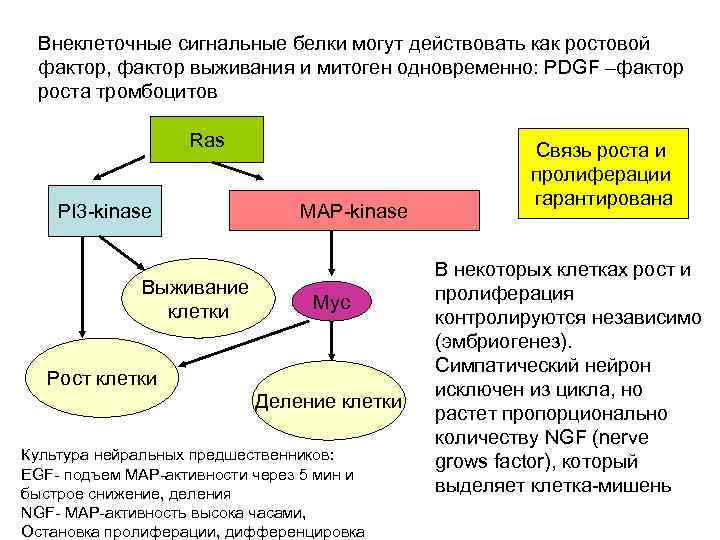
Внеклеточные сигнальные белки могут действовать как ростовой фактор, фактор выживания и митоген одновременно: PDGF –фактор роста тромбоцитов Ras PI 3 -kinase Выживание клетки MAP-kinase Myc Рост клетки Деление клетки Культура нейральных предшественников: EGF- подъем МАР-активности через 5 мин и быстрое снижение, деления NGF- MAP-активность высока часами, Остановка пролиферации, дифференцировка Связь роста и пролиферации гарантирована В некоторых клетках рост и пролиферация контролируются независимо (эмбриогенез). Симпатический нейрон исключен из цикла, но растет пропорционально количеству NGF (nerve grows factor), который выделяет клетка-мишень
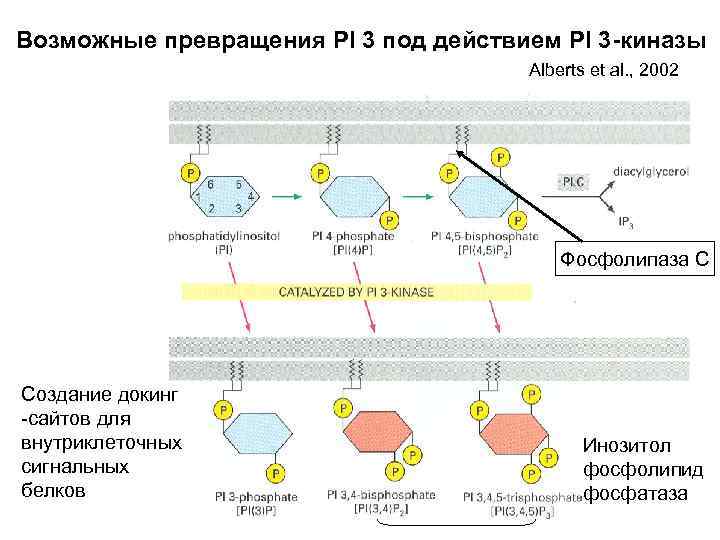
Возможные превращения PI 3 под действием PI 3 -киназы Alberts et al. , 2002 Фосфолипаза С Создание докинг -сайтов для внутриклеточных сигнальных белков Инозитол фосфолипид фосфатаза
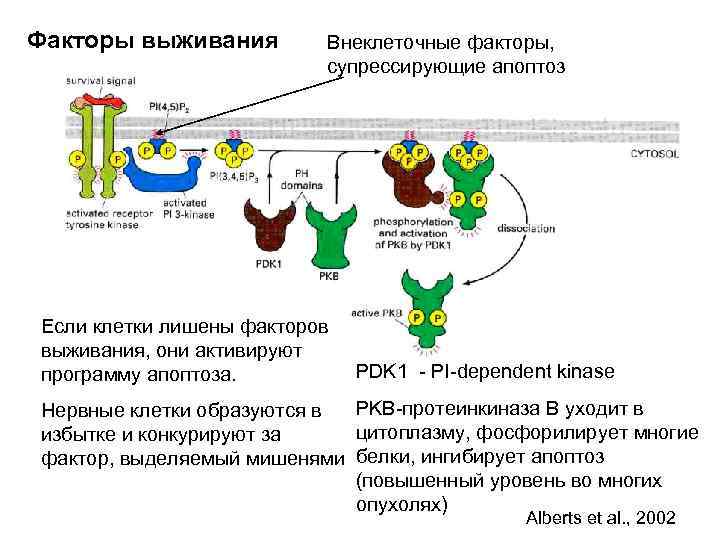
Факторы выживания Внеклеточные факторы, супрессирующие апоптоз Если клетки лишены факторов выживания, они активируют программу апоптоза. PDK 1 - PI-dependent kinase PKB-протеинкиназа В уходит в Нервные клетки образуются в цитоплазму, фосфорилирует многие избытке и конкурируют за фактор, выделяемый мишенями белки, ингибирует апоптоз (повышенный уровень во многих опухолях) Alberts et al. , 2002
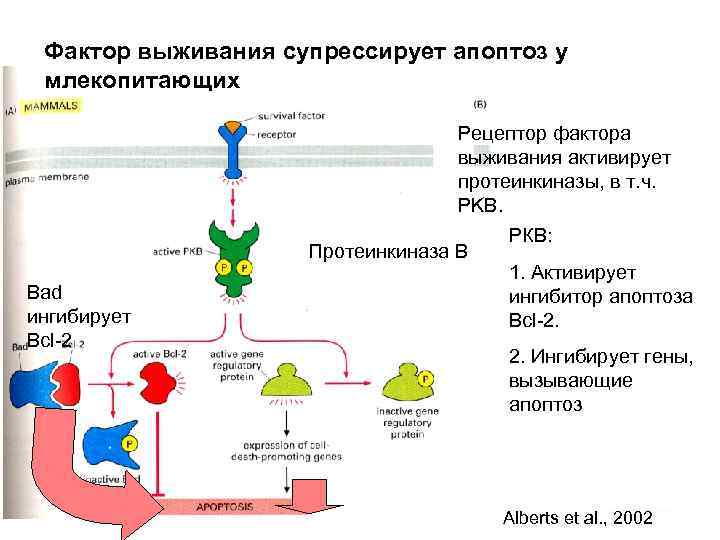
Фактор выживания супрессирует апоптоз у млекопитающих Рецептор фактора выживания активирует протеинкиназы, в т. ч. PKB. Протеинкиназа В Bad ингибирует Bcl-2 РКВ: 1. Активирует ингибитор апоптоза Bcl-2. 2. Ингибирует гены, вызывающие апоптоз Alberts et al. , 2002
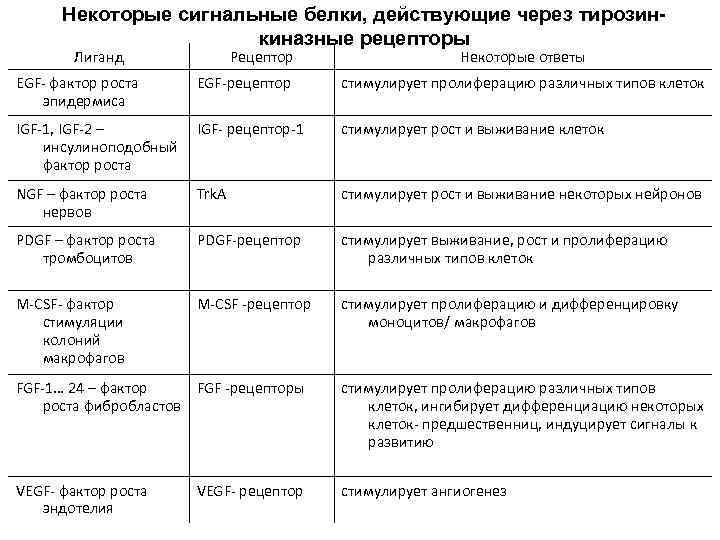
Некоторые сигнальные белки, действующие через тирозинкиназные рецепторы Лиганд Рецептор Некоторые ответы EGF- фактор роста эпидермиса EGF-рецептор стимулирует пролиферацию различных типов клеток IGF-1, IGF-2 – инсулиноподобный фактор роста IGF- рецептор-1 стимулирует рост и выживание клеток NGF – фактор роста нервов Trk. A стимулирует рост и выживание некоторых нейронов PDGF – фактор роста тромбоцитов PDGF-рецептор стимулирует выживание, рост и пролиферацию различных типов клеток M-CSF- фактор стимуляции колоний макрофагов M-CSF -рецептор стимулирует пролиферацию и дифференцировку моноцитов/ макрофагов FGF-1… 24 – фактор FGF -рецепторы роста фибробластов стимулирует пролиферацию различных типов клеток, ингибирует дифференциацию некоторых клеток- предшественниц, индуцирует сигналы к развитию VEGF- фактор роста эндотелия стимулирует ангиогенез VEGF- рецептор

Инсулиноподобный фактор роста IGF-1 Собаки крупных пород имели аллель гена IGF-1, ассоциированный с большей экспрессией, собаки мелких пород – слабоэкспрессирующийся аллель. У человека в промоторе гена обнаружен вариабельный участок, состоящий из CA-повторов, число которых может варьировать от 10 до 24 (в среднем их 19). Данные говорят о корреляции числа CAповторов с уровнем экспрессии гена. В одинаковой степени как малое, так и большое число этих повторов ассоциируется со снижением циркуляции IGF-1. Носители 19 CA-повторов (их также называют носителями аллеля 192) в процессе тренировок развивают силу в большей степени, чем носители других аллелей. Рецептор инсулиноподобного фактора роста IGFR-1 У долгожителей (старше 100 лет) и их детей чаще встречались мутации рецептора к инсулиноподобному фактору роста-1. У носителей мутаций был нарушен процесс связывания клеток с ИФР-1, повышение уровня ИФР-1 в крови на 37% Каскад IGFR-1 влияет на продолжительность жизни
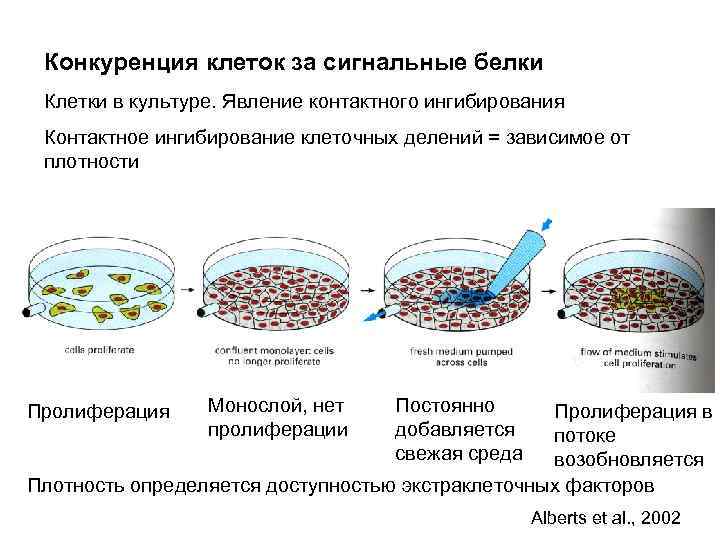
Конкуренция клеток за сигнальные белки Клетки в культуре. Явление контактного ингибирования Контактное ингибирование клеточных делений = зависимое от плотности Пролиферация Монослой, нет пролиферации Постоянно добавляется свежая среда Пролиферация в потоке возобновляется Плотность определяется доступностью экстраклеточных факторов Alberts et al. , 2002
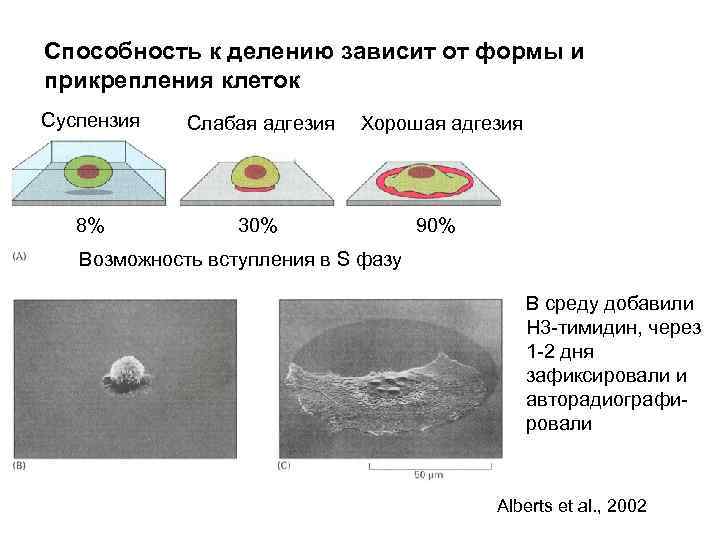
Способность к делению зависит от формы и прикрепления клеток Суспензия Слабая адгезия Хорошая адгезия 8% 30% 90% Возможность вступления в S фазу В среду добавили Н 3 -тимидин, через 1 -2 дня зафиксировали и авторадиографировали Alberts et al. , 2002
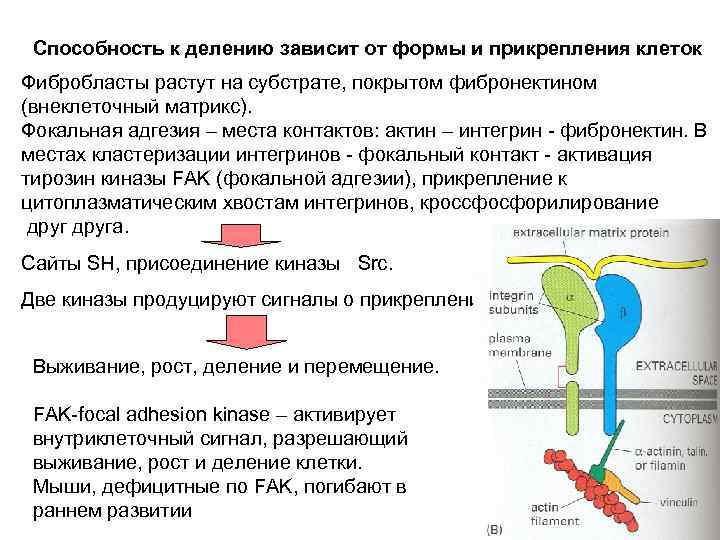
Способность к делению зависит от формы и прикрепления клеток Фибробласты растут на субстрате, покрытом фибронектином (внеклеточный матрикс). Фокальная адгезия – места контактов: актин – интегрин - фибронектин. В местах кластеризации интегринов - фокальный контакт - активация тирозин киназы FAK (фокальной адгезии), прикрепление к цитоплазматическим хвостам интегринов, кроссфосфорилирование друга. Сайты SH, присоединение киназы Src. Две киназы продуцируют сигналы о прикреплении. Выживание, рост, деление и перемещение. FAK-focal adhesion kinase – активирует внутриклеточный сигнал, разрешающий выживание, рост и деление клетки. Мыши, дефицитные по FAK, погибают в раннем развитии

Цитокиновые рецепторы Jak-STAT – сигнальный путь: Интерфероновый рецептор Janus-киназы – цитоплазматические тирозин-киназы STAT – signal transducers and activators of transcription Лиганды: интерфероны α и γ (активация макрофагов, увеличение устойчивости к вирусной инфекции), Эритропоэтин (выживание, пролиферация и дифференцировка эритроидного ряда), гормон роста, пролактин
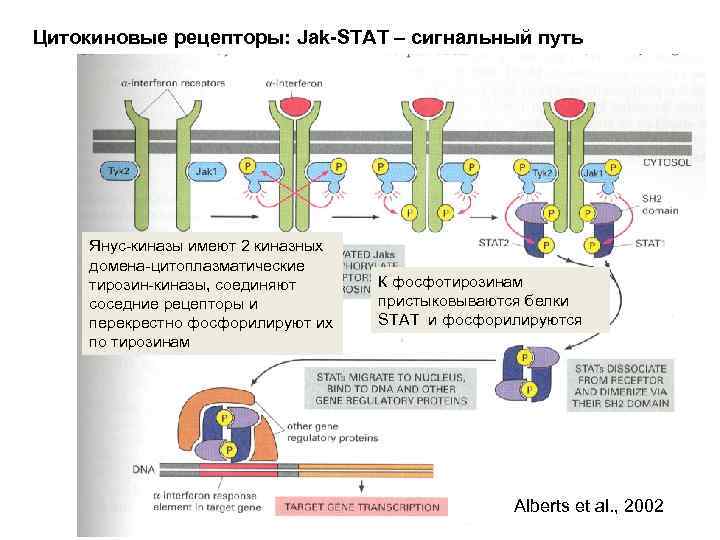
Цитокиновые рецепторы: Jak-STAT – сигнальный путь Янус-киназы имеют 2 киназных домена-цитоплазматические тирозин-киназы, соединяют соседние рецепторы и перекрестно фосфорилируют их по тирозинам К фосфотирозинам пристыковываются белки STAT и фосфорилируются Alberts et al. , 2002

Внеклеточные сигналы, ингибирующие рост TGF-β –большое семейство родственных белков. Растворимые димеры, действуют как гормоны или локальные медиаторы, градуирующие морфогены. Суперсемейство: TGF-β, активины и BMP TGF-β ингибирует пролиферацию нескольких типов клеток, блокируя клеточный цикл в G 1 или стимулируя апоптоз. Градуирующие морфогены в эмбриогенезе Рецепторы TGF-β - серин-треонин киназы. Активируется путь Smads. Изменения в транскрипции генов, регулирующих клеточные деления, дифференцировка, образование внеклеточного матрикса и смерть. BMP- bone morphogenetic protein из семейства TGF-β. Помогает включить апоптоз в тканях между развивающимися пальцами, в молочной железе Myostatin (то же семейство) – ингибирует пролиферацию миобластов.

Внеклеточные сигналы, ингибирующие рост Белки семейства TGF β (Трансформирующий фактор роста β) Действуют как гормоны или локальные медиаторы Представитель суперсемейства родственных полипептидов, участвующих в клеточной дифференцировке и эмбриогенезе (Dpp(dros)=BMP 4(mam)). Формирование костей, хрящей, развитие половых органов. Выполняют функции факторов роста и подавляют рост. Чаще противодействуют митогенам, вызывая задержку клеточного цикла и развитие морфологических структур эмбриона. Стимулирует: - синтез белков внеклеточного матрикса (коллагены 1, 4, фибронектин) - остеогенную активность - рост симпатических нейронов -дифференцировку клеток гладкой мускулатуры -Хемотаксический фактор для моноцитов, фибробластов, астроцитов. -Подавляет пролиферацию и функцию Т и В-лимфоцитов, эндотелиальных и эпителиальных клеток. -Вызывает апоптоз (перепонка между пальцами, молочная железа) - Секретируется определенными бластомерами, вызывая гаструляцию Гомодимеры, масса 25 к. Да. Секретируются в виде предшественника и активируются протеолизом
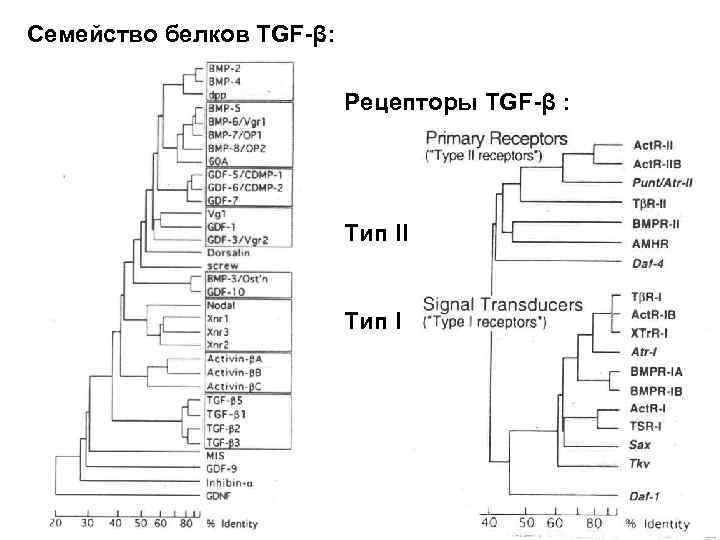
Семейство белков TGF-β: Рецепторы TGF-β : Тип II Тип I
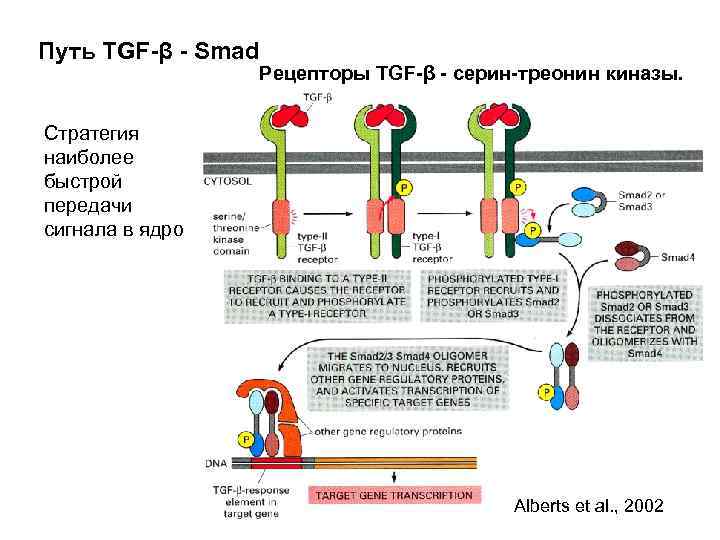
Путь TGF-β - Smad Рецепторы TGF-β - серин-треонин киназы. Стратегия наиболее быстрой передачи сигнала в ядро Alberts et al. , 2002
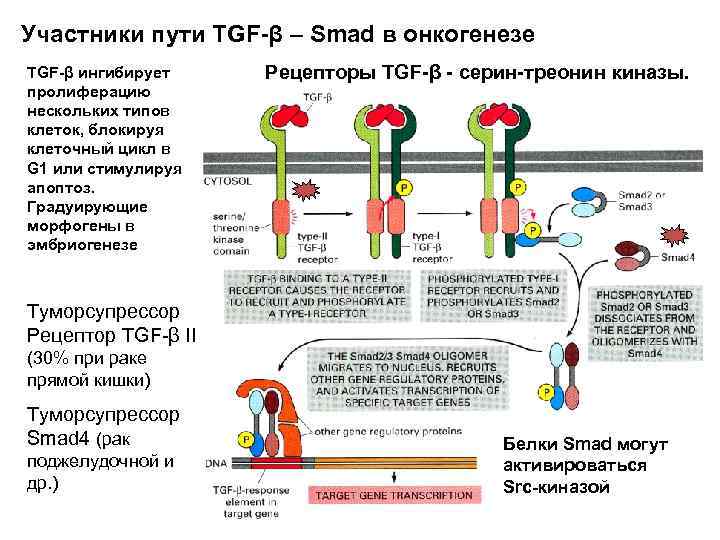
Участники пути TGF-β – Smad в онкогенезе TGF-β ингибирует пролиферацию нескольких типов клеток, блокируя клеточный цикл в G 1 или стимулируя апоптоз. Градуирующие морфогены в эмбриогенезе Рецепторы TGF-β - серин-треонин киназы. Туморсупрессор Рецептор TGF-β II (30% при раке прямой кишки) Туморсупрессор Smad 4 (рак поджелудочной и др. ) Белки Smad могут активироваться Src-киназой
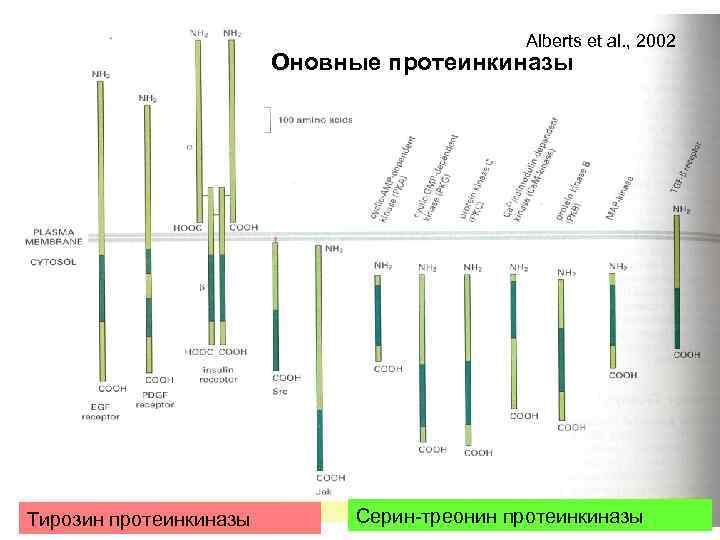
Alberts et al. , 2002 Оновные протеинкиназы Тирозин протеинкиназы Серин-треонин протеинкиназы
Короткий курс генетики КЦ 16.ppt