ГЕНЕТИКА БАКТЕРИЙ Конъюгация


ГЕНЕТИКА БАКТЕРИЙ

Конъюгация Передача генетического материала в виде плазмиды от клетки- донора к клетке- реципиенту при непосредственном контакте клеток через половые ворсинки (пили)

Опыт E. L. Tatum, J. Ledenberg (1946) E. coli До рекомбинации Ауксотроф-1 Ауксотроф-2 биот(+), трион(+), биот(-) трион(-) мет(-), лей(-) мет(+) лей(+) После рекомбинации прототроф биот(+), трион(+), мет(+), лей(+)

F-фактор – фактор фертильности (от англ. fertility – плодовитость) • Конъюгации подвержено 0, 001% бактерий • Участвовать в конъюгации в качестве клетки-донора способны F+ бактерии • Небольшой фрагмент ДНК • Свободно лежит в цитоплазме

F-фактор – фактор фертильности (от англ. fertility – плодовитость) • Автономен • Обладает свойствами репликона • Размножается в процессе деления • Кодирует образование половых ворсинок (пилей) • Кодирует другую информацию (капсула, спора, ферменты)

Hfr-фактор – фактор высокой частоты рекомбинаций (от англ. high frequency of recombination) • Конъюгации подвержено 40 -60% бактерий • Интегрирован в ДНК клетки (является эписомой) • Всегда находится в одной и той же точке цепи ДНК • Во время конъюгации выполняет роль тягача, перетягивая за собой ДНК клетки-донора в клетку-реципиента

Этапы конъюгации • Образование ЦПМ мостика • Перенос ДНК клетки-донора с помощью F-фактора или Hfr- фактора • Интеграция ДНК клетки-донора в клетку-реципиента

Варианты интеграции ДНК клетки- донора в клетку-реципиента • Интеграция ДНК клетки-донора и ДНК клетки-реципиента • Образование плазмиды без интеграции • Интеграция плазмиды в геном клетки-реципиента

Трансдукция • Перенос генетического материала от клетки-донора к клетке-реципиенту с помощью умеренного бактериофага

Этапы трансдукции • Расщепление ДНК клетки-донора при размножении в ней умеренного бактериофага • Включение ДНК клетки-донора в ДНК бактериофага • Перенос ДНК клетки-донора и ДНК бактериофага в клетку-реципиента • Интеграция ДНК клетки-донора и ДНК бактериофага в ДНК клетки-реципиента

Типы трансдукции • Неспецифическая – вызывается умеренным бактериофагом без постоянной точки фиксации в бактериальной ДНК, при этом возможен перенос любого участка ДНК • Специфическая – вызывается умеренным бактериофагом с постоянной точкой фиксации в ДНК бактерии • Абортивная – вызывается умеренным бактериофагом, не обладающим свойствами репликона, переходит только в одну дочернюю клетку
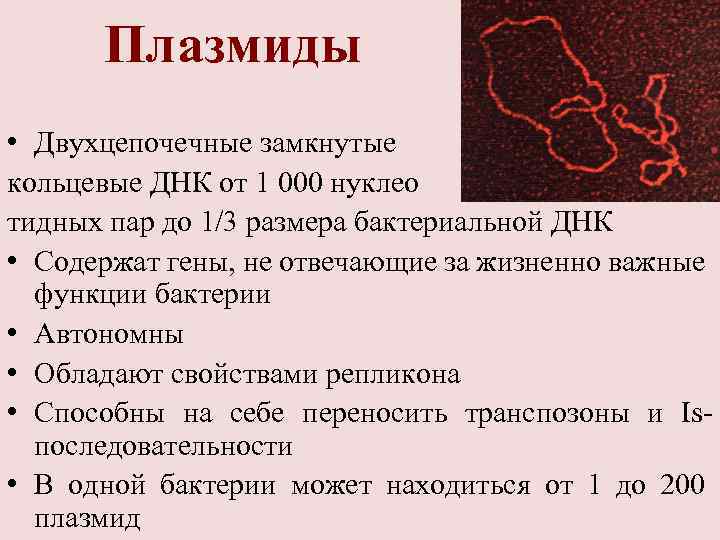
Плазмиды • Двухцепочечные замкнутые кольцевые ДНК от 1 000 нуклео тидных пар до 1/3 размера бактериальной ДНК • Содержат гены, не отвечающие за жизненно важные функции бактерии • Автономны • Обладают свойствами репликона • Способны на себе переносить транспозоны и Is- последовательности • В одной бактерии может находиться от 1 до 200 плазмид

Виды плазмид • Чистые – самостоятельные репликоны, автономные от ДНК • Эписомы – коинтегрированные репликоны, обратимо встраиваются в ДНК бактерий • Крупные – трансмиссивные (конъюгативные) • Мелкие – мобилизуемые, способны к передаче информации в присутствии крупных трансмиссивных плазмид, используя их аппарат конъюгации • Криптические – молчащие

Разновидности плазмид • R-плазмиды – антибиотикоустойчивость (синтез β- лактамаз) • F-фактор – чистая плазмида (образование половых пилей) • Hfr-фактор – эписома (образование половых пилей) • Расщепляющие плазмиды – информация о синтезе ферментов деградации (очистка окружающей среды) • Плазмиды бактериоциногенности – способность бактерий синтезировать антибиотикоподобные вещества (пептиды) • Плазмиды факторов патогенности – способность бактерий продуцировать факторов патогенности

Генная инженерия • Целенаправленное создание новых генетических конструкций, рекомбинантных молекул ДНК in vitro с последующим введением их в живую клетку • Создание новых организмов с новыми свойствами

Cоздание рекомбинантных молекул ДНК • Выделение нужных генов • Создание вектора трансплантации фрагмента ДНК в клетку • Селекция клеток, несущих рекомбинантную ДНК

Рекомбинантные (генноинжененрные) препараты Более 500 • Гормоны (инсулин) • Интерлейкины (интерферон) • Тканевой активатор плазминогена • Вакцины (вакцина против гепатита В)

Области применения генной инженерии • Создание рекомбинантных молекул ДНК • Рашифровка генетической карты (паспорта) человека • Использование генотерапии (β- талассемия) • Разработка биологического оружия • Применение в диагностике для обнаружения в исследуемом материале специфических фрагментов ДНК

Метод молекулярных зондов (молекулярной гибридизации) • Исследуемый материал нагревается до 95° • ДНК расплетается • Обнаруживается специфический фрагмент ДНК с помощью комплиментарной копии этого участка с меткой (ДНК-зонд) • Недостаток метода – невысокая чувствительность

Полимеразная цепная реакция (ПЦР) Компоненты и оборудование • Исследуемый материал • Праймеры – небольшие фрагменты ДНК, комплиментарные специфическим генам возбудителя • Полинуклеотиды • ДНК-полимераза (Taq-полимераза) • Термоциклер

Полимеразная цепная реакция (ПЦР) Этапы • Нагревание реакционной смеси до 95°для денатурации ДНК • Отжиг (охлаждение) до 40 -60°, праймеры встраиваются в ДНК • Удвоение ДНК под действием ДНК-полимеразы (Taq -полимеразы) • Процесс повторяется 25 -40 раз для десяти- и более кратного увеличения генетического материала (амплификации) • Идентификация генетического материала с помощью электрофореза в геле или флюоресценции в режиме реального времени

ПЦР-диагностика • Гепатиты • Герпетическая инфекция • Инфекции, передающиеся половым путем • Вирус папилломы человека • Туберкулез и др.

Особое значение ПЦР-диагностики • Хронические инфекции • Идентификация внутриклеточных (хламидии, риккетсии) и мембранных (микоплазмы, уреаплазмы) паразитов • Выявление возбудителей сапронозных инфекций (легионеллезы, актиномикозы, псевдотуберкулез, иерсиниоз и др. ) • Обнаружение трудно культивируемых (хламидии) и медленно растущих (микобактерии) микроорганизмов • Маркировка возбудителей по эпидемиологическим показаниям

