Лекция 10.ppt
- Количество слайдов: 64

Генетические методы диагностики инфекционных заболеваний доцент, к. м. н. Самоукина А. М. Кафедра микробиологии и вирусологии с курсом иммунологии ГБОУ ВПО Тверская ГМА Минздравсоцразвития России

Методы диагностики инфекционных заболеваний n Прямые n Косвенные 1. Микроскопический метод Бактериологический метод Выявление антигенов микроорганизма Выявление РНК/ДНК микроорганизма 1. Серологический метод Инструментальный анализ (морфологические изменения) Гистология 2. 3. 4. 2. 3.

Микроскопический метод Достоинства: - Быстр и прост в выполнении, не требует наличия дорогостоящего оборудования n Недостатки: - Ультрамикроскопические размеры (вирусы, микоплазмы) - Морфологическое сходство ряда микроорганизмов - Субъективизм - Сложность стандартизации и автоматизации n

Бактериологический метод n 1. 2. Достоинства: Возможность изучения целого ряда клинически важных фенотипических свойств микроорганизмов. При условии эффективности выделения – наилучшее соответствие причинной обусловленности ассоциации.

Бактериологический метод n 1. 2. 3. Недостатки: «Некультивируемость» микроорганизма Длительность анализа Опасность

Бактериологический метод n 1. 2. 3. 4. 5. «Некультивируемость» микроорганизма Отсутствие адекватных сред или невозможность подобрать условия культивирования для определенных микроорганизмов Неправильный забор клинического материала Несоблюдение условий доставки проб в лабораторию Высев из клинического материала микроорганизма, ингибирующего рост этиологического агента Прием пациентами антибиотиков перед проведением бактериологического анализа

Иммунологический подход Направления: 1. Выявление антител (серология): Ig G, Ig M, Ig A, авидность 2. Выявление антигенов микроорганизма 3. Выявление специфического клеточного ответа n

Иммунологический подход n 1. 2. 3. 4. 5. Достоинства: Быстрота анализа Низкая стоимость Возможность стандартизации и автоматизации Высокая воспроизводимость результатов анализа Высокая пропускная способность

Иммунологический подход n 1. 2. 3. Недостатки: Непредсказуемая специфичность, необходимость в подтверждающих тестах Низкая аналитическая чувствительность, особенно актуально для прямых методов Для косвенных методов характерно несоответствие принципам причинной обусловленности ассоциации (состояние макроорганизма)

Причины обнаружения антител класса Ig M 1. 2. 3. 4. 5. 6. 7. Острая инфекция Реактивация инфекции Затухающая инфекция (антитела класса Ig M могут циркулировать до 1 -3 лет) Антигенный контакт без развития инфекции Локальная инфекция Перекрестно-реагирующие антитела Артефактный результат анализа

Молекулярная диагностика (син. молекулярно-биологическая диагностика) раздел диагностики in vitro, включающий все специфические методы, направленные на анализ нерегулярных биополимеров – ДНК, РНК и белков.

Разделы молекулярной диагностики n Молекулярногенетический анализ ДНК и РНК генотипический подход n Протеомный анализ (белки)

Генотипический подход к идентификации микроорганизмов n - Достоинства: Соответствует принципам причинной обусловленности ассоциации Возможность получения результатов независимо от «культивируемости» микроорганизмов Математически возможная чувствительность Высокая информативность и точность генетических маркеров Возможность стандартизации и автоматизации Возможность проведения строгих количественных измерений Низкая стоимость анализа

Генотипический подход к идентификации микроорганизмов n - Недостатки: Сложная связь важных в клинике фенотипических признаков и генотипических маркеров Неэффективность подхода при выявлении микроорганизмов, для которых характерно их отсутствие (исчезающе низкое содержание) в биологических жидкостях

Строение нуклеиновых кислот Нуклеиновые кислоты ДНК (дезоксирибонуклеиновая кислота) – содержит генетическую информацию РНК (рибонуклеиновая кислота) – участвует в синтезе белка Нуклеотиды – мономеры, из которых состоят нуклеиновые кислоты n

ДНК-структура n n Генетический материал в человеческой клетке представлен двойной цепью ДНК, содержащей около 3 млрд. пар оснований Длина нити ДНК в вытянутом состоянии составляет около 2 м – в свернутом диаметр составляет тысячную миллиметра Две нити ДНК формируют двойную спираль. Эта двойная спираль свернута таким образом, чтобы она могла разместиться внутри клетки.

Строение нуклеотидов n n Каждый нуклеотид состоит из фосфатной группы, пятиуглеродного сахара (пентозы) и азотсодержащего основания. Когда нуклеотиды полимеризуются фосфатная группа одного нуклеотида связывается с сахаром другого нуклеотида, а последний в свою очередь, ковалентно связан с молекулой азотистого основания. Нуклеотиды - присоединяются друг к другу таким образом, что фосфатная группа одного присоединяется к сахару другого и образуют сахарофосфатный остов молекулы. Азотистые основания располагаются по одну сторону от него.
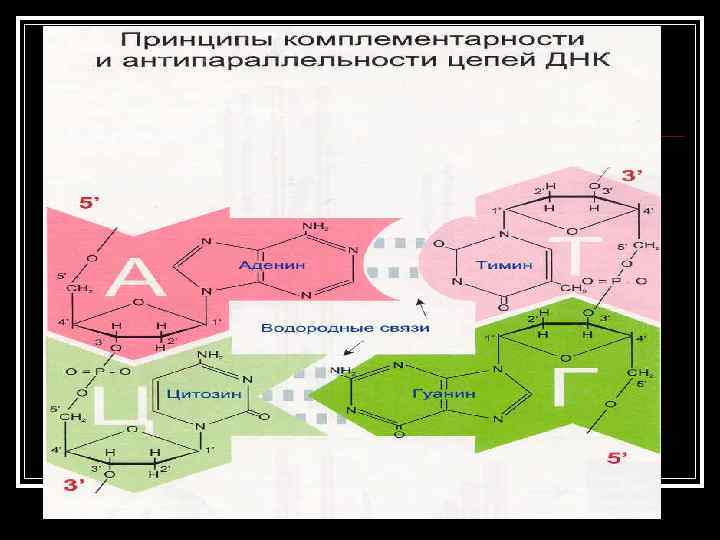

Образование двухцепочечной ДНК происходит по принципу комплементарности n n Комплементарность – последовательность нуклеотидов в одной цепи автоматически определяет строго соответствующую ей последовательность нуклеотидов в комплементарной ей цепи. Так азотистое основание Аденин (А) всегда взаимодействует только с комплементарным ему азотистым основанием Тимин (Т) в молекулах ДНК Комплементарность оснований обеспечивается системой водородных связей.
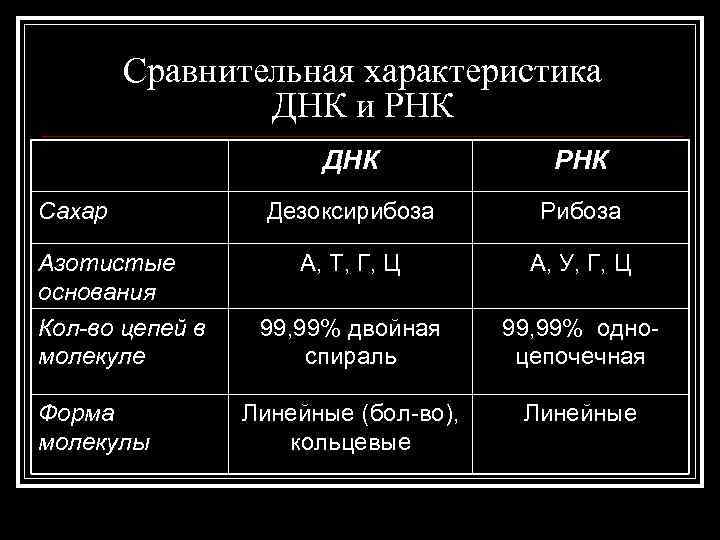
Сравнительная характеристика ДНК и РНК ДНК Сахар Азотистые основания Кол-во цепей в молекуле Форма молекулы РНК Дезоксирибоза Рибоза А, Т, Г, Ц А, У, Г, Ц 99, 99% двойная спираль 99, 99% одноцепочечная Линейные (бол-во), кольцевые Линейные

Центральная догма молекулярной биологии Генетическая информация сначала переводится на язык рибонуклеотидов (ДНК транскрибируется в РНК), а затем аминокислот (РНК транслируется в белки). n Гены – это только те сегменты ДНК, которые кодируют белки. n

Репликация ДНК в клетке – прообраз полимеразной цепной реакции n n Полимеразная цепная реакция (ПЦР) – молекулярно-биологическая реакция, направленная на синтез большого количества копий специфического фрагмента ДНК in vitro. ПЦР представляет собой многократное увеличение числа копий (амплификация) специфического участка ДНК катализируемое ферментом ДНК- полимеразой.

Изобретение ПЦР n n n Принцип ПЦР сформулировал Гобинд Корана в 1971 г. В 1983 г. Кэри Мюллису удалось провести ПЦР В 1993 г. за изобретение ПЦР Кэри Мюллису вручена Нобелевская премия по химии

Естественная репликация ДНК включает в себя несколько стадий: n n n 1) Денатурация ДНК (расплетение двойной спирали, расхождение нитей ДНК); 2) Образование коротких двухцепочечных участков ДНК (затравок, необходимых для инициации синтеза ДНК); 3) Синтез новой цепи ДНК (комплементарное достраивание обеих нитей)

ПЦР диагностика инфекционных заболеваний n Данный процесс используется для получения копий коротких участков ДНК, специфичных для конкретных микроорганизмов, т. е. осуществляется целенаправленный поиск специфических участков, что и является целью молекулярно-генетической диагностики инфекционных заболеваний.
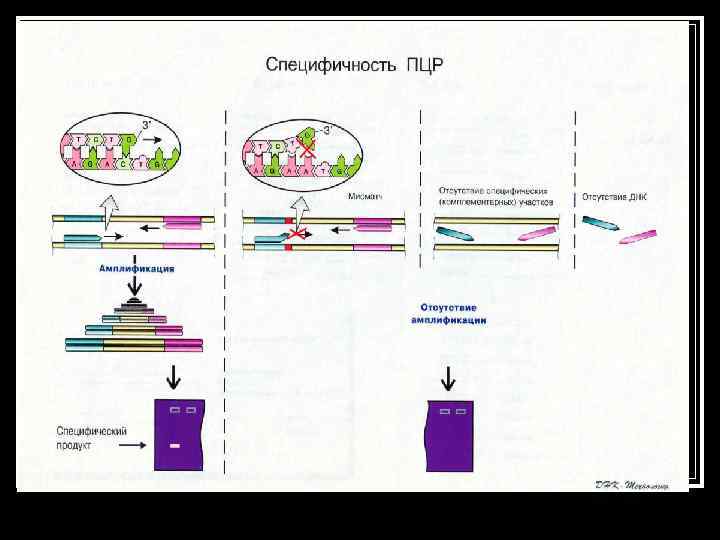

ПЦР диагностика инфекционных заболеваний n Открытие термостабильной ДНКполимеразы (Taq-полимеразы) из термофильных бактерий Thermis aquaticus , оптимум работы которой находится в области 70 -72°С, позволило сделать процесс репликации ДНК циклическим и использовать его для работы in vitro.

ПЦР диагностика инфекционных заболеваний n При многократном повторении циклов синтеза происходит экспоненциальное увеличение числа копий специфического фрагмента ДНК, что позволяет из небольшого количества анализируемого материала, который может содержать единичные клетки микроорганизмов получить достаточное количество ДНК копий для идентификации их методом электрофореза.

ПЦР диагностика инфекционных заболеваний n Для создания стартовых блоков в заданных участках ДНК используют две олигонуклеотидные затравки (20 нуклеотидных пар), называемые праймерами. Праймеры комплементарны последовательностям ДНК на левой и правой границах специфического фрагмента и ориентированы таким образом, что достраивание новой цепи ДНК протекает только между ними.
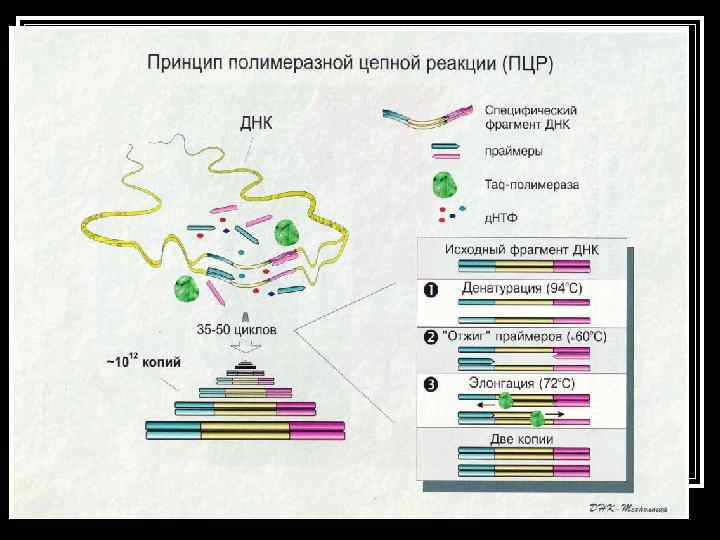

Основные компоненты ПЦР n n n ДНК-матрица (ДНК или ее часть, содержащая искомый специфический фрагмент); Праймеры Смесь дезоксинуклеотидтрифосфатов (д. НТФ) Фермент Taq-полимераза Буферный раствор (реакционная среда, содержащая ионы Mg 2+, необходимые для поддержания активности фермента).

Основные компоненты ПЦР n Праймеры (синтетические олигонуклеотиды (20 -30 нуклеотидных пар), комплементарные последовательностям ДНК на границах определяемого специфического фрагмента). Выбор специфического фрагмента и подбор праймеров играет важнейшую роль в специфичности проведения амплификации, что сказывается на качестве проведения анализа.

Основные компоненты ПЦР n Смесь дезоксинуклеотидтрифосфатов (д. НТФ) (смесь четырех д. НТФ, являющихся материалом для синтеза новых комплементарных цепей ДНК).

Основные компоненты ПЦР n Фермент Taq-полимераза (термостабильная ДНК-полимераза, катализирующая удлинение цепей праймеров путем последовательного присоединения нуклеотидных оснований к растущей цепи синтезируемой ДНК).

Основные компоненты ПЦР n Буферный раствор (реакционная среда, содержащая ионы Mg 2+, необходимые для поддержания активности фермента).

Основные компоненты ПЦР n Для определения специфических участков генома РНК-содержащих вирусов, сначала получают ДНК-копию с РНК-матрицы, используя реакцию обратной транскрипции (RT), катализируемую ферментом ревертазой (обратной транскриптазой).
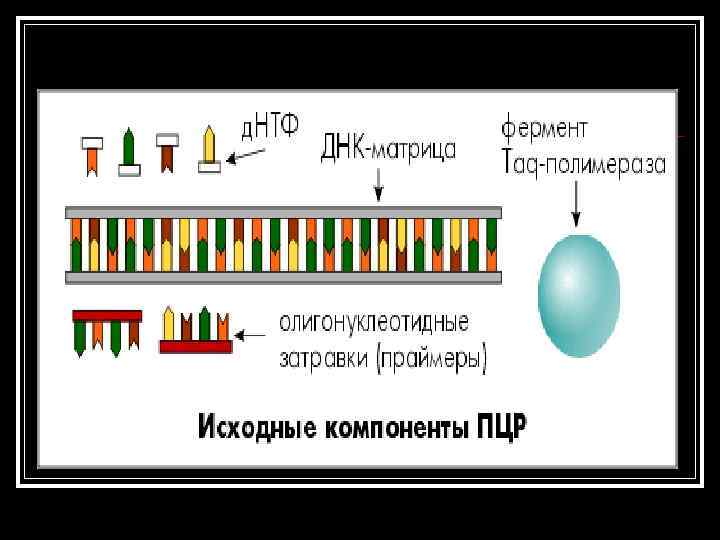

n Для получения достаточного количества копий искомого характеристического фрагмента ДНК амплификация включает несколько (20 -40) циклов.

Этапы амплификации 1 этап: Денатурация ДНК n 2 этап: Присоединение праймеров (отжиг). n 3 этап: Достраивание цепей ДНК n

Этапы амплификации 1 этап: Денатурация ДНК (расплетение двойной спирали) Протекает при 93 -95°С течение 30 -40 сек. n 2 этап: Присоединение праймеров (отжиг). Присоединение праймеров происходит комплементарно к соответствующим последовательностям на противоположных цепях ДНК на границах специфического участка. Для каждой пары праймеров существует своя температура отжига, значения которой располагаются в интервале 50 -65°С. Время отжига - 20 -60 сек. n

Этапы амплификации n 3 этап: Достраивание цепей ДНК Комплементарное достраивание цепей ДНК происходит от 5’-конца к 3’-концу цепи в противоположных направлениях, начиная с участков присоединения праймеров. Материалом для синтеза новых цепей ДНК служат добавляемые в раствор дезоксирибонуклеотидтрифосфаты (д. НТФ). Процесс синтеза катализируется ферментом термостабильной ДНК-полимеразой (Taqполимеразой) и проходит при температуре 7072°С. Время протекания синтеза - 20 -40 сек.
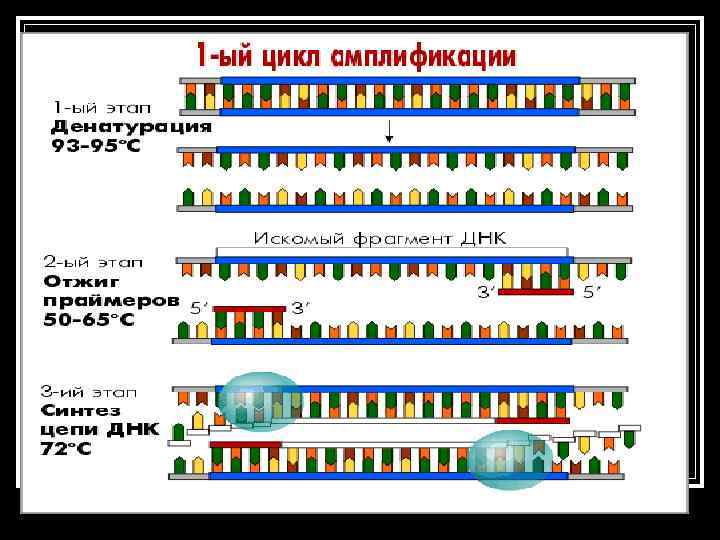

Этапы ПЦР n Образовавшиеся в первом цикле амплификации новые цепи ДНК служат матрицами для второго цикла амплификации, в котором происходит образование искомого специфического фрагмента ДНК (ампликона). В последующих циклах амплификации ампликоны служат матрицей для синтеза новых цепей. Таким образом, происходит накопление ампликонов в растворе по формуле 2 n, где n-число циклов амлификации. Этого количества достаточно для достоверной визуальной детекции этого фрагмента методом электрофореза в агарозном геле.


Этапы ПЦР n Процесс амплификации проводится в специальном программируемом термостате (амплификаторе), который по заданной программе автоматически осуществляет смену температур согласно числу циклов амплификации

Методика проведения анализа с использованием метода ПЦР включает три этапа: 1. Выделение ДНК (РНК) из клинического образца n 2. Амплификация специфических фрагментов ДНК n 3. Детекция продуктов амплификации n
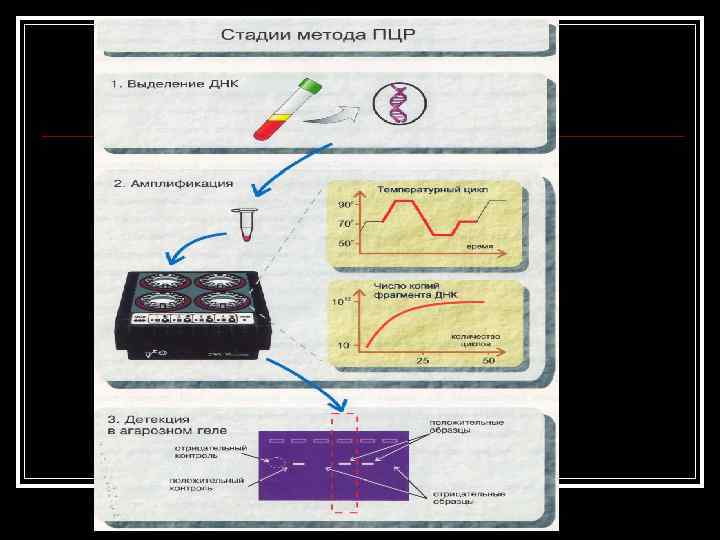

Выделение ДНК (РНК) n На данной стадии проведения анализа клиническая проба подвергается специальной обработке, в результате которой происходит лизис клеточного материала, удаление белковых и полисахаридных фракций, и получение раствора ДНК или РНК, свободной от ингибиторов и готовой для дальнейшей амплификации. Выбор методики выделения ДНК (РНК) в основном определяется характером обрабатываемого клинического материала.

Амплификация специфических фрагментов ДНК n На данной стадии происходит накопление коротких специфических фрагментов ДНК в количестве, необходимом для их дальнейшей детекции. В большинстве методик определения специфических фрагментов генома используется т. н. “классический вариант направленной ПЦР. Для повышения специфичности и чувствительности анализа в некоторых методиках используется метод “гнездной” (nested) ПЦР, в котором используются 2 пары праймеров (“внешние” - для 1 стадии, и “внутренние” - для 2 -ой стадии).

Детекция продуктов амплификации n В большинстве методик на данном этапе проводится разделение смеси продуктов амплификации, полученной на 2 -ой стадии, методом горизонтального электрофореза в агарозном геле. До проведения электрофоретического разделения, к амплификационной смеси добавляется раствор бромистого этидия, образующий с двухцепочечными фрагментами ДНК прочные соединения внедрения. Эти соединения под действием УФ-облучения способны флуоресцировать, что регистрируется в виде оранжево-красных светящихся полос после электрофоретического разделения амплификационной смеси в агарозном геле.

Преимущества ПЦР для диагностики инфекционных заболеваний n Прямое определение наличия возбудителей Многие традиционные методы диагностики, например иммуноферментный анализ, выявляют белки-маркеры, являющиеся продуктами жизнедеятельности инфекционных агентов, что дает лишь опосредованное свидетельство наличия инфекции. Выявление специфического участка ДНК возбудителя методом ПЦР дает прямое указание на присутствие возбудителя инфекции.

Преимущества ПЦР для диагностики инфекционных заболеваний n Высокая специфичность метода ПЦР обусловлена тем, что в исследуемом материале выявляется уникальный, характерный только для данного возбудителя фрагмент ДНК. Специфичность задается нуклеотидной последовательностью праймеров, что исключает возможность получения ложных результатов, в отличие от метода иммуноферментного анализа, где нередки ошибки в связи с перекрестно-реагирующими антигенами.

Преимущества ПЦР для диагностики инфекционных заболеваний n Высокая чувствительность Метод ПЦР позволяет выявлять даже единичные клетки бактерий или вирусов. ПЦР-диагностика обнаруживает наличие возбудителей инфекционных заболеваний в тех случаях, когда другими методами (иммунологическими, бактериологическими, микроскопическими) это сделать невозможно. Чувствительность ПЦР-анализа составляет 10 -1000 клеток в пробе (чувствительность иммунологических и микроскопических тестов – 103 -105 клеток).

Преимущества ПЦР для диагностики инфекционных заболеваний n Универсальность процедуры выявления различных возбудителей Материалом для исследования методом ПЦР служит ДНК возбудителя. Метод основан на выявлении фрагмента ДНК или РНК, являющегося специфичным для конкретного организма. Сходство химического состава всех нуклеиновых кислот позволяет применять унифицированные методы проведения лабораторных исследований. Это дает возможность диагностировать несколько возбудителей из одной биопробы. В качестве исследуемого материала могут использоваться различные биологические выделения (слизь, моча, мокрота), соскобы эпителиальных клеток, кровь, сыворотка.

Преимущества ПЦР для диагностики инфекционных заболеваний n Высокая скорость получения результата анализа Для проведения ПЦР-анализа не требуется выделение и выращивание культуры возбудителя, что занимает большое количество времени. Унифицированный метод обработки биоматериала и детекции продуктов реакции, и автоматизация процесса амплификации дают возможность провести полный анализ за 4 -4. 5 часа.

Преимущества ПЦР для диагностики инфекционных заболеваний n Возможность диагностики не только острых, но и латентных инфекций Особенно эффективен метод ПЦР для диагностики инфекций, вызванных трудно культивируемыми, некультивируемыми микроорганизмами, с которыми часто приходится сталкиваться при латентных и хронических инфекциях, поскольку этот метод позволяет избежать сложностей при культивировании в лабораторных условиях. Применение ПЦР-диагностики также очень эффективно в отношении возбудителей с высокой антигенной изменчивостью и внутриклеточных паразитов.

Области применения ПЦР Диагностика инфекционных заболеваний n Генотипирование n Выявление трансгенов n Диагностика наследственной патологии n
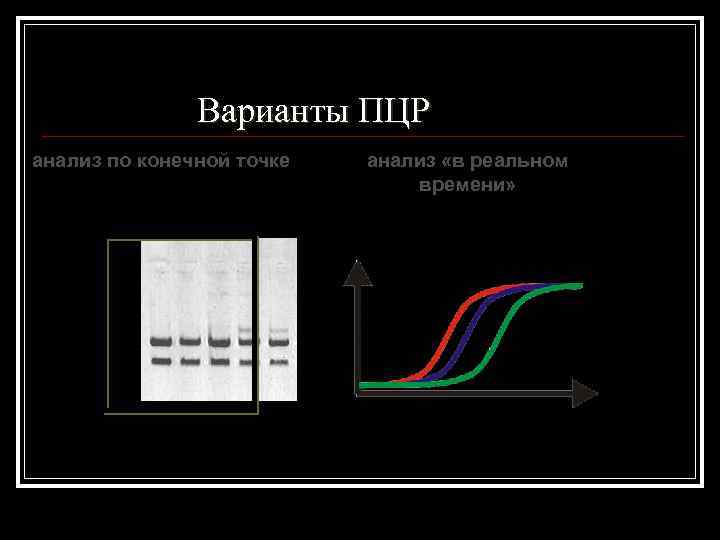
Варианты ПЦР анализ по конечной точке анализ «в реальном времени»

Что такое ПЦР «в реальном времени» ? 1. «Real-time» ПЦР (широкое понятие) – ПЦР с регистрацией накопления ДНК во время амплификации (синонимы: Real. Time PCR, «флуоресцентная» ПЦР ). 2. «Real-time» ПЦР (узкое понятие) – модификации ПЦР, в которых измерение флуоресценции непосредственно во время реакции используется для количественного анализа (синонимы: quantitative PCR (q. PCR), kinetic PCR).

Особенности: n n n Позволяет проводить количественный анализ (ДНК, к. ДНК, РНК) Повышает достоверность исследования за счет использования олигонуклеотидных зондов Уменьшает риск контаминации продуктами ПЦР Снижает требования к организации лаборатории Сокращает время исследования Упрощает ведение документации и трактовку результатов исследования

Гибридизация нуклеиновых кислот n Принцип метода обусловлен способностью ДНК специфически гибридизировать (соединяться) с комплементарными фрагментами искусственно созданных нитей ДНК, меченных изотопами или ферментами.

Гибридизация нуклеиновых кислот n Метод основан на способности двухцепочечной ДНК при повышенной температуре (90°С) денатурировать, т. е. расплетаться на две нити, а при понижении температуры на 10°С вновь восстанавливать исходную структуру.

Гибридизация нуклеиновых кислот n Метод требует наличия молекулярного зонда (одноцепочечной молекулы нуклеиновый кислоты, меченной радиоизотопом или ферментом) с которой сравнивают исследуемую ДНК.

Гибридизация нуклеиновых кислот n Для проведения МГ исследуемую ДНК расплетают указанным способом, одну нить фиксируют на специальном фильтре, который затем помещают в раствор, содержащий зонды. Создаются условия, благоприятные для образования двойной спирали. В случае комплементарности между зондом и исследуемой ДНК, они образуют между собой двойную спираль.
Лекция 10.ppt