Гемостаз.pptx
- Количество слайдов: 107
 ГЕМОСТАЗ ЭТО ФИЗИОЛОГИЧЕСКАЯ РЕАКЦИЯ ОРГАНИЗМА, НАПРАВЛЕННАЯ НА ПОДДЕРЖАНИЕ ЖИДКОГО СОСТОЯНИЯ КРОВИ, А ТАКЖЕ НА ПРЕДОТВРАЩЕНИЕ И ОСТАНОВКУ КРОВОТЕЧЕНИЯ ПРИ НАРУШЕНИИ ЦЕЛОСТНОСТИ СОСУДИСТОЙ СТЕНКИ.
ГЕМОСТАЗ ЭТО ФИЗИОЛОГИЧЕСКАЯ РЕАКЦИЯ ОРГАНИЗМА, НАПРАВЛЕННАЯ НА ПОДДЕРЖАНИЕ ЖИДКОГО СОСТОЯНИЯ КРОВИ, А ТАКЖЕ НА ПРЕДОТВРАЩЕНИЕ И ОСТАНОВКУ КРОВОТЕЧЕНИЯ ПРИ НАРУШЕНИИ ЦЕЛОСТНОСТИ СОСУДИСТОЙ СТЕНКИ.
 РЕГУЛЯЦИЯ СИСТЕМЫ ГЕМОСТАЗА. 1. Молекулярный уровень – предполагает поддержание гомеостатического баланса отдельных факторов, влияющих на сосудисто тромбоцитарный гемостаз, свертывание крови и фибринолиз. 2. Клеточный уровень регуляции – осуществляется по типу обратной афферентации путём взаимодействия активированных факторов и продуктов их распада со специфическими клеточными рецепторами. 3. Органный уровень регуляции – обеспечивает оптимальные условия функционирования системы гемостаза в различных участках сосудистого русла. Благодаря этому уровню проявляется мозаичность сосудисто тромбоцитарного гемостаза, свертывания крови и фибринолиза. 4. Нервно-гуморальная регуляция – контролирует состояние системы гемостаза от молекулярного до органного уровня, обеспечивая целостность реакции на уровне организма, главным образом, через симпатический и парасимпатический отделы вегетативной нервной системы, а также гормоны и различные биологически активные соединения.
РЕГУЛЯЦИЯ СИСТЕМЫ ГЕМОСТАЗА. 1. Молекулярный уровень – предполагает поддержание гомеостатического баланса отдельных факторов, влияющих на сосудисто тромбоцитарный гемостаз, свертывание крови и фибринолиз. 2. Клеточный уровень регуляции – осуществляется по типу обратной афферентации путём взаимодействия активированных факторов и продуктов их распада со специфическими клеточными рецепторами. 3. Органный уровень регуляции – обеспечивает оптимальные условия функционирования системы гемостаза в различных участках сосудистого русла. Благодаря этому уровню проявляется мозаичность сосудисто тромбоцитарного гемостаза, свертывания крови и фибринолиза. 4. Нервно-гуморальная регуляция – контролирует состояние системы гемостаза от молекулярного до органного уровня, обеспечивая целостность реакции на уровне организма, главным образом, через симпатический и парасимпатический отделы вегетативной нервной системы, а также гормоны и различные биологически активные соединения.
 ЛЁГКИЕ И ИХ РОЛЬ В ГЕМОСТАЗЕ
ЛЁГКИЕ И ИХ РОЛЬ В ГЕМОСТАЗЕ
 • Среди многочисленный нересираторных функций лёгких важное место занимает регуляция гемостазиологического баланса между малым и большим кругами кровообращения. • Обнаруженная в лёгких в норме высокая плазминовая и низкая тромбопластиновая активность позволяет им выполнять роль мощного фактора, снижающего гемостатический потенциал крови, циркулирующей по малому кругу кровообращения. • Кроме того, лёгкие выступают в роли своеобразного фильтра для активированных тромбоцитов, поступающих из венозного русла.
• Среди многочисленный нересираторных функций лёгких важное место занимает регуляция гемостазиологического баланса между малым и большим кругами кровообращения. • Обнаруженная в лёгких в норме высокая плазминовая и низкая тромбопластиновая активность позволяет им выполнять роль мощного фактора, снижающего гемостатический потенциал крови, циркулирующей по малому кругу кровообращения. • Кроме того, лёгкие выступают в роли своеобразного фильтра для активированных тромбоцитов, поступающих из венозного русла.

 ОСНОВНЫЕ МЕХАНИЗМЫ СИСТЕМЫ РЕГУЛЯЦИИ АГРЕГАНТНОГО СОСТОЯНИЯ КРОВИ. 1. Механизмы гемостаза (их несколько) обеспечивают остановку кровотечения. 2. Механизмы антисвёртывания поддерживают жидкое состояние крови. 3. Механизмы фибринолиза обеспечивают растворение тромба (кровяного сгустка) и восстановление просвета сосуда (реканализацию).
ОСНОВНЫЕ МЕХАНИЗМЫ СИСТЕМЫ РЕГУЛЯЦИИ АГРЕГАНТНОГО СОСТОЯНИЯ КРОВИ. 1. Механизмы гемостаза (их несколько) обеспечивают остановку кровотечения. 2. Механизмы антисвёртывания поддерживают жидкое состояние крови. 3. Механизмы фибринолиза обеспечивают растворение тромба (кровяного сгустка) и восстановление просвета сосуда (реканализацию).
 МОРФОЛОГИЧЕСКИЕ КОМПОНЕНТЫ СИСТЕМЫ ГЕМОСТАЗА. 1. Сосудистая стенка. 2. Тромбоциты и другие клеточные элементы крови. 3. Плазменные компоненты – белки, пептиды и небелковые медиаторы гемостаза, цитокины, гормоны. 4. Костный мозг, печень, селезёнка.
МОРФОЛОГИЧЕСКИЕ КОМПОНЕНТЫ СИСТЕМЫ ГЕМОСТАЗА. 1. Сосудистая стенка. 2. Тромбоциты и другие клеточные элементы крови. 3. Плазменные компоненты – белки, пептиды и небелковые медиаторы гемостаза, цитокины, гормоны. 4. Костный мозг, печень, селезёнка.
 ФУНКЦИОНАЛЬНЫЕ КОМПОНЕНТЫ СИСТЕМЫ ГЕМОСТАЗА. 1. Прокоагулянты. 2. Антикоагулянты. 3. Профибринолитики. 4. Ингибиторы фибринолиза.
ФУНКЦИОНАЛЬНЫЕ КОМПОНЕНТЫ СИСТЕМЫ ГЕМОСТАЗА. 1. Прокоагулянты. 2. Антикоагулянты. 3. Профибринолитики. 4. Ингибиторы фибринолиза.
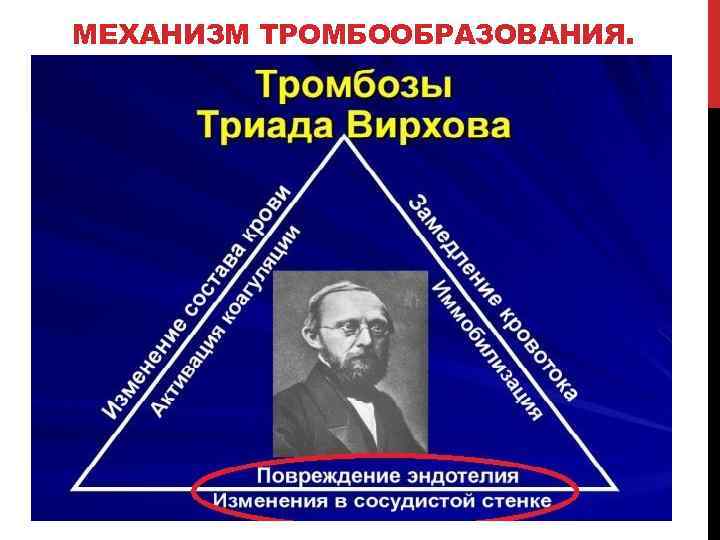 МЕХАНИЗМ ТРОМБООБРАЗОВАНИЯ.
МЕХАНИЗМ ТРОМБООБРАЗОВАНИЯ.
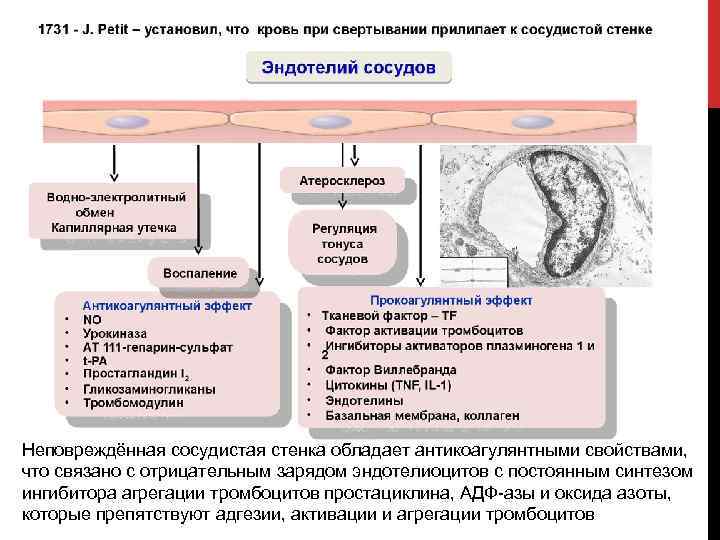 Неповреждённая сосудистая стенка обладает антикоагулянтными свойствами, что связано с отрицательным зарядом эндотелиоцитов с постоянным синтезом ингибитора агрегации тромбоцитов простациклина, АДФ азы и оксида азоты, которые препятствуют адгезии, активации и агрегации тромбоцитов
Неповреждённая сосудистая стенка обладает антикоагулянтными свойствами, что связано с отрицательным зарядом эндотелиоцитов с постоянным синтезом ингибитора агрегации тромбоцитов простациклина, АДФ азы и оксида азоты, которые препятствуют адгезии, активации и агрегации тромбоцитов
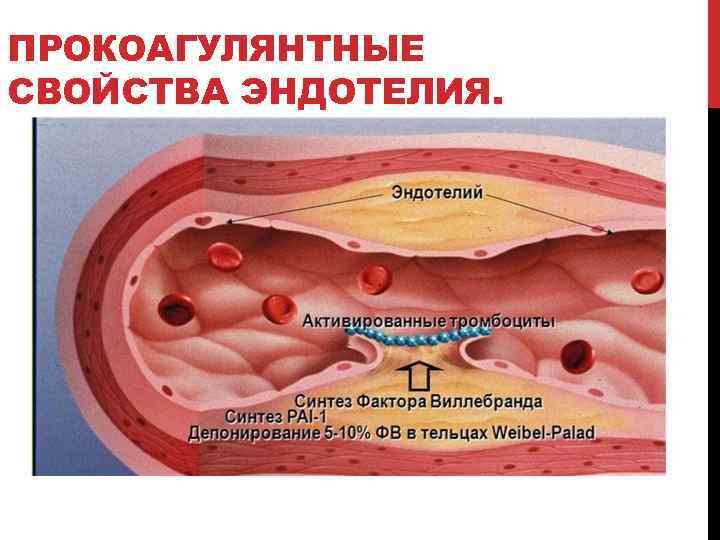 ПРОКОАГУЛЯНТНЫЕ СВОЙСТВА ЭНДОТЕЛИЯ.
ПРОКОАГУЛЯНТНЫЕ СВОЙСТВА ЭНДОТЕЛИЯ.
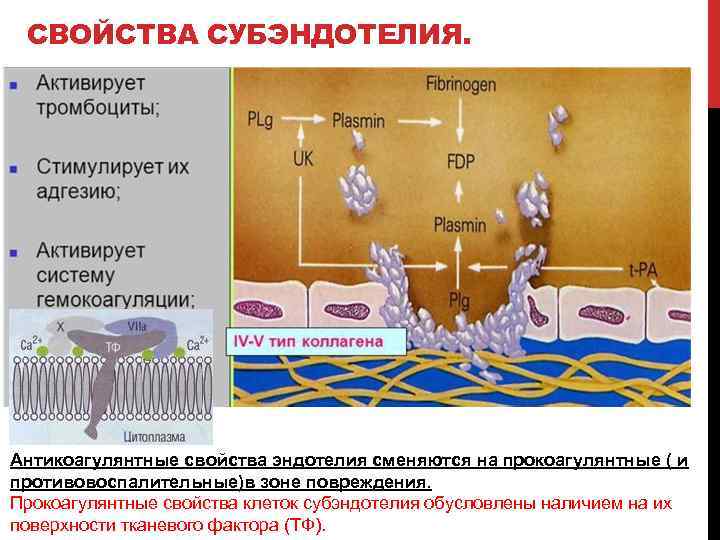 СВОЙСТВА СУБЭНДОТЕЛИЯ. Антикоагулянтные свойства эндотелия сменяются на прокоагулянтные ( и противовоспалительные)в зоне повреждения. Прокоагулянтные свойства клеток субэндотелия обусловлены наличием на их поверхности тканевого фактора (ТФ).
СВОЙСТВА СУБЭНДОТЕЛИЯ. Антикоагулянтные свойства эндотелия сменяются на прокоагулянтные ( и противовоспалительные)в зоне повреждения. Прокоагулянтные свойства клеток субэндотелия обусловлены наличием на их поверхности тканевого фактора (ТФ).
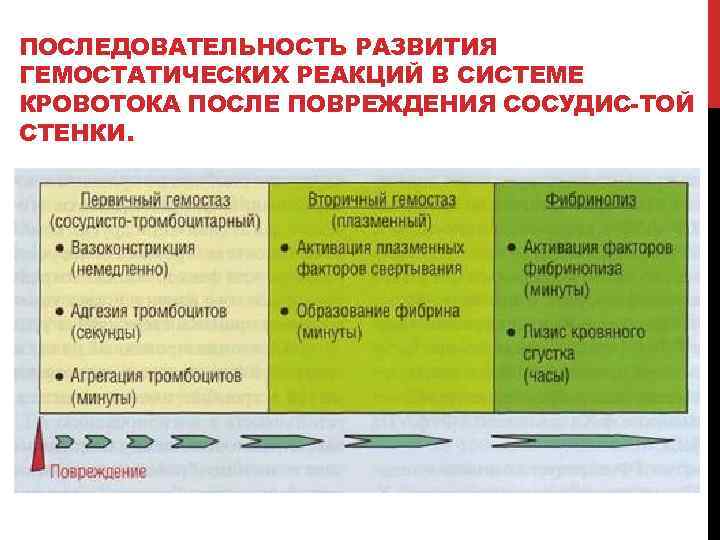 ПОСЛЕДОВАТЕЛЬНОСТЬ РАЗВИТИЯ ГЕМОСТАТИЧЕСКИХ РЕАКЦИЙ В СИСТЕМЕ КРОВОТОКА ПОСЛЕ ПОВРЕЖДЕНИЯ СОСУДИС ТОЙ СТЕНКИ.
ПОСЛЕДОВАТЕЛЬНОСТЬ РАЗВИТИЯ ГЕМОСТАТИЧЕСКИХ РЕАКЦИЙ В СИСТЕМЕ КРОВОТОКА ПОСЛЕ ПОВРЕЖДЕНИЯ СОСУДИС ТОЙ СТЕНКИ.
 СОСУДИСТО ТРОМБОЦИТАРНЫЙ ГЕМОСТАЗ. Состоит из: 1. Вазоконстрикции; 2. Формирования тромбоцитарного тромба Цель – начальная остановка кровотечения. Результат – образование тромбоцитарного тромба в месте повреждения сосуда.
СОСУДИСТО ТРОМБОЦИТАРНЫЙ ГЕМОСТАЗ. Состоит из: 1. Вазоконстрикции; 2. Формирования тромбоцитарного тромба Цель – начальная остановка кровотечения. Результат – образование тромбоцитарного тромба в месте повреждения сосуда.
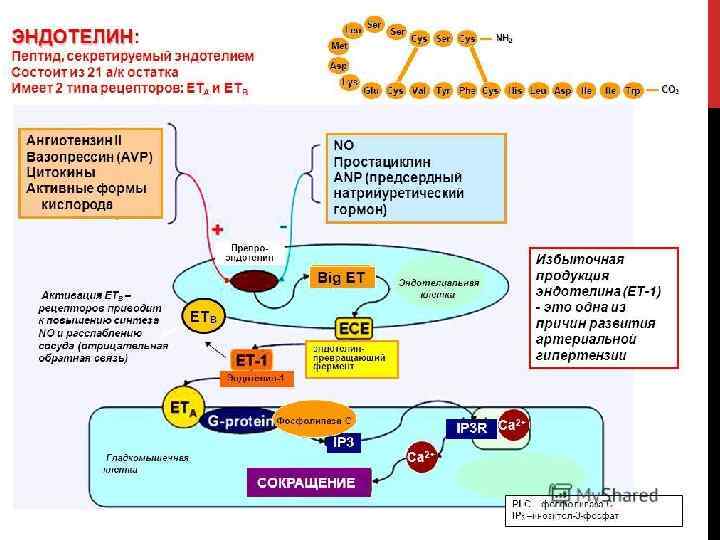
 ВАЗОКОНСТРИКЦИЯ В первый момент после повреждения сосуда развивается вазоконстрикция в мелких сосудах, имеющих мышечный слой. Ведущую роль в вазоконстрикции играет эндотелин-1. В первые минуты это прекращает кровотечение из капилляров, мелких вен и артериол, или, по крайней мере, значительно снижает кровопотерю. Спазм создаёт условия для более эффективного тромбоцитарного гемостаза.
ВАЗОКОНСТРИКЦИЯ В первый момент после повреждения сосуда развивается вазоконстрикция в мелких сосудах, имеющих мышечный слой. Ведущую роль в вазоконстрикции играет эндотелин-1. В первые минуты это прекращает кровотечение из капилляров, мелких вен и артериол, или, по крайней мере, значительно снижает кровопотерю. Спазм создаёт условия для более эффективного тромбоцитарного гемостаза.
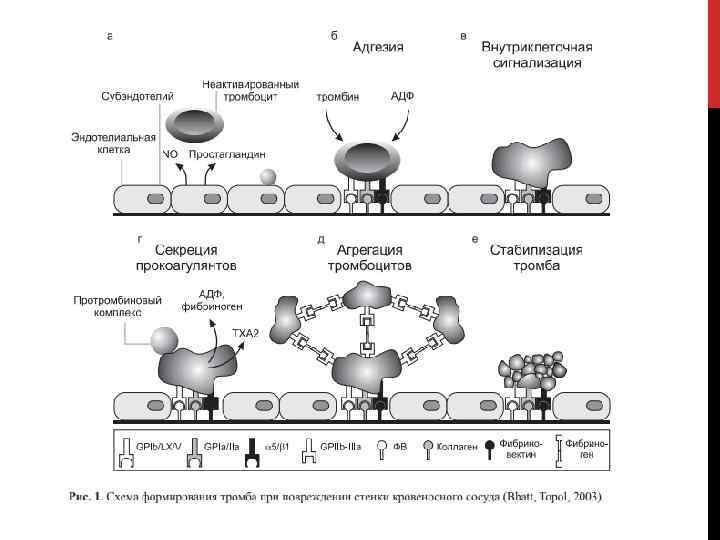
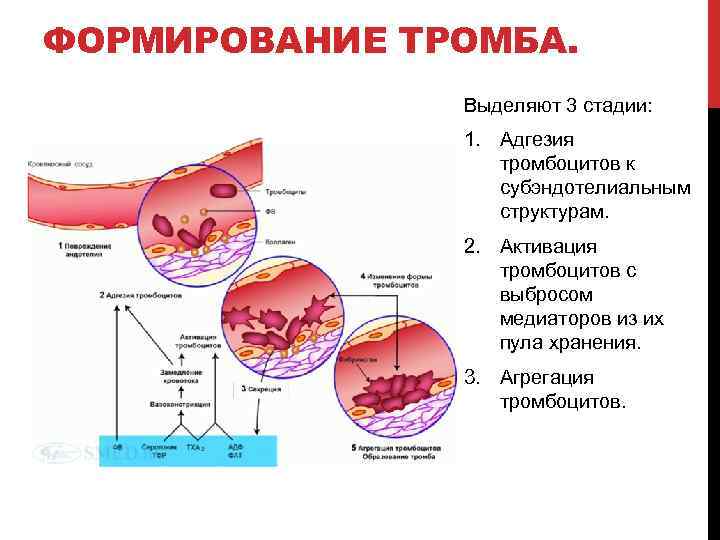 ФОРМИРОВАНИЕ ТРОМБА. Выделяют 3 стадии: 1. Адгезия тромбоцитов к субэндотелиальным структурам. 2. Активация тромбоцитов с выбросом медиаторов из их пула хранения. 3. Агрегация тромбоцитов.
ФОРМИРОВАНИЕ ТРОМБА. Выделяют 3 стадии: 1. Адгезия тромбоцитов к субэндотелиальным структурам. 2. Активация тромбоцитов с выбросом медиаторов из их пула хранения. 3. Агрегация тромбоцитов.
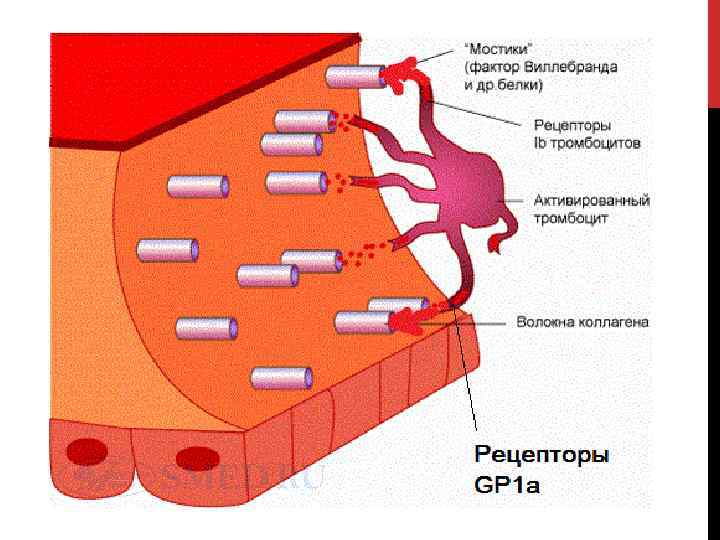
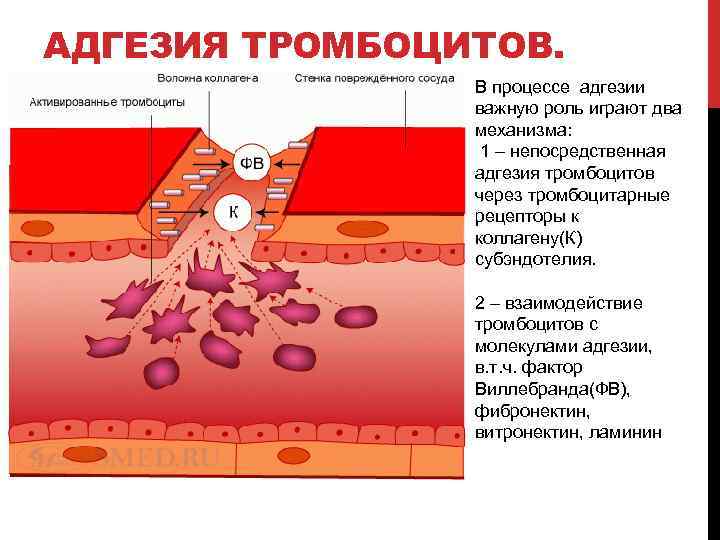 АДГЕЗИЯ ТРОМБОЦИТОВ. В процессе адгезии важную роль играют два механизма: 1 – непосредственная адгезия тромбоцитов через тромбоцитарные рецепторы к коллагену(К) субэндотелия. 2 – взаимодействие тромбоцитов с молекулами адгезии, в. т. ч. фактор Виллебранда(ФВ), фибронектин, витронектин, ламинин
АДГЕЗИЯ ТРОМБОЦИТОВ. В процессе адгезии важную роль играют два механизма: 1 – непосредственная адгезия тромбоцитов через тромбоцитарные рецепторы к коллагену(К) субэндотелия. 2 – взаимодействие тромбоцитов с молекулами адгезии, в. т. ч. фактор Виллебранда(ФВ), фибронектин, витронектин, ламинин
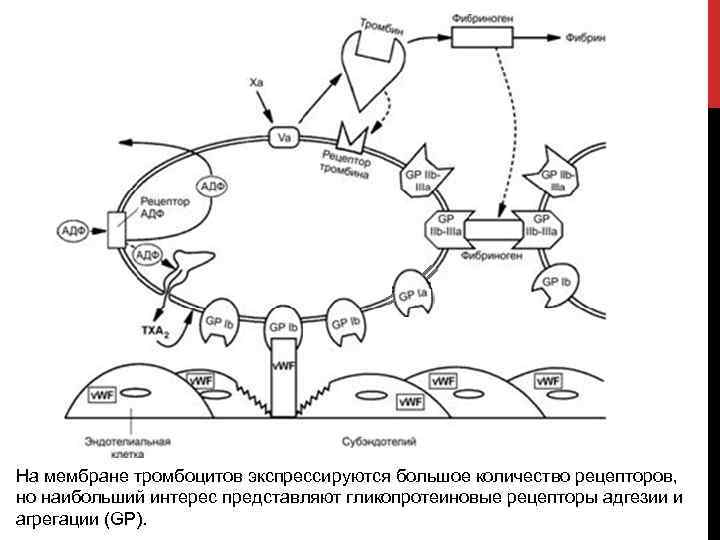 На мембране тромбоцитов экспрессируются большое количество рецепторов, но наибольший интерес представляют гликопротеиновые рецепторы адгезии и агрегации (GP).
На мембране тромбоцитов экспрессируются большое количество рецепторов, но наибольший интерес представляют гликопротеиновые рецепторы адгезии и агрегации (GP).
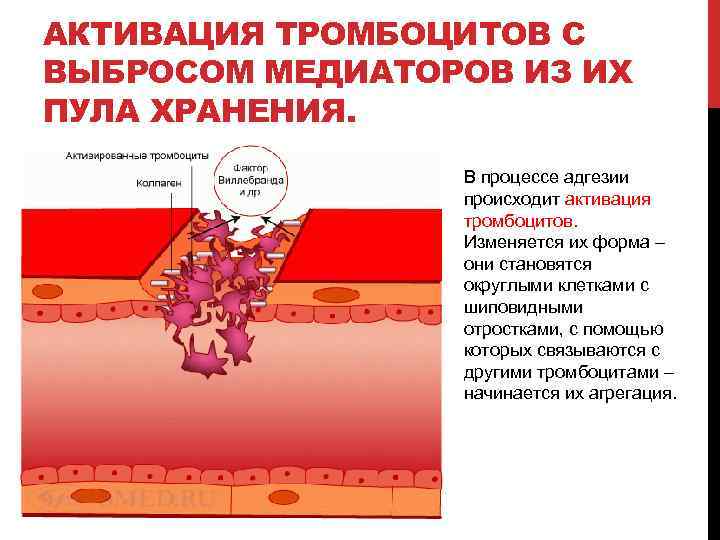 АКТИВАЦИЯ ТРОМБОЦИТОВ С ВЫБРОСОМ МЕДИАТОРОВ ИЗ ИХ ПУЛА ХРАНЕНИЯ. В процессе адгезии происходит активация тромбоцитов. Изменяется их форма – они становятся округлыми клетками с шиповидными отростками, с помощью которых связываются с другими тромбоцитами – начинается их агрегация.
АКТИВАЦИЯ ТРОМБОЦИТОВ С ВЫБРОСОМ МЕДИАТОРОВ ИЗ ИХ ПУЛА ХРАНЕНИЯ. В процессе адгезии происходит активация тромбоцитов. Изменяется их форма – они становятся округлыми клетками с шиповидными отростками, с помощью которых связываются с другими тромбоцитами – начинается их агрегация.
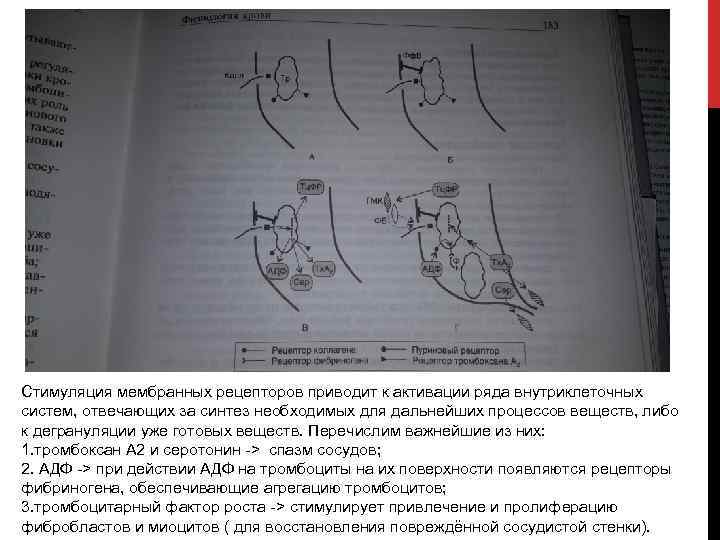 Стимуляция мембранных рецепторов приводит к активации ряда внутриклеточных систем, отвечающих за синтез необходимых для дальнейших процессов веществ, либо к дегрануляции уже готовых веществ. Перечислим важнейшие из них: 1. тромбоксан А 2 и серотонин > спазм сосудов; 2. АДФ > при действии АДФ на тромбоциты на их поверхности появляются рецепторы фибриногена, обеспечивающие агрегацию тромбоцитов; 3. тромбоцитарный фактор роста > стимулирует привлечение и пролиферацию фибробластов и миоцитов ( для восстановления повреждённой сосудистой стенки).
Стимуляция мембранных рецепторов приводит к активации ряда внутриклеточных систем, отвечающих за синтез необходимых для дальнейших процессов веществ, либо к дегрануляции уже готовых веществ. Перечислим важнейшие из них: 1. тромбоксан А 2 и серотонин > спазм сосудов; 2. АДФ > при действии АДФ на тромбоциты на их поверхности появляются рецепторы фибриногена, обеспечивающие агрегацию тромбоцитов; 3. тромбоцитарный фактор роста > стимулирует привлечение и пролиферацию фибробластов и миоцитов ( для восстановления повреждённой сосудистой стенки).
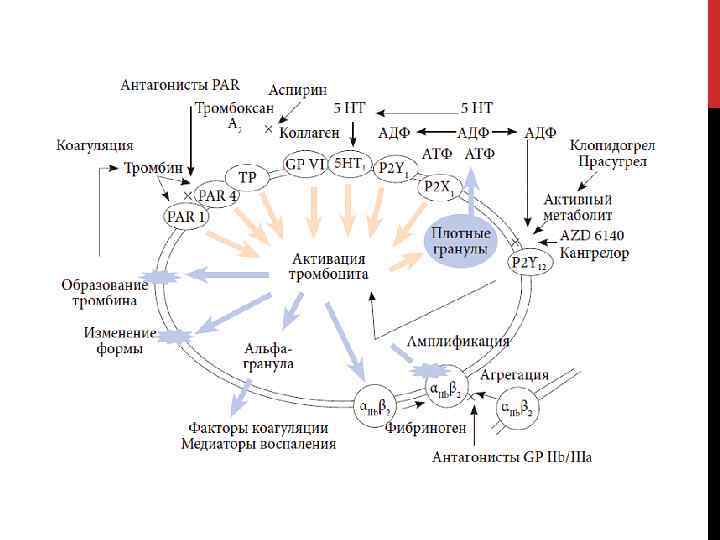
 АКТИВАЦИЯ ТРОМБОЦИТОВ
АКТИВАЦИЯ ТРОМБОЦИТОВ
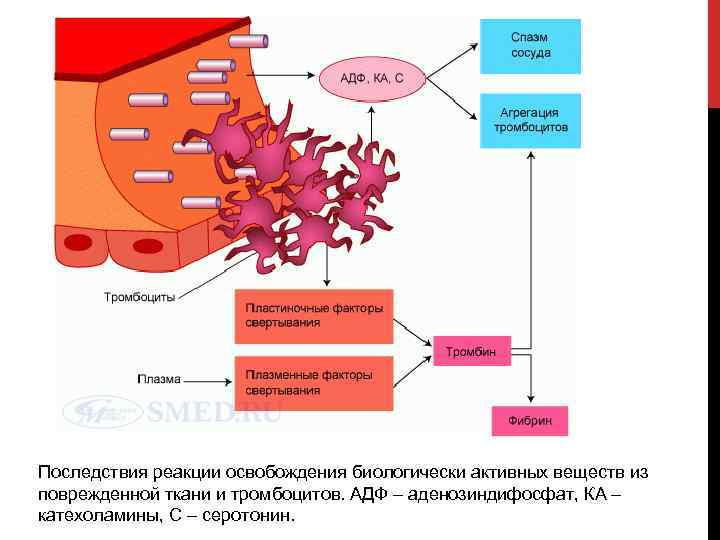 Последствия реакции освобождения биологически активных веществ из поврежденной ткани и тромбоцитов. АДФ – аденозиндифосфат, КА – катехоламины, С – серотонин.
Последствия реакции освобождения биологически активных веществ из поврежденной ткани и тромбоцитов. АДФ – аденозиндифосфат, КА – катехоламины, С – серотонин.
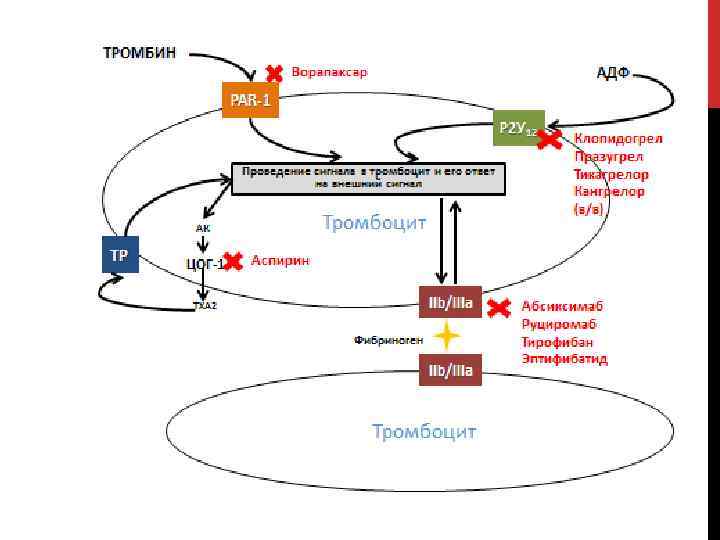
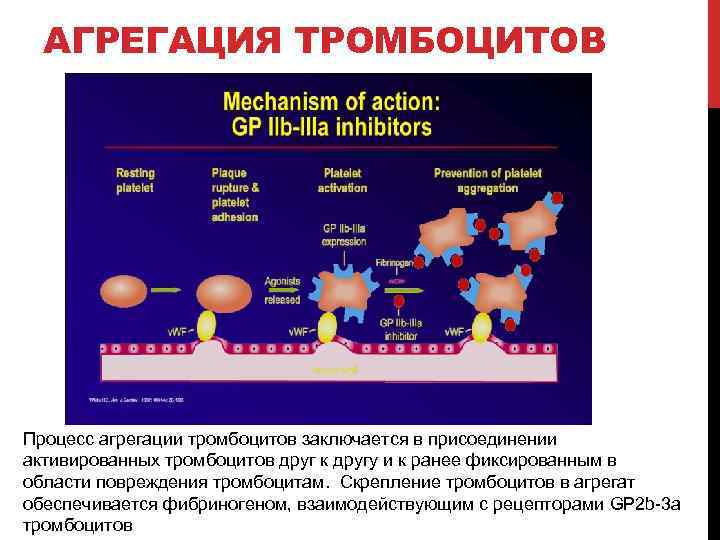 АГРЕГАЦИЯ ТРОМБОЦИТОВ Процесс агрегации тромбоцитов заключается в присоединении активированных тромбоцитов друг к другу и к ранее фиксированным в области повреждения тромбоцитам. Скрепление тромбоцитов в агрегат обеспечивается фибриногеном, взаимодействующим с рецепторами GP 2 b 3 a тромбоцитов
АГРЕГАЦИЯ ТРОМБОЦИТОВ Процесс агрегации тромбоцитов заключается в присоединении активированных тромбоцитов друг к другу и к ранее фиксированным в области повреждения тромбоцитам. Скрепление тромбоцитов в агрегат обеспечивается фибриногеном, взаимодействующим с рецепторами GP 2 b 3 a тромбоцитов
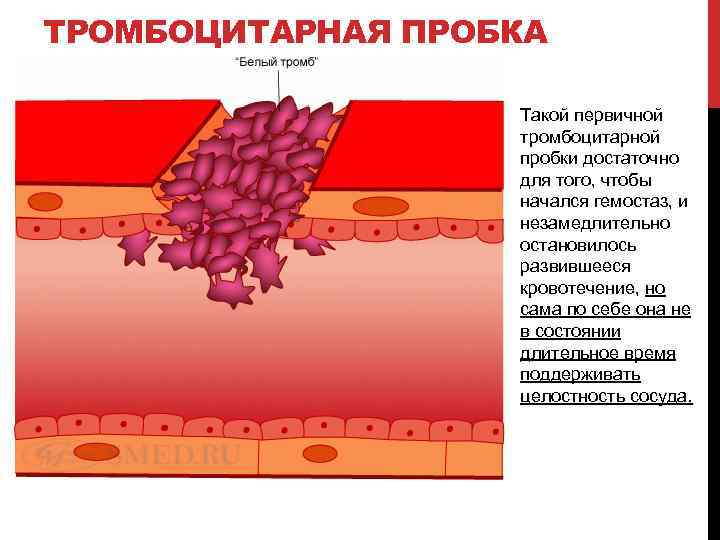 ТРОМБОЦИТАРНАЯ ПРОБКА Такой первичной тромбоцитарной пробки достаточно для того, чтобы начался гемостаз, и незамедлительно остановилось развившееся кровотечение, но сама по себе она не в состоянии длительное время поддерживать целостность сосуда.
ТРОМБОЦИТАРНАЯ ПРОБКА Такой первичной тромбоцитарной пробки достаточно для того, чтобы начался гемостаз, и незамедлительно остановилось развившееся кровотечение, но сама по себе она не в состоянии длительное время поддерживать целостность сосуда.
 Первичной тромбоцитарной пробки ( «белого» тромба) достаточно для окончательной остановки капиллярного кровотечения, однако в более крупных сосудах она постепенно вымывается током крови, что может привести к возобновлению кровотечения. Поэтому тромбоцитарный тромб укрепляется фибрином с включением других форменных элементов крови, в результате чего образуется «красный» тромб.
Первичной тромбоцитарной пробки ( «белого» тромба) достаточно для окончательной остановки капиллярного кровотечения, однако в более крупных сосудах она постепенно вымывается током крови, что может привести к возобновлению кровотечения. Поэтому тромбоцитарный тромб укрепляется фибрином с включением других форменных элементов крови, в результате чего образуется «красный» тромб.
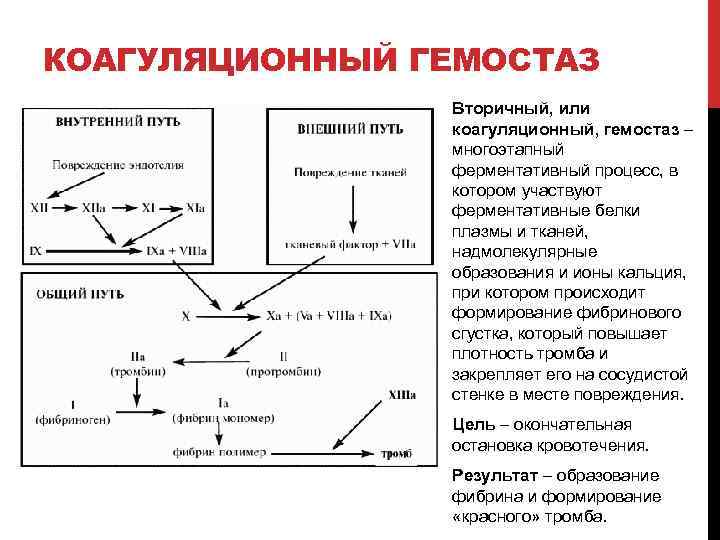 КОАГУЛЯЦИОННЫЙ ГЕМОСТАЗ Вторичный, или коагуляционный, гемостаз – многоэтапный ферментативный процесс, в котором участвуют ферментативные белки плазмы и тканей, надмолекулярные образования и ионы кальция, при котором происходит формирование фибринового сгустка, который повышает плотность тромба и закрепляет его на сосудистой стенке в месте повреждения. Цель – окончательная остановка кровотечения. Результат – образование фибрина и формирование «красного» тромба.
КОАГУЛЯЦИОННЫЙ ГЕМОСТАЗ Вторичный, или коагуляционный, гемостаз – многоэтапный ферментативный процесс, в котором участвуют ферментативные белки плазмы и тканей, надмолекулярные образования и ионы кальция, при котором происходит формирование фибринового сгустка, который повышает плотность тромба и закрепляет его на сосудистой стенке в месте повреждения. Цель – окончательная остановка кровотечения. Результат – образование фибрина и формирование «красного» тромба.
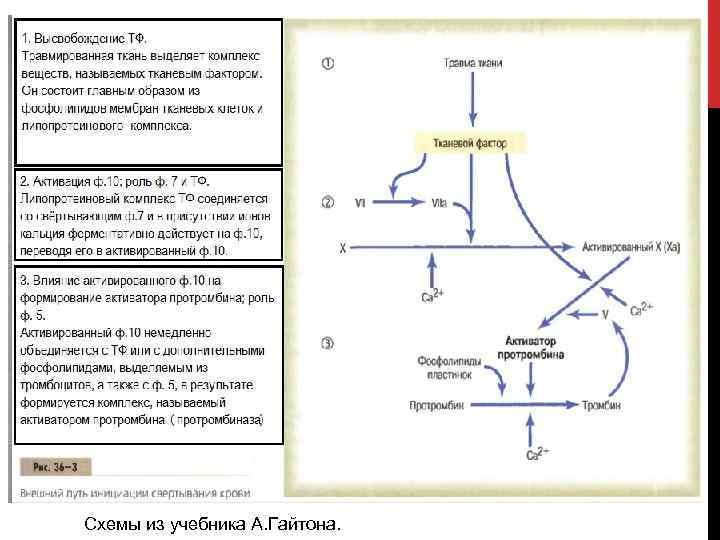 Схемы из учебника А. Гайтона.
Схемы из учебника А. Гайтона.
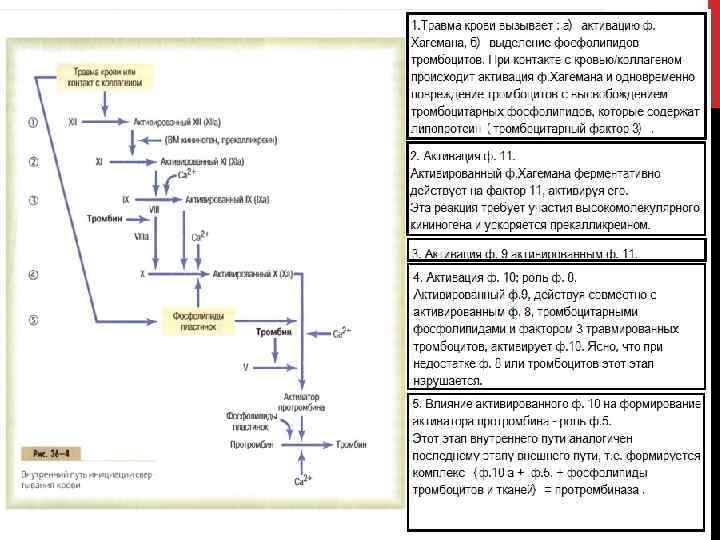
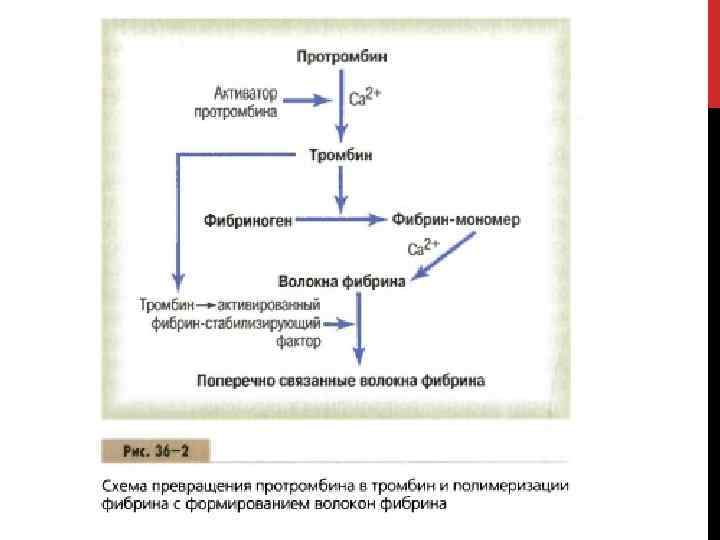
 Основы современной ферментной теории свёртывания крови были заложены в конце XIX – начале XX столетия профессором Тартуского (Дерптского) университета Александром-Адольфом Шмидтом (1877 г. ) и уроженцем Санкт Петербурга Паулом Моравитцем (1904 г. ), а также в работе С. Мурашева о специфичности действия фибрин ферментов (1904 г. ). Адольф Шмидт (Adolf Schmidt) — немецкий малаколог и врач.
Основы современной ферментной теории свёртывания крови были заложены в конце XIX – начале XX столетия профессором Тартуского (Дерптского) университета Александром-Адольфом Шмидтом (1877 г. ) и уроженцем Санкт Петербурга Паулом Моравитцем (1904 г. ), а также в работе С. Мурашева о специфичности действия фибрин ферментов (1904 г. ). Адольф Шмидт (Adolf Schmidt) — немецкий малаколог и врач.
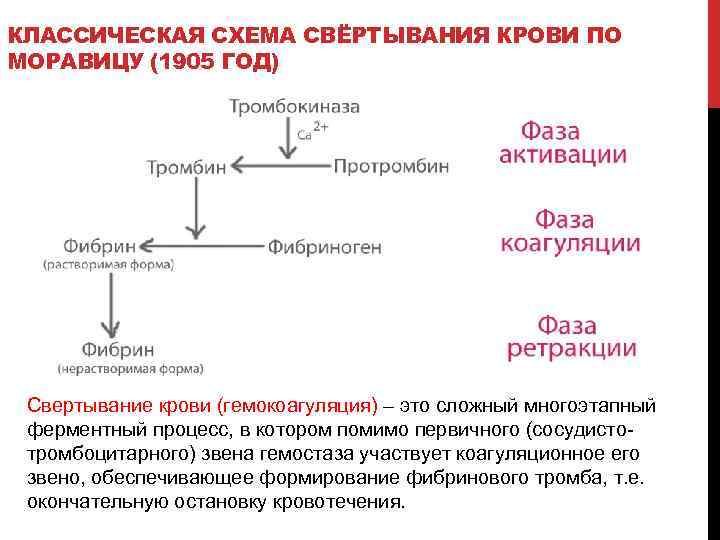 КЛАССИЧЕСКАЯ СХЕМА СВЁРТЫВАНИЯ КРОВИ ПО МОРАВИЦУ (1905 ГОД) Свертывание крови (гемокоагуляция) – это сложный многоэтапный ферментный процесс, в котором помимо первичного (сосудисто тромбоцитарного) звена гемостаза участвует коагуляционное его звено, обеспечивающее формирование фибринового тромба, т. е. окончательную остановку кровотечения.
КЛАССИЧЕСКАЯ СХЕМА СВЁРТЫВАНИЯ КРОВИ ПО МОРАВИЦУ (1905 ГОД) Свертывание крови (гемокоагуляция) – это сложный многоэтапный ферментный процесс, в котором помимо первичного (сосудисто тромбоцитарного) звена гемостаза участвует коагуляционное его звено, обеспечивающее формирование фибринового тромба, т. е. окончательную остановку кровотечения.
 КАСКАДНО МАТРИЧНАЯ (КЛЕТОЧНАЯ) ТЕОРИЯ (2002 Г) Разработанная и дополненная в начале се редине XX века теория гемостаза базировалась на исследованиях, выполненных in vitro, и не учи тывала реальные условия в системе кровообра щения. В последнее десятилетие под давлением на копившихся фактов взгляд на механизмы гемостатических реакций изменился. Наиболее значи мым шагом явилась разработка каскадно матричной теории свертывания крови, в которой учте ны не только реакции взаимодействия белков плазмы и тромбоцитов, но влияние компонентов сосудистой стенки и других клеток крови. Реак ции гемостаза привязали к конкретным структу рам на мембранах клеток и субэндотелия. Были учтены особенности мембранных рецепторов кле точных компонентов гемостаза и микроокруже ния, в котором происходят реакции.
КАСКАДНО МАТРИЧНАЯ (КЛЕТОЧНАЯ) ТЕОРИЯ (2002 Г) Разработанная и дополненная в начале се редине XX века теория гемостаза базировалась на исследованиях, выполненных in vitro, и не учи тывала реальные условия в системе кровообра щения. В последнее десятилетие под давлением на копившихся фактов взгляд на механизмы гемостатических реакций изменился. Наиболее значи мым шагом явилась разработка каскадно матричной теории свертывания крови, в которой учте ны не только реакции взаимодействия белков плазмы и тромбоцитов, но влияние компонентов сосудистой стенки и других клеток крови. Реак ции гемостаза привязали к конкретным структу рам на мембранах клеток и субэндотелия. Были учтены особенности мембранных рецепторов кле точных компонентов гемостаза и микроокруже ния, в котором происходят реакции.
 НЕОБХОДИМОСТЬ СОЗДАНИЯ НОВОЙ КАСКАДНО МАТРИЧНОЙ (КЛЕТОЧНОЙ) ТЕОРИИ СВЕРТЫВАНИЯ КРОВИ НАЗРЕЛА В РЕЗУЛЬТАТЕ НЕСТЫКОВОК КЛАССИЧЕСКОЙ ТЕОРИИ С ДАННЫМИ КЛИНИЧЕСКИХ НАБЛЮДЕНИЙ. 1. По классической версии отсутствие факторов VIII и IX у больных гемофилиями А и В не должно приводить к кровотечениям, т. к. существует внешний путь активации тромбина. Однако на деле внешнего пути оказывается недостаточно. 2. Отсутствие фактора Хагемана, инициатора внутреннего пути свертывания в классической теории, приводит к тромбофилиям, но не к кровотечениям, 3. Влияние активаторов XII фактора прекалликреина и высокомолекулярного кининогена на свертывание крови проявляется только в исследованиях in vitro, и их недостаток у пациента выявляется случайно, т. к. клинически никак не проявляется. 4. По клеточной теории "контактные" факторы (Хагемана (XIIа), калликреин, высокомо лекулярный кининоген) имеют весьма ограниченное значение при коагуляции с целью остановки кровотечения, но необходимы для формирования фибрина в ходе воспалительной реакции.
НЕОБХОДИМОСТЬ СОЗДАНИЯ НОВОЙ КАСКАДНО МАТРИЧНОЙ (КЛЕТОЧНОЙ) ТЕОРИИ СВЕРТЫВАНИЯ КРОВИ НАЗРЕЛА В РЕЗУЛЬТАТЕ НЕСТЫКОВОК КЛАССИЧЕСКОЙ ТЕОРИИ С ДАННЫМИ КЛИНИЧЕСКИХ НАБЛЮДЕНИЙ. 1. По классической версии отсутствие факторов VIII и IX у больных гемофилиями А и В не должно приводить к кровотечениям, т. к. существует внешний путь активации тромбина. Однако на деле внешнего пути оказывается недостаточно. 2. Отсутствие фактора Хагемана, инициатора внутреннего пути свертывания в классической теории, приводит к тромбофилиям, но не к кровотечениям, 3. Влияние активаторов XII фактора прекалликреина и высокомолекулярного кининогена на свертывание крови проявляется только в исследованиях in vitro, и их недостаток у пациента выявляется случайно, т. к. клинически никак не проявляется. 4. По клеточной теории "контактные" факторы (Хагемана (XIIа), калликреин, высокомо лекулярный кининоген) имеют весьма ограниченное значение при коагуляции с целью остановки кровотечения, но необходимы для формирования фибрина в ходе воспалительной реакции.
 Современная каскадно-матричная (клеточная) теория (2002 г) подразумевает, что в организме "внешний" и "внутренний" пути не изолированы друг от друга, а представляют собой единую систему, имеющую множество прямых и обратных положительных связей и перекрестных влияний отдельных факторов друг на друга.
Современная каскадно-матричная (клеточная) теория (2002 г) подразумевает, что в организме "внешний" и "внутренний" пути не изолированы друг от друга, а представляют собой единую систему, имеющую множество прямых и обратных положительных связей и перекрестных влияний отдельных факторов друг на друга.
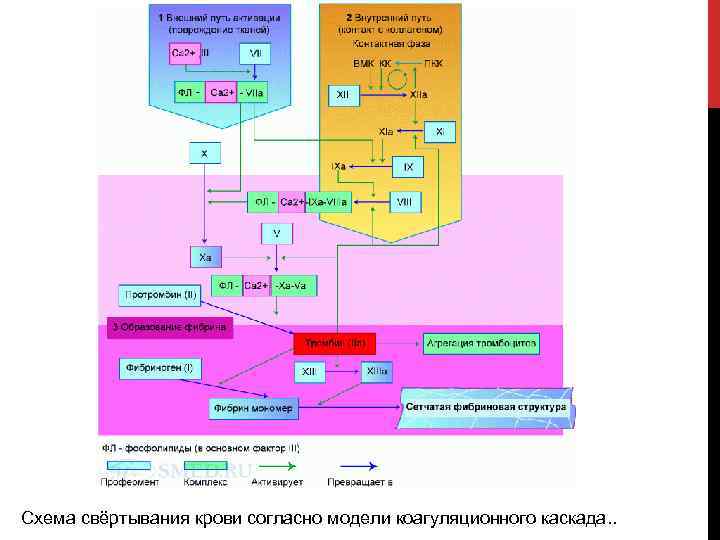 Схема свёртывания крови согласно модели коагуляционного каскада. .
Схема свёртывания крови согласно модели коагуляционного каскада. .
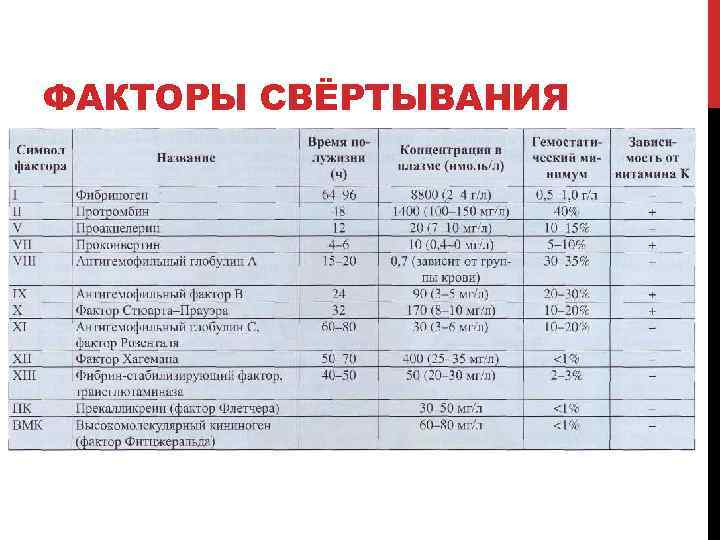 ФАКТОРЫ СВЁРТЫВАНИЯ
ФАКТОРЫ СВЁРТЫВАНИЯ
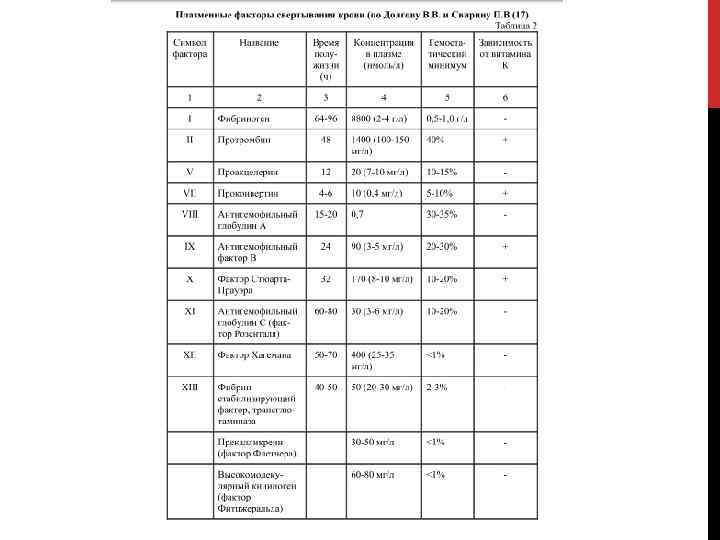
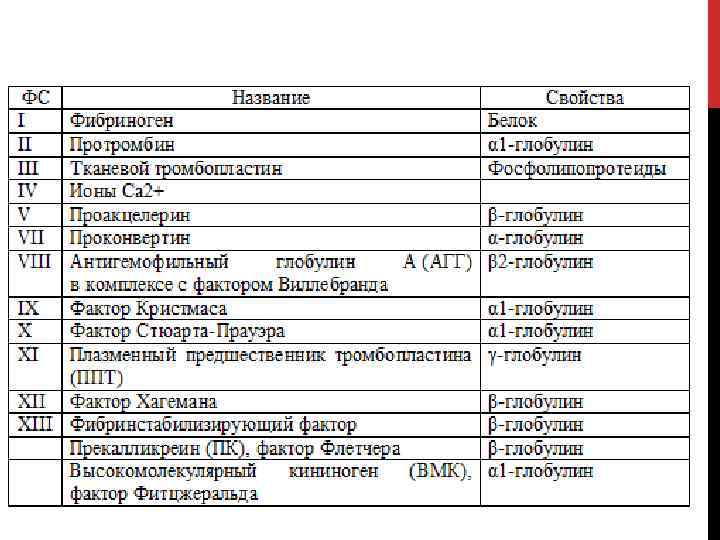
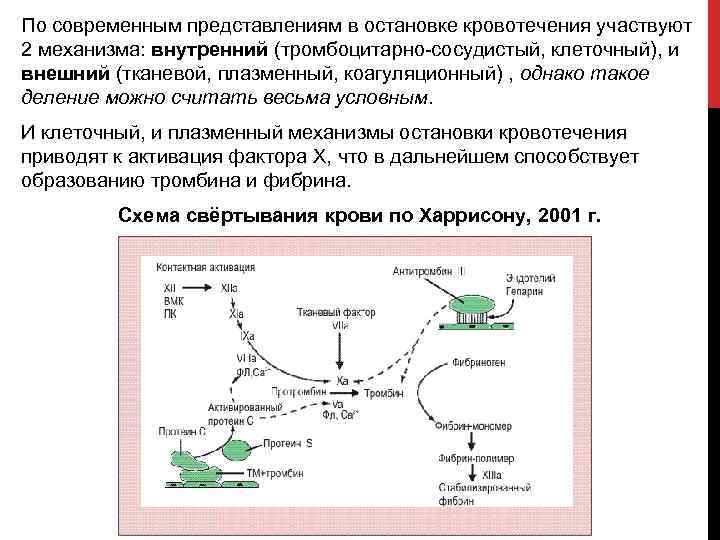 По современным представлениям в остановке кровотечения участвуют 2 механизма: внутренний (тромбоцитарно сосудистый, клеточный), и внешний (тканевой, плазменный, коагуляционный) , однако такое деление можно считать весьма условным. И клеточный, и плазменный механизмы остановки кровотечения приводят к активация фактора X, что в дальнейшем способствует образованию тромбина и фибрина. Схема свёртывания крови по Харрисону, 2001 г.
По современным представлениям в остановке кровотечения участвуют 2 механизма: внутренний (тромбоцитарно сосудистый, клеточный), и внешний (тканевой, плазменный, коагуляционный) , однако такое деление можно считать весьма условным. И клеточный, и плазменный механизмы остановки кровотечения приводят к активация фактора X, что в дальнейшем способствует образованию тромбина и фибрина. Схема свёртывания крови по Харрисону, 2001 г.
 С УЧЁТОМ ДАННЫХ О ЛОКАЛИЗАЦИИ И КОНТРОЛЕ КОАГУЛЯЦИОННЫХ РЕАКЦИЙ НА РАЗЛИЧНЫХ КЛЕТОЧНЫХ ПОВЕРХНОСТЯХ, ПРОЦЕСС СВЁРТЫВАНИЯ КРОВИ В НАСТОЯЩЕЕ ВРЕМЯ ПРЕДСТАВЛЯЮТ В ВИДЕ 3 ПЕРЕКРЫВАЮЩИХ ДРУГА ФАЗ: 1. Инициации (initiation) 2. Усиления (amplification) 3. Распространения (propagation). В результате выполнения трех стадий образуется тромбин, далее превращающий фибриноген в фибринмономеры. В некоторых источниках говорят о 4 стадиях: инициация, амплификация, распространение, терминация.
С УЧЁТОМ ДАННЫХ О ЛОКАЛИЗАЦИИ И КОНТРОЛЕ КОАГУЛЯЦИОННЫХ РЕАКЦИЙ НА РАЗЛИЧНЫХ КЛЕТОЧНЫХ ПОВЕРХНОСТЯХ, ПРОЦЕСС СВЁРТЫВАНИЯ КРОВИ В НАСТОЯЩЕЕ ВРЕМЯ ПРЕДСТАВЛЯЮТ В ВИДЕ 3 ПЕРЕКРЫВАЮЩИХ ДРУГА ФАЗ: 1. Инициации (initiation) 2. Усиления (amplification) 3. Распространения (propagation). В результате выполнения трех стадий образуется тромбин, далее превращающий фибриноген в фибринмономеры. В некоторых источниках говорят о 4 стадиях: инициация, амплификация, распространение, терминация.
 1 СТАДИЯ – ИНИЦИАЦИЯ ( «ВНЕШНИЙ ПУТЬ» )
1 СТАДИЯ – ИНИЦИАЦИЯ ( «ВНЕШНИЙ ПУТЬ» )
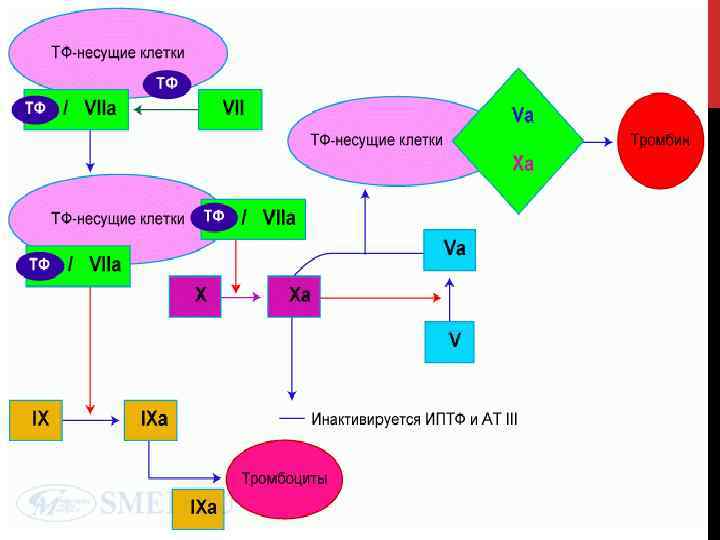
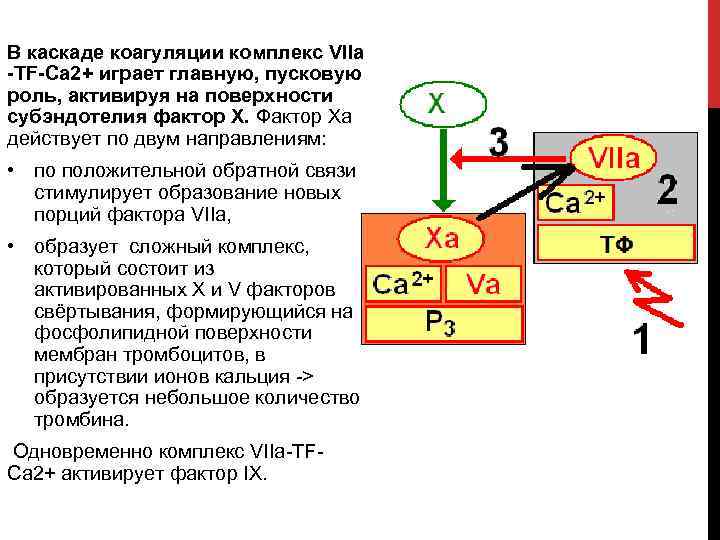 В каскаде коагуляции комплекс VIIа -TF-Ca 2+ играет главную, пусковую роль, активируя на поверхности субэндотелия фактор Х. Фактор Xa действует по двум направлениям: • по положительной обратной связи стимулирует образование новых порций фактора VIIa, • образует сложный комплекс, который состоит из активированных X и V факторов свёртывания, формирующийся на фосфолипидной поверхности мембран тромбоцитов, в присутствии ионов кальция > образуется небольшое количество тромбина. Одновременно комплекс VIIа TF Ca 2+ активирует фактор IX.
В каскаде коагуляции комплекс VIIа -TF-Ca 2+ играет главную, пусковую роль, активируя на поверхности субэндотелия фактор Х. Фактор Xa действует по двум направлениям: • по положительной обратной связи стимулирует образование новых порций фактора VIIa, • образует сложный комплекс, который состоит из активированных X и V факторов свёртывания, формирующийся на фосфолипидной поверхности мембран тромбоцитов, в присутствии ионов кальция > образуется небольшое количество тромбина. Одновременно комплекс VIIа TF Ca 2+ активирует фактор IX.
 2 СТАДИЯ – АМПЛИФИКАЦИЯ Как только обнажается субэндотелий, возникают условия для развития событий сосудисто тромбоцитарного гемостаза – адгезии и активации тромбоцитов, которые предоставляют фосфолипиды (тромбоцитарный тромбопластин) для присоединения факторов свертывания. Сильным стимулятором активации тромбоцитов является образуемый на 1 стадии тромбин. Тромбин превращает факторы V, VIII, XI в их активные формы. Эти активированные факторы и мигрирующий от субэндотелия фактор IXa связываются с поверхностью адгезированных тромбоцитов.
2 СТАДИЯ – АМПЛИФИКАЦИЯ Как только обнажается субэндотелий, возникают условия для развития событий сосудисто тромбоцитарного гемостаза – адгезии и активации тромбоцитов, которые предоставляют фосфолипиды (тромбоцитарный тромбопластин) для присоединения факторов свертывания. Сильным стимулятором активации тромбоцитов является образуемый на 1 стадии тромбин. Тромбин превращает факторы V, VIII, XI в их активные формы. Эти активированные факторы и мигрирующий от субэндотелия фактор IXa связываются с поверхностью адгезированных тромбоцитов.
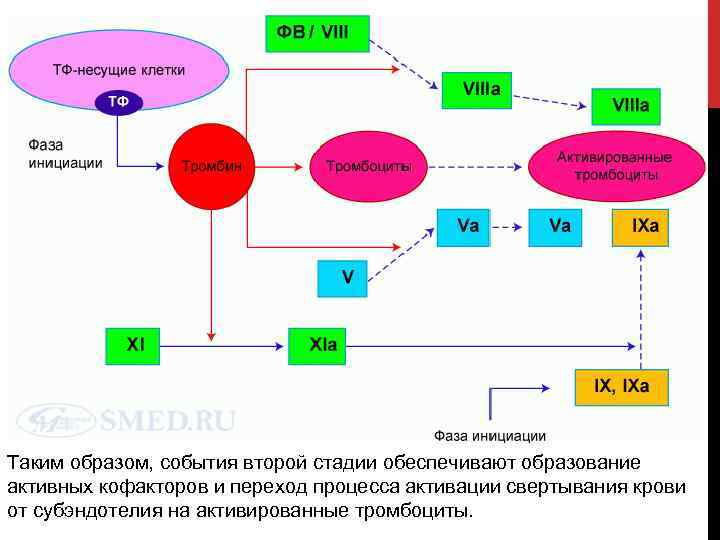 Таким образом, события второй стадии обеспечивают образование активных кофакторов и переход процесса активации свертывания крови от субэндотелия на активированные тромбоциты.
Таким образом, события второй стадии обеспечивают образование активных кофакторов и переход процесса активации свертывания крови от субэндотелия на активированные тромбоциты.
 Пространственное разграничение процессов коагуляции( фаза инициации – на поверхности ТФ несущих клеток, фаза усиления – на поверхности тромбоцитов) – один из механизмов ограничения их выраженности при отсутствии необходимости в свёртывании крови.
Пространственное разграничение процессов коагуляции( фаза инициации – на поверхности ТФ несущих клеток, фаза усиления – на поверхности тромбоцитов) – один из механизмов ограничения их выраженности при отсутствии необходимости в свёртывании крови.
 3 СТАДИЯ – ПРОПАГАЦИЯ( «ВНУТРЕННИЙ ПУТЬ» ) На стадии пропагации происходит каскадная активация факторов свертывания на поверхности тромбоцитов, имеющих рецепторы для активных и неактивных V, VIII, IX, X, XI факторов, для протромбина и тромбина. Активация на предыдущей стадии фактора VIII позволяет сейчас сформироваться на поверхности тромбоцитов комплексу IXa+VIIIa+Ca 2+ (теназный комплекс), который активирует фактор X. Под влиянием теназы скорость накопления фактора Xа увеличивается в 50 100 раз. Образующийся фактор Ха с фактором Va образуют протромбиназный комплекс, который наращивает темпы синтеза тромбина в зоне повреждения. Одновременно, под влиянием активированного тромбином фактора XIa (на второй стадии) появляются новые порции фактора IXа и количество теназы на поверхности тромбоцитов быстро нарастает. Эта положительная обратная связь усиливает свертывание еще в 5 10 тысяч раз. В результате третьей стадии образуется значительное количество тромбина, которого уже достаточно для образования фибрина и формирования гемостатического тромба. Полученный тромбин образует фибрин мономер из фибриногена и активирует фактор XIII. Также он активирует ингибитор фибринолиза TAFI, что дает время сформироваться плотному гемостатическому тромбу.
3 СТАДИЯ – ПРОПАГАЦИЯ( «ВНУТРЕННИЙ ПУТЬ» ) На стадии пропагации происходит каскадная активация факторов свертывания на поверхности тромбоцитов, имеющих рецепторы для активных и неактивных V, VIII, IX, X, XI факторов, для протромбина и тромбина. Активация на предыдущей стадии фактора VIII позволяет сейчас сформироваться на поверхности тромбоцитов комплексу IXa+VIIIa+Ca 2+ (теназный комплекс), который активирует фактор X. Под влиянием теназы скорость накопления фактора Xа увеличивается в 50 100 раз. Образующийся фактор Ха с фактором Va образуют протромбиназный комплекс, который наращивает темпы синтеза тромбина в зоне повреждения. Одновременно, под влиянием активированного тромбином фактора XIa (на второй стадии) появляются новые порции фактора IXа и количество теназы на поверхности тромбоцитов быстро нарастает. Эта положительная обратная связь усиливает свертывание еще в 5 10 тысяч раз. В результате третьей стадии образуется значительное количество тромбина, которого уже достаточно для образования фибрина и формирования гемостатического тромба. Полученный тромбин образует фибрин мономер из фибриногена и активирует фактор XIII. Также он активирует ингибитор фибринолиза TAFI, что дает время сформироваться плотному гемостатическому тромбу.
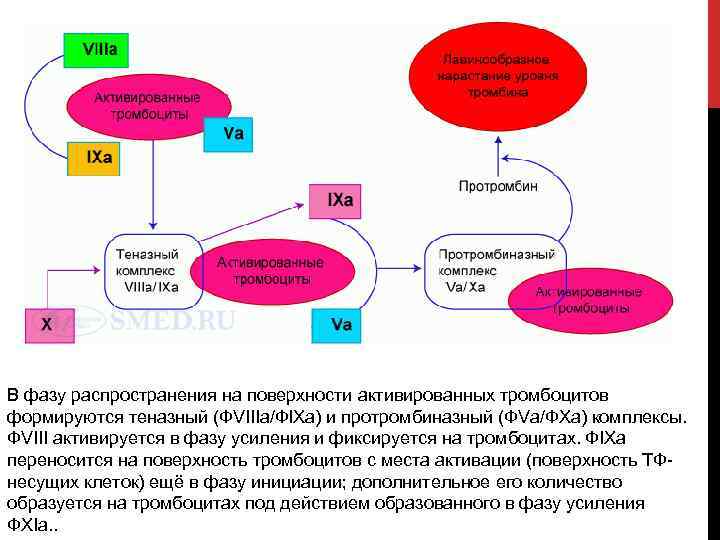 В фазу распространения на поверхности активированных тромбоцитов формируются теназный (ФVIIIa/ФIXa) и протромбиназный (ФVa/ФXa) комплексы. ФVIII активируется в фазу усиления и фиксируется на тромбоцитах. ФIXa переносится на поверхность тромбоцитов с места активации (поверхность ТФ несущих клеток) ещё в фазу инициации; дополнительное его количество образуется на тромбоцитах под действием образованного в фазу усиления ФXIa. .
В фазу распространения на поверхности активированных тромбоцитов формируются теназный (ФVIIIa/ФIXa) и протромбиназный (ФVa/ФXa) комплексы. ФVIII активируется в фазу усиления и фиксируется на тромбоцитах. ФIXa переносится на поверхность тромбоцитов с места активации (поверхность ТФ несущих клеток) ещё в фазу инициации; дополнительное его количество образуется на тромбоцитах под действием образованного в фазу усиления ФXIa. .
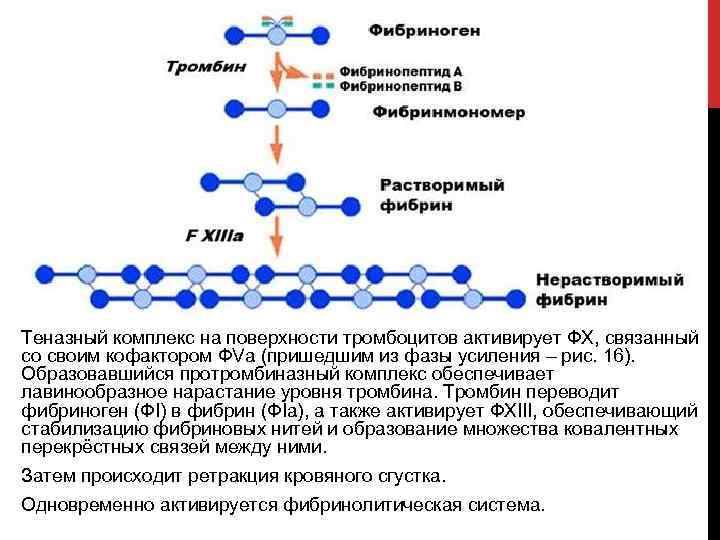 Теназный комплекс на поверхности тромбоцитов активирует ФX, связанный со своим кофактором ФVa (пришедшим из фазы усиления – рис. 16). Образовавшийся протромбиназный комплекс обеспечивает лавинообразное нарастание уровня тромбина. Тромбин переводит фибриноген (ФI) в фибрин (ФIa), а также активирует ФXIII, обеспечивающий стабилизацию фибриновых нитей и образование множества ковалентных перекрёстных связей между ними. Затем происходит ретракция кровяного сгустка. Одновременно активируется фибринолитическая система.
Теназный комплекс на поверхности тромбоцитов активирует ФX, связанный со своим кофактором ФVa (пришедшим из фазы усиления – рис. 16). Образовавшийся протромбиназный комплекс обеспечивает лавинообразное нарастание уровня тромбина. Тромбин переводит фибриноген (ФI) в фибрин (ФIa), а также активирует ФXIII, обеспечивающий стабилизацию фибриновых нитей и образование множества ковалентных перекрёстных связей между ними. Затем происходит ретракция кровяного сгустка. Одновременно активируется фибринолитическая система.
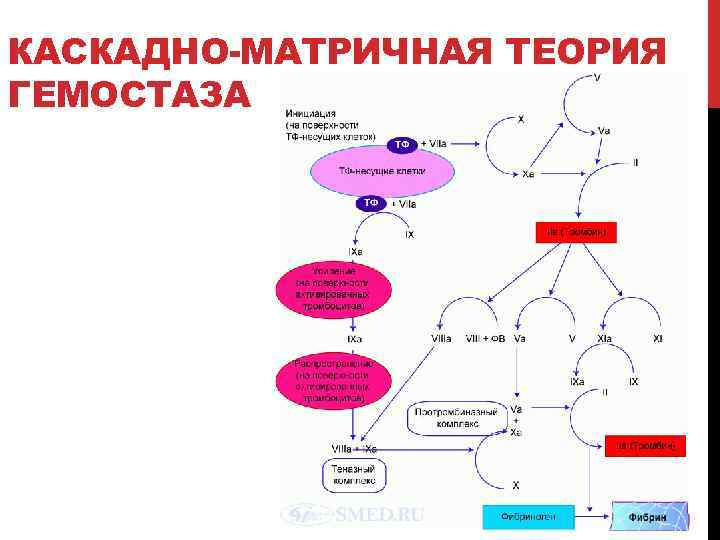 КАСКАДНО МАТРИЧНАЯ ТЕОРИЯ ГЕМОСТАЗА
КАСКАДНО МАТРИЧНАЯ ТЕОРИЯ ГЕМОСТАЗА
 НЕОБХОДИМОСТЬ СОЗДАНИЯ НОВОЙ КАСКАДНО МАТРИЧНОЙ (КЛЕТОЧНОЙ) ТЕОРИИ СВЕРТЫВАНИЯ КРОВИ НАЗРЕЛА В РЕЗУЛЬТАТЕ НЕСТЫКОВОК КЛАССИЧЕСКОЙ ТЕОРИИ С ДАННЫМИ КЛИНИЧЕСКИХ НАБЛЮДЕНИЙ. 1. По классической версии отсутствие факторов VIII и IX у больных гемофилиями А и В не должно приводить к кровотечениям, т. к. существует внешний путь активации тромбина. Однако на деле внешнего пути оказывается недостаточно. 2. Отсутствие фактора Хагемана, инициатора внутреннего пути свертывания в классической теории, приводит к тромбофилиям, но не к кровотечениям, 3. Влияние активаторов XII фактора прекалликреина и высокомолекулярного кининогена на свертывание крови проявляется только в исследованиях in vitro, и их недостаток у пациента выявляется случайно, т. к. клинически никак не проявляется. 4. По клеточной теории "контактные" факторы (Хагемана (XIIа), калликреин, высокомо лекулярный кининоген) имеют весьма ограниченное значение при коагуляции с целью остановки кровотечения, но необходимы для формирования фибрина в ходе воспалительной реакции.
НЕОБХОДИМОСТЬ СОЗДАНИЯ НОВОЙ КАСКАДНО МАТРИЧНОЙ (КЛЕТОЧНОЙ) ТЕОРИИ СВЕРТЫВАНИЯ КРОВИ НАЗРЕЛА В РЕЗУЛЬТАТЕ НЕСТЫКОВОК КЛАССИЧЕСКОЙ ТЕОРИИ С ДАННЫМИ КЛИНИЧЕСКИХ НАБЛЮДЕНИЙ. 1. По классической версии отсутствие факторов VIII и IX у больных гемофилиями А и В не должно приводить к кровотечениям, т. к. существует внешний путь активации тромбина. Однако на деле внешнего пути оказывается недостаточно. 2. Отсутствие фактора Хагемана, инициатора внутреннего пути свертывания в классической теории, приводит к тромбофилиям, но не к кровотечениям, 3. Влияние активаторов XII фактора прекалликреина и высокомолекулярного кининогена на свертывание крови проявляется только в исследованиях in vitro, и их недостаток у пациента выявляется случайно, т. к. клинически никак не проявляется. 4. По клеточной теории "контактные" факторы (Хагемана (XIIа), калликреин, высокомо лекулярный кининоген) имеют весьма ограниченное значение при коагуляции с целью остановки кровотечения, но необходимы для формирования фибрина в ходе воспалительной реакции.
 ПРОТИВОСВЁРТЫВАЮЩАЯ СИСТЕМА.
ПРОТИВОСВЁРТЫВАЮЩАЯ СИСТЕМА.
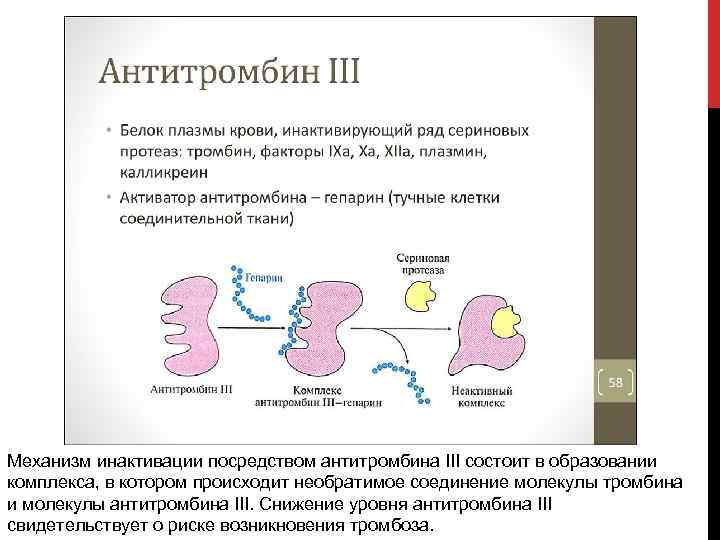 Механизм инактивации посредством антитромбина III состоит в образовании комплекса, в котором происходит необратимое соединение молекулы тромбина и молекулы антитромбина III. Снижение уровня антитромбина III свидетельствует о риске возникновения тромбоза.
Механизм инактивации посредством антитромбина III состоит в образовании комплекса, в котором происходит необратимое соединение молекулы тромбина и молекулы антитромбина III. Снижение уровня антитромбина III свидетельствует о риске возникновения тромбоза.
 АНТИТРОМБИН 3 (АТ 3). Антитромбин — основной плазменный белковый фактор, синтезируется, в основном, в сосудистом эндотелии и клетках печени. Оказывает основное угнетающее (антикоагуляционное) действие на процессы свёртывания крови. Состоит из двух различных функциональных доменов — гепарин связывающего и гепарин ингибирующего. Это основной плазматический белок в механизме инактивации тромбина (до 75 % угнетающей тромбин способности плазмы). При самостоятельном воздействии инактивация тромбина протекает медленно, по нарастающей. При наличии гепарина процесс инактивации развертывается очень быстро. Поэтому антитромбин III называют плазменным кофактором гепарина. Но в случае значительного снижения уровня антитромбина III гепарин почти не оказывает своего антикоагулянтного действия. Антитромбин III также принимает активное участие в инактивации факторов VIIA, IXA, XIA, XIIA.
АНТИТРОМБИН 3 (АТ 3). Антитромбин — основной плазменный белковый фактор, синтезируется, в основном, в сосудистом эндотелии и клетках печени. Оказывает основное угнетающее (антикоагуляционное) действие на процессы свёртывания крови. Состоит из двух различных функциональных доменов — гепарин связывающего и гепарин ингибирующего. Это основной плазматический белок в механизме инактивации тромбина (до 75 % угнетающей тромбин способности плазмы). При самостоятельном воздействии инактивация тромбина протекает медленно, по нарастающей. При наличии гепарина процесс инактивации развертывается очень быстро. Поэтому антитромбин III называют плазменным кофактором гепарина. Но в случае значительного снижения уровня антитромбина III гепарин почти не оказывает своего антикоагулянтного действия. Антитромбин III также принимает активное участие в инактивации факторов VIIA, IXA, XIA, XIIA.
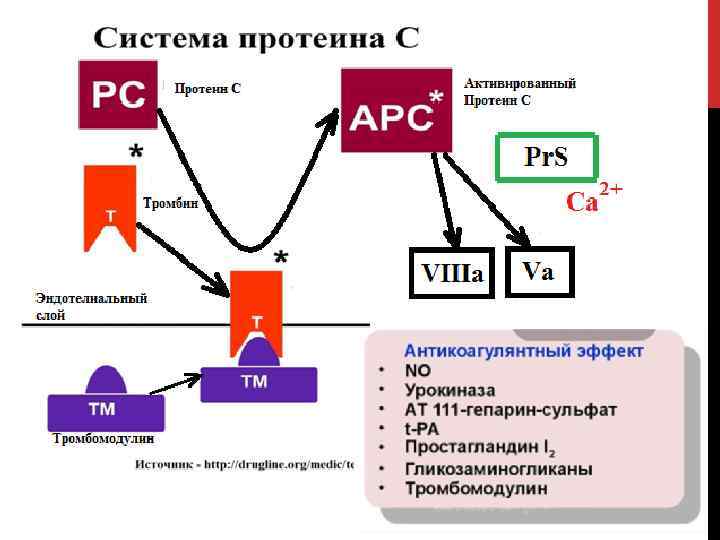
 ЧТО НАДО ЗНАТЬ О ПРОТЕИНЕ С: 1. Определения протеина С, как правило, проводится в рамках тестирования тромбофилии. Другие тесты включают в себя определение активности антитромбина, протеина S, генетическое тестирование на мутацию Leiden, мутацию гена протромбина G 20210 A, определение уровня гомоцистеина. 2. Протеин С имеет период полураспада приблизительно 6 часов. 3. Ген протеина C отображается на длинном плече хромосомы 2 в 2 q 13 -14 и кодирует белок из 419 аминокислот. 4. Активность протеина C повышается у здоровых лиц с возрастом. 5. Уровень протеина С резко падает при менингококковом сепсисе.
ЧТО НАДО ЗНАТЬ О ПРОТЕИНЕ С: 1. Определения протеина С, как правило, проводится в рамках тестирования тромбофилии. Другие тесты включают в себя определение активности антитромбина, протеина S, генетическое тестирование на мутацию Leiden, мутацию гена протромбина G 20210 A, определение уровня гомоцистеина. 2. Протеин С имеет период полураспада приблизительно 6 часов. 3. Ген протеина C отображается на длинном плече хромосомы 2 в 2 q 13 -14 и кодирует белок из 419 аминокислот. 4. Активность протеина C повышается у здоровых лиц с возрастом. 5. Уровень протеина С резко падает при менингококковом сепсисе.
 ИНГИБИТОР ВНЕШНЕГО ПУТИ. Открытие в последнее десятилетие ингибитора пути тканевого фактора (ИПТФ, ИВП, TFPI) стало важным шагом в пересмотре клас сического каскада свертывания крови и созда ния овременной каскадно матричной с теории гемостаза. ИВП ограничивает синтез тромбина комп лексом Ф ф. VII ф. Ха, блокируя Т его вскоре пос ле образования. Один из ингибирующих доменов ИВП связывается с ф. Ха, после чего другой до мен реагирует с активным центром ф. VII, когда последний связан с тканевым фактором. Аффин ность ИВП к ф. VIIа значительно повышается в присутствии гепарина. Образуется полностью неактивный тетрамолекулярный комп лекс ТФ ф. VII ИВП ф. Х. Помимо ингибирования, ИВП способствует поглощению и деграда ции этого комплекса. Таким образом, во внеш нем каскаде плазменного гемостаза формирует ся отрицательная обратная связь. ИВП, по видимому, ответственен при лече нии гепарином за удлинение ряда тестов коагулограммы, в частности АЧТВ. ИВП в плазме ча стично связан с липопротеидами низкой и очень низкой плотности (ЛПНП и ЛПОНП). В таком комплексе ИВП более устойчив к инактивации.
ИНГИБИТОР ВНЕШНЕГО ПУТИ. Открытие в последнее десятилетие ингибитора пути тканевого фактора (ИПТФ, ИВП, TFPI) стало важным шагом в пересмотре клас сического каскада свертывания крови и созда ния овременной каскадно матричной с теории гемостаза. ИВП ограничивает синтез тромбина комп лексом Ф ф. VII ф. Ха, блокируя Т его вскоре пос ле образования. Один из ингибирующих доменов ИВП связывается с ф. Ха, после чего другой до мен реагирует с активным центром ф. VII, когда последний связан с тканевым фактором. Аффин ность ИВП к ф. VIIа значительно повышается в присутствии гепарина. Образуется полностью неактивный тетрамолекулярный комп лекс ТФ ф. VII ИВП ф. Х. Помимо ингибирования, ИВП способствует поглощению и деграда ции этого комплекса. Таким образом, во внеш нем каскаде плазменного гемостаза формирует ся отрицательная обратная связь. ИВП, по видимому, ответственен при лече нии гепарином за удлинение ряда тестов коагулограммы, в частности АЧТВ. ИВП в плазме ча стично связан с липопротеидами низкой и очень низкой плотности (ЛПНП и ЛПОНП). В таком комплексе ИВП более устойчив к инактивации.
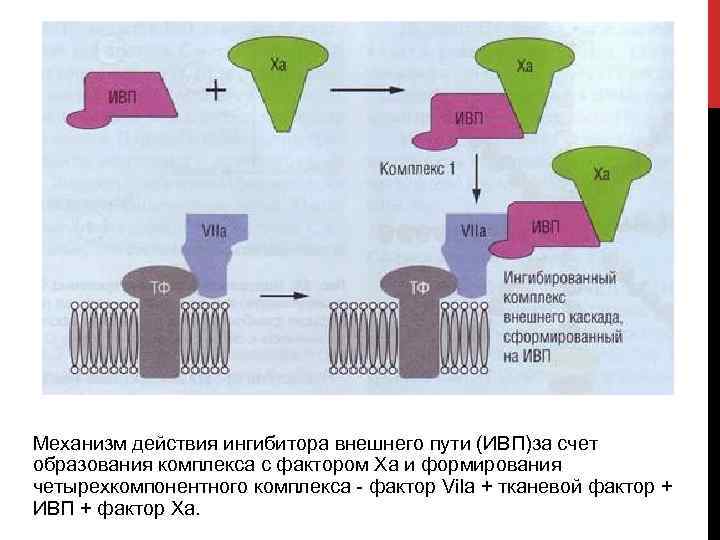 Механизм действия ингибитора внешнего пути (ИВП)за счет образования комплекса с фактором Ха и формирования четырехкомпонентного комплекса фактор Vila + тканевой фактор + ИВП + фактор Ха.
Механизм действия ингибитора внешнего пути (ИВП)за счет образования комплекса с фактором Ха и формирования четырехкомпонентного комплекса фактор Vila + тканевой фактор + ИВП + фактор Ха.
 Система протеина С, антитромбин 3, ингибитор внешнего пути – наиболее важные эффективные компоненты, очищающие плазму от активированных кофакторов плазменного гемостаза и ограничивающие процесс свёртывания крови.
Система протеина С, антитромбин 3, ингибитор внешнего пути – наиболее важные эффективные компоненты, очищающие плазму от активированных кофакторов плазменного гемостаза и ограничивающие процесс свёртывания крови.
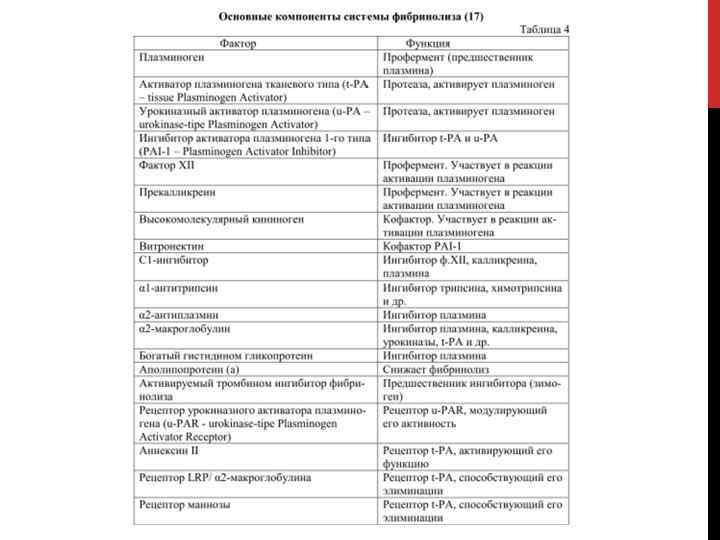
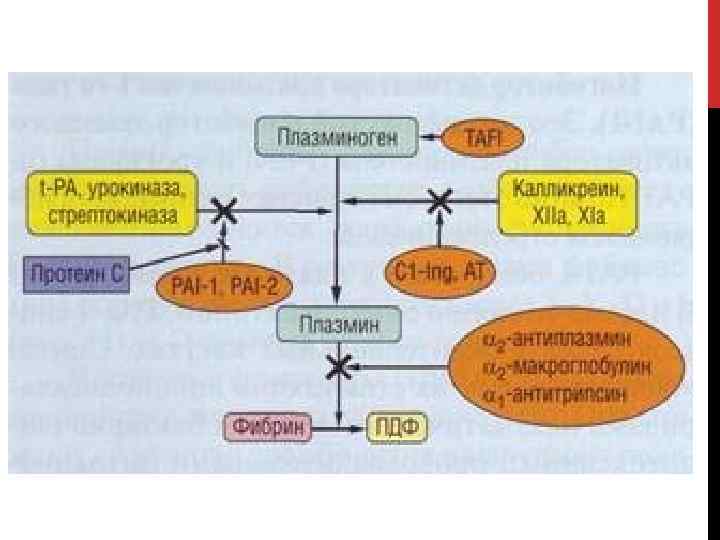
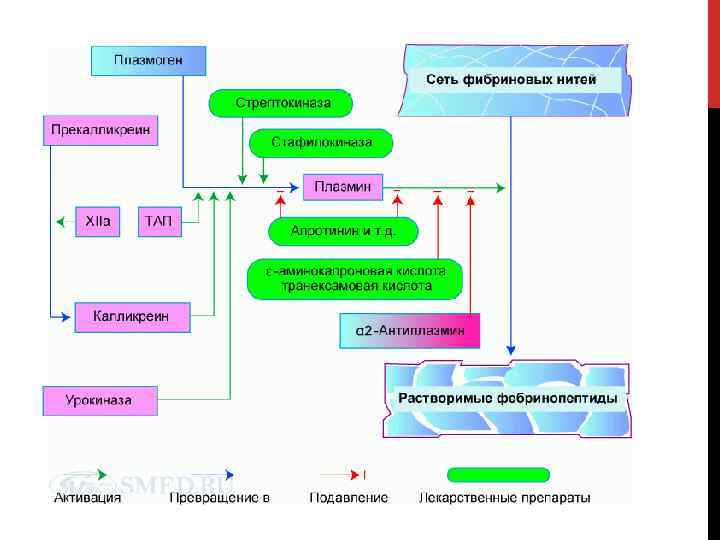
 ФИБРИНОЛИЗ. Компоненты фибринологической системы крови: 1. Плазмин; 2. Плазминоген; 3. Активаторы плазминогена; 4. Ингибиторы плазминогена;
ФИБРИНОЛИЗ. Компоненты фибринологической системы крови: 1. Плазмин; 2. Плазминоген; 3. Активаторы плазминогена; 4. Ингибиторы плазминогена;
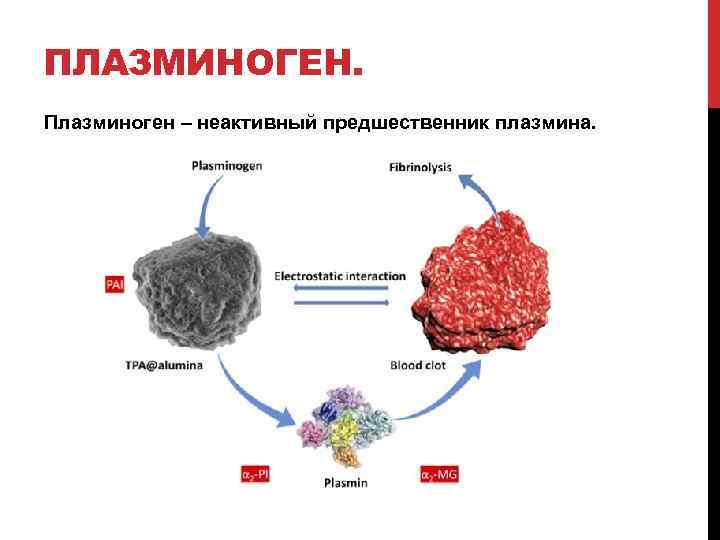 ПЛАЗМИНОГЕН. Плазминоген – неактивный предшественник плазмина.
ПЛАЗМИНОГЕН. Плазминоген – неактивный предшественник плазмина.
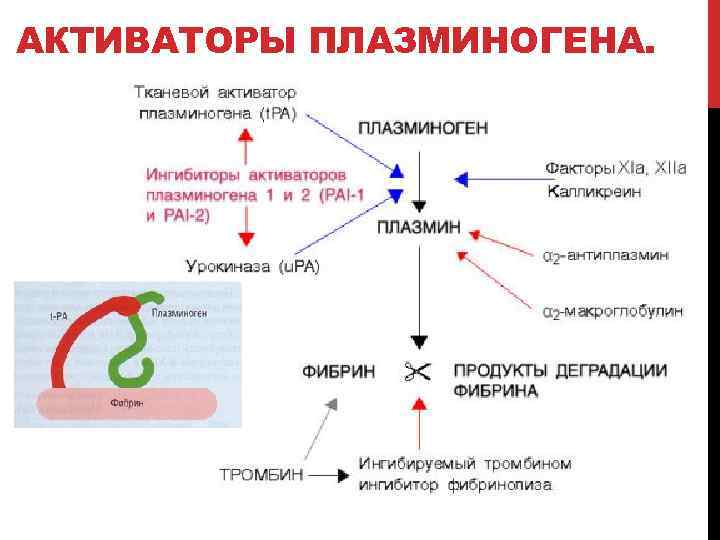 АКТИВАТОРЫ ПЛАЗМИНОГЕНА.
АКТИВАТОРЫ ПЛАЗМИНОГЕНА.
 ИНГИБИТОРЫ ПЛАЗМИНОГЕНА. Альфа 2 -антиплазмин (αг-АП). В физиологических условиях быстро инактивирует плазмин, образуя неактивные комплексы. Альфа 2 АП имеет высокое сродство к плазмину, взаимодействует с ним, уда ляя свободный плазмин из системы циркуляции. В результате время полужизни свободного плазмина составляет всего 0, 1 секунды. Если же плаз мин успевает соединиться с выпавшим фибрином, то взаимодействие плазмин αг АП резко снижа ется (примерно в 50 раз). Недостаточность αг АП проявляется кровотечениями, так как накаплива ющийся активный плазмин ускоренно разруша ет фибрин и фибриноген. αг АП белок острой фазы, однако при массивной активации фибри нолиза, в частности при ДВС синдроме, может на блюдаться истощение αг АП. Приобретенная не достаточность αг АП встречается значительно чаще, чем врожденная.
ИНГИБИТОРЫ ПЛАЗМИНОГЕНА. Альфа 2 -антиплазмин (αг-АП). В физиологических условиях быстро инактивирует плазмин, образуя неактивные комплексы. Альфа 2 АП имеет высокое сродство к плазмину, взаимодействует с ним, уда ляя свободный плазмин из системы циркуляции. В результате время полужизни свободного плазмина составляет всего 0, 1 секунды. Если же плаз мин успевает соединиться с выпавшим фибрином, то взаимодействие плазмин αг АП резко снижа ется (примерно в 50 раз). Недостаточность αг АП проявляется кровотечениями, так как накаплива ющийся активный плазмин ускоренно разруша ет фибрин и фибриноген. αг АП белок острой фазы, однако при массивной активации фибри нолиза, в частности при ДВС синдроме, может на блюдаться истощение αг АП. Приобретенная не достаточность αг АП встречается значительно чаще, чем врожденная.
 Альфа 2 -макроглобулин. Это неспецифический ингибитор. При актива ции фибринолиза образующийся из плазминогена (концентрация в плазме свыше 1, 5 мкмоль) плаз мин в первую очередь связывается αг антиплазмином (концентрация в плазме около 1 мкмоль). Пос ле олного насыщения αг антиплазмина дальней шая п нейтрализация плазмина осуществляется за счет αг макроглобулина. Кроме того, а 2 -макроглобулин инактивирует другие ферменты системы фибринолиза: урокиназу (u РА), тканевой ак тиватор плазминогена (t PA), плазменный калликреин, компоненты комплемента, бактериальные и лейкоцитарные протеазы, такие, как эластаза и катепсины.
Альфа 2 -макроглобулин. Это неспецифический ингибитор. При актива ции фибринолиза образующийся из плазминогена (концентрация в плазме свыше 1, 5 мкмоль) плаз мин в первую очередь связывается αг антиплазмином (концентрация в плазме около 1 мкмоль). Пос ле олного насыщения αг антиплазмина дальней шая п нейтрализация плазмина осуществляется за счет αг макроглобулина. Кроме того, а 2 -макроглобулин инактивирует другие ферменты системы фибринолиза: урокиназу (u РА), тканевой ак тиватор плазминогена (t PA), плазменный калликреин, компоненты комплемента, бактериальные и лейкоцитарные протеазы, такие, как эластаза и катепсины.
 Альфа 1 -антитрипсин. На его долю приходится бо лее 80% антипротеазной активности крови. В сы воротке 1 антитрипсин содержится в концентра ции 1, 4 3, 2 г/л, α или около 52 ммоль/л. Это основ ной ингибитор сериновых протеаз: трипсина, химотрипсина. Помимо этого, он принимает учас тие в инактивации плазмина, калликреина, рени на, урокиназы. Благодаря небольшим размерам он может проникать и функционировать в тканях (легкие, бронхи). А 1 антитрипсин белок острой фазы, его выработка увеличивается при реакциях, запускаемых через фактор некроза опухолей, ин терлейкин 1, интерлейкин 6, а также при высокой концентрации эстрогена в сыворотке в последнем триместре беременности, приеме эстрогенсодержащих противозачаточных препаратов.
Альфа 1 -антитрипсин. На его долю приходится бо лее 80% антипротеазной активности крови. В сы воротке 1 антитрипсин содержится в концентра ции 1, 4 3, 2 г/л, α или около 52 ммоль/л. Это основ ной ингибитор сериновых протеаз: трипсина, химотрипсина. Помимо этого, он принимает учас тие в инактивации плазмина, калликреина, рени на, урокиназы. Благодаря небольшим размерам он может проникать и функционировать в тканях (легкие, бронхи). А 1 антитрипсин белок острой фазы, его выработка увеличивается при реакциях, запускаемых через фактор некроза опухолей, ин терлейкин 1, интерлейкин 6, а также при высокой концентрации эстрогена в сыворотке в последнем триместре беременности, приеме эстрогенсодержащих противозачаточных препаратов.
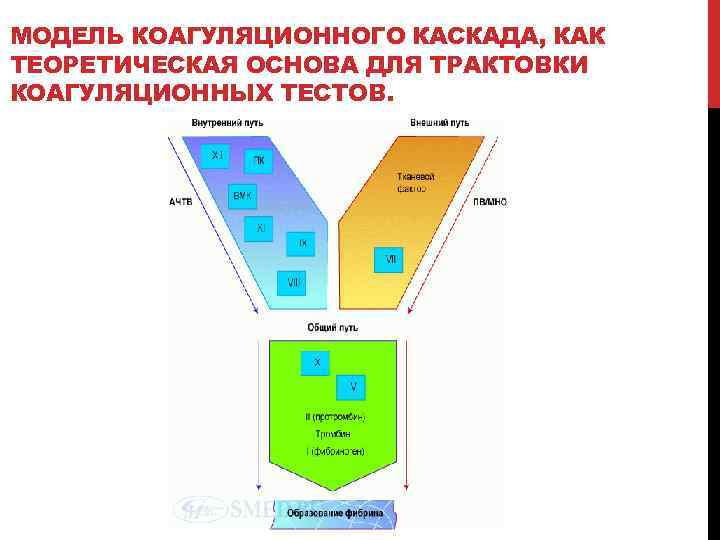 МОДЕЛЬ КОАГУЛЯЦИОННОГО КАСКАДА, КАК ТЕОРЕТИЧЕСКАЯ ОСНОВА ДЛЯ ТРАКТОВКИ КОАГУЛЯЦИОННЫХ ТЕСТОВ.
МОДЕЛЬ КОАГУЛЯЦИОННОГО КАСКАДА, КАК ТЕОРЕТИЧЕСКАЯ ОСНОВА ДЛЯ ТРАКТОВКИ КОАГУЛЯЦИОННЫХ ТЕСТОВ.
 ЛАБОРАТОРНАЯ ДИАГНОСТИКА СИСТЕМЫ ГЕМОСТАЗА Скрининговые, «глобальные» тесты Уточняющие, «локальные» (специфические) тесты Характеризуют результат работы всего каскада свертывания. Они подходят для диагностики общего состояния свертывающей системы крови и выраженности патологий, с одновременным учтом всех привходящих факторов влияний. Глобальные методы играют ключевую роль на первой стадии диагностики: они дают интегральную картину происходящих изменений в свертывающей системе и позволяют предсказывать тенденцию к гипер- или гипокоагуляции в целом. Характеризуют результат работы отдельных звеньев каскада свертывающей системы крови, а также отдельных факторов свертывания. Они незаменимы для возможного уточнения локализации патологии с точностью до фактора свертывания. 1. 2. 3. 4. 5. 6. 7. 1. 2. 3. Время кровотечения Количество тромбоцитов АЧТВ ПВ ТВ Концентрация фибриногена РФМК Агрегация тромбоцитов Активность фактора Виллебранда Д-димер
ЛАБОРАТОРНАЯ ДИАГНОСТИКА СИСТЕМЫ ГЕМОСТАЗА Скрининговые, «глобальные» тесты Уточняющие, «локальные» (специфические) тесты Характеризуют результат работы всего каскада свертывания. Они подходят для диагностики общего состояния свертывающей системы крови и выраженности патологий, с одновременным учтом всех привходящих факторов влияний. Глобальные методы играют ключевую роль на первой стадии диагностики: они дают интегральную картину происходящих изменений в свертывающей системе и позволяют предсказывать тенденцию к гипер- или гипокоагуляции в целом. Характеризуют результат работы отдельных звеньев каскада свертывающей системы крови, а также отдельных факторов свертывания. Они незаменимы для возможного уточнения локализации патологии с точностью до фактора свертывания. 1. 2. 3. 4. 5. 6. 7. 1. 2. 3. Время кровотечения Количество тромбоцитов АЧТВ ПВ ТВ Концентрация фибриногена РФМК Агрегация тромбоцитов Активность фактора Виллебранда Д-димер
 ЦЕЛИ ИССЛЕДОВАНИЯ ГЕМОСТАЗА 1. При наличии клинических проявлений – диагностика, определение причин нарушений гемостаза. 2. Перед инвазивной процедурой (операция и другое) – оценка риска кровотечения или тромбоза. 3. Контроль лечения препаратами, влияющими на гемостаз (антикоагулянты прямого и непрямого действия, тромболитические и анти. ТЦ препараты, ингибиторы протеаз и проч. ) Важен клинический этап – определение склонности к геморрагиям или тромбозам.
ЦЕЛИ ИССЛЕДОВАНИЯ ГЕМОСТАЗА 1. При наличии клинических проявлений – диагностика, определение причин нарушений гемостаза. 2. Перед инвазивной процедурой (операция и другое) – оценка риска кровотечения или тромбоза. 3. Контроль лечения препаратами, влияющими на гемостаз (антикоагулянты прямого и непрямого действия, тромболитические и анти. ТЦ препараты, ингибиторы протеаз и проч. ) Важен клинический этап – определение склонности к геморрагиям или тромбозам.
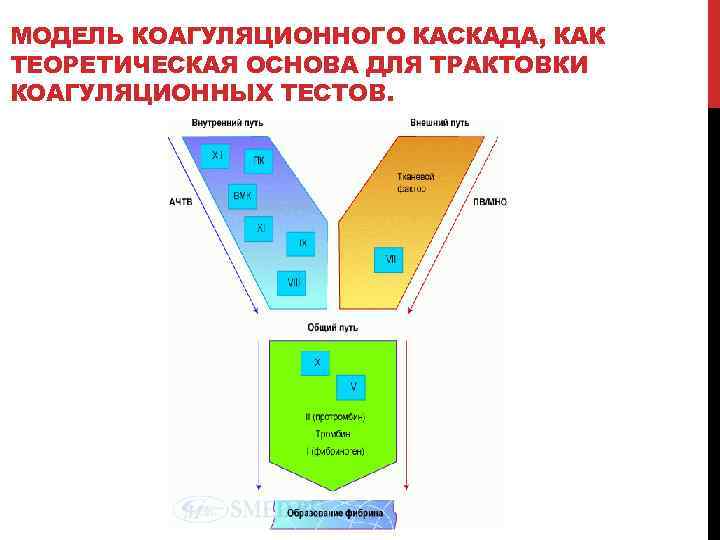 МОДЕЛЬ КОАГУЛЯЦИОННОГО КАСКАДА, КАК ТЕОРЕТИЧЕСКАЯ ОСНОВА ДЛЯ ТРАКТОВКИ КОАГУЛЯЦИОННЫХ ТЕСТОВ.
МОДЕЛЬ КОАГУЛЯЦИОННОГО КАСКАДА, КАК ТЕОРЕТИЧЕСКАЯ ОСНОВА ДЛЯ ТРАКТОВКИ КОАГУЛЯЦИОННЫХ ТЕСТОВ.
 ПЕРВИЧНЫЙ СКРИНИНГ НАРУШЕНИЙ ГЕМОСТАЗА Гемостазиограмма (коагулограмма), скрининг Это базовый набор тестов, применяемый для скрининговой оценки состояния свертывающей системы крови. Включает следующие показатели: 1. Время кровотечения. 2. Протромбин. 3. Фибриноген. 4. АЧТВ. 5. Тромбиновое время. Данный набор коагулологических тестов обычно применяют в комплексе с общим анализом крови, включающим оценку числа тромбоцитов, эритроцитов, гемоглобина, гематокрита и пр.
ПЕРВИЧНЫЙ СКРИНИНГ НАРУШЕНИЙ ГЕМОСТАЗА Гемостазиограмма (коагулограмма), скрининг Это базовый набор тестов, применяемый для скрининговой оценки состояния свертывающей системы крови. Включает следующие показатели: 1. Время кровотечения. 2. Протромбин. 3. Фибриноген. 4. АЧТВ. 5. Тромбиновое время. Данный набор коагулологических тестов обычно применяют в комплексе с общим анализом крови, включающим оценку числа тромбоцитов, эритроцитов, гемоглобина, гематокрита и пр.

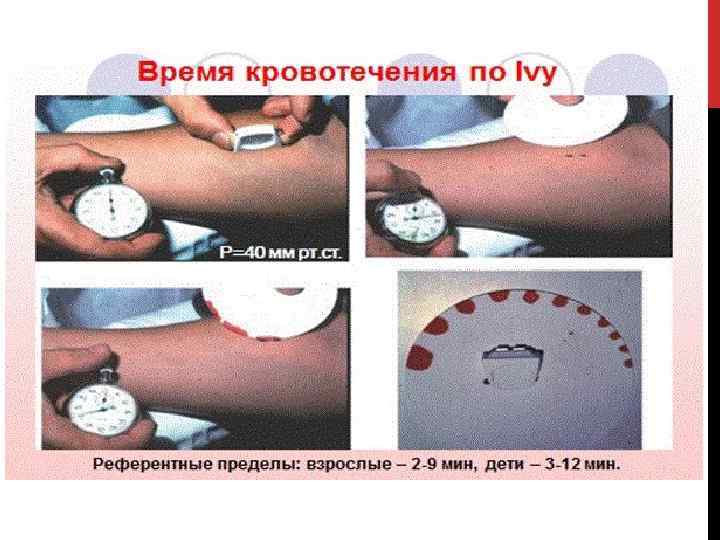
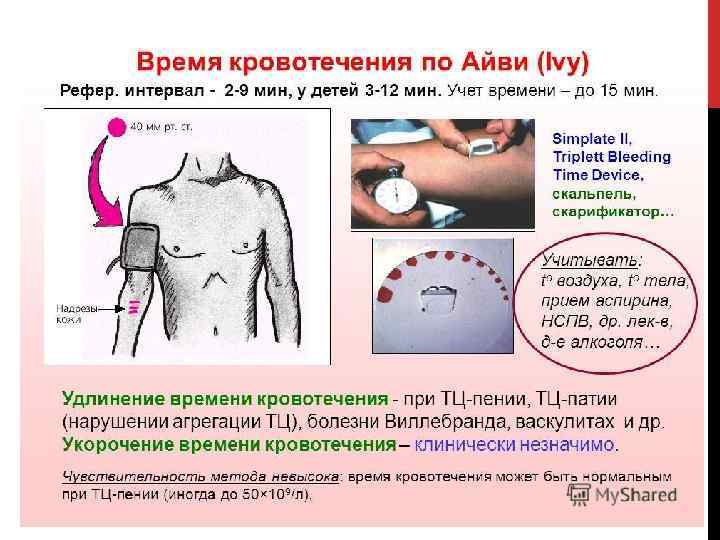
 ТЕСТЫ ТРОМБОЦИТАРНОГО ЗВЕНА. 1. Длительность кровотечения при стандартном проколе кожи по Duke, Ivy. 2. Количество тромбоцитов – в крови с ЭДТА. 3. Активность тромбоцитов – по спонтанной / индуцированной агрегации.
ТЕСТЫ ТРОМБОЦИТАРНОГО ЗВЕНА. 1. Длительность кровотечения при стандартном проколе кожи по Duke, Ivy. 2. Количество тромбоцитов – в крови с ЭДТА. 3. Активность тромбоцитов – по спонтанной / индуцированной агрегации.
 ВРЕМЯ КРОВОТЕЧЕНИЯ Время кровотечения это время от момента нанесения стандартной раны кожи до момента прекращения вытекания крови. Оно характеризует функциональную активность тромбоцитов и их взаимодействие с сосудистой стенкой. Этот скрининговый метод позволяет заподозрить тромбоцитопатии различного генеза, болезнь Виллебранда и нарушение проагрегантных свойств сосудистой стенки. После выявления удлинения или укорочения кровотечения нужно использовать более чувствительные и специфические методы. Недостатки метода: • Метод плохо стандартизируется, результаты теста позволяют лишь предположить наличие тех или иных нарушений; • Низкая чувствительность, отсутствие удлинения времени кровотечения не всегда позволяет исключить нарушения тромбоцитарного или сосудистого звеньев гемостаза; • Низкая специфичность не позволяют однозначно интерпретировать результаты; • Не соответствует современным санитарно эпидемиологическим требованиям;
ВРЕМЯ КРОВОТЕЧЕНИЯ Время кровотечения это время от момента нанесения стандартной раны кожи до момента прекращения вытекания крови. Оно характеризует функциональную активность тромбоцитов и их взаимодействие с сосудистой стенкой. Этот скрининговый метод позволяет заподозрить тромбоцитопатии различного генеза, болезнь Виллебранда и нарушение проагрегантных свойств сосудистой стенки. После выявления удлинения или укорочения кровотечения нужно использовать более чувствительные и специфические методы. Недостатки метода: • Метод плохо стандартизируется, результаты теста позволяют лишь предположить наличие тех или иных нарушений; • Низкая чувствительность, отсутствие удлинения времени кровотечения не всегда позволяет исключить нарушения тромбоцитарного или сосудистого звеньев гемостаза; • Низкая специфичность не позволяют однозначно интерпретировать результаты; • Не соответствует современным санитарно эпидемиологическим требованиям;
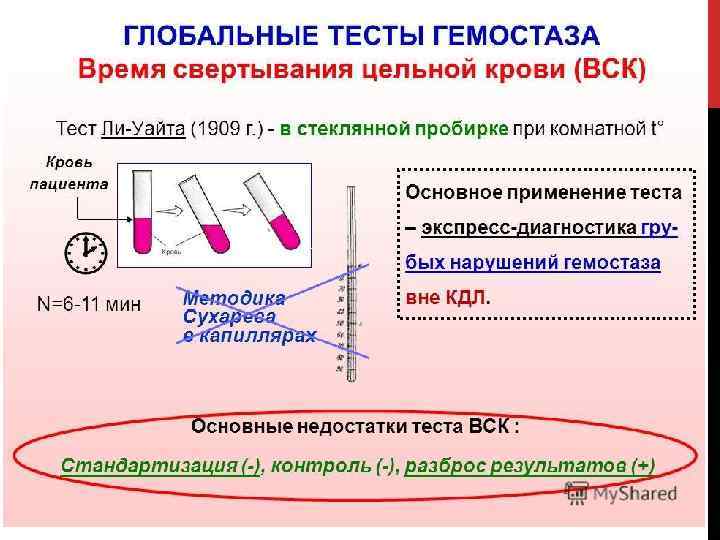
 ОПРЕДЕЛЕНИЕ ВРЕМЕНИ СВЕРТЫВАНИЯ КРОВИ 1. Метод Ли-Уайта (время свертывания венозной крови). 2. Метод Сухарева. 3. Метод Альтгаузена 4. Метод Бюркера (свертывание капиллярной крови). 5. Метод Duke. 6. Метод Ivy.
ОПРЕДЕЛЕНИЕ ВРЕМЕНИ СВЕРТЫВАНИЯ КРОВИ 1. Метод Ли-Уайта (время свертывания венозной крови). 2. Метод Сухарева. 3. Метод Альтгаузена 4. Метод Бюркера (свертывание капиллярной крови). 5. Метод Duke. 6. Метод Ivy.
 Если первоначально для точной оценки характеристик свертываемости крови применялось более тридцати различных методик, то в наше время из них сохранилось только две: 1. Метод Сухарева. Свертывание крови по Сухареву проводится для крови из капилляров (забор из пальца). 2. Способ Ли-Уайта. Исследование по Ли Уайте – для венозной крови (проба берется из вены).
Если первоначально для точной оценки характеристик свертываемости крови применялось более тридцати различных методик, то в наше время из них сохранилось только две: 1. Метод Сухарева. Свертывание крови по Сухареву проводится для крови из капилляров (забор из пальца). 2. Способ Ли-Уайта. Исследование по Ли Уайте – для венозной крови (проба берется из вены).
 МЕТОД СУХАРЕВА Методика: набирают в капилляр столбик крови высотой 25 30 мм, отмечают по секундомеру время. Наклоном капилляра переводят кровь на середину капилляра. Держа капилляр двумя пальцами, покачивают его на 30 45 градусов в обе стороны. Начало свертывания крови характеризуется замедлением движения крови при наклоне капилляра. Полное свертывание крови соответствует моменту полной остановки движения крови. В норме показатели свертывания крови должны быть такими: • Начало свертывания – от 30 секунд до 2 минут. • Завершение процесса свертывания – от 3 до 5 минут.
МЕТОД СУХАРЕВА Методика: набирают в капилляр столбик крови высотой 25 30 мм, отмечают по секундомеру время. Наклоном капилляра переводят кровь на середину капилляра. Держа капилляр двумя пальцами, покачивают его на 30 45 градусов в обе стороны. Начало свертывания крови характеризуется замедлением движения крови при наклоне капилляра. Полное свертывание крови соответствует моменту полной остановки движения крови. В норме показатели свертывания крови должны быть такими: • Начало свертывания – от 30 секунд до 2 минут. • Завершение процесса свертывания – от 3 до 5 минут.
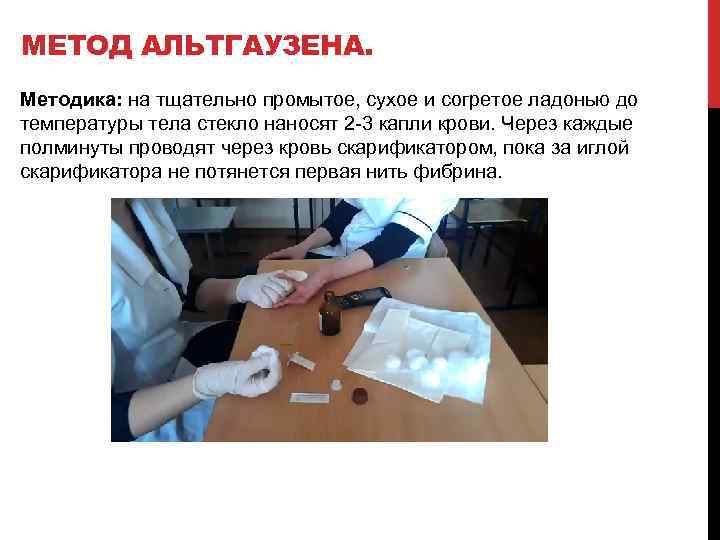 МЕТОД АЛЬТГАУЗЕНА. Методика: на тщательно промытое, сухое и согретое ладонью до температуры тела стекло наносят 2 3 капли крови. Через каждые полминуты проводят через кровь скарификатором, пока за иглой скарификатора не потянется первая нить фибрина.
МЕТОД АЛЬТГАУЗЕНА. Методика: на тщательно промытое, сухое и согретое ладонью до температуры тела стекло наносят 2 3 капли крови. Через каждые полминуты проводят через кровь скарификатором, пока за иглой скарификатора не потянется первая нить фибрина.


 КОЛИЧЕСТВО ТРОМБОЦИТОВ.
КОЛИЧЕСТВО ТРОМБОЦИТОВ.
 МЕТОДЫ ИССЛЕДОВАНИЯ КОАГУЛЯЦИОННОГО ГЕМОСТАЗА Основу современного исследования плазменного гемостаза составляют 4 базовых теста: 1. Протромбиновый тест 2. Активированное частичное тромбопластиновое время 3. Тромбиновое время 4. Количественное определение фибриногена
МЕТОДЫ ИССЛЕДОВАНИЯ КОАГУЛЯЦИОННОГО ГЕМОСТАЗА Основу современного исследования плазменного гемостаза составляют 4 базовых теста: 1. Протромбиновый тест 2. Активированное частичное тромбопластиновое время 3. Тромбиновое время 4. Количественное определение фибриногена
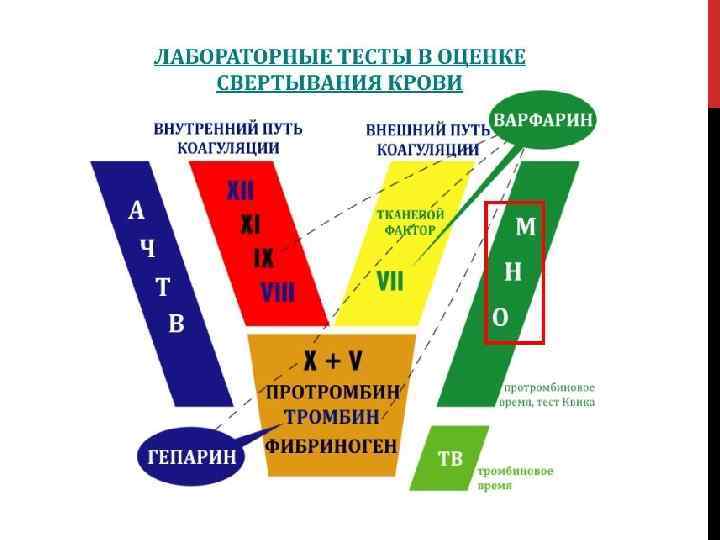
 ПРОТРОМБИНОВЫЙ ТЕСТ ПТ — один из наиболее часто выполняемых коагулологических анализов. Он был предложен А. Квиком и соавт. в 1935 г. , и его часто называют по имени первого из авторов методики тестом Квика. Протромбиновый тест — высокочувствительный и простой скрининговый тест, позволяющий выявить нарушения во внешнем пути свёртывания крови (ф. 2, 5, 7, 10) и рекомендуется для: мониторинга терапии непрямыми антикоагулянтами; диагностики наследственных и приобретённых коагулопатий; диагностики заболеваний печени. Результаты протромбинового теста могут быть представлены в различной форме: 1. Протромбиновое время 2. Протромбиновый индекс 3. Протромбин по Квику 4. МНО
ПРОТРОМБИНОВЫЙ ТЕСТ ПТ — один из наиболее часто выполняемых коагулологических анализов. Он был предложен А. Квиком и соавт. в 1935 г. , и его часто называют по имени первого из авторов методики тестом Квика. Протромбиновый тест — высокочувствительный и простой скрининговый тест, позволяющий выявить нарушения во внешнем пути свёртывания крови (ф. 2, 5, 7, 10) и рекомендуется для: мониторинга терапии непрямыми антикоагулянтами; диагностики наследственных и приобретённых коагулопатий; диагностики заболеваний печени. Результаты протромбинового теста могут быть представлены в различной форме: 1. Протромбиновое время 2. Протромбиновый индекс 3. Протромбин по Квику 4. МНО
 ПРОТРОМБИНОВОЕ ВРЕМЯ Исследование протромбинового времени представляет важнейший скрининговый тест для оценки системы свертывания крови. Определяют время образования фибринового сгустка в бедной тромбоцитами цитратной плазме при активации внешнего пути гемостаза тканевым тромбопластином, содержащим тканевый фактор и фосфолипиды, в присутствии ионов Са 2+ при 37 °С. Источником тромбопластина могут быть эритроциты, ткани мозга или другие ткани; может быть использован и рекомбинантный тромбопластин. Возможно определение протромбинового времени цельной крови на портативных коагулометрах со специальными картриджами. ПТВ позволяет оценить активность факторов свертывания I, II, V, VII и X.
ПРОТРОМБИНОВОЕ ВРЕМЯ Исследование протромбинового времени представляет важнейший скрининговый тест для оценки системы свертывания крови. Определяют время образования фибринового сгустка в бедной тромбоцитами цитратной плазме при активации внешнего пути гемостаза тканевым тромбопластином, содержащим тканевый фактор и фосфолипиды, в присутствии ионов Са 2+ при 37 °С. Источником тромбопластина могут быть эритроциты, ткани мозга или другие ткани; может быть использован и рекомбинантный тромбопластин. Возможно определение протромбинового времени цельной крови на портативных коагулометрах со специальными картриджами. ПТВ позволяет оценить активность факторов свертывания I, II, V, VII и X.
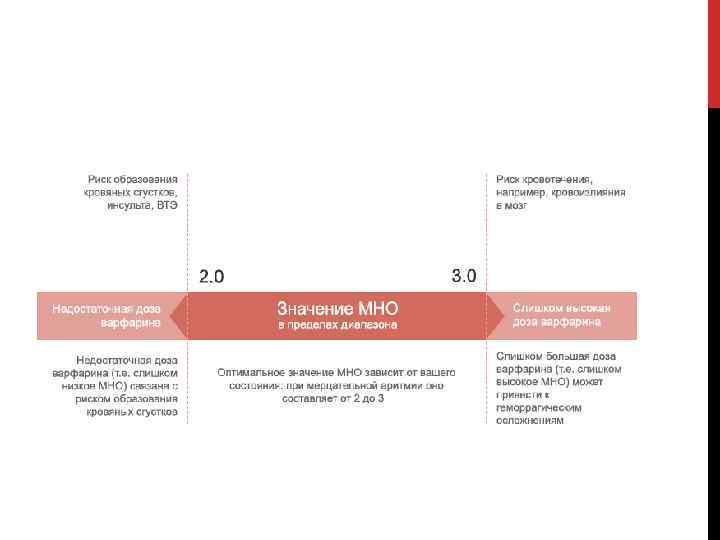
 Нормальный показатель протромбинового времени — 11 16 секунд, для МНО — 0, 85 1, 35. При терапии пероральными антикоагулянтами (варфарином) требуется более высокий целевой уровень МНО — обычно в диапазоне 2 3.
Нормальный показатель протромбинового времени — 11 16 секунд, для МНО — 0, 85 1, 35. При терапии пероральными антикоагулянтами (варфарином) требуется более высокий целевой уровень МНО — обычно в диапазоне 2 3.
 ТРОМБИНОВОЕ ВРЕМЯ. Один из базовых (скрининговых) тестов — тромбиновое время — предназначен для оценки конечного этапа свертывания крови, т. е. скорости превращения фибриногена в фибрин, для определения функциональной активности фибриногена и ингибиторов тромбина в плазме, таких как: • продукты деградации фибрина/фибриногена; • гепарин и гепариноиды; • при фибринолитической терапии. Определение тромбинового времени используется для контроля за гепаринотерапией и фибринолитической терапией, для диагностики активации фибринолиза.
ТРОМБИНОВОЕ ВРЕМЯ. Один из базовых (скрининговых) тестов — тромбиновое время — предназначен для оценки конечного этапа свертывания крови, т. е. скорости превращения фибриногена в фибрин, для определения функциональной активности фибриногена и ингибиторов тромбина в плазме, таких как: • продукты деградации фибрина/фибриногена; • гепарин и гепариноиды; • при фибринолитической терапии. Определение тромбинового времени используется для контроля за гепаринотерапией и фибринолитической терапией, для диагностики активации фибринолиза.
 Нормальная область времени свертывания составляет при активности тромбина 9 МЕ/мл — 7– 9 сек. при активности тромбина 6 МЕ/мл — 9– 12 сек; при активности тромбина 3 МЕ/мл — 15– 20 сек;
Нормальная область времени свертывания составляет при активности тромбина 9 МЕ/мл — 7– 9 сек. при активности тромбина 6 МЕ/мл — 9– 12 сек; при активности тромбина 3 МЕ/мл — 15– 20 сек;
 АЧТВ Активированное частичное тромбопластиновое время (АЧТВ) является показателем измерения эффективности «внутреннего» (путь контактной активации) и общего пути свертывания. Помимо выявления нарушений в процессе свертывания крови , АЧТВ также используется для контроля эффективности лечения гепарином, основным антикоагулянтом. Тест используется в сочетании с тестом протромбинового времени (ПВ), который измеряет внешний путь свертываемости. Для нормального АЧТВ требуется наличие следующих факторов свертывания крови: I, II, V, VIII, IX, X , XI и XII. Примечательно, что тест АЧТВ не диагностирует недостатки в VII или XIII факторах.
АЧТВ Активированное частичное тромбопластиновое время (АЧТВ) является показателем измерения эффективности «внутреннего» (путь контактной активации) и общего пути свертывания. Помимо выявления нарушений в процессе свертывания крови , АЧТВ также используется для контроля эффективности лечения гепарином, основным антикоагулянтом. Тест используется в сочетании с тестом протромбинового времени (ПВ), который измеряет внешний путь свертываемости. Для нормального АЧТВ требуется наличие следующих факторов свертывания крови: I, II, V, VIII, IX, X , XI и XII. Примечательно, что тест АЧТВ не диагностирует недостатки в VII или XIII факторах.
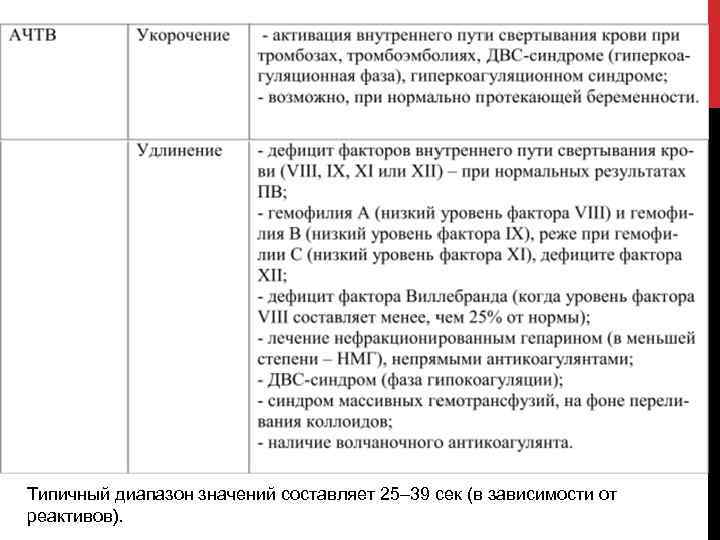 Типичный диапазон значений составляет 25– 39 сек (в зависимости от реактивов).
Типичный диапазон значений составляет 25– 39 сек (в зависимости от реактивов).
 ФИБРИНОГЕН. Определение содержания фибриногена в плазме крови человека является одним из основных тестов при исследовании гемостаза. Данный скрининговый тест предназначен для измерения содержания фибриногена в плазме при гиперфибриногенемии, которая связана с тяжестью воспалительных, иммунных, деструктивных процессов, а также является одним из факторов повышенного риска развития гипервискозного синдрома, артериальных тромбозов и инфарктов органов, а также при остром ДВС синдроме, при лечении фибринолитиками, при врожденных гипо и дисфибриногенемиях.
ФИБРИНОГЕН. Определение содержания фибриногена в плазме крови человека является одним из основных тестов при исследовании гемостаза. Данный скрининговый тест предназначен для измерения содержания фибриногена в плазме при гиперфибриногенемии, которая связана с тяжестью воспалительных, иммунных, деструктивных процессов, а также является одним из факторов повышенного риска развития гипервискозного синдрома, артериальных тромбозов и инфарктов органов, а также при остром ДВС синдроме, при лечении фибринолитиками, при врожденных гипо и дисфибриногенемиях.
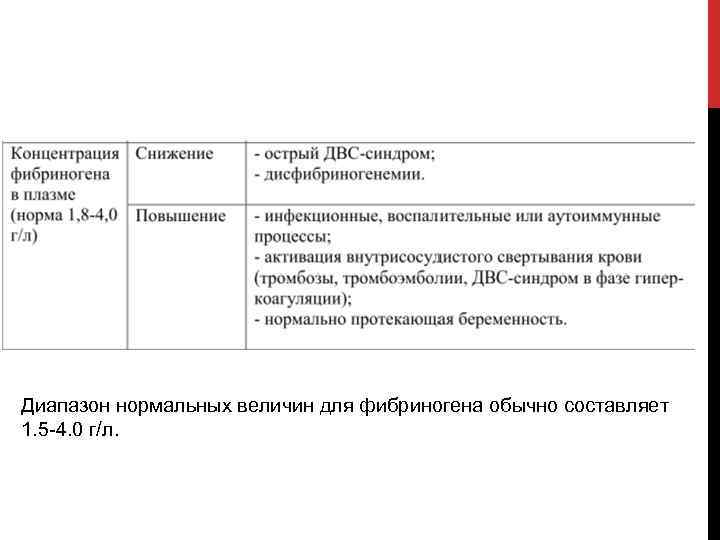 Диапазон нормальных величин для фибриногена обычно составляет 1. 5 4. 0 г/л.
Диапазон нормальных величин для фибриногена обычно составляет 1. 5 4. 0 г/л.
 СНИЖЕНИЕ УРОВНЯ ФИБРИНОГЕНА НАБЛЮДАЕТСЯ: — при ДВС-синдроме в стадии потребления (чаще в сочетании с удлинением АЧТВ, ПВ, ТВ и др. ), — при заболеваниях печени из-за снижения синтеза факторов свертывания крови, — при массивных переливаниях крови, приводящих к дилюционной коагулопатии, — после проведения тромболитической терапии, — при наследственном дефиците фибриногена (гипо- или афибриногенемии) или при дисфибриногенемии, которая часто ассоциируется со снижением уровня фибриногена. Дисфибриногенемия может также встречаться у пациентов с заболеваниями печени, связанными с аномальным увеличением содержание сиаловой кислоты.
СНИЖЕНИЕ УРОВНЯ ФИБРИНОГЕНА НАБЛЮДАЕТСЯ: — при ДВС-синдроме в стадии потребления (чаще в сочетании с удлинением АЧТВ, ПВ, ТВ и др. ), — при заболеваниях печени из-за снижения синтеза факторов свертывания крови, — при массивных переливаниях крови, приводящих к дилюционной коагулопатии, — после проведения тромболитической терапии, — при наследственном дефиците фибриногена (гипо- или афибриногенемии) или при дисфибриногенемии, которая часто ассоциируется со снижением уровня фибриногена. Дисфибриногенемия может также встречаться у пациентов с заболеваниями печени, связанными с аномальным увеличением содержание сиаловой кислоты.
 ПОВЫШЕНИЕ УРОВНЯ ФИБРИНОГЕНА НАБЛЮДАЕТСЯ: — у здорового человека по после 60 лет, при беременности, приеме пероральных контрацептивов, в период постменопаузы; — у курильщиков; — во время операции и в послеоперационном периоде; — при ожирении, сахарном диабете, атеросклеротическом поражении сосудов; — при ИБС, особенно при инфаркте миокарда; — при ДВС синдроме (в стадии гиперкоагуляции — чаще в сочетании с укорочением АЧТВ, ПВ, ТВ и др. ), при тромбозе сосудов; — при онкологических, инфекционных, воспалительных, аутоиммунных и других состояниях. Высокий уровень фибриногена в крови – независимый фактор тромбогенного риска. Повышение концентрации фибриногена выше 4, 5 г/л является прогностическим показателем развития инфаркта миокарда, инсульта, заболеваний периферических артерий.
ПОВЫШЕНИЕ УРОВНЯ ФИБРИНОГЕНА НАБЛЮДАЕТСЯ: — у здорового человека по после 60 лет, при беременности, приеме пероральных контрацептивов, в период постменопаузы; — у курильщиков; — во время операции и в послеоперационном периоде; — при ожирении, сахарном диабете, атеросклеротическом поражении сосудов; — при ИБС, особенно при инфаркте миокарда; — при ДВС синдроме (в стадии гиперкоагуляции — чаще в сочетании с укорочением АЧТВ, ПВ, ТВ и др. ), при тромбозе сосудов; — при онкологических, инфекционных, воспалительных, аутоиммунных и других состояниях. Высокий уровень фибриногена в крови – независимый фактор тромбогенного риска. Повышение концентрации фибриногена выше 4, 5 г/л является прогностическим показателем развития инфаркта миокарда, инсульта, заболеваний периферических артерий.


