Геморрагические лихорадки.ppt
- Количество слайдов: 66
 Геморрагические лихорадки
Геморрагические лихорадки
 Геморрагические лихорадки. o o Геморрагические лихорадки острые, природно очаговые инфекционные заболевания вирусной этиологии, характеризующиеся токсикозом, лихорадкой и геморрагическим синдромом. Встречаются в виде отдельных случаев или небольших вспышек в сельской местности, особенно в районах, недостаточно освоенных человеком.
Геморрагические лихорадки. o o Геморрагические лихорадки острые, природно очаговые инфекционные заболевания вирусной этиологии, характеризующиеся токсикозом, лихорадкой и геморрагическим синдромом. Встречаются в виде отдельных случаев или небольших вспышек в сельской местности, особенно в районах, недостаточно освоенных человеком.
 ЭТИОЛОГИЯ o Возбудители относятся к группе арбовирусов, к семейству бунья вирусов (Bunyaviridae) и принадлежит к самостоятельному роду Hantavirus. резервуаром которых являются преимущественно мышевидные грызуны и иксодовые клещи.
ЭТИОЛОГИЯ o Возбудители относятся к группе арбовирусов, к семейству бунья вирусов (Bunyaviridae) и принадлежит к самостоятельному роду Hantavirus. резервуаром которых являются преимущественно мышевидные грызуны и иксодовые клещи.
 ХАРАКТЕРИСТИКА ВОЗБУДИТЕЛЯ o Возбудитель сферической формы, 85 110 нм диаметром. Геном вируса состоит из трех сегментов: L , М , S одноцепочечной РНК, включает 4 полипептида: нуклеокапсида (N), гликопротеины мембраны (G 1 и G 2), РНК полимеразу. Размножается в цитоплазме инфицированных клеток. Хантавирусы способны инфицировать моноциты, клетки легких, почек, печени, слюнных желез, не вызывают цитолиза эндотелиальных клеток, поражение которых обусловлено иммунными механизмами (Алексеев О. А. и др. , 1998)
ХАРАКТЕРИСТИКА ВОЗБУДИТЕЛЯ o Возбудитель сферической формы, 85 110 нм диаметром. Геном вируса состоит из трех сегментов: L , М , S одноцепочечной РНК, включает 4 полипептида: нуклеокапсида (N), гликопротеины мембраны (G 1 и G 2), РНК полимеразу. Размножается в цитоплазме инфицированных клеток. Хантавирусы способны инфицировать моноциты, клетки легких, почек, печени, слюнных желез, не вызывают цитолиза эндотелиальных клеток, поражение которых обусловлено иммунными механизмами (Алексеев О. А. и др. , 1998)
 УСТОЙЧИВОСТЬ ВИРУСА o Вирус ГЛПС сохраняется во внешней среде при температуре от +4° до +20°С. В сыворотке крови, сохраняется свыше 4 суток при +4°С. Инактивируется при температуре +50°С в течение 30 мин. Хорошо сохраняется при температуре ниже 20°С. Вирус кислотолабилен полностью инактивируется при р. Н ниже 5, 0. Чувствителен к эфиру, хлороформу, ацетону, бензолу, дезоксихолату натрия, ультрафиолетовым лучам.
УСТОЙЧИВОСТЬ ВИРУСА o Вирус ГЛПС сохраняется во внешней среде при температуре от +4° до +20°С. В сыворотке крови, сохраняется свыше 4 суток при +4°С. Инактивируется при температуре +50°С в течение 30 мин. Хорошо сохраняется при температуре ниже 20°С. Вирус кислотолабилен полностью инактивируется при р. Н ниже 5, 0. Чувствителен к эфиру, хлороформу, ацетону, бензолу, дезоксихолату натрия, ультрафиолетовым лучам.
 КЛАССИФИКАЦИЯ ГЕМОРРАГИЧЕСКИХ ЛИХОРАДОК • ЖЕЛТАЯ ЛИХОРАДКА • ДЕНГЕ • ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА С ПОЧЕЧНЫМ СИНДРОМОМ • ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА • БОЛЕЗНЬ КЬЯСАНУРСКОГО ЛЕСА • ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА КРЫМ-КОНГО • ЛИХОРАДКА ЛАCСА • ЛИХОРАДКА МАРБУРГ • ЛИХОРАДКА ЭБОЛА • АРГЕНТИНСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА • БОЛИВИАНСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
КЛАССИФИКАЦИЯ ГЕМОРРАГИЧЕСКИХ ЛИХОРАДОК • ЖЕЛТАЯ ЛИХОРАДКА • ДЕНГЕ • ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА С ПОЧЕЧНЫМ СИНДРОМОМ • ОМСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА • БОЛЕЗНЬ КЬЯСАНУРСКОГО ЛЕСА • ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА КРЫМ-КОНГО • ЛИХОРАДКА ЛАCСА • ЛИХОРАДКА МАРБУРГ • ЛИХОРАДКА ЭБОЛА • АРГЕНТИНСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА • БОЛИВИАНСКАЯ ГЕМОРРАГИЧЕСКАЯ ЛИХОРАДКА
 Геморрагическая лихорадка с почечным синдромом (ГЛПС) o острое вирусное природно очаговое заболевание, характеризующееся системным по ражением мелких сосудов, геморрагическим диатезом, гемодинамическими расстройствами и своеобразным поражением почек по типу острого интерстициального нефрита с развитием острой почечной недостаточности. ГЛПС является наиболее распространенной на территории Российской Федерации природно очаговой инфекцией. Заболевание нередко протекает с опасными для жизни осложнениями, инфекционно токсическим шоком (ИТШ), острой почечной недостаточности (ОПН), кровоизлияниями в жизненно важные органы, ДВС синдромом, спон танными разрывами почек и др. Летальность составляет до 1 2% в европейских и до 5 10% в дальнево сточных регионах России (Ткаченко Е. А. , 2000). В РБ на протяжении последних летальность не превышает 0, 3 0, 5%, но вследствие высокой заболе ваемости остается значительной. По данным отделения гемодиализа РКБ им. Г. Куватова остается достаточно высокой 2, 6% (Загидуллин И. М. с соавт. , 1999).
Геморрагическая лихорадка с почечным синдромом (ГЛПС) o острое вирусное природно очаговое заболевание, характеризующееся системным по ражением мелких сосудов, геморрагическим диатезом, гемодинамическими расстройствами и своеобразным поражением почек по типу острого интерстициального нефрита с развитием острой почечной недостаточности. ГЛПС является наиболее распространенной на территории Российской Федерации природно очаговой инфекцией. Заболевание нередко протекает с опасными для жизни осложнениями, инфекционно токсическим шоком (ИТШ), острой почечной недостаточности (ОПН), кровоизлияниями в жизненно важные органы, ДВС синдромом, спон танными разрывами почек и др. Летальность составляет до 1 2% в европейских и до 5 10% в дальнево сточных регионах России (Ткаченко Е. А. , 2000). В РБ на протяжении последних летальность не превышает 0, 3 0, 5%, но вследствие высокой заболе ваемости остается значительной. По данным отделения гемодиализа РКБ им. Г. Куватова остается достаточно высокой 2, 6% (Загидуллин И. М. с соавт. , 1999).
 ПАТОГЕНЕЗ ГЛПС o o o o Патологический процесс развивается стадийно; различают 5 фаз: I. Заражение Внедрение вируса через слизистые оболочки дыхательных путей, пищеварительного тракта, поврежденные кожные покровы. Размножение вируса в лимфатических узлах и система мононуклеарных фагоцитов (СМФ). Перестройка реактивности организма, возможна сенсибилизация. II. Вирусемия и генерализация инфекции. Вирус оказывает инфекционно токсическое действие на рецепторы сосудов и нервную систему. Диссеминация вируса с возможным участием клеток крови и кроветворной системы. I и II фазы соответствуют инкубационному периоду заболевания. III. Токсико-аллергические и иммунологические реакции. Часть вируса захватывается клетками СМФ и удаляется из организма. Часть связывается в иммунные комплексы. При нарушении фагоцитарной активности макрофагов или при низком уровне антителообразования, ИК попадают в органы и ткани, повреждая стенки артериол и высшие вегетативные центры. Повышается активность гиалуронидазы, высвобождается гистамин и гистаминоподобные вещества, активируется калликреин кининовая система. Развивается деструктивный процесс в рыхлой соединительной ткани, нарушается проницаемость и тонус сосудов, геморрагический диатез с плазмореей в ткани, ДВС, микротромбозы.
ПАТОГЕНЕЗ ГЛПС o o o o Патологический процесс развивается стадийно; различают 5 фаз: I. Заражение Внедрение вируса через слизистые оболочки дыхательных путей, пищеварительного тракта, поврежденные кожные покровы. Размножение вируса в лимфатических узлах и система мононуклеарных фагоцитов (СМФ). Перестройка реактивности организма, возможна сенсибилизация. II. Вирусемия и генерализация инфекции. Вирус оказывает инфекционно токсическое действие на рецепторы сосудов и нервную систему. Диссеминация вируса с возможным участием клеток крови и кроветворной системы. I и II фазы соответствуют инкубационному периоду заболевания. III. Токсико-аллергические и иммунологические реакции. Часть вируса захватывается клетками СМФ и удаляется из организма. Часть связывается в иммунные комплексы. При нарушении фагоцитарной активности макрофагов или при низком уровне антителообразования, ИК попадают в органы и ткани, повреждая стенки артериол и высшие вегетативные центры. Повышается активность гиалуронидазы, высвобождается гистамин и гистаминоподобные вещества, активируется калликреин кининовая система. Развивается деструктивный процесс в рыхлой соединительной ткани, нарушается проницаемость и тонус сосудов, геморрагический диатез с плазмореей в ткани, ДВС, микротромбозы.
 ПАТОГЕНЕЗ ТРОМБОГЕМОРРАГИЧЕСКОГО СИНДРОМА o o o I. Стадия гиперкоагуляции начинается в клетках тканей поврежденного органа, что приводит к высвобождению коагуляционно активных веществ. Эта стадия обычно кратковременная. II. Стадия нарастающей коагулопатии потребления, непостоянной фибринолитической активности. Она характеризуется падением числа тромбоцитов и уровня фибриногена, а также расходом других плазменных факторов коагуляционнолитической системы организма. Это стадия начинающегося и нарастающего ДВС (неполный синдром ДВС). III. Стадия дефибриногенации и тотального, но не постоянного фибринолиза (дефибриногенационно фибринолитическая). Синоним этой стадии полный синдром ДВС. IV. Восстановительная стадия или стадия остаточных тромбозов и окклюзий. При благоприятном течении синдрома отмечается возвращение к физиологическим нормам всех факторов коагуляционнолитической системы организма 111 Фаза соответствует лихорадочному периоду болезни.
ПАТОГЕНЕЗ ТРОМБОГЕМОРРАГИЧЕСКОГО СИНДРОМА o o o I. Стадия гиперкоагуляции начинается в клетках тканей поврежденного органа, что приводит к высвобождению коагуляционно активных веществ. Эта стадия обычно кратковременная. II. Стадия нарастающей коагулопатии потребления, непостоянной фибринолитической активности. Она характеризуется падением числа тромбоцитов и уровня фибриногена, а также расходом других плазменных факторов коагуляционнолитической системы организма. Это стадия начинающегося и нарастающего ДВС (неполный синдром ДВС). III. Стадия дефибриногенации и тотального, но не постоянного фибринолиза (дефибриногенационно фибринолитическая). Синоним этой стадии полный синдром ДВС. IV. Восстановительная стадия или стадия остаточных тромбозов и окклюзий. При благоприятном течении синдрома отмечается возвращение к физиологическим нормам всех факторов коагуляционнолитической системы организма 111 Фаза соответствует лихорадочному периоду болезни.
 o o IV. Фаза висцеральных поражений и обменных нарушений. Соответствуют концу лихорадочного периода и началу олигоурического. Вирус и аутоантитела вызывают повреждение гипофиза, надпочечников, почек, миокарда. Изменения в почках сопровождается снижением клубочковой фильтрации, нарушением канальцевой реабсорбции, приводящих к олигоанурии, массивной протеинурии, азотемии, нарушениям водно электролитного баланса и кислотно основного состояния (КОС), т. е. развитием ОПН. В эту фазу возможны осложнения: острая сердечно сосудистая недостаточность, коллапс, шок, массивные кровотечения, спонтанный разрыв почек, отек легких, отек головного мозга, азотемическая уремия, паралич вегетативных центров. V. Фаза анатомической репарации, восстановление нарушенных функций, формирование стойкого иммунитета. В результате иммунных реакций и саногенных процессов патологические изменения в почках регрессируют, что сопровождается полиурией вследствие снижения реабсорбционной способности канальцев и уменьшением азотемии с постепенным восстановлением почечной функции в течение 1 4 лет.
o o IV. Фаза висцеральных поражений и обменных нарушений. Соответствуют концу лихорадочного периода и началу олигоурического. Вирус и аутоантитела вызывают повреждение гипофиза, надпочечников, почек, миокарда. Изменения в почках сопровождается снижением клубочковой фильтрации, нарушением канальцевой реабсорбции, приводящих к олигоанурии, массивной протеинурии, азотемии, нарушениям водно электролитного баланса и кислотно основного состояния (КОС), т. е. развитием ОПН. В эту фазу возможны осложнения: острая сердечно сосудистая недостаточность, коллапс, шок, массивные кровотечения, спонтанный разрыв почек, отек легких, отек головного мозга, азотемическая уремия, паралич вегетативных центров. V. Фаза анатомической репарации, восстановление нарушенных функций, формирование стойкого иммунитета. В результате иммунных реакций и саногенных процессов патологические изменения в почках регрессируют, что сопровождается полиурией вследствие снижения реабсорбционной способности канальцев и уменьшением азотемии с постепенным восстановлением почечной функции в течение 1 4 лет.
 КЛИНИКА Выделяют 4 периода болезни: 1 Начальный, или лихорадочный (1 4 дня) 2 Олигоанурический (с 5 6 по 10 12 день) 3 Полиурический, ранней реконвалесценции (с 22 дня болезни). ГЛПС протекает в тяжелой, среднетяжелой, легкой и стертой формах.
КЛИНИКА Выделяют 4 периода болезни: 1 Начальный, или лихорадочный (1 4 дня) 2 Олигоанурический (с 5 6 по 10 12 день) 3 Полиурический, ранней реконвалесценции (с 22 дня болезни). ГЛПС протекает в тяжелой, среднетяжелой, легкой и стертой формах.
 Инкубационный период o продолжается от 4 до 49 дней (чаще всего от 14 до 21 дня). Иногда наблюдаются продромальные явления ( 2 3 дня) в виде недомогания, утомляемости, головной боли, миалгий и субфебрилитета.
Инкубационный период o продолжается от 4 до 49 дней (чаще всего от 14 до 21 дня). Иногда наблюдаются продромальные явления ( 2 3 дня) в виде недомогания, утомляемости, головной боли, миалгий и субфебрилитета.
 Начальный период o 5 6 дней характеризуется острым началом, повышением температуры до 38 40°С. Появляется головная боль, слабость, сухость во рту, снижение аппетита, тошнота, ломота в теле. Характерными являются жалобы на боли в глазных яблоках и снижение остроты зрения ( «туман» перед глазами, «мушки» ), которые бывают кратковременными и бесследно исчезают через 1 5 дней. Возможны кровянистые выделения из носа, образование геморрагических «корочек» в носовых ходах. У тяжелых больных в этот период присоединяются боли в пояснице и животе, рвота, макрогематурия, олигоанурия.
Начальный период o 5 6 дней характеризуется острым началом, повышением температуры до 38 40°С. Появляется головная боль, слабость, сухость во рту, снижение аппетита, тошнота, ломота в теле. Характерными являются жалобы на боли в глазных яблоках и снижение остроты зрения ( «туман» перед глазами, «мушки» ), которые бывают кратковременными и бесследно исчезают через 1 5 дней. Возможны кровянистые выделения из носа, образование геморрагических «корочек» в носовых ходах. У тяжелых больных в этот период присоединяются боли в пояснице и животе, рвота, макрогематурия, олигоанурия.
 Начальный период o Отмечается гиперемия кожи лица, шеи, верхних отделов груди. Слизистая оболочка зева гиперемирована, сосуды склер инъецированы, гиперемия конъюнктив, геморрагическая сыпь. Со 2 3 го дня болезни на слизистой мягкого неба появляется геморрагическая энантема, а с 3 5 го дня петехиальная сыпь в подмышечных впадинах, на груди, в области ключиц, иногда на шее, лице, боли в пояснице. Могут быть явления менингизма, возрастает риск развития ИТШ.
Начальный период o Отмечается гиперемия кожи лица, шеи, верхних отделов груди. Слизистая оболочка зева гиперемирована, сосуды склер инъецированы, гиперемия конъюнктив, геморрагическая сыпь. Со 2 3 го дня болезни на слизистой мягкого неба появляется геморрагическая энантема, а с 3 5 го дня петехиальная сыпь в подмышечных впадинах, на груди, в области ключиц, иногда на шее, лице, боли в пояснице. Могут быть явления менингизма, возрастает риск развития ИТШ.
 Олигоанурический период (с 5 6 го по 10 12 й дни болезни). o Температура снижается до нормы в виде короткого лизиса или замедленного кризиса, иногда повышаясь вновь до субфебрильных цифр «двугорбая» кривая. Снижение температуры не сопровождается улучшением состояния больного. Достигают максимума общетоксические проявления: усиливается головная боль, сухость во рту, тошнота, появляются неукротимая рвота, икота, анорексия, отмечается выраженная адинамия, боли в пояснице, боли в животе, метеоризм. Степень выраженности олигурии (менее 500 мл мочи в сут. ) коррелирует с тяжестью заболевания. Геморрагические про явления также зависят от тяжести болезни и могут выражаться в носовых, же лудочно кишечных, маточных кровотечениях, макрогематурии. Кровоизлияния в жизненно важные органы ЦНС, гипофиз, надпочечники в этот период могут быть причиной летального исхода.
Олигоанурический период (с 5 6 го по 10 12 й дни болезни). o Температура снижается до нормы в виде короткого лизиса или замедленного кризиса, иногда повышаясь вновь до субфебрильных цифр «двугорбая» кривая. Снижение температуры не сопровождается улучшением состояния больного. Достигают максимума общетоксические проявления: усиливается головная боль, сухость во рту, тошнота, появляются неукротимая рвота, икота, анорексия, отмечается выраженная адинамия, боли в пояснице, боли в животе, метеоризм. Степень выраженности олигурии (менее 500 мл мочи в сут. ) коррелирует с тяжестью заболевания. Геморрагические про явления также зависят от тяжести болезни и могут выражаться в носовых, же лудочно кишечных, маточных кровотечениях, макрогематурии. Кровоизлияния в жизненно важные органы ЦНС, гипофиз, надпочечники в этот период могут быть причиной летального исхода.
 Полиурический период (ранней реконвалесценции) наступает с 10 12 го дня болезни. o o Прекращается рвота, постепенно исчезают боли в пояснице и животе, нормализуются сон и аппетит, увеличивается суточное количество мо чи (до 3 10 л), характерна никтурия. Сохраняется слабость, сухость во рту, появляется жажда. Длительность полиурии и изогипостенурии в зависимости от тяжести клинического течения болезни может колебаться от нескольких дней до нескольких недель. Состояние больного прогрессивно улучшается. Однако темп улучшения состояния не всегда идет параллельно нарастанию диуреза. Иногда в первые дни полиурии еще нарастает азотемия, могут развиваться де гидратация, гипонатриемия, гипокалиемия.
Полиурический период (ранней реконвалесценции) наступает с 10 12 го дня болезни. o o Прекращается рвота, постепенно исчезают боли в пояснице и животе, нормализуются сон и аппетит, увеличивается суточное количество мо чи (до 3 10 л), характерна никтурия. Сохраняется слабость, сухость во рту, появляется жажда. Длительность полиурии и изогипостенурии в зависимости от тяжести клинического течения болезни может колебаться от нескольких дней до нескольких недель. Состояние больного прогрессивно улучшается. Однако темп улучшения состояния не всегда идет параллельно нарастанию диуреза. Иногда в первые дни полиурии еще нарастает азотемия, могут развиваться де гидратация, гипонатриемия, гипокалиемия.
 Период (поздней) реконвалесценции o начинается улучшения общего состояния, восстановления суточного диуреза, нормализации показателей мочевины и креатинина. Его длительность определяется скоростью восстановления почечных функций и колеблется от 3 недель до 2 3 лет. Наряду с этим наблюдается и вегето сосудистый синдром в виде гипотонии, приглушения сердечных тонов, одышки при незначительной физической нагрузке, тремора пальцев рук, повышенной потливости, бессонницы. В этот период может отмечаться тяжесть в пояснице, положительный симптом поколачивания по поясничной области, никтурия, длительно (до 1 года и более) может сохра няться изогипостенурия. Возможно присоединение вторичной бактериальной инфекции с развитием пиелонефрита, наиболее часто наблюдаемым у пере несших ОПН.
Период (поздней) реконвалесценции o начинается улучшения общего состояния, восстановления суточного диуреза, нормализации показателей мочевины и креатинина. Его длительность определяется скоростью восстановления почечных функций и колеблется от 3 недель до 2 3 лет. Наряду с этим наблюдается и вегето сосудистый синдром в виде гипотонии, приглушения сердечных тонов, одышки при незначительной физической нагрузке, тремора пальцев рук, повышенной потливости, бессонницы. В этот период может отмечаться тяжесть в пояснице, положительный симптом поколачивания по поясничной области, никтурия, длительно (до 1 года и более) может сохра няться изогипостенурия. Возможно присоединение вторичной бактериальной инфекции с развитием пиелонефрита, наиболее часто наблюдаемым у пере несших ОПН.
 ДИАГНОСТИКА o o o o Алгоритм обследования больных ГЛПС включает: Клинико неврологическое исследование; Изучение состояния глазного дна; Отоневрологическое обследование; выявляющее поражение вестибулярных структур, тонический характера нистагма, что свидетельствует об отеке мозга и наличии гипертензионного синдрома. Эхоэнцефалоскопия позволяет выявить степень смещения срединных структур мозга, размеры его желудочков, выраженность гипертензии. В норме ширина третьего желудочка у взрослых не превышает 3 4 мм. При гидроцефалии ширина 3 его желудочка увеличивается и регистрируется расщепленный или двузубцовый сигнал от его стенок. КТ и МРТ головного мозга. Анализ допплерографических параметров (УЗДГ).
ДИАГНОСТИКА o o o o Алгоритм обследования больных ГЛПС включает: Клинико неврологическое исследование; Изучение состояния глазного дна; Отоневрологическое обследование; выявляющее поражение вестибулярных структур, тонический характера нистагма, что свидетельствует об отеке мозга и наличии гипертензионного синдрома. Эхоэнцефалоскопия позволяет выявить степень смещения срединных структур мозга, размеры его желудочков, выраженность гипертензии. В норме ширина третьего желудочка у взрослых не превышает 3 4 мм. При гидроцефалии ширина 3 его желудочка увеличивается и регистрируется расщепленный или двузубцовый сигнал от его стенок. КТ и МРТ головного мозга. Анализ допплерографических параметров (УЗДГ).
 Специфические методы диагностики ерол. Согические методы исследования (РНИФ, ИФА, РИА). o o Метод флуоресцирующих антител (МФА). Метод высокоинформативен с подтверждаемостью диагноза до 96 98%. Допускается выявление серонегативных (до 4 6%) форм заболевания (Нафеев А. А. и др. , 2002). Исследование проводится с помощью парных сывороток, диагностическим титром считается 1: 80 и нарастание титра антител в 4 и более раз. Для повышения эффективности серодиагностики ГЛПС необходим наиболее ранний забор первой сыворотки (до 4 7 дня болезни). При взятии второй сыворотки не позже 15 го дня болезни (т. е. через 10 дней). Антитела к вирусу ГЛПС после перенесенной инфекции сохраняются пожизненно независимо от тяжести перенесенного заболевания. В целях ранней диагностики ИФА с обнаружением антител класса Ig. M и ПЦР с обнаружением фрагментов вирусной РНК (Иванов А. П. и др. , 1996; Деконенко А. Е. и др. , 1996).
Специфические методы диагностики ерол. Согические методы исследования (РНИФ, ИФА, РИА). o o Метод флуоресцирующих антител (МФА). Метод высокоинформативен с подтверждаемостью диагноза до 96 98%. Допускается выявление серонегативных (до 4 6%) форм заболевания (Нафеев А. А. и др. , 2002). Исследование проводится с помощью парных сывороток, диагностическим титром считается 1: 80 и нарастание титра антител в 4 и более раз. Для повышения эффективности серодиагностики ГЛПС необходим наиболее ранний забор первой сыворотки (до 4 7 дня болезни). При взятии второй сыворотки не позже 15 го дня болезни (т. е. через 10 дней). Антитела к вирусу ГЛПС после перенесенной инфекции сохраняются пожизненно независимо от тяжести перенесенного заболевания. В целях ранней диагностики ИФА с обнаружением антител класса Ig. M и ПЦР с обнаружением фрагментов вирусной РНК (Иванов А. П. и др. , 1996; Деконенко А. Е. и др. , 1996).
 ЛЕЧЕНИЕ o o o Больные подлежат обязательной госпитализации в инфекционный стационар в максимально ранние сроки, до раз вития всех клинических проявлений болезни. Транспортировка пациентов должна быть щадящей, нужно стараться избегать тряски езды с целью предупреждения усиления болевого синдрома, нарушения гемодинамики, развития спонтанных субкапсульных разрывов коркового вещества почки и кровоизлияния в околопочечную клетчатку. Больным ГЛПС назначается комплексная терапия. Важным компонентом лечения является правильно организованный уход и тщательный контроль за уровнем А/Д, пульса, появлением геморрагического синдрома, за суточным диурезом, объемом патологических потерь и т. д. Для своевременной коррекции проведенной терапии необходимо динамическое исследование лабораторных показателей: общие анализы крови и мочи, мочевина, креатинин крови, коагулограмму, кислотно основное состояние) электролиты сыворотки натрий, калий, хлориды.
ЛЕЧЕНИЕ o o o Больные подлежат обязательной госпитализации в инфекционный стационар в максимально ранние сроки, до раз вития всех клинических проявлений болезни. Транспортировка пациентов должна быть щадящей, нужно стараться избегать тряски езды с целью предупреждения усиления болевого синдрома, нарушения гемодинамики, развития спонтанных субкапсульных разрывов коркового вещества почки и кровоизлияния в околопочечную клетчатку. Больным ГЛПС назначается комплексная терапия. Важным компонентом лечения является правильно организованный уход и тщательный контроль за уровнем А/Д, пульса, появлением геморрагического синдрома, за суточным диурезом, объемом патологических потерь и т. д. Для своевременной коррекции проведенной терапии необходимо динамическое исследование лабораторных показателей: общие анализы крови и мочи, мочевина, креатинин крови, коагулограмму, кислотно основное состояние) электролиты сыворотки натрий, калий, хлориды.
 o o Больным устанавливается постельный режим, при легкой форме болезни до одной недели, среднетяжелой 2 3 недели и тяжелой 3 4 недели. Перевод больного в другой стационар оправдан только при острой необходимости для проведения гемодиализа, для ушивания разрывов почек, и очень осторожно. Важным компонентом лечения является рациональное питание больных. Пища должна быть легкоусвояемой, содержать достаточное количество витаминов, без ограничения поваренной соли. При выраженной азотемии следует ограничивать количество вводимого белка (мясо, рыбу), также продукты, богатые калием (чернослив, изюм, карто фель). В стадию полиурии, наоборот, в диету нужно включать калийсодержащие продукты. Нельзя допускать голодания, при этом усиливается катаболизм белков и нарастает азотемия. В первые дни болезни до развития ОПН показано обильное питье (чай, фруктовые соки, щелочные минеральные воды).
o o Больным устанавливается постельный режим, при легкой форме болезни до одной недели, среднетяжелой 2 3 недели и тяжелой 3 4 недели. Перевод больного в другой стационар оправдан только при острой необходимости для проведения гемодиализа, для ушивания разрывов почек, и очень осторожно. Важным компонентом лечения является рациональное питание больных. Пища должна быть легкоусвояемой, содержать достаточное количество витаминов, без ограничения поваренной соли. При выраженной азотемии следует ограничивать количество вводимого белка (мясо, рыбу), также продукты, богатые калием (чернослив, изюм, карто фель). В стадию полиурии, наоборот, в диету нужно включать калийсодержащие продукты. Нельзя допускать голодания, при этом усиливается катаболизм белков и нарастает азотемия. В первые дни болезни до развития ОПН показано обильное питье (чай, фруктовые соки, щелочные минеральные воды).
 Этиотропная терапия Обоснована клиническая эффективность следующих противовирусных препаратов, с разработкой оптимальных схем применения: донорского специфического иммуноглобулина против ГЛПС с высоким титром антител к вирусу 1: 1024 и 1: 2048, Рибавирина, Виферона, Йодантипирипа, Анандипа.
Этиотропная терапия Обоснована клиническая эффективность следующих противовирусных препаратов, с разработкой оптимальных схем применения: донорского специфического иммуноглобулина против ГЛПС с высоким титром антител к вирусу 1: 1024 и 1: 2048, Рибавирина, Виферона, Йодантипирипа, Анандипа.
 Рибавирин Синтетический аналог нуклеозидов с выраженным противовирусным действием. Обладает широким спектром активности против РНК содержащих вирусов.
Рибавирин Синтетический аналог нуклеозидов с выраженным противовирусным действием. Обладает широким спектром активности против РНК содержащих вирусов.
 Механизм действия § § Рибавирин монофосфат ингибирует инозин монофосфат дигидрогеназу, что приводит к синтезу РНК с аномальными 5’ концами; Рибавирин обладает прямым ингибирующим действием на вирусную РНК полимеразу; Рибавирин подавление синтеза белка и нуклеиновых кислот, снижает выработку провоспалительных цитокинов; Рибавирин индуцирует апоптоз инфицированных клеток.
Механизм действия § § Рибавирин монофосфат ингибирует инозин монофосфат дигидрогеназу, что приводит к синтезу РНК с аномальными 5’ концами; Рибавирин обладает прямым ингибирующим действием на вирусную РНК полимеразу; Рибавирин подавление синтеза белка и нуклеиновых кислот, снижает выработку провоспалительных цитокинов; Рибавирин индуцирует апоптоз инфицированных клеток.
 Индукторы ИФН o Представляются особенно перспективными препараты, сочетающие спо собность индуцировать образование эндогенного ИФН и непосредственную антивирусную активность. При ряде заболеваний использование индукторов ИФН имеет ряд преимуществ перед введением экзогенных ИФН. Во первых, индукторы стимулируют выработку собственных ИФН, которые не обладают антигенностью. Во вторых, синтез ИФН находится под контролем белков ре прессоров и не достигает уровня, способного оказать повреждающего действия на организм. В третьих, стоимость лечения индукторами существенно ниже, чем экзогенными ИФН.
Индукторы ИФН o Представляются особенно перспективными препараты, сочетающие спо собность индуцировать образование эндогенного ИФН и непосредственную антивирусную активность. При ряде заболеваний использование индукторов ИФН имеет ряд преимуществ перед введением экзогенных ИФН. Во первых, индукторы стимулируют выработку собственных ИФН, которые не обладают антигенностью. Во вторых, синтез ИФН находится под контролем белков ре прессоров и не достигает уровня, способного оказать повреждающего действия на организм. В третьих, стоимость лечения индукторами существенно ниже, чем экзогенными ИФН.
 Йодантипирин o Йодантипирин (1 фенил 2, 3 диметил 4 йодпиразолон) относится к группе нестероидных противовоспалительных средств, производных пиразолона, обладает противовоспалительными, антивирусными, иммуностимули рующими и интерфероногенными свойствами. Препарат является активным индуктором альфа и бетта интерферонов, существенно повышает активность фибробластов и индуцирует их антивирусную резистентность, задерживает проникновение вируса в клетку за счет стабилизирующего действия на биоло гические мембраны, значительно стимулирует продукцию антител.
Йодантипирин o Йодантипирин (1 фенил 2, 3 диметил 4 йодпиразолон) относится к группе нестероидных противовоспалительных средств, производных пиразолона, обладает противовоспалительными, антивирусными, иммуностимули рующими и интерфероногенными свойствами. Препарат является активным индуктором альфа и бетта интерферонов, существенно повышает активность фибробластов и индуцирует их антивирусную резистентность, задерживает проникновение вируса в клетку за счет стабилизирующего действия на биоло гические мембраны, значительно стимулирует продукцию антител.
 Анандин o o Одним из новых противовирусных препаратов является анандин. В соот ветствие с приказом № 269 от 14 июля 2000 года препарат разрешен для ме дицинского применения в качестве лекарственного средства и внесен в госу дарственный реестр. Препарат также апробирован нами. Анандин является но вым высокоактивным синтетическим органическим соединением, содержащим в своем составе диметиламинопропилкарбакридон, натрия цитрат, лимонную кислоту, метиленовый синий, воду для инъекций. Он является низкомолеку лярным индуктором цитокинов (интерферонов, интерлейкинов) эффективен практически против всех классов как РНК , так и ДНК содержащих вирусов, обладает выраженной иммуномодулирующей (стимулирующей и корригирую щей) и противовоспалительной активностью. Исследования показали, что анандин обладает интерферониндуцирующей способностью, характерной для производного акридона, значительно пре восходящей по активности его структурные предшественники.
Анандин o o Одним из новых противовирусных препаратов является анандин. В соот ветствие с приказом № 269 от 14 июля 2000 года препарат разрешен для ме дицинского применения в качестве лекарственного средства и внесен в госу дарственный реестр. Препарат также апробирован нами. Анандин является но вым высокоактивным синтетическим органическим соединением, содержащим в своем составе диметиламинопропилкарбакридон, натрия цитрат, лимонную кислоту, метиленовый синий, воду для инъекций. Он является низкомолеку лярным индуктором цитокинов (интерферонов, интерлейкинов) эффективен практически против всех классов как РНК , так и ДНК содержащих вирусов, обладает выраженной иммуномодулирующей (стимулирующей и корригирую щей) и противовоспалительной активностью. Исследования показали, что анандин обладает интерферониндуцирующей способностью, характерной для производного акридона, значительно пре восходящей по активности его структурные предшественники.
 Виферон o o o Виферон новый противовирусный и иммуномодулирующий препарат, изготавливаемый в форме суппозиториев, включающих рекомбинантный ИФН а 2 в и мембраностабилизирующие компоненты в терапевтически эф фективных дозах. Препарат назначается до 5 го дня болезни по 500 тыс. МБ и 1 млн. ME 2 раза в сутки с интервалом 12 часов в течение 5 дней, затем на 7, 9, 11, 13, 15 дни от начала интерферонотерапии. Результаты исследования показали, что виферон оказывает благоприятное влияние на интерфероногенез, иммуностимулирующий эффект и способст вует более легкому течению болезни. Побочных эффектов применении препарата не наблюдается, использование свечей ограничено у больных ГЛПС с диареей (в 6% случаев).
Виферон o o o Виферон новый противовирусный и иммуномодулирующий препарат, изготавливаемый в форме суппозиториев, включающих рекомбинантный ИФН а 2 в и мембраностабилизирующие компоненты в терапевтически эф фективных дозах. Препарат назначается до 5 го дня болезни по 500 тыс. МБ и 1 млн. ME 2 раза в сутки с интервалом 12 часов в течение 5 дней, затем на 7, 9, 11, 13, 15 дни от начала интерферонотерапии. Результаты исследования показали, что виферон оказывает благоприятное влияние на интерфероногенез, иммуностимулирующий эффект и способст вует более легкому течению болезни. Побочных эффектов применении препарата не наблюдается, использование свечей ограничено у больных ГЛПС с диареей (в 6% случаев).
 Патогенетическая терапия Ноотропные препараты (ноотропил, пирацетам, пикамилон), улучшающие метаболические процессы и мозговое кровообращение. Ноотропы назначаются по 5 10 мл парентерально в течение 10 15 дней с последующим переходом на таблетированную форму не менее 3 х недель. Применение церебролизина (или церебролизата) нежелательно в связи с наличием у данного контингента больных почечной патологии. o вазоактивные средства (кавинтон, трентал, танакан, нимотоп и др. ), . вазоактивные средства необходимо принимать в течение 1 1, 5 мес. в средних терапевти ческих дозах. При отеке мозга, психомоторном возбуждении, судорожном синдроме глюкокортикоиды, мочегонные, противосудорожные и седативные препараты. Витамины группы В o
Патогенетическая терапия Ноотропные препараты (ноотропил, пирацетам, пикамилон), улучшающие метаболические процессы и мозговое кровообращение. Ноотропы назначаются по 5 10 мл парентерально в течение 10 15 дней с последующим переходом на таблетированную форму не менее 3 х недель. Применение церебролизина (или церебролизата) нежелательно в связи с наличием у данного контингента больных почечной патологии. o вазоактивные средства (кавинтон, трентал, танакан, нимотоп и др. ), . вазоактивные средства необходимо принимать в течение 1 1, 5 мес. в средних терапевти ческих дозах. При отеке мозга, психомоторном возбуждении, судорожном синдроме глюкокортикоиды, мочегонные, противосудорожные и седативные препараты. Витамины группы В o
 Патогенетическая терапия o o o В начальном периоде и в первой половине олигурического периода, при отсутствии выраженного снижения диуреза (не менее 400— 500 мл мочи в су тки) показано применение 10% раствора глюкозы по 400— 600 мл внутривенно капельно в подогретом виде (36°С), со скоростью не более 50— 60 капель в 1 мин. Для восстановления микроциркуляции, уменьшения степени сгущения крови, при падении артериального давления, сосудистой недостаточности необходимо введение реополиглюкина. Введение излишней жидкости парентерально, особенно изотонического раствора хлорида натрия, чревато опасностью развития отека легких и мозга. Исходя из этого, общее количество жидкости, вводимой парентерально до 5 — 6 дня болезни, может превышать объем выводимой не более чем на 750, а позже на высоте почечной недостаточности — на 500 мл. Для улучшения микроциркуляции и почечного кровотока назначаются эуфиллин (2, 4% 10, 0), пентоксифиллин (5, 0 на растворе глюкозы), папаверин (2% 2, 0) внутривенно капельно.
Патогенетическая терапия o o o В начальном периоде и в первой половине олигурического периода, при отсутствии выраженного снижения диуреза (не менее 400— 500 мл мочи в су тки) показано применение 10% раствора глюкозы по 400— 600 мл внутривенно капельно в подогретом виде (36°С), со скоростью не более 50— 60 капель в 1 мин. Для восстановления микроциркуляции, уменьшения степени сгущения крови, при падении артериального давления, сосудистой недостаточности необходимо введение реополиглюкина. Введение излишней жидкости парентерально, особенно изотонического раствора хлорида натрия, чревато опасностью развития отека легких и мозга. Исходя из этого, общее количество жидкости, вводимой парентерально до 5 — 6 дня болезни, может превышать объем выводимой не более чем на 750, а позже на высоте почечной недостаточности — на 500 мл. Для улучшения микроциркуляции и почечного кровотока назначаются эуфиллин (2, 4% 10, 0), пентоксифиллин (5, 0 на растворе глюкозы), папаверин (2% 2, 0) внутривенно капельно.
 Патогенетическая терапия o o o o Для повышения резистентности сосудистой стенки рутин по 0, 02 три раза в день, 5% раствор аскорбиновой кислоты по 10 мл вв. Большие дозы ее (до 30 мл в день) могут вызывать внутрисосудистый гемолиз, так как аскорбиновая кислота трансформируется в оксалат кальция. Для снижения сосудистой про ницаемости применяются также глюконат кальция, антигистаминные препараты, ингибиторы протеаз. С наступлением ОПН терапия осуществляется с тщательным учетом вод но электролитного баланса и кислотно щелочного равновесия. Коррекция ацидоза 4% раствора гидрокарбоната натрия до 200 мл и полиионных солевых растворов. Анальгетики (анальгин с димедролом, баралгин, трамал, промедол) назначаются при болевом синдроме. При рвоте и икоте вводится внутривенно гипертонический (10%) раствор натрия хлорида от 10 до 30 мл, церукал в мышцу, глюконат кальция 10% 10 мл внутривенно, 0, 25% раствор новокаина внутрь, седативные средства. В комплексной терапии больных ГЛПС используется нейролептоаналгезия дропери дол с фентанилом. Помимо уменьшения болевого синдрома, рвоты, психомо торного возбуждения дроперидол также оказывает благоприятное действие на регуляцию гемодинамики. В олигоанурическом периоде необходимо введение лазикса в ударных дозах по 100 240 мг одномоментно. При наличии эффекта целесообразно
Патогенетическая терапия o o o o Для повышения резистентности сосудистой стенки рутин по 0, 02 три раза в день, 5% раствор аскорбиновой кислоты по 10 мл вв. Большие дозы ее (до 30 мл в день) могут вызывать внутрисосудистый гемолиз, так как аскорбиновая кислота трансформируется в оксалат кальция. Для снижения сосудистой про ницаемости применяются также глюконат кальция, антигистаминные препараты, ингибиторы протеаз. С наступлением ОПН терапия осуществляется с тщательным учетом вод но электролитного баланса и кислотно щелочного равновесия. Коррекция ацидоза 4% раствора гидрокарбоната натрия до 200 мл и полиионных солевых растворов. Анальгетики (анальгин с димедролом, баралгин, трамал, промедол) назначаются при болевом синдроме. При рвоте и икоте вводится внутривенно гипертонический (10%) раствор натрия хлорида от 10 до 30 мл, церукал в мышцу, глюконат кальция 10% 10 мл внутривенно, 0, 25% раствор новокаина внутрь, седативные средства. В комплексной терапии больных ГЛПС используется нейролептоаналгезия дропери дол с фентанилом. Помимо уменьшения болевого синдрома, рвоты, психомо торного возбуждения дроперидол также оказывает благоприятное действие на регуляцию гемодинамики. В олигоанурическом периоде необходимо введение лазикса в ударных дозах по 100 240 мг одномоментно. При наличии эффекта целесообразно
 Патогенетическая терапия o o o Уменьшению уремической интоксикации способствуют промывания же лудка и высокие клизмы с 2% раствором соды. При нарастании клинических и лабораторных показателей уремии (мочевина 26 ммоль/л и более, креатинин 800 1000 мкмоль/л и калий сыворотки крови бммоль/л и более) показано применение экстракорпорального гемодиа лиза. При ИТШ 3 5 день болезни интенсивная противошоковая терапия в условиях отделения реанимации и интенсивной терапии. Инфузионная терапия включает введение коллоидных и кристаллоидных растворов в соотношении 1: 2 (реополиглюкин, альбумин, плазма, 10% раствор глюкозы, ди соль, ацесоль, раствор Рингера. Показано применение глюкокортикостероидов. При ИТШ I степени, разовая доза преднизолона составляет 2 3 мг/кг массы, повторно вводится через 4 6 часов, суточная доза достигает 5 10 мг/кг массы; при II степени шока разовая доза 4 5 мг/кг с интервалом 3 4 часа, при этом суточная доза составляет 20 30 мг/кг; при III степени шока разовая доза 6 мг/кг и более, повторно через 3 4 часа и суточная доза достигает 30 50 мг/кг массы тела. При отсутствии эффекта от введения стероидов, показана капельная инфузия допамина из расчета 1 7 мг/кг массы в минуту, он улучшает и почечный кровоток.
Патогенетическая терапия o o o Уменьшению уремической интоксикации способствуют промывания же лудка и высокие клизмы с 2% раствором соды. При нарастании клинических и лабораторных показателей уремии (мочевина 26 ммоль/л и более, креатинин 800 1000 мкмоль/л и калий сыворотки крови бммоль/л и более) показано применение экстракорпорального гемодиа лиза. При ИТШ 3 5 день болезни интенсивная противошоковая терапия в условиях отделения реанимации и интенсивной терапии. Инфузионная терапия включает введение коллоидных и кристаллоидных растворов в соотношении 1: 2 (реополиглюкин, альбумин, плазма, 10% раствор глюкозы, ди соль, ацесоль, раствор Рингера. Показано применение глюкокортикостероидов. При ИТШ I степени, разовая доза преднизолона составляет 2 3 мг/кг массы, повторно вводится через 4 6 часов, суточная доза достигает 5 10 мг/кг массы; при II степени шока разовая доза 4 5 мг/кг с интервалом 3 4 часа, при этом суточная доза составляет 20 30 мг/кг; при III степени шока разовая доза 6 мг/кг и более, повторно через 3 4 часа и суточная доза достигает 30 50 мг/кг массы тела. При отсутствии эффекта от введения стероидов, показана капельная инфузия допамина из расчета 1 7 мг/кг массы в минуту, он улучшает и почечный кровоток.
 РЕАБИЛИТАЦИЯ o o Все больные, перенесшие среднетяжелую и тяжелую форму ГЛПС, нуждаются в осуществлении поэтапной реабилитации, включающей обязательную организацию полущадящего режима (строгое дозирование интеллектуальной и физической нагрузки, разумный режим дня), диспансерное наблюдение участ кового врача, инфекциониста, в некоторых случаях невролога. Данный кон тингент больных, особенно, перенесшие тяжелую форму ГЛПС, подлежит обя зательному осмотру невролога в поликлинике. В периоде реконвалесценции назначается стол № 15. Не ограничивается молочно растительные продукты. Противопоказаны пряности, уксус, хрен гор чица, майонез, перец. Категорически запрещается употребление алкоголя. Питье обильное: минеральная вода типа Ессентуки № 4, Боржоми, местные Мин воды (Волжанка). В дополнительном медикаментозном лечении и физиотера пии нуждаются реконвалесценты с наличием резидуальных явлений.
РЕАБИЛИТАЦИЯ o o Все больные, перенесшие среднетяжелую и тяжелую форму ГЛПС, нуждаются в осуществлении поэтапной реабилитации, включающей обязательную организацию полущадящего режима (строгое дозирование интеллектуальной и физической нагрузки, разумный режим дня), диспансерное наблюдение участ кового врача, инфекциониста, в некоторых случаях невролога. Данный кон тингент больных, особенно, перенесшие тяжелую форму ГЛПС, подлежит обя зательному осмотру невролога в поликлинике. В периоде реконвалесценции назначается стол № 15. Не ограничивается молочно растительные продукты. Противопоказаны пряности, уксус, хрен гор чица, майонез, перец. Категорически запрещается употребление алкоголя. Питье обильное: минеральная вода типа Ессентуки № 4, Боржоми, местные Мин воды (Волжанка). В дополнительном медикаментозном лечении и физиотера пии нуждаются реконвалесценты с наличием резидуальных явлений.
 ПРОФИЛАКТИКА o Борьба с ГЛПС в настоящее время строится на широком комплексе мероприятий, направленных на предупреждение или уменьшение контакта насе ления с грызунами. Учет заболеваемости и эпидемиологическое обследование каждого случая, завершающееся точными установлением места заражения, имеют для профилактики ГЛПС очень большое значение, так как прямо указы вают на существование очага инфекции, где популяция грызунов заражена воз будителем. Проведение дератизации в этом очаге приводит к снижению чис ленности грызунов и уменьшению возможности возникновения повторных за болеваний.
ПРОФИЛАКТИКА o Борьба с ГЛПС в настоящее время строится на широком комплексе мероприятий, направленных на предупреждение или уменьшение контакта насе ления с грызунами. Учет заболеваемости и эпидемиологическое обследование каждого случая, завершающееся точными установлением места заражения, имеют для профилактики ГЛПС очень большое значение, так как прямо указы вают на существование очага инфекции, где популяция грызунов заражена воз будителем. Проведение дератизации в этом очаге приводит к снижению чис ленности грызунов и уменьшению возможности возникновения повторных за болеваний.
 Жёлтая лихорадка (Febris flava) o Желтая лихорадка (синонимы: Yellow fever англ. ; Gelbfieber нем. ; Fievre jaune франц. ; Fiebre amarilla, Vomito negro исп. ) острое арбовирусное заболевание, передаваемое комарами, характеризуется лихорадкой, тяжелой интоксикацией, тромбогеморрагическим синдромом, поражением почек и печени.
Жёлтая лихорадка (Febris flava) o Желтая лихорадка (синонимы: Yellow fever англ. ; Gelbfieber нем. ; Fievre jaune франц. ; Fiebre amarilla, Vomito negro исп. ) острое арбовирусное заболевание, передаваемое комарами, характеризуется лихорадкой, тяжелой интоксикацией, тромбогеморрагическим синдромом, поражением почек и печени.
 Этиология. o Возбудитель вирус Viscerophilus tropicus, относится к семейству Togoviridae, роду Flavivirus, содержит РНК, является арбовирусом антигенной группы В. Имеет антигенное родство с вирусами японского энцефалита, денге и энцефалита Сент Луис. Патогенен для обезьян, белых мышей, а при внутримозговом заражении и для морских свинок. Диаметр вирусных частиц 17 25 нм. Вирус культивируется в развивающемся курином эмбрионе и культурах тканей. При длительном культивировании получены авирулентные штаммы (например 17 D), сохраняющие свои иммуногенные свойства. Эти штаммы используют в качестве вакцины. Вирус быстро инактивируется при высокой температуре, под воздействием дезинфицирующих средств. Длительно сохраняется в замороженном состоянии и при высушивании.
Этиология. o Возбудитель вирус Viscerophilus tropicus, относится к семейству Togoviridae, роду Flavivirus, содержит РНК, является арбовирусом антигенной группы В. Имеет антигенное родство с вирусами японского энцефалита, денге и энцефалита Сент Луис. Патогенен для обезьян, белых мышей, а при внутримозговом заражении и для морских свинок. Диаметр вирусных частиц 17 25 нм. Вирус культивируется в развивающемся курином эмбрионе и культурах тканей. При длительном культивировании получены авирулентные штаммы (например 17 D), сохраняющие свои иммуногенные свойства. Эти штаммы используют в качестве вакцины. Вирус быстро инактивируется при высокой температуре, под воздействием дезинфицирующих средств. Длительно сохраняется в замороженном состоянии и при высушивании.
 Эпидемиология. o Желтая лихорадка относится к карантинным болезням. Эндемичными очагами являются обширные территории Южной Америки (Боливия, Бразилия, Колумбия, Перу, Эквадор и др. ), а также экваториальной Африки. Источником и резервуаром инфекции служат дикие животные (обезьяны, опоссумы, редко другие виды), а также больной человек. Переносчики комары. Различают 2 типа желтой лихорадки: 1) городской (антропонозный) и 2) сельский (желтая лихорадка джунглей). При антропонозном типе заражение комара (Aedes aegypti) происходит при укусе больного человека в конце инкубационного периода или в первые 3 дня заболевания. При сельском типе желтой лихорадки источником инфекции являются обезьяны, а переносчиком комары Aedes aficanus, Aedes simpsoni.
Эпидемиология. o Желтая лихорадка относится к карантинным болезням. Эндемичными очагами являются обширные территории Южной Америки (Боливия, Бразилия, Колумбия, Перу, Эквадор и др. ), а также экваториальной Африки. Источником и резервуаром инфекции служат дикие животные (обезьяны, опоссумы, редко другие виды), а также больной человек. Переносчики комары. Различают 2 типа желтой лихорадки: 1) городской (антропонозный) и 2) сельский (желтая лихорадка джунглей). При антропонозном типе заражение комара (Aedes aegypti) происходит при укусе больного человека в конце инкубационного периода или в первые 3 дня заболевания. При сельском типе желтой лихорадки источником инфекции являются обезьяны, а переносчиком комары Aedes aficanus, Aedes simpsoni.
 Патогенез. o Вирус проникает в организм человека при укусе инфицированным комаром. Известны случаи лабораторных заражений аэрогенным путем. От места внедрения возбудитель распространяется по лимфатическим путям и достигает регионарных лимфатических узлов, где происходит его размножение и накопление. Спустя несколько дней вирус проникает в кровь, где его можно обнаружить в течение 3 5 дней. Гематогенным путем вирус проникает в различные органы (печень, селезенка, почки, костный мозг, лимфатические узлы), вызывая их поражение. Развивается тромбогеморрагический синдром, который проявляется в виде множественных кровоизлияний в различных органах. Печень увеличена, некротизированные печеночные клетки расположены небольшими очажками. Эти очаговые гомогенные эозинофильные тельца, обнаруживаемые в перисинусоидных пространствах печени, называют тельцами Каунсилмена. В центральных зонах печеночных долек отмечают жировую дегенерацию гепатоцитов. Поражение печени ведет к выраженной желтухе. Изменения обнаруживают в почках (отек, кровоизлияния, некроз почечных канальцев), селезенке, миокарде, лимфатических узлах. После перенесенной болезни развивается напряженный иммунитет, сохраняющийся в течение 6 8 лет.
Патогенез. o Вирус проникает в организм человека при укусе инфицированным комаром. Известны случаи лабораторных заражений аэрогенным путем. От места внедрения возбудитель распространяется по лимфатическим путям и достигает регионарных лимфатических узлов, где происходит его размножение и накопление. Спустя несколько дней вирус проникает в кровь, где его можно обнаружить в течение 3 5 дней. Гематогенным путем вирус проникает в различные органы (печень, селезенка, почки, костный мозг, лимфатические узлы), вызывая их поражение. Развивается тромбогеморрагический синдром, который проявляется в виде множественных кровоизлияний в различных органах. Печень увеличена, некротизированные печеночные клетки расположены небольшими очажками. Эти очаговые гомогенные эозинофильные тельца, обнаруживаемые в перисинусоидных пространствах печени, называют тельцами Каунсилмена. В центральных зонах печеночных долек отмечают жировую дегенерацию гепатоцитов. Поражение печени ведет к выраженной желтухе. Изменения обнаруживают в почках (отек, кровоизлияния, некроз почечных канальцев), селезенке, миокарде, лимфатических узлах. После перенесенной болезни развивается напряженный иммунитет, сохраняющийся в течение 6 8 лет.
 Симптомы и течение. Инкубационный период колеблется от 3 до 6 сут. В клиническом течении желтой лихорадки можно выделить 3 периода: o начальный лихорадочный период (стадия гиперемии); o период ремиссии; o реактивный период (стадия стаза).
Симптомы и течение. Инкубационный период колеблется от 3 до 6 сут. В клиническом течении желтой лихорадки можно выделить 3 периода: o начальный лихорадочный период (стадия гиперемии); o период ремиссии; o реактивный период (стадия стаза).
 o o o o внезапное начало, сильная головная боль, боли в пояснице, спине, конечностях. Температура 39 40°С и выше. Появляется гиперемия и одутловатость лица, отечность век, инъекция сосудов склер и конъюнктив. Тахикардия до 100 130 в 1 мин. мучительная жажда, тошнота, многократная рвота слизью, а затем желчью. гиперемия слизистой рта, язык сухой, края языка покрасневшие. На 3 4 й день болезни могут появиться цианоз, желтуха, незначительная примесь крови в рвотных массах. На 4 5 й день болезни самочувствие лучше, температура тела снижается до субфебрильной (стадия ремиссии). Однако через несколько часов температура вновь повышается, состояние больного прогрессивно ухудшается наступает реактивный период. Развивается тромбогеморрагический синдром в виде кровавой рвоты, кровотечений из носа, кишечника, матки, на коже появляются петехии и более крупные кровоизлияния. Лицо больного становится бледным. Пульс редкий (до 50 40 уд/мин), не соответствует повышенной температуре (симптом Фаже), АД падает, количество мочи уменьшается, иногда развивается анурия. Нарастает слабость, появляется бред. В тяжелых случаях смерть наступает от почечной недостаточности или инфекционного коллапса (и В легких случаях симптомы болезни выражены слабо, желтухи и тромбогеморрагического синдрома может не быть. При очень тяжелых формах больные могут умереть на 2 3 й день болезни еще до развития желтухи (молниеносные формы).
o o o o внезапное начало, сильная головная боль, боли в пояснице, спине, конечностях. Температура 39 40°С и выше. Появляется гиперемия и одутловатость лица, отечность век, инъекция сосудов склер и конъюнктив. Тахикардия до 100 130 в 1 мин. мучительная жажда, тошнота, многократная рвота слизью, а затем желчью. гиперемия слизистой рта, язык сухой, края языка покрасневшие. На 3 4 й день болезни могут появиться цианоз, желтуха, незначительная примесь крови в рвотных массах. На 4 5 й день болезни самочувствие лучше, температура тела снижается до субфебрильной (стадия ремиссии). Однако через несколько часов температура вновь повышается, состояние больного прогрессивно ухудшается наступает реактивный период. Развивается тромбогеморрагический синдром в виде кровавой рвоты, кровотечений из носа, кишечника, матки, на коже появляются петехии и более крупные кровоизлияния. Лицо больного становится бледным. Пульс редкий (до 50 40 уд/мин), не соответствует повышенной температуре (симптом Фаже), АД падает, количество мочи уменьшается, иногда развивается анурия. Нарастает слабость, появляется бред. В тяжелых случаях смерть наступает от почечной недостаточности или инфекционного коллапса (и В легких случаях симптомы болезни выражены слабо, желтухи и тромбогеморрагического синдрома может не быть. При очень тяжелых формах больные могут умереть на 2 3 й день болезни еще до развития желтухи (молниеносные формы).
 Диагноз и дифференциальный диагноз o o Из лабораторных исследований диагностическое значение имеют: лейкопения, нейтропения, обнаружение белка и цилиндров в моче, а также увеличение содержания билирубина в сыворотке крови, остаточного азота и значительное повышение активности сывороточных аминотрансфераз. Характерные изменения выявляются при гистологическом исследовании биоптатов печени. Из серологических методов используют РСК, реакция нейтрализации и РТГА, однако последняя часто дает положительные реакции и с другими вирусами. Исследования проводят с парными сыворотками. В настоящее время используют выделение вируса из крови методом инокуляции материала на культуру клеток москитов или путем введения материала в грудную полость москитов.
Диагноз и дифференциальный диагноз o o Из лабораторных исследований диагностическое значение имеют: лейкопения, нейтропения, обнаружение белка и цилиндров в моче, а также увеличение содержания билирубина в сыворотке крови, остаточного азота и значительное повышение активности сывороточных аминотрансфераз. Характерные изменения выявляются при гистологическом исследовании биоптатов печени. Из серологических методов используют РСК, реакция нейтрализации и РТГА, однако последняя часто дает положительные реакции и с другими вирусами. Исследования проводят с парными сыворотками. В настоящее время используют выделение вируса из крови методом инокуляции материала на культуру клеток москитов или путем введения материала в грудную полость москитов.
 Лихорадка Денге o Денге (синонимы: dengue awn нем. , франц. , исп. ; dangy fever, breakbonefever англ. ; denguero итал, лихорадка денге, костоломная лихорадка, суставная лихорадка, лихорадка жирафов, пятидневная лихорадка, семидневная лихорадка, финиковая болезнь) острая вирусная болезнь, протекающая с лихорадкой, интоксикацией, миалгией и артралгией, экзантемой, лимфаденопатией, лейкопенией. Некоторые варианты денге протекают с геморрагическим синдромом. Относится к трансмиссивным зоонозам.
Лихорадка Денге o Денге (синонимы: dengue awn нем. , франц. , исп. ; dangy fever, breakbonefever англ. ; denguero итал, лихорадка денге, костоломная лихорадка, суставная лихорадка, лихорадка жирафов, пятидневная лихорадка, семидневная лихорадка, финиковая болезнь) острая вирусная болезнь, протекающая с лихорадкой, интоксикацией, миалгией и артралгией, экзантемой, лимфаденопатией, лейкопенией. Некоторые варианты денге протекают с геморрагическим синдромом. Относится к трансмиссивным зоонозам.
 Этиология o Возбудители денге относятся к вирусам семейства Togaviridae рода Flavivirus (арбовирусы антигенной группы В). Содержат РНК, имеют двухслойную липидную оболочку из фосфолипидов и холестерола, размеры вириона 40 45 нм в диаметре. Инактивируется при обработке протеолитическими ферментами и прогревании выше 60°С, под влиянием ультрафиолетового облучения. Известно 4 типа вируса денге, различных в антигенном отношении. Вирусы денге имеют антигенное родство с вирусами желтой лихорадки, японского и западно нильского энцефалитов. Размножается на культурах тканей и клетках почек обезьян, хомяков, KB и др. В сыворотке крови больных вирус сохраняется при комнатной температуре до 2 мес, а высушенный до 5 лет.
Этиология o Возбудители денге относятся к вирусам семейства Togaviridae рода Flavivirus (арбовирусы антигенной группы В). Содержат РНК, имеют двухслойную липидную оболочку из фосфолипидов и холестерола, размеры вириона 40 45 нм в диаметре. Инактивируется при обработке протеолитическими ферментами и прогревании выше 60°С, под влиянием ультрафиолетового облучения. Известно 4 типа вируса денге, различных в антигенном отношении. Вирусы денге имеют антигенное родство с вирусами желтой лихорадки, японского и западно нильского энцефалитов. Размножается на культурах тканей и клетках почек обезьян, хомяков, KB и др. В сыворотке крови больных вирус сохраняется при комнатной температуре до 2 мес, а высушенный до 5 лет.
 o o Источником инфекции служат больной человек, обезьяны и, возможно, летучие мыши. Передача инфекции у человека осуществляется комарами Aedes aegypti, у обезьян A. albopictus. Комар A. aegypti становится заразным через 8 12 дней после питания кровью больного человека. Комар остается инфицированным до 3 мес и более. Вирус способен развиваться в теле комара лишь при температуре воздуха не ниже 22°С. В
o o Источником инфекции служат больной человек, обезьяны и, возможно, летучие мыши. Передача инфекции у человека осуществляется комарами Aedes aegypti, у обезьян A. albopictus. Комар A. aegypti становится заразным через 8 12 дней после питания кровью больного человека. Комар остается инфицированным до 3 мес и более. Вирус способен развиваться в теле комара лишь при температуре воздуха не ниже 22°С. В
 o o Геморрагическая форма развивается лишь у местных жителей. При этой форме поражаются преимущественно мелкие сосуды, где выявляются набухание эндотелия, периваскулярный отек и инфильтрация мононуклеарами. Повышение проницаемости сосудов приводит к нарушению объема плазмы, аноксии тканей, метаболическому ацидозу. С поражением сосудов и нарушением агрегатного состояния крови связано развитие распространенных геморрагических явлений. В более тяжелых случаях возникают множественные кровоизлияния в эндо и перикарде, плевре, брюшине, слизистой оболочке желудка и кишечника, в головном мозге. Вирус денге оказывает также токсическое действие, с которым связаны дегенеративные изменения в печени, почках, миокарде. После перенесенного заболевания иммунитет длится около 2 лет, однако он типоспецифичен, возможны повторные заболевания в тот же сезон (через 2 3 мес) за счет заражения другим типом.
o o Геморрагическая форма развивается лишь у местных жителей. При этой форме поражаются преимущественно мелкие сосуды, где выявляются набухание эндотелия, периваскулярный отек и инфильтрация мононуклеарами. Повышение проницаемости сосудов приводит к нарушению объема плазмы, аноксии тканей, метаболическому ацидозу. С поражением сосудов и нарушением агрегатного состояния крови связано развитие распространенных геморрагических явлений. В более тяжелых случаях возникают множественные кровоизлияния в эндо и перикарде, плевре, брюшине, слизистой оболочке желудка и кишечника, в головном мозге. Вирус денге оказывает также токсическое действие, с которым связаны дегенеративные изменения в печени, почках, миокарде. После перенесенного заболевания иммунитет длится около 2 лет, однако он типоспецифичен, возможны повторные заболевания в тот же сезон (через 2 3 мес) за счет заражения другим типом.
 o По клиническому течению различают лихорадочную форму денге (классическую) и геморрагическую лихорадку денге.
o По клиническому течению различают лихорадочную форму денге (классическую) и геморрагическую лихорадку денге.
 Омская геморрагическая лихорадка o o острое вирусное заболевание, характеризующееся природной очаговостью, лихорадкой, геморрагическим синдромом и поражением нервной системы. Этиология. Возбудитель относится к группе арбовирусов, семейству Togaviridae, роду Flavivirus (группа В). Относится к мелким вирусам, диаметр частиц 35 40 нм, содержит РНК, при температуре 4°С инактивируется через 29 дней, при 56°С через 25 мин. В лиофилизированном состоянии может сохраняться до 4 лет. Вирус при пассаже на ондатрах и белых мышах становится высоковирулентным, морские свинки и белые крысы малочувствительны к вирусу.
Омская геморрагическая лихорадка o o острое вирусное заболевание, характеризующееся природной очаговостью, лихорадкой, геморрагическим синдромом и поражением нервной системы. Этиология. Возбудитель относится к группе арбовирусов, семейству Togaviridae, роду Flavivirus (группа В). Относится к мелким вирусам, диаметр частиц 35 40 нм, содержит РНК, при температуре 4°С инактивируется через 29 дней, при 56°С через 25 мин. В лиофилизированном состоянии может сохраняться до 4 лет. Вирус при пассаже на ондатрах и белых мышах становится высоковирулентным, морские свинки и белые крысы малочувствительны к вирусу.
 Эпидемиология. o Первые описания омской геморрагической лихорадки были сделаны местными врачами в Омской области в период с 1940 по 1945 гг. (Б. П. Первушин, Г. А. Сиземова и др. ). С 1946 г. омская геморрагическая лихорадка выделена в самостоятельную нозологическую форму. Было установлено, что основным резервуаром инфекции является узкочерепная полевка, а переносчиком клещ D. pictus. Другим путем передачи инфекции был контактный. Заболевание наступало после контакта с ондатрой (местное население знало об этом и даже было название "ондатровая болезнь"). Природные очаги омской геморрагической лихорадки были выявлены в степных и лесостепных районах Омской, Новосибирской, Тюменской, Курганской, Оренбургской областей. Резервуаром инфекции в природе являются в основном водяная крыса, рыжая полевка, ондатра, а также клещи D. pictus, D. marginatus, которые могут передавать вирус потомству трансовариально. Омская геморрагическая лихорадка неконтагиозна. Случаев заражения от человека не наблюдалось.
Эпидемиология. o Первые описания омской геморрагической лихорадки были сделаны местными врачами в Омской области в период с 1940 по 1945 гг. (Б. П. Первушин, Г. А. Сиземова и др. ). С 1946 г. омская геморрагическая лихорадка выделена в самостоятельную нозологическую форму. Было установлено, что основным резервуаром инфекции является узкочерепная полевка, а переносчиком клещ D. pictus. Другим путем передачи инфекции был контактный. Заболевание наступало после контакта с ондатрой (местное население знало об этом и даже было название "ондатровая болезнь"). Природные очаги омской геморрагической лихорадки были выявлены в степных и лесостепных районах Омской, Новосибирской, Тюменской, Курганской, Оренбургской областей. Резервуаром инфекции в природе являются в основном водяная крыса, рыжая полевка, ондатра, а также клещи D. pictus, D. marginatus, которые могут передавать вирус потомству трансовариально. Омская геморрагическая лихорадка неконтагиозна. Случаев заражения от человека не наблюдалось.
 Болезнь Кьясанурского леса o o o Начиная с 1955 года в Индии, на небольшой территории тропических лесов в штате Майсор, провинции Шимога (южная часть страны) ежегодно регистрировались вспышки ранее неизвестной болезни среди лиц, работавших на заготовке леса. Все случаи заболеваний приходились на весенне летние месяцы, а наибольшая часть их наблюдалась в апреле мае. Практически все заболевшие отмечали, что за 7 10 дней до начала заболевания они подвергались нападению клещей. В 1957 году T. H. Work и его коллеги от обезьян и больных людей выделели вирус возбудитель данного заболевания. Последующие экспериментальные работы показали, что вирусы достаточно хорошо культивируются. Было доказана их патогенность для белых мышей и обезьян. Синонимы: Кьясанурская лесная болезнь Индии; Fievre hemorragique de la foret de Kyasanur; Maladie de la foret de Kyasanur.
Болезнь Кьясанурского леса o o o Начиная с 1955 года в Индии, на небольшой территории тропических лесов в штате Майсор, провинции Шимога (южная часть страны) ежегодно регистрировались вспышки ранее неизвестной болезни среди лиц, работавших на заготовке леса. Все случаи заболеваний приходились на весенне летние месяцы, а наибольшая часть их наблюдалась в апреле мае. Практически все заболевшие отмечали, что за 7 10 дней до начала заболевания они подвергались нападению клещей. В 1957 году T. H. Work и его коллеги от обезьян и больных людей выделели вирус возбудитель данного заболевания. Последующие экспериментальные работы показали, что вирусы достаточно хорошо культивируются. Было доказана их патогенность для белых мышей и обезьян. Синонимы: Кьясанурская лесная болезнь Индии; Fievre hemorragique de la foret de Kyasanur; Maladie de la foret de Kyasanur.
 o o o Болезнь Кьясанурского леса (БКЛ) острое природно очаговое арбовирусное заболевание, характеризующееся тяжелым течением с выраженным геморрагическим синдромом. Впервые как самостоятельная клиническая единица болезнь Кьясанурского леса была обнаружена в тропических лесах западной области Майсур в южной Индии в 1957 г. Этиология. Возбудитель относится к экологической группе арбовирусов семейства тогавирусов рода флавивирусов (группа В). В отличие от других вирусов этой группы он ассоциирован не с энцефалитом, а с геморрагической лихорадкой. Вирус близок к возбудителям омской геморрагической лихорадки, желтой лихорадки и денге. Геном вируса представлен односпиральной РНК. В настоящее время геном вируса тщательно исследуется, проведено секвенирование важнейших белков вириона по результатам которых возможно получение рекомбинантной вакцины.
o o o Болезнь Кьясанурского леса (БКЛ) острое природно очаговое арбовирусное заболевание, характеризующееся тяжелым течением с выраженным геморрагическим синдромом. Впервые как самостоятельная клиническая единица болезнь Кьясанурского леса была обнаружена в тропических лесах западной области Майсур в южной Индии в 1957 г. Этиология. Возбудитель относится к экологической группе арбовирусов семейства тогавирусов рода флавивирусов (группа В). В отличие от других вирусов этой группы он ассоциирован не с энцефалитом, а с геморрагической лихорадкой. Вирус близок к возбудителям омской геморрагической лихорадки, желтой лихорадки и денге. Геном вируса представлен односпиральной РНК. В настоящее время геном вируса тщательно исследуется, проведено секвенирование важнейших белков вириона по результатам которых возможно получение рекомбинантной вакцины.
 Эпидемиология. o o Переносчиками инфекции для человека служат клещи вида Haemaphysalis spinigera, из которых закономерно выделяется вирус. В настоящее время принято считать, что основная роль в циркуляции вирусов в природе принадлежит клещам H. spinigera, которые не нападают на людей, но паразитируют на мелких лесных млекопитающих и являются основными хранителями вирусов в межэпидемический период. Клещи Haemaphysalis spinigera в свою очередь инфицируются в личиночной и нимфальной стадиях при питании на мелких млекопитающих, а при переходе в имагинальную стадию развития преимущественно нападают на крупных млекопитающих (коровы, обезьяны) и птиц. Приматы Macaca radiata и Presbytis entellus (на фотографии) играют важную роль в поддержании циркуляции вирусов болезни Кьясанурского леса в Индии.
Эпидемиология. o o Переносчиками инфекции для человека служат клещи вида Haemaphysalis spinigera, из которых закономерно выделяется вирус. В настоящее время принято считать, что основная роль в циркуляции вирусов в природе принадлежит клещам H. spinigera, которые не нападают на людей, но паразитируют на мелких лесных млекопитающих и являются основными хранителями вирусов в межэпидемический период. Клещи Haemaphysalis spinigera в свою очередь инфицируются в личиночной и нимфальной стадиях при питании на мелких млекопитающих, а при переходе в имагинальную стадию развития преимущественно нападают на крупных млекопитающих (коровы, обезьяны) и птиц. Приматы Macaca radiata и Presbytis entellus (на фотографии) играют важную роль в поддержании циркуляции вирусов болезни Кьясанурского леса в Индии.
 Геморрагическая лихорадка Крым-Конго o o (синонимы: геморрагическая лихорадка Крым Конго Хазер, крымско конголезская лихорадка, среднеазиатская геморрагическая лихорадка, карахалак; Crimean Congo hemorrhagic fever, Crimean hemorrhagic fever англ. ) острое вирусное заболевание, относящееся к зоонозам с природной очаговостью. Характеризуется двухволновой лихорадкой, общей интоксикацией и выраженным тромбогеморрагическим синдромом. Возбудитель открыт в 1945 г. М. П. Чумаковым. Является РНК содержащим вирусом, относится к семейству Bunyaviridae, род Nairovirus. В 1956 г. идентичный по антигенному составу вирус был выделен из крови больного лихорадкой мальчика. Возбудитель получил название вирус Конго. Вирионы сферической формы 92 96 нм в диаметре. Наиболее чувствительны к вирусу клетки почек эмбриона свиней, сирийских хомячков и обезьян. В лиофилизированном состоянии сохраняется свыше 2 лет. Локализуется преимущественно в цитоплазме.
Геморрагическая лихорадка Крым-Конго o o (синонимы: геморрагическая лихорадка Крым Конго Хазер, крымско конголезская лихорадка, среднеазиатская геморрагическая лихорадка, карахалак; Crimean Congo hemorrhagic fever, Crimean hemorrhagic fever англ. ) острое вирусное заболевание, относящееся к зоонозам с природной очаговостью. Характеризуется двухволновой лихорадкой, общей интоксикацией и выраженным тромбогеморрагическим синдромом. Возбудитель открыт в 1945 г. М. П. Чумаковым. Является РНК содержащим вирусом, относится к семейству Bunyaviridae, род Nairovirus. В 1956 г. идентичный по антигенному составу вирус был выделен из крови больного лихорадкой мальчика. Возбудитель получил название вирус Конго. Вирионы сферической формы 92 96 нм в диаметре. Наиболее чувствительны к вирусу клетки почек эмбриона свиней, сирийских хомячков и обезьян. В лиофилизированном состоянии сохраняется свыше 2 лет. Локализуется преимущественно в цитоплазме.
 Эпидемиология. o Резервуаром вируса являются дикие мелкие млекопитающие: лесная мышь, малый суслик, заяц русак, ушастый еж. Переносчиком и хранителем являются клещи, преимущественно из рода Hyalomma. Заболеваемость характеризуется сезонностью с максимумом с мая по август (в нашей стране). Болезнь наблюдалась в Крыму, Астраханской, Ростовской областях, Краснодарском и Ставропольском краях, а также в Средней Азии, Китае, Болгарии, Югославии, в большинстве стран Африки к югу от Сахары (Конго, Кения, Уганда, Нигерия и др. ). В 80% случаев заболевают лица в возрасте от 20 до 60 лет. Самка клеща рода Hyalomma переносчик заболевания.
Эпидемиология. o Резервуаром вируса являются дикие мелкие млекопитающие: лесная мышь, малый суслик, заяц русак, ушастый еж. Переносчиком и хранителем являются клещи, преимущественно из рода Hyalomma. Заболеваемость характеризуется сезонностью с максимумом с мая по август (в нашей стране). Болезнь наблюдалась в Крыму, Астраханской, Ростовской областях, Краснодарском и Ставропольском краях, а также в Средней Азии, Китае, Болгарии, Югославии, в большинстве стран Африки к югу от Сахары (Конго, Кения, Уганда, Нигерия и др. ). В 80% случаев заболевают лица в возрасте от 20 до 60 лет. Самка клеща рода Hyalomma переносчик заболевания.
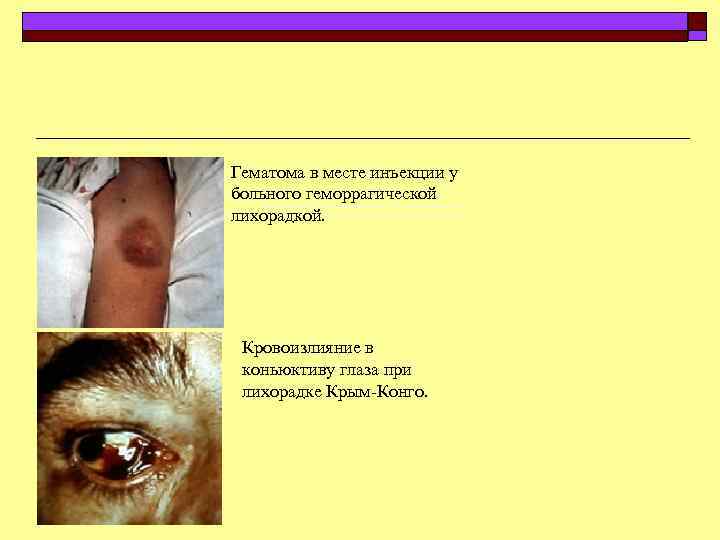 Гематома в месте инъекции у больного геморрагической лихорадкой. Кровоизлияние в коньюктиву глаза при лихорадке Крым Конго.
Гематома в месте инъекции у больного геморрагической лихорадкой. Кровоизлияние в коньюктиву глаза при лихорадке Крым Конго.
 Лихорадка Ласса o o острая вирусная болезнь из группы зоонозов с природной очаговостью. Характеризуется тяжелым течением, высокой летальностью, тромбогеморрагическим синдромом, язвенным стоматитом, поражением органов дыхания, почек, центральной нервной системы, миокардитом. Этиология. Возбудитель относится к аренавирусам, семейство Arenaviridae, род Arenavirus. Имеет антигенное родство с другими аренавирусами (вирусом лимфоцитарного хориоменингита, возбудителями геморрагических лихорадок Южной Америки вирусами Такарибе, Хунин, Мачупо и др. ). Вирион сферической формы, диаметр 70 150 нм, имеет липидную оболочку, на которой расположены ворсинки нередко булавовидной формы длиной около 10 нм, содержит РНК.
Лихорадка Ласса o o острая вирусная болезнь из группы зоонозов с природной очаговостью. Характеризуется тяжелым течением, высокой летальностью, тромбогеморрагическим синдромом, язвенным стоматитом, поражением органов дыхания, почек, центральной нервной системы, миокардитом. Этиология. Возбудитель относится к аренавирусам, семейство Arenaviridae, род Arenavirus. Имеет антигенное родство с другими аренавирусами (вирусом лимфоцитарного хориоменингита, возбудителями геморрагических лихорадок Южной Америки вирусами Такарибе, Хунин, Мачупо и др. ). Вирион сферической формы, диаметр 70 150 нм, имеет липидную оболочку, на которой расположены ворсинки нередко булавовидной формы длиной около 10 нм, содержит РНК.
 Эпидемиология. o В 1969 г. в городе Ласса (Нигерия) среди миссионеров возникло высококонтагиозное вирусное заболевание. В дальнейшем вспышки этой болезни наблюдались в Сьерра Леоне и Либерии. Существование очагов инфекции серологически доказано и в других странах Африки (Берег Слоновой Кости, Гвинея, Мали, Мозамбик, Сенегал и др. ). Летальность достигала 36 67%. Резервуар инфекции многососковая крыса (Mastomys natalensis), широко распространенная в Западной Африке. Характерна длительная персистенция вируса у инфицированных животных; он выделяется с мочой, слюной, обнаружен в секрете респираторного трактата. Сохраняется в высохших выделениях.
Эпидемиология. o В 1969 г. в городе Ласса (Нигерия) среди миссионеров возникло высококонтагиозное вирусное заболевание. В дальнейшем вспышки этой болезни наблюдались в Сьерра Леоне и Либерии. Существование очагов инфекции серологически доказано и в других странах Африки (Берег Слоновой Кости, Гвинея, Мали, Мозамбик, Сенегал и др. ). Летальность достигала 36 67%. Резервуар инфекции многососковая крыса (Mastomys natalensis), широко распространенная в Западной Африке. Характерна длительная персистенция вируса у инфицированных животных; он выделяется с мочой, слюной, обнаружен в секрете респираторного трактата. Сохраняется в высохших выделениях.
 Лихорадка Марбург o o (синонимы: болезнь Марбурга, геморрагическая лихорадка Мариди; Marburg disease англ. ) острая вирусная болезнь, характеризующаяся тяжелым течением, высокой летальностью, геморрагическим синдромом, поражением печени, желудочно кишечного тракта и центральной нервной системы. Этиология. Вирусы Марбурга и Эбола сходны по своей морфологии, но отличаются по антигенной структуре. Характерен полиморфизм, вирионы могут быть червеобразной, спиралевидной и округлой формы. Длина их колеблется от 665 до 1200 нм, диаметр поперечного сечения 70 80 нм. По ультраструктуре и антигенному составу отличаются от всех известных вирусов. Вирусные частицы содержат РНК, липопротеин; присутствия гемагглютининов и гемолизинов не выявлено. Антигенная активность связана с вирусными частицами, существования растворимого антигена не доказано. Вирусы выделяются и пассируются на морских свинках и в культуре перевиваемых клеток почки зеленой мартышки (Vero). При пассировании в культурах тканей вирус оказывает неполный цитопатический эффект или вовсе его не вызывает. Относится к семейству Filoviridae, роду Lyssavirus.
Лихорадка Марбург o o (синонимы: болезнь Марбурга, геморрагическая лихорадка Мариди; Marburg disease англ. ) острая вирусная болезнь, характеризующаяся тяжелым течением, высокой летальностью, геморрагическим синдромом, поражением печени, желудочно кишечного тракта и центральной нервной системы. Этиология. Вирусы Марбурга и Эбола сходны по своей морфологии, но отличаются по антигенной структуре. Характерен полиморфизм, вирионы могут быть червеобразной, спиралевидной и округлой формы. Длина их колеблется от 665 до 1200 нм, диаметр поперечного сечения 70 80 нм. По ультраструктуре и антигенному составу отличаются от всех известных вирусов. Вирусные частицы содержат РНК, липопротеин; присутствия гемагглютининов и гемолизинов не выявлено. Антигенная активность связана с вирусными частицами, существования растворимого антигена не доказано. Вирусы выделяются и пассируются на морских свинках и в культуре перевиваемых клеток почки зеленой мартышки (Vero). При пассировании в культурах тканей вирус оказывает неполный цитопатический эффект или вовсе его не вызывает. Относится к семейству Filoviridae, роду Lyssavirus.
 Эпидемиология. o Первые вспышки заболевания возникли в 1967 году одновременно в гг. Марбурге и Франкфурте на Майне, один больной наблюдался в это время в Югославии. Источником инфекции в основном служили ткани африканских зеленых мартышек (25 больных), были и вторичные заболевания (6 больных) у двух врачей, одной медсестры, работника морга и жены ветеринарного врача. Из 25 первично зараженных больных 7 человек умерли. В дальнейшем подобные заболевания наблюдались в Судане (район деревни Мариди, болезнь назвали лихорадкой Мариди), в Кении, ЮАР. Источником инфекции и резервуаром вируса в природе во время всех этих вспышек были африканские зеленые мартышки (Ceropithecus aethiops), у которых инфекция может протекать инаппарантно. Участие других животных в природных очагах инфекции, а также пути передачи инфекции обезьянам пока не изучены.
Эпидемиология. o Первые вспышки заболевания возникли в 1967 году одновременно в гг. Марбурге и Франкфурте на Майне, один больной наблюдался в это время в Югославии. Источником инфекции в основном служили ткани африканских зеленых мартышек (25 больных), были и вторичные заболевания (6 больных) у двух врачей, одной медсестры, работника морга и жены ветеринарного врача. Из 25 первично зараженных больных 7 человек умерли. В дальнейшем подобные заболевания наблюдались в Судане (район деревни Мариди, болезнь назвали лихорадкой Мариди), в Кении, ЮАР. Источником инфекции и резервуаром вируса в природе во время всех этих вспышек были африканские зеленые мартышки (Ceropithecus aethiops), у которых инфекция может протекать инаппарантно. Участие других животных в природных очагах инфекции, а также пути передачи инфекции обезьянам пока не изучены.
 Лихорадка Эбола o o острая вирусная высококонтагиозная болезнь, характеризуется тяжелым течением, высокой летальностью и развитием геморрагического синдрома. В 1976 г. в Южном Судане и Северном Заире вспыхнула эпидемия геморрагической лихорадки. В Судане заболело около 300 человек (умерло 151), в Заире заболело 237, из которых умерло 211 человек. Был выделен вирус в местности около реки Эбола в Заире, отсюда название лихорадка Эбола. По своим морфологическим свойствам вирус Эбола не отличается от вируса Марбург, но отличается от него в антигенном отношении. Относится также к семейству рабдовирусов, роду лиссавирусов.
Лихорадка Эбола o o острая вирусная высококонтагиозная болезнь, характеризуется тяжелым течением, высокой летальностью и развитием геморрагического синдрома. В 1976 г. в Южном Судане и Северном Заире вспыхнула эпидемия геморрагической лихорадки. В Судане заболело около 300 человек (умерло 151), в Заире заболело 237, из которых умерло 211 человек. Был выделен вирус в местности около реки Эбола в Заире, отсюда название лихорадка Эбола. По своим морфологическим свойствам вирус Эбола не отличается от вируса Марбург, но отличается от него в антигенном отношении. Относится также к семейству рабдовирусов, роду лиссавирусов.
 Этиология. o В 1976 г. в Южном Судане и Северном Заире вспыхнула эпидемия геморрагической лихорадки. В Судане заболело около 300 человек (умерло 151), в Заире заболело 237, из которых умерло 211 человек. Был выделен вирус в местности около реки Эбола в Заире, отсюда название лихорадка Эбола. По своим морфологическим свойствам вирус Эбола не отличается от вируса Марбург, но отличается от него в антигенном отношении. Относится также к семейству рабдовирусов, роду лиссавирусов.
Этиология. o В 1976 г. в Южном Судане и Северном Заире вспыхнула эпидемия геморрагической лихорадки. В Судане заболело около 300 человек (умерло 151), в Заире заболело 237, из которых умерло 211 человек. Был выделен вирус в местности около реки Эбола в Заире, отсюда название лихорадка Эбола. По своим морфологическим свойствам вирус Эбола не отличается от вируса Марбург, но отличается от него в антигенном отношении. Относится также к семейству рабдовирусов, роду лиссавирусов.
 Эпидемиология. o Резервуаром вируса в природе считаются грызуны, обитающие около жилья человека. Больной человек представляет опасность для окружающих. Были отмечены случаи вторичного и третичного распространения инфекции, в основном среди персонала госпиталя. Вирус выделяется от больных около 3 нед. Возможна передача инфекции через недостаточно простерилизованные иглы и другие инструменты.
Эпидемиология. o Резервуаром вируса в природе считаются грызуны, обитающие около жилья человека. Больной человек представляет опасность для окружающих. Были отмечены случаи вторичного и третичного распространения инфекции, в основном среди персонала госпиталя. Вирус выделяется от больных около 3 нед. Возможна передача инфекции через недостаточно простерилизованные иглы и другие инструменты.
 Аргентинская геморрагическая лихорадка o o острая вирусная болезнь, относящаяся к зоонозам с природной очаговостью. Характеризуется лихорадкой, экзантемой, разной выраженностью тромбогеморрагическим синдромом. Возбудитель вирус Хунин (по названию города, где зарегистрированы первые случаи болезни) относится к аренавирусам, к которым относятся возбудители лихорадки Ласса и боливийской геморрагической лихорадки. Вирус патогенен для новорожденных белых мышей и хомяков. Культивируют на куриных эмбрионах и в культуре перевиваемых клеток.
Аргентинская геморрагическая лихорадка o o острая вирусная болезнь, относящаяся к зоонозам с природной очаговостью. Характеризуется лихорадкой, экзантемой, разной выраженностью тромбогеморрагическим синдромом. Возбудитель вирус Хунин (по названию города, где зарегистрированы первые случаи болезни) относится к аренавирусам, к которым относятся возбудители лихорадки Ласса и боливийской геморрагической лихорадки. Вирус патогенен для новорожденных белых мышей и хомяков. Культивируют на куриных эмбрионах и в культуре перевиваемых клеток.
 o Резервуаром и источником инфекции являются грызуны Calomis laucha, Calomis musculinus. Вирусы выделялись также от гамазовых клещей. Заболеваемость характеризуется сезонностью с февраля по июнь, пик заболеваемости в мае. Заболевают преимущественно сельские жители. Заражение происходит воздушно пылевым путем, вдыхая пыль, инфицированную грызунами. Заражение может наступить и через продукты питания, инфицированные мочой грызунов. Эпидемические вспышки наблюдались ежегодно, число заболевших колебалось от 100 до 3500 человек.
o Резервуаром и источником инфекции являются грызуны Calomis laucha, Calomis musculinus. Вирусы выделялись также от гамазовых клещей. Заболеваемость характеризуется сезонностью с февраля по июнь, пик заболеваемости в мае. Заболевают преимущественно сельские жители. Заражение происходит воздушно пылевым путем, вдыхая пыль, инфицированную грызунами. Заражение может наступить и через продукты питания, инфицированные мочой грызунов. Эпидемические вспышки наблюдались ежегодно, число заболевших колебалось от 100 до 3500 человек.
 Боливианская геморрагическая лихорадка o o острая вирусная болезнь, характеризуется природной очаговостью, лихорадкой, развитием тромбогеморрагического синдрома. По клинической картине сходна с аргентинской геморрагической лихорадкой. Этиология. Возбудитель, названный вирусом Мачупо, (по названию реки в очаге заболевания) относится к аренавирусам. По своим свойствам сходен с вирусом Хунин, но отличается от него в антигенном отношении.
Боливианская геморрагическая лихорадка o o острая вирусная болезнь, характеризуется природной очаговостью, лихорадкой, развитием тромбогеморрагического синдрома. По клинической картине сходна с аргентинской геморрагической лихорадкой. Этиология. Возбудитель, названный вирусом Мачупо, (по названию реки в очаге заболевания) относится к аренавирусам. По своим свойствам сходен с вирусом Хунин, но отличается от него в антигенном отношении.
 Эпидемиология. o Резервуаром и источником инфекции являются грызуны Calomys callosus, у которых отмечается хроническое течение инфекции и выделение вируса с мочой. Инфицирование человека может происходить через загрязненные грызунами воду и продукты, а также при вдыхании инфицированной пыли. Наблюдались случаи заражения людей от больного человека. Заболевание наблюдается в течение всего года. Распространено в некоторых районах Боливии. За период с 1959 по 1963 г. из общего числа проживающих в эндемичном регионе 4000 6000 переболело 750 человек.
Эпидемиология. o Резервуаром и источником инфекции являются грызуны Calomys callosus, у которых отмечается хроническое течение инфекции и выделение вируса с мочой. Инфицирование человека может происходить через загрязненные грызунами воду и продукты, а также при вдыхании инфицированной пыли. Наблюдались случаи заражения людей от больного человека. Заболевание наблюдается в течение всего года. Распространено в некоторых районах Боливии. За период с 1959 по 1963 г. из общего числа проживающих в эндемичном регионе 4000 6000 переболело 750 человек.