БХ КРОВИ-1.ppt
- Количество слайдов: 55

ГБУ ВПО «Башкирский государственный медицинский университет» Министерства здравоохранения и социального развития РФ БИОХИМИЯ КРОВИ - 1 Лекция для студентов II курса лечебного факультета профессора Князевой О. А.

• Кровь – жидкая внутренняя среда организма, общий объем ~ 7% от массы тела – 5 -6 л, состоит из плазмы (55%) и форменных элементов (эритроцитов, лейкоцитов, тромбоцитов).

Функции крови • • • 1. Транспортная: трофическая - транспорт пит. в-в; выделительная - транспорт конечных метаболитов; дыхательная - транспорт газов: О 2, СО 2

2. Защитная: • неспецифические и специфические защитные факторы; • система свертыванияпротивосвертывания крови

• • 3. Регуляторная: поддержание осмотического и онкотического давления; • поддержание кислотнощелочного баланса; • поддержание водного баланса; • терморегуляторная.

• Плазма крови представляет собой кровь, лишенную клеточных элементов, а сыворотка крови – кроме того лишена и фибриногена.

• В состав плазмы входит вода (90 -91%) и большое число неорганических и органических соединений, из которых 6, 6 -8, 5% белки

Общее содержание белка составляет: • у новорожденных – 47 -70 г/л; • у 6 -12 месячных – 60 -80 г/л; • к 3 -5 годам – 65 -85 г/л.

В плазме здорового человека выявляется 5 основных фракций: • • • А α 1 α 2 β γ Взрослые 55 -60% 3 -6% 5 -9% 7 -14% 14 -22% 6 -12 мес 50 -60% 6 -8% 8 -12% 12 -18% 10 -16%
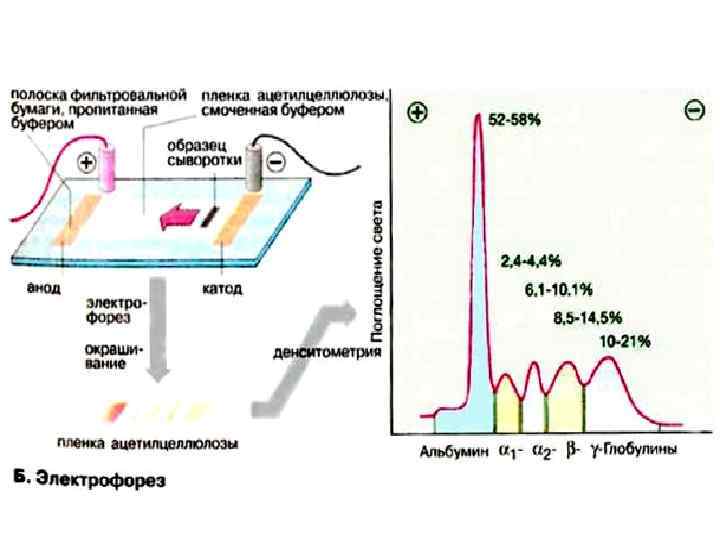

Альбумин • М. м. ~ 66300 Д, Д • концентрация 35 -45 г/л • Молекула имеет глобулярную форму и при воспалительных состояниях легко проходит через сосудистую стенку. • При воспалении почек – в моче протеинурия.

• Особенность – способность связывать б. ч. различных соединений: жирные кислоты, стероиды, билирубин, гемин, органические красители, ЛВ (салицилаты, сульфамидные средства, барбитураты, антибиотики), ионы Са, Cu и т. д.

Функции: • 1) транспортная • 2) регуляция коллоидноосмотического давления плазмы • 3) поддержание белкового резерва организма
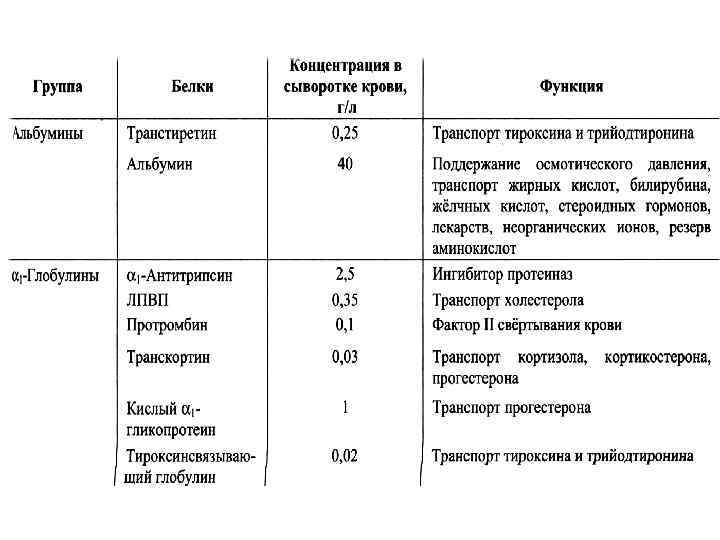
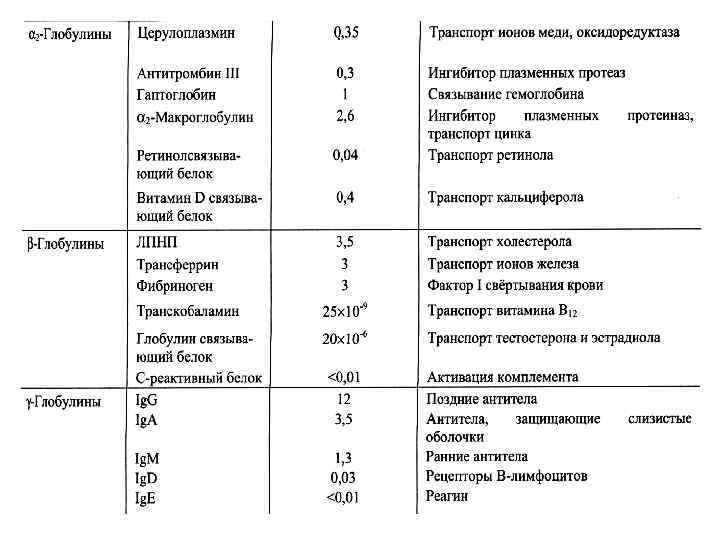

α- глобулины • Ингибиторы протеаз: α 1 -антитрипсин, α 2 макроглобулин, интер-αтрипсиновый ингибитор, α 1 антихимотрипсин, антитромбин, антиплазмин и др.

• Церулоплазмин – белок острой фазы. Транспортер меди и цинка, регулятор обмена меди в печени, антиоксидант, полиаминооксидаза.

β-глобулины • Гемопексин - связывает и транспортирует гем. • С-реактивный белок – белок острой фазы: с= 0, 01 г/л. С ↑ при о. инфекциях, витамин-К-зависимый ингибитор ССК, стимулирующий фибринолиз, играет роль в иммунных процессах, фагоцитозе.

Белки острой фазы Стимулируют синтез белков острой фазы ~ 30 белков: • провоспалительные интерлейкины (1, ФНО, 6, 11, γинтерферон); • глюкокортикоиды; • факторы роста

• • • Резко ↑ концентрация Среактивного белка – в 100 -1000 раз. ~ в 2 раза: - α 1 -антитрипсина - α 1 -кислого гликопротеина - гаптоглобина - фибриногена ~ в 1, 5 раза: - С 3 и С 4 факторов комплемента - церулоплазмина

Общие функции белков острой фазы: • - повышение опсонизации бактерий и др. клеток; • - антипротеазная активность; • - связывание свободных радикалов; • - бактериостатическое действие; • - активация комплемента; • - усиление свертывания крови.

• • Функции некоторых белков острой фазы: - С-реактивный белок – опсонин, увеличивает фагоцитоз (в 20 1000 раз); - α 1 -антитрипсин – ингибитор трипсина; - α 2 - макроглобулин – ингибитор протеаз; - С 3, С 4, пропердин – увеличение активности комплемента;

• - протромбин – свертывание крови; • - плазминоген – фактор фибринолиза; • - церулоплазмин – транспорт Cu, оксидаза; • - ферритин – связывание железа; • - гаптоглобин – ингибитор катепсинов, связывание свободного гемоглобина.

• • Т. о. , белки крови выполняют различные функции: - транспортную; - защитную; - коллоидо-осмотическую (при ↓ С до 45 г/л – отеки); - трофическую; - поддержание р. Н ; - гормональную (белки-гормоны); - ферментативную (белкиферменты)

• а) конститутивные – выполняют специальные функции (белкиферменты калликреинкининовой системы, белки системы гемостаза, белки системы комплемента и др. );

• б) индикаторные ферменты – это ферменты, не имеющие специализированной функции, поступающие частично из тканей при цитолизе, при ↑ проницаемости клеточных мембран, особенно их С в плазме ↑ при воспалении, инфаркте, дистрофии и др.

Б. ч. из них обладает тканевой специфичностью: • печень → Ал. АТ, Ас. АТ, ЛДГ, альдолаза, холинэстераза; • поджелудочная железа → амилаза, липаза, трипсин, эластаза; • миокард → креатинфосфокиназа, ЛДГ, Ас. АТ и др. ; • простата → кислая фосфатаза.
![• Белки плазмы синтезируются в печени на 80%: Печень ↔ [белки плазмы крови] • Белки плазмы синтезируются в печени на 80%: Печень ↔ [белки плазмы крови]](https://present5.com/presentation/3/12786480_169944478.pdf-img/12786480_169944478.pdf-28.jpg)
• Белки плазмы синтезируются в печени на 80%: Печень ↔ [белки плазмы крови] ↔ тканевые белки

Небелковые компоненты • Неорганические: Na, K, Ca, Mg, P, Cl, F, I, Fe, Cu, Mn и др. • Органические: - содержащие азот (амины, аминокислоты, аммиак, мочевина, креатинин, глутатион, пептиды, билирубин и др. )

- углеводы – глюкоза, галактоза, фруктоза и др. - метаболиты – лактат, пируват, цитрат и др. - липиды – холестерин, ТАГ, ФЛ и др. - кетоновые тела.

Поддержание кислотнощелочного баланса: • 1. Буферные системы крови • 2. Система дыхания • 3. Мочевыделительная система

Буферные системы крови 1 – бикарбонатная (10% всей буферной емкости) H 2 CO 3 ↔ H+ + HCO 32 – фосфатная (1% от буф. емк. крови) H 2 PO 42 - ↔ H+ + HPO 4 -

3 – белковая 4 – гемоглобиновая (75% от всей буф. емк. крови): НHb ↔ H+ + КHb оксигемоглобиновая: НHb. О 2 ↔ H+ + КHb. О 2
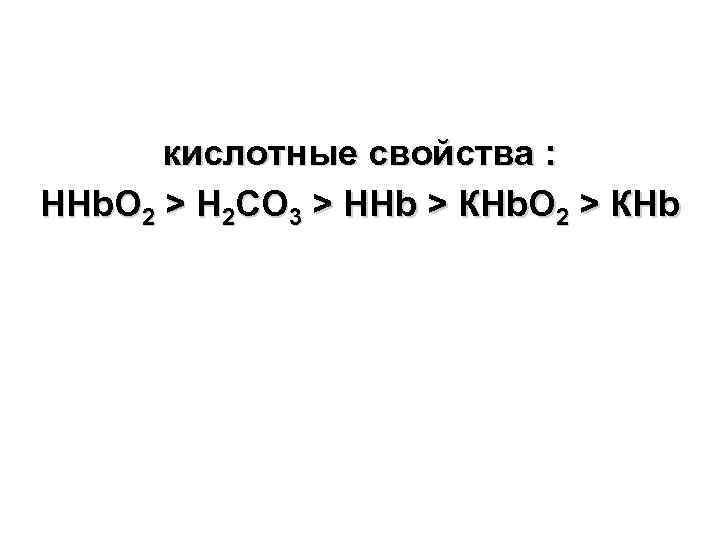
кислотные свойства : НHb. О 2 > H 2 CO 3 > НHb > КHb. О 2 > КHb

• Буферные св-ва Hb - за счет способности к взаимодействию кислых соединений с КHb Н-р: КHb + H 2 CO 3 → КHCO 3 + НHb

Попадая в капилляры легких, НHb, превращается в НHb. О 2 → подкисление крови → вытеснению части H 2 CO 3 из бикарбонатов и → ↓ щелочного резерва крови (способности крови связывать СО 2)

Присоединение О 2 к НHb постепенно: от 1 мол. О 2 до 4 -х (1 г НHb - 1, 34 мл О 2)

Взаимодействие О 2 с Hb зависит: • 1 - от парциального давления О 2 Проявляется кооперативный эффект: после присоединения 1 -й мол-лы О 2 сродство НHb к О 2 резко ↑ Поэтому V последующих реакций резко ↑
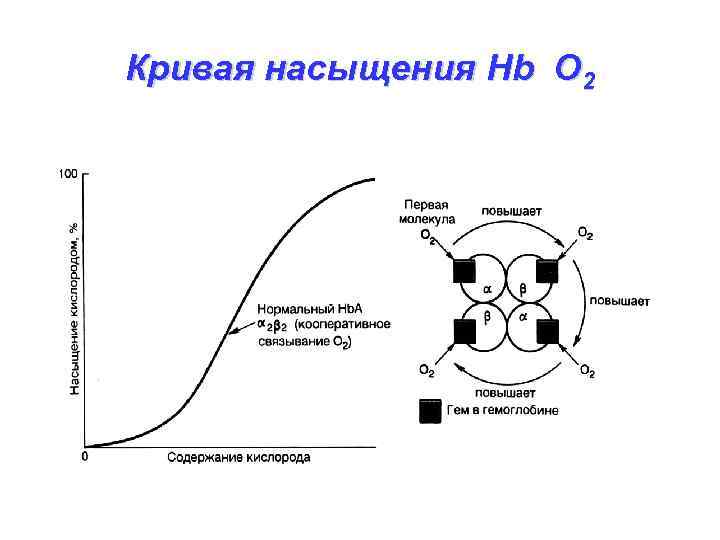
Кривая насыщения Hb O 2

2 - от р. Н: чем > кислая среда, тем сродство НHb к О 2 ↓, поэтому диссоциация НHb. О 2 в кислой среде ↑ 3 - от tо: чем < tо, тем легче образуется НHb. О 2, поэтому при высокой tо гипоксия

4 - от концентрации газа: чем > концентрация, тем сродство НHb к О 2 ↓ и диссоциация НHb. О 2 ↑

• • • Гипоксия – недостаточное поступление О 2: - экзогенная – мало О 2 во вдыхаемом воздухе, - дыхательная – недостаточная функция легких, - циркуляторная – нарушение кровообращения, - гемическая – ↓ кислородной емкости крови, - тканевая – ↓ утилизации О 2 в тканях.

Перенос СО 2 • Основная масса СО 2 переносится в растворенном виде плазмой крови, лишь 3 -8 % СО 2 связывается с Hb в виде карбаминов: • Hb-NH 2 + H 2 CO 3 ↔ Hb-NH-COОН

СО 2 + Н 2 О ↔ Н 2 СО 3 ↔ Н+ + НСО 3 - • В капиллярах тканей СО 2 ↑ и реакция смещается вправо. • В легких удаление СО 2 смещает равновесие влево.

• Сродство Hb к О 2 в присутствии СО 2 резко ↓, СО 2 выталкивает О 2 из НHb. О 2 в тканях. • В легких, наоборот, О 2 вытесняет СО 2 из крови в альвеолярный воздух.

НHb. О 2 > H 2 CO 3 > НHb > КHb. О 2 > КHb • H 2 CO 3 способна вытеснять Hb из его солей, превращаясь в бикарбонат: H 2 CO 3 + КHb → КHCO 3 + НHb
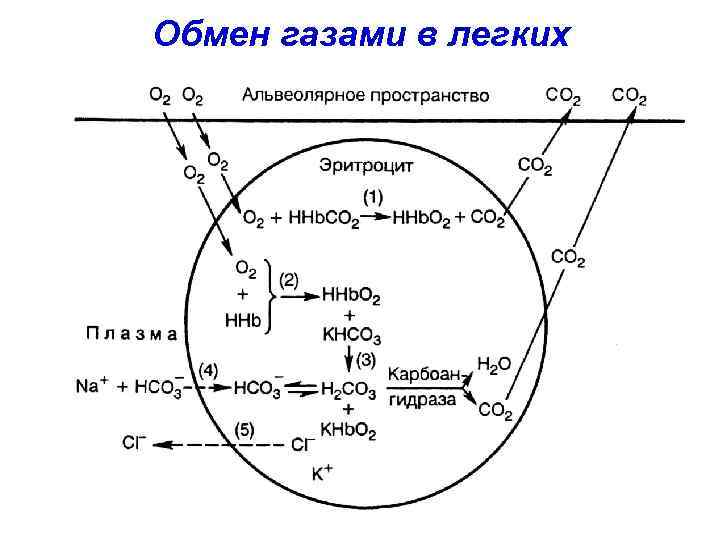
Обмен газами в легких
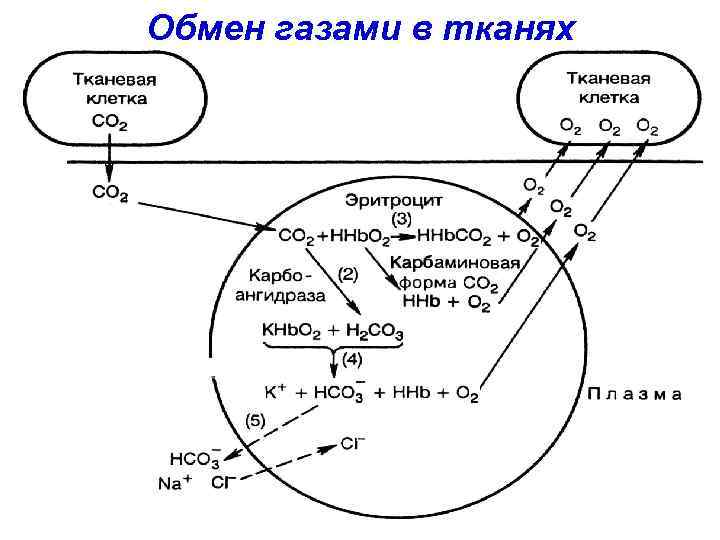
Обмен газами в тканях

Биохимия эритроцитов (Е) • Образуются из стволовых клеток костного мозга • Т - 120 сут • Размножение и превращение начальных клеток Е стимулирует цитокин ИЛ-3 • Далее пролиферацию и дифференцировку регулирует гормон эритропоэтин

• В качестве энергетического материала Е используют только глюкозу, которая поступает с помощью ГЛЮТ-2 и используется • в анаэробном гликолизе ~ 90% • в ПФ пути ~ 10%

• Особенность гликолиза в Е наличие шунта, приводящего к образованию 2, 3 -ДФГ, который взаимодействует с KHb. O 2: 2, 3 -ДФГ + KHb. O 2 → KHb-2, 3 -ДФГ +О 2 • в условиях гипоксии ↑ [2, 3 -ДФГ ] и диссоциация KHb. O 2
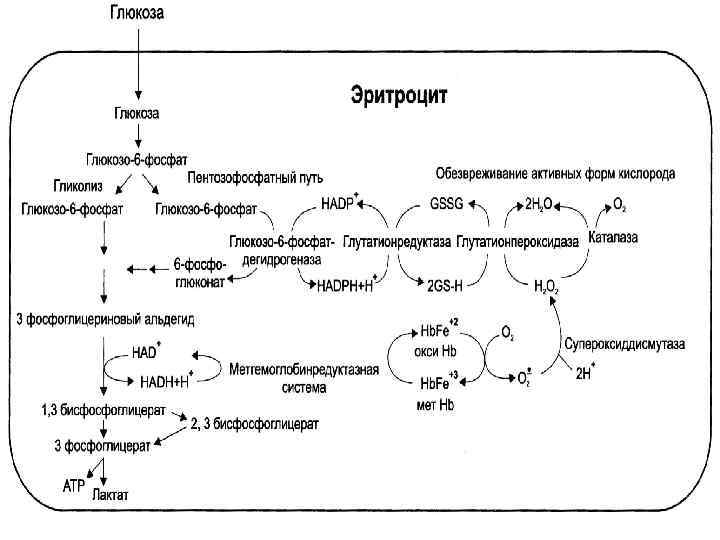

• НАДФН необходим Е для восстановления глутатиона: Глу. S-SГлу → 2 Глу. SH • Глу. SH участвует в разрушении Н 2 О 2 с помощью СОД и Глу. SHпероксидазы

• В Е имеются отдельные ферменты ЦТК, ДЦ, β- окисления ЖК • Синтез ФЛ • Синтез НТ - за счет реутилизации азотистых оснований • Белки не синтезируются • Высокая [K+] и низкая – [Na+] (в плазме наоборот)

Функции Е • дыхательная функция транспорт О 2 и СО 2 (95% сух. ост. НHb ~1 млн м-л) • участвуют в транспорте: пептидов, АМК, белков
БХ КРОВИ-1.ppt