лекция 4 Биологич. окисление 2012.ppt
- Количество слайдов: 112

ГБОУ ВПО УГМА Минздравсоцразвития России Кафедра биохимии Лекция 4 Биологическое окисление: пути использования кислорода в тканях, цикл Кребса Екатеринбург - 2012

План лекции • • 1. История развития учения о биологическом окислении. Теории Баха, Палладина. 2. Современные представления о БО. 3. Окислительно-восстановительные системы, потенциалы. 4. Кислород – сильный окислитель. Пути использования в клетке (оксидазный, моно- и диоксигеназный, пероксидазный). 5. Этапы утилизации энергии питательных веществ. 6. Перевод биополимеров в мономеры. 7. Частичное расщепление мономеров (моноуглеводов, аминокислот, жирных кислот) до субстратов биологического окисления (СБО) – анаэробное окисление.

• 8. Окисление субстратов биологического окисления до СО 2 и Н 2 О. • 9. Цикл Кребса (цикл лимонной кислоты, цикл трикарбоновых кислот - ЦТК). • 10. Открытие ЦТК. • 11. Реакции ЦТК. Ферменты ЦТК (номенклатура), коферменты (строение). • 12. Энергетический баланс ЦТК. • 13. Субстратное фосфорилирование. • 14. Окислительное фосфорилирование • 15. Анаболическая функция ЦТК. • 16. Регуляция ЦТК.

• • • Влияние на скорость реакции ЦТК: Концентрации ацетилкоэнзима А и оксалоцетата. Активности цитратсинтазы и регуляторных ферментов (СДГ, α-КГДГ, изо-ЦДГ). Скорость окисления НАДН в НАД+. Концентрации АТФ, АДФ, АМФ. Концентрации кислорода (дыхательная цепь). 17. Витамин РР. Строение вит. РР. Участие в образовании НАД+, механизм действия. Источники витамина РР. Метаболические нарушения при его недостаточности. Клинические проявления.

Определение понятия • Биологическое окисление – совокупность окислительновосстановительных реакций в организме

История развития учения о биологическом окислении (БО) I. А. Лавуазье 1777 г. : «горение - процесс соединения веществ с О 2, горение и дыхание - один процесс» Отличия дыхания от горения : ü Идет при низкой температуре ü без пламени ü в присутствии воды

II. А. Н. Бах 1897 г. «ПЕРЕКИСНАЯ ТЕОРИЯ МЕДЛЕННОГО ОКИСЛЕНИЯ» О 2 активируется в результате разрыва одной связи (-О-О-) --> присоединяется к оксидазам --> из окисляемого субстрата (S) образуется перекись:
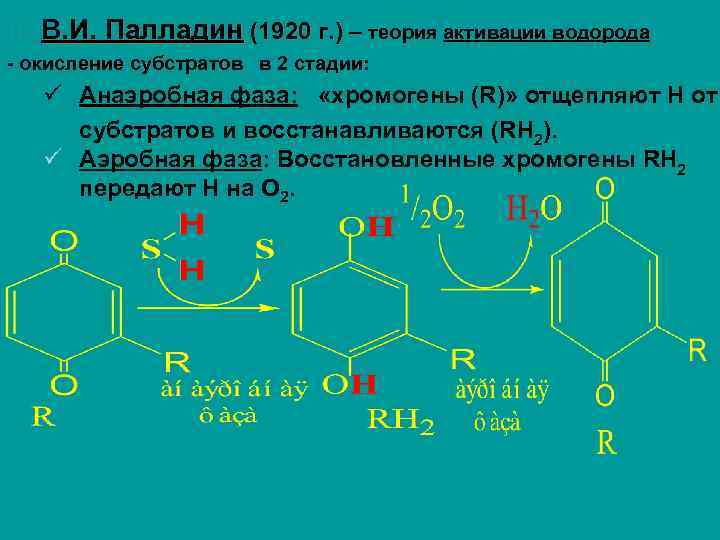
III. В. И. Палладин (1920 г. ) – теория активации водорода - окисление субстратов в 2 стадии: ü Анаэробная фаза: «хромогены (R)» отщепляют Н от субстратов и восстанавливаются (RH 2). ü Аэробная фаза: Восстановленные хромогены RH 2 передают Н на О 2.

IV. Современный этап (2 половина 20 века) ü Кейлин Дейвид: «цитохромы способны передавать H+ и e- с окисляемого S на O 2. » ü Шенбайн : БО – каталитический процесс, в котором используется активный кислород. ü О. Варбург - фермент – цитохромоксидаза. «БО - это дегидрирование и активирование О 2» .
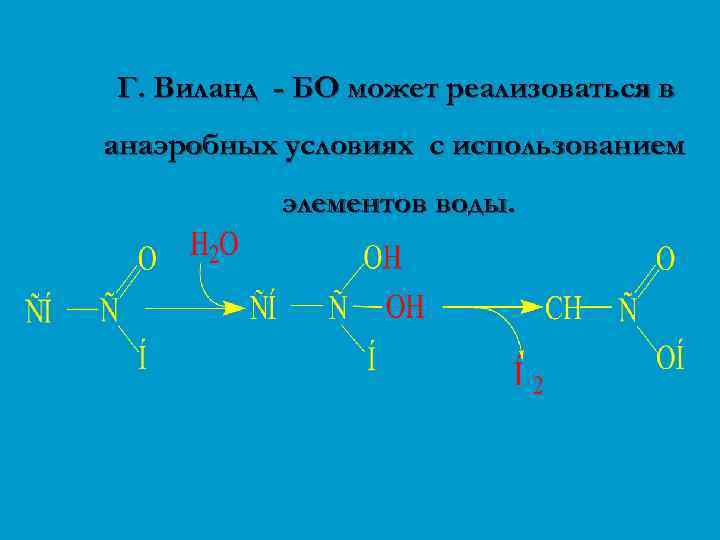
Г. Виланд - БО может реализоваться в анаэробных условиях с использованием элементов воды.

Современные представления о БО 1. происходит аэробно или анаэробно; 2. в аэробных организмах существует несколько путей использования О 2; 3. реакции БО необходимы для: ü получения энергии; ü синтеза новых веществ; ü разрушения чужеродных веществ; 4. многостадийный процесс с ведущей ролью оксидоредуктаз.

Основные понятия ü Окислительно-восстановительные реакции (ОВР) – реакции, в которых меняется степень окисления субстрата (S) за счет присоединения/отщепления: 1 е‾; 2 е‾ и 2 Н+; Атомов кислорода; ü Биологическое окисление (БО) – совокупность ОВР, которые протекают в живых клетках;

ü Субстрат БО – вещество, способное отдавать е ; ־ ü Тканевое дыхание – окисление органических веществ в клетках, сопровождающееся потреблением О 2 и выделением воды; ü Субстрат тканевого дыхания – это вещество, которое отдает электрон в цепь окислительного фосфорилирования;

ü Дыхательная цепь – цепь переноса электронов от субстратов БО к О 2 –по мере увеличения сродства к электрону располагаются ее элементы: 1. НАД– и НАДФ–зависимые ДГ(ИДГ, альфа-КГДГ); 2. ФАД– и ФМН– зависимые ДГ (СДГ); 3. Коэнзим Q; 4. Цитохромы; и Белки, содержащие негеминовое железо.

Редокс-потенциалы В окислительно-восстановительной системе участвует окисленная и восстановленная формы одного соединения, которые образуют Редокс–пару. ü Разные редокс–пары обладают различным сродством к е . ־ Мерой сродства служит Редокс–потенциал (Ео'). Т. о. направленность движения е , ־ их поступление на определенные акцепторы определяется величиной Ео'.
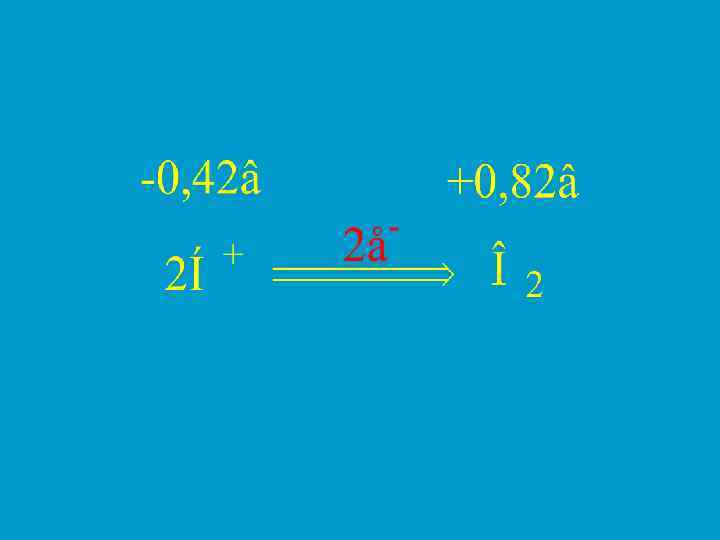

Пути использования О 2 в клетке 1. Оксидазный – основной потребитель кислорода Функция: 90% О 2 используется для синтеза АТФ из АДФ и Ф; 2. Монооксигеназный (Обеспечивает включение 1 атома кислорода в молекулу субстрата) Функции: ü синтез новых веществ, ü обезвреживание ксенобиотиков;

3. Диоксигеназный (Обеспечивает включение молекулы кислорода в молекулу субстрата) Функция: ü деградация АК; ü синтез новых веществ; 4. Пероксидазный и свободнорадикальный Функции: ü внутриклеточное пищеварение; ü разрушение бактерий, вирусов, онко- и стареющих клеток; ü образование БАВ - регуляторов
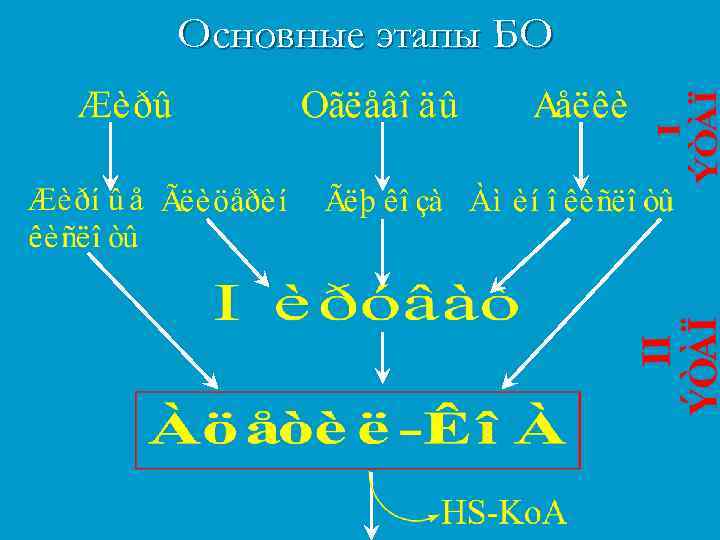
Основные этапы БО

NB!!! n Ацетил-Ко. А – универсальный продукт катаболизма углеводов, белков, липидов, основной субстрат ЦТК
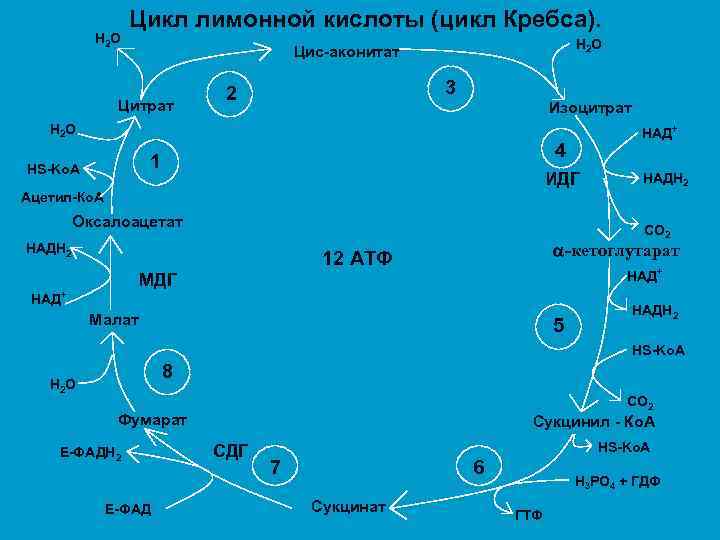
Н 2 О Цикл лимонной кислоты (цикл Кребса). Н 2 О Цис-аконитат Цитрат 3 2 Изоцитрат Н 2 О 4 1 HS-Ko. A НАД+ ИДГ НАДН 2 Ацетил-Ко. А Оксалоацетат СО 2 НАДН 2 -кетоглутарат 12 АТФ НАД+ МДГ НАД+ Малат 5 НАДН 2 НS-Ko. A 8 Н 2 О CO 2 Фумарат Е-ФАДН 2 Е-ФАД Сукцинил - Ко. А СДГ HS-Ko. A 7 6 Сукцинат H 3 PO 4 + ГДФ ГТФ
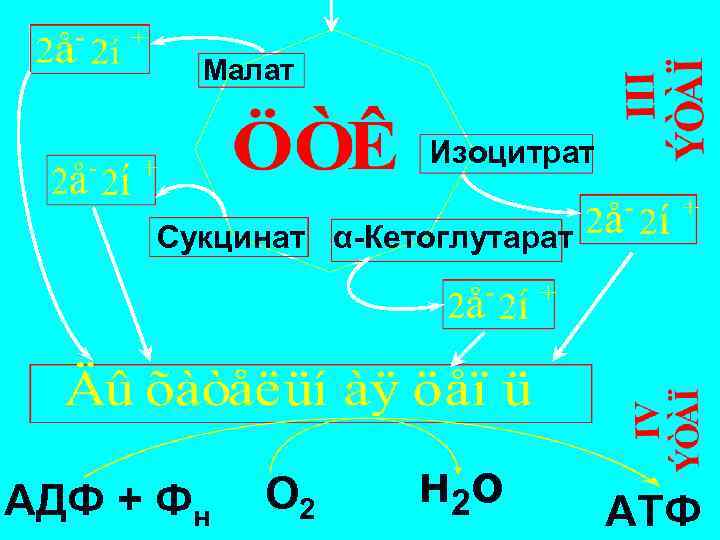
Малат Изоцитрат Сукцинат α-Кетоглутарат АДФ + Фн О 2 н 2 о АТФ

Конечные продукты катаболизма - В БО - Н 2 О и СО 2 (В обмене белков и нуклеиновых кислот – мочевина и мочевая кислота).

Значение этапов БО I. Гидролиз полимеров белков, полисахаридов, триглицеридов до мономеров всасываются в кровь в промежуточный обмен. II. В ходе катаболизма Мономеры (моносахара, жирные кислоты и аминокислоты) превращаются в универсальное вещество – Ацетил–Ко. А.

3. 4. В ЦТК из Ацетил–Ко. А образуются субстраты тканевого дыхания: изоцитрат, α–КГ, сукцинат и малат. Окисление субстратов тканевого дыхания восстановление коферментов НАДН 2 и ФАДН 2 отдают протоны в редокс–цепь окислительного фосфорилирования

ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦИКЛ КРЕБСА) ü процесс окисления Ацетил–Ко. А универсального продукта катаболизма углеводов, жиров и белков; ü протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе или на внутренней поверхности внутренней мембраны МХ; ü участвуют 5 витаминов В 1, В 2, РР, пантотеновая кислота и липоевая кислота в виде коферментов тиаминпирофосфата, ФАД, НАД+, Ко. А и липоата.
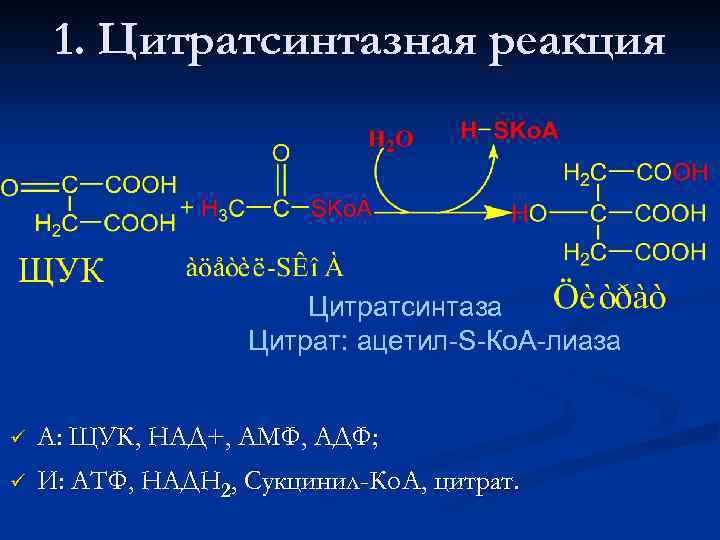
1. Цитратсинтазная реакция Цитратсинтаза Цитрат: ацетил-S-Ко. А-лиаза ü А: ЩУК, НАД+, АМФ, АДФ; ü И: АТФ, НАДН 2, Сукцинил-Ко. А, цитрат.

2. Аконитазная реакция Аконитаза Цитрат: гидро-лиаза ü Аконитаза Цитрат: гидро-лиаза Аконитаза взаимодействует с цитратом ассиметрично: она всегда действует на ту часть молекулы цитрата, которая образовалась из оксалоацетата. Возможно, что цис-аконитат не является обязательным между цитратом и изоцитратом и образуется на боковой ветви основного пути.
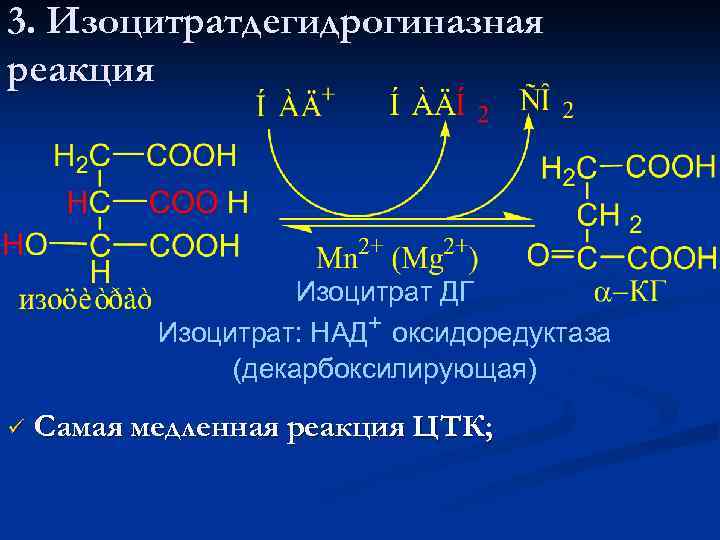
3. Изоцитратдегидрогиназная реакция Изоцитрат ДГ Изоцитрат: НАД+ оксидоредуктаза (декарбоксилирующая) ü Самая медленная реакция ЦТК;

Витамин РР (никотинамид, антипеллагрический витамин)
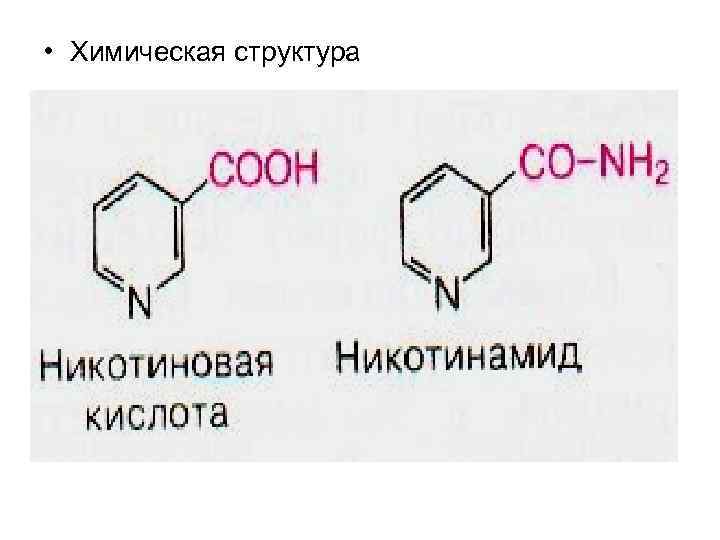
• Химическая структура
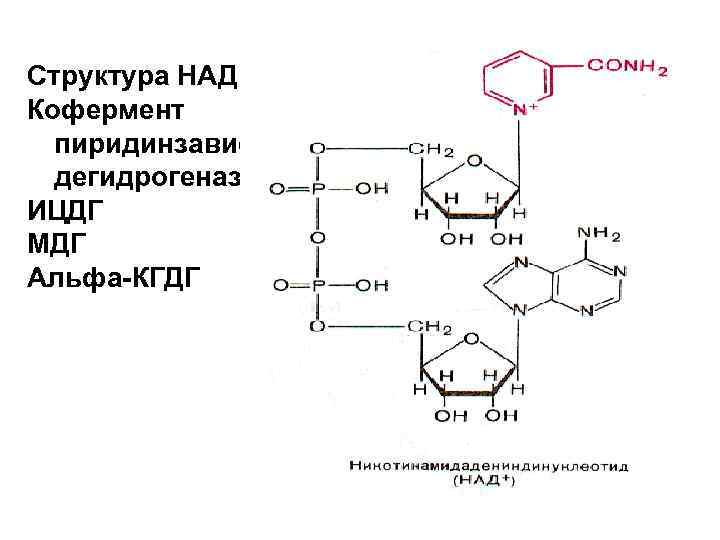
Структура НАД – Кофермент пиридинзависимых дегидрогеназ ИЦДГ МДГ Альфа-КГДГ
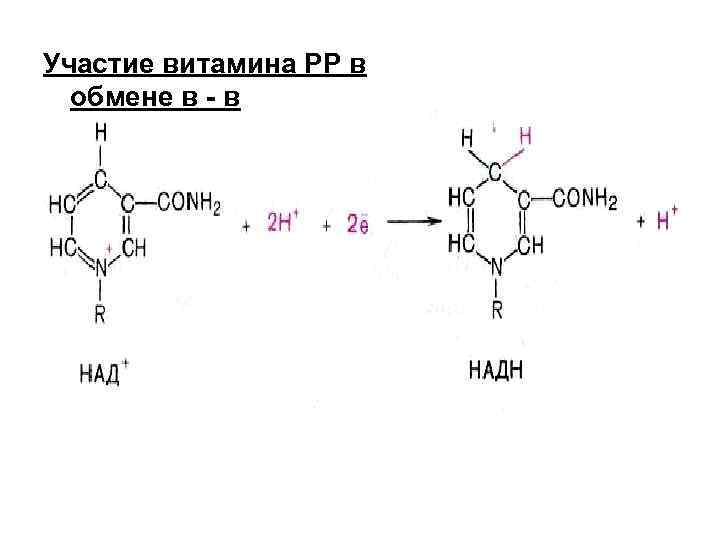
Участие витамина РР в обмене в - в
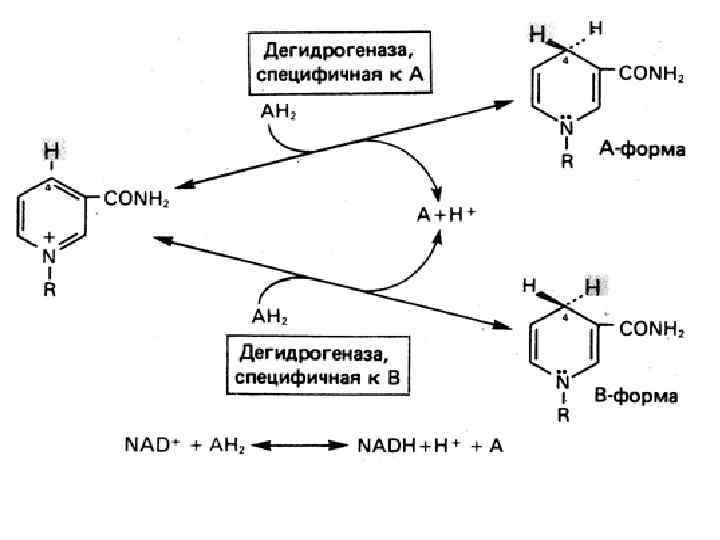
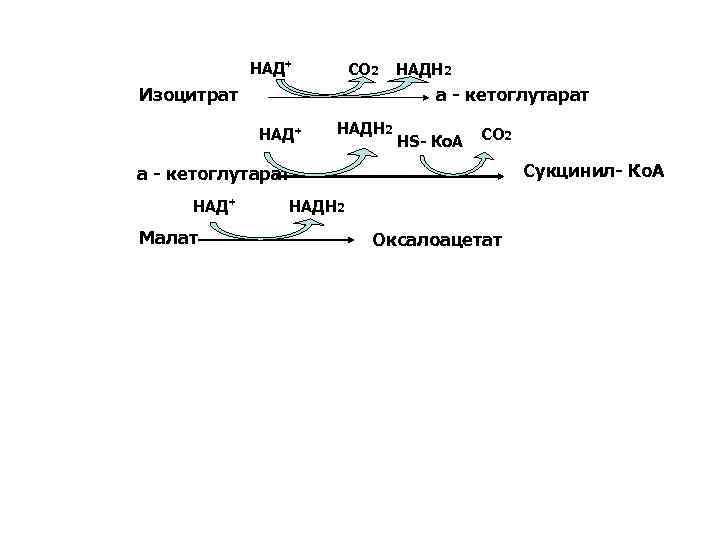
НАД+ СО 2 Изоцитрат НАДН 2 а - кетоглутарат НАД+ НАДН 2 НS- Ко. А СО 2 Сукцинил- Ко. А а - кетоглутарат НАД+ Малат НАДН 2 Оксалоацетат
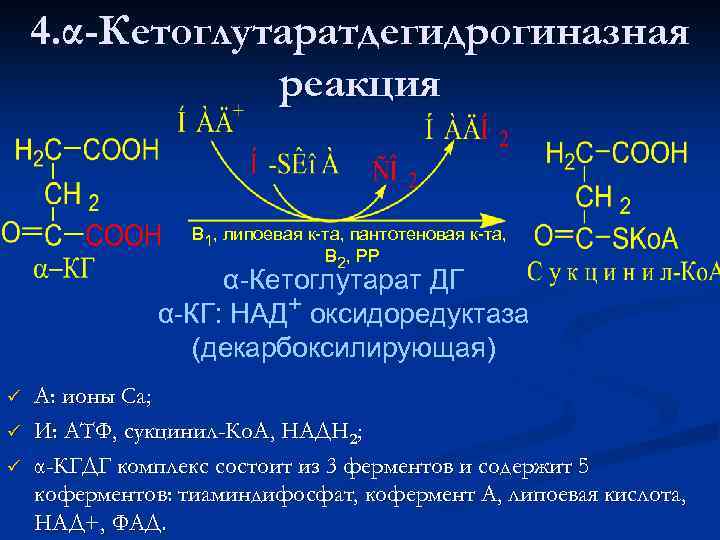
4. α-Кетоглутаратдегидрогиназная реакция В 1, липоевая к-та, пантотеновая к-та, В 2, РР α-Кетоглутарат ДГ α-КГ: НАД+ оксидоредуктаза (декарбоксилирующая) ü ü ü А: ионы Са; И: АТФ, сукцинил-Ко. А, НАДH 2; α-КГДГ комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД.
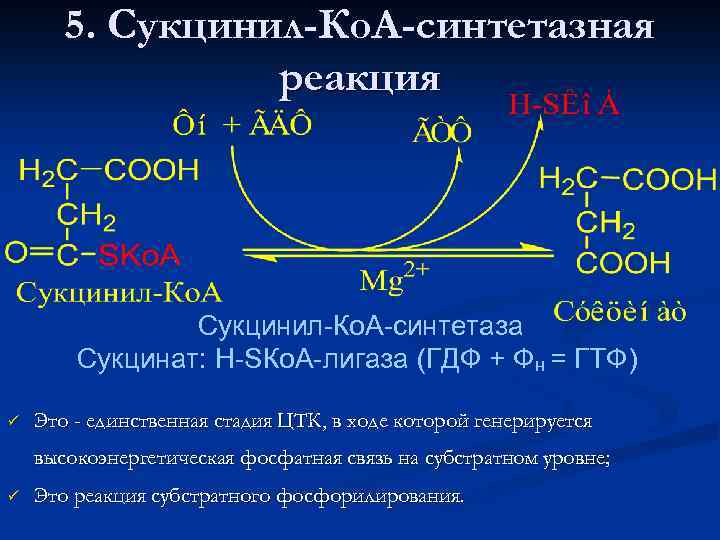
5. Сукцинил-Ко. А-синтетазная реакция Сукцинил-Ко. А-синтетаза Сукцинат: Н-SКо. А-лигаза (ГДФ + Фн = ГТФ) ü Это - единственная стадия ЦТК, в ходе которой генерируется высокоэнергетическая фосфатная связь на субстратном уровне; ü Это реакция субстратного фосфорилирования.
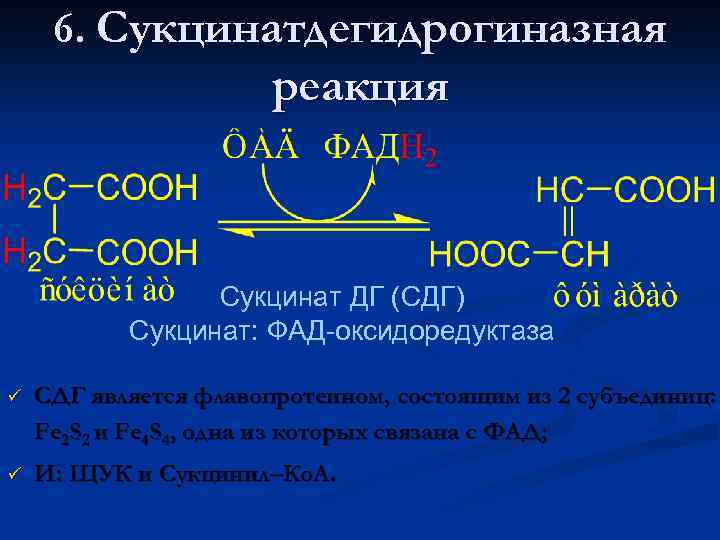
6. Сукцинатдегидрогиназная реакция Сукцинат ДГ (СДГ) Сукцинат: ФАД-оксидоредуктаза ü СДГ является флавопротеином, состоящим из 2 субъединиц: Fe 2 S 2 и Fe 4 S 4, одна из которых связана с ФАД; ü И: ЩУК и Сукцинил–Ко. А.

n ФАД – кофермент флавинзависимых дегидрогеназ (СДГ сукцинатдегидрогеназа)
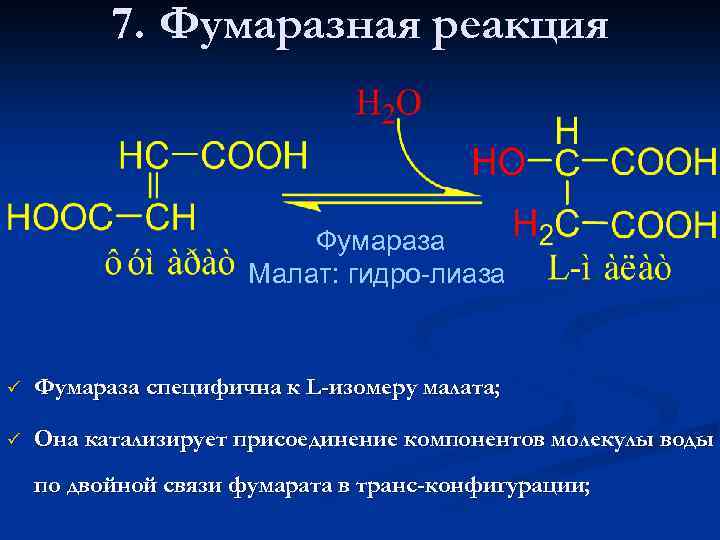
7. Фумаразная реакция Фумараза Малат: гидро-лиаза ü Фумараза специфична к L-изомеру малата; ü Она катализирует присоединение компонентов молекулы воды по двойной связи фумарата в транс-конфигурации;
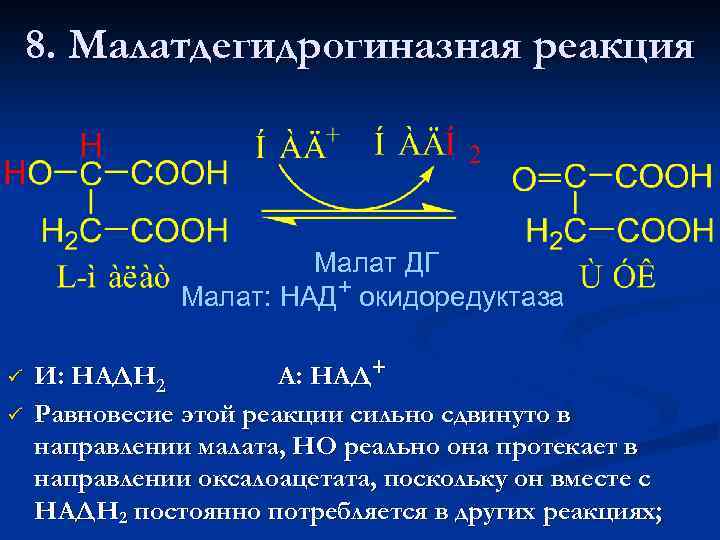
8. Малатдегидрогиназная реакция Малат ДГ Малат: НАД+ окидоредуктаза ü ü И: НАДН 2 А: НАД+ Равновесие этой реакции сильно сдвинуто в направлении малата, НО реально она протекает в направлении оксалоацетата, поскольку он вместе с НАДН 2 постоянно потребляется в других реакциях;
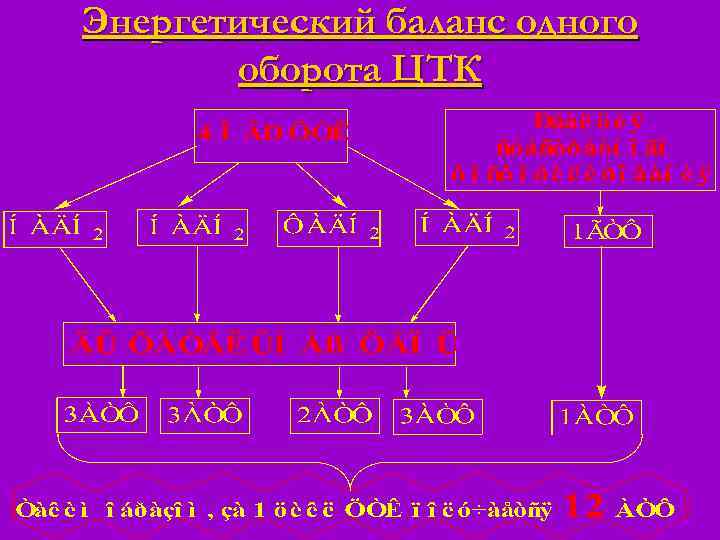
Энергетический баланс одного оборота ЦТК

NB!!! Окисление 1 молекулы Ацетил-Ко. А в ЦТК дает n 12 молекул АТФ n 3 молекулы НАДН 2 n 1 ФАДН 2

NB !!! Основные субстраты биологического окисления: n Изоцитрат n Альфа-кетоглутарат n Сукцинат n Малат

Окислительное фосфорилирование - синтез АТФ из АДФ и Н 3 РО 4 за счет энергии движения электронов по дыхательной цепи. происходит на внутренней мембране митохондрий.
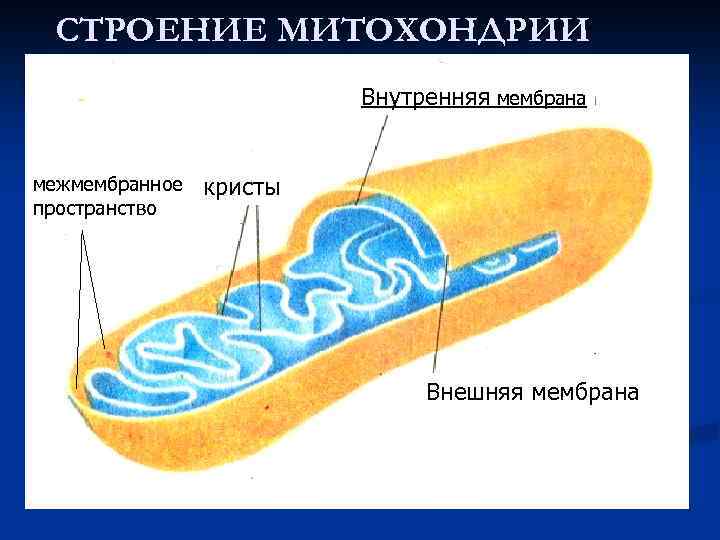
СТРОЕНИЕ МИТОХОНДРИИ Внутренняя мембрана межмембранное пространство кристы Внешняя мембрана

История окислительного фосфорилирования Исследовано английским ученым П. Митчеллом. В 1966 г. сформулировал хемиосмотическую гипотезу. В 1978 г. - Нобелевская премия

Хемиосмотическая теория Митчелла 1) Внутренняя мембрана митохондрий непроницаема для всех ионов. 2) Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов. 3) При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+ из матрикса в межмембранное пространство. 4) При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровож дается синтезом АТФ.

Основатели хемиосмотической теории Питер Митчелл Владимир Скулачев
Окислительное Фосфорилирование Процесс окисления Процесс фосфорилирования

75 -ЛЕТИЕ ОТКРЫТИЯ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ В. А. ЭНГЕЛЬГАРДТОМ В КАЗАНИ Д. М. Зубаиров, И. Г. Мустафин Казанский государственный медицинский университет

Кафедра биохимии медицинского факультета Казанского университета n Первые шаги биологической химии в России тесно связаны с подъемом и расцветом казанской школы химиков. Первая кафедра биологической химии была основана в Казанском университете в 1963 -1964 годах. Решающее влияние как на создание кафедры, так и на становление ее руководителя проф. А. Я. Данилевского оказал А. М. Бутлеров.

Бутлеровский институт Казанского университета


Владимир Александрович Энгельгардт в лаборатории кафедры биохимии Казанского мединститута открыл окислительное фосфорилирование в 1931 году.

Манометры к аппарату О. Варбурга. n Манометры к аппарату Варбурга, на которых В. А. Энгельгардт открыл окислительное фосфорилирование, в музее кафедры биохимии Казанского медицинского университета
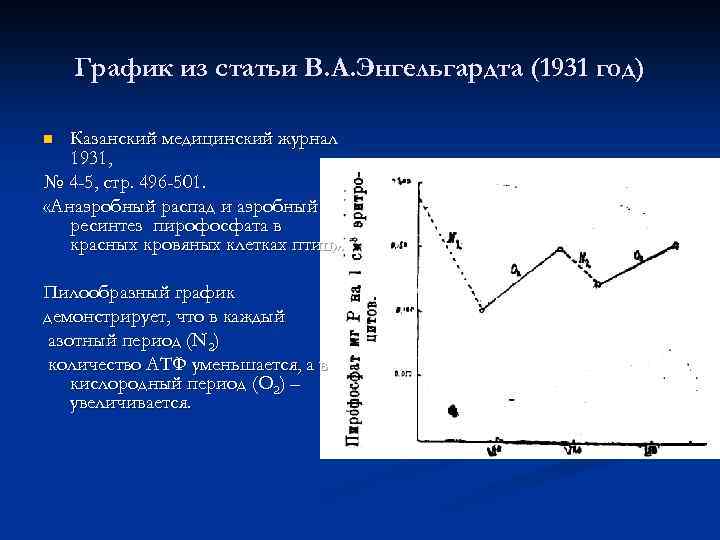
График из статьи В. А. Энгельгардта (1931 год) Казанский медицинский журнал 1931, № 4 -5, стр. 496 -501. «Анаэробный распад и аэробный ресинтез пирофосфата в красных кровяных клетках птиц» . n Пилообразный график демонстрирует, что в каждый азотный период (N 2) количество АТФ уменьшается, а в кислородный период (О 2) – увеличивается.

Университетская, дом 13

Премия Академии Наук РТ им. В. А. Энгельгардта n n Энгельгардт В. А. оставил глубокий след в истории мировой науки, который восхищает искусством понимания внутренних закономерностей, происходящих в живых организмах. Учреждение регулярной премии имени В. А. Энгельгардта по биологическим наукам – не только дань памяти гениальному ученому, но и ориентир высокого полета научной мысли для новых поколений ученых.

Владимир Александрович Белитцер n Впервые ввёл понятие коэффициента фосфорилирования — отношения связанного фосфата к поглощённому кислороду.



П. Митчел. n В 1961 году Питер Митчел опубликовал статью «Сопряжение окисления и фосфорилирования механизмом хемиосмотического типа» [Mitchell P. Coupling of phosphorylation to electron and hydrogen transfer by a chemiosmotic type of mechanism. Nature. 1961, 191, p. 144 -148]. П. Митчел открыл, что ток электронов вызывает выброс, катапультирование, протонов из матрикса митохондрий в межмембранное пространство.
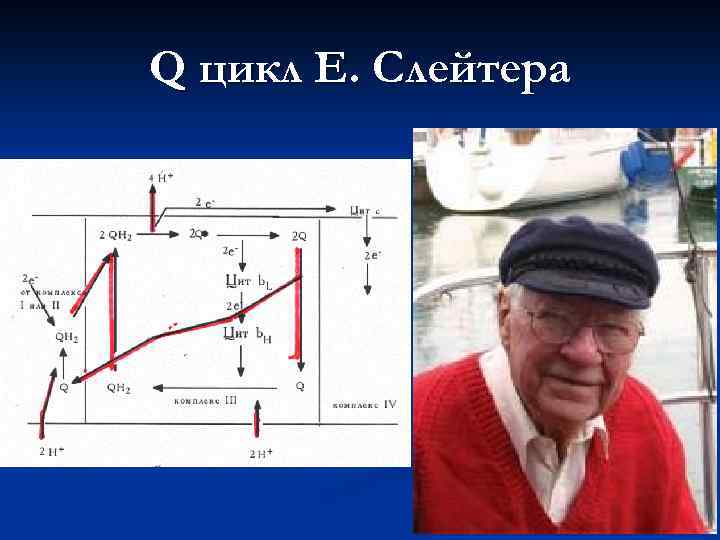
Q цикл Е. Слейтера

Лауреат Нобелевской премии Пол Бойер
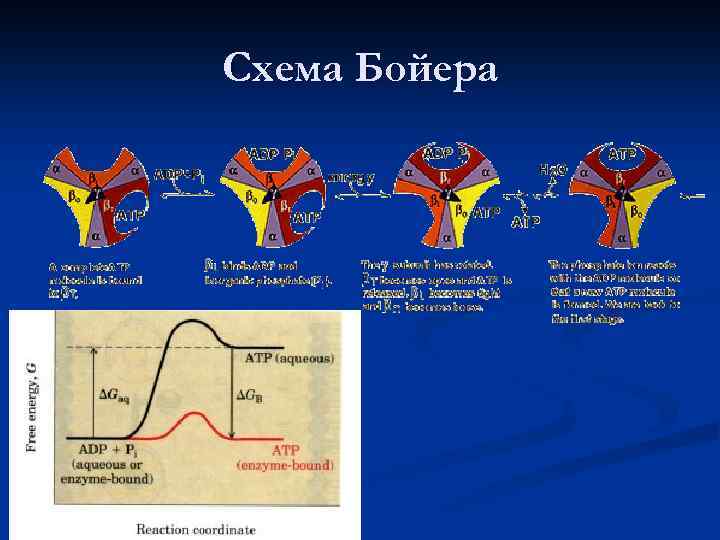
Схема Бойера

Лауреат Нобелевской премии Джон Уолкер Провел кристаллографическое изучение АТФ-синтазы. Доказал, что гипотеза Бойера о молекулярной машине верна. n

Субстратное фосфорилирование – образование АТФ из АДФ за счет энергии макроэргического соединения. Фосфорилирование субстрата – перенос фосфорной группы с АТФ на субстрат.

Биологическое значение Основная функция ЦТК – образование водородных эквивалентов, которые в цепи окислительного фосфорилирования обеспечивают синтез макроэргических соединений; n ЦТК выполняет ведущую роль в процессах: n глюконеогенеза; n переаминирования и дезаминирования АК; n липогенеза; n синтеза гема. n

ЦТК играет важную роль в процессах анаболизма (промежуточные продукты ЦТК): 3. ü ü 4. из Цитрата синтез жирных кислот; из α-КГ и ЩУК синтез аминокислот; из ЩУК синтез углеводов; из Сукцинил-Ко. А синтез гема гемоглобина; ЦТК интегрирует все виды обмена веществ.

Биороль ЦТК Интегративная функция — цикл является связующим звеном между реакциями анаболизма и катаболизма. n Катаболическая функция — превращение различных веществ в субстраты цикла: n Жирные кислоты, пируват, Лей, Фен — Ацетил-Ко. А. n Арг, Гис, Глу — α-кетоглутарат. n Фен, тир — фумарат. n Анаболическая функция — использование субстратов цикла на синтез органических веществ: n Оксалацетат — глюкоза, Асп, Асн. n Сукцинил-Ко. А — синтез гема. n CО 2 — реакции карбоксилирования.

n n n Водорододонорная функция — цикл Кребса поставляет на дыхательную цепь митохондрий протоны в виде трех НАДН. Н+ и одного ФАДН 2. Энергетическая функция — 3 НАДН. Н+ дает 7. 5 моль АТФ, 1 ФАДН 2 дает 1. 5 моль АТФ на дыхательной цепи. Кроме того в цикле путем субстратного фосфорилирования синтезируется 1 ГТФ, а затем из него синтезируется АТФ посредствам трансфосфорилирования: ГТФ + АДФ = АТФ + ГДФ.

Мнемоническое правило Целый Ананас И Кусочек Суфле Сегодня Фактически Мой Обед, n что соответствует ряду — цитрат, (цис-) аконитат, изоцитрат, (альфа-) кетоглутарат, сукцинил-Co. A, сукцинат, фумарат, малат, оксалоацетат. n

Щуку ацетил лимонил, n А нарцисса конь боялся, n Он над ним изолимонно n Альфа-кето-глютарался. n Сукцинился коэнзимом, n Янтарился фумарово, n Яблочек припас на зиму, n В щуку обратился снова. n

(щавелевоуксусная кислота, n лимонная кислота, n цис-аконитовая кислота, n изолимонная кислота, n α-кетоглутаровая кислота, n сукцинил-Co. A, n янтарная кислота, n фумаровая кислота, яблочная кислота, щавелевоуксусная кислота). n

Регуляция ЦТК 1. Цикл Кребса осуществляется с участием 4 регуляторных ферментов: ü ü α-КГДГ; ü 3. изоцитрат ДГ; ü 2. Цитратсинтазы; СДГ; Ингибирует ЦТК – НАДН 2 и АТФ, которые являются продуктами ЦТК и цепи окислительного фосфорилирования; Активируют ЦТК – НАД+ и АДФ; 4. Регуляторные функции выполняет первая пусковая реакция цикла. 5. Скорость ее зависит от концентрации ЩУК, Ацетил-Ко. А и активности ферментов;

6. Стимулирует ЦТК гормон инсулин, ингибирует – глюкагон. 7. O 2 регулирует реакции ЦТК, переводя восстановленные формы НAДH 2, ФAДH 2 в окисленные. 8. Уровень NH 3 : Высокая концентрация аммиака связывает α–КГ и цикл блокируется; 9. СУБСТРАТЫ реакции активируют ее, а ПРОДУКТЫ – тормозят.

Энергетический баланс одного оборота ЦТК n n n В 4 окислительно-восстановительных реакциях ЦТК образуются 3 НАДН 2 и 1 ФАДН 2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования ДЦ из 1 НАДН 2 образуется 3 АТФ, из 1 ФАДН 2 – 2 АТФ. Из ГТФ, образующейся в ЦТК за счет субстратного фосфорилирования , синтезируется 1 АТФ. Таким образом, за 1 цикл ЦТК из 3 НАДН 2, 1 ФАДН 2 и 1 ГТФ получается 12 АТФ.

Работа дыхательной цепи и окислительного фосфорилирования
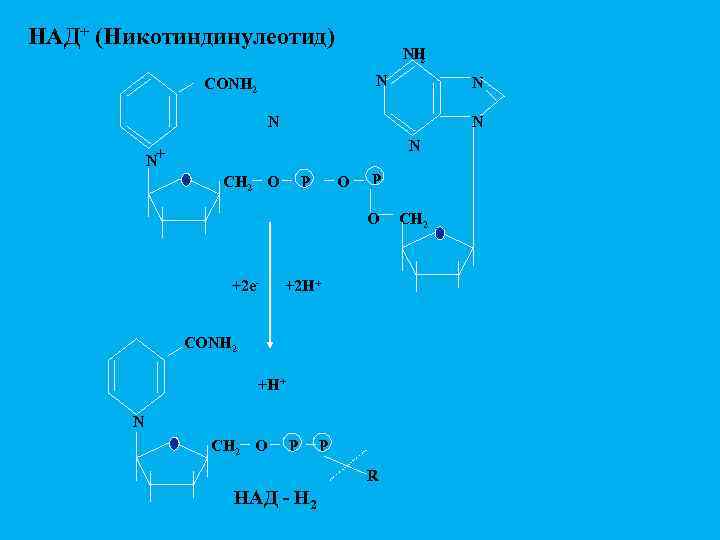
НАД+ (Никотиндинулеотид) NH 2 N CONH 2 N N N+ P CH 2 O O P O +2 e- +2 H+ CONH 2 +H+ N CH 2 O P P R НАД - H 2 CH 2
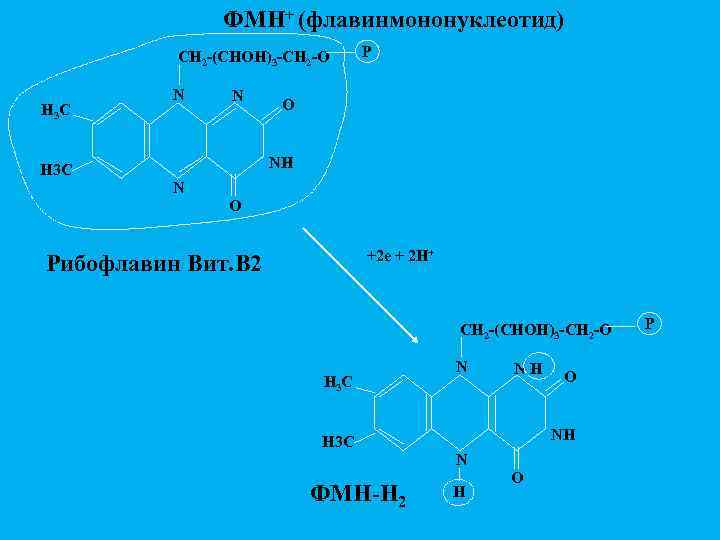
ФМН+ (флавинмононуклеотид) CH 2 -(CHOH)3 -CH 2 -O H 3 C N N P O NH H 3 C N O +2 e + 2 H+ Рибофлавин Вит. B 2 CH 2 -(CHOH)3 -CH 2 -O H 3 C N NH NH H 3 C N ФМН-Н 2 O H O P
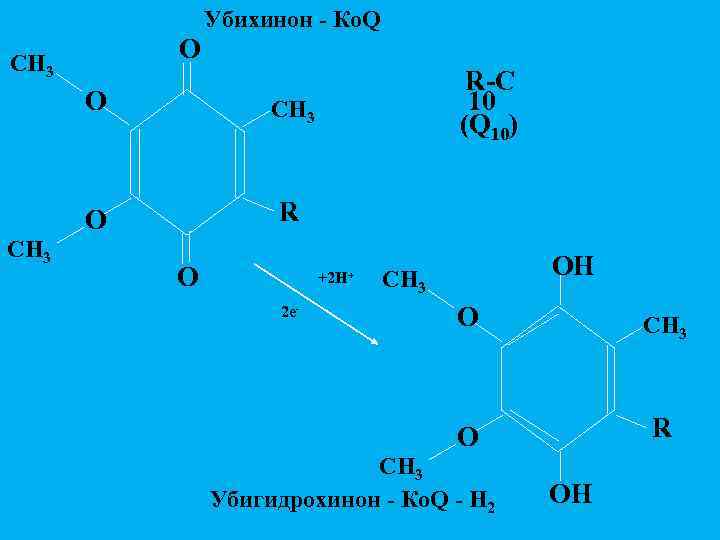
Убихинон - Ко. Q O CH 3 O R-C 10 (Q 10) R O +2 H+ OH CH 3 O 2 e- R CH 3 Убигидрохинон - Ко. Q - H 2 OH
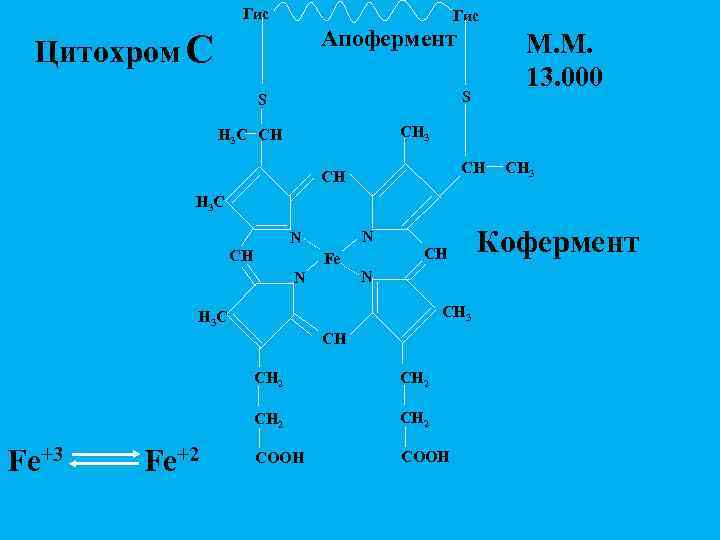
Гис Апофермент Цитохром С М. М. 13. 000 S S CH 3 H 3 C CH CH 3 H 3 C N N CH CH Fe N N CH 3 H 3 C CH СН 2 Fe+3 Fe+2 СН 2 СООН Кофермент
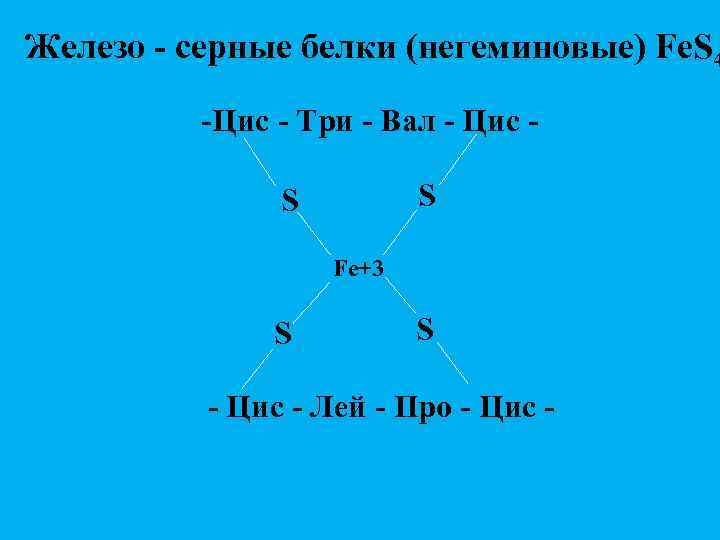
Железо - серные белки (негеминовые) Fe. S 4 -Цис - Три - Вал - Цис S S Fe+3 S S - Цис - Лей - Про - Цис -
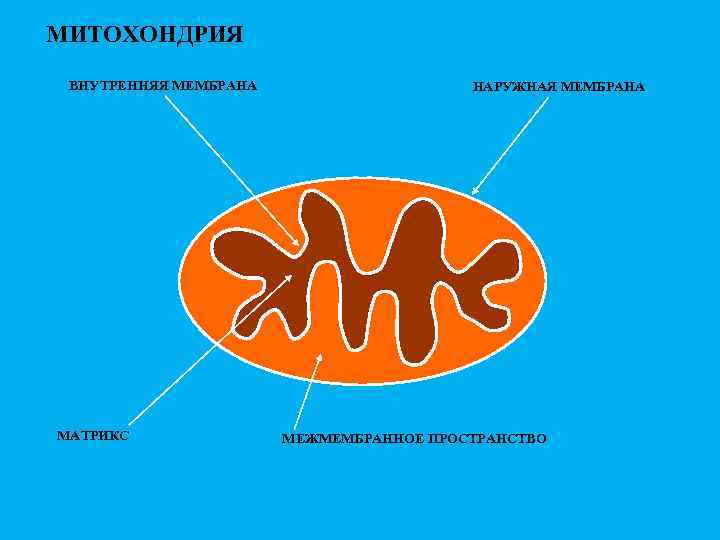
МИТОХОНДРИЯ ВНУТРЕННЯЯ МЕМБРАНА МАТРИКС НАРУЖНАЯ МЕМБРАНА МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО
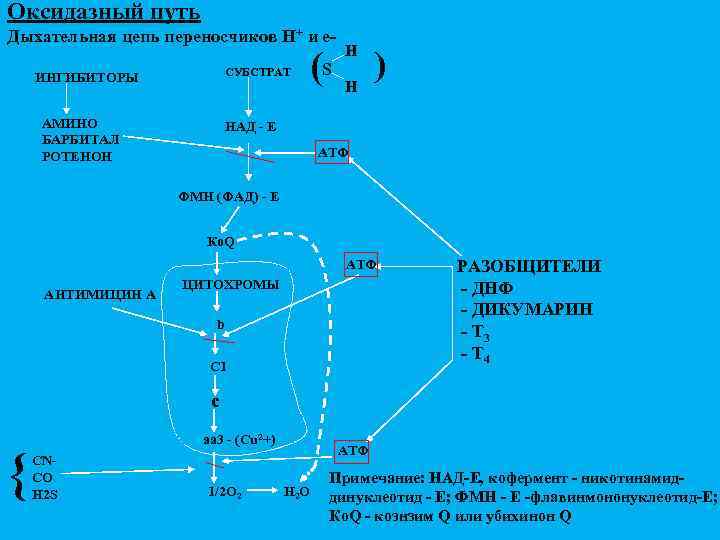
Оксидазный путь Дыхательная цепь переносчиков Н+ и е. СУБСТРАТ ИНГИБИТОРЫ АМИНО БАРБИТАЛ РОТЕНОН (S H H ) НАД - Е АТФ ФМН (ФАД) - Е Ко. Q АТФ АНТИМИЦИН А ЦИТОХРОМЫ b C 1 РАЗОБЩИТЕЛИ - ДНФ - ДИКУМАРИН - Т 3 - Т 4 c { aa 3 - (Cu 2+) CNCO H 2 S 1/2 O 2 АТФ H 2 O Примечание: НАД-Е, кофермент - никотинамиддинуклеотид - Е; ФМН - Е -флавинмононуклеотид-Е; Ко. Q - коэнзим Q или убихинон Q
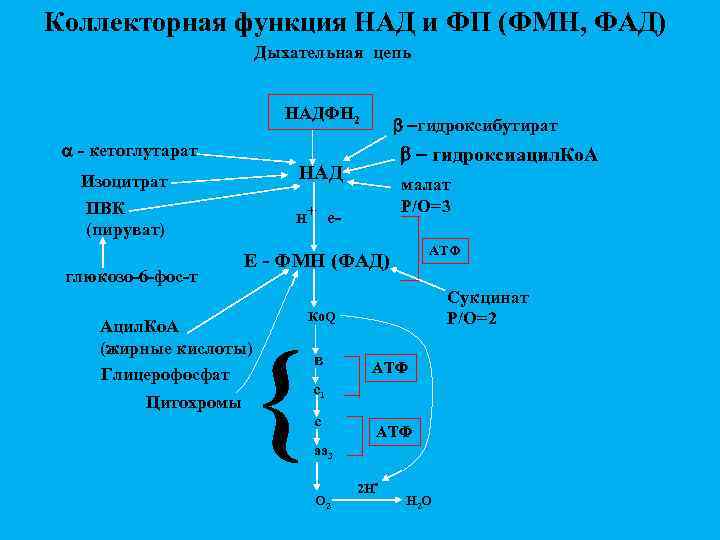
Коллекторная функция НАД и ФП (ФМН, ФАД) Дыхательная цепь НАДФН 2 b -гидроксибутират - кетоглутарат НАД Изоцитрат ПВК (пируват) глюкозо-6 -фос-т Н малат Р/О=3 + е- АТФ Е - ФМН (ФАД) Ацил. Ко. А (жирные кислоты) Глицерофосфат Цитохромы b - гидроксиацил. Ко. А { Сукцинат Р/О=2 Ко. Q в АТФ с1 с АТФ аа 3 О 2 2 Н . Н 2 О
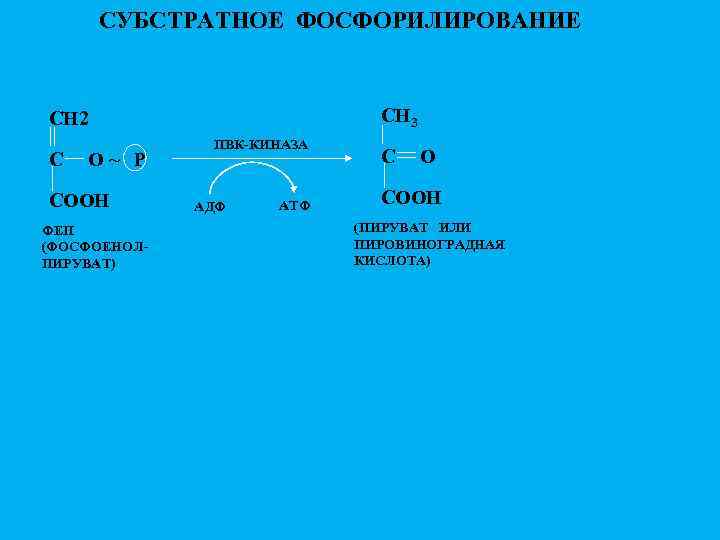
СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ СН 3 СН 2 С O~ Р СООН ФЕП (ФОСФОЕНОЛПИРУВАТ) ПВК-КИНАЗА АДФ АТФ С O СООН (ПИРУВАТ ИЛИ ПИРОВИНОГРАДНАЯ КИСЛОТА)

W + АДФ + Фнеорг Энергия АТФ + Н 2 О 1936 г. проф. Энгельгардт В. Н. Р/О = 3 1940 - 41 г. проф. Белицер (Киев) АТФ АДФ + 7, 6 ккал + Фн
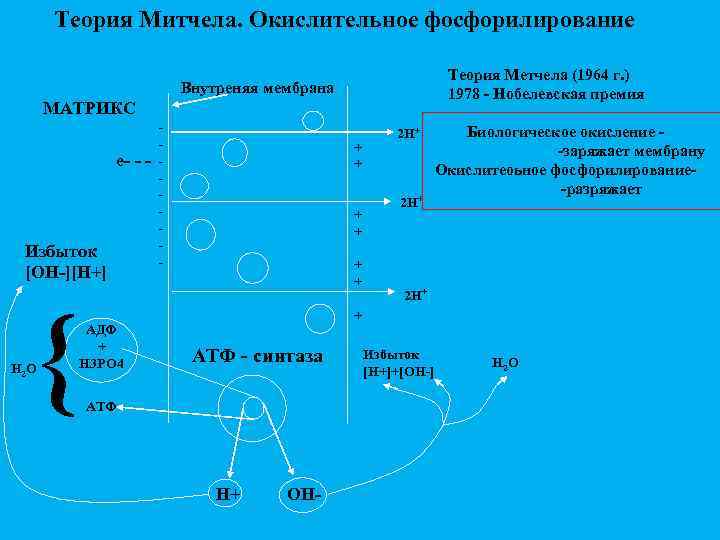
Теория Митчела. Окислительное фосфорилирование Теория Метчела (1964 г. ) 1978 - Нобелевская премия Внутреняя мембрана МАТРИКС e- - - Избыток [OH-][H+] { Н 2 О АДФ + Н 3 РО 4 - + + + 2 H+ Биологическое окисление -заряжает мембрану Окислитеоьное фосфорилирование-разряжает 2 H+ + АТФ - синтаза АТФ H+ OH- Избыток [H+]+[OH-] Н 2 О
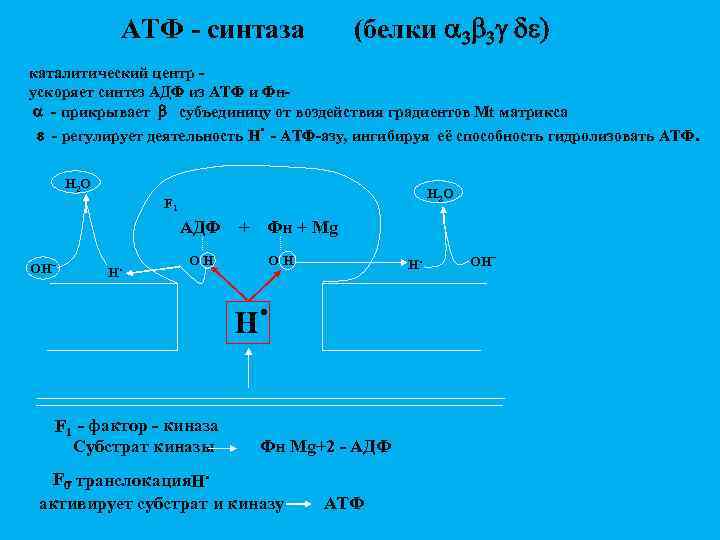
(белки 3 b 3 g de) АТФ - синтаза каталитический центр ускоряет синтез АДФ из АТФ и Фн - прикрывает b субъединицу от воздействия градиентов Mt матрикса . e - регулирует деятельность Н - АТФ-азу, ингибируя её способность гидролизовать АТФ. H 2 O F 1 АДФ OH- H. OH F 1 - фактор - киназа Субстрат киназы F - транслокация. H. + Фн + Mg H. OH . H Фн Mg+2 - АДФ 0 активирует субстрат и киназу АТФ OH-
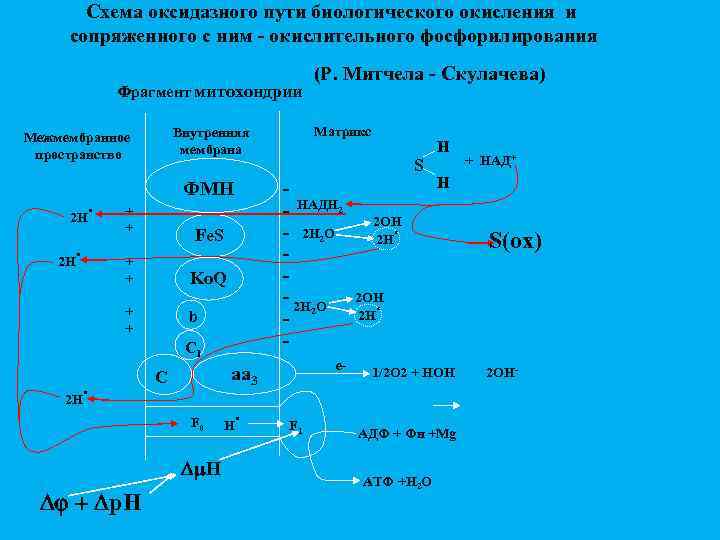
Схема оксидазного пути биологического окисления и сопряженного с ним - окислительного фосфорилирования Фрагмент митохондрии 2 Н . ФМН + + Ko. Q b C 1 . е- aa 3 C F 0 Dm. H Dj + Dp. H S - НАДН 2 - 2 Н 2 О - 2 Н О 2 - Fe. S + + 2 Н Матрикс Внутренняя мембрана Межмембранное пространство Н (Р. Митчела - Скулачева) . F 1 H + НАД+ H 2 ОН. 2 Н S(ox) 2 ОН. 2 Н 1/2 О 2 + НОН АДФ + Фн +Mg АТФ +Н 2 О 2 ОН-
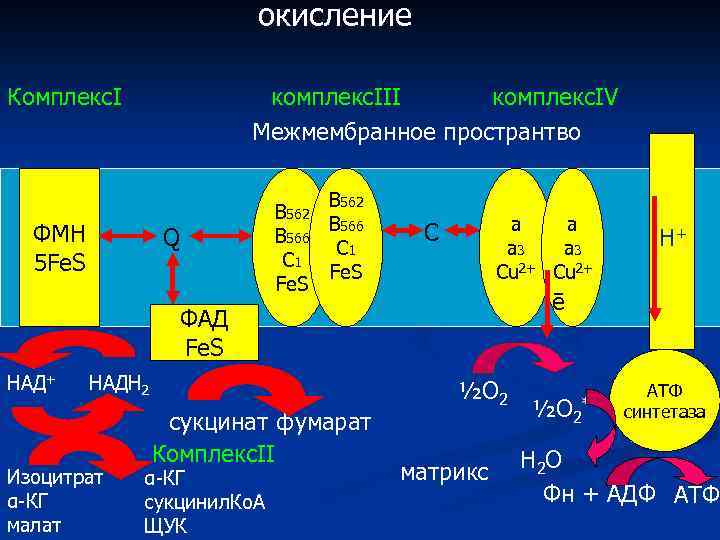
окисление КомплексΙ комплексΙΙΙ комплексΙV Межмембранное пространтво ФМН 5 Fе. S Q В 562 В 566 С 1 Fe. S а а а 3 Сu 2+ C ē ФАД Fe. S НАД+ НАДН 2 Изоцитрат α-КГ малат сукцинат фумарат КомплексΙΙ α-КГ сукцинил. Ко. А ЩУК Н+ ½О 2 матрикс ½О 2 * АТФ синтетаза Н 2 О Фн + АДФ АТФ
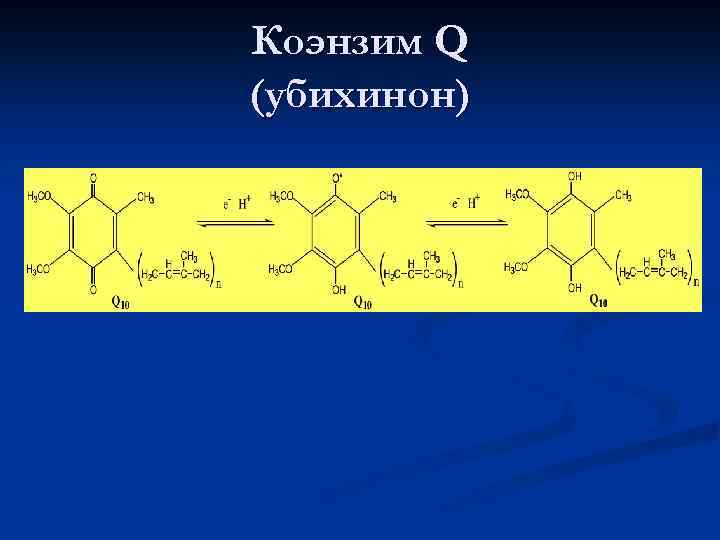
Коэнзим Q (убихинон)
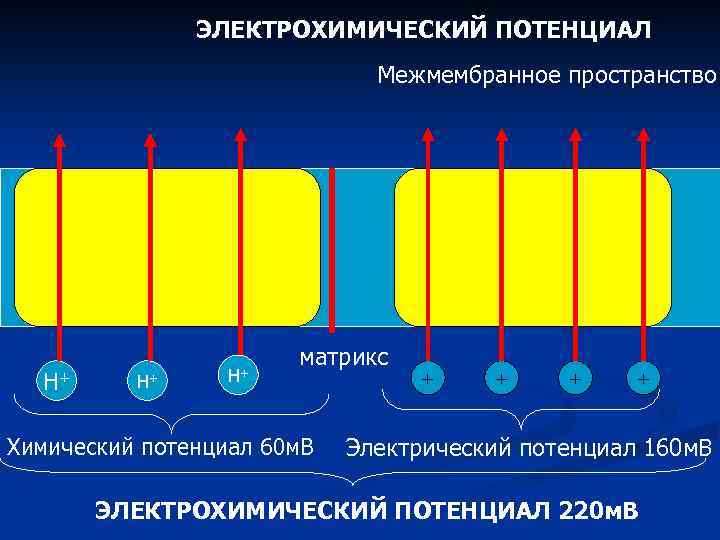
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ Межмембранное пространство Н+ Н+ Н+ матрикс Химический потенциал 60 м. В + + Электрический потенциал 160 м. В ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ 220 м. В
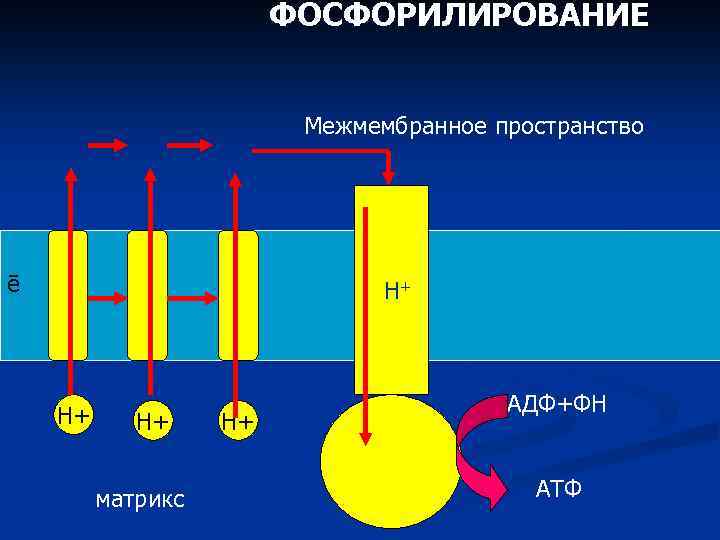
ФОСФОРИЛИРОВАНИЕ Межмембранное пространство ē Н+ Н+ Н+ матрикс Н+ АДФ+ФН АТФ
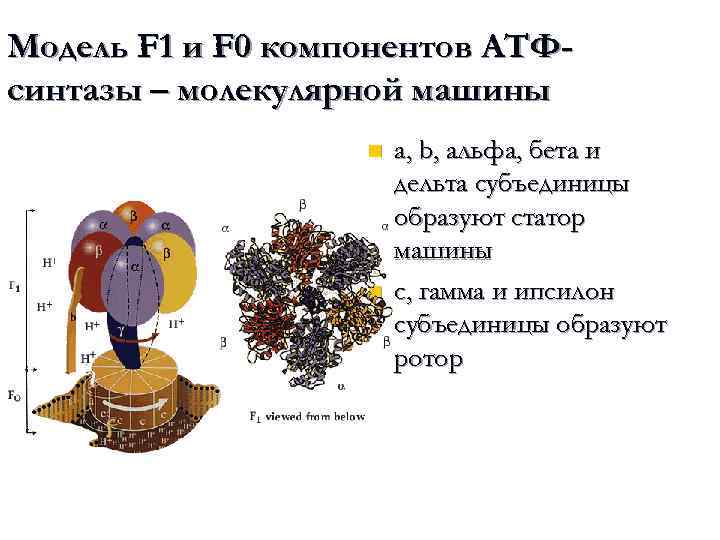
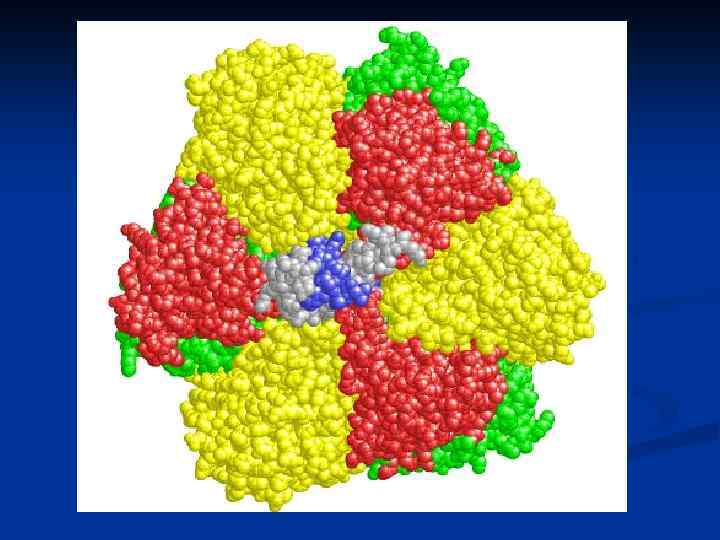
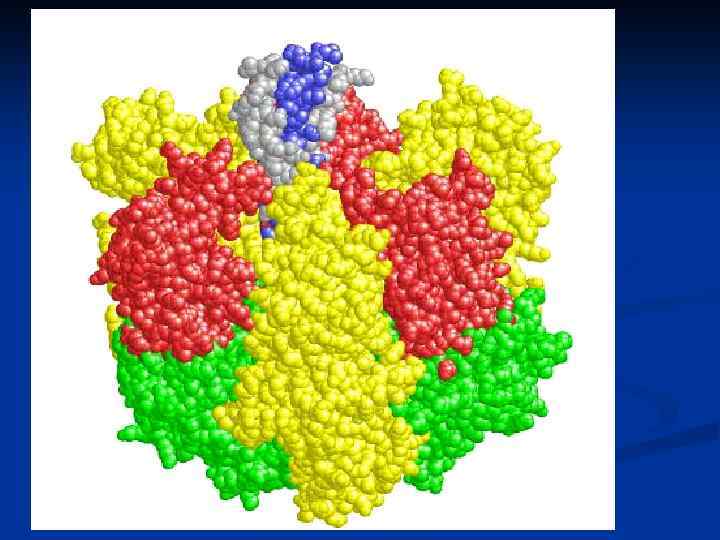
Модель F 1 и F 0 компонентов АТФсинтазы – молекулярной машины n n a, b, альфа, бета и дельта субъединицы образуют статор машины с, гамма и ипсилон субъединицы образуют ротор
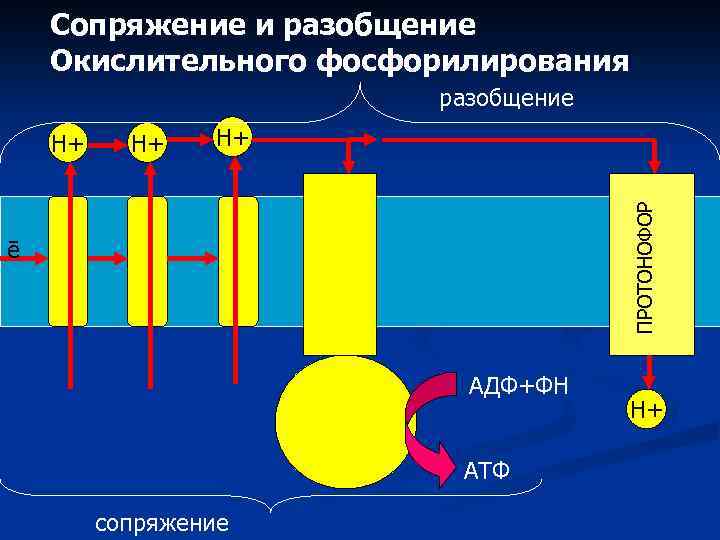
Сопряжение и разобщение Окислительного фосфорилирования разобщение Н+ Н+ ПРОТОНОФОР Н+ ē АДФ+ФН АТФ сопряжение Н+
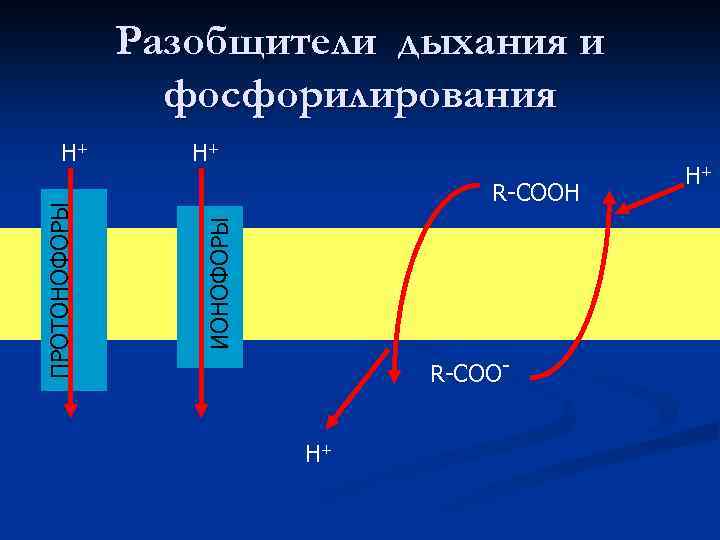
Разобщители дыхания и фосфорилирования Н+ R-СООН ИОНОФОРЫ ПРОТОНОФОРЫ Н+ R-СООН+ Н+

Коэффициент фосфорилирования n Обмен АТФ-АДФ стремится нейтрализовать мембранный потенциал. 25% общей энергии переноса электронов затрачивается на этот процесс. Соотношение между выбросом протонов из матрикса митохондрий и возврат их по протонным каналам не приводит к синтезу АТФ в стехиометрическом соотношении. Поэтому нельзя однозначно ответить на вопрос, сколько молекул АТФ образуется при окислении цитоплазматической молекулы НАД·Н митохондриями эукариотических клеток.

Современные данные n прежние значения коэффициента Р/O равные 3 и 2, завышены, более реальными являются n Р/O = 2, 5 для полной n и Р/O = 1, 5 для укороченной дыхательной цепи.
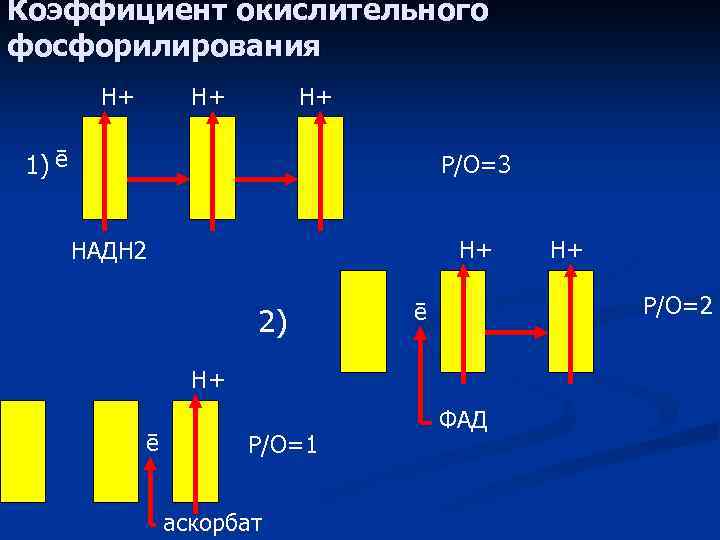
Коэффициент окислительного фосфорилирования Н+ Н+ Н+ 1) ē Р/О=3 Н+ НАДН 2 2) Р/О=2 ē Н+ ē Р/О=1 аскорбат Н+ ФАД
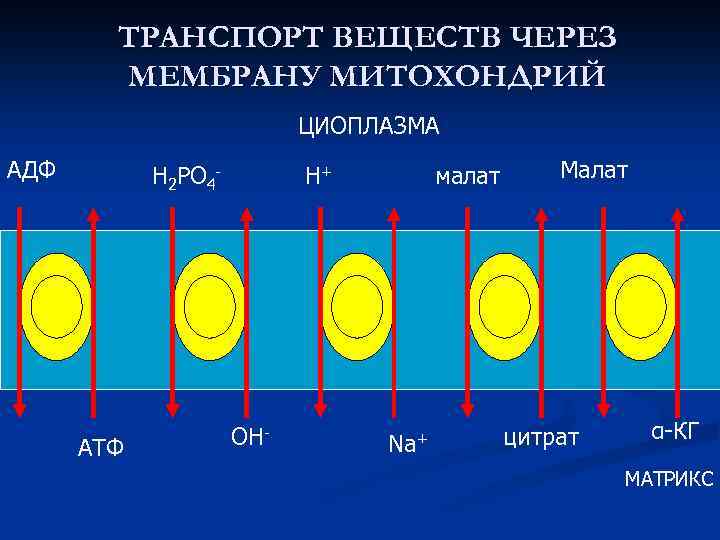
ТРАНСПОРТ ВЕЩЕСТВ ЧЕРЕЗ МЕМБРАНУ МИТОХОНДРИЙ ЦИОПЛАЗМА АДФ Н 2 РО 4 - АТФ Н+ ОН- малат Na+ Малат цитрат α-КГ МАТРИКС

Дыхательный контроль - Зависимость интенсивности дыхания митохондрий от концентрации АДФ. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30— 50 г Молекула АТФ «живёт» меньше минуты. В сутки у человека синтезируется 40— 60 кг АТФ и столько же распадается.
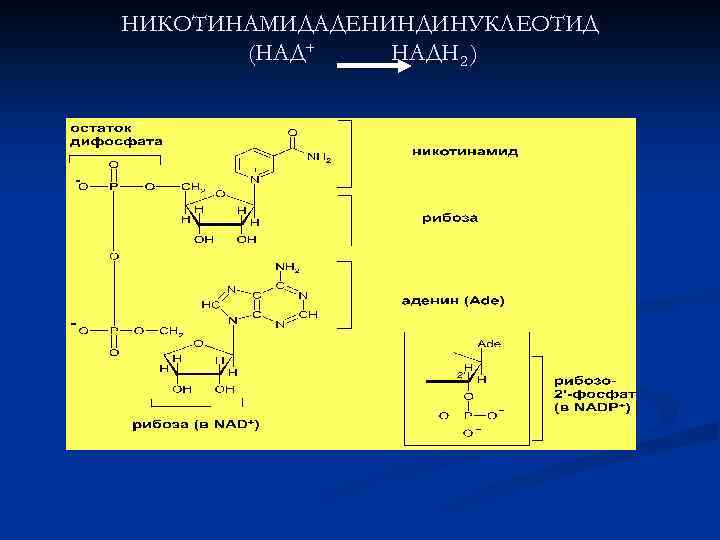
НИКОТИНАМИДАДЕНИНДИНУКЛЕОТИД (НАД+ НАДН 2 )
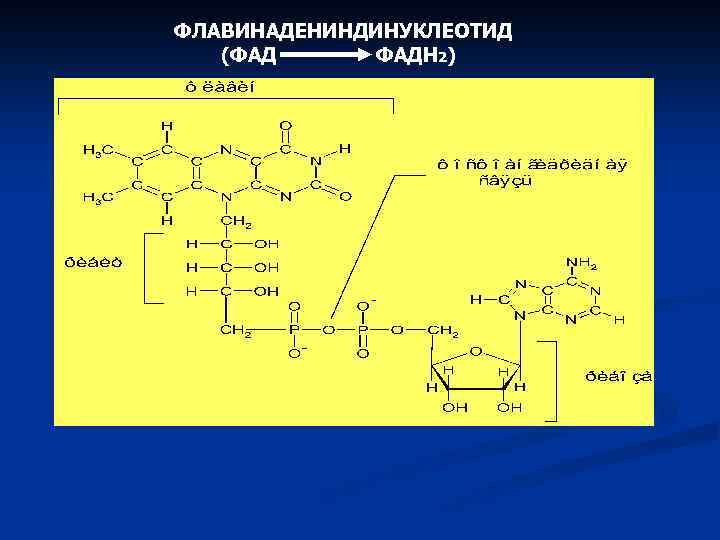
ФЛАВИНАДЕНИНДИНУКЛЕОТИД (ФАД ФАДН 2)

1. Биологическое значение ЦТК образование водородных эквивалентов, которые в цепи окислительного фосфорилирования обеспечивают синтез макроэргических соединений; 2. выполняет ведущую роль в : ü глюконеогенезе; ü переаминировании и дезаминировании аминокислот; ü липогенезе; ü синтезе гема.

3. роль в процессах анаболизма (промежуточные продукты ЦТК): ü из Цитрата синтез жирных кислот; ü из α-КГ и ЩУК - синтез аминокислот; ü из ЩУК синтез углеводов; ü из Сукцинил-Ко. А синтез гема гемоглобина; 4. интегрирует все виды обмена веществ.

Регуляция ЦТК 1. Регуляторные (ключевые, лимитирующие) ферменты: А. Цитратсинтаза; В. Изоцитратдегидрогеназа С. α-Кетоглутаратдегидрогеназа Д. Сукцинатдегидрогеназа 2. ↓ – НАДН 2 и АТФ 3. ↑ – НАД+ и АДФ 4. Первая - пусковая реакция ЦТК зависит от концентрации ЩУК, Ацетил. Ко. А

↑ 5. - инсулин, ингибирует – глюкагон 6. ↑ O 2 , переводя восстановленные формы НAДH 2, ФAДH 2 в окисленные 7. Высокая концентрация аммиака связывает α–КГ и цикл ↓ 8. Субстраты всех реакции ↑ ее, продукты –↓
лекция 4 Биологич. окисление 2012.ppt