5. Конспект урока. Газообразные вещества.ppt
- Количество слайдов: 23

Газообразные вещества
Газообразное вещество Газообразные вещества – это вещество, в котором частицы движутся свободно, хаотично.

Газ (газообразное состояние) • Газ – это агрегатное состояние вещества, характеризующееся очень слабыми связями между составляющими его частицами (молекулами, атомами или ионами), а также их большой подвижностью.

Особенности газов • Легко сжимаются. • Не имеют собственной формы и объема • Любые газы смешиваются друг с другом в любых соотношениях.

Закон Авогадро В равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.

Число Авогадро • Значение NA = 6, 022…× 1023 называется числом Авогадро. • Это универсальная постоянная для мельчайших частиц любого вещества.

Следствие из закона Авогадро 1 моль любого газа при н. у. (760 мм рт. ст. и 00 С) занимает объем 22, 4 л. Vm = 22. 4 л/моль – молярный объем газов

Важнейшие природные смеси газов Состав воздуха: • φ(N 2) = 78%; • φ(O 2) = 21%; • φ(CO 2) = 0. 03 Природный газ – это смесь углеводородов.

Получение водорода. В промышленности: • Крекинг и риформинг углеводородов в процессе переработки нефти: C 2 H 6 (t = 10000 С) → 2 C + 3 H 2 • Из природного газа. CH 4 + O 2 + 2 H 2 O → 2 CO 2 +6 H 2 O

Водород H 2 В лаборатории: Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную серную кислоту: Zn + 2 HCl → Zn. Cl 2 + H 2 Взаимодействие кальция с водой: Ca + 2 H 2 O → Ca(OH)2 + H 2 Гидролиз гидридов: Ca. H 2 + 2 H 2 O → Ca(OH)2 +2 H 2 Действие щелочей на цинк или алюминий: Zn + 2 Na. OH + 2 H 2 O Na 2[Zn(OH)4] + H 2

Свойства водорода • Самый лёгкий газ, он легче воздуха в 14, 5 раз. • Водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха. • Молекула водорода двухатомна — Н 2. При нормальных условиях — это газ без цвета, запаха и вкуса.

Кислород В промышленности: • Из воздуха. • Основным промышленным способом получения кислорода, является криогенная ректификация. В лаборатории: • Из перманганата калия (марганцовки): 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + О 2 ↑; 2 H 2 O 2 = 2 Н 2 О + О 2↑.

Свойства кислорода • При нормальных условиях кислород — это газ без цвета, вкуса и запаха. • 1 л его имеет массу 1, 429 г. Немного тяжелее воздуха. Слабо растворяется в воде и спирте Хорошо растворяется в расплавленном серебре. Является парамагнетиком.

Оксид углерода (IV) В лаборатории: • Из мела, известняка или мрамора: Na 2 CO 3 + 2 HCl = 2 Na. Cl + CO 2↑ +H 2 O Сa. CO 3 + HCl = Ca. Cl 2 + CO 2↑ + H 2 O В природе: • Фотосинтез в растениях: C 6 H 12 O 6 + 6 O 2 = 6 CO 2 + 6 H 2 O

Оксид углерода (IV) • Оксид углерода (IV) (углекислый газ) – это бесцветный газ, без запаха, со слегка кисловатым вкусом. • Тяжелее воздуха, растворим в воде, при сильном охлаждении кристаллизуется в виде белой снегообразной массы – «сухого льда» . • При атмосферном давлении он не плавится, а испаряется, температура сублимации -78 °С.

Аммиак (н. у. ) – это бесцветный газ с резким характерным запахом (запах нашатырного спирта). Аммиак почти вдвое легче воздуха, растворимость NH 3 в воде чрезвычайно велика. В лаборатории аммиак получают: • Взаимодействием щелочей с солями аммония: NH 4 Cl + Na. OH = Na. Cl + H 2 O + NH 3↑ В промышленности: • Взаимодействие водорода и азота: 3 H + N = 2 NH

Этилен В лаборатории: • Дегидратация этилового спирта В промышленности: • Крекинг нефтепродуктов: C 4 H 10 → C 2 H 6 + C 2 H 4 этан этен

• Этилен — бесцветный газ, обладающий слабым сладковатым запахом и относительно высокой плотностью. • Этилен горит светящимся пламенем; с воздухом и кислородом образует взрывоопасную смесь. • В воде этилен практически нерастворим.
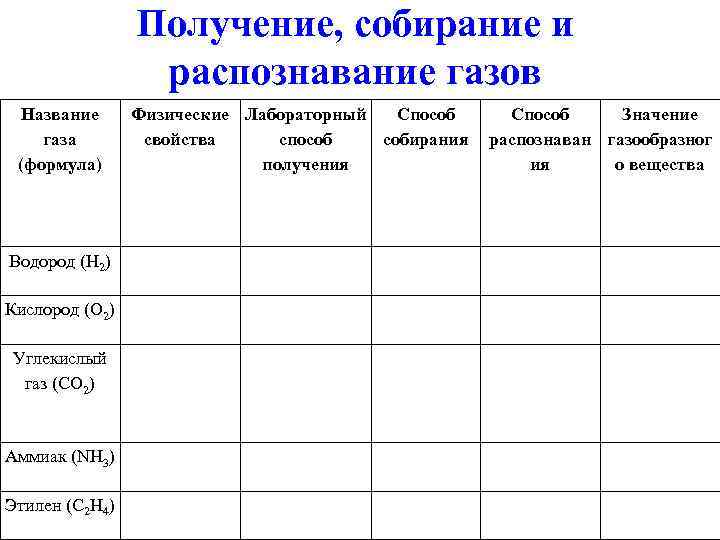
Получение, собирание и распознавание газов Название газа (формула) Водород (H 2) Кислород (O 2) Углекислый газ (CO 2) Аммиак (NH 3) Этилен (С 2 H 4) Физические Лабораторный Способ свойства способ собирания получения Способ Значение распознаван газообразног ия о вещества

Задачи Задача № 1. 13, 5 грамм цинка (Zn) взаимодействуют с соляной кислотой (HCl). Объемная доля выхода водорода (H 2) составляет 85 %. Вычислить объем водорода, который выделился? Задача № 2. Имеется газовая смесь, массовые доли газа в которой равны (%): метана – 65, водорода – 35. Определите объемные доли газов в этой смеси.

Задача № 1 1) Запишем уравнение реакции взаимодействия цинка (Zn) с соляной кислотой (HCl): Zn + 2 HCl = Zn. Cl 2 + H 2 2) n (Zn) = 13, 5 / 65 = 0, 2 (моль). 3) 1 моль Zn вытесняет 1 моль водорода (H 2), а 0, 2 моль Zn вытесняет х моль водорода (H 2). Получаем: V теор. (H 2) = 0, 2 ∙ 22, 4 = 4, 48 (л). 4) Вычислим объем водорода практический по формуле: V практ. (H 2) = 85 ⋅ 4, 48 / 100 = 3, 81 (л).

Задача № 2 Имеется газовая смесь, массовые доли газа в которой равны (%): метана – 65, водорода – 35. Определите объемные доли газов в этой смеси.

5. Конспект урока. Газообразные вещества.ppt