Газообразное состояние вещества2.ppt
- Количество слайдов: 14

Газообразное состояние вещества Химия 11 класс

Основные свойства ГАЗООБРАЗНОГО СОСТОЯНИЯ ВЕЩЕСТВА Газы не имеют формы и объема, занимают весь объем Легко сжимаются Смешиваются друг с другом Почему? Свойства газов объясняются тем, что расстояния между молекулами много больше самих молекул, поэтому молекулы слабо притягиваются друг к другу

Закон Авогадро: В равных объемах различных газов при одинаковых условиях (T, P) содержится одинаковое число молекул.

Следствия: - Порции различных газов, содержащих равные количества вещества (одинаковое число молекул) при одинаковых условиях занимают один и тот же объем. - При нормальных условиях (н. у. )1 моль любого газа занимает объем 22, 4 л. н. у. это 273 К и 101300 Па или 0ºС и 760 мм рт. ст. для газов.

Относительная плотность II газа по I газу D

Какой объем при н. у. занимает 8, 8 г углекислого газа? Ответ: V (CO 2) =4, 48 л (н. у. )

Вычислить плотность озона по азоту и воздуху. Ответ:

Газовые смеси Объемные доли газов будут совпадать с молярными, т. е. с долями количеств веществ, образовавших смесь. Следствие из закона Авогадро.


Задача • Для газовой смеси, состоящей из 25 л азота и 175 л кислорода вычислить: - объемные доли газов в смеси; - массовые доли газов в смеси; - среднюю молекулярную массу смеси; - плотность этой смеси по водороду


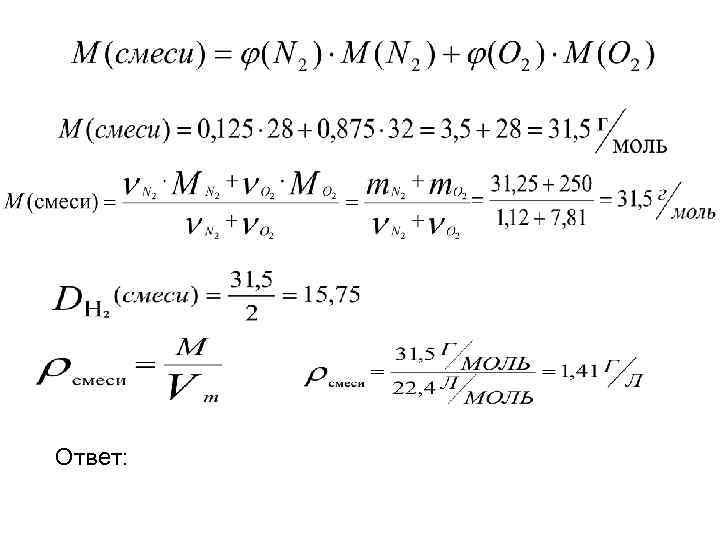
Ответ:

Домашнее задание • Найти плотность по кислороду и массовые доли газов смеси, состоящей из 5 л метана и 20 л неона (ответ: D= 0, 6; 16, 7% метана и 83, 3% неона
Газообразное состояние вещества2.ppt