главная подгруппа 5 группы.ppt
- Количество слайдов: 175

ГАОУ СПО «Казанский медицинский колледж» Электронный учебный модуль информационного типа на тему: «Главная подгруппа V группы» Специальность: «Фармация» Дисциплина: «Неорганическая химия» Преподаватель: Шакурова Н. С. 2010 г.

Содержание ЭДМ Введение Рекомендации по работе с ЭДМ Требования ГОС Цели занятия Учебная информация 1. Общая характеристика элементов 2. Азот и его свойства 3. Физические и химические свойства аммиака 4. Соли аммония и применение их в медицине

Содержание ЭДМ 5. Оксиды азота 6. 7. 8. 9. 10. Азотистая кислота и ее соли Азотная кислота Фосфор и его свойства Соединения фосфора Химические свойства важнейших соединений мышьяка, сурьмы, висмута Термины и определения Литература

Введение Учебный материал представлен в соответствии с требованиями Государственного образовательного стандарта по дисциплине «Неорганическая химия» в цикле профессиональных дисциплин, предназначенных для специальности «Фармация» . Электронный дидактический материал информационного типа на тему: «Главная подгруппа V группы» предназначен для проведения практического занятия и самостоятельной работы студентов медицинских училищ и колледжей СМОУ РТ и РФ.

Рекомендации по работе с ЭДМ 1. Ознакомьтесь с требованиями ГОС по данной теме. 2. Изучите информационный материал занятия. 3. Выучите термины и определения. 4. Выполните задания для закрепления знаний по учебнику Ерохин Ю. М. (Сборник задач и упражнений. - 2005. -304 с. ). Ответить на вопросы стр. 90, 1 -17. Выполнить упражнения стр. 91 -92, 18 -25, 28, 29.

ТРЕБОВАНИЯ ГОСУДАРСТВЕННОГО ОБРАЗОВАТЕЛЬНОГО СТАНДАРТА к уровню подготовки специалистов в области химии для специальности «Фармация» После изучения темы «Главная подгруппа V группы» студент должен УМЕТЬ: • доказывать химическими реакциями свойства соединений азота (солей аммония, нитритов, нитратов) и фосфора (фосфатов, гидрофосфатов).

ТРЕБОВАНИЯ ГОСУДАРСТВЕННОГО ОБРАЗОВАТЕЛЬНОГО СТАНДАРТА к уровню подготовки специалистов в области химии для специальности «Фармация» студент должен ЗНАТЬ: • характеристику элементов V группы главной подгруппы по положению в периодической системе Д. И. Менделеева; • физические и химические свойства азота и фосфора; • особые свойства азотной кислоты.

Цели занятия Учебная: добиться прочного усвоения системы знаний, формирование практических умений и навыков. Развивающая: формирование навыков самообразования, самореализации личности и развитие речи, мышления, памяти.

Цели занятия Воспитательная: привитие умений и навыков учебной работы и коллективного труда. Формирование у студентов целостного миропонимания и современного научного мировоззрения.
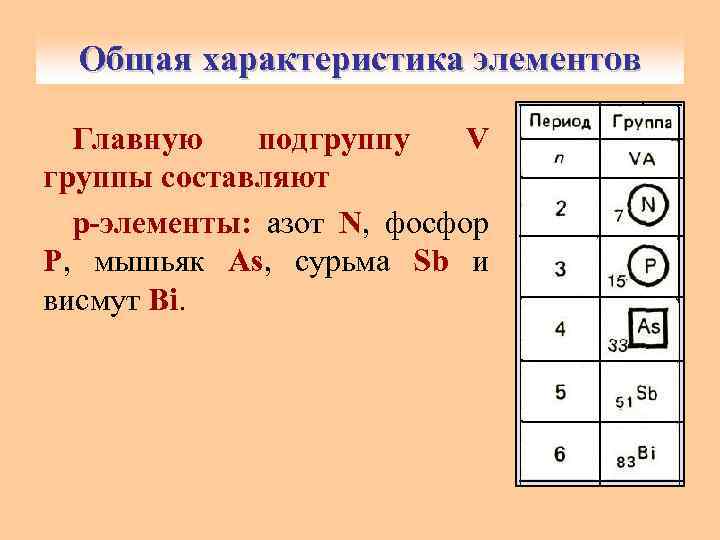
Общая характеристика элементов Главную подгруппу V группы составляют р-элементы: азот N, фосфор Р, мышьяк As, сурьма Sb и висмут Bi.

Общая характеристика элементов Строение электронных оболочек Строение внешнего электронного слоя атомов элементов V группы представляется следующим образом: np ns ns 2 np 3 (n-номер уровня, совпадающий с номером периода, в котором находится данный элемент).
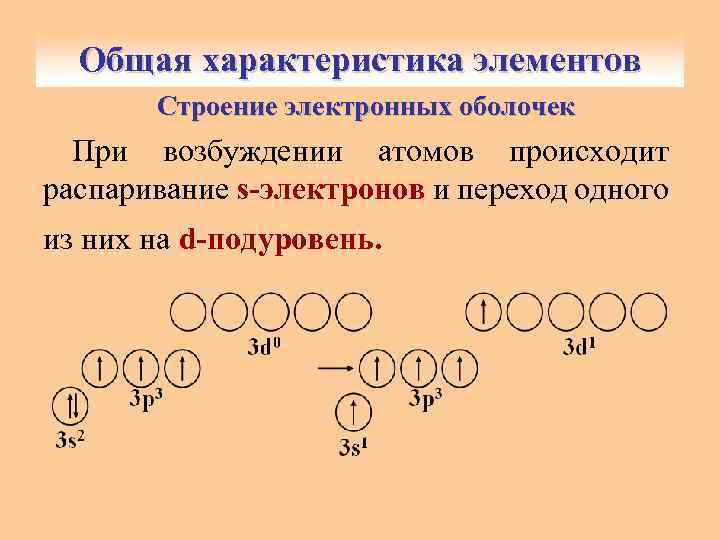
Общая характеристика элементов Строение электронных оболочек При возбуждении атомов происходит распаривание s-электронов и переход одного из них на d-подуровень.

Общая характеристика элементов Строение электронных оболочек У атома фосфора в состоянии электроны энергетического уровня конфигурацию 3 s 13 p 33 d 1. возбужденном внешнего приобретают Исключением является атом азота, внешние электроны которого не имеют dподуровня.

Общая характеристика элементов Степени окисления в соединениях Высшая степень окисления в соединениях равна +5; низшая степень окисления равна-3 (кроме Sb и Bi). В связи с этим высшие оксиды имеют общую формулу R 2 O 5, а водородные соединения — RH 3. Из промежуточных степеней окисления +3 является общей для всех элементов.

Общая характеристика элементов Сравнительная характеристика химических свойств Первые два элемента (азот и фосфор) являются типичными неметаллами, мышьяк уже проявляет признаки металличности, значительно усиливающиеся у сурьмы и висмута, которые принадлежат к металлам. Неметаллические свойства ослабевают N P As Sb Bi

Общая характеристика элементов Сравнительная характеристика химических свойств Различия проявляются как в свойствах простых веществ, образуемых элементами, так и в свойствах сложных веществ, прежде всего оксидов и гидроксидов:

Общая характеристика элементов Сравнительная характеристика химических свойств Соединения со степенью окисления элементов +5 имеют более кислотный характер, но их устойчивость снижается с увеличением порядкового номера элемента так, что для сурьмы и висмута они вообще не являются характерными.

Азот и его свойства Азот - первый и наиболее важный элемент главной подгруппы V группы, неметалл семейства р-элементов. Основная часть свободного азота приходится на атмосферу: 78, 09% по объему. Над каждым гектаром земной поверхности постоянно «висят» 8 тыс. тонн азота.

Азот и его свойства Валентность атома азота В связи с отсутствием на втором энергетическом уровне d-подуровня число неспаренных электронов не может увеличиваться за счет перехода атома в возбужденное состояние. Максимальная валентность азота ограничена числом валентных атомных орбиталей и не может быть выше IV.

Азот и его свойства Степени окисления атома азота По величине относительной электро- отрицательности азот уступает лишь фтору и кислороду и в соединениях с ними проявляет положительные степени окисления от +1 до +5. В соединениях отрицательными с менее элементами электро(металлами, водородом) азот имеет степень окисления -3.

Азот и его свойства Неорганические соединения азота Из неорганических соединений азота наиболее важными являются следующие вещества: Степень окисления -3 Химические NH 3 соединения 0 +1 +2 +3 +4 N 2 O NO N 2 O 3 NO 2 N 2 O 5 HNO 2 HNO 3 KNO 2, KNO 3 Na. NO 2 Na. NO 3 Na 3 N, Ca 3 N 2 NH 4 C 1, (NH 4)2 SO 4 +5
Азот и его свойства Органические соединения азота В составе органических сложных соединений (белков, нуклеиновых кислот и др. ) азот присутствует во всех живых организмах.

Азот и его свойства Химическая связь в молекуле азота Молекулы азота N 2 состоят из двух атомов, связанных между собой тройной ковалентной неполярной связью. Эта связь, очень прочная, разрывается лишь при очень высоких температурах (> 3000 °С).

Азот и его свойства Физические свойства азота При обычных условиях азот представляет собой бесцветный газ, не имеющий запаха и вкуса, мало растворимый в воде. Так как молекула азота неполярна, то он имеет низкие температуры плавления (-210 0 С) и кипения(-196 0 С).

Азот и его свойства Получение азота Свободный азот в лабораторных условиях получают путем термического разложения азотосодержащих соединений, например: (NH 4)2 Cr 2 O 7=N 2↑+Cr 2 O 3+4 H 2 O↑

Азот и его свойства Молекулярный азот — химически малоактивное вещество. При обычной температуре азот взаимодействует только с литием; остальные реакции протекают при высоких температурах и в большинстве случаев являются обратимыми.

Азот и его свойства Получение азота Образование нитридов При взаимодействии с металлами образуются нитриды: активными

Азот и его свойства Получение азота. Гидролиз нитридов Нитриды в водных растворах подвергаются необратимому гидролизу, в результате которого выделяется аммиак: Mg 3 N 2+6 H 2 O=2 NH 3↑+3 Mg(OH)2↓

Азот и его свойства Получение азота. Взаимодействие азота с водородом происходит только при высокой температуре в присутствии катализатора:

Азот и его свойства Химические реакции, в которых азот выступал бы в качестве восстановителя, практически не осуществляются. Так, азот непосредственно галогенами. не взаимодействует с

Азот и его свойства Эндотермическая реакция с кислородом протекает обратимо искровых разрядов: при температуре

Физические и химические свойства аммиака Одним из важнейших соединений азота является аммиак - NH 3. В организме человека является одним из продуктов метаболизма аминокислот и белков, поступивших с пищей или присутствующих в самой клетке в качестве запасных веществ.

Физические и химические свойства аммиака Применение аммиака в медицине В медицинской практике применяют 10% ный раствор аммиака (нашатырный спирт) для вывода из обморочного состояния. При вдыхании аммиак оказывает возбуждающее влияние на дыхательный центр. При больших дозах наступает удушье.

Физические и химические свойства аммиака При обычных условиях аммиак представляет собой бесцветный газ с характерным резким запахом, легче воздуха, очень хорошо растворимый в воде. Раствор NH 3 в воде называют аммиачной водой, или нашатырным спиртом.

Физические и химические свойства аммиака Восстановительные свойства аммиака В аммиаке азот имеет самую низкую степень окисления (-3), поэтому может отдавать электроны и является сильным восстановителем. С другой стороны, аммиак проявляет основные свойства.

Восстановленные свойства аммиака 1. Взаимодействие с галогенами: 2. Взаимодействие с кислородом: а) горение аммиака без катализатора участия

Восстановленные свойства аммиака б) окисление катализатора аммиака с участием 3. Восстановление металлов из их оксидов.

Кислотно-основные свойства аммиака Кислотно-основные свойства проявляются в способности молекул аммиака присоединять к себе протон Н+ по донорноакцепторному механизму.

Кислотно-основные свойства аммиака В состоянии равновесия в растворе образуется некоторый избыток гидроксидионов ОН- и, следовательно среда приобретает щелочной характер (р. Н > 7)

Кислотно-основные свойства аммиака По донорно-акцепторному происходит механизму и взаимодействие аммиака с кислотами с образованием солей аммония: 2 NH 3+ H 2 SO 4 = (NH 4)2 SO 4 сульфат аммония

Кислотно-основные свойства аммиака NH 3 + HCI = NH 4 C 1 хлорид аммония

Соли аммония - это сложные вещества, образованные катионом аммония и анионами кислотных остатков. Все соли аммония кристаллические - вещества, твердые хорошо растворимые в воде. Они обладают всеми свойствами солей.

Соли аммония Разложение солей аммония при нагревании 1. Неокислительно-восстановительное разложение (анион не является окислителем): NH 4 C 1 = NH 3 + HC 1 (NH 4)2 SO 4 =2 NH 3 + H 2 SO 4 (NH 4)3 PO 4 = 3 NH 3 + H 3 PO 4

Соли аммония Разложение солей аммония при нагревании 2. Окислительно-восстановительное разложение (анион является окислителем).

Соли аммония Гидролиз солей аммония. Так как соли аммония образованы слабым основанием — NH 4 OH, то они в водных растворах подвергаются гидролизу по катиону, который описывается общим сокращенным ионным уравнением: Растворы солей, образованных аммиаком и сильными кислотами, имеют кислую реакцию.

Соли аммония Гидролиз солей аммония. Соли, образованные аммиаком и слабыми кислотами, подвергаются гидролизу и по катиону, и по аниону, например: Среда растворов таких солей близка к нейтральной.

Соли аммония Качественная реакция на катион При добавлении щелочи к водному раствору соли аммония происходит взаимодействие гидроксильных ионов с ионами аммония:

Соли аммония Гидролиз солей аммония. Качественная реакция на катион При нагревании раствора аммиак улетучивается за счет уменьшения его растворимости, что легко определяется по характерному запаху аммиака или по посинению красной лакмусовой бумаги.

Применение солей аммония в медицине Из солей аммония в медицинской практике в качестве мочегонного средства применяют аммоний хлорид NH 4 C 1. В крови в результате гидролиза аммония хлорида по катиону повышается кислотность: NH 4+ + 2 H 2 O =NH 3·H 2 О +H 3 О+

Применение солей аммония в медицине Кроме того, протоны образуются в результате превращения аммоний-иона в мочевину:

Применение солей аммония в медицине Для нейтрализации избытка ионов Н 3 О+ почки мобилизуют и выделяют в мочу ионы натрия, с которыми одновременно выделяется соответствующее количество воды. Вместе с тем аммоний хлорид может быть эффективным средством против защелачивания крови (коррекция алкалоза).
Применение солей аммония в медицине. Образующиеся протоны Н 3 О+, при введении хлорида аммония, нейтрализуют ОН ─ - ионы: NH 4+ Н 3 О + +ОН- Н 2 О

Превращение производных аммиака в организме Аминогруппа – NH 2 входит в состав различных биолигандов, играющих важную роль в процессах аминокислот, жизнедеятельности: нуклеотидов, нуклеиновых кислот и т. д. В процессах распада этих веществ в организме образуется аммиак.

Превращение производных аммиака в организме. Повышение концентрации аммиака в крови может вызывать повторяющуюся рвоту, возбуждение, припадки с потерей сознания и судорогами. При хронической врожденной гипераммониемии наблюдается отставание умственного развития.

Превращение производных аммиака в организме В крови при p. H 7, 4 аммиак почти полностью находится в виде ионов аммония. Ионы аммония, несмотря на то, что они в крови находятся в большом избытке, не могут проникать через клеточные мембраны, в то время как нейтральные молекулы NH 3 легко проходят через эти мембраны и могут воздействовать на мозг.

Оксиды азота Азот — единственный элемент в своей подгруппе, образующий 5 оксидов, различных по физическим и химическим свойствам. (табл. 1. )

Оксиды азота Диоксид aзoтa NO 2. Способы получения. 1. Взаимодействие концентрированной азотной кислоты с тяжелыми металлами, например:

Оксиды азота Диоксид aзoтa NO 2. Способы получения. 2. Термическое разложение тяжелых металлов, например: Pb(NO 3)2=2 Pb. O+4 NO 2↑+O 2↑ 3. Разложение азотной кислоты: нитратов

Оксиды азота. Диоксид aзoтa NO 2. Способы получения. 4. В промышленности диоксид азота получают из NH 3: 4 NH 3 + 5 О 2= 4 NO + 6 Н 2 О 2 NO + О 2 = 2 NO 2

Оксиды азота Химические свойства диоксида азота. 1. В отсутствие кислорода происходит диспропорционирование N+4 в молекуле NО 2 (самоокисление — самовосстановление):

Оксиды азота. Химические свойства диоксида азота. 2. В присутствии кислорода (на воздухе) атомы кислорода окисляют атомы азота до высшей степени окисления:

Оксиды азота Химические свойства диоксида азота 3. Окислительные свойства диоксида азота.

Азотистая кислота HNO 2 и ее соли. НNО 2 существует только в виде водных растворов, устойчивых ниже 0°С. При более высоких температурах кислота постепенно разлагается: 3 HNO 2 = HNO 3 + 2 NO↑ + Н 2 О

Азотистая кислота HNO 2 и ее соли. Азотистая кислота принадлежит к слабым кислотам, ее константа диссоциации невелика

Азотистая кислота HNO 2 и ее соли. HNO 2 - слабый электролит Как кислота HNO 2 взаимодействует с химически активными металлами, их оксидами и гидроксидами. Mg+2 HNO 2→Mg(NO 2)2+H 2↑ Mg. O+2 HNO 2→Mg(NO 2)2+H 2 О

Азотистая кислота HNO 2 и ее соли Окислительно - восстановительные свойства HNO 2 Азотистая кислота проявляет как окислительные, так и восстановительные свойства:

Азотистая кислота HNO и ее соли. Азотистая кислота HNO 22 и ее соли. Нитриты - соли азотистой кислотыв большинстве кристаллические своем бесцветные вещества, растворимые в воде (кроме Ag. NO 2). хорошо

Азотистая кислота HNO 2 и ее соли. Разложение нитритов Нитриты различных металлов отличаются между собой отношением к нагреванию. Нитриты щелочных металлов плавятся без разложения, а остальные нитриты при нагревании разлагаются: Na. NO 2≠(реакция не происходит) Ca(NO 2)2 =Ca. O +NO 2+NO Ag. NO 2= Ag + NO 2

Азотистая кислота HNO и ее соли. Азотистая кислота HNO 22 и ее соли. Токсическое действие нитритов и нитратов Нитриты до последнего времени добавляли в качестве консервантов в колбасу, сосиски и другие мясные продукты. Хотя консерванты добавляют в очень незначительных количествах, существует мнение, что они опасны для человека.

Азотистая кислота HNO и ее соли. Азотистая кислота HNO 22 и ее соли. Токсическое действие нитритов и нитратов Одна из причин ядовитых свойств азотистой кислоты или нитритов в том, что они являются дезаминирующим и агентами, способствуют окислению нуклеиновых оснований. аминогрупп

Азотистая кислота HNO 2 и ее соли. Токсическое действие нитритов и нитратов Особенно сильное действие оказывает азотистая кислота, образующаяся из органических предшественников, например нитрозаминов, а также из нитросоединений.

Азотистая кислота HNO 2 и ее соли. Токсическое действие нитритов и нитратов При этом изменяется структура нуклеиновых оснований ДНК и их способность к образованию водородных связей, т. е. происходят повреждения в ДНК.

Азотистая кислота HNO 2 и ее соли. Токсическое действие нитритов и нитратов Токсическое действие нитритов проявляется и в том, что под их воздействием гемоглобин метгемоглобин, превращается который не в способен связывать и переносить кислород:

Азотистая кислота HNO и ее соли. Азотистая кислота HNO 22 и ее соли. Токсическое действие нитритов и нитратов Попадая в кровь, нитриты вызывают кислородную недостаточность. Аналогично действуют неорганические нитраты.

Азотистая кислота HNO 2 и ее соли. Лекарственные препараты В очень незначительных количествах некоторые неорганические нитриты (соединения типа R—О—N=O) и органические нитраты (R—О—NO 2) улучшают коронарное кровообращение и применяются для профилактики при ишемической болезни сердца и снятия приступов стенокардии.

Азотистая кислота HNO 2 и ее соли. Лекарственные препараты Представителями лекарственных нитритов и нитратов являются натрий нитрит Na. NO 2 и нитроглицерин (органическое соединение). Однако в настоящее время Na. NO 2 почти не используют, так как он может вызвать осложнения из-за гипоксии в организме. метгемоглобиновой

Азотная кислота 3 и ее Азотная кислота HNOHNO 3 соли. Азотная кислота — одна из наиболее сильных кислот. Физические свойства Азотная кислота в чистом состоянии без примеси воды — бесцветная, «дымящая» на воздухе жидкость с плотностью 1, 50 г/см 3; Ткип. =+83°С; Тпл. =-41°С.

Азотная кислота HNO 3 и ее соли. При длительном хранении и при нагревании она приобретает желтый оттенок вследствие выделения желто-бурового газа NO 2: 4 HNO 3=4 NО 2 ↑+ О 2 + 2 Н 2 О С водой азотная кислота смешивается в любых соотношениях.

Азотная кислота HNO 3 Химические свойства I. HNO 3 — сильный электролит В водных растворах молекулы HNO 3 полностью диссоциируют на ионы:

Азотная кислота HNO Азотная кислота 3 и ее 3 Азотная кислота HNOHNO 3 соли. Проявляя свойства взаимодействует: кислот, HNO 3 а) с оксидами металлов: 2 HNO 3 + Са. О = Ca(NO 3)2 + Н 2 О: б) с основаниями и амфотерными гидроксидами: 2 HNO 3 +Ва(ОН)2=Ba(NO 3)2+2 Н 2 О:

Азотная кислота HNO 3 в) с солями более слабых кислот: 2 HNO 3 +Na 2 CO 3=2 Na. NO 3+Н 2 О+СО 2; г) с аммиаком: HNO 3 + NH 3 = NH 4 NO 3;

Азотная кислота HNO 3 II. HNO 3 — сильный окислитель Ярко выраженная окислительная способность является самым характерным химическим свойством азотной кислоты. Она окисляет почти все металлы, многие неметаллы и сложные вещества.

Азотная кислота HNO 3 Окислительные свойства HNO 3 обусловлены присутствием в составе ее аниона NO 3 -, в котором атом азота проявляет высшую степень окисления N+5. Продукты окисления зависят как от концентрации кислоты, так активности восстановителя. (табл. 2) и от

Азотная кислота. HNO 3 3 Азотная кислота HNO 1. Взаимодействие HNO 3 с металлами Общие принципы взаимодействия HNO 3 с различными металлами: Кислота Металл Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb H 2 Cu, Нg, Ag, Pt, Au Разбавл енная HNO 3 соль+NH 3↑+H 2 O соль+NO↑+H 2 O Al (или NH 4 NO 3) Концент Cr Fe рирован соль+N 2 О↑+H 2 O соль+NO 2↑+H 2 O ная Al HNO 3 Pt, Au

Азотная кислота HNO 3 4 Pb+10 HNO 3=4 Pb(NO 3)2+N 2 O↑+5 H 2 O

Азотная кислота HNO 33 Азотная кислота HNO 2. Взаимодействие HNO 3 с неметаллами При взаимодействии с азотной кислотой неметаллы, как правило, окисляются до их высшей степени окисления:

Азотная кислота HNO Азотная кислота. HNO 3 3 В случае использования концентрированной кислоты выделяется бурый газ NO 2.

Азотная кислота HNO 3 В настоящее время HNO 3 получают по следующей схеме:

Применение азотной кислоты Азотная производства кислота используется азотных для удобрений; взрывчатых веществ (порох, тротил и др. ); ракетного топлива; анилина и анилиновых красителей; лекарственных полимерных материалов. препаратов;

Соли азотной кислоты – нитраты. Нитраты - бесцветные кристаллические вещества, хорошо растворимые в воде. Особенностью нитратов является их неустойчивость при нагревании и характер термического разложения.
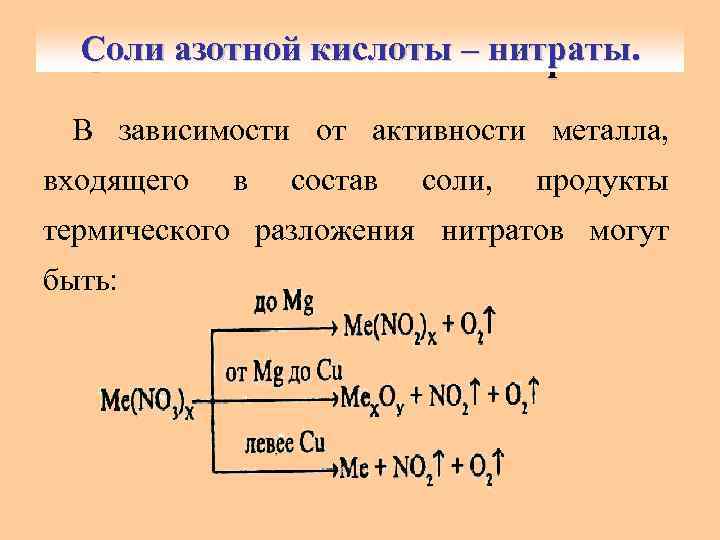
Соли азотной кислоты – нитраты. В зависимости от активности металла, входящего в состав соли, продукты термического разложения нитратов могут быть:

Фосфор и его свойства Характеристика элемента Фосфор — это неметалл семейства рэлементов, ближайший аналог азота. В своих соединениях фосфор проявляет валентности, равные III и V; степени окисления (наиболее характерные): -3, 0, +3, +5. (табл. 3)

Фосфор и его свойства Аллотропия фосфора В настоящее время известно, что фосфор существует в виде нескольких аллотропных модификаций, различающихся строению между молекул, собой по физическим свойствам и химической активности.

Фосфор и его свойства Аллотропия фосфора Белый фосфор - при обычных условиях твердое вещество, похожее на воск и окрашенное примесями в желтоватый цвет. На воздухе быстро окисляется, при этом выделяется энергия не в виде теплоты, а в виде света, поэтому белый фосфор в темноте светится.

Фосфор и его свойства Аллотропия фосфора Химическая активность белого фтора намного превосходит активность всех других его аллотропных модификаций. Белый фосфор самопроизвольно воспламеняется на воздухе. Он очень ядовит, даже в малых дозах действует смертельно!

Фосфор и его свойства Аллотропия фосфора Красный фосфор - по свойствам резко отличается от белого фосфора: он характеризуется большой плотностью, не ядовит. Химическая активность гораздо ниже: он очень медленно окисляется на воздухе, не светится в темноте, загорается только при 260 °С.

Фосфор и его свойства Аллотропия фосфора Черный фосфор очень напоминает по свойствам графит: он жирный на ощупь, обладает электро- и теплопроводностью. Из всех аллотропных модификаций черный фосфор негорюч. наименее активен, практически

Фосфор и его свойства Получение фосфора Сырьем для получения фосфора служат фосфориты и апатиты, содержащие фосфат кальция Са 3(РО 4)2. Измельченные природные материалы смешивают с песком (Si. O 2) и углем (С) и накаливают в электрических печах без доступа воздуха:

Фосфор и его свойства Химические свойства 1. Реакции, в которых фосфор выступает как восстановитель, более многочисленны и протекают очень легко. При этом образуются соединения, содержащие фосфор в степени окисления +3 и +5.

Фосфор и его свойства При медленном окислении или недостатке окислителя При избытке окислителя 4 Р +ЗО 2 = 2 Р 2 О 3 4 Р+ 5 О 2 = 2 Р 2 О 5 2 Р +ЗС 12 = 2 РС 13 2 Р +5 С 12 = 2 РС 15 2 Р + 3 S = P 2 S 3 2 Р + 5 S = P 2 S 5

Фосфор и его свойства Химические свойства Азотная и концентрированная серная кислоты также окисляют фосфор до высшей степени окисления (+5), при этом образуется ортофосфорная кислота:

Взаимодействие фосфора с азотной кислотой 3 P+5 HNO 3+2 H 2 O=3 H 3 PO 4+5 NO↑

Фосфор и его свойства Химические свойства 2. Как окислитель (Р° + 3ē → Р-3), фосфор взаимодействует непосредственно почти со всеми металлами, образуя фосфиды, например: которые легко гидролизуются: Ва 3 Р 2 + 6 Н 2 О = 2 РН 3↑ + 3 Ва(ОН)2 Непосредственно с водородом фосфор не взаимодействует.

Соединения фосфора Фосфин РН 3 Водородное соединение — РН 3 - это бесцветный газ с чесночным запахом, малорастворим в воде, хорошо растворим в органических растворителях. Фосфин — очень ядовитое вещество; он использовался как одно из первых боевых отравляющих веществ.

Соединения фосфора Получение фосфина 1) действием соляной кислоты на фосфиды металлов, например; Са 3 Р 2 + 6 НС 1 = 2 РН 3↑ + ЗСа. Сl 2 2) действием водных растворов щелочей на фосфор при нагревании: 3) при необратимом гидролизе водных растворов фосфидов металлов: Mg 3 P 2 + 6 Н 2 О = 2 РН 3↑ + 3 Mg(OH)2↓

Соединения фосфора Химические свойства фосфина По химическим свойствам фосфин напоминает аммиак, сочетая в себе слабые основные свойства и восстановительную способность. Как восстановитель фосфин более активен по сравнению с аммиаком. Он легко окисляется кислородом воздуха:

Соединения фосфора Химические свойства фосфина Основные свойства РН 3 очень сильно ослаблены по сравнению с аммиаком. Образуемый при взаимодействии с водой гидроксид фосфония РН 4 ОН имеет степень диссоциации в несколько раз меньшую, чем гидроксид аммония NH 4 OH.

Соединения фосфора Химические свойства фосфина Фосфин РН 3 взаимодействует только с сильными безводными кислотами, например: РН 3 + НС 1 = РН 4 С 1; PH 3+HCl. O 4=PH 4 Cl. O 4

Соединения фосфора Оксиды фосфора и фосфорные кислоты. Фосфор образует большое число различных оксидов и кислородсодержащих кислот. Наиболее кислородные устойчивыми соединения, фосфор в степени окисления +5. являются содержащие

Соединения фосфора Получение оксида фосфора (III) ( 1. Оксид фосфора (III), или фосфористый ангидрид Р 2 О 3 получают при медленном окислении фосфора, или когда фосфор сгорает кислорода. при недостаточном доступе

Соединения фосфора Свойства оксида фосфора (III) ( Оксид фосфора (III) растворяется в воде: Р 2 О 3+ Н 2 О=2 НРО 2 метафосфористая кислота НРО 2+Н 2 О=Н 3 РО 3 ортофосфористая кислота

Соединения фосфора Свойства оксида фосфора (III) ( Фосфористый ангидрид и фосфористая кислота обладают сильными восстановительными свойствами, так как фосфор из состояния Р+3 стремится перейти в состояние Р+5.

Соединения фосфора Получение оксида фосфора (V) ( 2. Оксид фосфора (V), или фосфорный ангидрид Р 2 О 5 — белый порошок без запаха. Он образуется при горении фосфора на воздухе или в кислороде в виде белой объемистой снегообразной массы: 4 Р + 5 О 2 = 2 Р 2 О 5

Соединения фосфора Получение оксида фосфора (V) ( Р 2 О 5 — типичный кислотный оксид, проявляет соединений: все свойства этого взаимодействует основными оксидами, щелочами. с типа водой,

Соединения фосфора Получение оксида фосфора (V) ( При взаимодействии Р 2 О 5 с водой могут образоваться различные кислоты: Р 2 О 5 + Н 2 О = 2 НРО 3 метафосфорная кислота Р 2 О 5 + 2 Н 2 О =Н 4 Р 2 О 7 пирофосфорная кислота Р 2 О 5 + ЗН 2 О = 2 Н 3 РО 4 ортофосфорная кислота образуются при недостатке Н 2 О

Соединения фосфора Получение оксида фосфора (V) ( При взаимодействии с основными оксидами образуются соответствующие соли фосфорной кислоты — фосфаты: Р 2 О 5 + 3 Na 2 O =2 Na 3 PO 4 Р 2 О 5 + 3 Са. О = Са 3(РО 4)2

Соединения фосфора Получение оксида фосфора (V) ( При взаимодействии с щелочами образуются фосфаты, гидрофосфаты и дигидрофосфаты, в зависимости от соотношения реагентов: Р 2 О 5 + 6 Na. OH = 2 Na 3 PO 4 + 3 Н 2 О фосфат натрия Р 2 О 5 + 4 Na. OH = 2 Na 2 HPO 4 + H 2 O гидрофосфат натрия Р 2 О 5+ 2 Na. OH + Н 2 О = 2 Na. H 2 PO 4 дигидрофосфат натрия

Соединения фосфора Получение оксида фосфора (V) ( Окислительные свойства у Р 2 О 5 не выражены, поскольку высшая степень окисления (+5) является для фосфора очень устойчивой.

Соединения фосфора Получение оксида фосфора (V) ( 3. Фосфорная (ортофосфорная) кислота Н 3 РО 4 — наиболее устойчивая и практически важная кислота, образуемая фосфором. В чистом виде это бесцветное кристаллическое вещество, плавящееся при температуре 42 °С, очень хорошо растворимое в воде.

Соединения фосфора Химические свойства Н 3 РО 4 Фосфорная кислота Н 3 РО 4 проявляет все важнейшие свойства типичных кислот: взаимодействует с металлами, стоящими в ряду активности до водорода, с оксидами металлов, с основаниями, с солями более слабых кислот, с аммиаком.

Соединения фосфора Химические свойства Н 3 РО 4 Анионы фосфорной кислоты не проявляют окислительных свойств, что связано с устойчивой степенью окисления +5 у фосфора.

Соединения фосфора Соли фосфорной кислоты Как трехосновная кислота Н 3 РО 4 образует три ряда солей: средние (нормальные) соли фосфаты; кислые соли — гидрофосфаты и дигидрофосфаты.

Соединения фосфора Соли фосфорной кислоты Качественная реакция на фосфат-ион. 3 Ag. NO 3+Na 3 PO 4=Ag 3 PO 4↓+3 Na. NO 3

Соединения фосфора. Соли фосфорной кислоты Большинство средних солей — фосфатов — нерастворимо в воде. Исключением являются лишь фосфаты щелочных металлов и аммония. Многие же кислые соли фосфорной кислоты хорошо растворяются в воде, причем наиболее растворимыми являются дигидрофосфаты.

Соединения фосфора Применение солей фосфорной кислоты Ортофосфорная кислота и трудно-растворимые фосфаты алюминия Аl. РО 4 и цинка Zn 3(PO 4)2 входят в состав фосфат-цементов, применяемых в стоматологии в качестве пломбировочного материала.
Биологическая роль соединений фосфора С биологической точки зрения чрезвычайно важными являются бионеорганические производные дифосфорной кислоты Н 4 Р 2 О 7 и не выделенной в свободном виде трифосфорной кислоты Н 5 Р 3 О 10. Это аденозиндифосфорная кислота (АДФ) аденозинтрифосфорная кислота (АТФ).
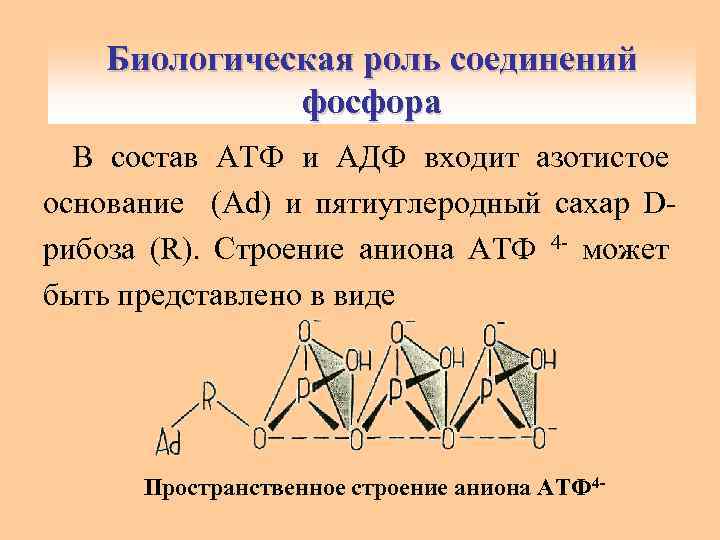
Биологическая роль соединений фосфора В состав АТФ и АДФ входит азотистое основание (Ad) и пятиуглеродный сахар Dрибоза (R). Строение аниона АТФ 4 - может быть представлено в виде Пространственное строение аниона АТФ 4 -
Биологическая роль соединений фосфора Являясь бионеорганическими производными дифосфорной и трифосфорной кислот, АДФ и АТФ во многом ведут себя при ионизации аналогично этим кислотам с несколько большим» значением р. Ка. Так, для дифосфорной кислоты значение р. Ка третьей ступени составляет 6, 7 а для АТФ р. Ка второй ступени равно 7, 2.

Биологическая роль соединений фосфора При физиологическом р. Н 7, 4 АТФ и АДФ практически полностью существуют в виде анионов АТФ 4 - фосфатные и группы ионизированы. АДФ 3 -, т. е. почти их полностью

Биологическая роль соединений фосфора Подобно анионам полифосфорных кислот анионы АТФ 4 - и АДФ 3 - подвергаются гидролизу. В результате присоединения одной молекулы воды АТФ 4 - гидролизуется до аниона аденозиндифосфата АДФ 3 - и водород фосфатиона Н 3 РО 42 - : пространственное строение АДФ 3 - аниона

Биологическая роль соединений фосфора Как и полифосфорные кислоты, АДФ и АТФ образуют с катионами металлов комплексные соли. Так, во внутриклеточной жидкости АТФ и АДФ присутствуют главным образом в виде комплексов с магнием: Мg. АТФ 2 - и Мg. АДФ-.

Биологическая роль соединений фосфора В очень многих ферментативных реакциях, в которых АТФ участвует в качестве донора фосфатной группы, активной формой АТФ является комплекс Мg. АТФ 2 -. Главным образом этой причине магний — жизненно необходимый элемент для организма.

Свойства важнейших соединений мышьяка, сурьмы, висмута Общая характеристика Массовая доля элементов в земной коре составляет: As - 1, 7· 10 -4 %, Sb-5· 10 -5%, Bi 2· 10 -5%. Для мышьяка одинаково характерны степени окисления +3 и +5, сурьма чаще проявляет в соединениях степень окисления +3, хотя имеются соединения, в которых Sb проявляет степень окисления +5 (Sb 2 O 5, Sb. CI 5 и др. ).

Свойства важнейших соединений мышьяка, сурьмы, висмута Общая характеристика Для висмута известно много соединений Bi 3+, в то время как вещества, содержащие Bi 5+, немногочисленны и являются сильными окислителями. Соединения мышьяка, сурьмы и висмута очень ядовиты, в особенности катионные соли As 3+ и арсин As. H 3.

Свойства важнейших соединений мышьяка, сурьмы, висмута Соединения с неметаллами При переходе от фосфора к мышьяку, сурьме и висмуту усиливается тенденция к образованию соединений с серой и лигандами. серосодержащими

Свойства важнейших соединений мышьяка, сурьмы, висмута Соединения с неметаллами В отличие от азота (в биомолекулах наиболее характерны связи с водородом и углеродом) и фосфора (характерны связи с кислородом) более тяжелые элементы группы VA As, Sb, Bi склонны образовывать связи с кислородом и с серой. В частности, в природе As, Sb и Bi, как правило, встречаются в виде сульфидов As 2 S 3, Sb 2 S 3, Bi 2 S 3.

Свойства важнейших соединений мышьяка, сурьмы, висмута Соединения с неметаллами Среди соединений мышьяка, сурьмы и висмута со степенью окисления — 3 интерес представляют газообразные водородные соединения: арсин As. H 3, стибин Sb. H 3 и висмутин Bi. H 3. Все они очень токсичны.

Свойства важнейших соединений мышьяка, сурьмы, висмута Соединения с неметаллами Степень окисления +3 мышьяк и его аналоги проявляют в галогенидах ЭГ 3, оксидах Э 2 О 3 и сульфидах Э 2 S 3. Мышьяк (III) оксид Аs 2 О 3 — амфотерный оксид с преобладанием кислотных свойств. As 2 O 3 растворяется в воде с образованием гидроксида: As 2 O 3(т)+ЗН 2 О(ж)=2 H 3 As. O 3(p) или As(OH)3

Свойства важнейших соединений мышьяка, сурьмы, висмута Гидроксиды Мышьяк (III) гидроксид — амфотерен, но так же, как у As 2 O 3, у него преобладают кислотные свойства. В свободном состоянии Аs(ОН)3 не выделен, в водном растворе ведет себя как слабая кислота H 3 As. О 3, называемая ортомышьяковистой (мышьяковистой).

Свойства важнейших соединений мышьяка, сурьмы, висмута Гидроксиды В водных кислота растворах находится в мышьяковистая равновесии метамышьяковистой кислотой HAs. О 2: H 3 As. О 3 HAs. O 2 + H 2 O с

Свойства важнейших соединений мышьяка, сурьмы, висмута Соли мышьяковой кислоты Соли H 3 As. О 3 кислоты ортоарсенитами метаарсенитами. обычно и Из HAs. О 2 водных кристаллизуются состава МЭО 2. называются кислоты растворов метаарсениты

Свойства важнейших соединений мышьяка, сурьмы, висмута Токсичность соединений мышьяка Соединения особенности мышьяка (V) (III) и в очень токсичны. Механизм токсического действия объясняют способностью блокировать мышьяка сульфгидрильные группы —SH ферментов и других биологически активных соединений.

Свойства важнейших соединений мышьяка, сурьмы, висмута Токсичность соединений мышьяка В организме человека мышьяк взаимодействует с глутатионом — веществом, представляющим собой соединение трех аминокислот — глутаминовой кислоты, цистеина и глицина. При этом блокируется сульфгидрильная группа и глутатион теряет одну из важных своих биологических функций — восстановление токсичных пероксидов.

Свойства важнейших соединений мышьяка, сурьмы, висмута Токсичность соединений мышьяка Упрощенно этот процесс можно представить следующим образом: где R — радикал глутамата-иона.

Свойства важнейших соединений мышьяка, сурьмы, висмута Токсичность соединений мышьяка Мышьяк может замещать йод, селен и фосфор. Нарушая биохимические процессы метаболизма в организме As является антиметаболитом этих элементов. Смертельная составляет мышьяка. доза для приблизительно человека 0, 1— 0, 3 г

Свойства важнейших соединений мышьяка, сурьмы, висмута. Токсичность соединений мышьяка В отличие от фосфора, у которого токсичны только соединения фосфорa (III), мышьяк токсичен и в степени окисления +5. Последнее обусловлено тем, что в организме человека мышьяк (V) легко восстанавливается до соединений мышьяка (III).

Свойства важнейших соединений мышьяка, сурьмы, висмута Токсичность соединений мышьяка Соединения мышьяка не только убивают, но и помогают в борьбе за жизнь. Так, при остром отравлении мышьяком (III) оксидом As 2 O 3 смерть наступает примерно через 70 ч. В то же время это вещество применяют наружно (препарат белый мышьяк) при кожных заболеваниях.

Свойства важнейших соединений мышьяка, сурьмы, висмута Применение в медицинской практике В стоматологической практике As 2 O 3 используют для омертвления (некротизации) мягких тканей зуба. Кроме того, этот препарат назначают в микродозах (0, 001 г на прием) при малокровии, истощении, нервозности. Организм может привыкнуть к As 2 O 3, если его вводить постепенно, увеличивая дозу.

Свойства важнейших соединений мышьяка, сурьмы, висмута Применение в медицинской практике В медицинской практике используют и раствор калия арсенита К 3 Аs. О 3 (Фаулеров раствор мышьяка). Препарат применяют при тех заболеваниях, что и As 2 O 3. же

Свойства важнейших соединений мышьяка, сурьмы, висмута Применение в медицинской практике Применение К 3 Аs. О 3 Аs 2 О 3 при одних и тех заболеваниях объясняется тем, что обоих случаях в кислой среде желудка образуется мышьяковистая кислота: As 2 O 3 + ЗН 2 О = 2 H 3 As. О 3 As. O 33 - + 3 H+ = H 3 As. О 3 Механизм действия этих препаратов связан с блокированием сульфгидрильных групп.

Свойства важнейших соединений мышьяка, сурьмы, висмута Применение в медицинской практике Сурьма (III) оксид Sb 2 O 3 и висмут (III) оксид Bi 2 O 3 в воде нерастворимы. Оксид сурьмы — амфотерен, а оксид висмута имеет основной характер. Bi 2 O 3 (50— 55%) входит в состав препарата ксероформ. Применяют наружно как вяжущее средство, подсушивающее и антисептическое средство.

Свойства важнейших соединений мышьяка, сурьмы, висмута Гидролиз солей Sb 3+ и Bi 3+ При гидролизе солей Sb 3+ и Bi 3+ образуются оксосоли: Sb. Cl 3 + Н 2 О Sb. OCl + 2 HCl Bi(NO 3)3 + H 2 O Bi. ONO 3 + 2 HNO 3 Оксосоли Sb 3+ и Bi 3+ можно рассматривать как соединения радикалов антимонила (стибила) Sb. O+ и висмутила Вi. O+. Отсюда их названия: антимонил хлорид, висмутил нитрат.

Свойства важнейших соединений мышьяка, сурьмы, висмута Применение Bi(NO 3)3 в фармации Препарат висмута нитрат основной состоит из смеси продуктов гидролиза Bi(NO 3)3: Bi(OH)2 NO 3, Bi. ONO 3 и дегидратированного висмута гидроксида Bi. OOH. Применяют Bi(NO 3)3 в качестве вяжущего и отчасти антисептического средства при желудочно-кишечных заболеваниях.
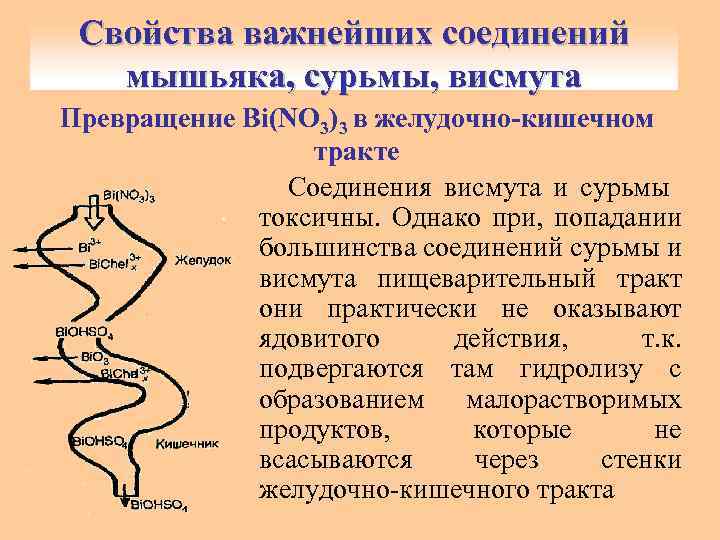
Свойства важнейших соединений мышьяка, сурьмы, висмута Превращение Bi(NO 3)3 в желудочно-кишечном тракте Соединения висмута и сурьмы токсичны. Однако при, попадании большинства соединений сурьмы и висмута пищеварительный тракт они практически не оказывают ядовитого действия, т. к. подвергаются там гидролизу с образованием малорастворимых продуктов, которые не всасываются через стенки желудочно-кишечного тракта

Свойства важнейших соединений мышьяка, сурьмы, висмута. Важнейшие соединения As(V), Sb(V), Bi(V). Оксиды высшей степени окисления тяжелых элементов VA-группы As(V), Sb(V), Bi(V) типа Э 2 О 5 при обычных условиях — твердые вещества. Устойчивость этих оксидов уменьшается при переходе от мышьяка к висмуту: As 2 O 5—Sb 2 O 5—Bi 2 O 5 устойчивость падает

Свойства важнейших соединений мышьяка, сурьмы, висмута. Важнейшие соединения As(V), Sb(V), Bi(V). При растворении в воде As 2 O 5 образуется мышьяковая кислота H 3 As. O 4: As 2 O 5 + 3 H 2 O = 2 H 3 As. O 4 Это кислота средней силы (К 1= 6· 10 -3, К 2=2· 10 -7, К 3=3· 10 -12) — аналог ортофосфорной кислоты Н 3 РО 4.

Свойства важнейших соединений мышьяка, сурьмы, висмута. Важнейшие соединения As(V), Sb(V), Bi(V). Оксид Sb 2 O 5 плохо растворим в воде. При попытке получения сурьмяных кислот образуется осадок Sb 2 O 5 · х Н 2 О. В свободном состоянии не кислородные кислоты Bi (V). выделены и

Свойства важнейших соединений мышьяка, сурьмы, висмута. Соли мышьяковистой кислоты Соли H 3 As. O 4 — арсенаты вследствие сходства строения электронных оболочек атомов Р и As похожи на ортофосфаты. Существует три ряда солей: арсенаты, например Na 3 As 04, Ca 3(As. O 4)2, водородарсенаты, например Na 2 HAs. O 4, Ca. HAs. O 4, и диводородарсенаты, например Na. H 2 As. О 4, Ca(H 2 As. О 4)2.

Свойства важнейших соединений мышьяка, сурьмы, висмута. Применение соединений мышьяка В медицинской практике используют Na. H 2 As. O 4 • 7 H 2 O в виде 1%-ного раствора при нервных расстройствах, легких формах малокровия. Механизм действия препарата также, очевидно, связан блокированием сульфгидрильных групп белков, ферментов.

Свойства белого фосфора

Аллотропное превращение красного фосфора

Горение красного фосфора

Таблица 1 Характеристика свойств оксидов азота Химическая формула и название Физические свойства Химические свойства Взаимодейст вие с водой N 2 O оксид азота (I), «веселящий газ» Газ без цвета, слабый приятный запах, растворим в воде. Обладает наркотическим действием Несолеобразующий оксид. При высокой температуре разлагается: 2 N 2 O = 2 N 2+O 2 Не взаимодейств ует NO оксид азота (II), монооксид азота Газ без цвета, без запаха, малорастворим в воде, ядовит Несолеобразующий оксид. Не взаимодейств ует N 2 O 3 оксид азота (III), азотистый ангидрид Газ красно-бурого цвета, при охлаждении сгущается в синюю жидкость, растворим в воде Кислотный оксид. При нагревании выше температуры кипения легко разлагается: Образует азотистую кислоту: N 2 O 5+H 2 O= 2 HNО 3 N 2 O 3= NО+NO 2

Таблица 1 Характеристика свойств оксидов азота Химическая формула и название Физические свойства Химические свойства NO 2 оксид азота (IV), диоксид азота Газ бурового цвета с характерным запахом, хорошо растворим в воде, ядовит Кислотный оксид. Легко димеризуется: N 2 O 5 оксид азота (V), азотный ангидрид Бесцветные кристаллы, расплывающиеся на воздухе. Растворим в воде Кислотный оксид молекулы неустойчивы, легко разлагаются 2 NO 2 N 2 О 4 2 N 2 O 5= 4 NО 2+O 2 разложение происходит со взрывом Взаимодействие с водой Образует кислоты: а) в отсутствии О 2 б) в присутствии О 2 —HNО 3 Образует азотную кислоту: N 2 O 5+H 2 O= 2 HNО 3
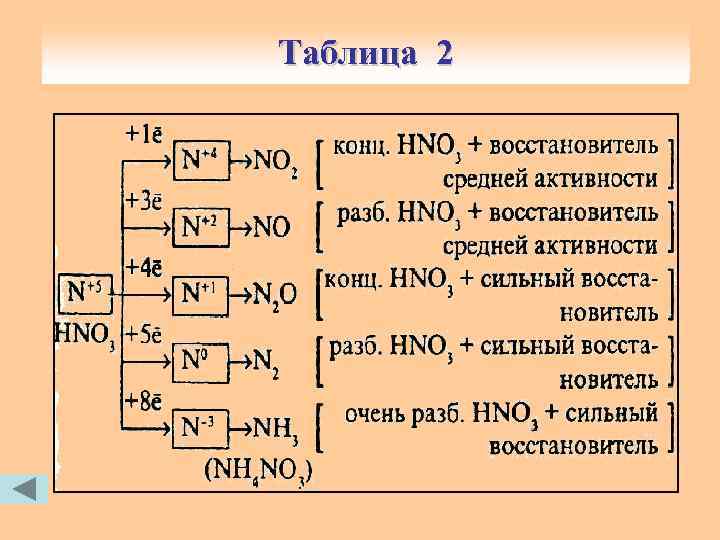
Таблица 2 Азотная кислота HNO 3

Таблица 3 Степень окисления Вещества -3 PH 3 фосфин фосфиды Na 3 P Ca 3 P 2 и др. 0 P простое вещество +3 P 2 O 3 +5 P 2 O 5 оксид фосфора (III) фосфора(V) HPO 2 HPO 3 и H 3 PO 4, их солифосфиты фосфаты: Na. PO 2 Na. PO 3, K 3 PO 3 и др. Ca 3(PO 4)2 и др. Наиболее устойчивы соединения фосфора со степенью окисления +5

Термины и определения. способность атома химического элемента образовывать химические связи с другими атомами. Гемоглобин - дыхательный пигмент, содержащийся в эритроцитах и обусловливающий цвет крови. Представляет собой сложный белок, образованный белком, глобином, связанным с гемом. Осуществляет транспорт кислорода из легких в ткани, а из последних СО 2 в легкие. Валентность

Термины и определения. Гидролиз - взаимодействие ионов соли с водой, приводящее к образованию слабого электролита и изменению р. Н- среды. Дезоксирибонуклеиновая кислота (ДНК) – полинуклеотид, содержащий в качестве оснований аденин, гуанин, цитозин, а сахарный компонент представлен 2 -дезокси - D-рибозой.

Термины и определения. Катализатор - вещество, влияющее на скорость химической реакции или возбуждающее ее, но в конечном итоге остающееся неизменным. Ковалентная связь - связь, формирующаяся между двумя (и более) атомами обобществления ими электронов. путем

Термины и определения. Метаболизм - полная совокупность катализируемых ферментами превращений органических молекул в организме. Метгемоглобин - гемоглобин в котором железо трехвалентно. Метгемоглобин не присоединяет кислород и поэтому не может обеспечить дыхание тканей.

Термины и определения. Степень окисления (состояние окисления)целочисленный условный заряд (положительный или отрицательный), приписываемый атому в молекуле или ионе на основе совокупности формальных правил, условно допускающих, что все молекулы состоят из ионов.

Термины и определения. Ферменты - соединения белковой природы, выполняющие роль катализаторов в биохимических реакциях. Иначе называются биокатализаторами.

Термины и определения. Электроотрицательность – способность атома притягивать к себе электроны других атомов. Эндотермические реакции сопровождающиеся поглощением тепловой энергии.

Литература Пустовалова Л. М. Неорганическая химия: серия «Среднее профессиональное образование» , Ростов-на-Дону: Феникс, 2005. -252 с. Барковский Е. В. Аналитическая химия: учеб. пособие - Мн. : Высш. Шк. , 2004. -351 с.

Литература Л. М. Пустовалова, И. Е. Никанорова. – Общая химия: Ростов-на-Дону: Феникс, 2005. – 478 с. Бабков А. В. Химия: учебник для студ. сред. мед. учеб. заведений. - М. : издательский центр «Академия» , 2003. -272 с. Глинка Н. Л. Общая химия. Учебное пособие. -Интеграл-пресс. -2008 г. -
главная подгруппа 5 группы.ppt