в помощь к теме галогены простые вещества.ppt
- Количество слайдов: 12
 Галогены Характеристика элементов группы галогенов и простых веществ
Галогены Характеристика элементов группы галогенов и простых веществ
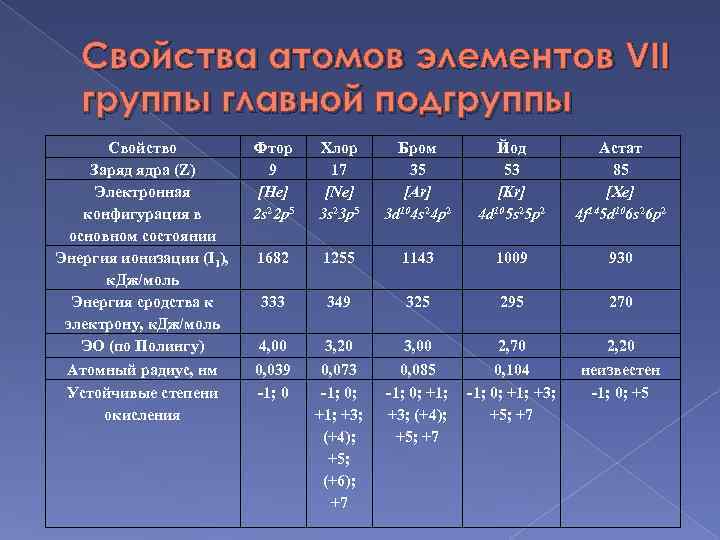 Свойства атомов элементов VII группы главной подгруппы Свойство Заряд ядра (Z) Электронная конфигурация в основном состоянии Энергия ионизации (I 1), к. Дж/моль Энергия сродства к электрону, к. Дж/моль ЭО (по Полингу) Атомный радиус, нм Устойчивые степени окисления Фтор 9 [He] 2 s 22 p 5 Хлор 17 [Ne] 3 s 23 p 5 Бром 35 [Ar] 3 d 104 s 24 p 2 Йод 53 [Kr] 4 d 105 s 25 p 2 Астат 85 [Xe] 4 f 145 d 106 s 26 p 2 1682 1255 1143 1009 930 333 349 325 295 270 4, 00 0, 039 -1; 0 3, 20 0, 073 -1; 0; +1; +3; (+4); +5; (+6); +7 3, 00 0, 085 -1; 0; +1; +3; (+4); +5; +7 2, 70 0, 104 -1; 0; +1; +3; +5; +7 2, 20 неизвестен -1; 0; +5
Свойства атомов элементов VII группы главной подгруппы Свойство Заряд ядра (Z) Электронная конфигурация в основном состоянии Энергия ионизации (I 1), к. Дж/моль Энергия сродства к электрону, к. Дж/моль ЭО (по Полингу) Атомный радиус, нм Устойчивые степени окисления Фтор 9 [He] 2 s 22 p 5 Хлор 17 [Ne] 3 s 23 p 5 Бром 35 [Ar] 3 d 104 s 24 p 2 Йод 53 [Kr] 4 d 105 s 25 p 2 Астат 85 [Xe] 4 f 145 d 106 s 26 p 2 1682 1255 1143 1009 930 333 349 325 295 270 4, 00 0, 039 -1; 0 3, 20 0, 073 -1; 0; +1; +3; (+4); +5; (+6); +7 3, 00 0, 085 -1; 0; +1; +3; (+4); +5; +7 2, 70 0, 104 -1; 0; +1; +3; +5; +7 2, 20 неизвестен -1; 0; +5
 Получение хлора Промышленные методы: 1) Метод Шееле Mn. O 2 + 4 HCl → Mn. Cl 2 + Cl 2↑ + 2 H 2 O 2) В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. 4 HCl + O 2 → 2 H 2 O + 2 Cl 2 Минерал пиролюзит 3) Электролиз водного раствора хлорида натрия 2 Na. Cl + 2 H 2 О → H 2↑ + Cl 2↑ + 2 Na. OH Анод: 2 Cl- — 2 е- → Cl 20↑ Катод: 2 H 2 O + 2 e- → H 2↑ + 2 OH-
Получение хлора Промышленные методы: 1) Метод Шееле Mn. O 2 + 4 HCl → Mn. Cl 2 + Cl 2↑ + 2 H 2 O 2) В 1867 году Диконом был разработан метод получения хлора каталитическим окислением хлороводорода кислородом воздуха. 4 HCl + O 2 → 2 H 2 O + 2 Cl 2 Минерал пиролюзит 3) Электролиз водного раствора хлорида натрия 2 Na. Cl + 2 H 2 О → H 2↑ + Cl 2↑ + 2 Na. OH Анод: 2 Cl- — 2 е- → Cl 20↑ Катод: 2 H 2 O + 2 e- → H 2↑ + 2 OH-
 Получение хлора в промышленности 4) Реакция серного ангидрида с поваренной солью: 2 Na. Cl + 2 SO 3 = Na 2 S 2 O 7 + SO 2 + Cl 2 5) Разложение пиросульфата натрия при 480 °С 2 Na. Cl + 2 Na 2 S 2 O 7 = 3 Na 2 SO 4 + SO 2 + Cl 2 6) Метод Сольве основан на пропускании горячего воздуха над раскаленной смесью хлорида кальция и кварцевого песка: 2 Ca. Cl 2 + 2 Si. O 2 + O 2 = 2 Ca Si. O 3 + 2 Cl 2↑
Получение хлора в промышленности 4) Реакция серного ангидрида с поваренной солью: 2 Na. Cl + 2 SO 3 = Na 2 S 2 O 7 + SO 2 + Cl 2 5) Разложение пиросульфата натрия при 480 °С 2 Na. Cl + 2 Na 2 S 2 O 7 = 3 Na 2 SO 4 + SO 2 + Cl 2 6) Метод Сольве основан на пропускании горячего воздуха над раскаленной смесью хлорида кальция и кварцевого песка: 2 Ca. Cl 2 + 2 Si. O 2 + O 2 = 2 Ca Si. O 3 + 2 Cl 2↑
 Получение хлора в лаборатории В лаборатории хлор получают взаимодействием концентрированной соляной кислоты с сильными окислителями: 16 HCl + 2 KMn. O 4 = 5 Cl 2 + 2 KCl + 2 Mn. Cl 2 + 8 H 2 O
Получение хлора в лаборатории В лаборатории хлор получают взаимодействием концентрированной соляной кислоты с сильными окислителями: 16 HCl + 2 KMn. O 4 = 5 Cl 2 + 2 KCl + 2 Mn. Cl 2 + 8 H 2 O
 Получение брома и йода При получении свободных брома и йода чаще всего пользуются вытеснением их хлором по реакциям, например: Mg. Br 2 + Сl 2 = Mg. Cl 2 + Вr 2 2 KJ + Сl 2 = 2 КСl + J 2
Получение брома и йода При получении свободных брома и йода чаще всего пользуются вытеснением их хлором по реакциям, например: Mg. Br 2 + Сl 2 = Mg. Cl 2 + Вr 2 2 KJ + Сl 2 = 2 КСl + J 2
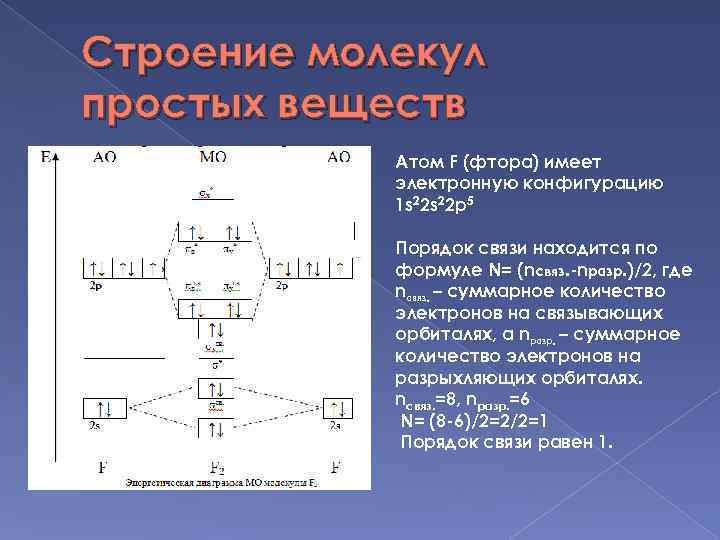 Строение молекул простых веществ Атом F (фтора) имеет электронную конфигурацию 1 s 22 p 5 Порядок связи находится по формуле N= (nсвяз. -nразр. )/2, где nсвяз. – суммарное количество электронов на связывающих орбиталях, а nразр. – суммарное количество электронов на разрыхляющих орбиталях. nсвяз. =8, nразр. =6 N= (8 -6)/2=2/2=1 Порядок связи равен 1.
Строение молекул простых веществ Атом F (фтора) имеет электронную конфигурацию 1 s 22 p 5 Порядок связи находится по формуле N= (nсвяз. -nразр. )/2, где nсвяз. – суммарное количество электронов на связывающих орбиталях, а nразр. – суммарное количество электронов на разрыхляющих орбиталях. nсвяз. =8, nразр. =6 N= (8 -6)/2=2/2=1 Порядок связи равен 1.
 Сравнение электронного строения молекул фтора и хлора
Сравнение электронного строения молекул фтора и хлора
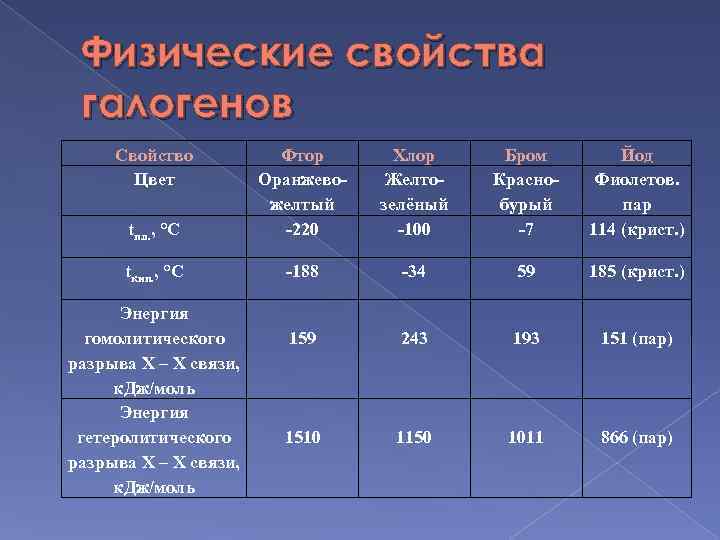 Физические свойства галогенов Свойство Цвет tпл. , °С Фтор Оранжевожелтый -220 Хлор Желтозелёный -100 Бром Краснобурый -7 Йод Фиолетов. пар 114 (крист. ) tкип. , °С -188 -34 59 185 (крист. ) 159 243 193 151 (пар) 1510 1150 1011 866 (пар) Энергия гомолитического разрыва Х – Х связи, к. Дж/моль Энергия гетеролитического разрыва Х – Х связи, к. Дж/моль
Физические свойства галогенов Свойство Цвет tпл. , °С Фтор Оранжевожелтый -220 Хлор Желтозелёный -100 Бром Краснобурый -7 Йод Фиолетов. пар 114 (крист. ) tкип. , °С -188 -34 59 185 (крист. ) 159 243 193 151 (пар) 1510 1150 1011 866 (пар) Энергия гомолитического разрыва Х – Х связи, к. Дж/моль Энергия гетеролитического разрыва Х – Х связи, к. Дж/моль
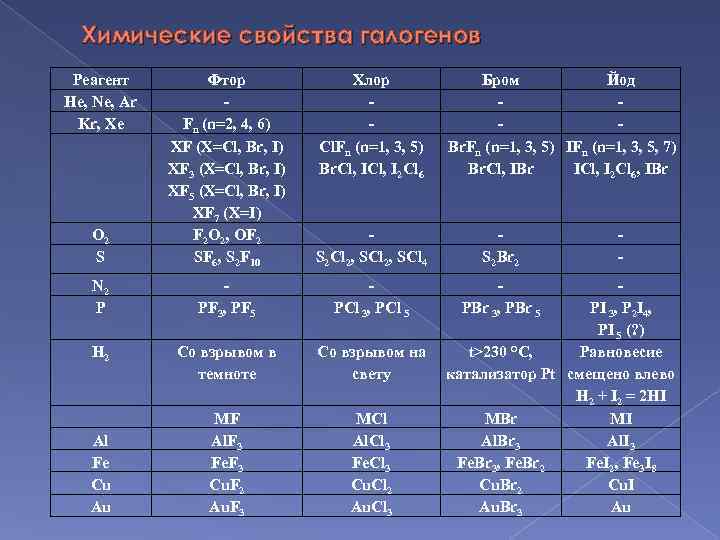 Химические свойства галогенов Реагент He, Ne, Ar Kr, Xe O 2 S Фтор Fn (n=2, 4, 6) XF (X=Cl, Br, I) XF 3 (X=Cl, Br, I) XF 5 (X=Cl, Br, I) XF 7 (X=I) F 2 O 2, OF 2 SF 6, S 2 F 10 S 2 Cl 2, SCl 4 S 2 Br 2 N 2 P PF 3, PF 5 PCl 3, PCl 5 PBr 3, PBr 5 H 2 Со взрывом в темноте Со взрывом на свету MF Al. F 3 Fe. F 3 Cu. F 2 Au. F 3 MCl Al. Cl 3 Fe. Cl 3 Cu. Cl 2 Au. Cl 3 Al Fe Cu Au Хлор Cl. Fn (n=1, 3, 5) Br. Cl, I 2 Cl 6 Бром Йод Br. Fn (n=1, 3, 5) IFn (n=1, 3, 5, 7) Br. Cl, IBr ICl, I 2 Cl 6, IBr - PI 3, P 2 I 4, PI 5 (? ) t>230 °С, Равновесие катализатор Pt смещено влево Н 2 + I 2 = 2 НI MBr MI Al. Br 3 Al. I 3 Fe. Br 3, Fe. Br 2 Fe. I 2, Fe 3 I 8 Cu. Br 2 Cu. I Au. Br 3 Au
Химические свойства галогенов Реагент He, Ne, Ar Kr, Xe O 2 S Фтор Fn (n=2, 4, 6) XF (X=Cl, Br, I) XF 3 (X=Cl, Br, I) XF 5 (X=Cl, Br, I) XF 7 (X=I) F 2 O 2, OF 2 SF 6, S 2 F 10 S 2 Cl 2, SCl 4 S 2 Br 2 N 2 P PF 3, PF 5 PCl 3, PCl 5 PBr 3, PBr 5 H 2 Со взрывом в темноте Со взрывом на свету MF Al. F 3 Fe. F 3 Cu. F 2 Au. F 3 MCl Al. Cl 3 Fe. Cl 3 Cu. Cl 2 Au. Cl 3 Al Fe Cu Au Хлор Cl. Fn (n=1, 3, 5) Br. Cl, I 2 Cl 6 Бром Йод Br. Fn (n=1, 3, 5) IFn (n=1, 3, 5, 7) Br. Cl, IBr ICl, I 2 Cl 6, IBr - PI 3, P 2 I 4, PI 5 (? ) t>230 °С, Равновесие катализатор Pt смещено влево Н 2 + I 2 = 2 НI MBr MI Al. Br 3 Al. I 3 Fe. Br 3, Fe. Br 2 Fe. I 2, Fe 3 I 8 Cu. Br 2 Cu. I Au. Br 3 Au
 Химические свойства галогенов В атмосфере фтора сгорает вода, стеклянная вата и порошок кварца, разлагаются многие соли: Si. O 2 + 2 F 2 = Si. F 4 + O 2 2 F 2 + Na 2 SO 4 = 2 Na. F + SO 2 F 2 + O 2 От фтора к иоду окислительная способность уменьшается, восстановительные свойства усиливаются. 2 KI + Cl 2 = I 2 + 2 KCl (фиолетовое окрашивание) I 2 + 5 Cl 2 + 6 Н 2 О = 2 НIО 3 + 10 НCl (обесцвечивание за счет образования йодноватой кислоты) Хлор реагирует с оксидами некоторых металлов (Mg, Al, Fe, W) с образованием хлоридов или оксохлоридов (WО 2 Cl 2) 2 Mg. O + 2 Cl 2 = 2 Mg. Cl 2 + O 2
Химические свойства галогенов В атмосфере фтора сгорает вода, стеклянная вата и порошок кварца, разлагаются многие соли: Si. O 2 + 2 F 2 = Si. F 4 + O 2 2 F 2 + Na 2 SO 4 = 2 Na. F + SO 2 F 2 + O 2 От фтора к иоду окислительная способность уменьшается, восстановительные свойства усиливаются. 2 KI + Cl 2 = I 2 + 2 KCl (фиолетовое окрашивание) I 2 + 5 Cl 2 + 6 Н 2 О = 2 НIО 3 + 10 НCl (обесцвечивание за счет образования йодноватой кислоты) Хлор реагирует с оксидами некоторых металлов (Mg, Al, Fe, W) с образованием хлоридов или оксохлоридов (WО 2 Cl 2) 2 Mg. O + 2 Cl 2 = 2 Mg. Cl 2 + O 2
 Химические свойства галогенов Жидкий бром реагирует со многими простыми веществами энергичнее газообразного хлора. В водной среде бром окисляет серу до серной кислоты: 3 Br 2 + S + 4 Н 2 О = 6 HBr + H 2 SO 4 Манганат калия окисляет до перманганата: 2 K 2 Mn. O 4 + Br 2 = 2 KMn. O 4 + 2 KBr Окислительные свойства йода выражены слабее, чем у других галогенов. Йод не способен окислить даже серу. В тоже время для йода характерны восстановительные свойства. Под действием сильных окислителей йод окисляется до йодноватой кислоты: 3 I 2 (тв. ) + 10 НNО 3 (100%) = 6 НIО 3 + 10 NО 2↑ + 2 Н 2 О Ag. NO 3 + I 2 + 2 C 5 H 5 N = Ag. I↓ + [I(C 5 H 5 N)2]+NO 3 -
Химические свойства галогенов Жидкий бром реагирует со многими простыми веществами энергичнее газообразного хлора. В водной среде бром окисляет серу до серной кислоты: 3 Br 2 + S + 4 Н 2 О = 6 HBr + H 2 SO 4 Манганат калия окисляет до перманганата: 2 K 2 Mn. O 4 + Br 2 = 2 KMn. O 4 + 2 KBr Окислительные свойства йода выражены слабее, чем у других галогенов. Йод не способен окислить даже серу. В тоже время для йода характерны восстановительные свойства. Под действием сильных окислителей йод окисляется до йодноватой кислоты: 3 I 2 (тв. ) + 10 НNО 3 (100%) = 6 НIО 3 + 10 NО 2↑ + 2 Н 2 О Ag. NO 3 + I 2 + 2 C 5 H 5 N = Ag. I↓ + [I(C 5 H 5 N)2]+NO 3 -


