Хлор.pptx
- Количество слайдов: 35

Галогены (солеобразующие)

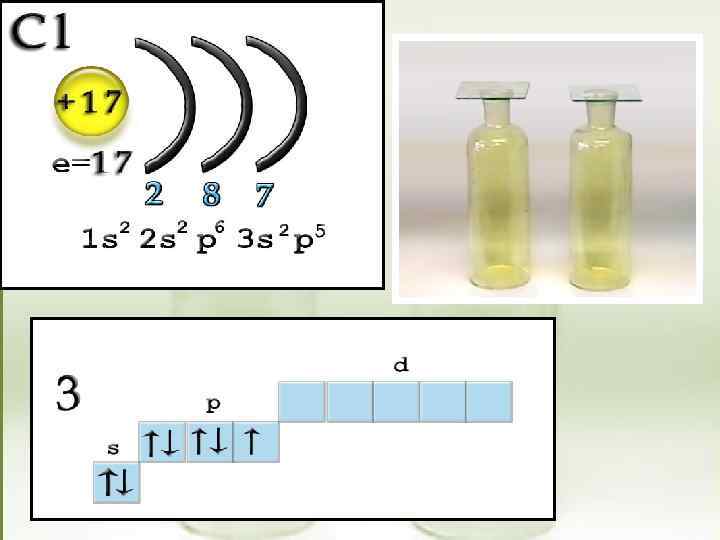
Электронные формулы F 1 S 22 P 5 CI 1 S 22 P 63 S 23 P 5 S Br … 4 S 24 P 5 I 2 … 5 S 25 P 5 Вывод: галогены - р - элементы На внешнем энергетическом уровне 7 электронов, один из них неспаренный.
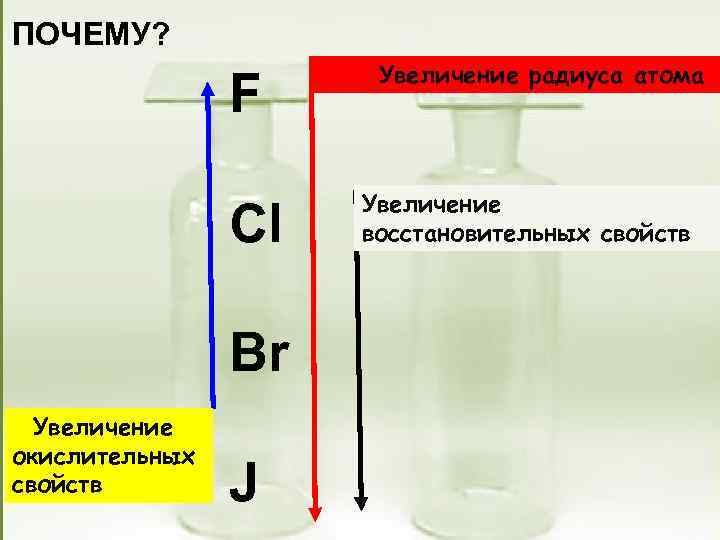
ПОЧЕМУ? F Cl Br Увеличение окислительных свойств J Увеличение радиуса атома Увеличение восстановительных свойств

Br 2 CI 2 Простые вещества F 2 I 2

Химическая связь КН Кристаллическая решетка молекулярная
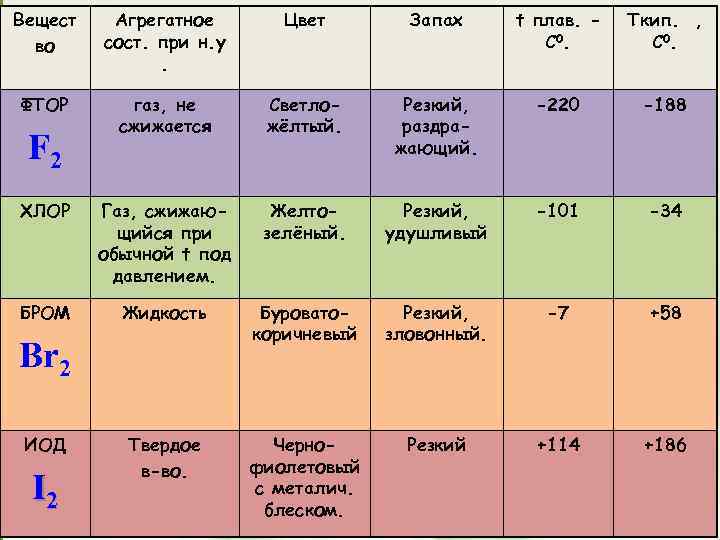
Вещест во Агрегатное сост. при н. у. Цвет Запах t плав. C 0. Tкип. , C 0. ФТОР газ, не сжижается Cветложёлтый. Резкий, раздражающий. -220 -188 ХЛОР Газ, сжижающийся при обычной t под давлением. Желтозелёный. Резкий, удушливый -101 -34 БРОМ Жидкость Буроватокоричневый Резкий, зловонный. -7 +58 Твердое в-во. Чернофиолетовый с металич. блеском. Резкий +114 +186 F 2 Br 2 ИОД I 2


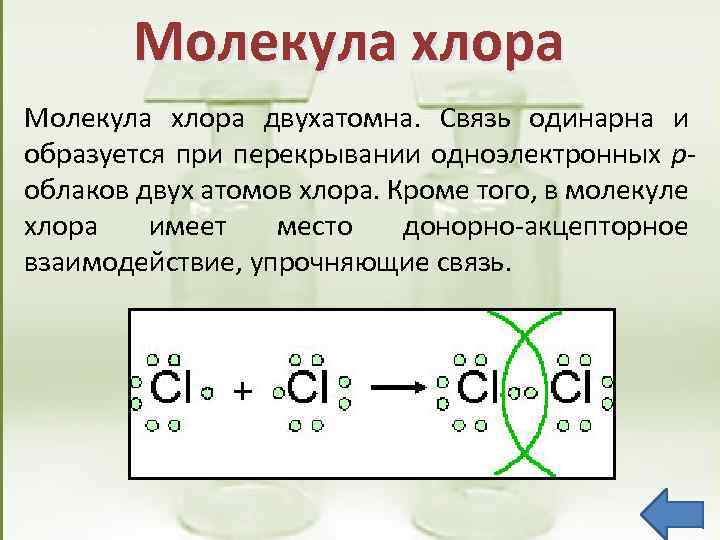
Молекула хлора двухатомна. Связь одинарна и образуется при перекрывании одноэлектронных роблаков двух атомов хлора. Кроме того, в молекуле хлора имеет место донорно-акцепторное взаимодействие, упрочняющие связь.

Физические свойства

Минералы Карналлит Каменная соль = поваренная соль = галит Сильвин

Получение 1. Электролиз хлоридов щелочных металлов (Na. Cl, KCl). 2. Окисление HCl кислородом воздуха 4 HCl + O 2 = 2 Cl 2 + 2 H 2 O 3. В лаборатории 2 KMn. O 4+16 HCl (конц. ) = 2 KCl+2 Mn. Cl 2+8 H 2 O+5 Cl 2 Mn. O 2 + 4 HCl = Mn. Cl 2 + 2 H 2 O 6 HCl + KCl. O 3 = 3 Cl 2 + KCl + 3 H 2 O

Получение 2 KMn. O 4+16 HCl (конц. )= 2 KCl + 2 Mn. Cl 2 + 8 H 2 O + 5 Cl 2

Химические свойства Хлор – активный окислитель. Энергично реагирует с металлами и большинством неметаллов (за исключением O 2, N 2 и благородных газов). Вступает также в реакции диспропорционирования, для протекания которых наиболее благоприятна щелочная среда, способствующая образованию простых и сложных анионов.

С Металлами Хлор - один из самых активных неметаллов. При взаимодействии с металлами с переменной валентностью (Fe, Cr) в отличие от соляной кислоты заставляет их проявлять большую степень окисления: 2 K + Cl 2 = 2 КCl 2 Al + 3 Cl 2 = 2 Al. Cl 3 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 Cu + Cl 2 = Cu. Cl 2

Cu+Cl 2=Cu. Cl 2 2 Fe+3 Cl 2 = 2 Fe. Cl 3

С Неметаллами H 2 + Cl 2 = 2 HCl(на свету) 2 Cl 2 + C = CCl 4 3 Cl 2 + 2 P (крист. ) = 2 PCl 3 5 Cl 2 + 2 P = 2 PCl 5

5 Cl 2 + 2 Sb = 2 Sb. Cl 5 Образует соединения с другими галогенами: Cl 2 + F 2 = 2 Cl. F Cl 2 + 3 F 2 = 2 Cl. F 3, t = 200– 400 °C Cl 2 + 5 F 2 = 2 Cl. F 5

С Водой Хлор растворяется вводе (в 1 объеме воды растворяется 2 объема хлора) с образованием "хлорной воды": Cl 2 + H 2 O = HCl + HCl. O Со щелочами Cl 2 + 2 KOH(хол) = KCl + KCl. O(гипохлорит) + H 2 O Cl 2 + 6 KOH(гор) = 5 KCl + KCl. O 3(хлорат) + 3 H 2 O

С Бескислородными Кислотами Cl 2 + HBr = 2 HCl + Br 2 Cl 2 + HI = 2 HCl + I 2 С Солями Cl 2 + 2 Na. I = 2 Na. Cl + I 2 Cl 2 + Fe. Cl 2 = 2 Fe. Cl 3

Хлор в органике Хлор является активным реагентом в органическом синтезе. Его атомы входят в состав молекул соединений, относящихся к различным классам органических веществ. 1. Cn. H 2 n+2 + Cl 2 (на свету) = Cn. H 2 n+1 Cl + HCl [р. Семенова] 2. Cn. H 2 n + Cl 2 = Cn. H 2 n. Cl 2 3. Cn. H 2 n-2 + Cl 2 – в несколько стадий 4. C 6 H 6 + Cl 2 (Al. Cl 3) = C 6 H 5 Cl + HCl C 6 H 6 + Cl 2 (на свету) = гексахлоран Гомологи бензола + Cl 2 (на свету) = замещение по радикальному механизму (Cl к альфа-H) 5. R-CH 2 -COOH + Cl 2 (PCl 5) = R-CHCl-COOH + HCl

• Для обеззараживания воды — «хлорирования» . • В химическом производстве соляной кислоты, хлорной извести, бертолетовой соли, хлоридов металлов, ядов, лекарств, удобрений.

• Производство хлорорганических инсектицидов — веществ, убивающих вредных для посевов насекомых, но безопасных для растений. На получение средств защиты растений расходуется значительная часть производимого хлора. • Использовался как оружие массового поражения и в производстве других отравляющих веществ массового поражения: иприт, фосген.
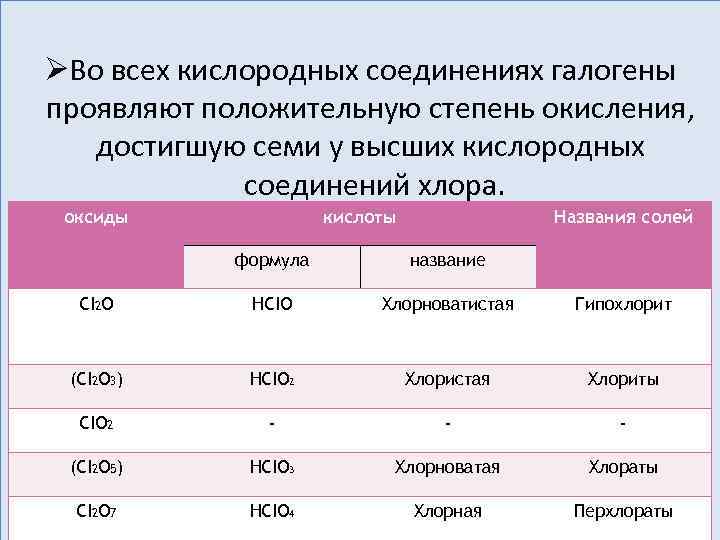
ØВо всех кислородных соединениях галогены проявляют положительную степень окисления, достигшую семи у высших кислородных соединений хлора. оксиды кислоты Названия солей формула название CI 2 O HCIO Хлорноватистая Гипохлорит (CI 2 O 3) HCIO 2 Хлористая Хлориты CIO 2 - - - (CI 2 O 5) HCIO 3 Хлорноватая Хлораты CI 2 O 7 HCIO 4 Хлорная Перхлораты

Хлорноватистая кислота Ø Получение: CI 2 + H 2 O ↔ HCIO + HCI. Ø Свойства : - очень неустойчива : 2 HCIO = 2 HCI + O 2 - очень сильный окислитель; её образованием при взаимодействии хлора с водой объясняются белящие свойства хлора; - образует соли – гипохлориты; - взаимодействует с щелочью HCI + HCIO + 2 KOH = KCI + KCIO + 2 H 2 O.

Гипохлориты – соли хлорноватистой кислоты - Смесь солей хлорноватистой и соляной кислот называется жавелевой водой и применяется для отбеливания: 2 KOH + Cl 2 = KCl. O + KCl + Н 2 O. - Гипохлорит кальция (Ca(CIO) 2)- белильная или хлористая известь применяется для отбелки растительного волокна (тканей, бумаги), для дезинфекции выгребных ям, отхожих мест, сточных канав и т. д. , для дегазации местности, заражённой отравляющими веществами.
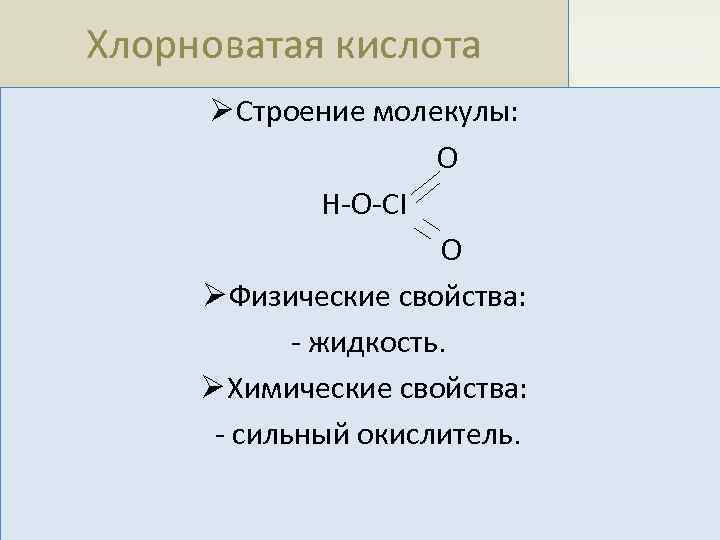
Хлорноватая кислота Ø Строение молекулы: O H-O-CI O Ø Физические свойства: - жидкость. Ø Химические свойства: - сильный окислитель.

Хлораты соли хлорноватой кислоты Ø Получение хлората калия: 3 KCIO = KCIO 3 + 2 KCI (при нагревании) 6 KOH +3 CI 2 = 5 KCI + KCIO 3 +3 H 2 O (горячий р-р) Ø Свойства хлората калия: при нагревании разлагаются 2 KCIO 3 = 2 KCI + 3 O 2. (бертолетова соль) Образует смеси, сильно взрывающиеся при ударе, с горючими веществами (серой, углём, фосфором). Ø Применение бертолетовой соли: - в артиллерийском деле, - пиротехнике, - производстве спичек.

Хлорная кислота Ø Строение молекулы Ø Физические свойства: O H-O- CI=O O -жидкость, - без цвета, - замерзает при температуре -112˚С. Ø Химические свойства: - очень устойчивая, - очень сильная кислота, α = 88%. - Взаимодействует с фосфорным ангидридом с образованием хлорного ангидрида 2 HCIO 4 + P 2 O 5 = 2 HPO 3 + CI 2 O 7

Ø Выводы С увеличением валентности хлора растёт устойчивость его кислородных кислот, а их окислительная способность уменьшается: HCIO окислительные свойства уменьшаются. Сила кислородных кислот хлора увеличивается с увеличением степени окисления последнего: HCIO сила кислот увеличивается. 2 2 3 3 4 4

физические свойства хлороводорода Соединения хлора - газ; - без цвета; - с резким запахом; - легко обращается в жидкость; - хорошо растворяется в воде (в 1 л воды 500 л хлороводорода); - температура плавления -112˚С; - температура кипения -84˚С. - К нагреванию менее устойчив по сравнению с фтороводородом, но более устойчив в сравнении с бромоводородом и йодоводородом.

Получение хлороводорода Ø В промышленности: действие концентрированной серной кислоты на соли галогеноводородных кислот 2 Na. CI + H SO = Na. Н SO + 2 HCI (при очень сильном нагревании). 2 4 4

Соляная кислота Ø Получение: - растворением хлороводорода в воде; - синтез путём сжигания водорода в струе хлора H 2 + CI 2 = 2 HCI + 183, 1 к. Дж. Ø Физические свойства: -жидкость; - бесцветная; - с резким запахом.

Ø Химические свойства: - легко вступает во взаимодействие с металлами, выделяя водород и образуя соли – хлориды Zn + 2 HCI = Zn. CI + H - взаимодействует с основными оксидами Cu. O + 2 HCI = Cu. CI +H O - взаимодействует с основаниями AI(OH) +3 HCI = AICI +3 H O -взаимодействует с солями Ag. NO + HCI = Ag. CI +HNO - взаимодействует с аммиаком с образованием солей аммония NH +HCI = NH CI - взаимодействует с хлорной известью Ca(CIO) + 4 HCI = Ca. CI +2 H O 2 2 2 3 2 3 3 2 3 4 2 2 2
Хлор.pptx