 Галогены – рождающие соли
Галогены – рождающие соли
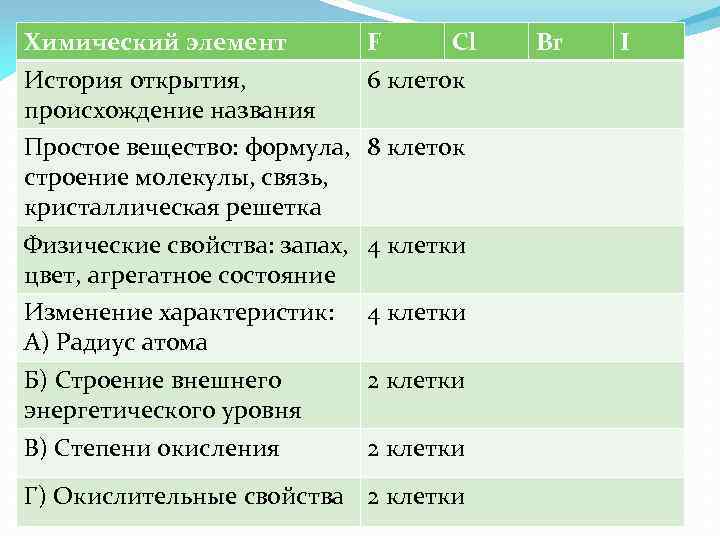 Химический элемент F Cl История открытия, происхождение названия 6 клеток Простое вещество: формула, 8 клеток строение молекулы, связь, кристаллическая решетка Физические свойства: запах, 4 клетки цвет, агрегатное состояние Изменение характеристик: А) Радиус атома 4 клетки Б) Строение внешнего энергетического уровня 2 клетки В) Степени окисления 2 клетки Г) Окислительные свойства 2 клетки Br I
Химический элемент F Cl История открытия, происхождение названия 6 клеток Простое вещество: формула, 8 клеток строение молекулы, связь, кристаллическая решетка Физические свойства: запах, 4 клетки цвет, агрегатное состояние Изменение характеристик: А) Радиус атома 4 клетки Б) Строение внешнего энергетического уровня 2 клетки В) Степени окисления 2 клетки Г) Окислительные свойства 2 клетки Br I
 История открытия: В 1886 году французскому химику Анри Муассану удалось получить фтор. От «Фторос» – «разрушение, гибель» В 1774 г. Карл Шееле открыл хлор. От “Хлорос” –как желто-зеленый. В 1826 г. Балар открыл бром. От “Бромос” - зловонный. В 1811 г. Куртуа открыл иод. От “Иодэс” – фиолетовый.
История открытия: В 1886 году французскому химику Анри Муассану удалось получить фтор. От «Фторос» – «разрушение, гибель» В 1774 г. Карл Шееле открыл хлор. От “Хлорос” –как желто-зеленый. В 1826 г. Балар открыл бром. От “Бромос” - зловонный. В 1811 г. Куртуа открыл иод. От “Иодэс” – фиолетовый.
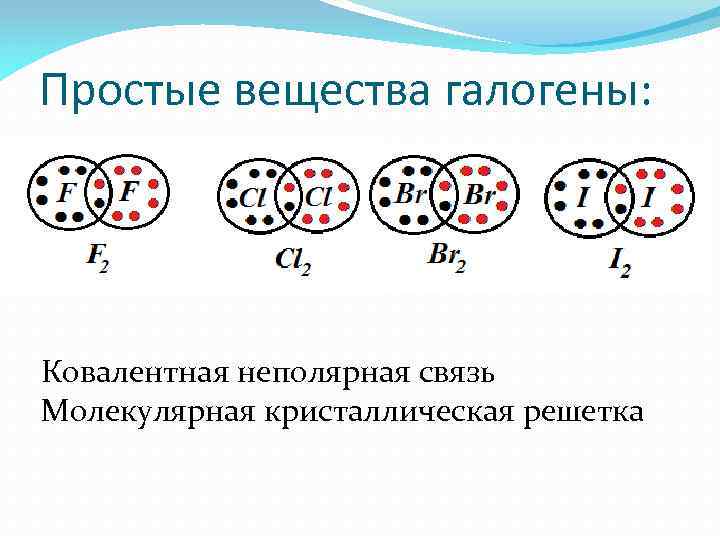 Простые вещества галогены: Ковалентная неполярная связь Молекулярная кристаллическая решетка
Простые вещества галогены: Ковалентная неполярная связь Молекулярная кристаллическая решетка
 Физические свойства галогенов: Фтор Хлор Бром Йод
Физические свойства галогенов: Фтор Хлор Бром Йод
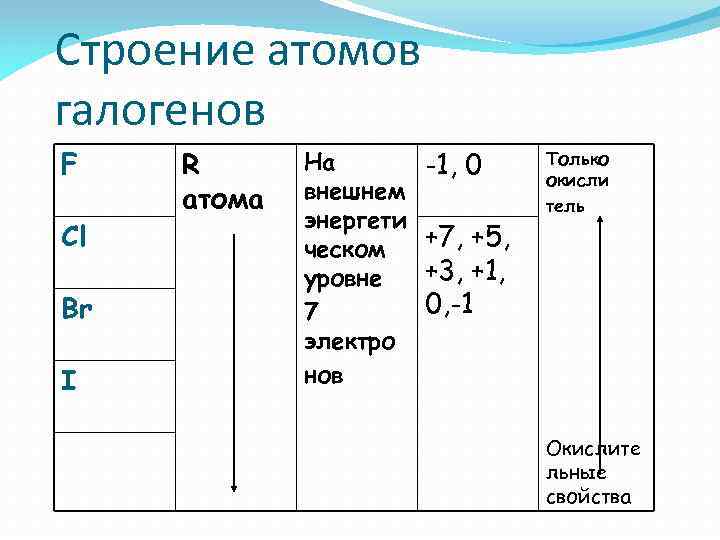 Строение атомов галогенов F Cl Br I R атома На внешнем энергети ческом уровне 7 электро нов -1, 0 +7, +5, +3, +1, 0, -1 Только окисли тель Окислите льные свойства
Строение атомов галогенов F Cl Br I R атома На внешнем энергети ческом уровне 7 электро нов -1, 0 +7, +5, +3, +1, 0, -1 Только окисли тель Окислите льные свойства
 Химические свойства галогенов: 1) Взаимодействие с металлами: Zn 0 + F 20 → Zn+2 F 2 -1 Zn 0 - 2 e- → Zn+2 2 1 в-ль 2 0 + 2 e- → 2 F-1 2 1 о-ль F 2 Al + I 2 → Sb + Cl 2 → 2) Взаимодействие с неметаллами: Н 20 + F 20 = 2 H+FН 20 - 2 е-→ 2 H+ 2 1 в-ль 2 0 + 2 е- → 2 F- 2 1 в-ль F 2
Химические свойства галогенов: 1) Взаимодействие с металлами: Zn 0 + F 20 → Zn+2 F 2 -1 Zn 0 - 2 e- → Zn+2 2 1 в-ль 2 0 + 2 e- → 2 F-1 2 1 о-ль F 2 Al + I 2 → Sb + Cl 2 → 2) Взаимодействие с неметаллами: Н 20 + F 20 = 2 H+FН 20 - 2 е-→ 2 H+ 2 1 в-ль 2 0 + 2 е- → 2 F- 2 1 в-ль F 2
 Si + 2 Cl 2 = Si. Cl 4 3) Галогены способны вытеснять друга из соединений (кроме фтора). Галоген, располагающийся выше вытесняет те, что ниже (по ПСХЭ). Cl 2 + 2 HI → 2 HCl + I 2 Cl 2 + 2 KBr → 2 KCl + Br 2 4) Cl 2 + Н 2 О HCl + HCl. O
Si + 2 Cl 2 = Si. Cl 4 3) Галогены способны вытеснять друга из соединений (кроме фтора). Галоген, располагающийся выше вытесняет те, что ниже (по ПСХЭ). Cl 2 + 2 HI → 2 HCl + I 2 Cl 2 + 2 KBr → 2 KCl + Br 2 4) Cl 2 + Н 2 О HCl + HCl. O
 Подумайте…. Что образуется в данной реакции, оксид фтора или фторид кислорода? F 2 + O 2
Подумайте…. Что образуется в данной реакции, оксид фтора или фторид кислорода? F 2 + O 2
 Домашнее задание: § 18, № 5, 6, с. 110
Домашнее задание: § 18, № 5, 6, с. 110