
Галогены (F, Cl, Br, I, At)

Общая характеристика элементов o o o Галоген – рождающий соль Галогены – неметаллы Структура внешнего электронного слоя атомов галогенов: ns 2 np 5(nd 0) • Степени окисления: -I, 0, I; за счёт d-АО III, IV, V, VII
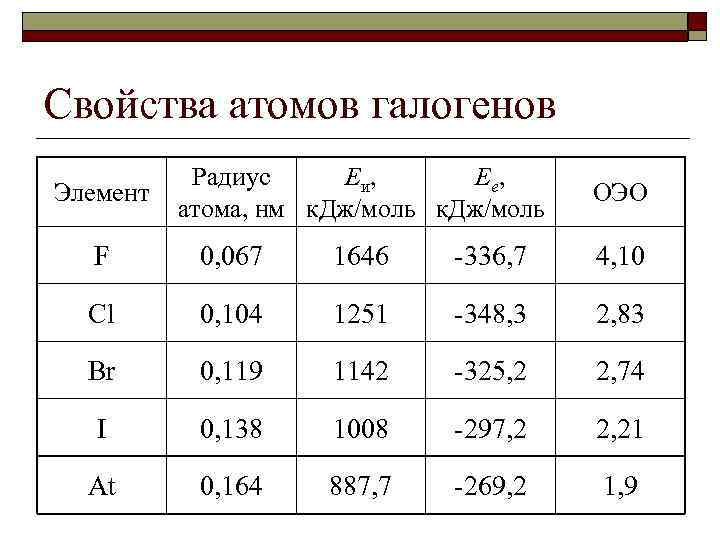
Свойства атомов галогенов Элемент Радиус E и, E e, атома, нм к. Дж/моль ОЭО F 0, 067 1646 -336, 7 4, 10 Cl 0, 104 1251 -348, 3 2, 83 Br 0, 119 1142 -325, 2 2, 74 I 0, 138 1008 -297, 2 2, 21 At 0, 164 887, 7 -269, 2 1, 9

Простые вещества o o Молекулы галогенов двухатомны из-за наличия у атомов одного неспаренного электрона В обычных условиях: F 2 – зеленоватый газ, Cl 2 – жёлто-зелёный газ, Br 2 – бурая дымящая жидкость, I 2 – чёрно-фиолетовые кристаллы

Получение простых веществ o Методы получения сводятся к превращению: 2 Г- → Г 2 F 2 1. 2. Pt. F 6 = Pt. F 4 + F 2 (при нагревании) KF· 2 HF = H 2 + F 2 + KF (при электролизе расплава)

Получение простых веществ Cl 2 2 Na. Cl + 2 H 2 O = 2 Na. OH + Cl 2 + H 2 (при электролизе раствора) 2. 2 La. Cl 3 = 2 La + 3 Cl 2 (при электролизе расплава) 3. 2 KCl = 2 K + Cl 2 (при электролизе расплава) 4. 16 HCl + 2 KMn. O 4 = = 5 Cl 2 + 2 KCl + 2 Mn. Cl 2 + 8 H 2 O (лабораторный метод) 5. 4 HCl + Mn. O 2 = Cl 2 + Mn. Cl 2 + 2 H 2 O (лабораторный метод) Другие окислители: Pb. O 2, KCl. O 3 1.

Получение простых веществ Br 2 1. 2 KBr + Mn. O 2 + 2 H 2 SO 4 = = Br 2 + K 2 SO 4 + Mn. SO 4 + 2 H 2 O 2 KBr + Cl 2 = 2 KCl + Br 2 I 2 1. 2 KI + Mn. O 2 + 2 H 2 SO 4 = = I 2 + K 2 SO 4 + Mn. SO 4 + 2 H 2 O 2 KI + Cl 2 = 2 KCl + I 2
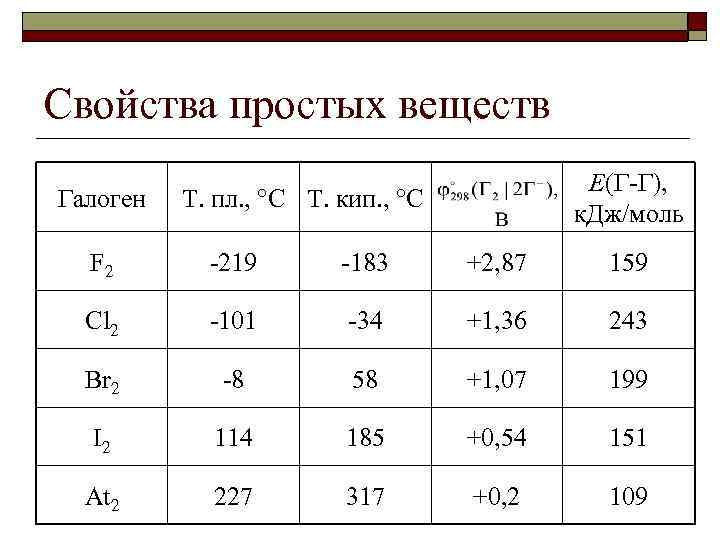
Свойства простых веществ Галоген E(Г-Г), к. Дж/моль Т. пл. , °C Т. кип. , °C F 2 -219 -183 +2, 87 159 Cl 2 -101 -34 +1, 36 243 Br 2 -8 58 +1, 07 199 I 2 114 185 +0, 54 151 At 2 227 317 +0, 2 109

Химические свойства простых веществ o o o Галогены проявляют свойства окислителей В ряду F 2, Cl 2, Br 2, I 2 окислительная способность уменьшается Любой Г 2 с меньшим атомным номером окисляет любой Г- с большим атомным номером: F 2 + 2 Cl- = 2 F- + Cl 2 + 2 Br- = 2 Cl- + Br 2 + 2 I- = 2 Br- + I 2

Химические свойства простых веществ o o Галогены реагируют почти со всеми простыми веществами, очень легко – с металлами, образуя галогениды 2 Na + Cl 2 = 2 Na. Cl F 2 пассивирует при 20 °C Al, Fe, Ni, Cu, Zn F 2 не реагирует с O 2, N 2, C(алмаз), He, Ne, Ar Cl 2 , Br 2, I 2 не реагируют с O 2, N 2, He-Rn

Химические свойства простых веществ H 2 легко реагирует с F 2 (со взрывом), Cl 2, труднее с Br 2, реакция с I 2 обратима H 2 + F 2 = 2 HF; r. H < 0 H 2 + Cl 2 = 2 HCl (при hν или при нагревании); r. H < 0 H 2 + Br 2 = 2 HBr (при нагревании); r. H < 0 H 2 + I 2 = 2 HI (при нагревании); r. H > 0 – равновесие сильно смещено влево o

Химические свойства простых веществ o o Реакции F 2 с другими неметаллами Si + 2 F 2 = Si. F 4 S + 3 F 2 = SF 6 Cl 2 + 3 F 2 = 2 Cl. F 3 Xe + F 2 = Xe. F 2 Реакции F 2 с оксидами Si. O 2 + F 2 = Si. F 4

Взаимодействие галогенов с водой 2 F 2 + 2 H 2 O = 4 HF + O 2 o При 20 °C в 1 л воды растворяется 2, 5 л Cl 2 (хлорная вода): Cl 2 + H 2 O = HCl + HCl. O (равновесие сильно смещено влево) o При 20 °C в 100 г воды растворяется 3, 5 г Br 2 (бромная вода): Br 2 + H 2 O = HBr + HBr. O (равновесие смещено влево ещё сильнее) o При 20 °C в 100 г воды растворяется 0, 02 г I 2 (иодная вода): I 2 + H 2 O = HI + HIO (равновесие смещено влево почти полностью) o

Растворимость в органических растворителях Br 2 и I 2 хорошо растворяются в органических растворителях: CS 2, C 2 H 5 OH, (C 2 H 5)2 O, CHCl 3, CCl 4, C 6 H 6 Br 2 окрашивает раствор в CCl 4 в жёлтый или оранжевый цвет I 2 окрашивает раствор в CCl 4 в розовый или малиновый цвет o

Химические свойства простых веществ o o o Галогены как окислители Fe. Cl 2 + Cl 2 = 2 Fe. Cl 3 Na 2 SO 3 + Br 2 + H 2 O = Na 2 SO 4 + 2 HBr H 2 S + I 2 = S + 2 HI I 2 с крахмалом образует комплекс синего цвета I 2 легко растворяется в водном растворе KI: I 2 + KI = KI 3 - бурый
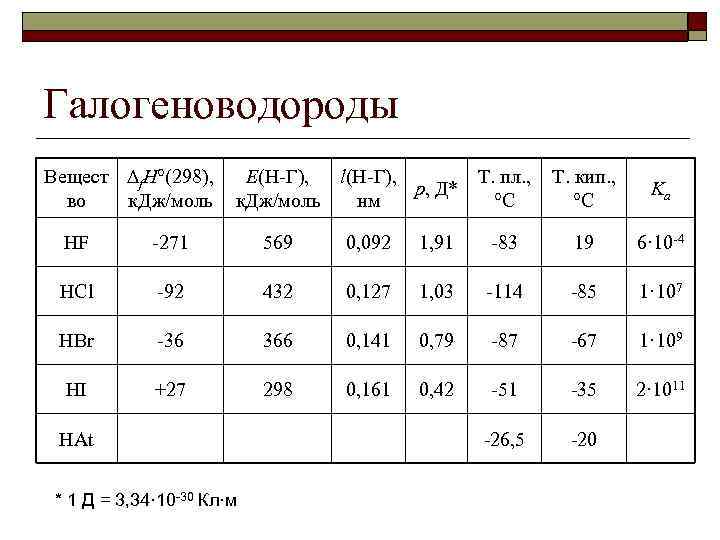
Галогеноводороды Вещест f. H°(298), во к. Дж/моль E(H-Г), к. Дж/моль l(H-Г), Т. пл. , p, Д* нм °C Т. кип. , °C Ka HF -271 569 0, 092 1, 91 -83 19 6· 10 -4 HCl -92 432 0, 127 1, 03 -114 -85 1· 107 HBr -36 366 0, 141 0, 79 -87 -67 1· 109 HI +27 298 0, 161 0, 42 -51 -35 2· 1011 -26, 5 -20 HAt * 1 Д = 3, 34· 10 -30 Кл·м

Галогеноводороды – бесцветные газы с резким удушливым запахом, токсичны HF имеет аномально высокие значения температур плавления и кипения из-за образования водородных связей – (HF)n

Получение галогеноводородов o Синтез из простых веществ 1) Цепной механизм реакции 2) Реакции идут до конца 1) 200 -250 °C 2) Избыток H 2 3) Катализатор (Pt)

Получение галогеноводородов o Вытеснение из галогенидов металлов сильными неокисляющими кислотами n HF и HCl Ca. F 2 + H 2 SO 4 = Ca. SO 4↓ + 2 HF↑ Na. Cl + H 2 SO 4 = Na. HSO 4 + HCl↑ При нагревании Na. Cl + Na. HSO 4 = Na 2 SO 4 + HCl↑ n HBr и HI KBr + H 3 PO 4 = KH 2 PO 4 + HBr↑ KI + H 3 PO 4 = KH 2 PO 4 + HI↑

Получение галогеноводородов o o При хлорировании углеводородов (при нагревании или УФ-облучении) RH + Cl 2 = RCl + HCl↑ При взаимодействии галогенов с восстановителями I 2 + H 2 S = S + 2 HI↑

Получение галогеноводородов o Гидролиз галогенидов неметаллов при недостатке H 2 O Si. Cl 4 + 2 H 2 O = Si. O 2 + 4 HCl↑ SBr 4 + 2 H 2 O = SO 2↑ + 4 HBr↑ PBr 3 + 3 H 2 O = H 3 PO 3 + 3 HBr↑ PI 3 + 3 H 2 O = H 3 PO 3 + 3 HI↑ или 2 P + 3 I 2 + 6 H 2 O = 2 H 3 PO 3 + 6 HI↑
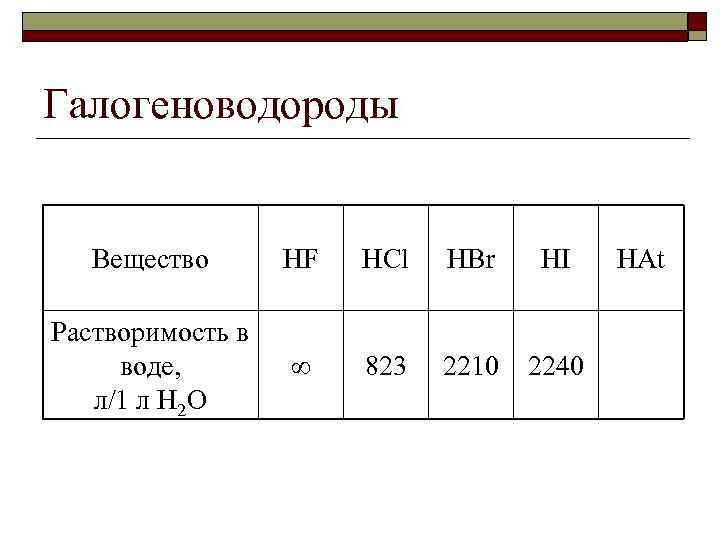
Галогеноводороды Вещество HF HCl HBr HI Растворимость в воде, л/1 л H 2 O ∞ 823 2210 2240 HAt

Свойства галогеноводородов o В водных растворах: HF – слабая кислота HCl, HBr, HI, HAt – сильные кислоты q Водные растворы: HF – фтороводородная кислота, плавиковая кислота HCl – хлороводородная кислота, соляная кислота HBr – бромоводородная кислота HI – иодоводородная кислота

Фтороводородная кислота o HF сильно ассоциирована даже в растворах (HF)n K = 5, 1 o o При c(HF) = 1 моль/л [HF 2 -] в 10 раз больше [F-] H 2 F 2 + KOH = KHF 2 + H 2 O KHF 2 + KOH = 2 KF + H 2 O Реакции с Si. O 2 и силикатами Si. O 2 + 4 HF = Si. F 4↑ + 2 H 2 O Si. F 4 + 2 HF = H 2[Si. F 6]

ОВР галогеноводородов o o Галогеноводороды-окислители Fe + 2 HCl = Fe. Cl 2 + H 2↑ 2 Al + 6 HBr = 2 Al. Br 3 + 3 H 2↑ Галогеноводороды-восстановители 2 HBr + Cl 2 = 2 HCl + Br 2 2 HI + S = H 2 S↑ + I 2 4 HI + O 2 = 2 H 2 O + 2 I 2 4 HBr + O 2 = 2 H 2 O + 2 Br 2 4 HCl + O 2 = 2 H 2 O + 2 Cl 2 – обратимая реакция

Галогениды металлов MHlgn o o o Получение 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 Mg. O + 2 HF = Mg. F 2 + H 2 O Ca. CO 3 + 2 HBr = Ca. Br 2 + CO 2 + H 2 O Хорошо растворяются в воде: фториды Na+, K+, Rb+, Cs+, NH 4+, Ag+, Sn 2+, Hg 2+, большинство хлоридов, бромидов и иодидов. Плохо растворяются в воде: большинство фторидов, Ag. Cl, Ag. Br, Ag. I, Pb. Cl 2, Pb. Br 2, Pb. I 2, Hg 2 Cl 2, Bi. I 3

ОВР галогенидов o o Ионы Hlg- (кроме иона F-), особенно ионы I -, окисляются ионами некоторых металлов 2 Cu. Cl 2 + 4 KI = 2 Cu. I↓ + I 2 + 4 KCl 2 Fe. Cl 3 + 2 KI = 2 Fe. Cl 2 + I 2 + 2 KCl По этой причине галогениды некоторых металлов в высоких состояниях окисления не существуют

Фториды o Фториды, подобно оксидам и гидроксидам, делятся на: n n n кислотные – фториды неметаллов и металлов в высоких состояниях окисления, основные – фториды щелочных, щелочноземельных металлов и металлов в низких состояниях окисления амфотерные – Al. F 3

Фториды o o Реакции основных и кислотных фторидов 2 Na. F + Si. F 4 = Na 2[Si. F 6] KF + Sb. F 5 = K[Sb. F 6] Реакции амфотерных фторидов Al. F 3 + 3 Na. F = Na 3[Al. F 6] 2 Al. F 3 + 3 Si. F 4 = Al 2[Si. F 6]3

Оксиды галогенов o o o Галогены непосредственно с кислородом не реагируют, так как эти реакции эндотермичны ( r. H > 0), r. S < 0 и, следовательно, r. G > 0 Оксиды галогенов – кислотные оксиды Оксиды хлора устойчивее оксидов брома

Фторид кислорода OF 2 o o OIIF 2 -I – светло-жёлтый газ, не растворяющийся в воде и не реагирующий с ней 2 Na. OH(разб. ) + 2 F 2 = 2 Na. F + OF 2 + H 2 O OF 2 – сильный окислитель 2 H 2 + OF 2 = 2 HF + H 2 O 4 NH 3 + 3 OF 2 = 2 N 2 + 6 HF + 3 H 2 O

Оксид дихлора, Cl 2 O Получение 2 Cl 2 + 2 Hg. O = Cl. Hg. OHg. Cl + Cl 2 O↑ при 0 °C 2 HCl. O = Cl 2 O↑ + H 2 O - в H 2 SO 4 o Разложение 4 Cl 2 O = 2 Cl. O 2 + 3 Cl 2 o Реакция с водой Cl 2 O + H 2 O = 2 HCl. O o

Диоксид хлора, Cl. O 2 o o o Получение а) KCl. O 3 + H 2 SO 4 = HCl. O 3 + KHSO 4 3 HCl. O 3 = 2 Cl. O 2↑ + HCl. O 4 + H 2 O б) 2 KCl. O 3 + H 2 C 2 O 4 + H 2 SO 4 = = K 2 SO 4 + 2 CO 2↑ + 2 Cl. O 2↑ + 2 H 2 O в) 2 KCl. O 3 + SO 2 + H 2 SO 4 = 2 Cl. O 2↑ + KHSO 4 Разложение 2 Cl. O 2 = Cl 2 + 2 O 2 – со взрывом Реакции с водой и щёлочью 6 Cl. O 2 + 3 H 2 O = 5 HCl. O 3 + HCl 2 Cl. O 2 + 2 KOH = KCl. O 2 + KCl. O 3 + H 2 O

Гексаоксид дихлора, Cl 2 O 6 o o o Получение 2 Cl. O 2 + 2 O 3 = 2 O 2 + Cl 2 O 6 Разложение Cl 2 O 6 = 2 Cl. O 2 + O 2 Cl 2 O 6 = 2 Cl. O 3 – при нагревании Реакция со щёлочью Cl 2 O 6 + 2 KOH = KCl. O 3 + KCl. O 4 + H 2 O

Гептаоксид дихлора, Cl 2 O 7 Получение 2 HCl. O 4 + P 2 O 5 = Cl 2 O 7 + 2 HPO 3 o Разложение 2 Cl 2 O 7 = 2 Cl 2 + 7 O 2 – выше 120 °C со взрывом o Реакция с водой Cl 2 O 7 + H 2 O = 2 HCl. O 4 o

Пентаоксид дииода, I 2 O 5 o o Получение 2 HIO 3 = I 2 O 5 + H 2 O – при 240 °C Разложение 2 I 2 O 5 = 2 I 2 + 5 O 2 – при 300 °C Реакция с водой I 2 O 5 + H 2 O = 2 HIO 3 Реакция для количественного определения CO I 2 O 5 + 5 CO = I 2 + 5 CO 2
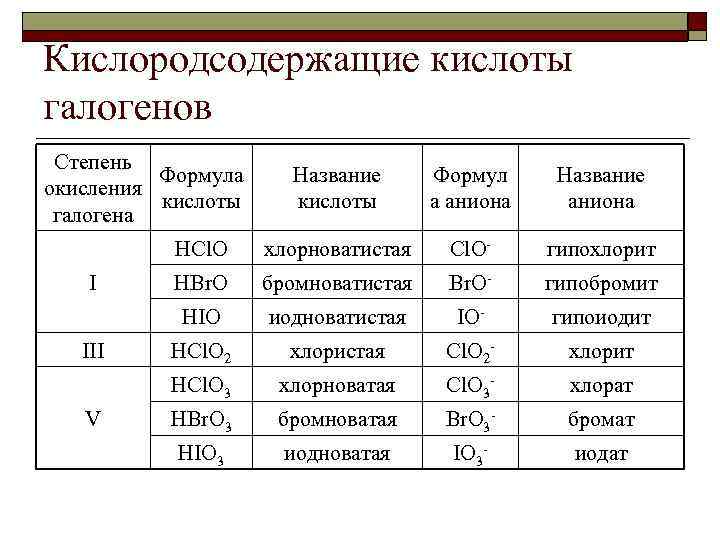
Кислородсодержащие кислоты галогенов Степень Формула окисления кислоты галогена хлорноватистая Cl. O- гипохлорит HBr. O бромноватистая Br. O- гипобромит иодноватистая IO- гипоиодит HCl. O 2 хлористая Cl. O 2 - хлорит HCl. O 3 V Название аниона HIO III Формул а аниона HCl. O I Название кислоты хлорноватая Cl. O 3 - хлорат HBr. O 3 бромноватая Br. O 3 - бромат HIO 3 иодноватая IO 3 - иодат
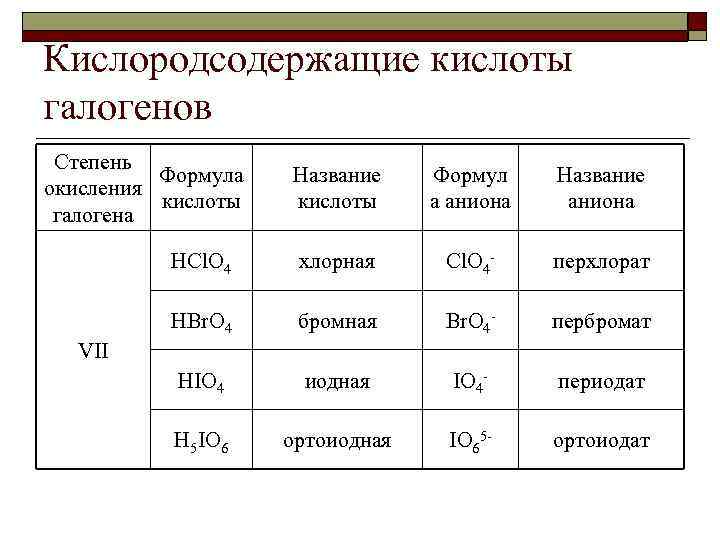
Кислородсодержащие кислоты галогенов Степень Формула окисления кислоты галогена Название кислоты Формул а аниона Название аниона HCl. O 4 хлорная Cl. O 4 - перхлорат HBr. O 4 бромная Br. O 4 - пербромат HIO 4 иодная IO 4 - периодат H 5 IO 6 ортоиодная IO 65 - ортоиодат VII

Кислородсодержащие кислоты галогенов o o Большинство кислот неустойчивы в свободном состоянии и разлагаются Известны следующие кислоты в свободном состоянии: HCl. O 4, HIO 3, H 5 IO 6 Соли кислот стабильнее самих кислот Кислоты и их соли являются сильными окислителями, особенно в кислой среде
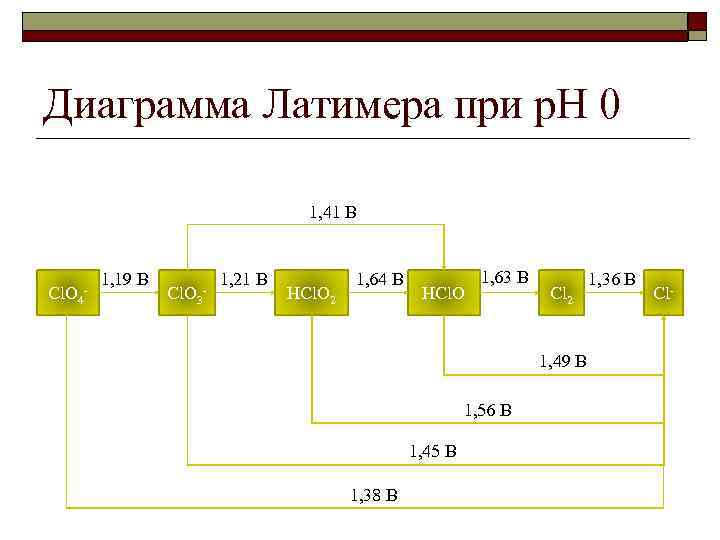
Диаграмма Латимера при p. H 0 1, 41 В Cl. O 4 - 1, 19 В Cl. O 3 - 1, 21 В HCl. O 2 1, 64 В HCl. O 1, 63 В Cl 2 1, 49 В 1, 56 В 1, 45 В 1, 38 В 1, 36 В Cl-
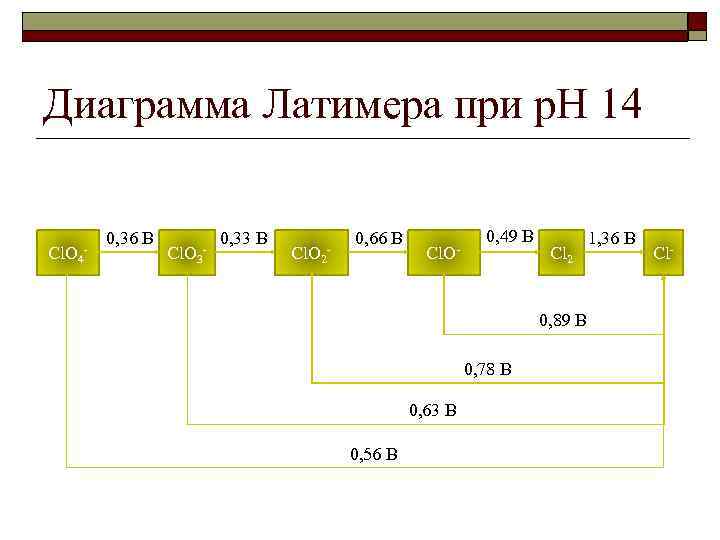
Диаграмма Латимера при p. H 14 Cl. O 4 - 0, 36 В Cl. O 3 - 0, 33 В Cl. O 2 - 0, 66 В Cl. O- 0, 49 В Cl 2 0, 89 В 0, 78 В 0, 63 В 0, 56 В 1, 36 В Cl-

Хлорноватистая, бромноватистая, иодноватистая кислоты, HHlg. O o Получение (хлрная, бромная, иодная вода) Hlg 2 + H 2 O = HHlg + HHlg. O Hlg Cl Br I K 4, 2· 10 -4 7, 2· 10 -9 2· 10 -13

Хлорноватистая, бромноватистая, иодноватистая кислоты, HHlg. O o В щелочной среде равновесие смещено вправо n При 20 °C Cl 2 + 2 KOH = KCl. O + KCl + H 2 O – жавелевая вода Cl 2 + Ca(OH)2 = H 2 O + Ca. Cl(OCl) – хлорная (белильная) известь n При нагревании 3 Cl 2 + 6 KOH = KCl. O 3 + 5 KCl + 3 H 2 O n При 20 °C 3 Br 2 + 6 KOH = KBr. O 3 + 5 KBr + 3 H 2 O 3 I 2 + 6 KOH = KIO 3 + 5 KI + 3 H 2 O

Хлорноватистая, бромноватистая, иодноватистая кислоты, HHlg. O o Разложение n В темноте 3 HCl. O = 2 HCl + HCl. O 3 + 5 HCl = 3 Cl 2 + 3 H 2 O n o На свету 2 HCl. O = 2 HCl + O 2 Эти процессы наиболее медленны у HCl. O

Гипохлориты Сильные окислители в кислых средах Na. OCl + 2 Na. I + H 2 SO 4 = = Na. Cl + I 2 + Na 2 SO 4 + H 2 O Ca. OCl 2 + HCl =Ca. Cl 2 + H 2 O Ca. OCl 2 + CO 2 + H 2 O = HCl. O + Ca. Cl(HCO 3) = Ca. CO 3 + Cl 2 + H 2 O o Разложение при нагревании (Co 2+) 2 Ca. OCl 2 = 2 Ca. Cl 2 + O 2 o

Хлористая кислота, HCl. O 2 Получение 2 Cl. O 2 + H 2 O 2 + 2 Na. OH = = 2 Na. Cl. O 2 + 2 H 2 O Na. Cl. O 2 + H 2 SO 4 = HCl. O 2 + Na. HSO 4 o Разложение 4 HCl. O 2 = HCl + HCl. O 3 + 2 Cl. O 2 + H 2 O o

Хлорноватая кислота, HCl. O 3 Получение 6 Ba(OH)2 + 6 Cl 2 = 5 Ba. Cl 2 + Ba(Cl. O 3)2 + 6 H 2 O Ba(Cl. O 3)2 + H 2 SO 4 = 2 HCl. O 3 + Ba. SO 4↓ o Разложение 3 HCl. O 3 = 2 Cl. O 2 + HCl. O 4 + H 2 O o

Хлораты o o o Сильные окислители в кислой среде KCl. O 3 – хлорат калия, бертолетова соль 2 KCl. O 3 + 3 S = 3 SO 2 + 2 KCl 5 KCl. O 3 + 6 P = 3 P 2 O 5 + 5 KCl KCl. O 3 + Al = Al 2 O 3 + KCl Разложение n При 400 °C 4 KCl. O 3 = 3 KCl. O 4 + KCl n При 200 -250 °C (Mn. O 2) 2 KCl. O 3 = 2 KCl + 3 O 2

Бромноватая кислота, HBr. O 3 Иодноватая кислота, HIO 3 o Получение HBr. O 3 n n o o См. HCl. O 3 Br 2 + 5 Cl 2 + 6 H 2 O = 2 HBr. O 3 + 10 HCl Разложение 4 HBr. O 3 = 2 Br 2 + 5 O 2 + 2 H 2 O Получение HIO 3 3 I 2 + 10 HNO 3 = 6 HIO 3 + 10 NO + 2 H 2 O

Хлорная кислота, HCl. O 4 o Получение n o Электролиз растворов KCl. O 3 или KCl. O 3 + H 2 O = KCl. O 4 + H 2 KCl + H 2 O = KCl. O 4 + 4 H 2 KCl. O 4 + H 2 SO 4 = HCl. O 4 + KHSO 4 Разложение при нагревании 4 HCl. O 4 = 4 Cl. O 2 + 3 O 2 + 2 H 2 O

Перхлораты o o Перхлораты в растворах не проявляют окислительных свойств Разложение при нагревании 4 NH 4 Cl. O 4 = 2 N 2 O + 2 Cl 2 + 8 H 2 O + 3 O 2
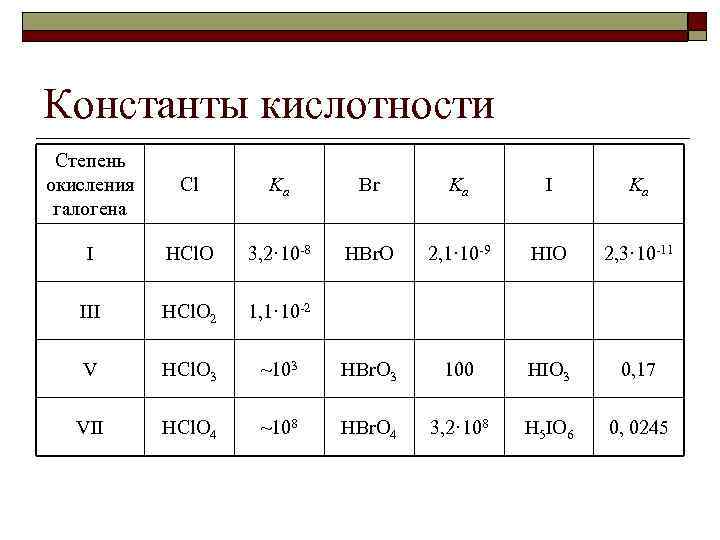
Константы кислотности Степень окисления галогена Cl Ka Br Ka I HCl. O 3, 2· 10 -8 HBr. O 2, 1· 10 -9 HIO 2, 3· 10 -11 III HCl. O 2 1, 1· 10 -2 V HCl. O 3 ~103 HBr. O 3 100 HIO 3 0, 17 VII HCl. O 4 ~108 HBr. O 4 3, 2· 108 H 5 IO 6 0, 0245
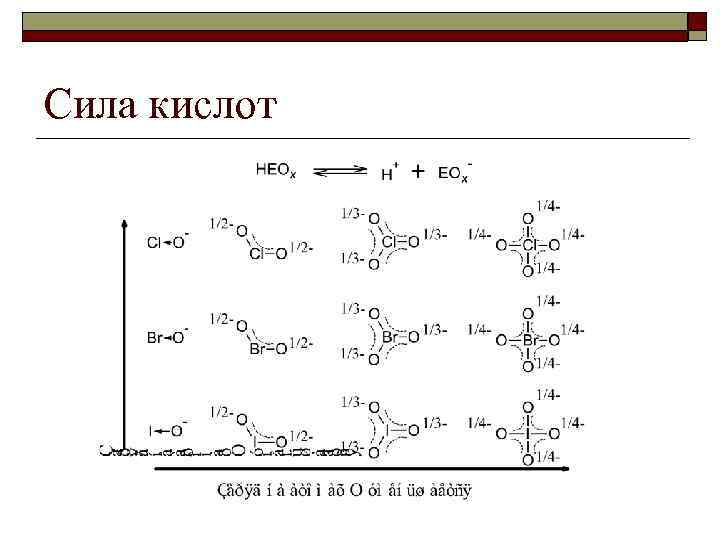
Сила кислот

Сила кислот o Чем меньше отрицательный заряд на атомах кислорода аниона кислоты, тем сильнее кислота