HAlogen(30).ppt
- Количество слайдов: 26
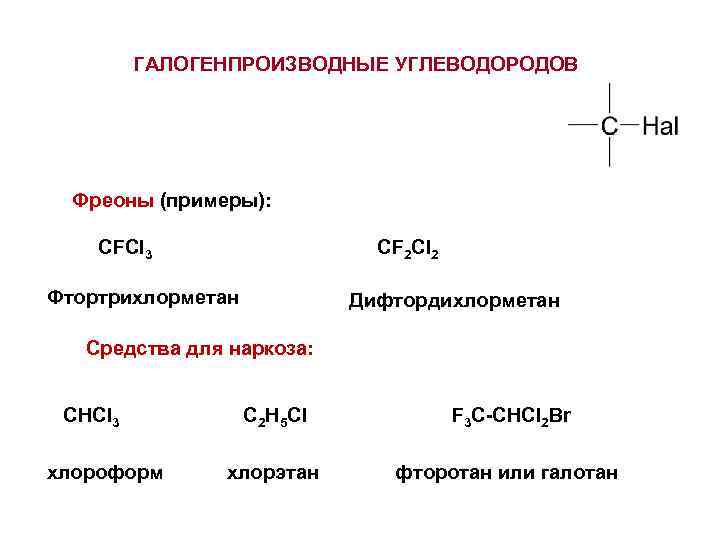 ГАЛОГЕНПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Фреоны (примеры): CFCl 3 CF 2 Cl 2 Фтортрихлорметан Дифтордихлорметан Средства для наркоза: CHCl 3 хлороформ C 2 H 5 Cl F 3 C-CHCl 2 Br хлорэтан фторотан или галотан
ГАЛОГЕНПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Фреоны (примеры): CFCl 3 CF 2 Cl 2 Фтортрихлорметан Дифтордихлорметан Средства для наркоза: CHCl 3 хлороформ C 2 H 5 Cl F 3 C-CHCl 2 Br хлорэтан фторотан или галотан
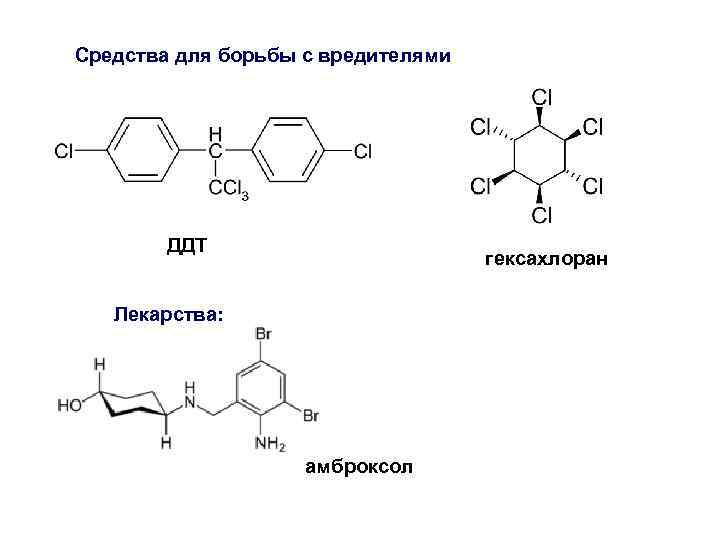 Средства для борьбы с вредителями ДДТ гексахлоран Лекарства: амброксол
Средства для борьбы с вредителями ДДТ гексахлоран Лекарства: амброксол
 Биомолекулы: тироксин (гормон щитовидной железы)
Биомолекулы: тироксин (гормон щитовидной железы)
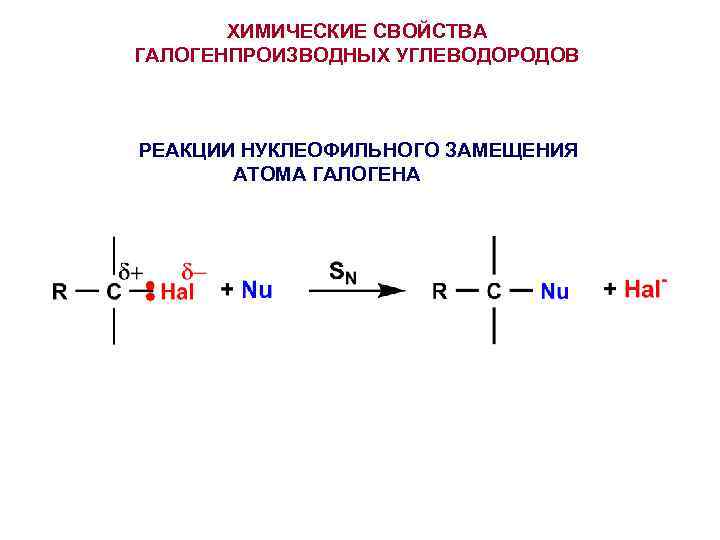 ХИМИЧЕСКИЕ СВОЙСТВА ГАЛОГЕНПРОИЗВОДНЫХ УГЛЕВОДОРОДОВ РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ АТОМА ГАЛОГЕНА
ХИМИЧЕСКИЕ СВОЙСТВА ГАЛОГЕНПРОИЗВОДНЫХ УГЛЕВОДОРОДОВ РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ АТОМА ГАЛОГЕНА
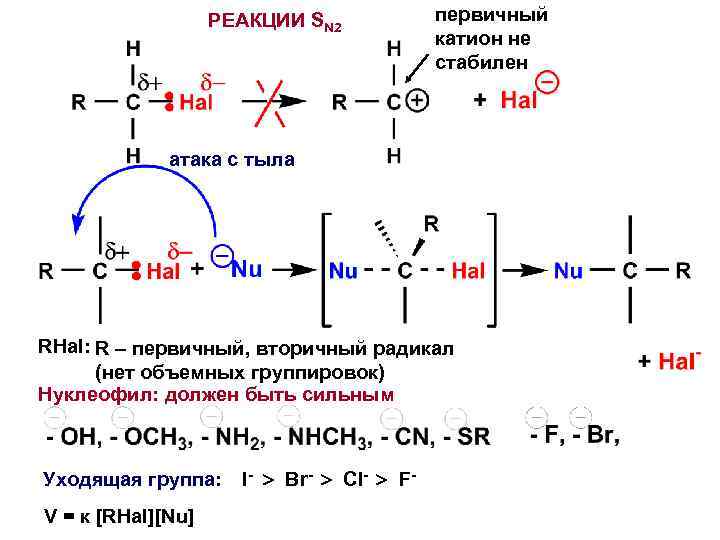 РЕАКЦИИ SN 2 первичный катион не стабилен атака с тыла RHal: R – первичный, вторичный радикал (нет объемных группировок) Нуклеофил: должен быть сильным Уходящая группа: V = к [RHal][Nu] I- Br- Cl- F-
РЕАКЦИИ SN 2 первичный катион не стабилен атака с тыла RHal: R – первичный, вторичный радикал (нет объемных группировок) Нуклеофил: должен быть сильным Уходящая группа: V = к [RHal][Nu] I- Br- Cl- F-
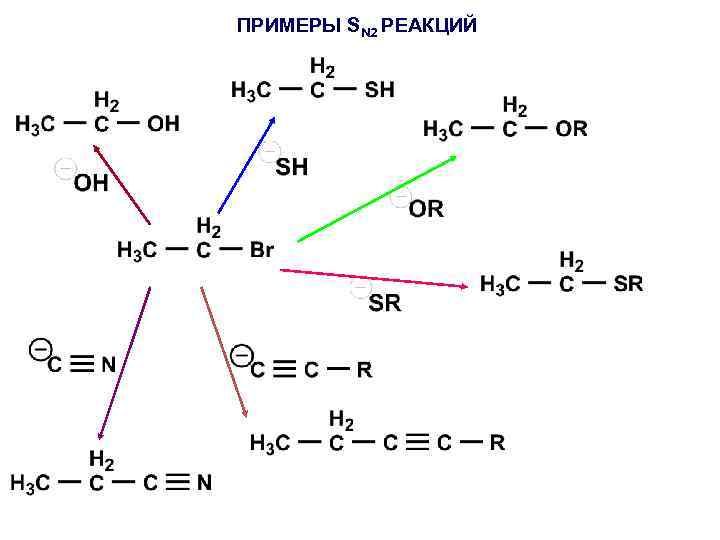 ПРИМЕРЫ SN 2 РЕАКЦИЙ
ПРИМЕРЫ SN 2 РЕАКЦИЙ
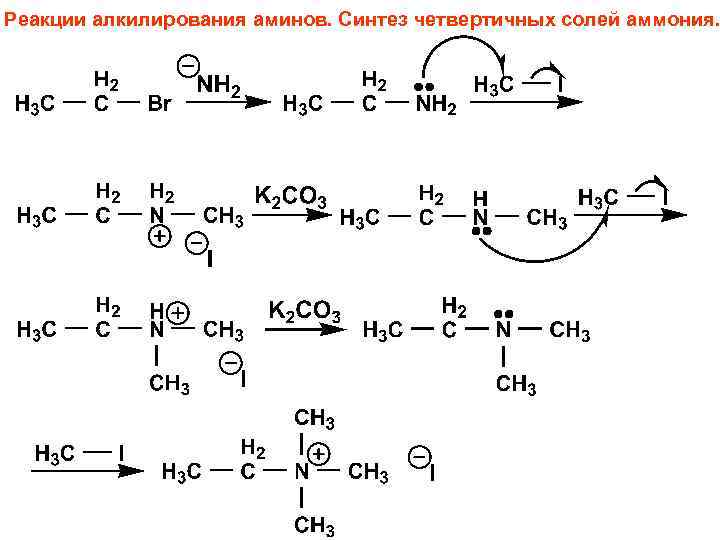 Реакции алкилирования аминов. Синтез четвертичных солей аммония.
Реакции алкилирования аминов. Синтез четвертичных солей аммония.
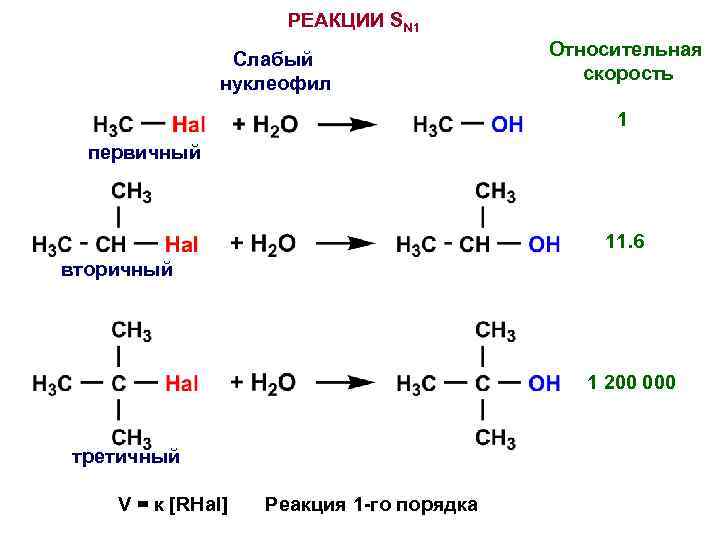 РЕАКЦИИ SN 1 Слабый нуклеофил Относительная скорость 1 первичный 11. 6 вторичный 1 200 000 третичный V = к [RHal] Реакция 1 -го порядка
РЕАКЦИИ SN 1 Слабый нуклеофил Относительная скорость 1 первичный 11. 6 вторичный 1 200 000 третичный V = к [RHal] Реакция 1 -го порядка
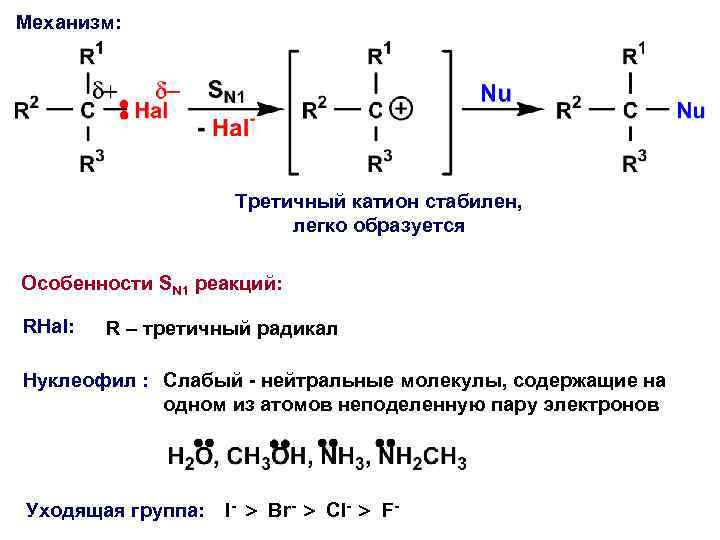 Механизм: Третичный катион стабилен, легко образуется Особенности SN 1 реакций: RHal: R – третичный радикал Нуклеофил : Слабый - нейтральные молекулы, содержащие на одном из атомов неподеленную пару электронов Уходящая группа: I- Br- Cl- F-
Механизм: Третичный катион стабилен, легко образуется Особенности SN 1 реакций: RHal: R – третичный радикал Нуклеофил : Слабый - нейтральные молекулы, содержащие на одном из атомов неподеленную пару электронов Уходящая группа: I- Br- Cl- F-
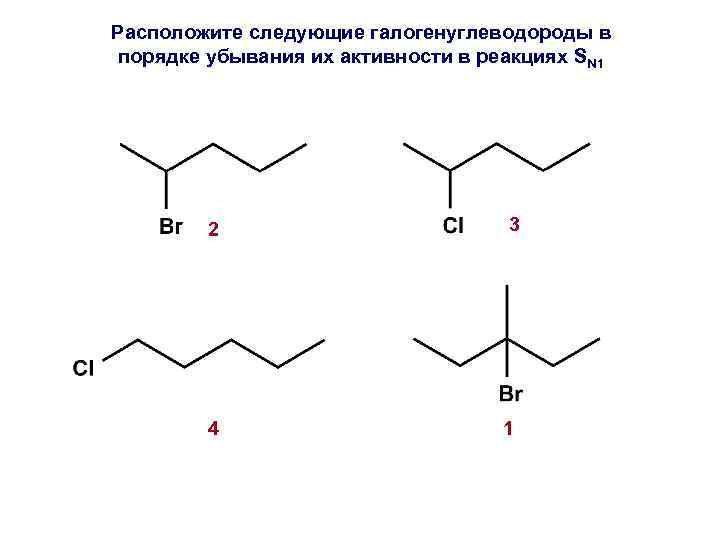 Расположите следующие галогенуглеводороды в порядке убывания их активности в реакциях SN 1 2 3 4 1
Расположите следующие галогенуглеводороды в порядке убывания их активности в реакциях SN 1 2 3 4 1
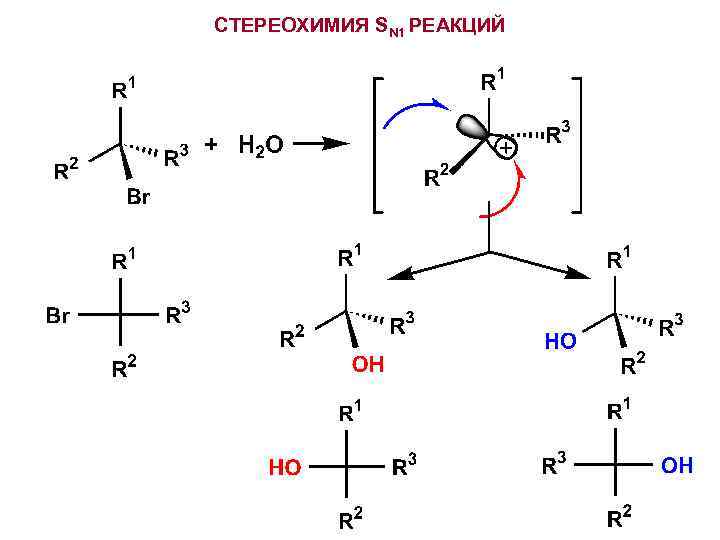 СТЕРЕОХИМИЯ SN 1 РЕАКЦИЙ
СТЕРЕОХИМИЯ SN 1 РЕАКЦИЙ
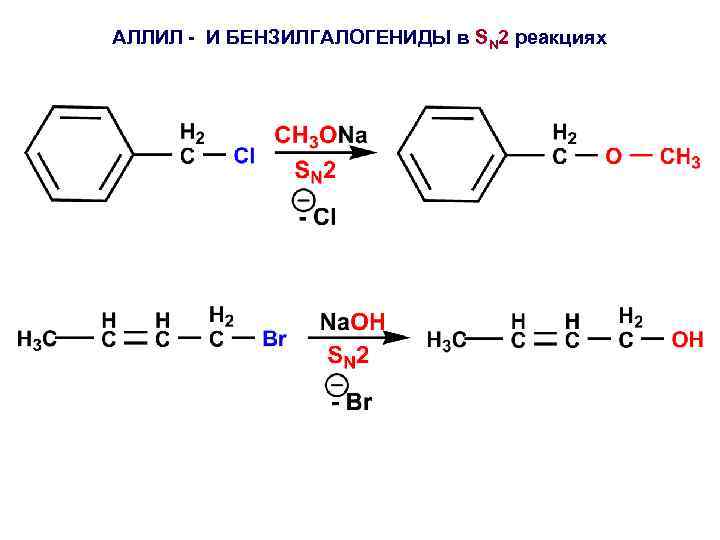 АЛЛИЛ - И БЕНЗИЛГАЛОГЕНИДЫ в SN 2 реакциях
АЛЛИЛ - И БЕНЗИЛГАЛОГЕНИДЫ в SN 2 реакциях
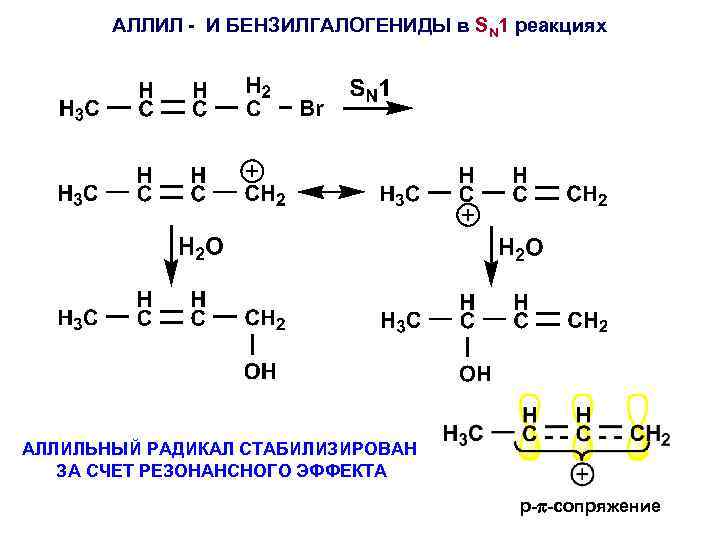 АЛЛИЛ - И БЕНЗИЛГАЛОГЕНИДЫ в SN 1 реакциях АЛЛИЛЬНЫЙ РАДИКАЛ СТАБИЛИЗИРОВАН ЗА СЧЕТ РЕЗОНАНСНОГО ЭФФЕКТА p- -сопряжение
АЛЛИЛ - И БЕНЗИЛГАЛОГЕНИДЫ в SN 1 реакциях АЛЛИЛЬНЫЙ РАДИКАЛ СТАБИЛИЗИРОВАН ЗА СЧЕТ РЕЗОНАНСНОГО ЭФФЕКТА p- -сопряжение
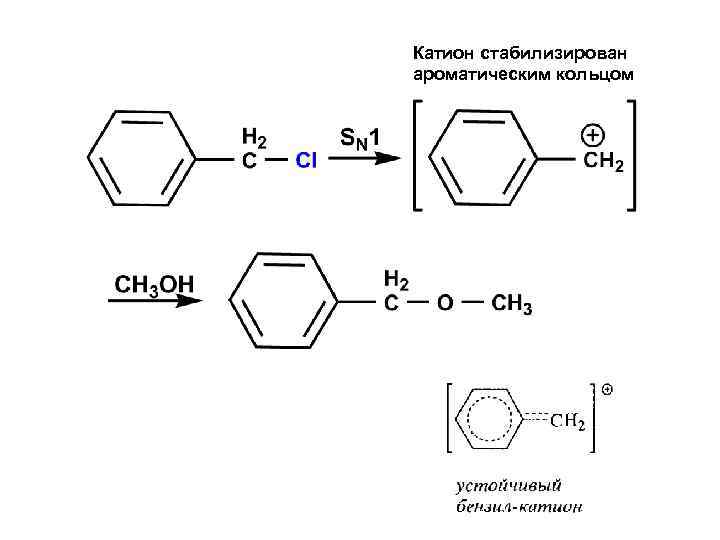 Катион стабилизирован ароматическим кольцом
Катион стабилизирован ароматическим кольцом
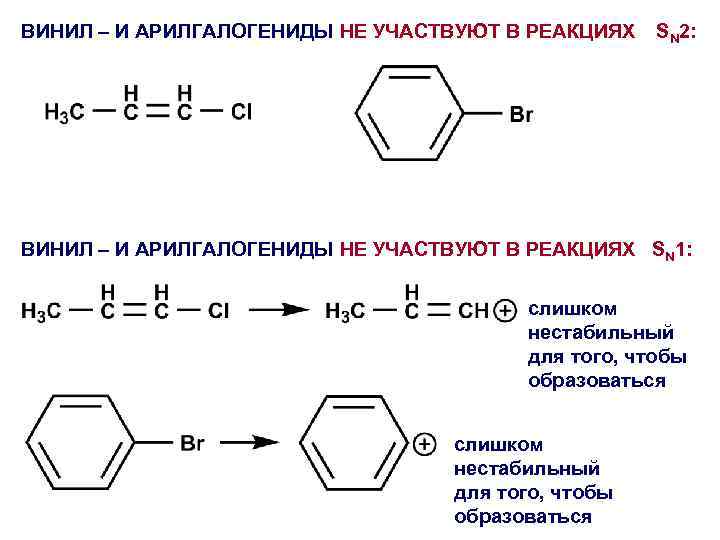 ВИНИЛ – И АРИЛГАЛОГЕНИДЫ НЕ УЧАСТВУЮТ В РЕАКЦИЯХ SN 2: ВИНИЛ – И АРИЛГАЛОГЕНИДЫ НЕ УЧАСТВУЮТ В РЕАКЦИЯХ SN 1: слишком нестабильный для того, чтобы образоваться
ВИНИЛ – И АРИЛГАЛОГЕНИДЫ НЕ УЧАСТВУЮТ В РЕАКЦИЯХ SN 2: ВИНИЛ – И АРИЛГАЛОГЕНИДЫ НЕ УЧАСТВУЮТ В РЕАКЦИЯХ SN 1: слишком нестабильный для того, чтобы образоваться
 СРАВНЕНИЕ МЕХАНИЗМОВ SN 1 и SN 2 РЕАКЦИЙ SN 2 одностадийный механизм SN 1 двустадийный механизм (карбокатион – интермедиат) обращение конфигурации стереоцентра в продукте рацемизация бимолекулярная скорость определяющая стадия одномолекулярная скорость определяющая стадия Изменение реакционной способности: 1 o > 2 o > 3 o Изменение реакционной способности: 3 o > 2 o > 1 o
СРАВНЕНИЕ МЕХАНИЗМОВ SN 1 и SN 2 РЕАКЦИЙ SN 2 одностадийный механизм SN 1 двустадийный механизм (карбокатион – интермедиат) обращение конфигурации стереоцентра в продукте рацемизация бимолекулярная скорость определяющая стадия одномолекулярная скорость определяющая стадия Изменение реакционной способности: 1 o > 2 o > 3 o Изменение реакционной способности: 3 o > 2 o > 1 o
 СРАВНЕНИЕ реакционной способности алкил галогенидов в реакциях нуклеофильного замещения 1 o алкил галогенид 2 o алкил галогенид 3 o алкил галогенид винил- и арилгалогениды 1 o и 2 o аллил- и бензилгалогениды 3 o аллил- и бензилгалогениды SN 2 и SN 1 ни SN 2, ни SN 1 SN 2 и SN 1
СРАВНЕНИЕ реакционной способности алкил галогенидов в реакциях нуклеофильного замещения 1 o алкил галогенид 2 o алкил галогенид 3 o алкил галогенид винил- и арилгалогениды 1 o и 2 o аллил- и бензилгалогениды 3 o аллил- и бензилгалогениды SN 2 и SN 1 ни SN 2, ни SN 1 SN 2 и SN 1
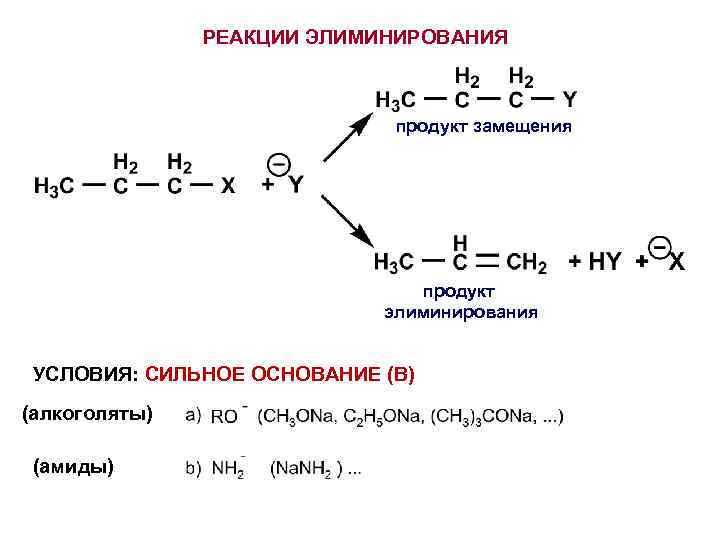 РЕАКЦИИ ЭЛИМИНИРОВАНИЯ продукт замещения продукт элиминирования УСЛОВИЯ: СИЛЬНОЕ ОСНОВАНИЕ (В) (алкоголяты) (амиды)
РЕАКЦИИ ЭЛИМИНИРОВАНИЯ продукт замещения продукт элиминирования УСЛОВИЯ: СИЛЬНОЕ ОСНОВАНИЕ (В) (алкоголяты) (амиды)
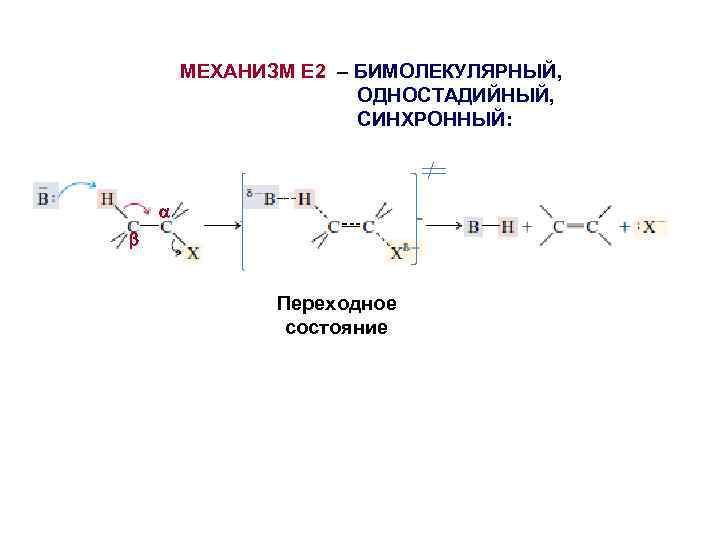 МЕХАНИЗМ Е 2 – БИМОЛЕКУЛЯРНЫЙ, ОДНОСТАДИЙНЫЙ, СИНХРОННЫЙ: Переходное состояние
МЕХАНИЗМ Е 2 – БИМОЛЕКУЛЯРНЫЙ, ОДНОСТАДИЙНЫЙ, СИНХРОННЫЙ: Переходное состояние
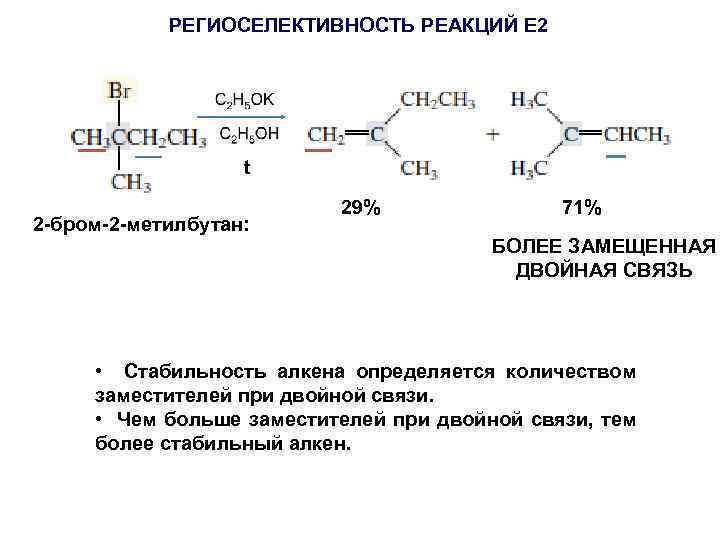 РЕГИОСЕЛЕКТИВНОСТЬ РЕАКЦИЙ E 2 t 2 -бром-2 -метилбутан: 29% 71% БОЛЕЕ ЗАМЕЩЕННАЯ ДВОЙНАЯ СВЯЗЬ • Стабильность алкена определяется количеством заместителей при двойной связи. • Чем больше заместителей при двойной связи, тем более стабильный алкен.
РЕГИОСЕЛЕКТИВНОСТЬ РЕАКЦИЙ E 2 t 2 -бром-2 -метилбутан: 29% 71% БОЛЕЕ ЗАМЕЩЕННАЯ ДВОЙНАЯ СВЯЗЬ • Стабильность алкена определяется количеством заместителей при двойной связи. • Чем больше заместителей при двойной связи, тем более стабильный алкен.
 Александр Зайцев Правило Зайцева: протон отрывается от -углерода, связанного с меньшим количеством атомов водорода.
Александр Зайцев Правило Зайцева: протон отрывается от -углерода, связанного с меньшим количеством атомов водорода.
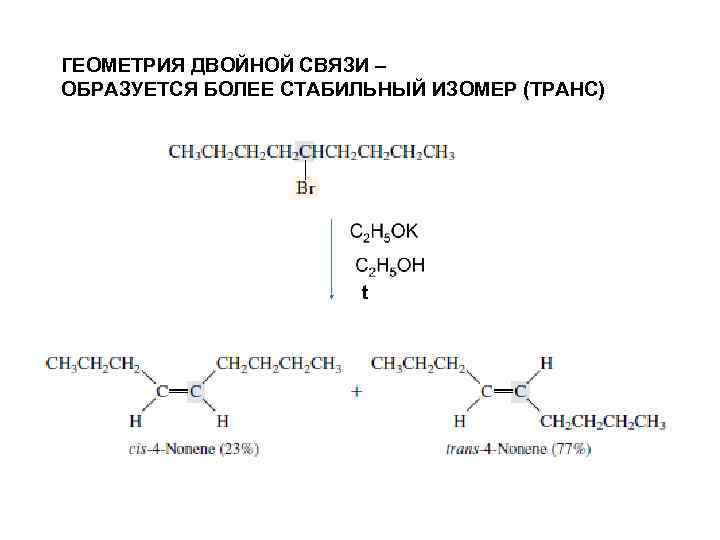 ГЕОМЕТРИЯ ДВОЙНОЙ СВЯЗИ – ОБРАЗУЕТСЯ БОЛЕЕ СТАБИЛЬНЫЙ ИЗОМЕР (ТРАНС) t
ГЕОМЕТРИЯ ДВОЙНОЙ СВЯЗИ – ОБРАЗУЕТСЯ БОЛЕЕ СТАБИЛЬНЫЙ ИЗОМЕР (ТРАНС) t
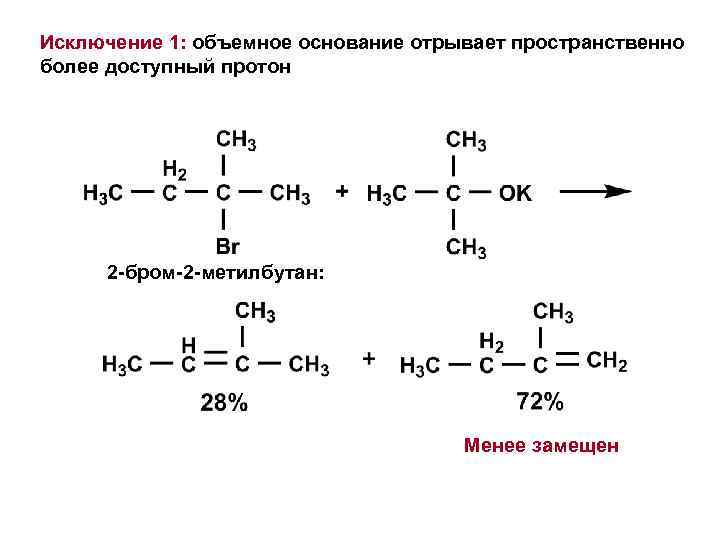 Исключение 1: объемное основание отрывает пространственно более доступный протон 2 -бром-2 -метилбутан: Менее замещен
Исключение 1: объемное основание отрывает пространственно более доступный протон 2 -бром-2 -метилбутан: Менее замещен
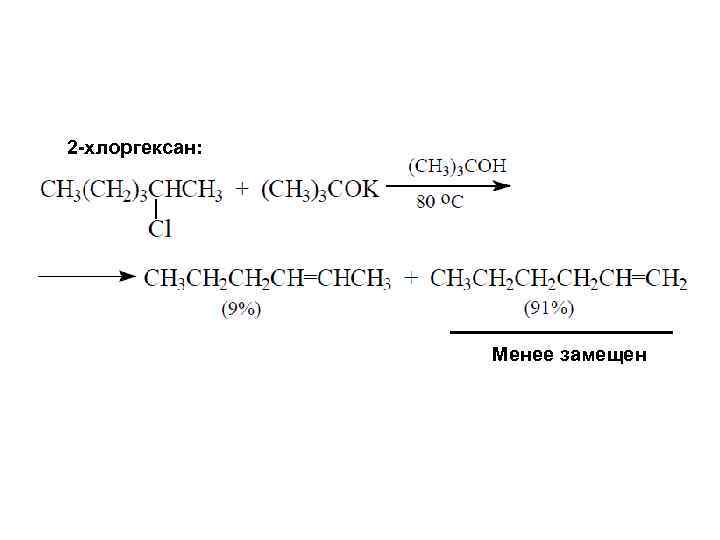 2 -хлоргексан: Менее замещен
2 -хлоргексан: Менее замещен
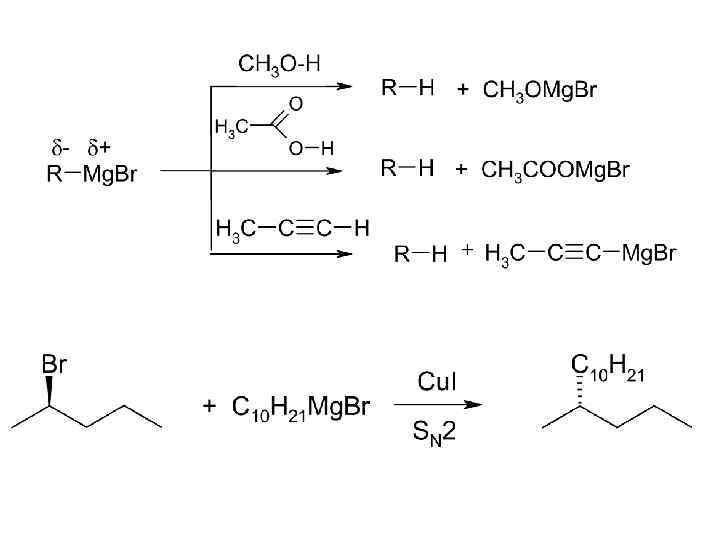
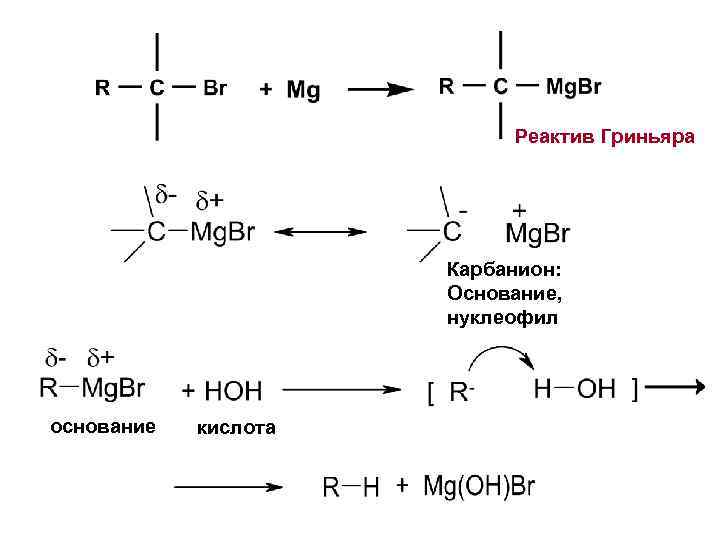 Реактив Гриньяра Карбанион: Основание, нуклеофил основание кислота
Реактив Гриньяра Карбанион: Основание, нуклеофил основание кислота