 ГАЛОГЕНПРОИЗВОДНЫЕ АЛКАНОВ 1
ГАЛОГЕНПРОИЗВОДНЫЕ АЛКАНОВ 1
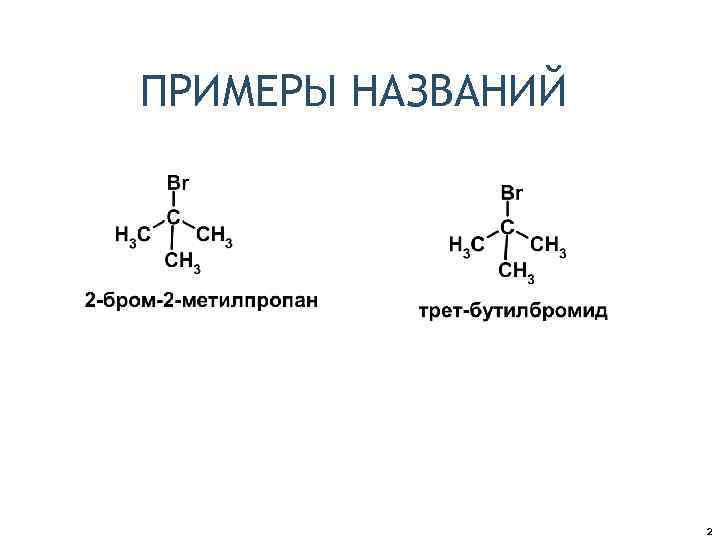 ПРИМЕРЫ НАЗВАНИЙ 2
ПРИМЕРЫ НАЗВАНИЙ 2
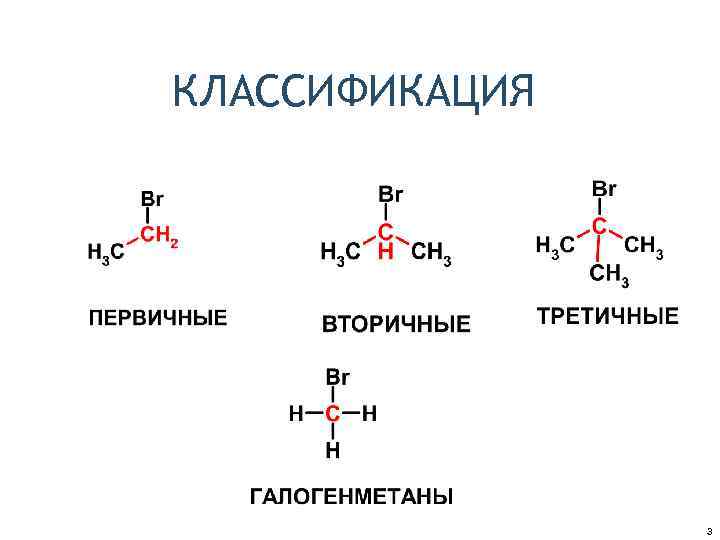 КЛАССИФИКАЦИЯ 3
КЛАССИФИКАЦИЯ 3
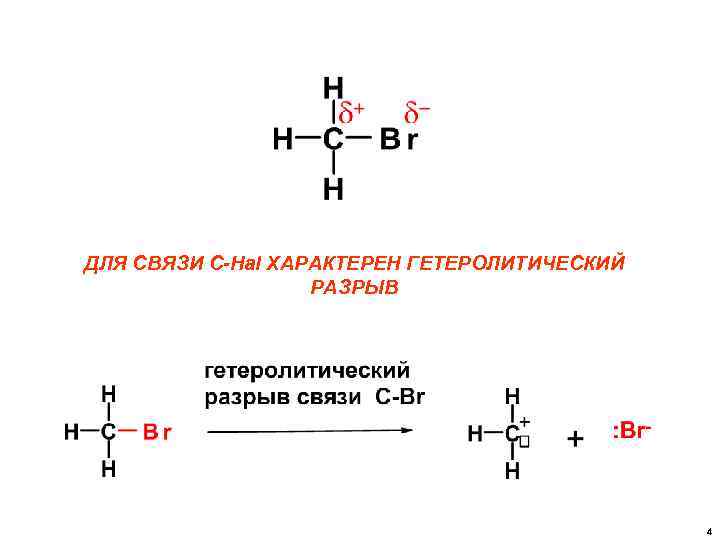 ДЛЯ СВЯЗИ C-Hal ХАРАКТЕРЕН ГЕТЕРОЛИТИЧЕСКИЙ РАЗРЫВ 4
ДЛЯ СВЯЗИ C-Hal ХАРАКТЕРЕН ГЕТЕРОЛИТИЧЕСКИЙ РАЗРЫВ 4
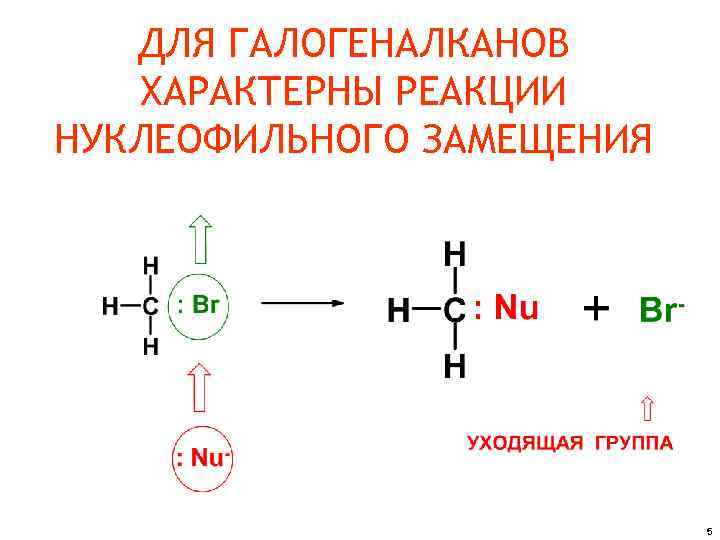 ДЛЯ ГАЛОГЕНАЛКАНОВ ХАРАКТЕРНЫ РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ 5
ДЛЯ ГАЛОГЕНАЛКАНОВ ХАРАКТЕРНЫ РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ 5
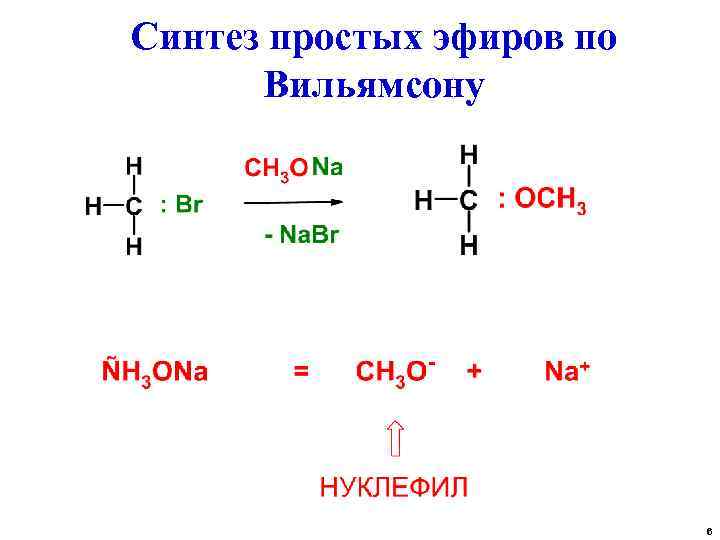 Синтез простых эфиров по Вильямсону 6
Синтез простых эфиров по Вильямсону 6
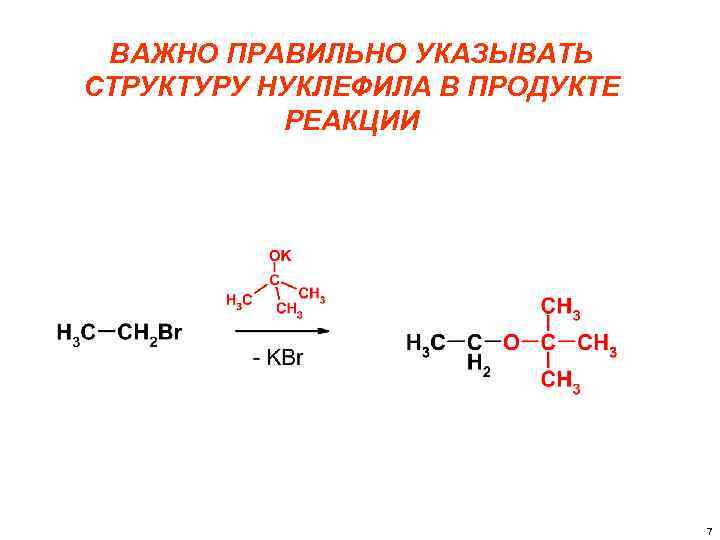 ВАЖНО ПРАВИЛЬНО УКАЗЫВАТЬ СТРУКТУРУ НУКЛЕФИЛА В ПРОДУКТЕ РЕАКЦИИ 7
ВАЖНО ПРАВИЛЬНО УКАЗЫВАТЬ СТРУКТУРУ НУКЛЕФИЛА В ПРОДУКТЕ РЕАКЦИИ 7
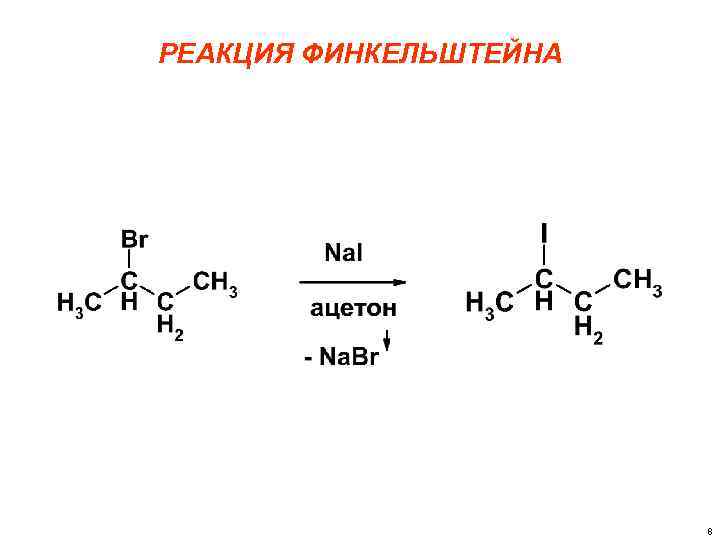 РЕАКЦИЯ ФИНКЕЛЬШТЕЙНА 8
РЕАКЦИЯ ФИНКЕЛЬШТЕЙНА 8
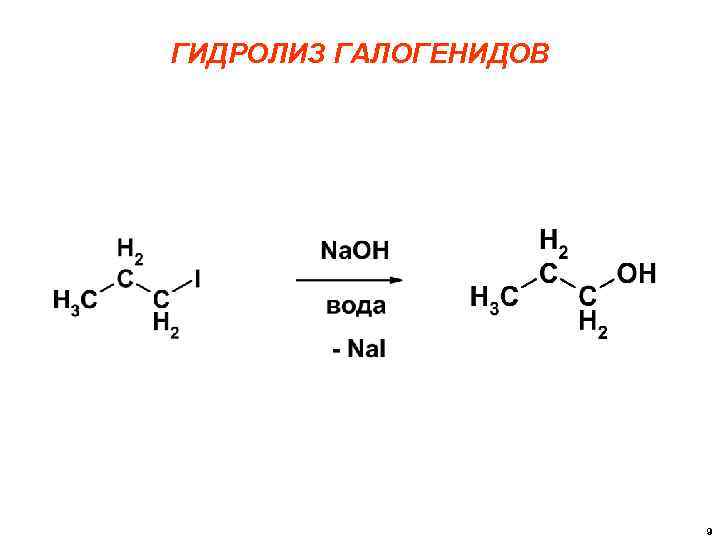 ГИДРОЛИЗ ГАЛОГЕНИДОВ 9
ГИДРОЛИЗ ГАЛОГЕНИДОВ 9
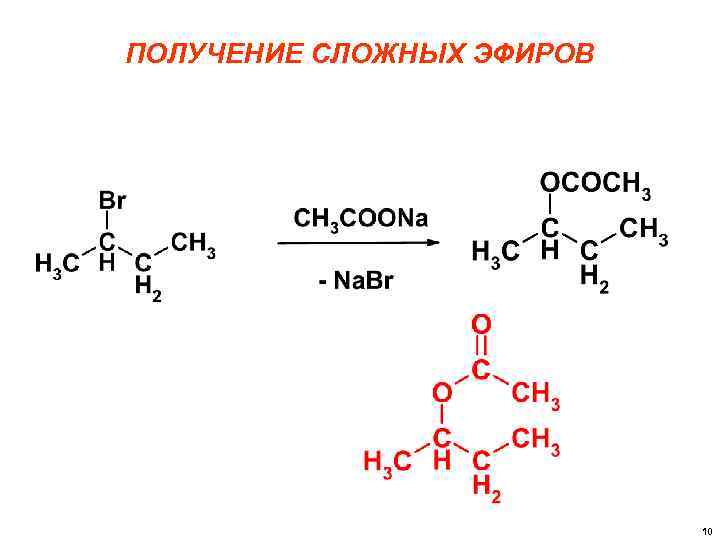 ПОЛУЧЕНИЕ СЛОЖНЫХ ЭФИРОВ 10
ПОЛУЧЕНИЕ СЛОЖНЫХ ЭФИРОВ 10
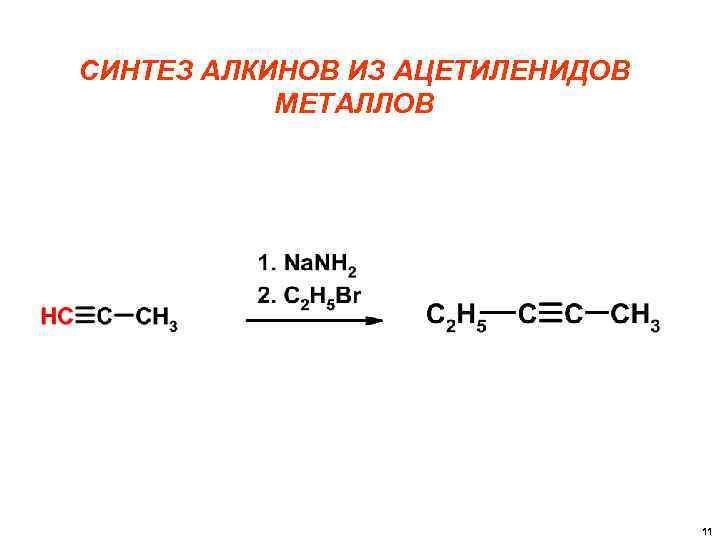 СИНТЕЗ АЛКИНОВ ИЗ АЦЕТИЛЕНИДОВ МЕТАЛЛОВ 11
СИНТЕЗ АЛКИНОВ ИЗ АЦЕТИЛЕНИДОВ МЕТАЛЛОВ 11
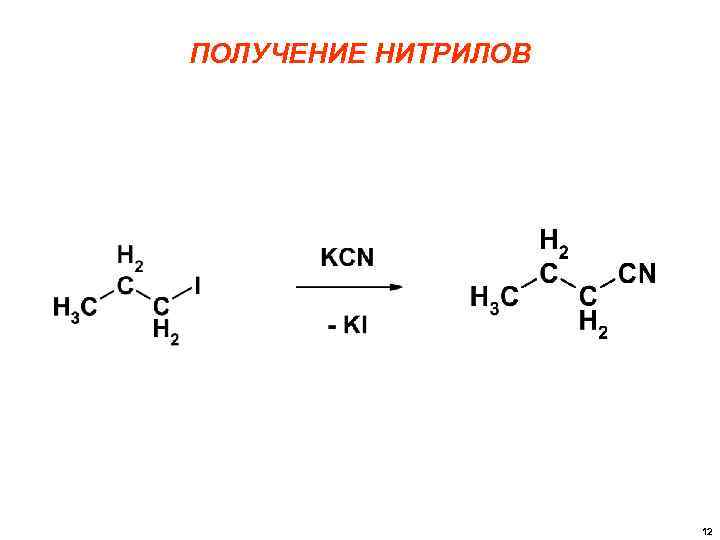 ПОЛУЧЕНИЕ НИТРИЛОВ 12
ПОЛУЧЕНИЕ НИТРИЛОВ 12
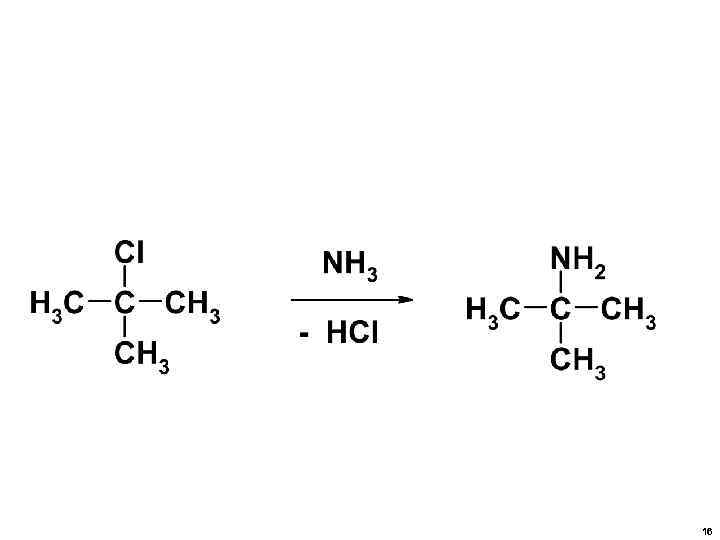
 • Na. OH и HOH (т. е. Н 2 О) • Na. NH 2 и NH 3 • CH 3 ONa и СH 3 OH • ДАЮТ ОДИНАКОВЫЙ ПРОДУКТ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ С ТОЙ ЛИШЬ РАЗНИЦЕЙ, ЧТО ВЫДЕЛЯЕТСЯ НЕ Na. Hal, а HHal. 13
• Na. OH и HOH (т. е. Н 2 О) • Na. NH 2 и NH 3 • CH 3 ONa и СH 3 OH • ДАЮТ ОДИНАКОВЫЙ ПРОДУКТ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ С ТОЙ ЛИШЬ РАЗНИЦЕЙ, ЧТО ВЫДЕЛЯЕТСЯ НЕ Na. Hal, а HHal. 13
 • ЭТО СВЯЗАНО С ТЕМ, ЧТО НА ДВУХВАЛЕНТНОМ КИСЛОРОДЕ (КАК В Н 2 О) И НА ТРЕХВАЛЕНТНОМ АЗОТЕ (КАК В NH 3) ЕСТЬ НЕПОДЕЛЕННЫЕ ЭЛЕКТРОННЫЕ ПАРЫ, ТО ЕСТЬ ЭТИ МОЛЕКУЛЫ – НУКЛЕОФИЛЬНЫ. 14
• ЭТО СВЯЗАНО С ТЕМ, ЧТО НА ДВУХВАЛЕНТНОМ КИСЛОРОДЕ (КАК В Н 2 О) И НА ТРЕХВАЛЕНТНОМ АЗОТЕ (КАК В NH 3) ЕСТЬ НЕПОДЕЛЕННЫЕ ЭЛЕКТРОННЫЕ ПАРЫ, ТО ЕСТЬ ЭТИ МОЛЕКУЛЫ – НУКЛЕОФИЛЬНЫ. 14
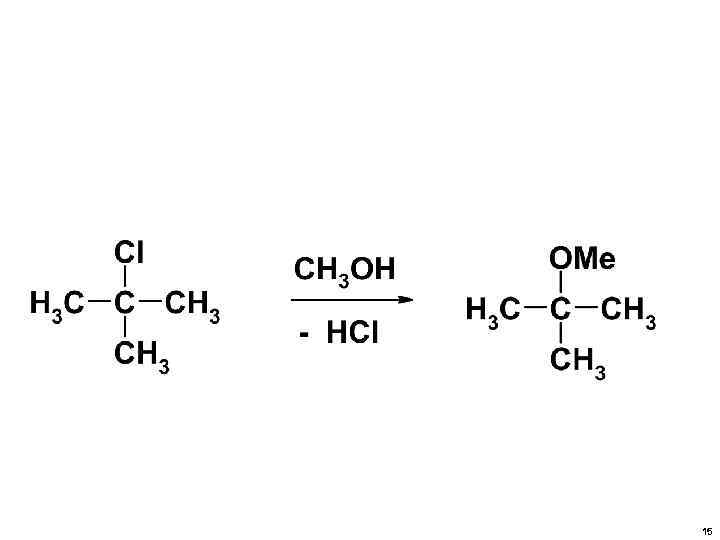 15
15
 16
16
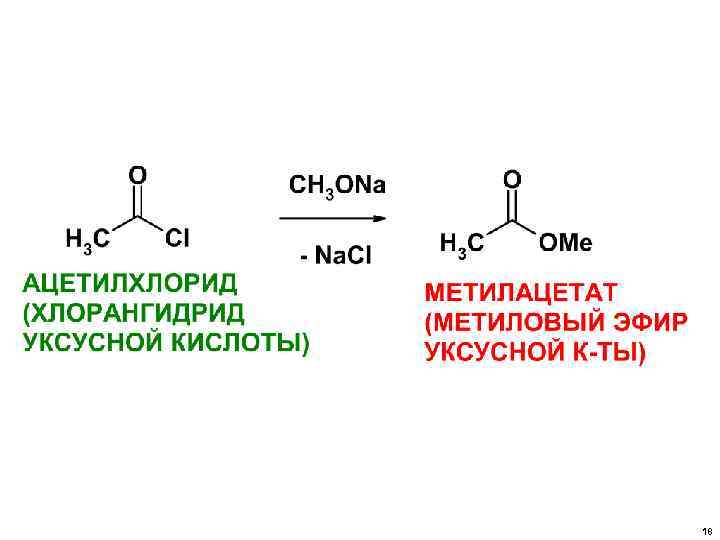
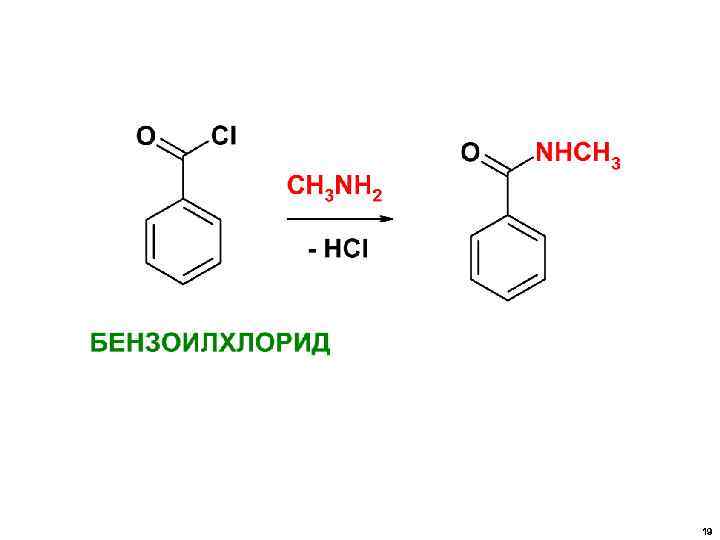
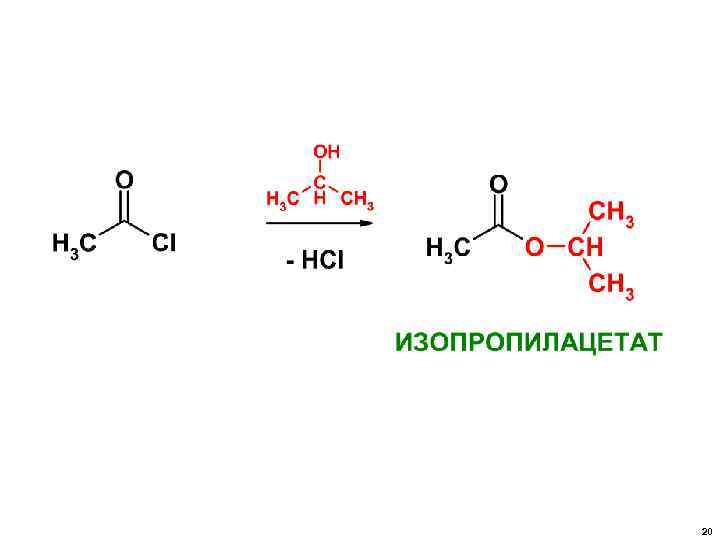
 • РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ ХАРАКТЕРНЫ НЕ ТОЛЬКО АЛКИЛГАЛОГЕНИДАМ, НО И ГАЛОГЕНАНГИДРИДАМ КАРБОНОВЫХ КИСЛОТ и т. д. 17
• РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ ХАРАКТЕРНЫ НЕ ТОЛЬКО АЛКИЛГАЛОГЕНИДАМ, НО И ГАЛОГЕНАНГИДРИДАМ КАРБОНОВЫХ КИСЛОТ и т. д. 17
 18
18
 19
19
 20
20
 • РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ ХАРАКТЕРНЫ НЕ ТОЛЬКО ДЛЯ СВЯЗЕЙ С-Hal, НО И ДЛЯ ДРУГИХ КОВАЛЕНТНЫХ ПОЛЯРНЫХ СВЯЗЕЙ, К ПРИМЕРУ, С-О. 21
• РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ ХАРАКТЕРНЫ НЕ ТОЛЬКО ДЛЯ СВЯЗЕЙ С-Hal, НО И ДЛЯ ДРУГИХ КОВАЛЕНТНЫХ ПОЛЯРНЫХ СВЯЗЕЙ, К ПРИМЕРУ, С-О. 21
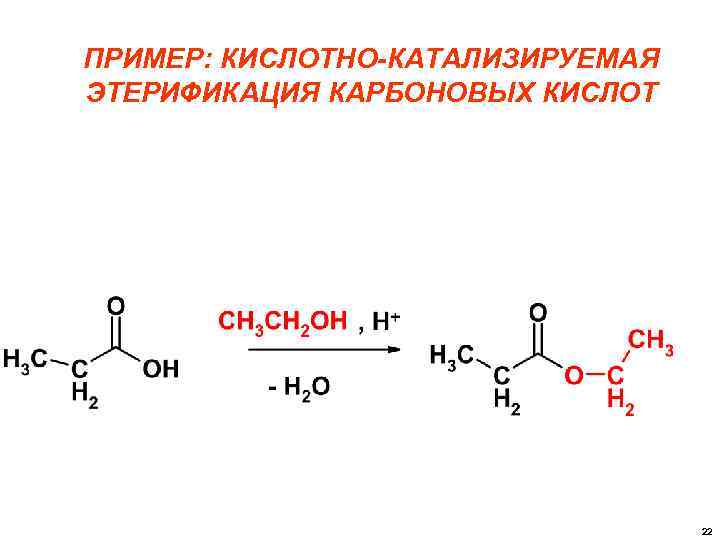 ПРИМЕР: КИСЛОТНО-КАТАЛИЗИРУЕМАЯ ЭТЕРИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ 22
ПРИМЕР: КИСЛОТНО-КАТАЛИЗИРУЕМАЯ ЭТЕРИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ 22
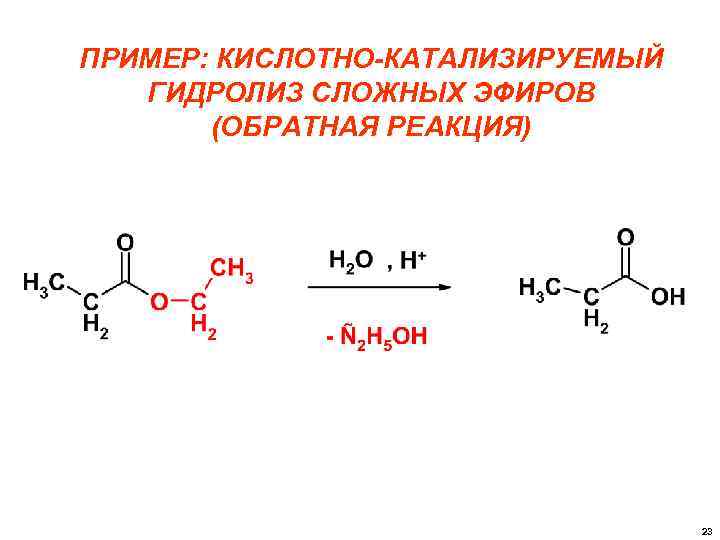 ПРИМЕР: КИСЛОТНО-КАТАЛИЗИРУЕМЫЙ ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ (ОБРАТНАЯ РЕАКЦИЯ) 23
ПРИМЕР: КИСЛОТНО-КАТАЛИЗИРУЕМЫЙ ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ (ОБРАТНАЯ РЕАКЦИЯ) 23
 НЕУЖЕЛИ ВСЕ ТАК ПРОСТО? • ИСКЛЮЧЕНИЕ ИЗ ПРАВИЛ: СИЛЬНОЕ ОСНОВАНИЕ ПРИ ВЗАИМОДЕЙСТВИИ С ТРЕТИЧНЫМИ ГАЛОГЕНИДАМИ ДАЮТ ПРЕИМУЩЕСТВЕННО ПРОДУКТ РЕАКЦИИ ЭЛИМИНИРОВАНИЯ (ОТЩЕПЛЕНИЯ ГАЛОГЕНОВОДОРОДА). 24
НЕУЖЕЛИ ВСЕ ТАК ПРОСТО? • ИСКЛЮЧЕНИЕ ИЗ ПРАВИЛ: СИЛЬНОЕ ОСНОВАНИЕ ПРИ ВЗАИМОДЕЙСТВИИ С ТРЕТИЧНЫМИ ГАЛОГЕНИДАМИ ДАЮТ ПРЕИМУЩЕСТВЕННО ПРОДУКТ РЕАКЦИИ ЭЛИМИНИРОВАНИЯ (ОТЩЕПЛЕНИЯ ГАЛОГЕНОВОДОРОДА). 24
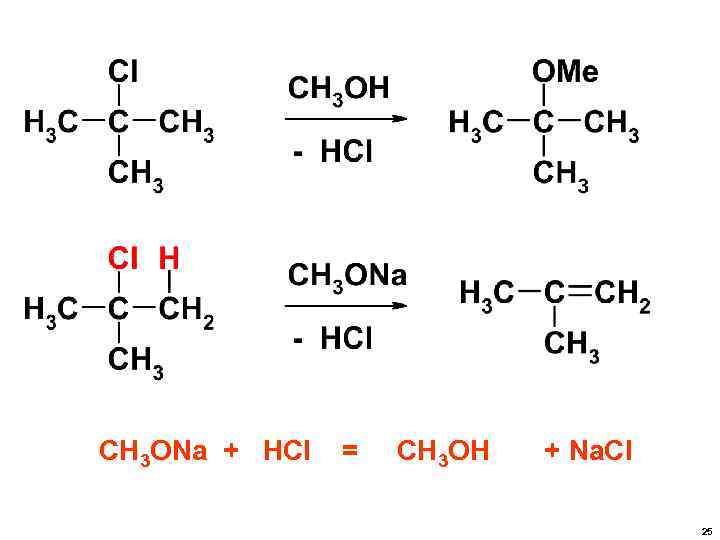 CH 3 ONa + HCl = CH 3 OH + Na. Cl 25
CH 3 ONa + HCl = CH 3 OH + Na. Cl 25
 • ПРИМЕРЫ СИЛЬНЫХ ОСНОВАНИЙ: • • KOH • CH 3 ONa • (CH 3)3 COK • Na. NH 2 26
• ПРИМЕРЫ СИЛЬНЫХ ОСНОВАНИЙ: • • KOH • CH 3 ONa • (CH 3)3 COK • Na. NH 2 26
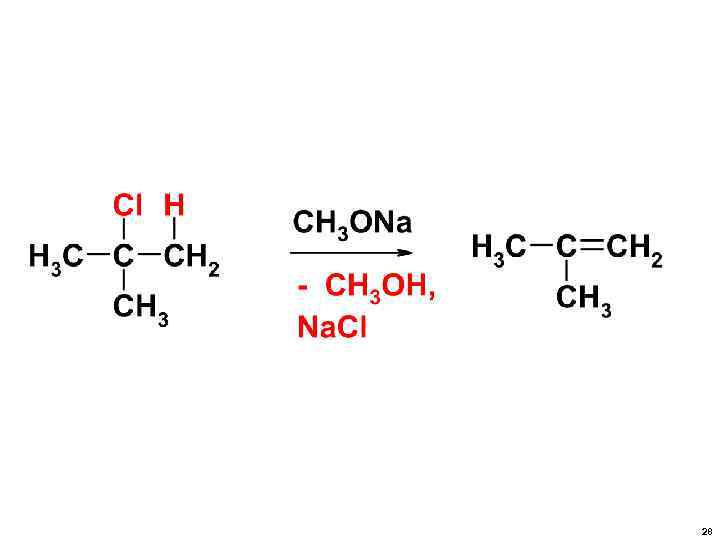
 • ЧТО ДЕЛАЮТ СИЛЬНЫЕ ОСНОВАНИЯ? • • СВЯЗЫВАЮТ ПРОТОН H+ ОБРАЗОВАНИЕМ МАЛОДИССОЦИИРОВАННОГО СОЕДИНЕНИЯ • • H+ + OH= H 2 O • H+ + CH 3 O= CH 3 OH • С 27
• ЧТО ДЕЛАЮТ СИЛЬНЫЕ ОСНОВАНИЯ? • • СВЯЗЫВАЮТ ПРОТОН H+ ОБРАЗОВАНИЕМ МАЛОДИССОЦИИРОВАННОГО СОЕДИНЕНИЯ • • H+ + OH= H 2 O • H+ + CH 3 O= CH 3 OH • С 27
 28
28
 • МЕХАНИЗМ РЕАКЦИЙ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ В АЛКИЛГАЛОГЕНИДАХ 29
• МЕХАНИЗМ РЕАКЦИЙ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ В АЛКИЛГАЛОГЕНИДАХ 29
 • РЕАКЦИЯ ПРОТЕКАЕТ ПО ОДНОМУ ИЗ ДВУХ ПУТЕЙ- SN 1 или SN 1 - А ИМЕННО ПО НАИБОЛЕЕ УДОБНОМУ ДЛЯ РЕАКЦИИ. 30
• РЕАКЦИЯ ПРОТЕКАЕТ ПО ОДНОМУ ИЗ ДВУХ ПУТЕЙ- SN 1 или SN 1 - А ИМЕННО ПО НАИБОЛЕЕ УДОБНОМУ ДЛЯ РЕАКЦИИ. 30
 • ОСНОВНОЙ ФАКТОР, ВЛИЯЮЩИЙ НА МЕХАНИЗМ РЕАКЦИИ – СТРОЕНИЕ СУБСТРАТА. • ТРЕТИЧНЫЕ СУБСТРАТЫ РЕАГИРУЮТ ПО МЕХАНИЗМУ SN 1, ОСТАЛЬНЫЕ – ПО SN 2. 31
• ОСНОВНОЙ ФАКТОР, ВЛИЯЮЩИЙ НА МЕХАНИЗМ РЕАКЦИИ – СТРОЕНИЕ СУБСТРАТА. • ТРЕТИЧНЫЕ СУБСТРАТЫ РЕАГИРУЮТ ПО МЕХАНИЗМУ SN 1, ОСТАЛЬНЫЕ – ПО SN 2. 31
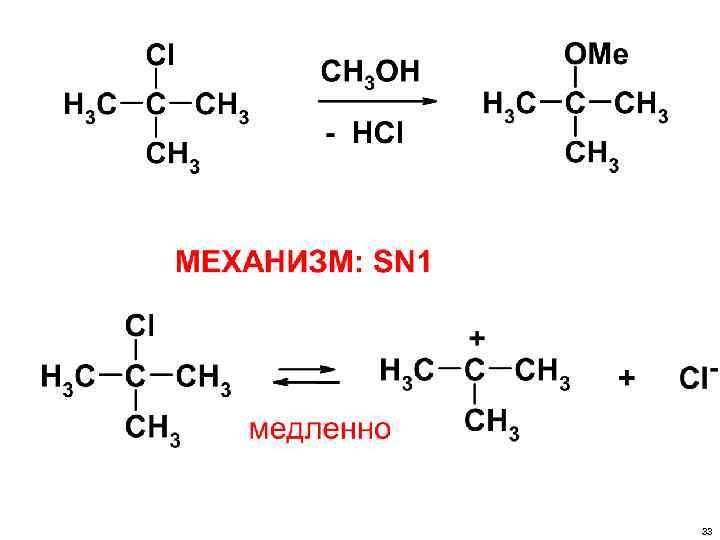
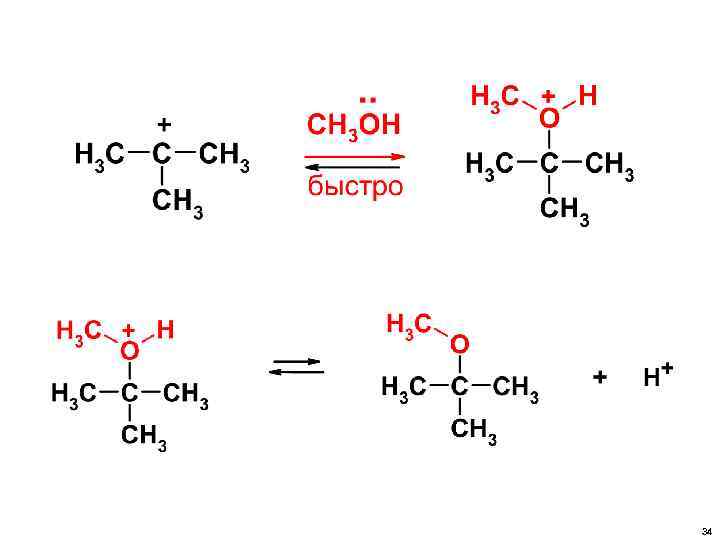
 • В РЕАКЦИЯХ SN 1 СНАЧАЛА УХОДИТ УХОДЯЩАЯ ГРУППА, А ПОТОМ НА ОСВОБОДИВШЕЕСЯ МЕСТО ПРИХОДИТ НУКЛЕОФИЛ. 32
• В РЕАКЦИЯХ SN 1 СНАЧАЛА УХОДИТ УХОДЯЩАЯ ГРУППА, А ПОТОМ НА ОСВОБОДИВШЕЕСЯ МЕСТО ПРИХОДИТ НУКЛЕОФИЛ. 32
 33
33
 34
34
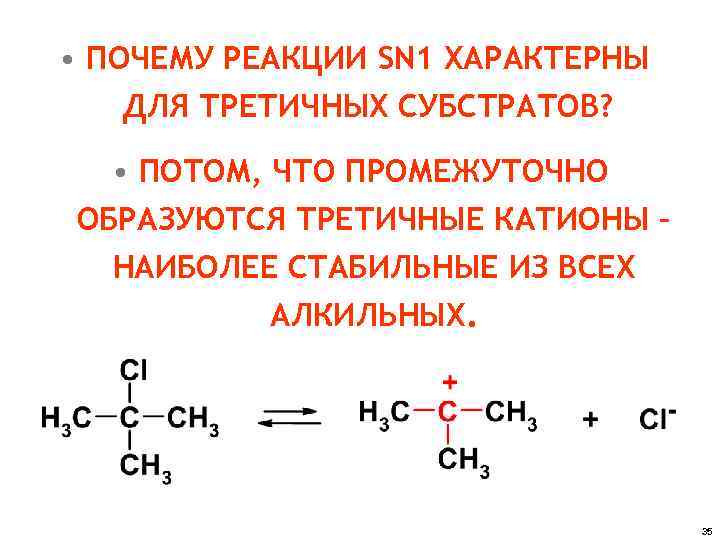 • ПОЧЕМУ РЕАКЦИИ SN 1 ХАРАКТЕРНЫ ДЛЯ ТРЕТИЧНЫХ СУБСТРАТОВ? • ПОТОМ, ЧТО ПРОМЕЖУТОЧНО ОБРАЗУЮТСЯ ТРЕТИЧНЫЕ КАТИОНЫ – НАИБОЛЕЕ СТАБИЛЬНЫЕ ИЗ ВСЕХ АЛКИЛЬНЫХ. 35
• ПОЧЕМУ РЕАКЦИИ SN 1 ХАРАКТЕРНЫ ДЛЯ ТРЕТИЧНЫХ СУБСТРАТОВ? • ПОТОМ, ЧТО ПРОМЕЖУТОЧНО ОБРАЗУЮТСЯ ТРЕТИЧНЫЕ КАТИОНЫ – НАИБОЛЕЕ СТАБИЛЬНЫЕ ИЗ ВСЕХ АЛКИЛЬНЫХ. 35
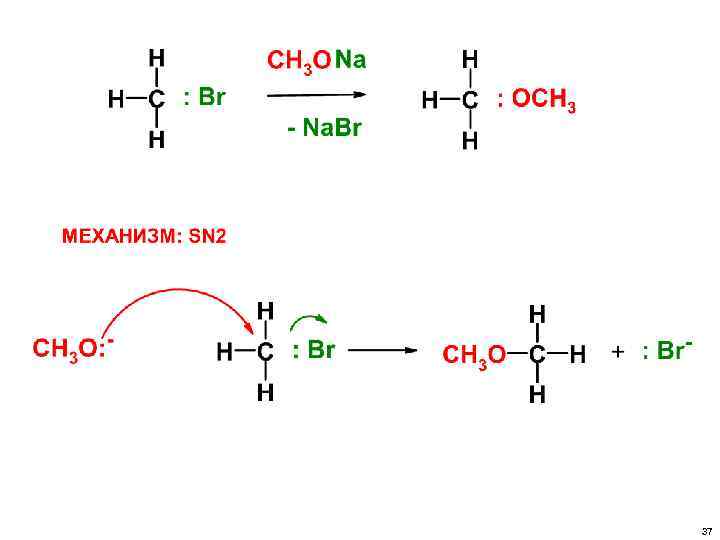
 • В РЕАКЦИЯХ SN 2 УХОДЯЩАЯ ГРУППА УХОДИТ ОДНОВРЕМЕННО С ПРИХОДОМ НУКЛЕОФИЛА. РЕАКЦИЯ ПРОТЕКАЕТ В ОДНУ СТАДИЮ. 36
• В РЕАКЦИЯХ SN 2 УХОДЯЩАЯ ГРУППА УХОДИТ ОДНОВРЕМЕННО С ПРИХОДОМ НУКЛЕОФИЛА. РЕАКЦИЯ ПРОТЕКАЕТ В ОДНУ СТАДИЮ. 36
 37
37
 • ПОЧЕМУ РЕАКЦИИ SN 2 ХАРАКТЕРНЫ ДЛЯ ПЕРВИЧНЫХ, ВТОРИЧНЫХ СУБСТРАТОВ, А ТАКЖЕ ДЛЯ ГАЛОГЕНМЕТАНОВ? • ПОТОМУ, ЧТО ПУТЬ SN 1 НЕВЫГОДЕН ИЗ-ЗА НИЗКОЙ СТАБИЛЬНОСТИ КАТИОНА. 38
• ПОЧЕМУ РЕАКЦИИ SN 2 ХАРАКТЕРНЫ ДЛЯ ПЕРВИЧНЫХ, ВТОРИЧНЫХ СУБСТРАТОВ, А ТАКЖЕ ДЛЯ ГАЛОГЕНМЕТАНОВ? • ПОТОМУ, ЧТО ПУТЬ SN 1 НЕВЫГОДЕН ИЗ-ЗА НИЗКОЙ СТАБИЛЬНОСТИ КАТИОНА. 38
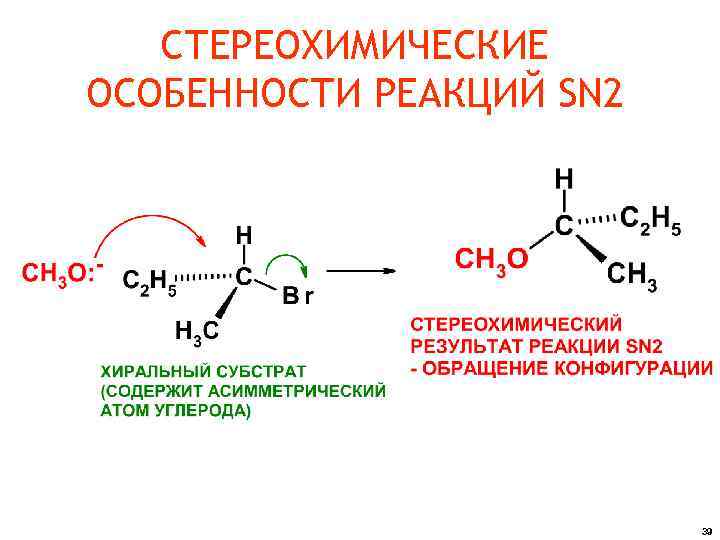 СТЕРЕОХИМИЧЕСКИЕ ОСОБЕННОСТИ РЕАКЦИЙ SN 2 39
СТЕРЕОХИМИЧЕСКИЕ ОСОБЕННОСТИ РЕАКЦИЙ SN 2 39
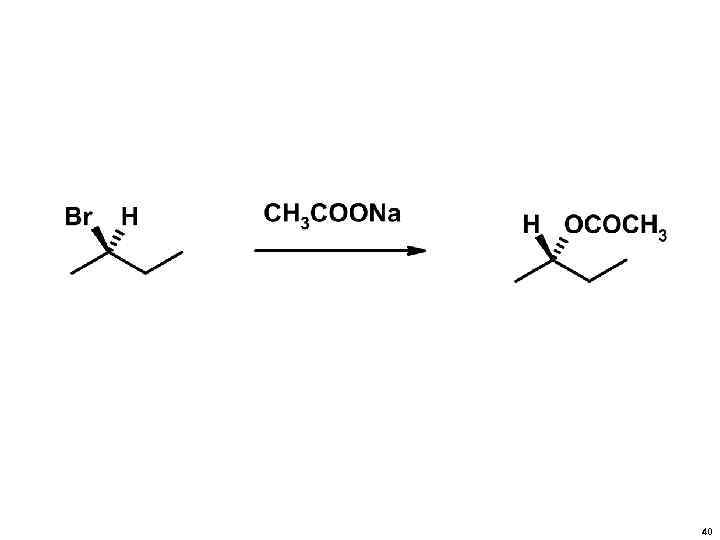 40
40