Galogenuv-Sulf-Nitr.ppt
- Количество слайдов: 12
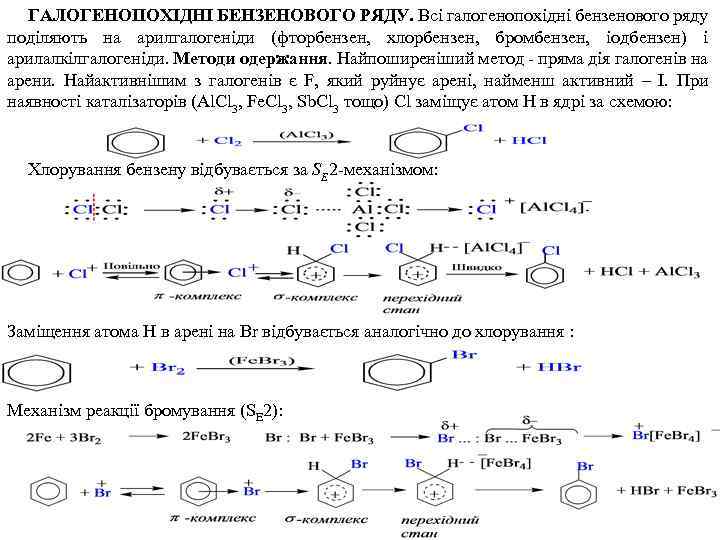
ГАЛОГЕНОПОХІДНІ БЕНЗЕНОВОГО РЯДУ. Всі галогенопохідні бензенового ряду поділяють на арилгалогеніди (фторбензен, хлорбензен, бромбензен, іодбензен) і арилалкілгалогеніди. Методи одержання. Найпоширеніший метод - пряма дія галогенів на арени. Найактивнішим з галогенів є F, який руйнує арені, найменш активний – І. При наявності каталізаторів (Al. Cl 3, Fe. Cl 3, Sb. Cl 3 тощо) Cl заміщує атом H в ядрі за схемою: Хлорування бензену відбувається за SE 2 -механізмом: Заміщення атома Н в арені на Br відбувається аналогічно до хлорування : Механізм реакції бромування (SE 2):
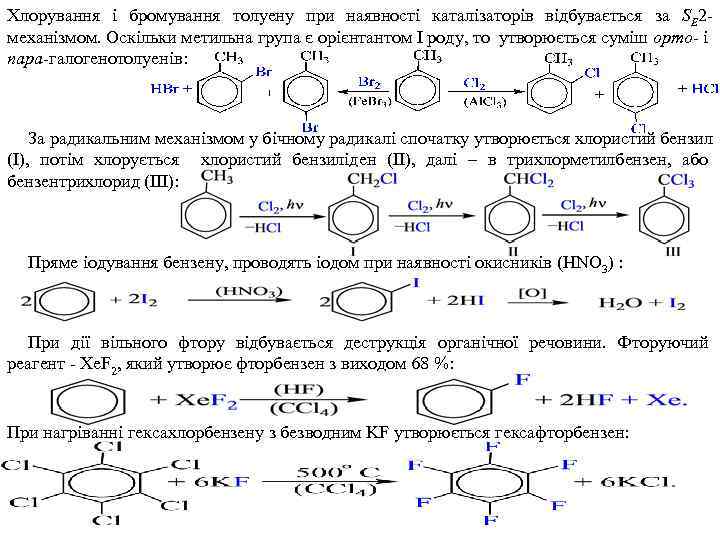
Хлорування і бромування толуену при наявності каталізаторів відбувається за SE 2 механізмом. Оскільки метильна група є орієнтантом I роду, то утворюється суміш орто- і пара-галогенотолуенів: За радикальним механізмом у бічному радикалі спочатку утворюється хлористий бензил (І), потім хлорується хлористий бензиліден (II), далі – в трихлорметилбензен, або бензентрихлорид (III): Пряме іодування бензену, проводять іодом при наявності окисників (HNO 3) : При дії вільного фтору відбувається деструкція органічної речовини. Фторуючий реагент - Xe. F 2, який утворює фторбензен з виходом 68 %: При нагріванні гексахлорбензену з безводним KF утворюється гексафторбензен:
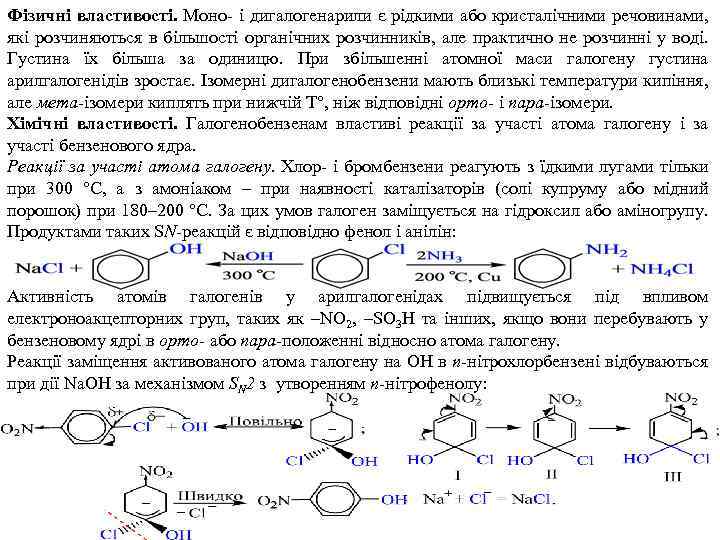
Фізичні властивості. Моно- і дигалогенарили є рідкими або кристалічними речовинами, які розчиняються в більшості органічних розчинників, але практично не розчинні у воді. Густина їх більша за одиницю. При збільшенні атомної маси галогену густина арилгалогенідів зростає. Ізомерні дигалогенобензени мають близькі температури кипіння, але мета-ізомери киплять при нижчій T°, ніж відповідні орто- і пара-ізомери. Хімічні властивості. Галогенобензенам властиві реакції за участі атома галогену і за участі бензенового ядра. Реакції за участі атома галогену. Хлор- і бромбензени реагують з їдкими лугами тільки при 300 °С, а з амоніаком – при наявності каталізаторів (солі купруму або мідний порошок) при 180– 200 °С. За цих умов галоген заміщується на гідроксил або аміногрупу. Продуктами таких SN-реакцій є відповідно фенол і анілін: Активність атомів галогенів у арилгалогенідах підвищується під впливом електроноакцепторних груп, таких як –NO 2, –SO 3 H та інших, якщо вони перебувають у бензеновому ядрі в орто- або пара-положенні відносно атома галогену. Реакції заміщення активованого атома галогену на ОН в п-нітрохлорбензені відбуваються при дії Na. OH за механізмом SN 2 з утворенням п-нітрофенолу:
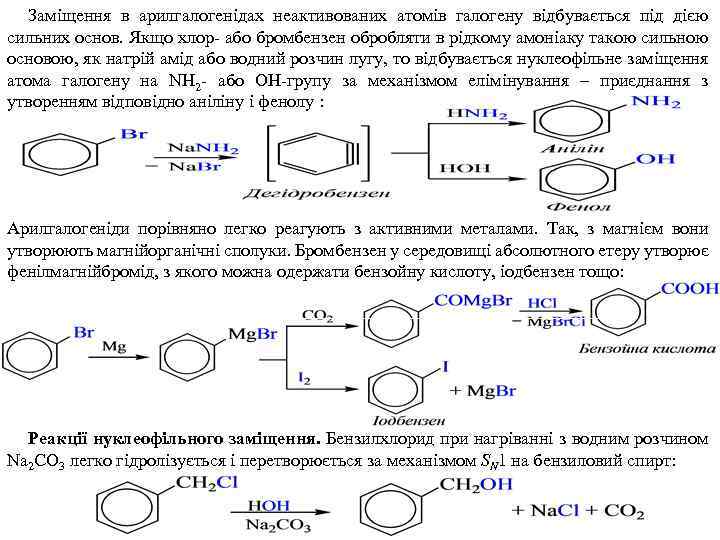
Заміщення в арилгалогенідах неактивованих атомів галогену відбувається під дією сильних основ. Якщо хлор- або бромбензен обробляти в рідкому амоніаку такою сильною основою, як натрій амід або водний розчин лугу, то відбувається нуклеофільне заміщення атома галогену на NH 2 - або ОН-групу за механізмом елімінування – приєднання з утворенням відповідно аніліну і фенолу : Арилгалогеніди порівняно легко реагують з активними металами. Так, з магнієм вони утворюють магнійорганічні сполуки. Бромбензен у середовищі абсолютного етеру утворює фенілмагнійбромід, з якого можна одержати бензойну кислоту, іодбензен тощо: Реакції нуклеофільного заміщення. Бензилхлорид при нагріванні з водним розчином Na 2 CO 3 легко гідролізується і перетворюється за механізмом SN 1 на бензиловий спирт:
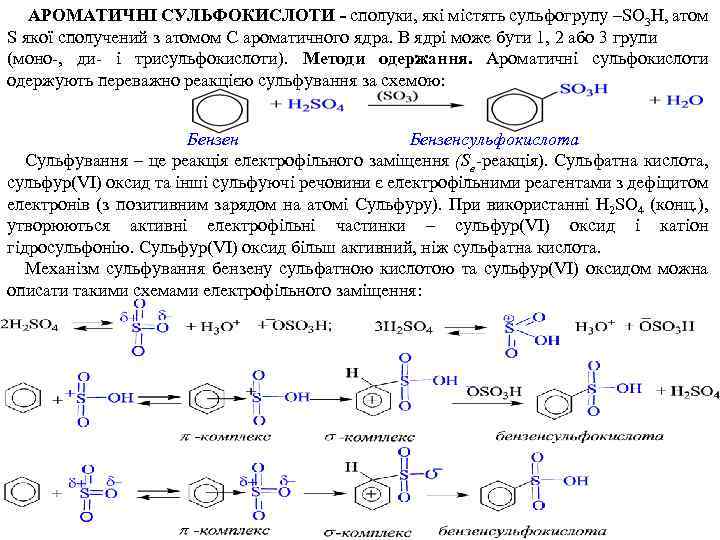
АРОМАТИЧНІ СУЛЬФОКИСЛОТИ - сполуки, які містять сульфогрупу –SO 3 H, атом S якої сполучений з атомом C ароматичного ядра. В ядрі може бути 1, 2 або 3 групи (моно-, ди- і трисульфокислоти). Методи одержання. Ароматичні сульфокислоти одержують переважно реакцією сульфування за схемою: Бензенсульфокислота Сульфування – це реакція електрофільного заміщення (Se-реакція). Сульфатна кислота, сульфур(VI) оксид та інші сульфуючі речовини є електрофільними реагентами з дефіцитом електронів (з позитивним зарядом на атомі Сульфуру). При використанні H 2 SO 4 (конц. ), утворюються активні електрофільні частинки – сульфур(VІ) оксид і катіон гідросульфонію. Сульфур(VI) оксид більш активний, ніж сульфатна кислота. Механізм сульфування бензену сульфатною кислотою та сульфур(VI) оксидом можна описати такими схемами електрофільного заміщення:
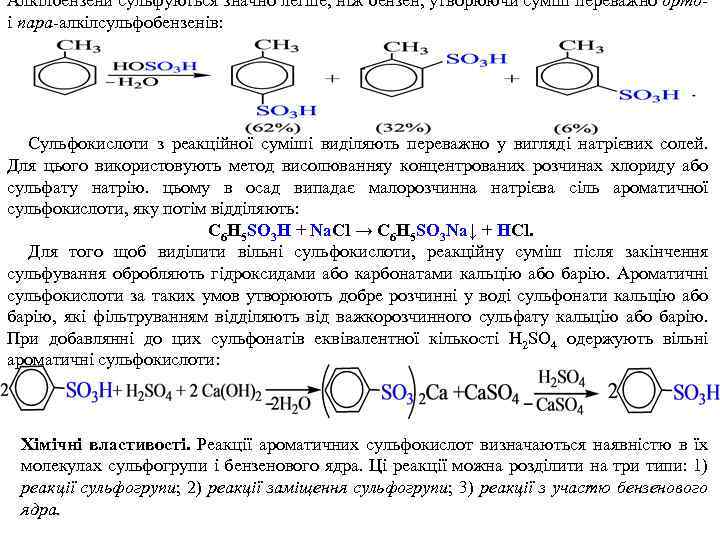
Алкілбензени сульфуються значно легше, ніж бензен, утворюючи суміш переважно ортоі пара-алкілсульфобензенів: Сульфокислоти з реакційної суміші виділяють переважно у вигляді натрієвих солей. Для цього використовують метод висолюванняу концентрованих розчинах хлориду або сульфату натрію. цьому в осад випадає малорозчинна натрієва сіль ароматичної сульфокислоти, яку потім відділяють: С 6 H 5 SO 3 H + Na. Cl → С 6 H 5 SO 3 Na↓ + HCl. Для того щоб виділити вільні сульфокислоти, реакційну суміш після закінчення сульфування обробляють гідроксидами або карбонатами кальцію або барію. Ароматичні сульфокислоти за таких умов утворюють добре розчинні у воді сульфонати кальцію або барію, які фільтруванням відділяють від важкорозчинного сульфату кальцію або барію. При добавлянні до цих сульфонатів еквівалентної кількості H 2 SO 4 одержують вільні ароматичні сульфокислоти: Хімічні властивості. Реакції ароматичних сульфокислот визначаються наявністю в їх молекулах сульфогрупи і бензенового ядра. Ці реакції можна розділити на три типи: 1) реакції сульфогрупи; 2) реакції заміщення сульфогрупи; 3) реакції з участю бензенового ядра.
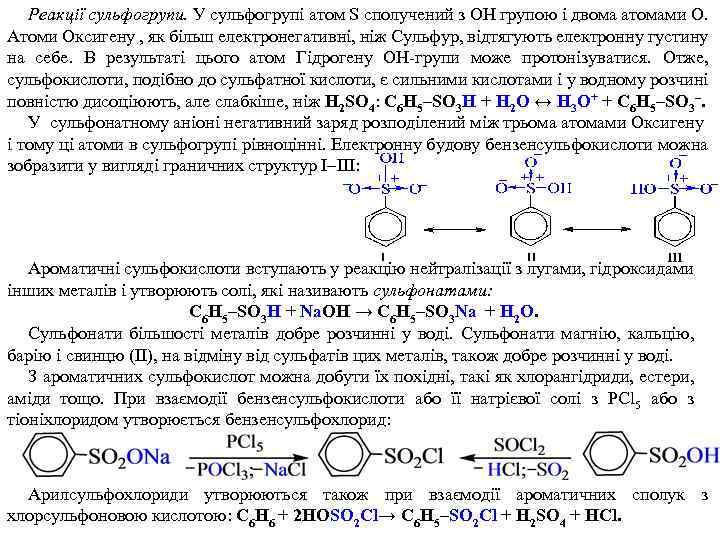
Реакції сульфогрупи. У сульфогрупі атом S сполучений з OH групою і двома атомами O. Атоми Оксигену , як більш електронегативні, ніж Сульфур, відтягують електронну густину на себе. В результаті цього атом Гідрогену ОН-групи може протонізуватися. Отже, сульфокислоти, подібно до сульфатної кислоти, є сильними кислотами і у водному розчині повністю дисоціюють, але слабкіше, ніж H 2 SO 4: C 6 H 5–SO 3 H + H 2 O ↔ H 3 O+ + C 6 H 5–SO 3–. У сульфонатному аніоні негативний заряд розподілений між трьома атомами Оксигену і тому ці атоми в сульфогрупі рівноцінні. Електронну будову бензенсульфокислоти можна зобразити у вигляді граничних структур І–III: Ароматичні сульфокислоти вступають у реакцію нейтралізації з лугами, гідроксидами інших металів і утворюють солі, які називають сульфонатами: C 6 H 5–SO 3 H + Na. OH → C 6 H 5–SO 3 Na + H 2 O. Сульфонати більшості металів добре розчинні у воді. Сульфонати магнію, кальцію, барію і свинцю (II), на відміну від сульфатів цих металів, також добре розчинні у воді. З ароматичних сульфокислот можна добути їх похідні, такі як хлорангідриди, естери, аміди тощо. При взаємодії бензенсульфокислоти або її натрієвої солі з РСl 5 або з тіоніхлоридом утворюється бензенсульфохлорид: Арилсульфохлориди утворюються також при взаємодії ароматичних сполук з хлорсульфоновою кислотою: C 6 H 6 + 2 HOSO 2 Cl→ C 6 H 5–SO 2 Cl + H 2 SO 4 + HCl.
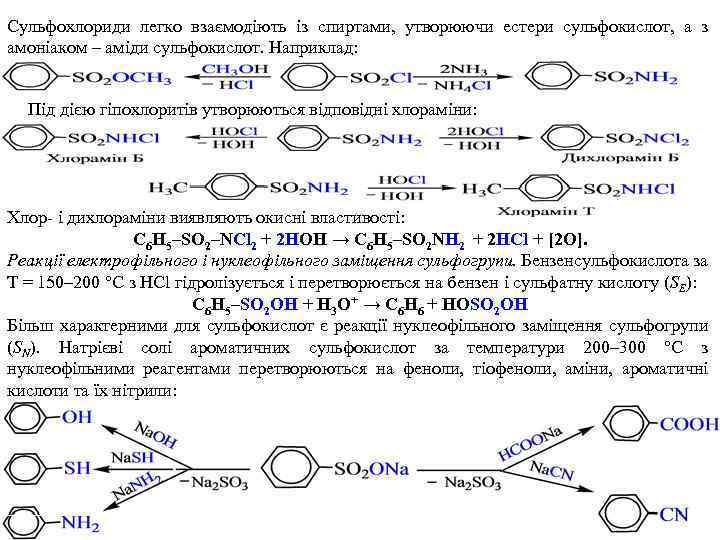
Сульфохлориди легко взаємодіють із спиртами, утворюючи естери сульфокислот, а з амоніаком – аміди сульфокислот. Наприклад: Під дією гіпохлоритів утворюються відповідні хлораміни: Хлор- і дихлораміни виявляють окисні властивості: C 6 H 5–SO 2–NCl 2 + 2 HOH → C 6 H 5–SO 2 NH 2 + 2 HCl + [2 O]. Реакції електрофільного і нуклеофільного заміщення сульфогрупи. Бензенсульфокислота за Т = 150– 200 °С з HCl гідролізується і перетворюється на бензен і сульфатну кислоту (SE): C 6 H 5–SO 2 OH + H 3 O+ → C 6 H 6 + HOSO 2 OH Більш характерними для сульфокислот є реакції нуклеофільного заміщення сульфогрупи (SN). Натрієві солі ароматичних сульфокислот за температури 200– 300 °С з нуклеофільними реагентами перетворюються на феноли, тіофеноли, аміни, ароматичні кислоти та їх нітрили:
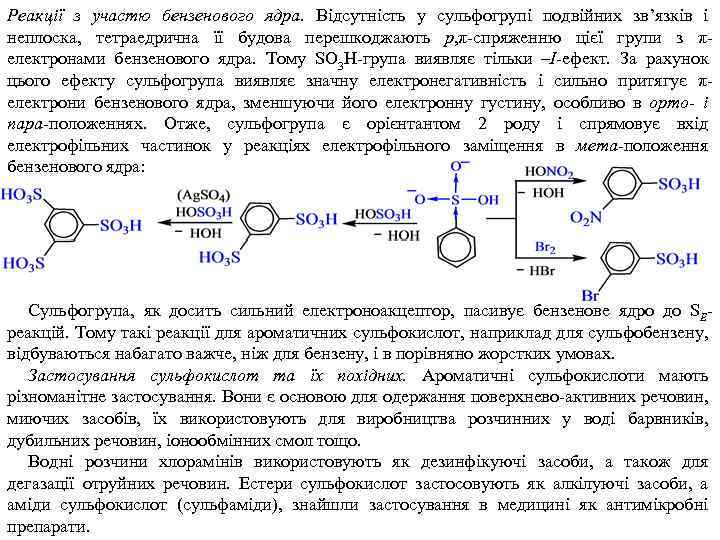
Реакції з участю бензенового ядра. Відсутність у сульфогрупі подвійних зв’язків і неплоска, тетраедрична її будова перешкоджають p, π-спряженню цієї групи з πелектронами бензенового ядра. Тому SO 3 H-група виявляє тільки –I-ефект. За рахунок цього ефекту сульфогрупа виявляє значну електронегативність і сильно притягує πелектрони бензенового ядра, зменшуючи його електронну густину, особливо в орто- і пара-положеннях. Отже, сульфогрупа є орієнтантом 2 роду і спрямовує вхід електрофільних частинок у реакціях електрофільного заміщення в мета-положення бензенового ядра: Сульфогрупа, як досить сильний електроноакцептор, пасивує бензенове ядро до SEреакцій. Тому такі реакції для ароматичних сульфокислот, наприклад для сульфобензену, відбуваються набагато важче, ніж для бензену, і в порівняно жорстких умовах. Застосування сульфокислот та їх похідних. Ароматичні сульфокислоти мають різноманітне застосування. Вони є основою для одержання поверхнево-активних речовин, миючих засобів, їх використовують для виробництва розчинних у воді барвників, дубильних речовин, іонообмінних смол тощо. Водні розчини хлорамінів використовують як дезинфікуючі засоби, а також для дегазації отруйних речовин. Естери сульфокислот застосовують як алкілуючі засоби, а аміди сульфокислот (сульфаміди), знайшли застосування в медицині як антимікробні препарати.

НІТРОСПОЛУКИ АРОМАТИЧНОГО РЯДУ Ароматичні нітросполуки є речовинами, що містять нітрогрупу –NO 2, атом Нітрогену якої сполучений з атомом Карбону ароматичного ядра. Ароматичні нітросполуки можуть містити одну, дві і три нітрогрупи. Загальна формула ароматичних мононітросполук Сn. H 2 n– 7–NO 2. Прикладом найпростішої ароматичної нітросполуки є нітробензен С 6 Н 5–NO 2. Методи одержання. Ароматичні нітросполуки одержують переважно реакцією нітрування. Як нітруючі реагенти найчастіше застосовують суміш концентрованих HNO 3 і H 2 SO 4 (нітруюча суміш), суміш селітри (Na. NO 3 або KNO 3) з H 2 SO 4 (конц. ), HNO 3 різної концентрації, оксиди нітрогену. Класичний приклад такої реакції - нітрування бензену. При його перемішуванні з нітруючою сумішшю за Т =40– 50 °С утворює нітробензен з виходом ~95 %: Бензен Нітробензен За механізмом реакція нітрування є SE 2 -реакцією. Нітруючим реагентом при нітруванні HNO 3 (конц. ) є нітроній-катіон +NO 2, який утворюються в результаті дисоціації цієї кислоти: 2 HONO 2 ↔ NO 2+ + NO 3– + H 2 O. В нітруючій суміші нітроній-катіон генерується в процесі рівноважної реакції: 2 HONO 2 + 2 H 2 SO 4 ↔ NO 2+ + H 3 O+ +HOSO 3–. Існування катіона +NO 2 підтверджується тим, що електропровідність нітруючої суміші значно вища, ніж електропровідність окремо взятих HNO 3 і H 2 SO 4. Відносна енергетична стабільність +NO 2 пояснюється взаємодією вільних пар pелектронів sр2 -атомів Оксигену з вакантною р-орбіталлю атома нітрогену, який знаходиться в sp-гібридизованому стані.
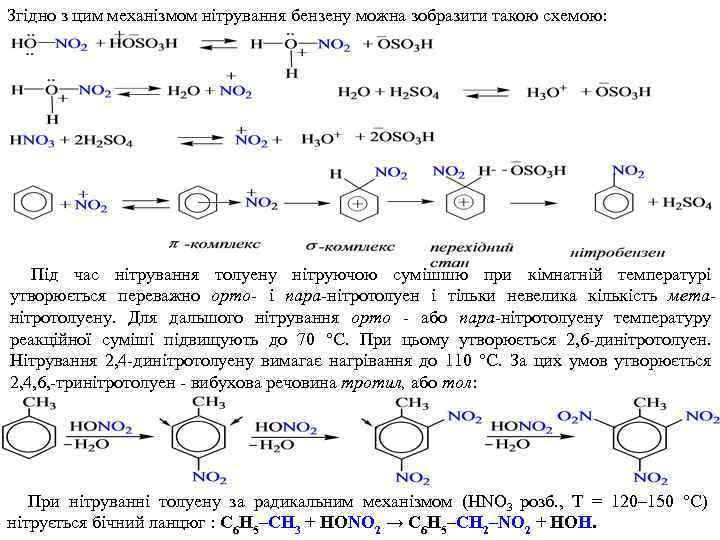
Згідно з цим механізмом нітрування бензену можна зобразити такою схемою: Під час нітрування толуену нітруючою сумішшю при кімнатній температурі утворюється переважно орто- і пара-нітротолуен і тільки невелика кількість метанітротолуену. Для дальшого нітрування орто - або пара-нітротолуену температуру реакційної суміші підвищують до 70 °С. При цьому утворюється 2, 6 -динітротолуен. Нітрування 2, 4 -динітротолуену вимагає нагрівання до 110 °С. За цих умов утворюється 2, 4, 6, -тринітротолуен - вибухова речовина тротил, або тол: При нітруванні толуену за радикальним механізмом (HNO 3 розб. , T = 120– 150 °С) нітрується бічний ланцюг : C 6 H 5–CH 3 + HONO 2 → C 6 H 5–CH 2–NO 2 + HOH.
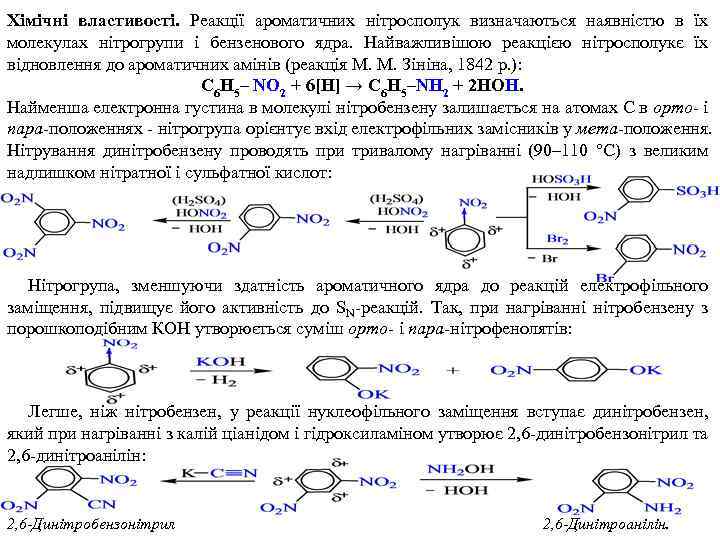
Хімічні властивості. Реакції ароматичних нітросполук визначаються наявністю в їх молекулах нітрогрупи і бензенового ядра. Найважливішою реакцією нітросполукє їх відновлення до ароматичних амінів (реакція М. М. Зініна, 1842 р. ): C 6 H 5– NO 2 + 6[H] → C 6 H 5–NH 2 + 2 HOH. Найменша електронна густина в молекулі нітробензену залишається на атомах С в орто- і пара-положеннях - нітрогрупа орієнтує вхід електрофільних замісників у мета-положення. Нітрування динітробензену проводять при тривалому нагріванні (90– 110 °С) з великим надлишком нітратної і сульфатної кислот: Нітрогрупа, зменшуючи здатність ароматичного ядра до реакцій електрофільного заміщення, підвищує його активність до SN-реакцій. Так, при нагріванні нітробензену з порошкоподібним КОН утворюється суміш орто- і пара-нітрофенолятів: Легше, ніж нітробензен, у реакції нуклеофільного заміщення вступає динітробензен, який при нагріванні з калій ціанідом і гідроксиламіном утворює 2, 6 -динітробензонітрил та 2, 6 -динітроанілін: 2, 6 -Динітробензонітрил 2, 6 -Динітроанілін.
Galogenuv-Sulf-Nitr.ppt