Презентация1сера cont.ppt
- Количество слайдов: 18
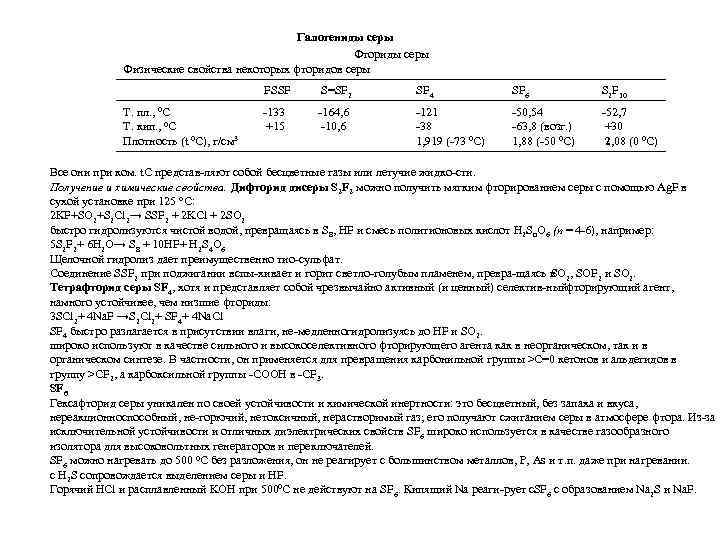 Галогениды серы Фториды серы Физические свойства некоторых фторидов серы FSSF Т. пл. , 0 C Т. кип. , 0 C Плотность (t 0 C), г/см 3 S=SF 2 SF 4 SF 6 S 2 F 10 133 +15 164, 6 10, 6 121 38 1, 919 ( 73 0 C) 50, 54 63, 8 (возг. ) 1, 88 ( 50 0 C) 52, 7 +30 2, 08 (0 0 C) Все они при ком. t. C представ ляют собой бесцветные газы или летучие жидко сти. Получение и химические свойства. Дифторид дисеры S 2 F 2 можно получить мягким фторированием серы с помощью Ag. F в сухой установке при 125 °С: 2 KF+SO 2+S 2 Cl 2→ SSF 2 + 2 KCl + 2 SO 2 быстро гидролизуются чистой водой, превращаясь в S 8, HF и смесь политионовых кислот H 2 Sn. O 6 (п = 4 6), например: 5 S 2 F 2+ 6 H 2 O→ S 8 + 10 HF+ H 2 S 4 O 6 Щелочной гидролиз дает преимущественно тио сульфат. Соединение SSF 2 при поджигании вспы хивает и горит светло голубым пламенем, превра щаясь в 2, SOF 2 и SO 2. SO Тетрафторид серы SF 4, хотя и представляет собой чрезвычайно активный (и ценный) селектив ныйфторирующий агент, намного устойчивее, чем низшие фториды: 3 SCl 2+ 4 Na. F →S 2 Cl 2+ SF 4+ 4 Na. Cl SF 4 быстро разлагается в присутствии влаги, не медленногидролизуясь до HF и SO 2. широко используют в качестве сильного и высокоселективного фторирующего агента как в неорганическом, так и в органическом синтезе. В частности, он применяется для превращения карбонильной группы >С=0 кетонов и альдегидов в группу >CF 2, а карбоксильной группы СООН в CF 3. SF 6 Гексафторид серы уникален по своей устойчивости и химической инертности: это бесцветный, без запаха и вкуса, нереакционноспособный, не горючий, нетоксичный, нерастворимый газ; его получают сжиганием серы в атмосфере фтора. Из за исключительной устойчивости и отличных диэлектрических свойств SF 6 широко используется в качестве газообразного изолятора для высоковольтных генераторов и переключателей. SF 6 можно нагревать до 500 0 C без разложения, он не реагирует с большинством металлов, Р, As и т. п. даже при нагревании. с H 2 S сопровождается выделением серы и HF. Горячий HCl и расплавленный KOH при 5000 C не действуют на SF 6. Кипящий Na реаги рует с. SF 6 с образованием Na 2 S и Na. F.
Галогениды серы Фториды серы Физические свойства некоторых фторидов серы FSSF Т. пл. , 0 C Т. кип. , 0 C Плотность (t 0 C), г/см 3 S=SF 2 SF 4 SF 6 S 2 F 10 133 +15 164, 6 10, 6 121 38 1, 919 ( 73 0 C) 50, 54 63, 8 (возг. ) 1, 88 ( 50 0 C) 52, 7 +30 2, 08 (0 0 C) Все они при ком. t. C представ ляют собой бесцветные газы или летучие жидко сти. Получение и химические свойства. Дифторид дисеры S 2 F 2 можно получить мягким фторированием серы с помощью Ag. F в сухой установке при 125 °С: 2 KF+SO 2+S 2 Cl 2→ SSF 2 + 2 KCl + 2 SO 2 быстро гидролизуются чистой водой, превращаясь в S 8, HF и смесь политионовых кислот H 2 Sn. O 6 (п = 4 6), например: 5 S 2 F 2+ 6 H 2 O→ S 8 + 10 HF+ H 2 S 4 O 6 Щелочной гидролиз дает преимущественно тио сульфат. Соединение SSF 2 при поджигании вспы хивает и горит светло голубым пламенем, превра щаясь в 2, SOF 2 и SO 2. SO Тетрафторид серы SF 4, хотя и представляет собой чрезвычайно активный (и ценный) селектив ныйфторирующий агент, намного устойчивее, чем низшие фториды: 3 SCl 2+ 4 Na. F →S 2 Cl 2+ SF 4+ 4 Na. Cl SF 4 быстро разлагается в присутствии влаги, не медленногидролизуясь до HF и SO 2. широко используют в качестве сильного и высокоселективного фторирующего агента как в неорганическом, так и в органическом синтезе. В частности, он применяется для превращения карбонильной группы >С=0 кетонов и альдегидов в группу >CF 2, а карбоксильной группы СООН в CF 3. SF 6 Гексафторид серы уникален по своей устойчивости и химической инертности: это бесцветный, без запаха и вкуса, нереакционноспособный, не горючий, нетоксичный, нерастворимый газ; его получают сжиганием серы в атмосфере фтора. Из за исключительной устойчивости и отличных диэлектрических свойств SF 6 широко используется в качестве газообразного изолятора для высоковольтных генераторов и переключателей. SF 6 можно нагревать до 500 0 C без разложения, он не реагирует с большинством металлов, Р, As и т. п. даже при нагревании. с H 2 S сопровождается выделением серы и HF. Горячий HCl и расплавленный KOH при 5000 C не действуют на SF 6. Кипящий Na реаги рует с. SF 6 с образованием Na 2 S и Na. F.
 Хлориды, бромиды и иодиды серы Сера легко хлорируется путем прямой реакции с хлором. S 2 Cl 2 — ядовитая, золотисто желтую жидкость с отвратительным запа хом (т. пл. 76 °С, т. кип. 138 °С, d 20 = 1, 677 г/см 3). Дальнейшее хлори рование. S 2 Cl 2 (желательно в присутствии следовых количеств такого катализатора, как Fe. Cl 3) дает лету чий, вишнево красный жидкийдихлорид серы SCl 2: т. пл. 122 °С, т. кип. 59 °С, d 20= 1, 621 г/см 3 SCl 2 похож на S 2 Cl 2 по своему запаху и токсичности. S 2 Cl 2, так и SCl 2 легко реагируют с водой с образованием ряда продуктов, таких как H 2 S, SO 2, H 2 SO 3, H 2 SO 4 и политионовых кислот H 2 Sx. O 6. Окисление SCl 2 дает тионилхлорид SOCl 2 и сульфурилхлорид SO 2 Cl 2. S 2 CI 2 и SCI 2 относятся к важ ным продуктам химической промышленности. Главная область применения S 2 CI 2 парофазная вулканизация некоторых видов резины; в качестве хлорирующего агента это соединение использует ся при получении моно идихлоргидринов, а так же для вскрытия некоторых минералов в гидро металлургии. Менее устойчивый гомолог. SCI 2 примечателен легкостью присоединения по двойным связям в олефинах: так, тиохлорирование этена дает известное отрав ляющее вещество кожно нарывного действия «горчичный газ» : SCl 2 + 2 CH 2=CH 2 → S(CH 2 Cl)2 Бромиды серы изучены еще хуже и надежных данных о них немного. Вероятно, SBr 2 при ком натной температуре не существует. Наиболее изученное соединение (которое также можно получить пря мым синтезом из простых веществ при 100 °С)— это гранатово красная маслянистая жидкость со става. S 2 Br 2, имеет следующие характеристики: т. пл. 46 °С, т. кип. 54 °С (при 0, 18 мм рт. ст. ) d (20 °С) = 2, 629 г/см 3; даже при комнат ной температуре. S 2 Br 2 склонен диссоциировать на бром и серу. Иодиды серы — тема, представляющая значи тельный интерес, хотя соединения, содержащие связи. S I, до последнего времени были фактичес ки неизвестны. Чистый S 2 I 2 был впервые выделен (как темное красно коричневое твердое вещество) в ходе реак ции S 2 Cl 2 со смесью HI и N 2 в фреоне в качестве растворителя при 78 °С в присутствии каталити ческого количества I 2. термически неустойчиво и быстро разлагаются при температуре выше 30 °С до S, I 2.
Хлориды, бромиды и иодиды серы Сера легко хлорируется путем прямой реакции с хлором. S 2 Cl 2 — ядовитая, золотисто желтую жидкость с отвратительным запа хом (т. пл. 76 °С, т. кип. 138 °С, d 20 = 1, 677 г/см 3). Дальнейшее хлори рование. S 2 Cl 2 (желательно в присутствии следовых количеств такого катализатора, как Fe. Cl 3) дает лету чий, вишнево красный жидкийдихлорид серы SCl 2: т. пл. 122 °С, т. кип. 59 °С, d 20= 1, 621 г/см 3 SCl 2 похож на S 2 Cl 2 по своему запаху и токсичности. S 2 Cl 2, так и SCl 2 легко реагируют с водой с образованием ряда продуктов, таких как H 2 S, SO 2, H 2 SO 3, H 2 SO 4 и политионовых кислот H 2 Sx. O 6. Окисление SCl 2 дает тионилхлорид SOCl 2 и сульфурилхлорид SO 2 Cl 2. S 2 CI 2 и SCI 2 относятся к важ ным продуктам химической промышленности. Главная область применения S 2 CI 2 парофазная вулканизация некоторых видов резины; в качестве хлорирующего агента это соединение использует ся при получении моно идихлоргидринов, а так же для вскрытия некоторых минералов в гидро металлургии. Менее устойчивый гомолог. SCI 2 примечателен легкостью присоединения по двойным связям в олефинах: так, тиохлорирование этена дает известное отрав ляющее вещество кожно нарывного действия «горчичный газ» : SCl 2 + 2 CH 2=CH 2 → S(CH 2 Cl)2 Бромиды серы изучены еще хуже и надежных данных о них немного. Вероятно, SBr 2 при ком натной температуре не существует. Наиболее изученное соединение (которое также можно получить пря мым синтезом из простых веществ при 100 °С)— это гранатово красная маслянистая жидкость со става. S 2 Br 2, имеет следующие характеристики: т. пл. 46 °С, т. кип. 54 °С (при 0, 18 мм рт. ст. ) d (20 °С) = 2, 629 г/см 3; даже при комнат ной температуре. S 2 Br 2 склонен диссоциировать на бром и серу. Иодиды серы — тема, представляющая значи тельный интерес, хотя соединения, содержащие связи. S I, до последнего времени были фактичес ки неизвестны. Чистый S 2 I 2 был впервые выделен (как темное красно коричневое твердое вещество) в ходе реак ции S 2 Cl 2 со смесью HI и N 2 в фреоне в качестве растворителя при 78 °С в присутствии каталити ческого количества I 2. термически неустойчиво и быстро разлагаются при температуре выше 30 °С до S, I 2.
 Оксиды-галогениды серы Сера образует два основных ряда оксидов галогединов (оксогалогенидов) — тионилдигалогениды SIVOХ 2 и сульфурилдигалогениды SVI 02 X 2 Тионилфториды и тионил хлориды — бесцветные летучие жидкости; OSBr 2 значительно менее летуч и име ет оранжевый цвет. Самое важное среди тионильных соединений —SOCl 2; его легко получить хлорированием SO 2 с помощью PCl 5 или в промышленном масштабе пу тем переноса атома кислорода от. SO 3 к SCl 2: S 02 + PCl 5 → SOCl 2 + OPCl 3 ; S 03 + SCl 2 →SOCl 2 + SO 2 SOCl 2 энергично реагирует с водой. Тионилхлорид начинает разлагаться выше температуры кипения (76 °С), превра щаясь в. S 2 Cl 2, SO 2 и Cl 2; поэтому его больше ис пользуют в качестве окислителя и хлорирующего реагента в органической химии. SOF 2 удобный низкотемпературный фторирующий реагент в органиче ской химии: он превращает активные группы. C H и Р Н в C F и P F и замещает N H на N S(O)F. Сульфурилгалогениды подобно тионилгалогенидам — реакционноспособные бесцветные летучие жидкости или газы. Наиболее важное соединение среди них — сульфурилхлорид SO 2 Cl 2, который получают в промышленном масштабе прямым хлорированием SO 2 Служит удобным реагентом для введения Cl или S O 2 Cl в органические соедине ния. SO 2 Cl 2 можно рассматривать как дихлорангидрид серной кислоты.
Оксиды-галогениды серы Сера образует два основных ряда оксидов галогединов (оксогалогенидов) — тионилдигалогениды SIVOХ 2 и сульфурилдигалогениды SVI 02 X 2 Тионилфториды и тионил хлориды — бесцветные летучие жидкости; OSBr 2 значительно менее летуч и име ет оранжевый цвет. Самое важное среди тионильных соединений —SOCl 2; его легко получить хлорированием SO 2 с помощью PCl 5 или в промышленном масштабе пу тем переноса атома кислорода от. SO 3 к SCl 2: S 02 + PCl 5 → SOCl 2 + OPCl 3 ; S 03 + SCl 2 →SOCl 2 + SO 2 SOCl 2 энергично реагирует с водой. Тионилхлорид начинает разлагаться выше температуры кипения (76 °С), превра щаясь в. S 2 Cl 2, SO 2 и Cl 2; поэтому его больше ис пользуют в качестве окислителя и хлорирующего реагента в органической химии. SOF 2 удобный низкотемпературный фторирующий реагент в органиче ской химии: он превращает активные группы. C H и Р Н в C F и P F и замещает N H на N S(O)F. Сульфурилгалогениды подобно тионилгалогенидам — реакционноспособные бесцветные летучие жидкости или газы. Наиболее важное соединение среди них — сульфурилхлорид SO 2 Cl 2, который получают в промышленном масштабе прямым хлорированием SO 2 Служит удобным реагентом для введения Cl или S O 2 Cl в органические соедине ния. SO 2 Cl 2 можно рассматривать как дихлорангидрид серной кислоты.
 Оксиды серы Известно, что существует по крайней мере тринад цать оксидов серы, однако это изобилие не должно затмевать того факта, что SO 2 и SO 3 наиболее устойчивы и, несомненно, самые важные в экономическом отношении. Низшие оксиды В работе Р. Штойделя и его группы показано, что, когда цикло S 10 S 9 и S 8 ра створяют в CS 2 и окисляют свежеприготовленной CF 3 C(O)OOH при температуре ниже 10 °С, дос тигается умеренный выход (10 20%) соответству ющих кристаллических монооксидов Sn 0. Анало гичное окислениецикло S 7, α- и β S 6 в CH 2 Cl 2 дает кристаллические S 7 O, S 7 O 2, а также S 6 O. S 8 O сначала (1972 г. ) был получен реакцией SOCl 2 и H 2 S 7 в CS 2 при 40 °С: это одно из наиболее ус тойчивых соединений данного ряда, оно плавится (с разложением) при 78 °С. Все эти соединения оранжевые или темно желтые и разлагаются при нагревании до комнатной температуры или немно го выше нее с выделением. SO 2 и серы. Частицы S 2 O тоже неустойчивы, но время их жиз ни в газовой фазе при давлении менее 1 мм рт. составляет уже несколько дней. Типичные спосо бы получения таковы: а) пропускание потока SOCl 2 при давлении 0, 1 0, 5 мм рт. ст. над Ag 2 S, нагретым до 160 °С; б) сжигание S 8 в потоке O 2 при давле нии ~8 ммрт. ст. ; в) пропускание SO 2 при 120 0 C и давлении менее 1 мм рт. ст. через высоковольтный (~5 к. В) электрический разряд. Оксид S 2 O легко разлагается при комнатной температуре на SO 2 и серу.
Оксиды серы Известно, что существует по крайней мере тринад цать оксидов серы, однако это изобилие не должно затмевать того факта, что SO 2 и SO 3 наиболее устойчивы и, несомненно, самые важные в экономическом отношении. Низшие оксиды В работе Р. Штойделя и его группы показано, что, когда цикло S 10 S 9 и S 8 ра створяют в CS 2 и окисляют свежеприготовленной CF 3 C(O)OOH при температуре ниже 10 °С, дос тигается умеренный выход (10 20%) соответству ющих кристаллических монооксидов Sn 0. Анало гичное окислениецикло S 7, α- и β S 6 в CH 2 Cl 2 дает кристаллические S 7 O, S 7 O 2, а также S 6 O. S 8 O сначала (1972 г. ) был получен реакцией SOCl 2 и H 2 S 7 в CS 2 при 40 °С: это одно из наиболее ус тойчивых соединений данного ряда, оно плавится (с разложением) при 78 °С. Все эти соединения оранжевые или темно желтые и разлагаются при нагревании до комнатной температуры или немно го выше нее с выделением. SO 2 и серы. Частицы S 2 O тоже неустойчивы, но время их жиз ни в газовой фазе при давлении менее 1 мм рт. составляет уже несколько дней. Типичные спосо бы получения таковы: а) пропускание потока SOCl 2 при давлении 0, 1 0, 5 мм рт. ст. над Ag 2 S, нагретым до 160 °С; б) сжигание S 8 в потоке O 2 при давле нии ~8 ммрт. ст. ; в) пропускание SO 2 при 120 0 C и давлении менее 1 мм рт. ст. через высоковольтный (~5 к. В) электрический разряд. Оксид S 2 O легко разлагается при комнатной температуре на SO 2 и серу.
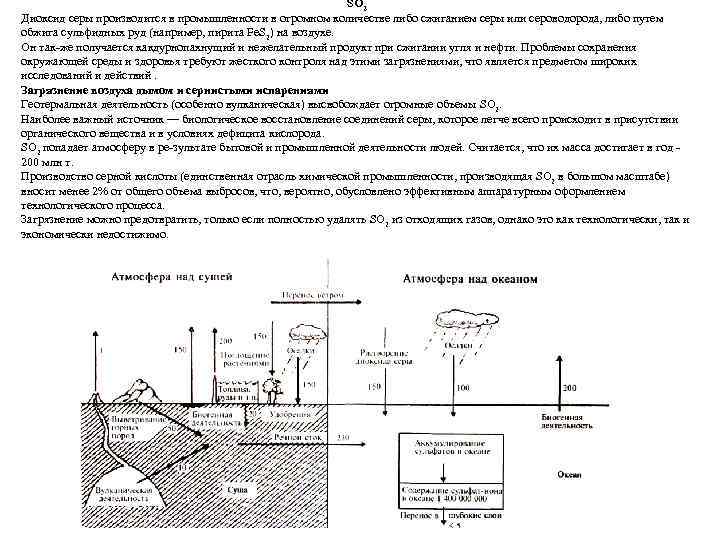 SO 2 Диоксид серы производится в промышленности в огромном количестве либо сжиганием серы или сероводорода, либо путем обжига сульфидных руд (например, пирита Fe. S 2) на воздухе. Он так же получается какдурнопахнущий и нежелательный продукт при сжигании угля и нефти. Проблемы сохранения окружающей среды и здоровья требуют жесткого контроля над этими загрязнениями, что является предметом широких исследований и действий. Загрязнение воздуха дымом и сернистыми испарениями Геотермальная деятельность (особенно вулканическая) высвобождает огромные объемы SO 2. Наиболее важный источник — биологическое восстановление соединений серы, которое легче всего происходит в присутствии органического вещества и в условиях дефицита кислорода. SO 2 попадает атмосферу в ре зультате бытовой и промышленной деятельности людей. Считается, что их масса достигает в год 200 млн т. Производство серной кислоты (единственная отрасль химической промышленности, производящая SO 2 в большом масштабе) вносит менее 2% от общего объема выбросов, что, вероятно, обусловлено эффективным аппаратурным оформлением технологического процесса. Загрязнение можно предотвратить, только если полностью удалять SO 2 из отходящих газов, однако это как технологически, так и экономически недостижимо.
SO 2 Диоксид серы производится в промышленности в огромном количестве либо сжиганием серы или сероводорода, либо путем обжига сульфидных руд (например, пирита Fe. S 2) на воздухе. Он так же получается какдурнопахнущий и нежелательный продукт при сжигании угля и нефти. Проблемы сохранения окружающей среды и здоровья требуют жесткого контроля над этими загрязнениями, что является предметом широких исследований и действий. Загрязнение воздуха дымом и сернистыми испарениями Геотермальная деятельность (особенно вулканическая) высвобождает огромные объемы SO 2. Наиболее важный источник — биологическое восстановление соединений серы, которое легче всего происходит в присутствии органического вещества и в условиях дефицита кислорода. SO 2 попадает атмосферу в ре зультате бытовой и промышленной деятельности людей. Считается, что их масса достигает в год 200 млн т. Производство серной кислоты (единственная отрасль химической промышленности, производящая SO 2 в большом масштабе) вносит менее 2% от общего объема выбросов, что, вероятно, обусловлено эффективным аппаратурным оформлением технологического процесса. Загрязнение можно предотвратить, только если полностью удалять SO 2 из отходящих газов, однако это как технологически, так и экономически недостижимо.
 Большая часть получаемого SO 2 используется в производстве серной кислоты, в качестве отбеливателя и дезинфицирующего средства, консерванта пищевых продуктов, хладагента и неводного растворителя. получение сульфитов и дитионитов синтез производных углеводородов по реакции сульфохлорирования. Диоксид серы SO 2 — бесцветный, ядовитый газ с резким запахом. Максимально допустимая 4 атмос ферная концентрация для человека 5∙ 10 %, однако многие зеленые растения получают 4%. SO не горит на воздухе и не поддерживает горение. серьезные повреждения уже при (1 2) ∙ 10 2 Наиболее важная химическая реакция SO 2 — это дальнейшее окисление до SO 3 в соответствии с рав новесием: SO 2+ O 2 → SO 3; ΔHобр = 95, 6 к. Дж/моль Константа равновесия (уравнение )быстро убывает с ростом температуры. Пропускают смесь SO 2 с воздухом над платиновой сеткой или, чаще, через контактный ка тализатор — смесь. V 2 O 5 и K 2 O, нанесенную на кизельгур или цеолит. Газообразный SO 2 хорошо растворим в воде (3927 см 3 SO 2 в 100 г H 2 O при 20 °С). Самостоятельно (ОВР в-ль, ок-ль) + реакции как кислотного оксида
Большая часть получаемого SO 2 используется в производстве серной кислоты, в качестве отбеливателя и дезинфицирующего средства, консерванта пищевых продуктов, хладагента и неводного растворителя. получение сульфитов и дитионитов синтез производных углеводородов по реакции сульфохлорирования. Диоксид серы SO 2 — бесцветный, ядовитый газ с резким запахом. Максимально допустимая 4 атмос ферная концентрация для человека 5∙ 10 %, однако многие зеленые растения получают 4%. SO не горит на воздухе и не поддерживает горение. серьезные повреждения уже при (1 2) ∙ 10 2 Наиболее важная химическая реакция SO 2 — это дальнейшее окисление до SO 3 в соответствии с рав новесием: SO 2+ O 2 → SO 3; ΔHобр = 95, 6 к. Дж/моль Константа равновесия (уравнение )быстро убывает с ростом температуры. Пропускают смесь SO 2 с воздухом над платиновой сеткой или, чаще, через контактный ка тализатор — смесь. V 2 O 5 и K 2 O, нанесенную на кизельгур или цеолит. Газообразный SO 2 хорошо растворим в воде (3927 см 3 SO 2 в 100 г H 2 O при 20 °С). Самостоятельно (ОВР в-ль, ок-ль) + реакции как кислотного оксида
 Триоксид серы SO 3 производится в огромном количестве каталитическим окислением SO 2: обычно его не выделяют, а немедленно превращают в H 2 SO 4. Его можно также получить путем термолиза сульфатов, хотя требуются доволь но высокие температуры. Ра ботать с чистым безводным. SO 3 трудно, поскольку он исключительно агрессивен и реагирует с боль шинством материалов Триоксид серы SO 3 энергично и с исключитель но большим экзотермическим эффектом реагирует с водой, образуя H 2 SO 4. Количества SO 3, превышающие стехиометрическое, дают олеум и смеси различных полисерных кислот. Галогеноводороды дают соответствующие галогеносерные кислоты состава HSO 3 X. SO 3 извлекает H 2 O из уг леводородов и других органических веществ, остав ляя углеродную основу. Активированный уголь или сульфиды металлов восстанавливают SO 3 до SO 2. Реакция с оксидами металлов (в частности с Fe 3 O 4) с образованием сульфатов используется в промышленности для удаления из отходящих газов нежелательной при меси побочного продукта. SO 3.
Триоксид серы SO 3 производится в огромном количестве каталитическим окислением SO 2: обычно его не выделяют, а немедленно превращают в H 2 SO 4. Его можно также получить путем термолиза сульфатов, хотя требуются доволь но высокие температуры. Ра ботать с чистым безводным. SO 3 трудно, поскольку он исключительно агрессивен и реагирует с боль шинством материалов Триоксид серы SO 3 энергично и с исключитель но большим экзотермическим эффектом реагирует с водой, образуя H 2 SO 4. Количества SO 3, превышающие стехиометрическое, дают олеум и смеси различных полисерных кислот. Галогеноводороды дают соответствующие галогеносерные кислоты состава HSO 3 X. SO 3 извлекает H 2 O из уг леводородов и других органических веществ, остав ляя углеродную основу. Активированный уголь или сульфиды металлов восстанавливают SO 3 до SO 2. Реакция с оксидами металлов (в частности с Fe 3 O 4) с образованием сульфатов используется в промышленности для удаления из отходящих газов нежелательной при меси побочного продукта. SO 3.
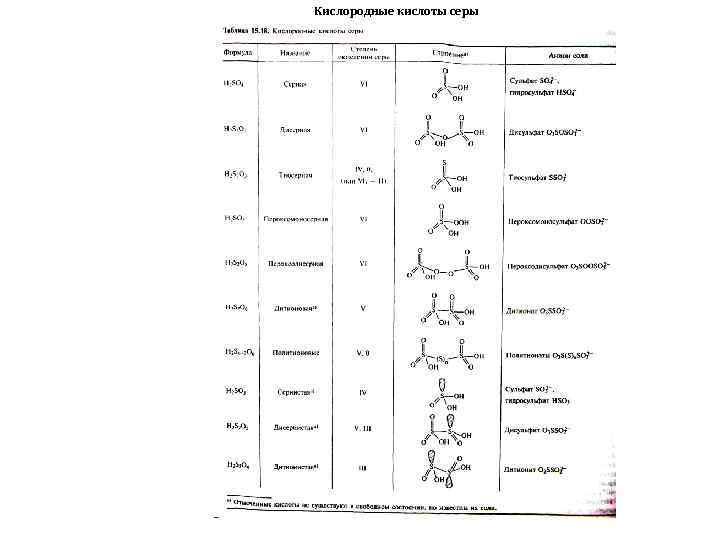 Кислородные кислоты серы
Кислородные кислоты серы
 Серная кислота H 2 SO 4 Безводная серная кислота — тяжелая, вязкая жид кость, которая легко смешивается с водой в лю бой пропорции: взаимодействие характеризуется исключительно большим экзотермическим эффек том (~880 к. Дж/ моль при бесконечном разбавле нии) и может привести к взрывному вскипанию и разбрызгиванию смеси, если воду добавлять к кис лоте; поэтому так важно всегда использовать об ратный порядок в приготовлении растворов и до бавлять кислоту в воду, медленно и при переме шивании. Применение H 2 SO 4 производство удобрений металлургия очи стка нефти краски, пигменты и полупродукты производства красителей, получение мыла и моющих средств, производство натураль ных и искусственных волокон физические свойства t плав = 10, 371, t кип≈300, с разложением, плотность – 1, 8267 Безводная H 2 SO 4 — ионная автодис социация(автопротолиз): 2 H 2 SO 4 → H 3 SO 4+ + HSO 4 K(25 0 C) = [H 3 SO+][HSO 4] = 2, 7 • 104 «чистая» безводная серная кислота в жидкой фазе — это далеко не индивидуальное ве щество, а смесь, в которой устанавливается дина мическое равновесие, включающее по меньшей мере семь вполне определенных частиц. Многие физические и химичес кие свойства безводной H 2 SO 4 как неводного ра створителя обусловлены этими равновесиями. В серной кислоте, выступающей в роли сольво системы, соединения, которые повышают концен трациюсольво иона HSO 4 , считаются основания ми, а те, которые повышают концентрацию иона. H 3 SO 4+ — кислотами. Основные растворы могут образоваться несколькими способа ми, типичные примеры таковы: а) Растворение гидросульфатов металлов: KHSO 4→ K++HSO 4 б) Сольволиз солей кислот, более слабых, чем H 2 SO 4: KNO 3 + H 2 SO 4→ K+ + HSO 4 + HNO 3 NH 4 Cl. O 4 + H 2 SO 4→ NH 4++HSO 4 + HCl. O 4 в) Протонирование соединений с неподеленной парой электронов: H 2 O + H 2 SO 4→ H 3 O+ + HSO 4 Me. COOH + H 2 SO 4→ Me. C(OH)2+ + HSO 4 г) Реакции дегидратации: HNO 3 + 2 H 2 SO 4→ NO 2+ + H 3 O+ + 2 HSO 4 Реакция с HNO 3 протекает количественно, и при сутствие в растворах. HNO 3, катиона нитроила NO 2+ в высокой концентрации позволяет объяснить детали механизма нитрова ния ароматических углеводородов с помощью этих растворов.
Серная кислота H 2 SO 4 Безводная серная кислота — тяжелая, вязкая жид кость, которая легко смешивается с водой в лю бой пропорции: взаимодействие характеризуется исключительно большим экзотермическим эффек том (~880 к. Дж/ моль при бесконечном разбавле нии) и может привести к взрывному вскипанию и разбрызгиванию смеси, если воду добавлять к кис лоте; поэтому так важно всегда использовать об ратный порядок в приготовлении растворов и до бавлять кислоту в воду, медленно и при переме шивании. Применение H 2 SO 4 производство удобрений металлургия очи стка нефти краски, пигменты и полупродукты производства красителей, получение мыла и моющих средств, производство натураль ных и искусственных волокон физические свойства t плав = 10, 371, t кип≈300, с разложением, плотность – 1, 8267 Безводная H 2 SO 4 — ионная автодис социация(автопротолиз): 2 H 2 SO 4 → H 3 SO 4+ + HSO 4 K(25 0 C) = [H 3 SO+][HSO 4] = 2, 7 • 104 «чистая» безводная серная кислота в жидкой фазе — это далеко не индивидуальное ве щество, а смесь, в которой устанавливается дина мическое равновесие, включающее по меньшей мере семь вполне определенных частиц. Многие физические и химичес кие свойства безводной H 2 SO 4 как неводного ра створителя обусловлены этими равновесиями. В серной кислоте, выступающей в роли сольво системы, соединения, которые повышают концен трациюсольво иона HSO 4 , считаются основания ми, а те, которые повышают концентрацию иона. H 3 SO 4+ — кислотами. Основные растворы могут образоваться несколькими способа ми, типичные примеры таковы: а) Растворение гидросульфатов металлов: KHSO 4→ K++HSO 4 б) Сольволиз солей кислот, более слабых, чем H 2 SO 4: KNO 3 + H 2 SO 4→ K+ + HSO 4 + HNO 3 NH 4 Cl. O 4 + H 2 SO 4→ NH 4++HSO 4 + HCl. O 4 в) Протонирование соединений с неподеленной парой электронов: H 2 O + H 2 SO 4→ H 3 O+ + HSO 4 Me. COOH + H 2 SO 4→ Me. C(OH)2+ + HSO 4 г) Реакции дегидратации: HNO 3 + 2 H 2 SO 4→ NO 2+ + H 3 O+ + 2 HSO 4 Реакция с HNO 3 протекает количественно, и при сутствие в растворах. HNO 3, катиона нитроила NO 2+ в высокой концентрации позволяет объяснить детали механизма нитрова ния ароматических углеводородов с помощью этих растворов.
 Серная кислота образует соли (сульфаты и гидросульфаты) со многими металлами. Часто они очень устойчивы, и фактически они являются наиболее важными минералами некоторых наиболее электроположительных элементов. Могут быть получены следующими способами: а) химическое растворение металлов (например, Fe) в водном растворе H 2 SO 4; б) нейтрализация H 2 SO 4 B водном растворе ок сидами илигидроксидами металлов (например, МОН); в) разложение солей летучих кислот (например, карбонатов) водной H 2 SO 4; г) обменная реакция между растворимым сульфатом и растворимой солью металла, нерастворимый сульфат которого хотят получить (например, Ba. SO 4); д) окисление сульфидов и сульфитов металлов. Самостоятельно добавить про свойства серной кислоты
Серная кислота образует соли (сульфаты и гидросульфаты) со многими металлами. Часто они очень устойчивы, и фактически они являются наиболее важными минералами некоторых наиболее электроположительных элементов. Могут быть получены следующими способами: а) химическое растворение металлов (например, Fe) в водном растворе H 2 SO 4; б) нейтрализация H 2 SO 4 B водном растворе ок сидами илигидроксидами металлов (например, МОН); в) разложение солей летучих кислот (например, карбонатов) водной H 2 SO 4; г) обменная реакция между растворимым сульфатом и растворимой солью металла, нерастворимый сульфат которого хотят получить (например, Ba. SO 4); д) окисление сульфидов и сульфитов металлов. Самостоятельно добавить про свойства серной кислоты
 Тиосерная кислота H 2 S 2 O 3 Попытки получить тиосерную кислоту подкислением устойчивых тиосульфатов несомненно безус пешны из за быстрого разложения свободной кис лоты в присутствии воды. Успешные синтезы в безводной среде были проведены М. Шмидтом и его сотрудниками в 1959 1961 гг. , : H 2 S + SO 3→ H 2 S 2 O 3 ∙n. Et 2 O в присутствии эфира при — 78 С Na 2 S 2 O 3 + 2 HCl → 2 Na. Cl + H 2 S 2 O 3 • 2 Et 2 O в присутствии эфира при — 78 С В отличие от свободной кислоты устойчивые соли тиосульфаты могут быть легко получены вза имодействием. H 2 S и сульфитов в водном растворе: 2 HS +4 HSO 3 → 3 S 2 O 32 + 3 H 2 O Тио сульфат можно также получить кипячением водного раствора сульфита или гидросульфита металла с порошком серы в соответствии со стехиометрией: Na 2 SO 3 + S 8 → Na 2 S 2 O 3 вода, 100 С Окисление на воздухе полисульфидов — альтернативный способ получения тиосульфата в промыш ленности: Na 2 S 5 + 3/2 O 2 → Na 2 S 2 O 3 + 3/x Sx Ca. S 2 + O 2 → Ca. S 2 O 3 Гидратированный тиосульфат натрия (гипосульфит) состава Na 2 S 2 O 3 • 5 H 2 O образует большие бес цветные, прозрачные кристаллы (т. пл. 48, 5 °С); он хорошо растворим в воде и используется в фото графии ( «фиксаж» ) для растворения (за счетком плексообразования) непрореагировавшего Ag. Br в фотоэмульсии: Ag. Br + 3 Na 2 S 2 O 3 → Na 5[Ag(S 2 O 3)3] + Na. Br Тиосульфат ион — восстановитель умеренной силы, S 4 O 62+ + 2 е → 2 S 2 O 32 ; E 0 = 0, 169 В Количественное окисление S 2 O 32 с помощью I 2 c образованием тетратионата и иодида служит основой иодометрического титрования в объемном хи мическом анализе: 2 2 O 32 + I 2 →S 4 O 62 + 2 I S Более сильные окислители превращают тиосульфаты в сульфаты: S 2 O 32 + 4 Cl 2 + 5 H 2 O → 2 HSO 4 +8 Н++8 Сl На этой реакции основано применение тиосульфатов в качестве «антихлора» в процессах отбели вания, где они служат для удаления избытка. Cl 2 из волокон.
Тиосерная кислота H 2 S 2 O 3 Попытки получить тиосерную кислоту подкислением устойчивых тиосульфатов несомненно безус пешны из за быстрого разложения свободной кис лоты в присутствии воды. Успешные синтезы в безводной среде были проведены М. Шмидтом и его сотрудниками в 1959 1961 гг. , : H 2 S + SO 3→ H 2 S 2 O 3 ∙n. Et 2 O в присутствии эфира при — 78 С Na 2 S 2 O 3 + 2 HCl → 2 Na. Cl + H 2 S 2 O 3 • 2 Et 2 O в присутствии эфира при — 78 С В отличие от свободной кислоты устойчивые соли тиосульфаты могут быть легко получены вза имодействием. H 2 S и сульфитов в водном растворе: 2 HS +4 HSO 3 → 3 S 2 O 32 + 3 H 2 O Тио сульфат можно также получить кипячением водного раствора сульфита или гидросульфита металла с порошком серы в соответствии со стехиометрией: Na 2 SO 3 + S 8 → Na 2 S 2 O 3 вода, 100 С Окисление на воздухе полисульфидов — альтернативный способ получения тиосульфата в промыш ленности: Na 2 S 5 + 3/2 O 2 → Na 2 S 2 O 3 + 3/x Sx Ca. S 2 + O 2 → Ca. S 2 O 3 Гидратированный тиосульфат натрия (гипосульфит) состава Na 2 S 2 O 3 • 5 H 2 O образует большие бес цветные, прозрачные кристаллы (т. пл. 48, 5 °С); он хорошо растворим в воде и используется в фото графии ( «фиксаж» ) для растворения (за счетком плексообразования) непрореагировавшего Ag. Br в фотоэмульсии: Ag. Br + 3 Na 2 S 2 O 3 → Na 5[Ag(S 2 O 3)3] + Na. Br Тиосульфат ион — восстановитель умеренной силы, S 4 O 62+ + 2 е → 2 S 2 O 32 ; E 0 = 0, 169 В Количественное окисление S 2 O 32 с помощью I 2 c образованием тетратионата и иодида служит основой иодометрического титрования в объемном хи мическом анализе: 2 2 O 32 + I 2 →S 4 O 62 + 2 I S Более сильные окислители превращают тиосульфаты в сульфаты: S 2 O 32 + 4 Cl 2 + 5 H 2 O → 2 HSO 4 +8 Н++8 Сl На этой реакции основано применение тиосульфатов в качестве «антихлора» в процессах отбели вания, где они служат для удаления избытка. Cl 2 из волокон.
 Дитионовая кислота H 2 S 2 O 6 В дитионовой кислоте и дитионат ионе S 2 O 6 степень окисления двух атомов серы уменьшается с VI до V за счет образования связи S S. Свободная кислота в чистом виде не получена, однако можно приготовить ее довольно концентрированные водные растворы, обрабатывая дитионат бария стехиометрическим количе ством серной кислоты: Ba. S 2 O 6 + H 2 S 04 →H 2 S 2 O 6 + Ba. SO 4 Кристаллические дитионаты термически устойчивы при температуре выше комнатной (например, K 2 S 2 O 6 разлагается при 258 °С до K 2 SO 4 и SO 2). Обычно их получают окислением соответствующих сульфитов. В промышленных условиях водные растворы SO 2 окисляют с помощью суспензии гидратированного Mn. O 2 или Fe 2 O 3: 2 Mn. O 2+ 3 SO 2 → Mn. SO 4+ Mn. S 2 O 6 вода 0 С Fe 2 O 3+ 3 SO 2 →{Fe 2 III(S 03)3} →Fe 11 SO 3 + Fe 11 S 2 O 6 Все дитионаты хорошо растворимы в воде и мо гут быть получены обычными реакциями обмена. Дитионаты относительно устойчивы к окислению в растворе, хотя сильные окислители, такие как га логены, дихромат ион и перманганат ион, окисляют их до сульфатов. Сильные восстановители (напри мер, амальгама натрия. Na/Hg) восстанавливают ди тионатыдо сульфитов и дитионитов S 2 O 42.
Дитионовая кислота H 2 S 2 O 6 В дитионовой кислоте и дитионат ионе S 2 O 6 степень окисления двух атомов серы уменьшается с VI до V за счет образования связи S S. Свободная кислота в чистом виде не получена, однако можно приготовить ее довольно концентрированные водные растворы, обрабатывая дитионат бария стехиометрическим количе ством серной кислоты: Ba. S 2 O 6 + H 2 S 04 →H 2 S 2 O 6 + Ba. SO 4 Кристаллические дитионаты термически устойчивы при температуре выше комнатной (например, K 2 S 2 O 6 разлагается при 258 °С до K 2 SO 4 и SO 2). Обычно их получают окислением соответствующих сульфитов. В промышленных условиях водные растворы SO 2 окисляют с помощью суспензии гидратированного Mn. O 2 или Fe 2 O 3: 2 Mn. O 2+ 3 SO 2 → Mn. SO 4+ Mn. S 2 O 6 вода 0 С Fe 2 O 3+ 3 SO 2 →{Fe 2 III(S 03)3} →Fe 11 SO 3 + Fe 11 S 2 O 6 Все дитионаты хорошо растворимы в воде и мо гут быть получены обычными реакциями обмена. Дитионаты относительно устойчивы к окислению в растворе, хотя сильные окислители, такие как га логены, дихромат ион и перманганат ион, окисляют их до сульфатов. Сильные восстановители (напри мер, амальгама натрия. Na/Hg) восстанавливают ди тионатыдо сульфитов и дитионитов S 2 O 42.
 Политионовые кислоты H 2 Sn. O 6 Многочисленные кислоты и соли этой группы имеют почтенную историю, а химия систем, в которых они существуют, восходит к исследованиям Джона Дальтона, посвященным поведению H 2 S в водных растворах SO 2 (1808 г. ). Такие растворы сейчас носят имя Г. Вакенродера (жидкость Вакен родера), который провел их систематическое изу чение (1846 г. ). В течение последующих 60 80 лет исследования показали присутствие многочисленных ионов, в частности тетратионат и пентатио нат ионов (S 4 O 62 и S 5 O 62 соответственно). В последние несколько десятилетий в результате работ Г. Шмидта и других ученых в Германии сформи ровалось новое представление: как. H 2 S может реагировать с SO 3 или HSO 3 Cl, образуя тиосерную кислоту H 2 S 2 O 3, так же в аналогичной реак ции с. H 2 S 2 образуется «дисульфанмоносульфоновая кислота» HS 2 SO 3 H; подобным образом полисульфаны H 2 Sn (и = 2 6) дают HSn. S 03 H. Реакции с обоих концов полисульфановой цепи приводят к образованию «полисульфандисульфоновых кислот» HO 3 SSn. SO 3 H которые чаще назвают политионовы ми кислотами (H 2 Sn+2 O 6). Известно много способов синтеза этих кислот. Типичные примеры таковы: а) Взаимодействие H 2 S и SO 2 B растворе Вакен родера. б) Реакции хлорсульфанов с HSO 3 или HS 2 O 3 , например: SCl 2 + 2 HSO 3 → [O 3 SSSO 3]2 + 2 HCl S 2 Cl 2 + 2 HSO 3 → [O 3 SS 2 SO 3]2 + 2 HCl SCl 2+ 2 HS 2 O 3 → [O 3 SS 3 SO 3]2 + 2 HCl и т. д. в) Окисление тиосульфатов мягкими окислите лями, такими как. I 2, Cu. II, S 2 O 82 , H 2 O 2. г) Специальные методы синтеза, отмеченные далее. Тритионат натрия Na 2 S 3 O 6 можно получить окис лением тиосульфата холодным раствором. H 2 O 2: 2 Na 2 S 2 O 3 + 4 H 2 O 2 → Na 2 S 3 O 6 +Na 2 SO 4+ 4 H 2 O Калийную (но не натриевую) соль получают по странной реакции SO 2 C тиосульфатом в водном растворе. Водные растворы кислоты H 2 S 3 O 6 мож но получить из. K 2 S 3 O 6 путем обработки винной или хлорной кислотой. Тетратионат натрия (и калия) M 2 S 4 O 6, может быть получен окислением тиосульфата с помощью I 2 , а сама кислота в свободном состоянии (в водном растворе) получается при добавлении стехиометрического количества винной кислоты. Пентатионат калия K 2 S 5 O 6 можно получить до бавлением ацетата калия к жидкости. Вакенродера, а раствор кислоты H 2 S 5 O 6 образуется при последую щем добавлении винной кислоты. Гексатионат калия K 2 S 6 O 6 лучше всего синтези ровать действием. KNO 2 на K 2 S 2 O 3 в концентриро ванной. HCl при низких температурах, хотя гекса тионат ион присутствует также в жидкости Вакен родера Безводные политионовые кислоты могут. быть получены в эфирном растворе следующими тремя общими способами: HSn. S 03 H + SO 3 → H 2 Sn+206 (n + 2 = 3, 4, 5, 6, 7, 8) H 2 Sn+2 SO 3 → H 2 Sn+2 O 6 (n +2 = 3, 4, 5, 6, 7, 8) 2 HSn. S 03 H+ I 2 → H 2 S 2 n+2 O 6 + 2 HI (2 n + 2 = 4, 6, 8, 10, 12, 14)
Политионовые кислоты H 2 Sn. O 6 Многочисленные кислоты и соли этой группы имеют почтенную историю, а химия систем, в которых они существуют, восходит к исследованиям Джона Дальтона, посвященным поведению H 2 S в водных растворах SO 2 (1808 г. ). Такие растворы сейчас носят имя Г. Вакенродера (жидкость Вакен родера), который провел их систематическое изу чение (1846 г. ). В течение последующих 60 80 лет исследования показали присутствие многочисленных ионов, в частности тетратионат и пентатио нат ионов (S 4 O 62 и S 5 O 62 соответственно). В последние несколько десятилетий в результате работ Г. Шмидта и других ученых в Германии сформи ровалось новое представление: как. H 2 S может реагировать с SO 3 или HSO 3 Cl, образуя тиосерную кислоту H 2 S 2 O 3, так же в аналогичной реак ции с. H 2 S 2 образуется «дисульфанмоносульфоновая кислота» HS 2 SO 3 H; подобным образом полисульфаны H 2 Sn (и = 2 6) дают HSn. S 03 H. Реакции с обоих концов полисульфановой цепи приводят к образованию «полисульфандисульфоновых кислот» HO 3 SSn. SO 3 H которые чаще назвают политионовы ми кислотами (H 2 Sn+2 O 6). Известно много способов синтеза этих кислот. Типичные примеры таковы: а) Взаимодействие H 2 S и SO 2 B растворе Вакен родера. б) Реакции хлорсульфанов с HSO 3 или HS 2 O 3 , например: SCl 2 + 2 HSO 3 → [O 3 SSSO 3]2 + 2 HCl S 2 Cl 2 + 2 HSO 3 → [O 3 SS 2 SO 3]2 + 2 HCl SCl 2+ 2 HS 2 O 3 → [O 3 SS 3 SO 3]2 + 2 HCl и т. д. в) Окисление тиосульфатов мягкими окислите лями, такими как. I 2, Cu. II, S 2 O 82 , H 2 O 2. г) Специальные методы синтеза, отмеченные далее. Тритионат натрия Na 2 S 3 O 6 можно получить окис лением тиосульфата холодным раствором. H 2 O 2: 2 Na 2 S 2 O 3 + 4 H 2 O 2 → Na 2 S 3 O 6 +Na 2 SO 4+ 4 H 2 O Калийную (но не натриевую) соль получают по странной реакции SO 2 C тиосульфатом в водном растворе. Водные растворы кислоты H 2 S 3 O 6 мож но получить из. K 2 S 3 O 6 путем обработки винной или хлорной кислотой. Тетратионат натрия (и калия) M 2 S 4 O 6, может быть получен окислением тиосульфата с помощью I 2 , а сама кислота в свободном состоянии (в водном растворе) получается при добавлении стехиометрического количества винной кислоты. Пентатионат калия K 2 S 5 O 6 можно получить до бавлением ацетата калия к жидкости. Вакенродера, а раствор кислоты H 2 S 5 O 6 образуется при последую щем добавлении винной кислоты. Гексатионат калия K 2 S 6 O 6 лучше всего синтези ровать действием. KNO 2 на K 2 S 2 O 3 в концентриро ванной. HCl при низких температурах, хотя гекса тионат ион присутствует также в жидкости Вакен родера Безводные политионовые кислоты могут. быть получены в эфирном растворе следующими тремя общими способами: HSn. S 03 H + SO 3 → H 2 Sn+206 (n + 2 = 3, 4, 5, 6, 7, 8) H 2 Sn+2 SO 3 → H 2 Sn+2 O 6 (n +2 = 3, 4, 5, 6, 7, 8) 2 HSn. S 03 H+ I 2 → H 2 S 2 n+2 O 6 + 2 HI (2 n + 2 = 4, 6, 8, 10, 12, 14)
 Сернистая кислота H 2 SO 3 Сернистая кислота никогда не была получена в чистом виде. Ее соли — сульфиты вполне устойчивы и многие из них известны в кристаллической форме; второй ряд солей, гидросульфиты (HSO 3 ), существуют в растворах. Недиссоциированная кислота H 2 SO 3 не была обнаружена: Первую константу диссоциации для «сернистой кислоты» в водном растворе определяют так: SO 2 ∙ n H 2 O → H 3 O+(aq) + HSO 3 (aq) K 1 (25 0 C) = 1, 6∙ 10 2 Вторая константа диссоциации рассчитывается по уравнению: HSO 3 (aq) → H 3 O+(aq) + SO 32 (aq); K 2(25 °С) = 1, 0∙ 1 0 7 K = [H 30+][S 032 ]/[HSO 3 ] Большинство сульфитов (за исключением производных щелочных металлов и аммония) практически нерастворимы. Сульфиты и гидросульфиты — восстановители умеренной силы и в зависимости от условий окисляются до дитионатов или до сульфатов. Реакция с иодом протекает количественно и при меняется в объемном анализе: HSO 3 +I 2 + H 2 O → HSO 4 + 2 Н+ + 2 I B то же время в присутствии сильных восстановителей сульфиты могут вести себя как окислители; так, амальгама натрия превращает их в дитиониты, а формиаты, окисляясь до оксалатов, превращают сульфиты в тиосульфаты: 2 SO 32 + 2 H 2 O + 2 Na/Hg → S 2 O 42 + 140 Н + 2 Na+ 2 SO 32 + 4 HCO 2 → SSO 32 + 2 C 2 O 42 + 20 Н + H 2 O При восстановлении SO 3 и HSO 3 элементарной серой также образуются тиосульфаты, в то время как восстановление с помощью H 2 S в жидкости Вакенродера дает политионаты. В промышленности растворы гидросульфита натрия получают пропусканием SO 2 в растворы Na 2 CO 3. Мировое производ ство безводной соли превышает 1 млн т в год; большую часть ее потребляет целлюлозо бумажная промышленность, другие области применения — удаление примеси кислорода при обработке воды для котлов, восстановитель в фотографии.
Сернистая кислота H 2 SO 3 Сернистая кислота никогда не была получена в чистом виде. Ее соли — сульфиты вполне устойчивы и многие из них известны в кристаллической форме; второй ряд солей, гидросульфиты (HSO 3 ), существуют в растворах. Недиссоциированная кислота H 2 SO 3 не была обнаружена: Первую константу диссоциации для «сернистой кислоты» в водном растворе определяют так: SO 2 ∙ n H 2 O → H 3 O+(aq) + HSO 3 (aq) K 1 (25 0 C) = 1, 6∙ 10 2 Вторая константа диссоциации рассчитывается по уравнению: HSO 3 (aq) → H 3 O+(aq) + SO 32 (aq); K 2(25 °С) = 1, 0∙ 1 0 7 K = [H 30+][S 032 ]/[HSO 3 ] Большинство сульфитов (за исключением производных щелочных металлов и аммония) практически нерастворимы. Сульфиты и гидросульфиты — восстановители умеренной силы и в зависимости от условий окисляются до дитионатов или до сульфатов. Реакция с иодом протекает количественно и при меняется в объемном анализе: HSO 3 +I 2 + H 2 O → HSO 4 + 2 Н+ + 2 I B то же время в присутствии сильных восстановителей сульфиты могут вести себя как окислители; так, амальгама натрия превращает их в дитиониты, а формиаты, окисляясь до оксалатов, превращают сульфиты в тиосульфаты: 2 SO 32 + 2 H 2 O + 2 Na/Hg → S 2 O 42 + 140 Н + 2 Na+ 2 SO 32 + 4 HCO 2 → SSO 32 + 2 C 2 O 42 + 20 Н + H 2 O При восстановлении SO 3 и HSO 3 элементарной серой также образуются тиосульфаты, в то время как восстановление с помощью H 2 S в жидкости Вакенродера дает политионаты. В промышленности растворы гидросульфита натрия получают пропусканием SO 2 в растворы Na 2 CO 3. Мировое производ ство безводной соли превышает 1 млн т в год; большую часть ее потребляет целлюлозо бумажная промышленность, другие области применения — удаление примеси кислорода при обработке воды для котлов, восстановитель в фотографии.
 Дисернистая кислота H 2 S 2 O 5 Подобно «сернистой кислоте» дисернистая неизвестна ни в свободном состоянии, ни в растворе. Ее соли легко получить из концентрированых растворов гидросульфитов: HSO 3 → S 2 O 52 + H 2 O. В отличие от дисульфатов дисульфиты образуются за счет формирования связи S S. Подкисление растворов дисульфитов приводит к регенерации HSO 3 и SO 2, и химические свойства S 2 O 5 в растворе практически такие же, как свойства сульфитов и гидросульфитов, несмотря на формальное присутствие Sv и SIII (а не SIV) в твердом состоянии. Дитионистая кислота H 2 S 2 O 4 Дитиониты S 2 O 42 вполне устойчивы в безводном состоянии, но в присутствии воды они диспропор ционируют (медленно при р. Н ≥ 7, быстро в кислом растворе): III IV II/VI 2 + H O → 2 HSO +SSO 2 2 S 2 O 4 2 3 3 Дитионистая кислота не существует в индивиду альном состоянии и вообще не обнаружена вводном растворе. Дитионит натрия широко используется как промышленный восстановитель и может быть получен восстановлением сульфита цинковой пылью, амальгамой натрия или электролитически, например: IV IV IV III HSO 3 + SO 2 n H 2 O + Zn →Zn. SO 3 + Zn. S 2 O 4 + (n+2) H 2 O Важнейшее применение дитионитов — в качестве восстановителей в крашении, отбеливание бумажной массы, соломы, глины, мыла и т. п. и в химических реак циях восстановления Мировое произ водство около 300 тыс т в год. Дитиониты — сильные восстановители, они вос станавливают растворенный. O 2, H 2 O 2, IO 3 и Mn. O 4 Подобным образом Cr. VI восстанавливается до Cr. III и Ti. O 2+ до Ti. III. Ионы тяжелых металлов, такие как Cu , Ag 1, Pb 11, Sb. III и Bi. III , восстанавли ваются до металлов. Многие из этих реакций при меняются в процессах обработки воды и контроля за загрязнениями.
Дисернистая кислота H 2 S 2 O 5 Подобно «сернистой кислоте» дисернистая неизвестна ни в свободном состоянии, ни в растворе. Ее соли легко получить из концентрированых растворов гидросульфитов: HSO 3 → S 2 O 52 + H 2 O. В отличие от дисульфатов дисульфиты образуются за счет формирования связи S S. Подкисление растворов дисульфитов приводит к регенерации HSO 3 и SO 2, и химические свойства S 2 O 5 в растворе практически такие же, как свойства сульфитов и гидросульфитов, несмотря на формальное присутствие Sv и SIII (а не SIV) в твердом состоянии. Дитионистая кислота H 2 S 2 O 4 Дитиониты S 2 O 42 вполне устойчивы в безводном состоянии, но в присутствии воды они диспропор ционируют (медленно при р. Н ≥ 7, быстро в кислом растворе): III IV II/VI 2 + H O → 2 HSO +SSO 2 2 S 2 O 4 2 3 3 Дитионистая кислота не существует в индивиду альном состоянии и вообще не обнаружена вводном растворе. Дитионит натрия широко используется как промышленный восстановитель и может быть получен восстановлением сульфита цинковой пылью, амальгамой натрия или электролитически, например: IV IV IV III HSO 3 + SO 2 n H 2 O + Zn →Zn. SO 3 + Zn. S 2 O 4 + (n+2) H 2 O Важнейшее применение дитионитов — в качестве восстановителей в крашении, отбеливание бумажной массы, соломы, глины, мыла и т. п. и в химических реак циях восстановления Мировое произ водство около 300 тыс т в год. Дитиониты — сильные восстановители, они вос станавливают растворенный. O 2, H 2 O 2, IO 3 и Mn. O 4 Подобным образом Cr. VI восстанавливается до Cr. III и Ti. O 2+ до Ti. III. Ионы тяжелых металлов, такие как Cu , Ag 1, Pb 11, Sb. III и Bi. III , восстанавли ваются до металлов. Многие из этих реакций при меняются в процессах обработки воды и контроля за загрязнениями.
 Соединения серы с азотом Исследование соединений серы с азотом — одна из наиболее активно развивающихся в настоящее время областей неорганической химии: получено множество новых циклических и ациклических соединений, которые имеют необычную структуру и порождают большие проблемы в применении к ним простой теории химической связи. В 1975 г. было обнаружено, что полимер (SN)x ведет себя как металл, электропроводность которого повышается с понижением температуры, и который становится сверхпроводником ниже 0, 33 К. Соединение S 4 N 4 впервые было получено в неочищенном виде У. Грегори в 1835 г. Другие важные соединения со связями S N, от крытие которых датируется первой половиной. XIX — это сульфаминовая кислота H[H 2 NSO 3], имидосульфоновая кислота HSO 3 N=NH, сульфа мид. SO 2(NН 2)2, нитрилтрисульфоновая кислота N(HSO 3)3, гидроксонитрилсульфоновые кислоты HSO 3 NH(OH) и (HSO 3)2 N(OH) и их многочисленные производные Бинарные нитриды серы a) Teтpaнитрид тетрасеры S 4 N 4 Это наиболее легко получаемый нитрид серы, он служит исходным реагентом для получения многих соединений серы с азотом. Эти оранжево желтые устойчивые на воздухе кристаллы получают пропусканием га зообразного аммиака в теплый раствор S 2 Cl 2 (или SCl 2) в CCl 4 или бензоле; суммарная стехиометрия 6 S 2 Cl 2+ 16 NH 3 → S 4 N 4+ 8 S+ 12 NH 4 Cl 6 SCl 2 + 16 NH 3 → S 4 N 4 + 2 S + 14 NH 4 Cl По другому способу можно нагревать смесь NH 4 CI и S 2 Cl 2 при 160 0 C: 6 S 2 Cl 2+ 4 NH 4 Cl → S 4 N 4+ 8 S+ 16 HCl выход 26 % Это соединение также получается в обратимой равновесной реакции серы с безводным жидким ам миаком: 10 4 NH 3 → S+ S 4 N 4+ 6 H 2 S S 4 N 4 устойчив на воздухе, и может взорваться при ударе или быстром нагревании. S 4 N 4 нерастворим в воде и не реагирует с ней, но легко подвергается щелочному гидролизу под дей ствием разбавленного раствора Na. OH, превращаясь в тиосульфат ион, тритионат ион и аммиак: 2 S 4 N 4+ 6 OH + 9 H 2 O → S 2 O 32 + 2 S 3 O 62 + 8 NH 3 Более концентрированные щелочи дают вместо тритионат иона сульфит ион: S 4 N 4 + 60 Н + 3 H 2 O → S 2 O 32 + 2 SO 32 + 4 NH 3
Соединения серы с азотом Исследование соединений серы с азотом — одна из наиболее активно развивающихся в настоящее время областей неорганической химии: получено множество новых циклических и ациклических соединений, которые имеют необычную структуру и порождают большие проблемы в применении к ним простой теории химической связи. В 1975 г. было обнаружено, что полимер (SN)x ведет себя как металл, электропроводность которого повышается с понижением температуры, и который становится сверхпроводником ниже 0, 33 К. Соединение S 4 N 4 впервые было получено в неочищенном виде У. Грегори в 1835 г. Другие важные соединения со связями S N, от крытие которых датируется первой половиной. XIX — это сульфаминовая кислота H[H 2 NSO 3], имидосульфоновая кислота HSO 3 N=NH, сульфа мид. SO 2(NН 2)2, нитрилтрисульфоновая кислота N(HSO 3)3, гидроксонитрилсульфоновые кислоты HSO 3 NH(OH) и (HSO 3)2 N(OH) и их многочисленные производные Бинарные нитриды серы a) Teтpaнитрид тетрасеры S 4 N 4 Это наиболее легко получаемый нитрид серы, он служит исходным реагентом для получения многих соединений серы с азотом. Эти оранжево желтые устойчивые на воздухе кристаллы получают пропусканием га зообразного аммиака в теплый раствор S 2 Cl 2 (или SCl 2) в CCl 4 или бензоле; суммарная стехиометрия 6 S 2 Cl 2+ 16 NH 3 → S 4 N 4+ 8 S+ 12 NH 4 Cl 6 SCl 2 + 16 NH 3 → S 4 N 4 + 2 S + 14 NH 4 Cl По другому способу можно нагревать смесь NH 4 CI и S 2 Cl 2 при 160 0 C: 6 S 2 Cl 2+ 4 NH 4 Cl → S 4 N 4+ 8 S+ 16 HCl выход 26 % Это соединение также получается в обратимой равновесной реакции серы с безводным жидким ам миаком: 10 4 NH 3 → S+ S 4 N 4+ 6 H 2 S S 4 N 4 устойчив на воздухе, и может взорваться при ударе или быстром нагревании. S 4 N 4 нерастворим в воде и не реагирует с ней, но легко подвергается щелочному гидролизу под дей ствием разбавленного раствора Na. OH, превращаясь в тиосульфат ион, тритионат ион и аммиак: 2 S 4 N 4+ 6 OH + 9 H 2 O → S 2 O 32 + 2 S 3 O 62 + 8 NH 3 Более концентрированные щелочи дают вместо тритионат иона сульфит ион: S 4 N 4 + 60 Н + 3 H 2 O → S 2 O 32 + 2 SO 32 + 4 NH 3
 б) Динитрид дисеры S 2 N 2 Если S 4 N 4 осторожно подвергать деполимеризации. Серебро применяет ся для удаления серы, образующейся при термичес ком разложении. S 4 N 4; при этом получается Ag 2 S, который служит катализатором образования S 2 N 2: S 4 N 4 + 8 Ag → 4 Ag 2 S + 2 N 2 S 4 N 4 → 2 S 2 N 2 в присутствии Ag 2 S S 2 N 2 образует крупные бесцветные кристаллы, нерастворимые в воде, но растворимые во многих органических растворителях. S 2 N 2 разлагается со взрывом при ударе или при нагревании выше 30 °С. Поэтому химические свойства этого соединения изучены еще недостаточно. Наиболее интересная реакция S 2 N 2 — это медленная самопроизвольная полимеризация в твердом состоянии при комнатной тем пературе с образованием кристаллического(SN)x. Политиазил (SN)x – полимерный нитрид серы, известный как политиазил, впервые был по лучен Ф. Буртом в 1910 г. К 1973 г. было установлено, что (SN)x действительно превращается в металл ниже тем пературы жидкого гелия, а в 1975 г. было показа но, что полимер становится сверхпроводником ниже 0, 26 К. (SN)x значительно более устойчив, чем его пред шественник. S 2 N 2. При нагревании на воздухе он разлагается со взрывом при ~240°С, однако в вакууме легко возгоняется при температуре около 135 °С.
б) Динитрид дисеры S 2 N 2 Если S 4 N 4 осторожно подвергать деполимеризации. Серебро применяет ся для удаления серы, образующейся при термичес ком разложении. S 4 N 4; при этом получается Ag 2 S, который служит катализатором образования S 2 N 2: S 4 N 4 + 8 Ag → 4 Ag 2 S + 2 N 2 S 4 N 4 → 2 S 2 N 2 в присутствии Ag 2 S S 2 N 2 образует крупные бесцветные кристаллы, нерастворимые в воде, но растворимые во многих органических растворителях. S 2 N 2 разлагается со взрывом при ударе или при нагревании выше 30 °С. Поэтому химические свойства этого соединения изучены еще недостаточно. Наиболее интересная реакция S 2 N 2 — это медленная самопроизвольная полимеризация в твердом состоянии при комнатной тем пературе с образованием кристаллического(SN)x. Политиазил (SN)x – полимерный нитрид серы, известный как политиазил, впервые был по лучен Ф. Буртом в 1910 г. К 1973 г. было установлено, что (SN)x действительно превращается в металл ниже тем пературы жидкого гелия, а в 1975 г. было показа но, что полимер становится сверхпроводником ниже 0, 26 К. (SN)x значительно более устойчив, чем его пред шественник. S 2 N 2. При нагревании на воздухе он разлагается со взрывом при ~240°С, однако в вакууме легко возгоняется при температуре около 135 °С.
 Соединения серы с азотом и кислородом Это классическая область неорганической химии, зародившаяся еще в середине XIX в. ; Гидразиды и гидроксиламиды серной кислоты тоже обсуждаются. Некоторые из этих соединений обладают примечательными свойствами, другие участвуют в камерном процессе получения серной кислоты. а) Оксиды серы-азота. Диоксид диазота трисеры S 3 N 2 O 2 лучше всего получать обработкой S 4 N 4 кипящим SOCl 2 B потоке SO 2: S 4 N 4 + 2 OSCl 2 → S 3 N 2 O 2 + 2 CI 2 + S 2 N 2 + S Это желтое твердое вещество с ациклической структурой. Пентаоксид S 3 N 2 O 5 также может быть получен не посредственно из. S 4 N 4 и SO 3. Он образует бесцвет ные, сильно преломляющие кристаллы, которые легко гидролизуются до сульфаминовой кислоты: S 3 N 2 O 5 + 3 H 2 O → 2 H 2 NSO 3 H + SO 2 б) Амиды серной кислоты. Амидосерная кислота (более известная как сульфаминовая кислота H[H 2 NSO 3]) является классическим неорганическим соединением и важным промышленным химикатом. Получение: 2 H 2 NOH + SO 2 → H[H 2 NSO 3] или NH 3 + SO 3 → H[H 2 NSO 3] В промышленности: Н 2 SO 4 (безводная) + мочевина → H[H 2 NSO 3] + NH 4 HSO 4 H[H 2 NSO 3] сухое нелетучее негигроскопичное б/цв, т плав 205, разлагается 260 С – SO 2 и SO 3, N 2 и вода. Сильная кислота (К=0, 101, растворимость 25 г в 100 г воды) Производство ~ 50000 т, применяется – очистка металлов, удаление накипи, моющие средства, стабилизаторы хлора в водных растворах. Соли – в антипиренах, для уничтожения сорняков, для получения гальванических покрытий. Растворы устойчивые при комнатн. t, выше гидролиз до NH 4 HSO 4 соли щелочных М устойчивы Сульфаминовая кислота в воде ведет себя как од ноосновная кислота. Под действием. Cl 2, Br 2 и Cl. O 3 она окисляется до азота и сульфат иона, например: 2 H[H 2 NSO 3] + KCl. O 3 → N 2 + 2 H 2 SO 4 + KCl + H 2 O Концентрированная HNO 3, взаимодействуя с суль фаминовой кислотой, дает чистый. N 2 O, в то вре мя как водный раствор азотистой кислоты HNO 2 реагирует количественно, образуя N 2: H[H 2 NSO 3] + HNO 3→ H 2 SO 4 + H 2 O + N 2 O H[H 2 NSO 3] + Na. NO 2 → Na. HSO 4 +H 2 O+ N 2 Последняя реакция находит применение в объем ном химическом анализе. Применение сульфами новой кислоты для стабилизации хлорированной воды основано на равновесии обратимой реакции образования N хлорсульфаминовой кислоты, ко торая сокращает потери хлора за счет испарения и медленно высвобождает хлорноватистую кислоту в обратимом процессе: Cl 2 + H 2 O → HOCl + HCl H[H 2 NS 03] + H 0 C 1 → HN(Cl)SO 3 H +H 2 O HOCl→ HCl + O 2
Соединения серы с азотом и кислородом Это классическая область неорганической химии, зародившаяся еще в середине XIX в. ; Гидразиды и гидроксиламиды серной кислоты тоже обсуждаются. Некоторые из этих соединений обладают примечательными свойствами, другие участвуют в камерном процессе получения серной кислоты. а) Оксиды серы-азота. Диоксид диазота трисеры S 3 N 2 O 2 лучше всего получать обработкой S 4 N 4 кипящим SOCl 2 B потоке SO 2: S 4 N 4 + 2 OSCl 2 → S 3 N 2 O 2 + 2 CI 2 + S 2 N 2 + S Это желтое твердое вещество с ациклической структурой. Пентаоксид S 3 N 2 O 5 также может быть получен не посредственно из. S 4 N 4 и SO 3. Он образует бесцвет ные, сильно преломляющие кристаллы, которые легко гидролизуются до сульфаминовой кислоты: S 3 N 2 O 5 + 3 H 2 O → 2 H 2 NSO 3 H + SO 2 б) Амиды серной кислоты. Амидосерная кислота (более известная как сульфаминовая кислота H[H 2 NSO 3]) является классическим неорганическим соединением и важным промышленным химикатом. Получение: 2 H 2 NOH + SO 2 → H[H 2 NSO 3] или NH 3 + SO 3 → H[H 2 NSO 3] В промышленности: Н 2 SO 4 (безводная) + мочевина → H[H 2 NSO 3] + NH 4 HSO 4 H[H 2 NSO 3] сухое нелетучее негигроскопичное б/цв, т плав 205, разлагается 260 С – SO 2 и SO 3, N 2 и вода. Сильная кислота (К=0, 101, растворимость 25 г в 100 г воды) Производство ~ 50000 т, применяется – очистка металлов, удаление накипи, моющие средства, стабилизаторы хлора в водных растворах. Соли – в антипиренах, для уничтожения сорняков, для получения гальванических покрытий. Растворы устойчивые при комнатн. t, выше гидролиз до NH 4 HSO 4 соли щелочных М устойчивы Сульфаминовая кислота в воде ведет себя как од ноосновная кислота. Под действием. Cl 2, Br 2 и Cl. O 3 она окисляется до азота и сульфат иона, например: 2 H[H 2 NSO 3] + KCl. O 3 → N 2 + 2 H 2 SO 4 + KCl + H 2 O Концентрированная HNO 3, взаимодействуя с суль фаминовой кислотой, дает чистый. N 2 O, в то вре мя как водный раствор азотистой кислоты HNO 2 реагирует количественно, образуя N 2: H[H 2 NSO 3] + HNO 3→ H 2 SO 4 + H 2 O + N 2 O H[H 2 NSO 3] + Na. NO 2 → Na. HSO 4 +H 2 O+ N 2 Последняя реакция находит применение в объем ном химическом анализе. Применение сульфами новой кислоты для стабилизации хлорированной воды основано на равновесии обратимой реакции образования N хлорсульфаминовой кислоты, ко торая сокращает потери хлора за счет испарения и медленно высвобождает хлорноватистую кислоту в обратимом процессе: Cl 2 + H 2 O → HOCl + HCl H[H 2 NS 03] + H 0 C 1 → HN(Cl)SO 3 H +H 2 O HOCl→ HCl + O 2


