Рибосомы.pptx
- Количество слайдов: 45

Функциональные активности и функциональные участки рибосом. Элонгационный цикл рибосомы.
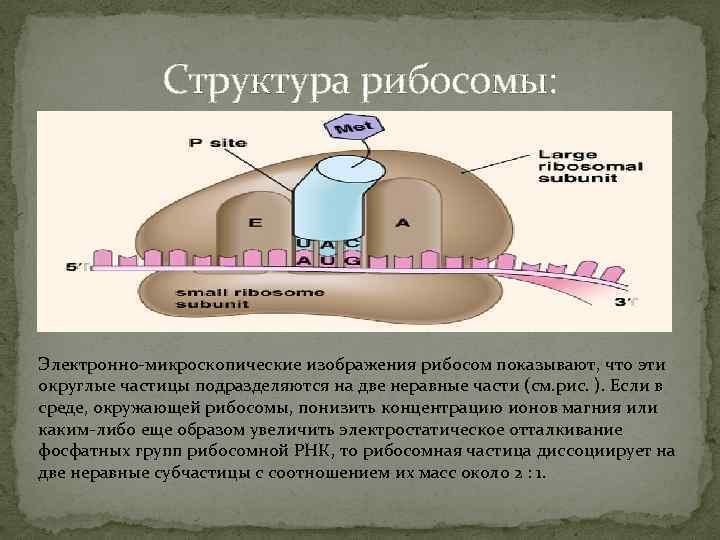
Структура рибосомы: Электронно-микроскопические изображения рибосом показывают, что эти округлые частицы подразделяются на две неравные части (см. рис. ). Если в среде, окружающей рибосомы, понизить концентрацию ионов магния или каким-либо еще образом увеличить электростатическое отталкивание фосфатных групп рибосомной РНК, то рибосомная частица диссоциирует на две неравные субчастицы с соотношением их масс около 2 : 1.
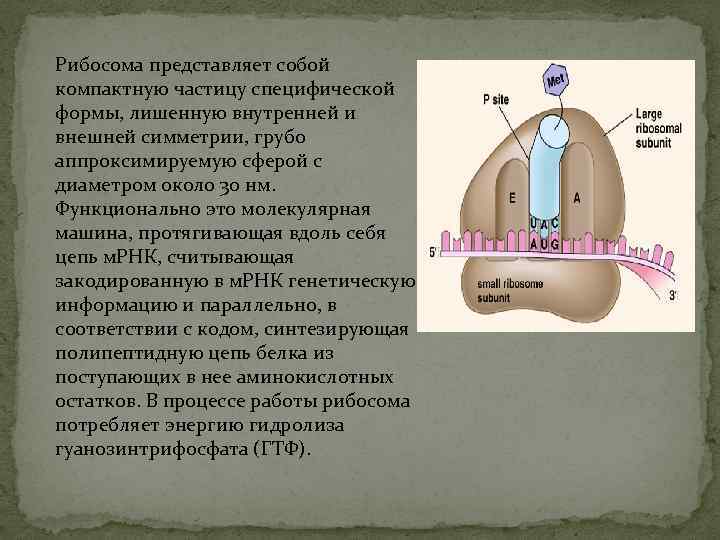
Рибосома представляет собой компактную частицу специфической формы, лишенную внутренней и внешней симметрии, грубо аппроксимируемую сферой с диаметром около 30 нм. Функционально это молекулярная машина, протягивающая вдоль себя цепь м. РНК, считывающая закодированную в м. РНК генетическую информацию и параллельно, в соответствии с кодом, синтезирующая полипептидную цепь белка из поступающих в нее аминокислотных остатков. В процессе работы рибосома потребляет энергию гидролиза гуанозинтрифосфата (ГТФ).
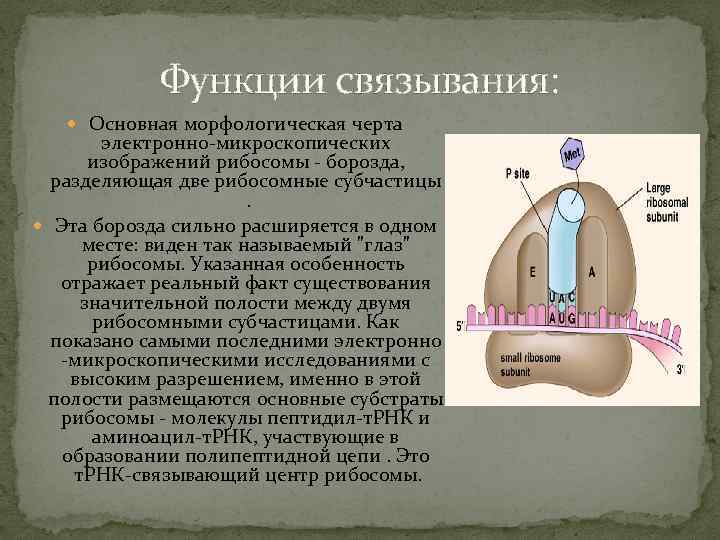
Функции связывания: Основная морфологическая черта электронно-микроскопических изображений рибосомы - борозда, разделяющая две рибосомные субчастицы . Эта борозда сильно расширяется в одном месте: виден так называемый "глаз" рибосомы. Указанная особенность отражает реальный факт существования значительной полости между двумя рибосомными субчастицами. Как показано самыми последними электронно -микроскопическими исследованиями с высоким разрешением, именно в этой полости размещаются основные субстраты рибосомы - молекулы пептидил-т. РНК и аминоацил-т. РНК, участвующие в образовании полипептидной цепи. Это т. РНК-связывающий центр рибосомы.

(справа внизу) видно, что две шеи находятся напротив друга и что между шеями как раз и расположен "глаз" - межсубчастичная полость, размещающая в себе молекулы двух субстратных т. РНК. Так каждая т. РНК в рибосоме одним своим концом - антикодоном - должна взаимодействовать с кодоном м. РНК, а другим, акцепторным концом, несущим аминокислоту или пептид, - с пептидилтрансферазным центром, то ее положение в рибосоме в отношении двух рибосомных субчастиц определяется однозначно: антикодон т. РНК сидит в шее малой субчастицы, а акцепторный конец - в шее большой субчастицы.

(слева), и непокрытая малой субчастицей площадка большой субчастицы у основания выступа. Наблюдения и эксперименты позволяют предполагать следующую картину событий: площадка принимает на себя поступающую в рибосому новую аминоацил-т. РНК в комплексе со специальным белком - фактором элонгации 1 (EF 1). При этом палочкообразный отросток взаимодействует с фактором и ориентируется более или менее перпендикулярно плоскости раздела между субчастицами. В результате образуется карман между непокрытой площадкой большой субчастицы, боковой поверхностью малой субчастицы и палочкообразным отростком. Этот же карман может принимать другой белок - фактор элонгации 2 (EF 2), связывающийся с рибосомой для производства механического акта - транслокации.
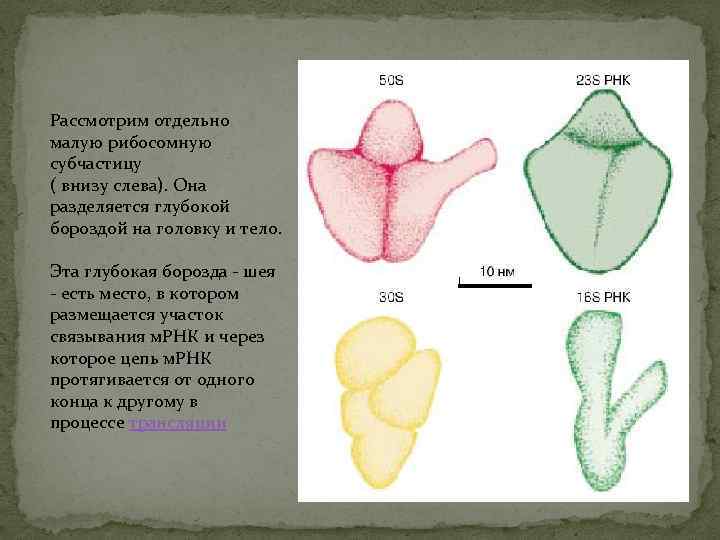
Рассмотрим отдельно малую рибосомную субчастицу ( внизу слева). Она разделяется глубокой бороздой на головку и тело. Эта глубокая борозда - шея - есть место, в котором размещается участок связывания м. РНК и через которое цепь м. РНК протягивается от одного конца к другому в процессе трансляции
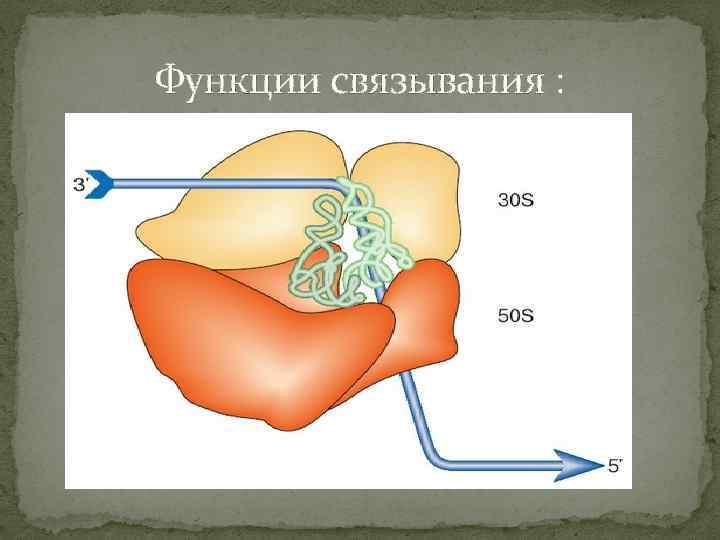
Функции связывания :
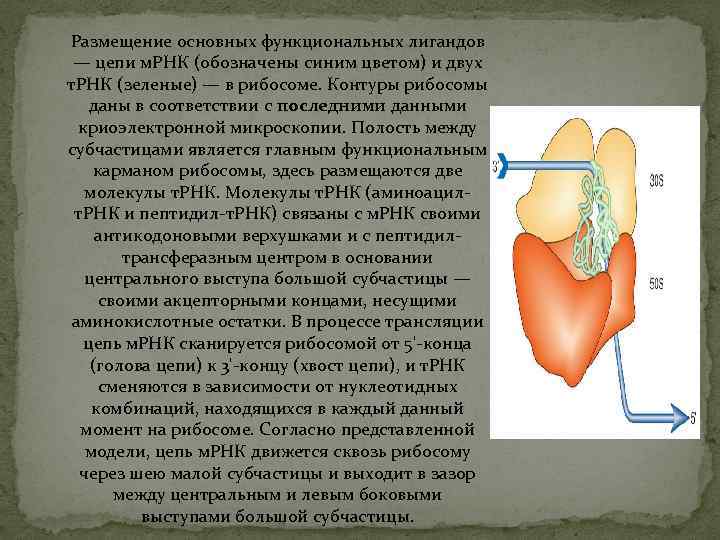
Размещение основных функциональных лигандов — цепи м. РНК (обозначены синим цветом) и двух т. РНК (зеленые) — в рибосоме. Контуры рибосомы даны в соответствии с последними данными криоэлектронной микроскопии. Полость между субчастицами является главным функциональным карманом рибосомы, здесь размещаются две молекулы т. РНК. Молекулы т. РНК (аминоацилт. РНК и пептидил-т. РНК) связаны с м. РНК своими антикодоновыми верхушками и с пептидилтрансферазным центром в основании центрального выступа большой субчастицы — своими акцепторными концами, несущими аминокислотные остатки. В процессе трансляции цепь м. РНК сканируется рибосомой от 5'-конца (голова цепи) к 3'-концу (хвост цепи), и т. РНК сменяются в зависимости от нуклеотидных комбинаций, находящихся в каждый данный момент на рибосоме. Согласно представленной модели, цепь м. РНК движется сквозь рибосому через шею малой субчастицы и выходит в зазор между центральным и левым боковыми выступами большой субчастицы.

Механизм действия: Биосинтез белка имеет два аспекта: химический и генетический. Белок строится из аминокислот путем последовательного добавления аминокислотных остатков к одному из концов растущей полипептидной цепи (удлинения) с одновременным сканированием матричного полинуклеотида (м. РНК), задающего порядок добавления различных аминокислотных остатков. Три последовательные химические реакции приводят к включению (добавлению) аминокислоты в полипептидную цепь строящегося белка: 1. аминокислота + АТФ >> аминоацил-аденилат + пирофосфат, 2. аминоацил-аденилат + т. РНК' >>аминоацил-т. РНК' + АМФ, 3. пептидил(n)-т. РНК + аминоацил-т. РНК' >> т. РНК + пептидил(n + 1)т. РНК'.

Первая реакция - активация аминокислоты за счет образования ангидридной связи между ее карбоксилом и фосфатом адениловой кислоты. Вторая реакция - акцептирование аминоацильного остатка молекулой т. РНК с образованием сложноэфирной связи между карбоксилом аминокислоты и гидроксилом концевого рибозного остатка т. РНК - происходят вне рибосомы, и обе реакции катализируется ферментом аминоацил-т. РНК-синтетазой. Третья реакция - транспептидация, то есть перенос карбоксильной группы растущего полипептида от гидроксила рибозного остатка т. РНК, принесшей предыдущий аминокислотный остаток в цепь, на аминогруппу аминокислотного остатка аминоацил-т. РНК - осуществляется в рибосоме и катализируется самой рибосомой, без постороннего фермента.

Таким образом, именно молекулы аминоацил-т. РНК являются формой поступления аминокислотных остатков в рибосомы. Генетическая сторона биосинтеза белка определяется тем, что поступление аминоацил-т. РНК в рибосому строго детерминировано матричной РНК (м. РНК), являющейся копией гена, и порядок чередования кодирующих триплетов (кодонов) вдоль цепи м. РНК однозначно задает структуру синтезируемого белка. Для этого рибосома сканирует цепь м. РНК по триплетам и последовательно выбирает из раствора аминоацил-т. РНК с соответствующими аминокислотными остатками, выбрасывая отработанные, деацилированные т. РНК. Итак, в процессе биосинтеза белка рибосома: а) принимает кодированную генетическую информацию от ДНК в виде м. РНК и расшифровывает ее, б) катализирует образование пептидных связей в реакции транспептидации в) передвигает цепь м. РНК и молекулы т. РНК (транслокация).
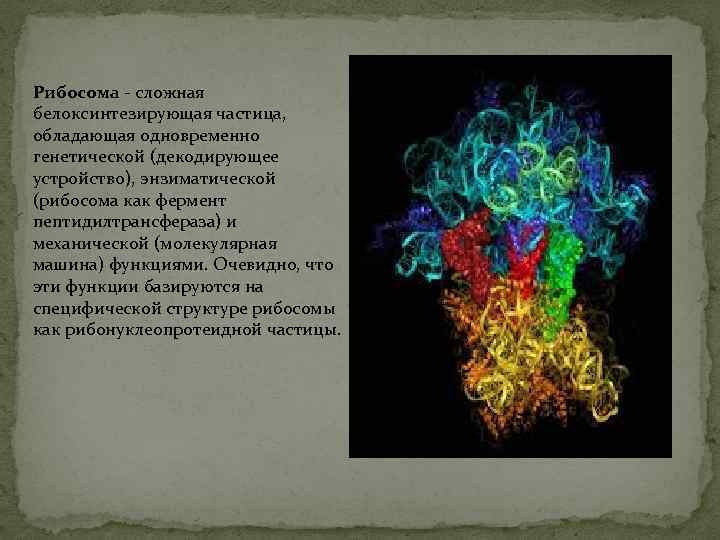
Рибосома - сложная белоксинтезирующая частица, обладающая одновременно генетической (декодирующее устройство), энзиматической (рибосома как фермент пептидилтрансфераза) и механической (молекулярная машина) функциями. Очевидно, что эти функции базируются на специфической структуре рибосомы как рибонуклеопротеидной частицы.
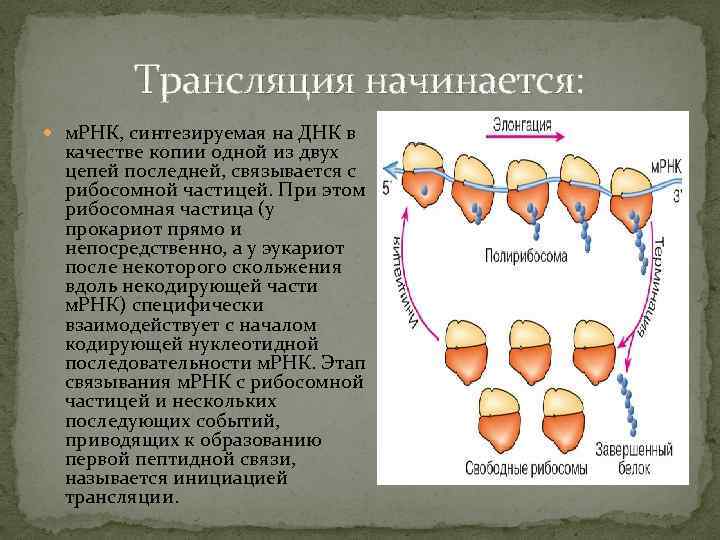
Трансляция начинается: м. РНК, синтезируемая на ДНК в качестве копии одной из двух цепей последней, связывается с рибосомной частицей. При этом рибосомная частица (у прокариот прямо и непосредственно, а у эукариот после некоторого скольжения вдоль некодирующей части м. РНК) специфически взаимодействует с началом кодирующей нуклеотидной последовательности м. РНК. Этап связывания м. РНК с рибосомной частицей и нескольких последующих событий, приводящих к образованию первой пептидной связи, называется инициацией трансляции.
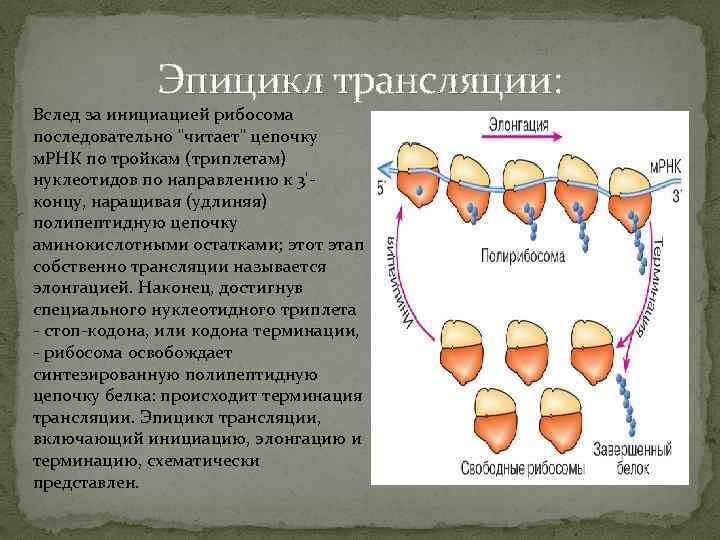
Эпицикл трансляции: Вслед за инициацией рибосома последовательно "читает" цепочку м. РНК по тройкам (триплетам) нуклеотидов по направлению к 3'концу, наращивая (удлиняя) полипептидную цепочку аминокислотными остатками; этот этап собственно трансляции называется элонгацией. Наконец, достигнув специального нуклеотидного триплета - стоп-кодона, или кодона терминации, - рибосома освобождает синтезированную полипептидную цепочку белка: происходит терминация трансляции. Эпицикл трансляции, включающий инициацию, элонгацию и терминацию, схематически представлен.

Эпицикл трансляции: 1) Инициация трансляции: свободная рибосомная частица ассоциирует с м. РНК у начала ее кодирующей последовательности нуклеотидов и начинает трансляцию на специальном иниициирующем кодоне, с участием специальной иниицаторной т. РНК; 2) Элонгация трансляции: затем считывает кодирующую последовательность нуклеотидов по триплетам (кодонам) в направлении 5'-3' и соответственно наращивает полипептидную цепь по одной аминокислоте, последовательно удлиняя ее С-конец; 3) Терминация трансляции: дойдя до специального стоптриплета (терминирующего кодона), прекращает трансляцию и освобождает законченную полипептидную цепь белка.

Рибосомные частицы, закончившие трансляцию и диссоциировавшие от м. РНК, снова готовы инициировать трансляцию и войти в эпицикл. После инициации, двигаясь по цепи м. РНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок м. РНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на м. РНК и начать трансляцию. Таким путем, двигаясь вдоль м. РНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна м. РНК ассоциирована со многими рибосомами, ее одновременно транслирующими, называется полирибосомой.

Генетические функции малой рибосомной субчастици: Характерным моментом инициации трансляции является то, что на этом этапе участвуют не целые рибосомы, а их отдельные субчастицы. Рибосома должна быть диссоциирована на две составляющие ее неравные субчастицы. Для этого клетка располагает специальными механизмами, обеспечивающими диссоциацию рибосом после терминации трансляции. Именно малая субчастица рибосомы (30 S у прокариот и 40 S у эукариот), и только она, связывается с м. РНК, то есть служит первичным приемником генетической информации для белоксинтезирующего аппарата. Лишь впоследствии, при завершении этапа инициации трансляции, к ней присоединяется большая субчастица (50 S у прокариот и 60 S у эукариот), образуя полную рибосомную частицу (70 S у прокариот и 80 S у эукариот), которая и будет производить элонгацию.
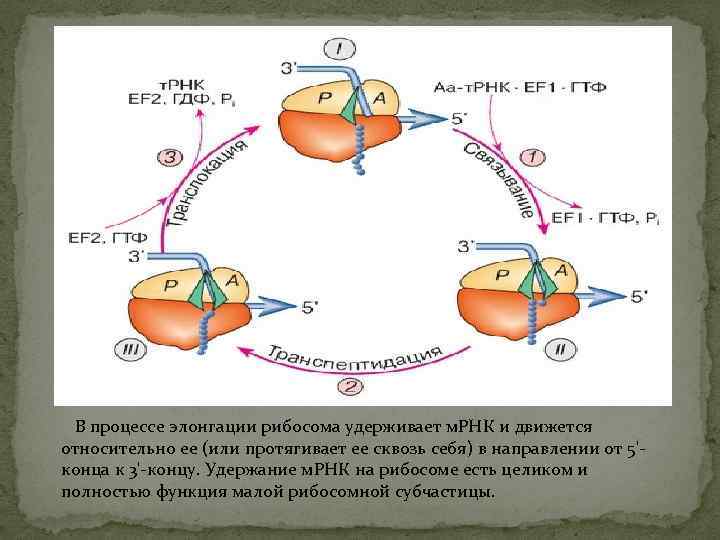
В процессе элонгации рибосома удерживает м. РНК и движется относительно ее (или протягивает ее сквозь себя) в направлении от 5'конца к 3'-концу. Удержание м. РНК на рибосоме есть целиком и полностью функция малой рибосомной субчастицы.
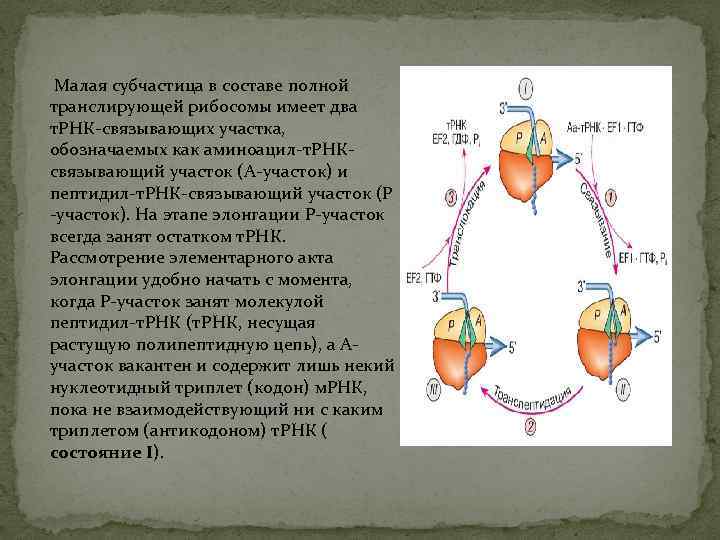
Малая субчастица в составе полной транслирующей рибосомы имеет два т. РНК-связывающих участка, обозначаемых как аминоацил-т. РНКсвязывающий участок (А-участок) и пептидил-т. РНК-связывающий участок (Р -участок). На этапе элонгации Р-участок всегда занят остатком т. РНК. Рассмотрение элементарного акта элонгации удобно начать с момента, когда Р-участок занят молекулой пептидил-т. РНК (т. РНК, несущая растущую полипептидную цепь), а Аучасток вакантен и содержит лишь некий нуклеотидный триплет (кодон) м. РНК, пока не взаимодействующий ни с каким триплетом (антикодоном) т. РНК ( состояние I).
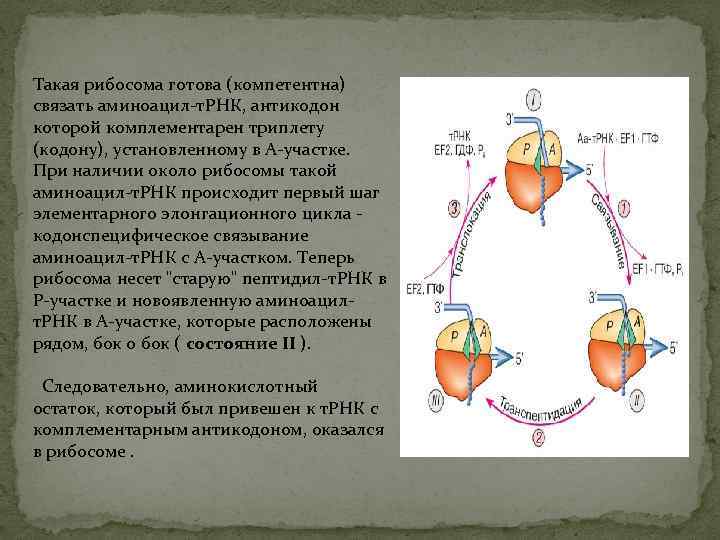
Такая рибосома готова (компетентна) связать аминоацил-т. РНК, антикодон которой комплементарен триплету (кодону), установленному в А-участке. При наличии около рибосомы такой аминоацил-т. РНК происходит первый шаг элементарного элонгационного цикла - кодонспецифическое связывание аминоацил-т. РНК с А-участком. Теперь рибосома несет "старую" пептидил-т. РНК в Р-участке и новоявленную аминоацилт. РНК в А-участке, которые расположены рядом, бок о бок ( состояние II ). Следовательно, аминокислотный остаток, который был привешен к т. РНК с комплементарным антикодоном, оказался в рибосоме.
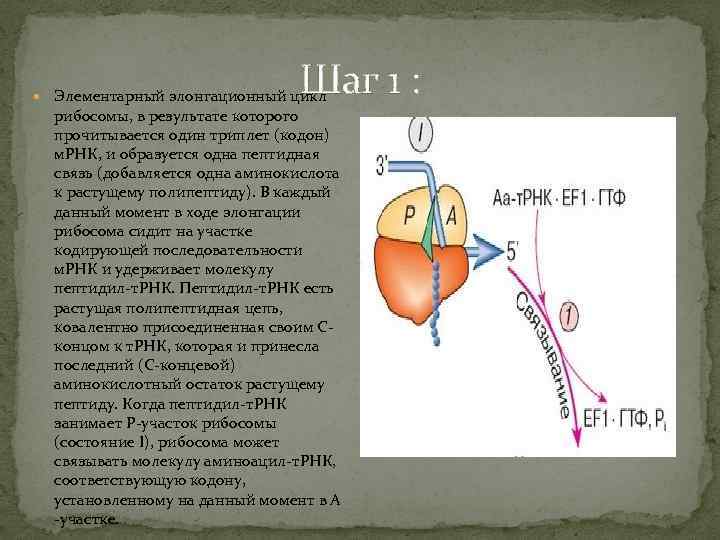
Шаг 1 : Элементарный элонгационный цикл рибосомы, в результате которого прочитывается один триплет (кодон) м. РНК, и образуется одна пептидная связь (добавляется одна аминокислота к растущему полипептиду). В каждый данный момент в ходе элонгации рибосома сидит на участке кодирующей последовательности м. РНК и удерживает молекулу пептидил-т. РНК. Пептидил-т. РНК есть растущая полипептидная цепь, ковалентно присоединенная своим Сконцом к т. РНК, которая и принесла последний (С-концевой) аминокислотный остаток растущему пептиду. Когда пептидил-т. РНК занимает Р-участок рибосомы (состояние I), рибосома может связывать молекулу аминоацил-т. РНК, соответствующую кодону, установленному на данный момент в А -участке.
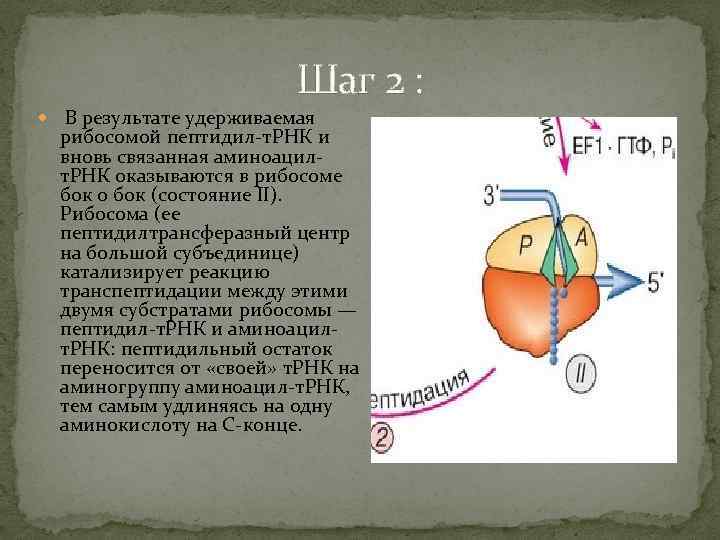
Шаг 2 : В результате удерживаемая рибосомой пептидил-т. РНК и вновь связанная аминоацилт. РНК оказываются в рибосоме бок о бок (состояние II). Рибосома (ее пептидилтрансферазный центр на большой субъединице) катализирует реакцию транспептидации между этими двумя субстратами рибосомы — пептидил-т. РНК и аминоацилт. РНК: пептидильный остаток переносится от «своей» т. РНК на аминогруппу аминоацил-т. РНК, тем самым удлиняясь на одну аминокислоту на С-конце.
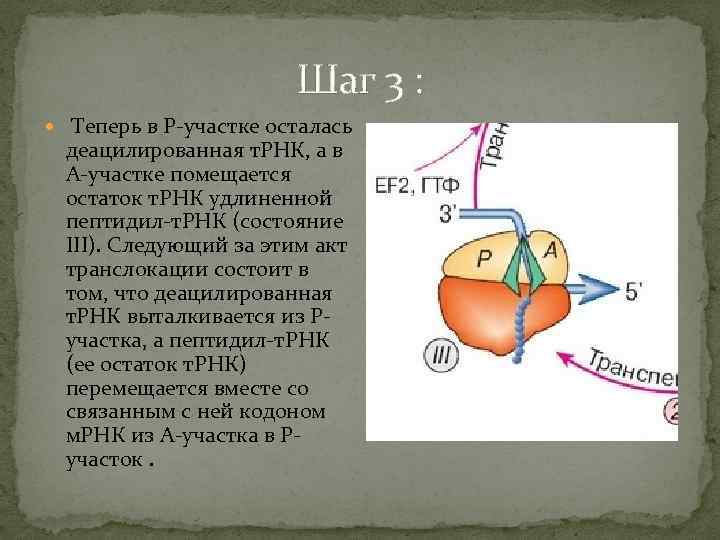
Шаг 3 : Теперь в Р-участке осталась деацилированная т. РНК, а в А-участке помещается остаток т. РНК удлиненной пептидил-т. РНК (состояние III). Следующий за этим акт транслокации состоит в том, что деацилированная т. РНК выталкивается из Ручастка, а пептидил-т. РНК (ее остаток т. РНК) перемещается вместе со связанным с ней кодоном м. РНК из А-участка в Ручасток.
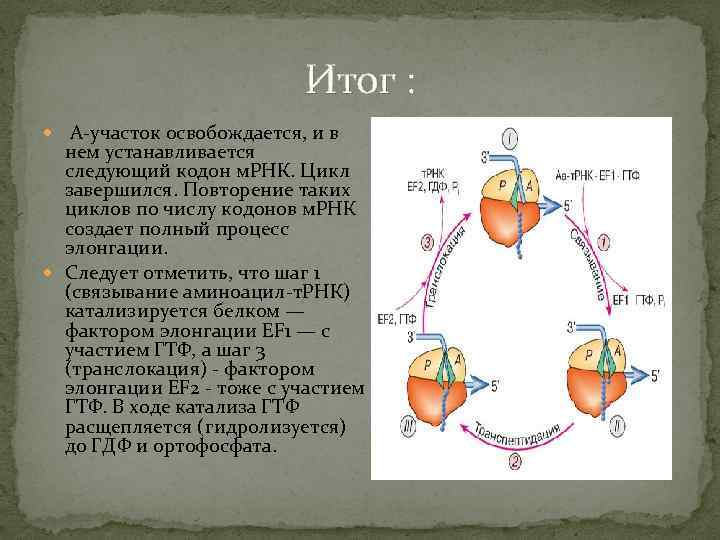
Итог : А-участок освобождается, и в нем устанавливается следующий кодон м. РНК. Цикл завершился. Повторение таких циклов по числу кодонов м. РНК создает полный процесс элонгации. Следует отметить, что шаг 1 (связывание аминоацил-т. РНК) катализируется белком — фактором элонгации EF 1 — с участием ГТФ, а шаг 3 (транслокация) - фактором элонгации EF 2 - тоже с участием ГТФ. В ходе катализа ГТФ расщепляется (гидролизуется) до ГДФ и ортофосфата.
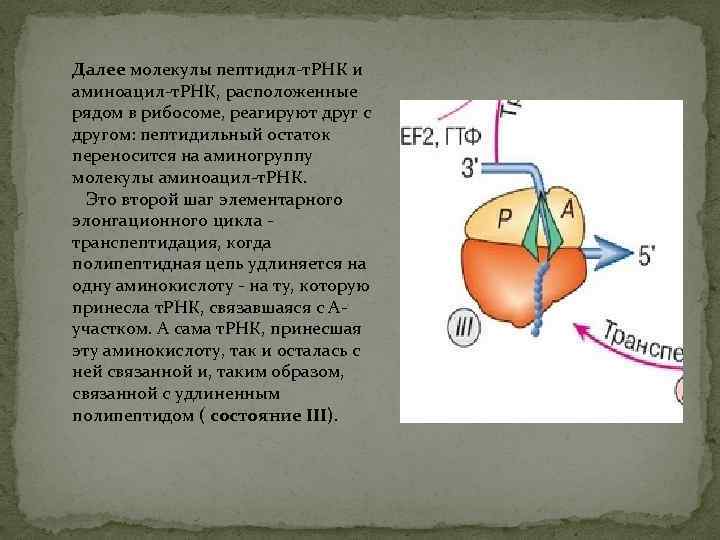
Далее молекулы пептидил-т. РНК и аминоацил-т. РНК, расположенные рядом в рибосоме, реагируют друг с другом: пептидильный остаток переносится на аминогруппу молекулы аминоацил-т. РНК. Это второй шаг элементарного элонгационного цикла - транспептидация, когда полипептидная цепь удлиняется на одну аминокислоту - на ту, которую принесла т. РНК, связавшаяся с Аучастком. А сама т. РНК, принесшая эту аминокислоту, так и осталась с ней связанной и, таким образом, связанной с удлиненным полипептидом ( состояние III).
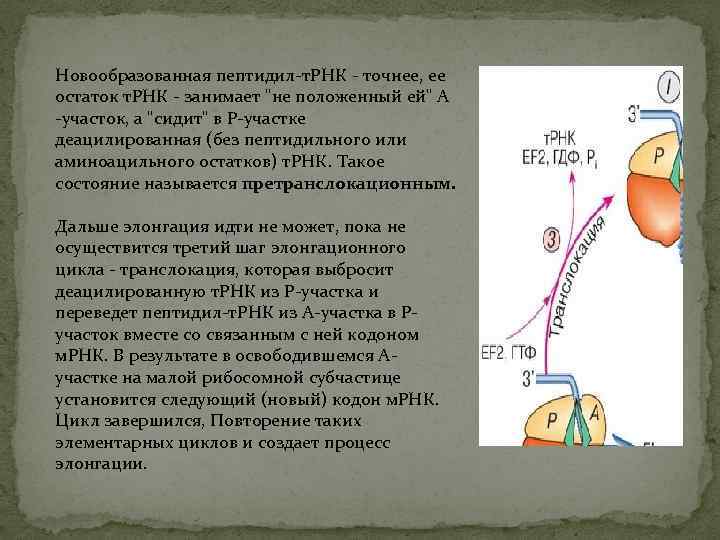
Новообразованная пептидил-т. РНК - точнее, ее остаток т. РНК - занимает "не положенный ей" А -участок, а "сидит" в Р-участке деацилированная (без пептидильного или аминоацильного остатков) т. РНК. Такое состояние называется претранслокационным. Дальше элонгация идти не может, пока не осуществится третий шаг элонгационного цикла - транслокация, которая выбросит деацилированную т. РНК из Р-участка и переведет пептидил-т. РНК из А-участка в Ручасток вместе со связанным с ней кодоном м. РНК. В результате в освободившемся Аучастке на малой рибосомной субчастице установится следующий (новый) кодон м. РНК. Цикл завершился, Повторение таких элементарных циклов и создает процесс элонгации.
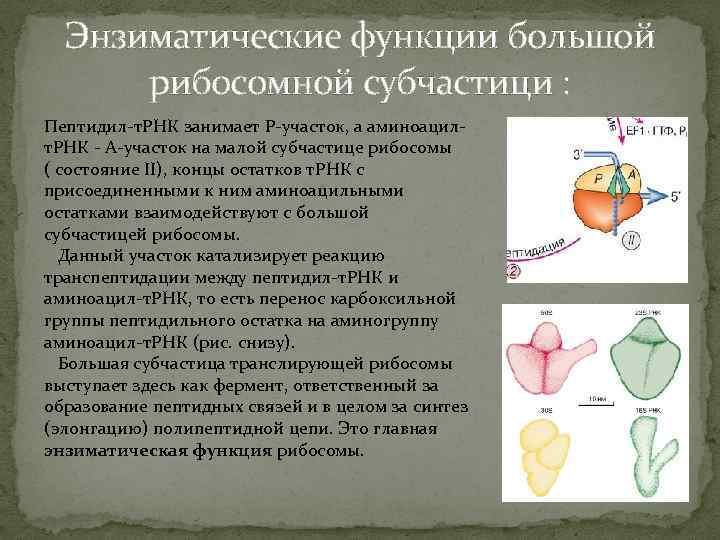
Энзиматические функции большой рибосомной субчастици : Пептидил-т. РНК занимает Р-участок, а аминоацилт. РНК - А-участок на малой субчастице рибосомы ( состояние II), концы остатков т. РНК с присоединенными к ним аминоацильными остатками взаимодействуют с большой субчастицей рибосомы. Данный участок катализирует реакцию транспептидации между пептидил-т. РНК и аминоацил-т. РНК, то есть перенос карбоксильной группы пептидильного остатка на аминогруппу аминоацил-т. РНК (рис. снизу). Большая субчастица транслирующей рибосомы выступает здесь как фермент, ответственный за образование пептидных связей и в целом за синтез (элонгацию) полипептидной цепи. Это главная энзиматическая функция рибосомы.
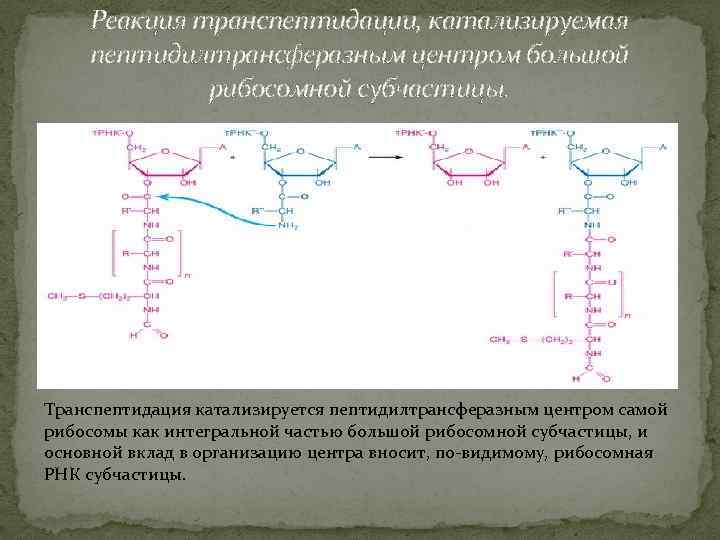
Реакция транспептидации, катализируемая пептидилтрансферазным центром большой рибосомной субчастицы. Транспептидация катализируется пептидилтрансферазным центром самой рибосомы как интегральной частью большой рибосомной субчастицы, и основной вклад в организацию центра вносит, по-видимому, рибосомная РНК субчастицы.
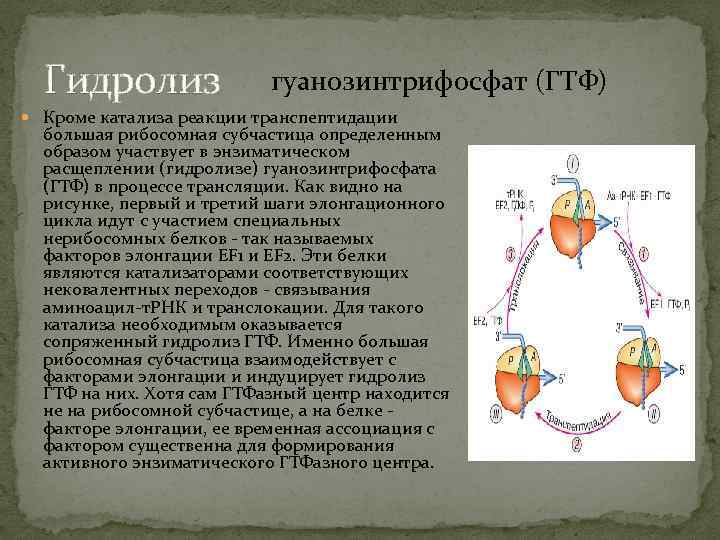
Гидролиз гуанозинтрифосфат (ГТФ) Кроме катализа реакции транспептидации большая рибосомная субчастица определенным образом участвует в энзиматическом расщеплении (гидролизе) гуанозинтрифосфата (ГТФ) в процессе трансляции. Как видно на рисунке, первый и третий шаги элонгационного цикла идут с участием специальных нерибосомных белков - так называемых факторов элонгации EF 1 и EF 2. Эти белки являются катализаторами соответствующих нековалентных переходов - связывания аминоацил-т. РНК и транслокации. Для такого катализа необходимым оказывается сопряженный гидролиз ГТФ. Именно большая рибосомная субчастица взаимодействует с факторами элонгации и индуцирует гидролиз ГТФ на них. Хотя сам ГТФазный центр находится не на рибосомной субчастице, а на белке - факторе элонгации, ее временная ассоциация с фактором существенна для формирования активного энзиматического ГТФазного центра.

Расположение функциональных центров на малой (вверху) и большой (внизу) субчастицах рибосомы : Существует четкое разделение труда между двумя неравными субчастицами рибосомы: малая субчастица выполняет генетические функции, будучи ответственной за прием и декодирование генетической информации, в то время как большая участвует в энзиматических реакциях в процессе трансляции. Схематическое изображение "разъятой" рибосомы с распределением ее основных функциональных центров на двух субчастицах
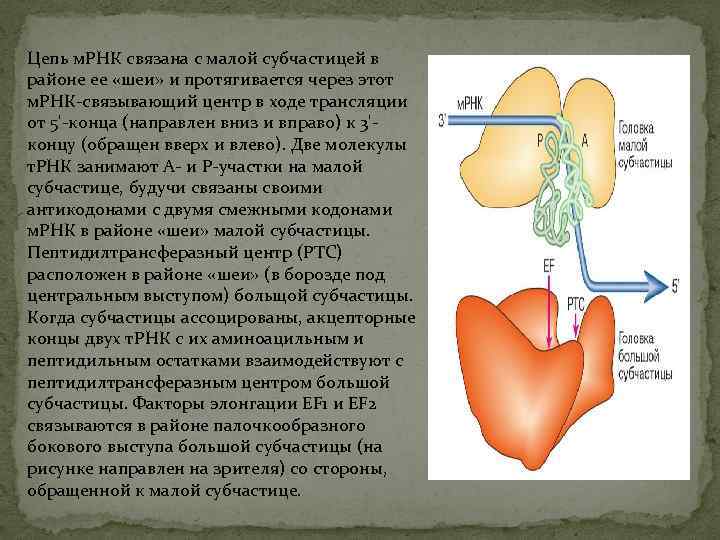
Цепь м. РНК связана с малой субчастицей в районе ее «шеи» и протягивается через этот м. РНК-связывающий центр в ходе трансляции от 5'-конца (направлен вниз и вправо) к 3'концу (обращен вверх и влево). Две молекулы т. РНК занимают А- и Р-участки на малой субчастице, будучи связаны своими антикодонами с двумя смежными кодонами м. РНК в районе «шеи» малой субчастицы. Пептидилтрансферазный центр (PTC) расположен в районе «шеи» (в борозде под центральным выступом) больщой субчастицы. Когда субчастицы ассоцированы, акцепторные концы двух т. РНК с их аминоацильным и пептидильным остатками взаимодействуют с пептидилтрансферазным центром большой субчастицы. Факторы элонгации EF 1 и EF 2 связываются в районе палочкообразного бокового выступа большой субчастицы (на рисунке направлен на зрителя) со стороны, обращенной к малой субчастице.
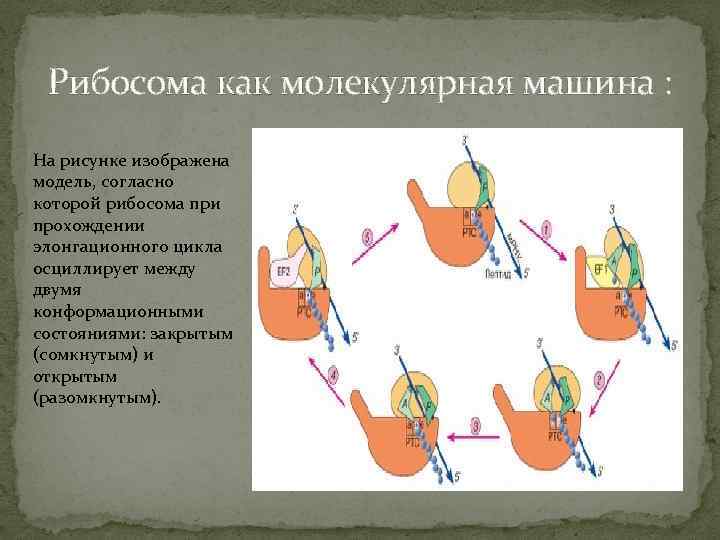
Рибосома как молекулярная машина : На рисунке изображена модель, согласно которой рибосома при прохождении элонгационного цикла осциллирует между двумя конформационными состояниями: закрытым (сомкнутым) и открытым (разомкнутым).
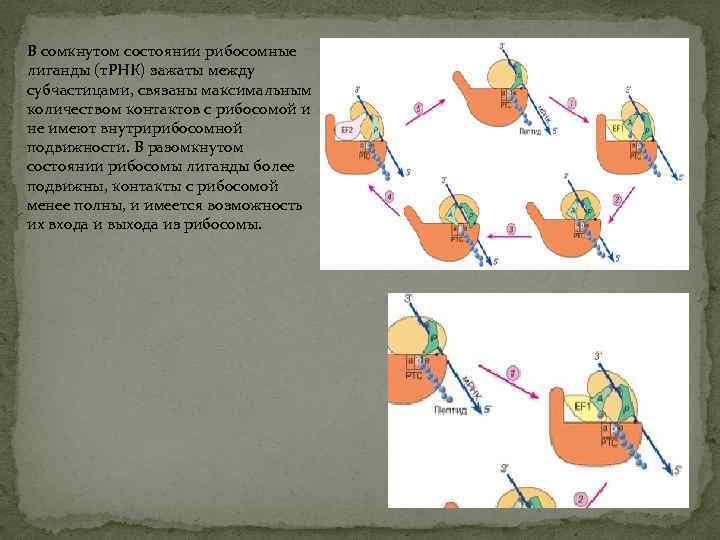
В сомкнутом состоянии рибосомные лиганды (т. РНК) зажаты между субчастицами, связаны максимальным количеством контактов с рибосомой и не имеют внутририбосомной подвижности. В разомкнутом состоянии рибосомы лиганды более подвижны, контакты с рибосомой менее полны, и имеется возможность их входа и выхода из рибосомы.

На первом этапе связывания аминоацил-т. РНК рибосома должна быть открыта для приема лиганда. Возможно, это открытое состояние фиксируется фактором элонгации EF 1. Далее EF 1 уходит, рибосомные субчастицы плотно смыкаются, и аминоацильный конец связавшейся аминоацил-т. РНК вступает в контакт с пептидилтрансферазным центром большой субчастицы. В сомкнутом состоянии пептидилт. РНК и аминоацил-т. РНК тесно сближены, и между ними происходит реакция транспептидации. Теперь, чтобы выбросить деацилированную т. РНК из рибосомы и дать свободу для перемещения остатка т. РНК молекулы пептидил-т. РНК из А-участка в Ручасток, рибосому надо приоткрыть, в частности путем раздвигания субчастиц. Это может осуществляться фактором элонгации EF 2. После ухода EF 2 с рибосомы она снова смыкается и ждет прихода очередной аминоацил-т. РНК с фактором элонгации EF 1.
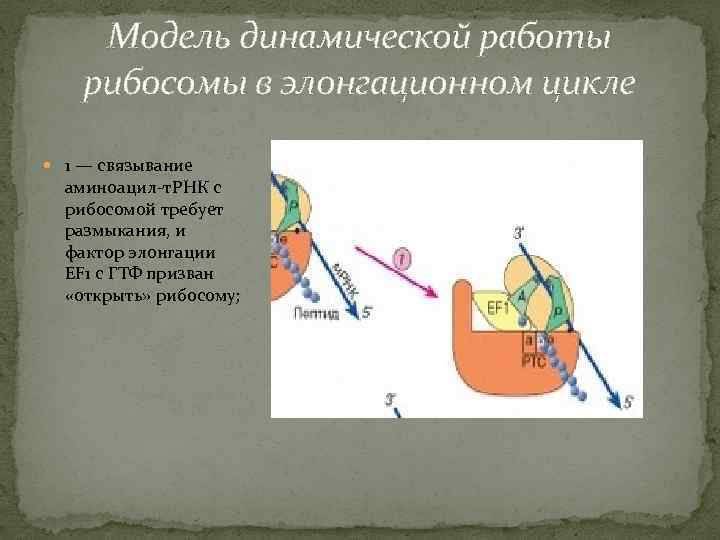
Модель динамической работы рибосомы в элонгационном цикле 1 — связывание аминоацил-т. РНК с рибосомой требует размыкания, и фактор элонгации EF 1 с ГТФ призван «открыть» рибосому;
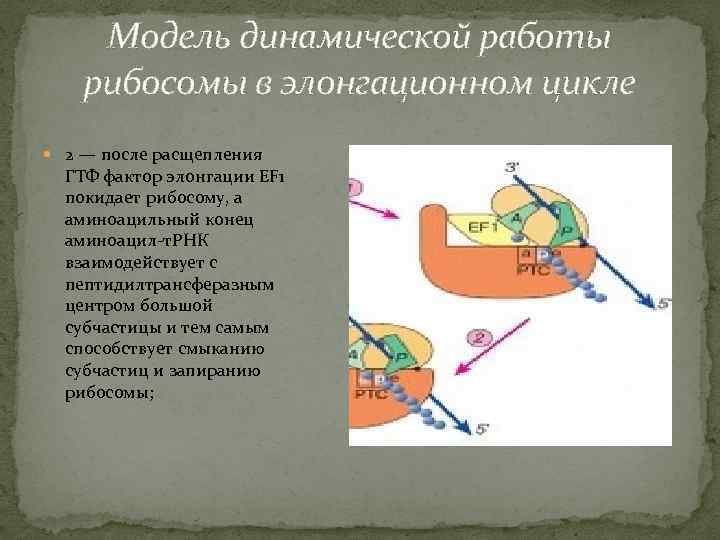
Модель динамической работы рибосомы в элонгационном цикле 2 — после расщепления ГТФ фактор элонгации EF 1 покидает рибосому, а аминоацильный конец аминоацил-т. РНК взаимодействует с пептидилтрансферазным центром большой субчастицы и тем самым способствует смыканию субчастиц и запиранию рибосомы;
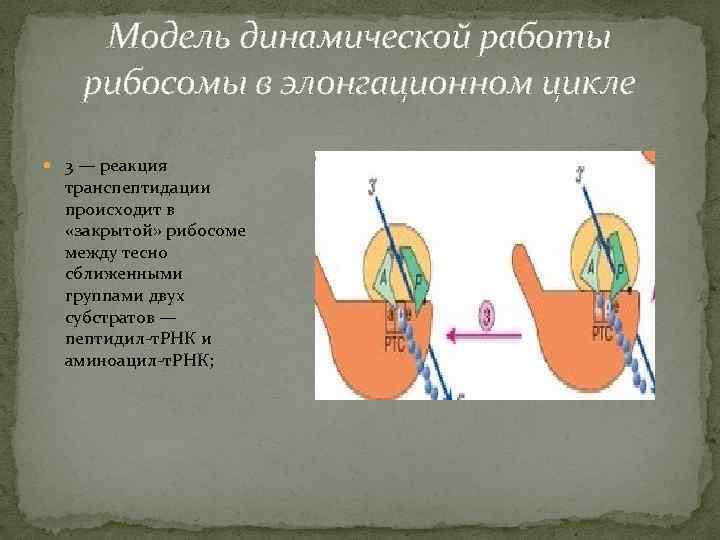
Модель динамической работы рибосомы в элонгационном цикле 3 — реакция транспептидации происходит в «закрытой» рибосоме между тесно сближенными группами двух субстратов — пептидил-т. РНК и аминоацил-т. РНК;
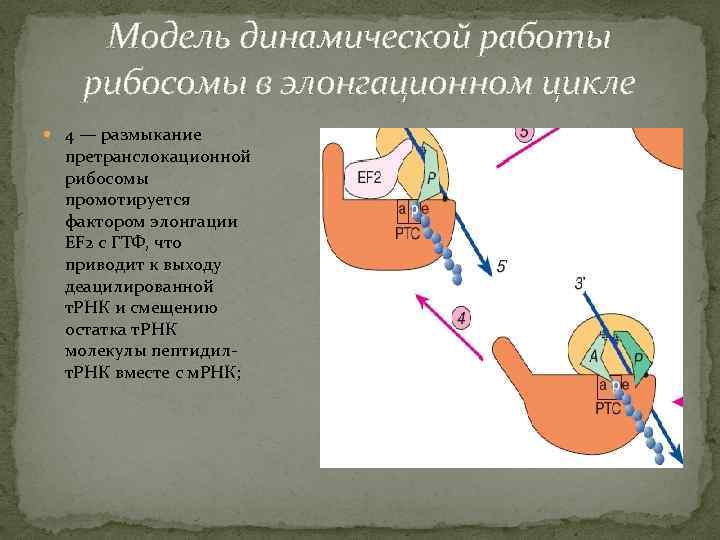
Модель динамической работы рибосомы в элонгационном цикле 4 — размыкание претранслокационной рибосомы промотируется фактором элонгации EF 2 с ГТФ, что приводит к выходу деацилированной т. РНК и смещению остатка т. РНК молекулы пептидилт. РНК вместе с м. РНК;

Модель динамической работы рибосомы в элонгационном цикле 5 — гидролиз ГТФ и как следствие уход фактора элонгации EF 2 снова дает возможность рибосом сомкнуться. Таким образом, транслирующая рибосома в ходе элонгационного цикла осциллирует между сомкнутым и разомкнутым состояниями.

Следует подчеркнуть : Процесс периодического смыкания-размыкания рибосомы является энергозависимым: факторы элонгации EF 1 и EF 2 взаимодействуют с рибосомой только будучи связанными с ГТФ (согласно модели, при этом взаимодействии происходит открывание рибосомы), а взаимодействие с рибосомой наводит ГТФазную активность, ГТФ гидролизуется, фактор элонгации теряет сродство к рибосоме. На каждое смыкание-размыкание рибосомы расходуется одна молекула ГТФ. Так как в каждом элонгационном цикле рибосома смыкается-размыкается дважды, то две молекулы ГТФ расходуются на каждый цикл. Это есть энергетическая плата за эффективное (быстрое и надежное) функционирование рибосомы как молекулярной машины. и уходит, и рибосома закрывается.
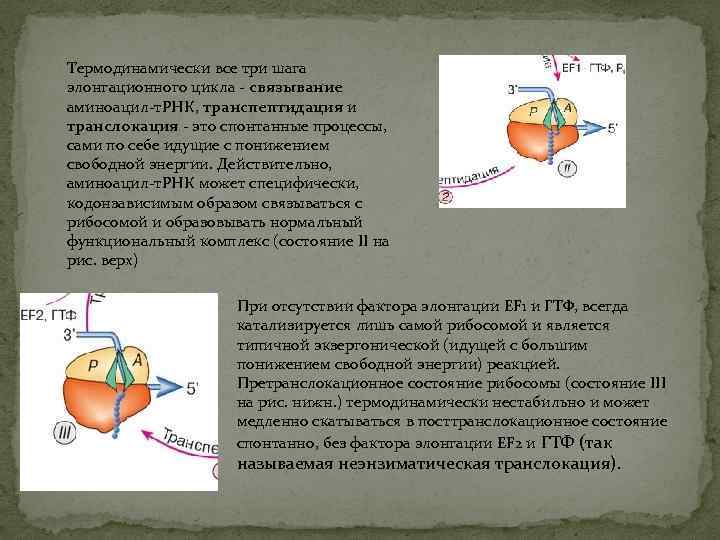
Термодинамически все три шага элонгационного цикла - связывание аминоацил-т. РНК, транспептидация и транслокация - это спонтанные процессы, сами по себе идущие с понижением свободной энергии. Действительно, аминоацил-т. РНК может специфически, кодонзависимым образом связываться с рибосомой и образовывать нормальный функциональный комплекс (состояние II на рис. верх) При отсутствии фактора элонгации EF 1 и ГТФ, всегда катализируется лишь самой рибосомой и является типичной экзергонической (идущей с большим понижением свободной энергии) реакцией. Претранслокационное состояние рибосомы (состояние III на рис. нижн. ) термодинамически нестабильно и может медленно скатываться в посттранслокационное состояние спонтанно, без фактора элонгации EF 2 и ГТФ (так называемая неэнзиматическая транслокация).
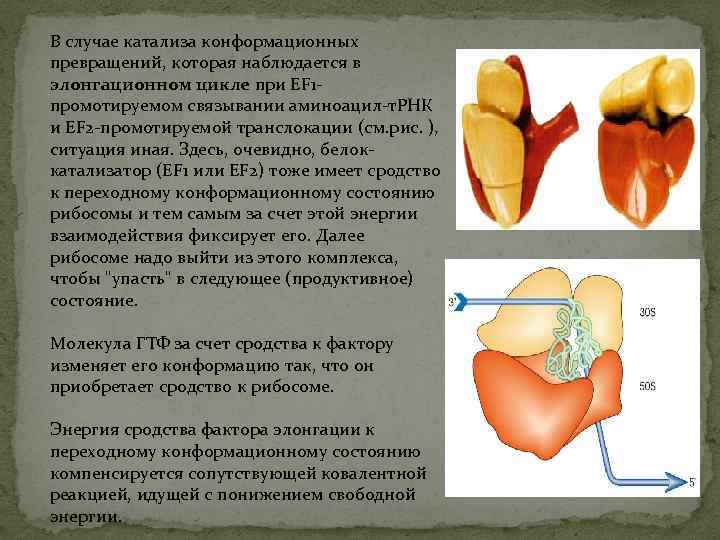
В случае катализа конформационных превращений, которая наблюдается в элонгационном цикле при EF 1 промотируемом связывании аминоацил-т. РНК и EF 2 -промотируемой транслокации (см. рис. ), ситуация иная. Здесь, очевидно, белоккатализатор (EF 1 или EF 2) тоже имеет сродство к переходному конформационному состоянию рибосомы и тем самым за счет этой энергии взаимодействия фиксирует его. Далее рибосоме надо выйти из этого комплекса, чтобы "упасть" в следующее (продуктивное) состояние. Молекула ГТФ за счет сродства к фактору изменяет его конформацию так, что он приобретает сродство к рибосоме. Энергия сродства фактора элонгации к переходному конформационному состоянию компенсируется сопутствующей ковалентной реакцией, идущей с понижением свободной энергии.

Таким образом Прямой гидролиз ГТФ представляется необходимым для "энзиматического" (фактор-промотируемого) катализа нековалентных конформационных переходов в элонгационном цикле. Основная роль этого гидролиза - разрушение лиганда, обеспечивающего сродство катализатора к переходному конформационному состоянию, чтобы дать возможность выйти из этого промежуточного комплекса и перейти к следующему - продуктивному — состоянию.

СПАСИБО ЗА ВНИМАНИЕ Набережные Челны 2012
Рибосомы.pptx