Сердце_10_ЯА_правка.ppt
- Количество слайдов: 78
 Функциональная анатомия сердечно-сосудистой системы Функциональная анатомия сердца Фило - и онтогенез сердца Читает старший преподаватель кафедры анатомии человека НГМУ Хорошевская Яна Александровна
Функциональная анатомия сердечно-сосудистой системы Функциональная анатомия сердца Фило - и онтогенез сердца Читает старший преподаватель кафедры анатомии человека НГМУ Хорошевская Яна Александровна
 Функциональная анатомия сердца Фило- и онтогенез сердца План лекции 1. 2. 3. 4. 5. Общие представления о циркуляторных системах организма Функциональная анатомия сердца. Филогенез сердца. Онтогенез сердца. Классификация пороков развития сердца.
Функциональная анатомия сердца Фило- и онтогенез сердца План лекции 1. 2. 3. 4. 5. Общие представления о циркуляторных системах организма Функциональная анатомия сердца. Филогенез сердца. Онтогенез сердца. Классификация пороков развития сердца.
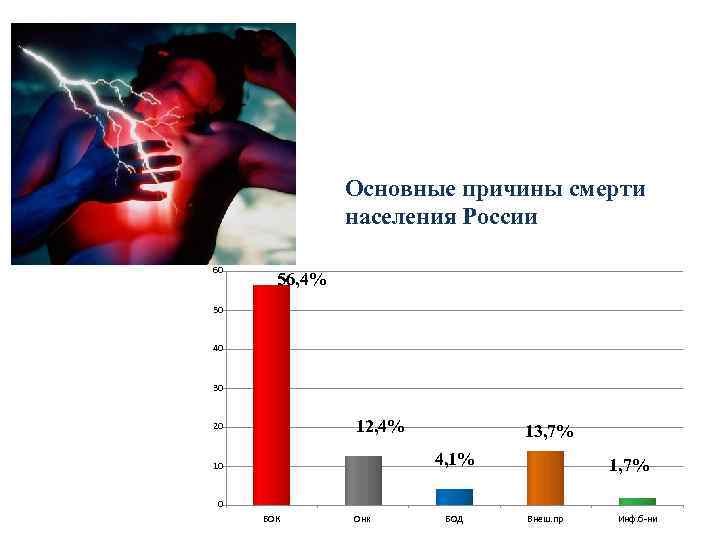 Основные причины смерти населения России 60 56, 4% 50 40 30 12, 4% 20 13, 7% 4, 1% 10 1, 7% 0 БОК Онк БОД Внеш. пр Инф. б-ни
Основные причины смерти населения России 60 56, 4% 50 40 30 12, 4% 20 13, 7% 4, 1% 10 1, 7% 0 БОК Онк БОД Внеш. пр Инф. б-ни
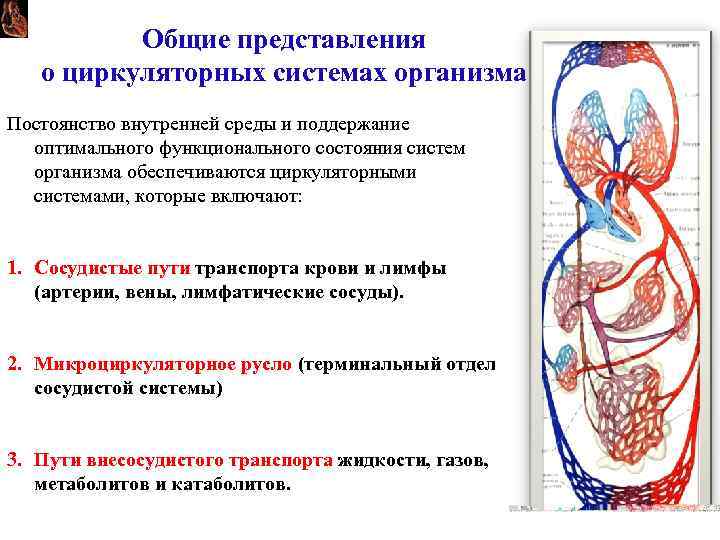 Общие представления о циркуляторных системах организма Постоянство внутренней среды и поддержание оптимального функционального состояния систем организма обеспечиваются циркуляторными системами, которые включают: 1. Сосудистые пути транспорта крови и лимфы (артерии, вены, лимфатические сосуды). 2. Микроциркуляторное русло (терминальный отдел сосудистой системы) 3. Пути внесосудистого транспорта жидкости, газов, метаболитов и катаболитов.
Общие представления о циркуляторных системах организма Постоянство внутренней среды и поддержание оптимального функционального состояния систем организма обеспечиваются циркуляторными системами, которые включают: 1. Сосудистые пути транспорта крови и лимфы (артерии, вены, лимфатические сосуды). 2. Микроциркуляторное русло (терминальный отдел сосудистой системы) 3. Пути внесосудистого транспорта жидкости, газов, метаболитов и катаболитов.
 Функции сердечно-сосудистой системы 1. Трофическая 2. Дыхательная 3. Экскреторная 4. Регуляторная (объем кровотока, перенос БАВ, гормонов) 5. Защитная (участие в иммунных и воспалительных реакциях)
Функции сердечно-сосудистой системы 1. Трофическая 2. Дыхательная 3. Экскреторная 4. Регуляторная (объем кровотока, перенос БАВ, гормонов) 5. Защитная (участие в иммунных и воспалительных реакциях)
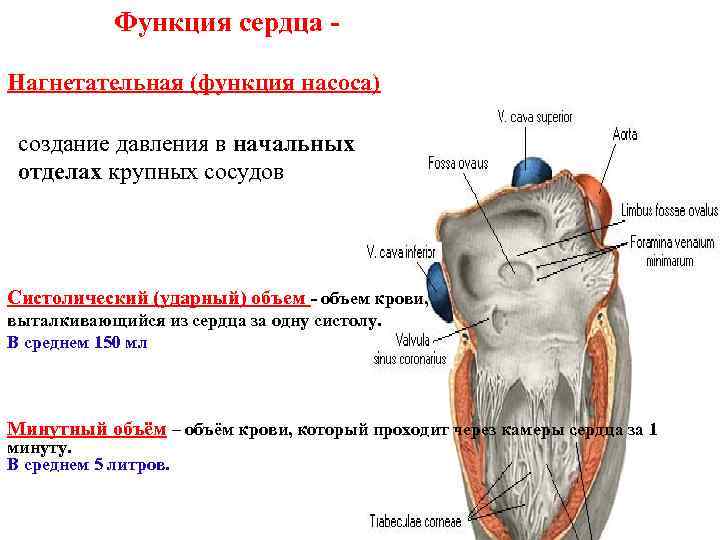 Функция сердца Нагнетательная (функция насоса) создание давления в начальных отделах крупных сосудов Систолический (ударный) объем - объем крови, выталкивающийся из сердца за одну систолу. В среднем 150 мл Минутный объём – объём крови, который проходит через камеры сердца за 1 минуту. В среднем 5 литров.
Функция сердца Нагнетательная (функция насоса) создание давления в начальных отделах крупных сосудов Систолический (ударный) объем - объем крови, выталкивающийся из сердца за одну систолу. В среднем 150 мл Минутный объём – объём крови, который проходит через камеры сердца за 1 минуту. В среднем 5 литров.
 Сокращается сердце более 49 миллионов раз в год За сутки сердце совершает более 100000 циклов Сердце транспортирует от 4 до 6 литров крови в минуту около 250 до 350 литров в час около 6000 до 9000 литров крови в день. У здорового человека в желудочках сердца находятся от 120 до 150 кубических сантиметров крови.
Сокращается сердце более 49 миллионов раз в год За сутки сердце совершает более 100000 циклов Сердце транспортирует от 4 до 6 литров крови в минуту около 250 до 350 литров в час около 6000 до 9000 литров крови в день. У здорового человека в желудочках сердца находятся от 120 до 150 кубических сантиметров крови.
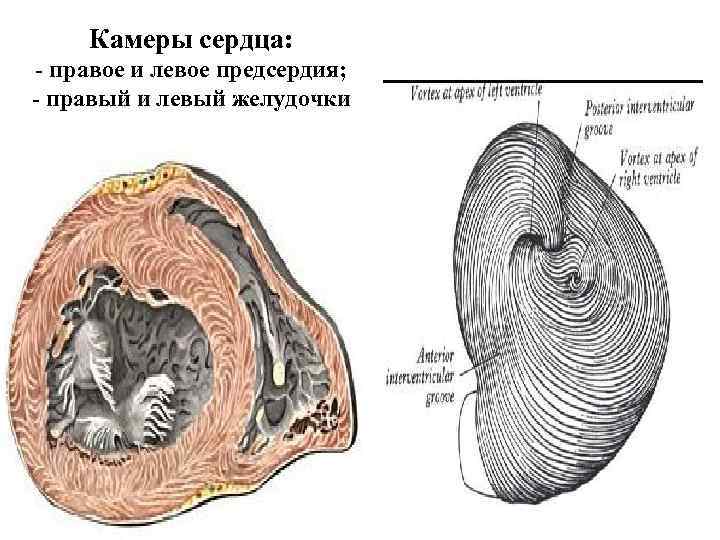 Камеры сердца: - правое и левое предсердия; - правый и левый желудочки
Камеры сердца: - правое и левое предсердия; - правый и левый желудочки
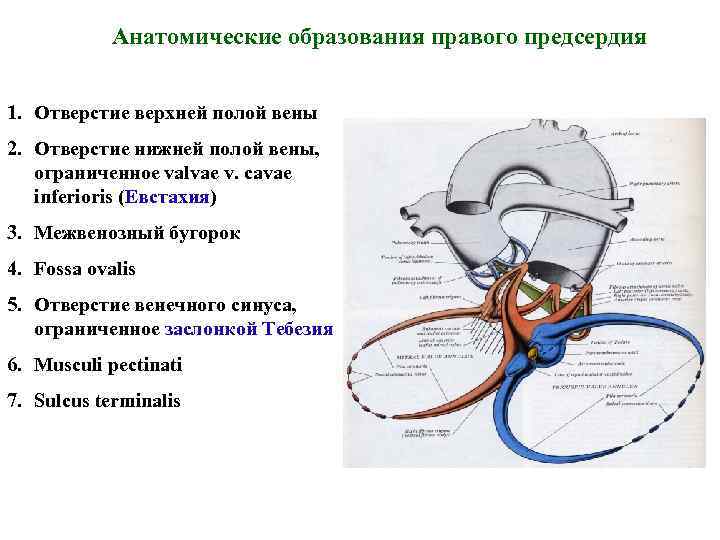 Анатомические образования правого предсердия 1. Отверстие верхней полой вены 2. Отверстие нижней полой вены, ограниченное valvae v. cavae inferioris (Евстахия) 3. Межвенозный бугорок 4. Fossa ovalis 5. Отверстие венечного синуса, ограниченное заслонкой Тебезия 6. Musculi pectinati 7. Sulcus terminalis
Анатомические образования правого предсердия 1. Отверстие верхней полой вены 2. Отверстие нижней полой вены, ограниченное valvae v. cavae inferioris (Евстахия) 3. Межвенозный бугорок 4. Fossa ovalis 5. Отверстие венечного синуса, ограниченное заслонкой Тебезия 6. Musculi pectinati 7. Sulcus terminalis
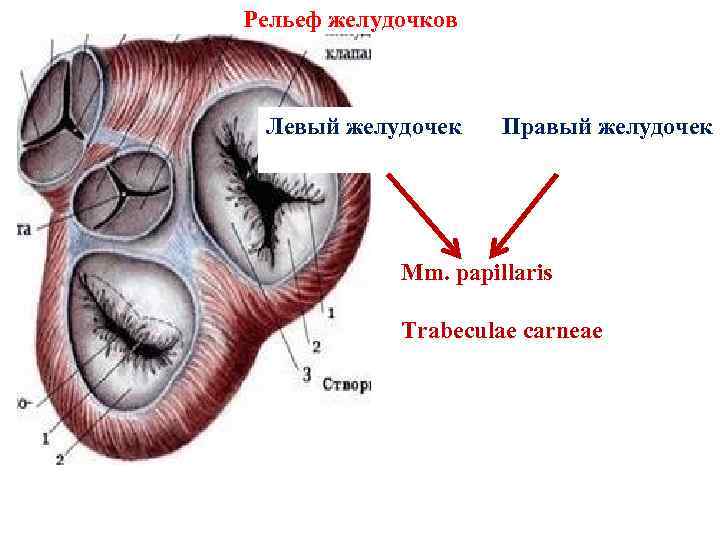 Рельеф желудочков Левый желудочек Правый желудочек Mm. papillaris Trabeculae carneae
Рельеф желудочков Левый желудочек Правый желудочек Mm. papillaris Trabeculae carneae
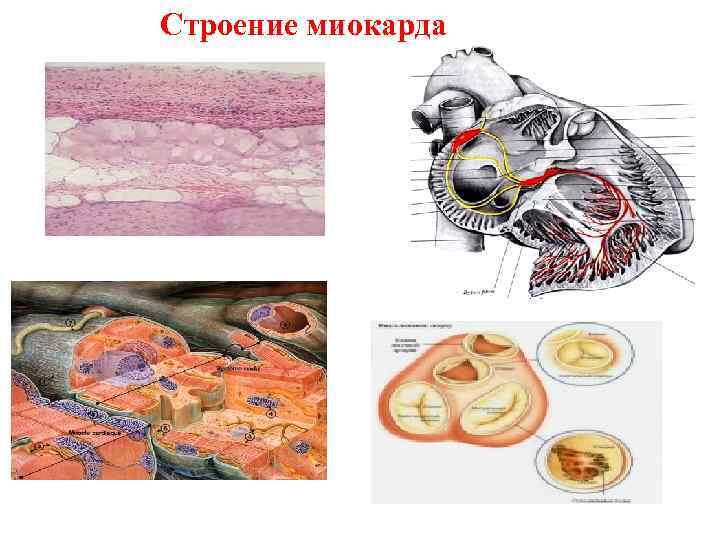 Строение миокарда
Строение миокарда
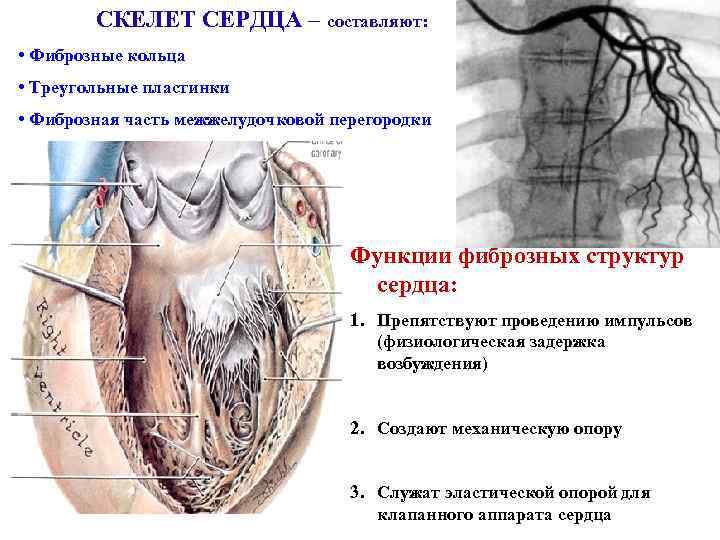 СКЕЛЕТ СЕРДЦА – составляют: • Фиброзные кольца • Треугольные пластинки • Фиброзная часть межжелудочковой перегородки Функции фиброзных структур сердца: 1. Препятствуют проведению импульсов (физиологическая задержка возбуждения) 2. Создают механическую опору 3. Служат эластической опорой для клапанного аппарата сердца
СКЕЛЕТ СЕРДЦА – составляют: • Фиброзные кольца • Треугольные пластинки • Фиброзная часть межжелудочковой перегородки Функции фиброзных структур сердца: 1. Препятствуют проведению импульсов (физиологическая задержка возбуждения) 2. Создают механическую опору 3. Служат эластической опорой для клапанного аппарата сердца
 Автоматизм — это способность сердца вырабатывать электрические импульсы при отсутствии внешних раздражений. Различают три центра автоматизма 1. Водитель ритма 1 порядка (пейсмекер, Кис-Фляка) (частота 60– 80 в минуту) 2. Водитель ритма 2 порядка (пейсмекер, Ашофф-Тавара) (частота 40– 60 в минуту) 3. Водитель ритма 3 порядка (пейсмекер) (частота 25– 45 в минуту)
Автоматизм — это способность сердца вырабатывать электрические импульсы при отсутствии внешних раздражений. Различают три центра автоматизма 1. Водитель ритма 1 порядка (пейсмекер, Кис-Фляка) (частота 60– 80 в минуту) 2. Водитель ритма 2 порядка (пейсмекер, Ашофф-Тавара) (частота 40– 60 в минуту) 3. Водитель ритма 3 порядка (пейсмекер) (частота 25– 45 в минуту)
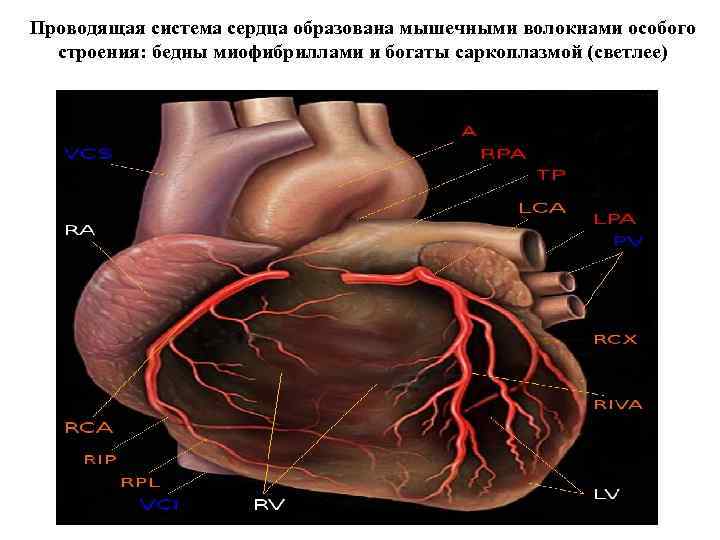 Проводящая система сердца образована мышечными волокнами особого строения: бедны миофибриллами и богаты саркоплазмой (светлее)
Проводящая система сердца образована мышечными волокнами особого строения: бедны миофибриллами и богаты саркоплазмой (светлее)
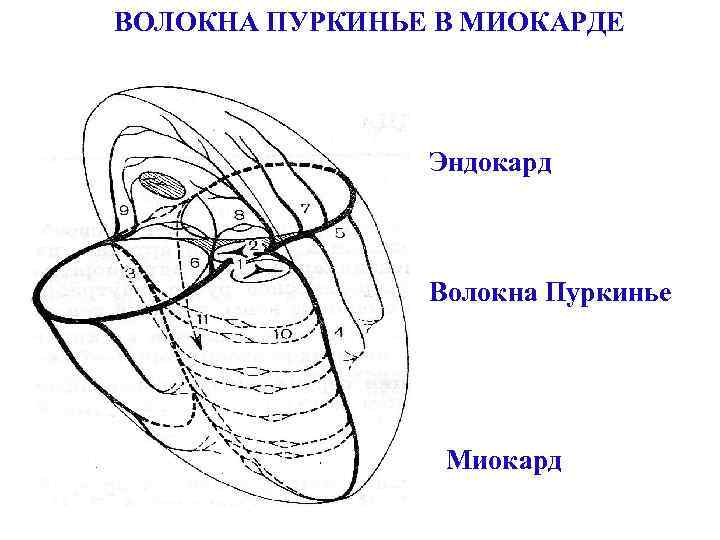 ВОЛОКНА ПУРКИНЬЕ В МИОКАРДЕ Эндокард Волокна Пуркинье Миокард
ВОЛОКНА ПУРКИНЬЕ В МИОКАРДЕ Эндокард Волокна Пуркинье Миокард
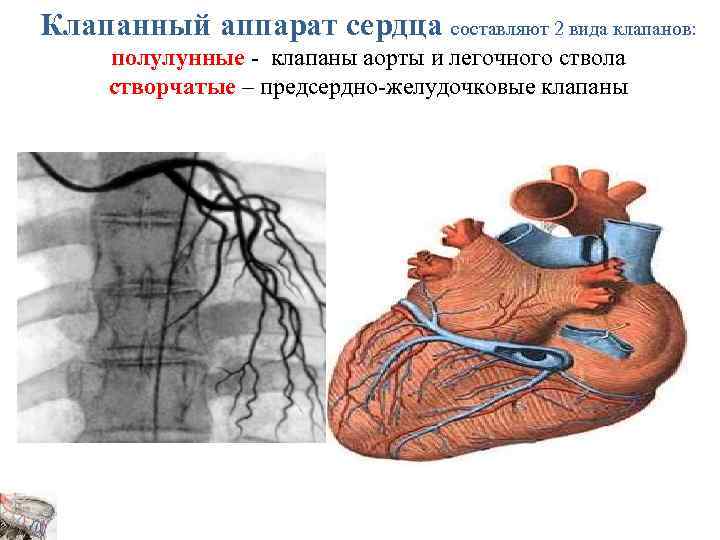 Клапанный аппарат сердца составляют 2 вида клапанов: полулунные - клапаны аорты и легочного ствола створчатые – предсердно-желудочковые клапаны
Клапанный аппарат сердца составляют 2 вида клапанов: полулунные - клапаны аорты и легочного ствола створчатые – предсердно-желудочковые клапаны
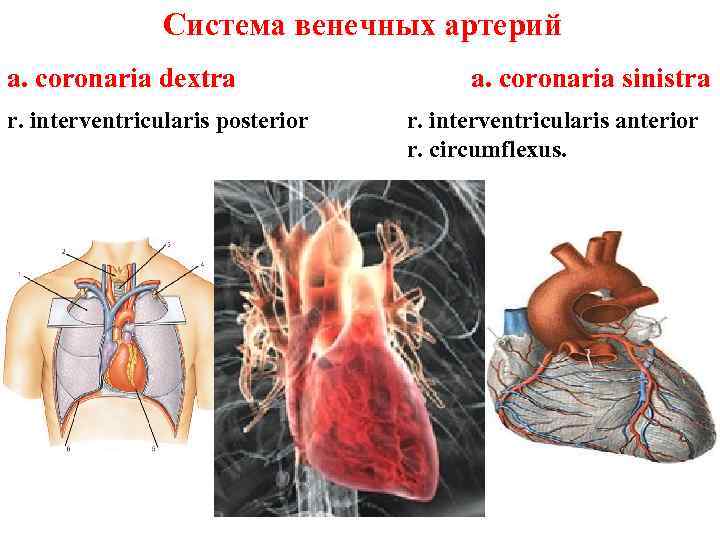 Система венечных артерий a. coronaria dextra r. interventricularis posterior a. coronaria sinistra r. interventricularis anterior r. circumflexus.
Система венечных артерий a. coronaria dextra r. interventricularis posterior a. coronaria sinistra r. interventricularis anterior r. circumflexus.
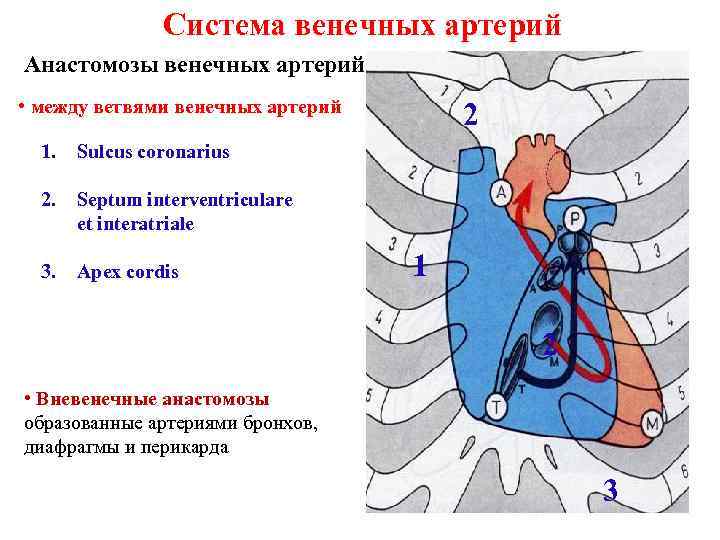 Система венечных артерий Анастомозы венечных артерий • между ветвями венечных артерий 1. Sulcus coronarius 2. Septum interventriculare et interatriale 3. Apex cordis 2 1 2 • Вневенечные анастомозы образованные артериями бронхов, диафрагмы и перикарда 3
Система венечных артерий Анастомозы венечных артерий • между ветвями венечных артерий 1. Sulcus coronarius 2. Septum interventriculare et interatriale 3. Apex cordis 2 1 2 • Вневенечные анастомозы образованные артериями бронхов, диафрагмы и перикарда 3
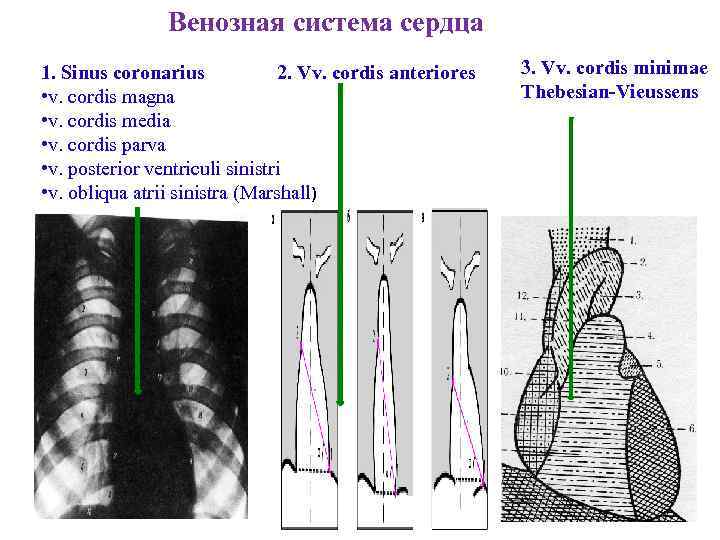 Венозная система сердца 1. Sinus coronarius 2. Vv. cordis anteriores • v. cordis magna • v. cordis media • v. cordis parva • v. posterior ventriculi sinistri • v. obliqua atrii sinistra (Marshall) 3. Vv. cordis minimae Thebesian-Vieussens
Венозная система сердца 1. Sinus coronarius 2. Vv. cordis anteriores • v. cordis magna • v. cordis media • v. cordis parva • v. posterior ventriculi sinistri • v. obliqua atrii sinistra (Marshall) 3. Vv. cordis minimae Thebesian-Vieussens
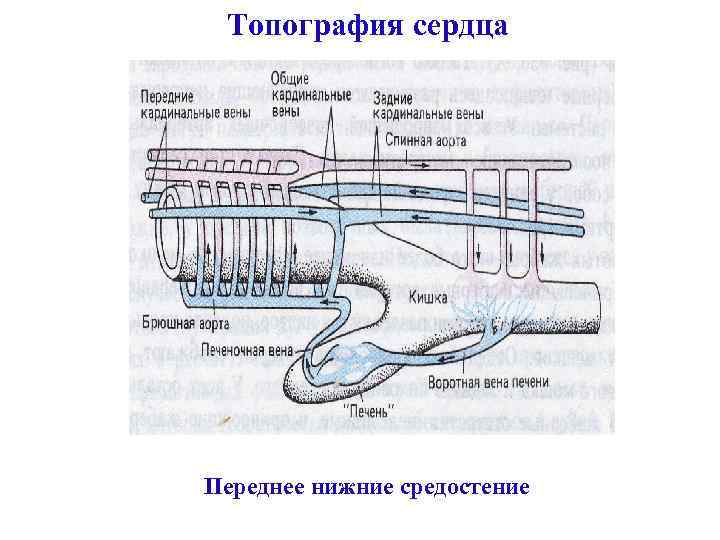 Топография сердца Переднее нижние средостение
Топография сердца Переднее нижние средостение
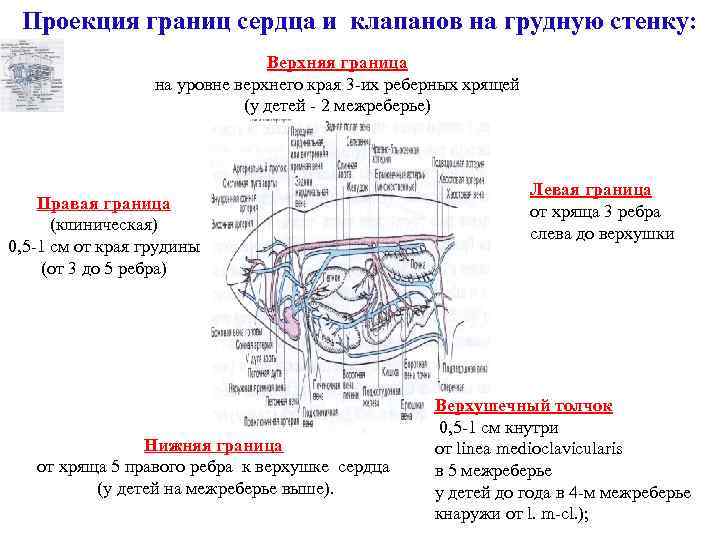 Проекция границ сердца и клапанов на грудную стенку: Верхняя граница на уровне верхнего края 3 -их реберных хрящей (у детей - 2 межреберье) Правая граница (клиническая) 0, 5 -1 см от края грудины (от 3 до 5 ребра) Нижняя граница от хряща 5 правого ребра к верхушке сердца (у детей на межреберье выше). Левая граница от хряща 3 ребра слева до верхушки Верхушечный толчок 0, 5 -1 см кнутри от linea medioclavicularis в 5 межреберье у детей до года в 4 -м межреберье кнаружи от l. m-cl. );
Проекция границ сердца и клапанов на грудную стенку: Верхняя граница на уровне верхнего края 3 -их реберных хрящей (у детей - 2 межреберье) Правая граница (клиническая) 0, 5 -1 см от края грудины (от 3 до 5 ребра) Нижняя граница от хряща 5 правого ребра к верхушке сердца (у детей на межреберье выше). Левая граница от хряща 3 ребра слева до верхушки Верхушечный толчок 0, 5 -1 см кнутри от linea medioclavicularis в 5 межреберье у детей до года в 4 -м межреберье кнаружи от l. m-cl. );
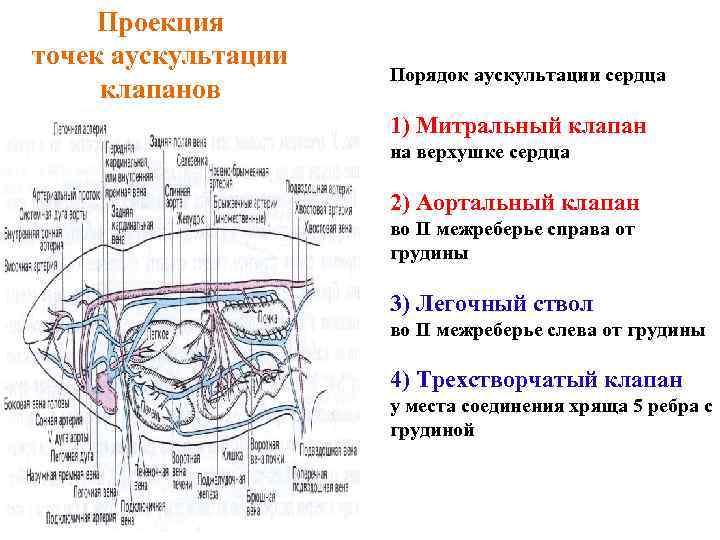 Проекция точек аускультации клапанов Порядок аускультации сердца 1) Митральный клапан на верхушке сердца 2) Аортальный клапан во II межреберье справа от грудины 3) Легочный ствол во II межреберье слева от грудины 4) Трехстворчатый клапан у места соединения хряща 5 ребра с грудиной
Проекция точек аускультации клапанов Порядок аускультации сердца 1) Митральный клапан на верхушке сердца 2) Аортальный клапан во II межреберье справа от грудины 3) Легочный ствол во II межреберье слева от грудины 4) Трехстворчатый клапан у места соединения хряща 5 ребра с грудиной
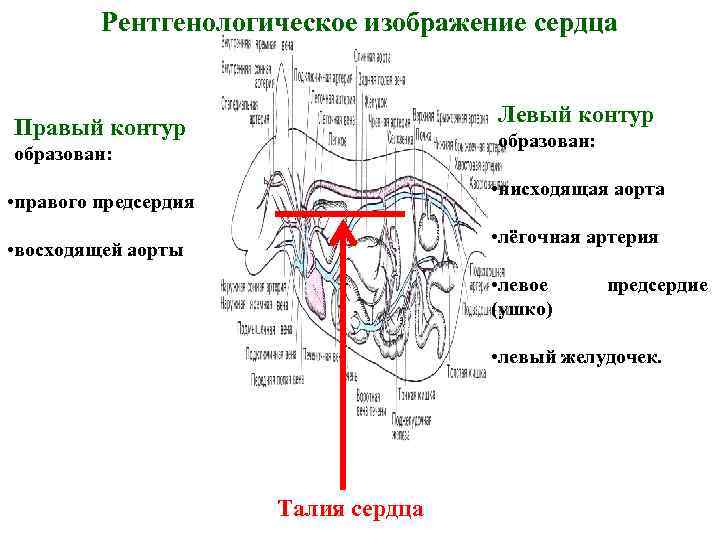 Рентгенологическое изображение сердца Левый контур Правый контур образован: • нисходящая аорта • правого предсердия • лёгочная артерия • восходящей аорты • левое (ушко) предсердие • левый желудочек. Талия сердца
Рентгенологическое изображение сердца Левый контур Правый контур образован: • нисходящая аорта • правого предсердия • лёгочная артерия • восходящей аорты • левое (ушко) предсердие • левый желудочек. Талия сердца
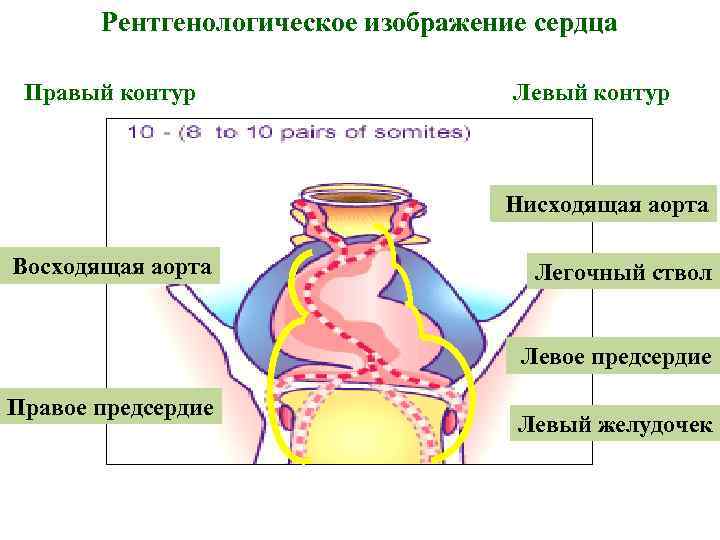 Рентгенологическое изображение сердца Правый контур Левый контур Нисходящая аорта Восходящая аорта Легочный ствол Левое предсердие Правое предсердие Левый желудочек
Рентгенологическое изображение сердца Правый контур Левый контур Нисходящая аорта Восходящая аорта Легочный ствол Левое предсердие Правое предсердие Левый желудочек
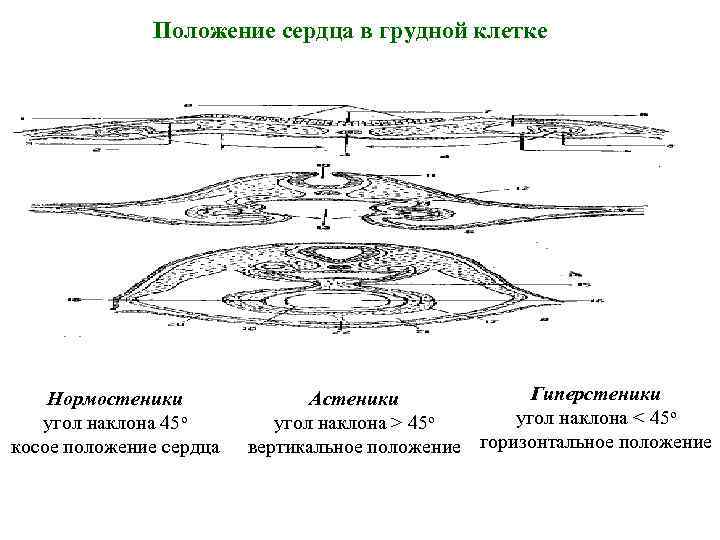 Положение сердца в грудной клетке Нормостеники угол наклона 45 о косое положение сердца Гиперстеники Астеники угол наклона < 45 о угол наклона > 45 о вертикальное положение горизонтальное положение
Положение сердца в грудной клетке Нормостеники угол наклона 45 о косое положение сердца Гиперстеники Астеники угол наклона < 45 о угол наклона > 45 о вертикальное положение горизонтальное положение
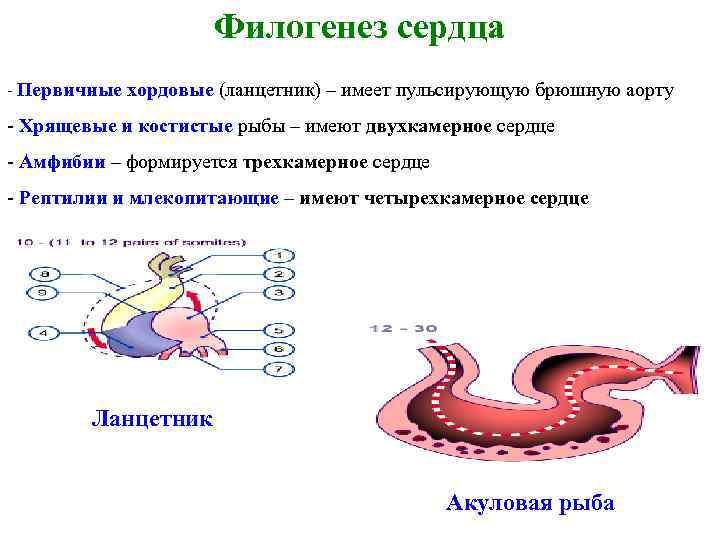 Филогенез сердца - Первичные хордовые (ланцетник) – имеет пульсирующую брюшную аорту - Хрящевые и костистые рыбы – имеют двухкамерное сердце - Амфибии – формируется трехкамерное сердце - Рептилии и млекопитающие – имеют четырехкамерное сердце Ланцетник Акуловая рыба
Филогенез сердца - Первичные хордовые (ланцетник) – имеет пульсирующую брюшную аорту - Хрящевые и костистые рыбы – имеют двухкамерное сердце - Амфибии – формируется трехкамерное сердце - Рептилии и млекопитающие – имеют четырехкамерное сердце Ланцетник Акуловая рыба
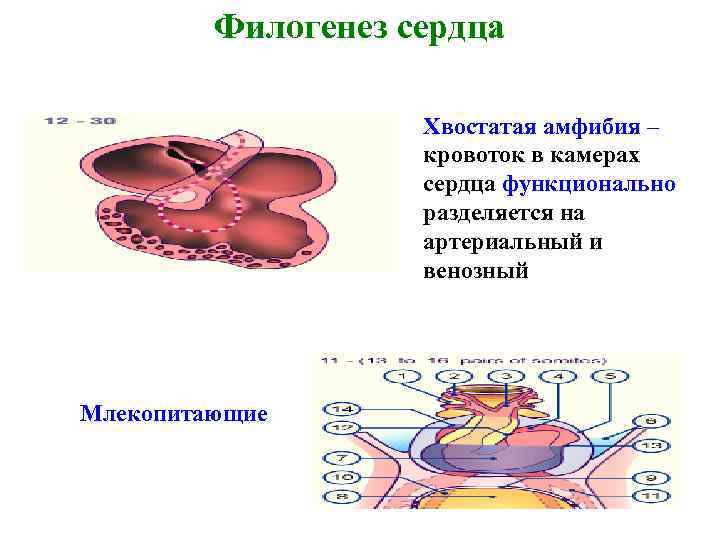 Филогенез сердца Хвостатая амфибия – кровоток в камерах сердца функционально разделяется на артериальный и венозный Млекопитающие
Филогенез сердца Хвостатая амфибия – кровоток в камерах сердца функционально разделяется на артериальный и венозный Млекопитающие
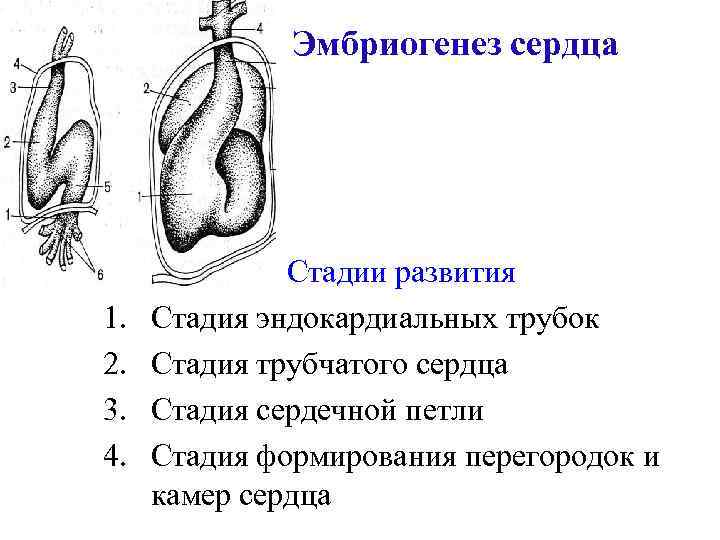 Эмбриогенез сердца 1. 2. 3. 4. Стадии развития Стадия эндокардиальных трубок Стадия трубчатого сердца Стадия сердечной петли Стадия формирования перегородок и камер сердца
Эмбриогенез сердца 1. 2. 3. 4. Стадии развития Стадия эндокардиальных трубок Стадия трубчатого сердца Стадия сердечной петли Стадия формирования перегородок и камер сердца
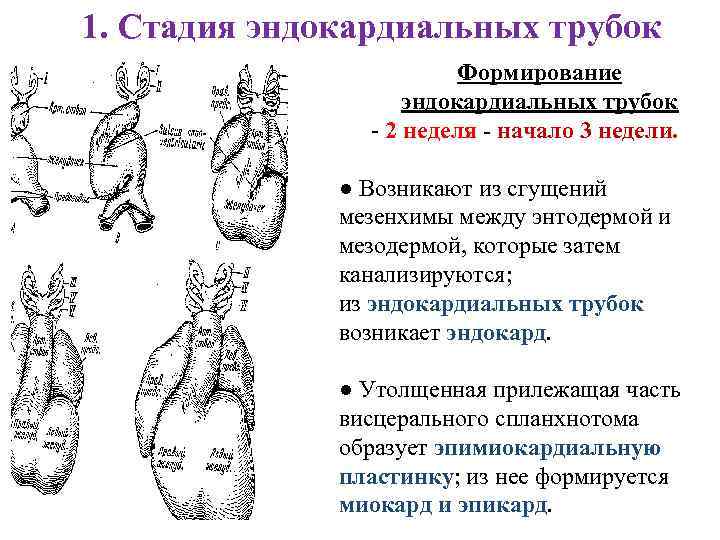 1. Стадия эндокардиальных трубок Формирование эндокардиальных трубок - 2 неделя - начало 3 недели. ● Возникают из сгущений мезенхимы между энтодермой и мезодермой, которые затем канализируются; из эндокардиальных трубок возникает эндокард. ● Утолщенная прилежащая часть висцерального спланхнотома образует эпимиокардиальную пластинку; из нее формируется миокард и эпикард.
1. Стадия эндокардиальных трубок Формирование эндокардиальных трубок - 2 неделя - начало 3 недели. ● Возникают из сгущений мезенхимы между энтодермой и мезодермой, которые затем канализируются; из эндокардиальных трубок возникает эндокард. ● Утолщенная прилежащая часть висцерального спланхнотома образует эпимиокардиальную пластинку; из нее формируется миокард и эпикард.
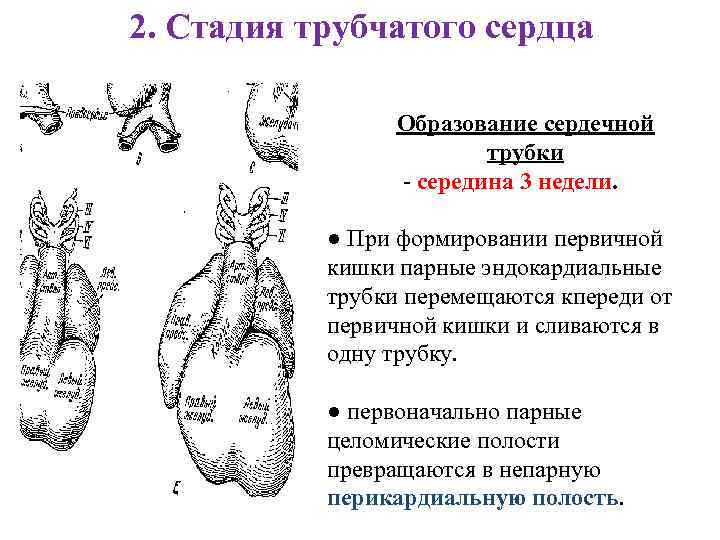 2. Стадия трубчатого сердца Образование сердечной трубки - середина 3 недели. ● При формировании первичной кишки парные эндокардиальные трубки перемещаются кпереди от первичной кишки и сливаются в одну трубку. ● первоначально парные целомические полости превращаются в непарную перикардиальную полость.
2. Стадия трубчатого сердца Образование сердечной трубки - середина 3 недели. ● При формировании первичной кишки парные эндокардиальные трубки перемещаются кпереди от первичной кишки и сливаются в одну трубку. ● первоначально парные целомические полости превращаются в непарную перикардиальную полость.
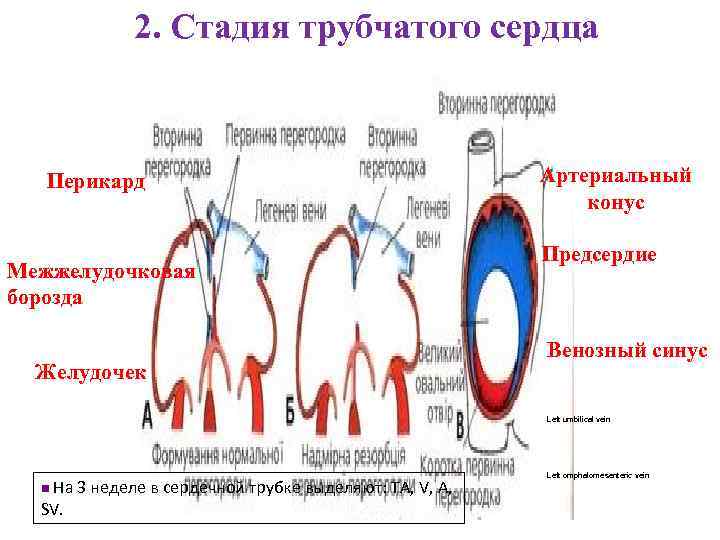 2. Стадия трубчатого сердца Перикард Межжелудочковая борозда Желудочек Артериальный конус Предсердие Венозный синус Left umbilical vein n На 3 неделе в сердечной трубке выделяют: ТА, V, А, SV. Left omphalomesenteric vein
2. Стадия трубчатого сердца Перикард Межжелудочковая борозда Желудочек Артериальный конус Предсердие Венозный синус Left umbilical vein n На 3 неделе в сердечной трубке выделяют: ТА, V, А, SV. Left omphalomesenteric vein
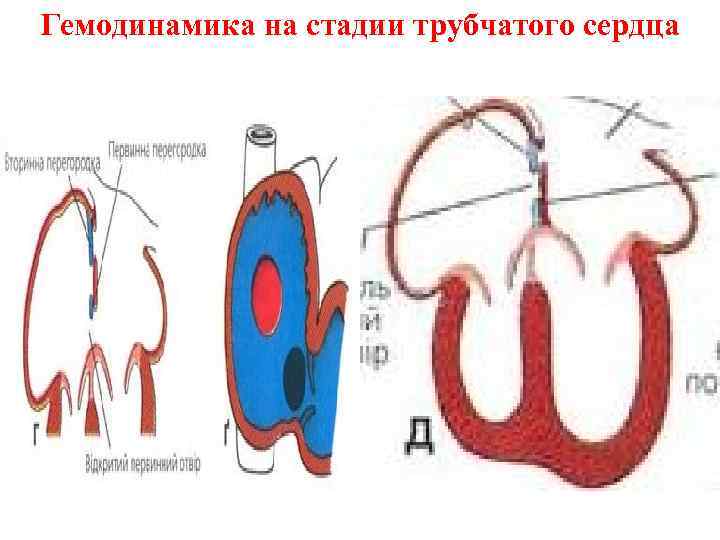 Гемодинамика на стадии трубчатого сердца
Гемодинамика на стадии трубчатого сердца
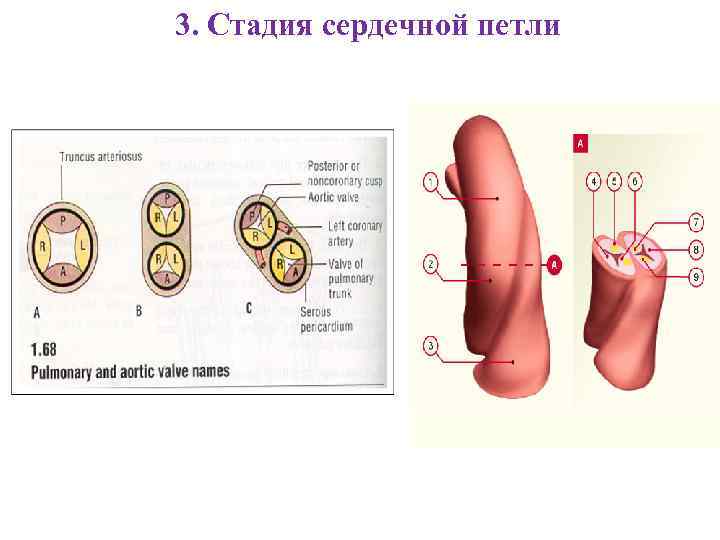 3. Стадия сердечной петли
3. Стадия сердечной петли
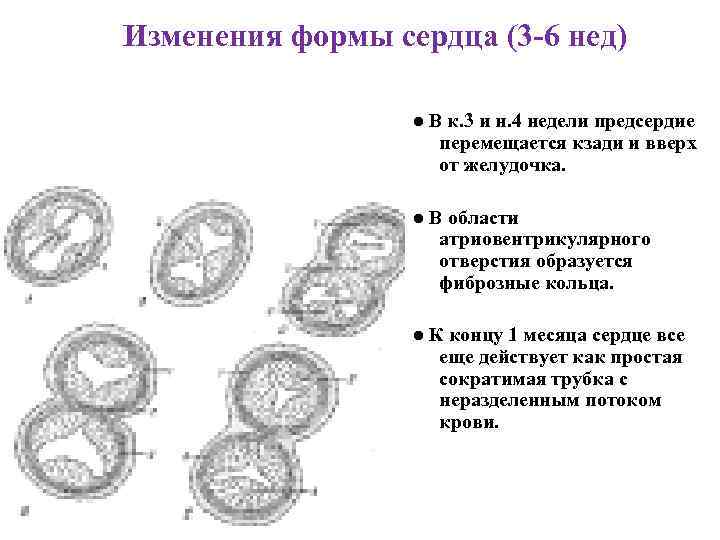 Изменения формы сердца (3 -6 нед) ● В к. 3 и н. 4 недели предсердие перемещается кзади и вверх от желудочка. ● В области атриовентрикулярного отверстия образуется фиброзные кольца. ● К концу 1 месяца сердце все еще действует как простая сократимая трубка с неразделенным потоком крови.
Изменения формы сердца (3 -6 нед) ● В к. 3 и н. 4 недели предсердие перемещается кзади и вверх от желудочка. ● В области атриовентрикулярного отверстия образуется фиброзные кольца. ● К концу 1 месяца сердце все еще действует как простая сократимая трубка с неразделенным потоком крови.
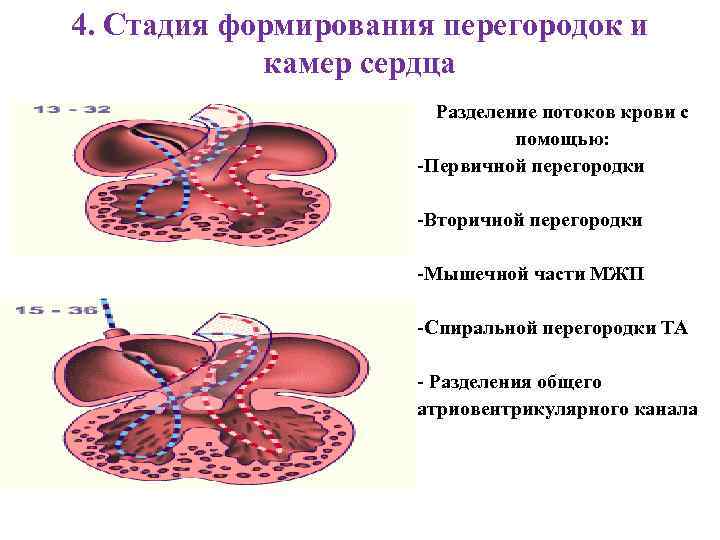 4. Стадия формирования перегородок и камер сердца Разделение потоков крови с помощью: -Первичной перегородки -Вторичной перегородки -Мышечной части МЖП -Спиральной перегородки ТА - Разделения общего атриовентрикулярного канала
4. Стадия формирования перегородок и камер сердца Разделение потоков крови с помощью: -Первичной перегородки -Вторичной перегородки -Мышечной части МЖП -Спиральной перегородки ТА - Разделения общего атриовентрикулярного канала
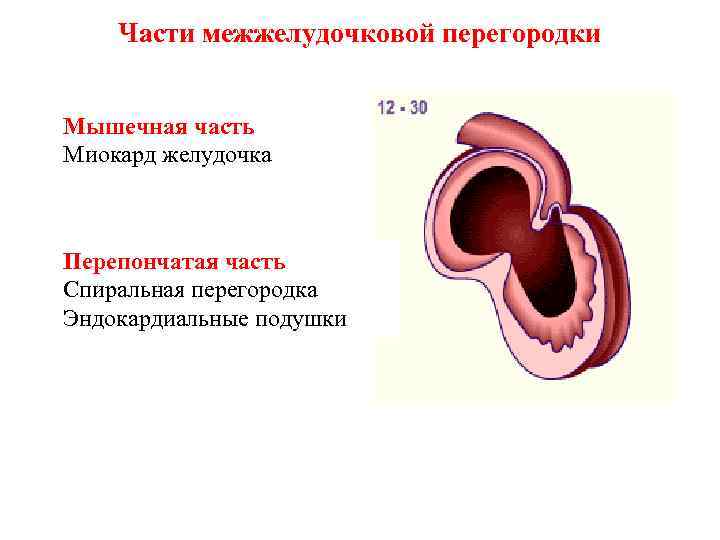 Части межжелудочковой перегородки Мышечная часть Миокард желудочка Перепончатая часть Спиральная перегородка Эндокардиальные подушки
Части межжелудочковой перегородки Мышечная часть Миокард желудочка Перепончатая часть Спиральная перегородка Эндокардиальные подушки
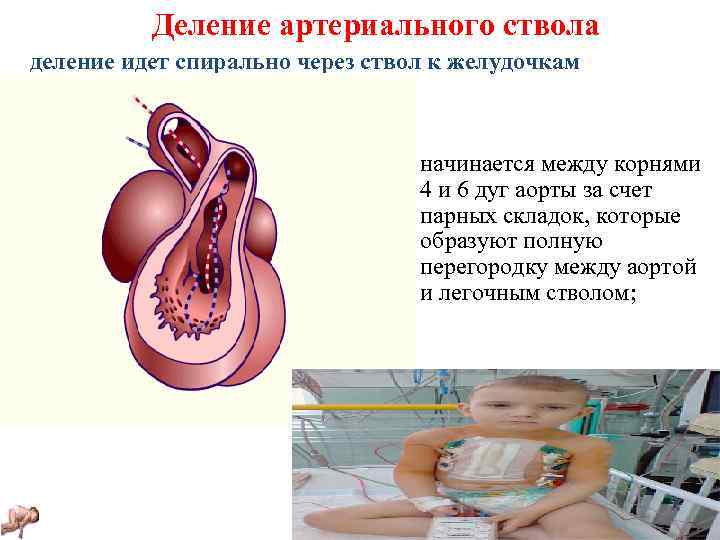 Деление артериального ствола деление идет спирально через ствол к желудочкам • начинается между корнями 4 и 6 дуг аорты за счет парных складок, которые образуют полную перегородку между аортой и легочным стволом;
Деление артериального ствола деление идет спирально через ствол к желудочкам • начинается между корнями 4 и 6 дуг аорты за счет парных складок, которые образуют полную перегородку между аортой и легочным стволом;
 Разделение потоков крови
Разделение потоков крови
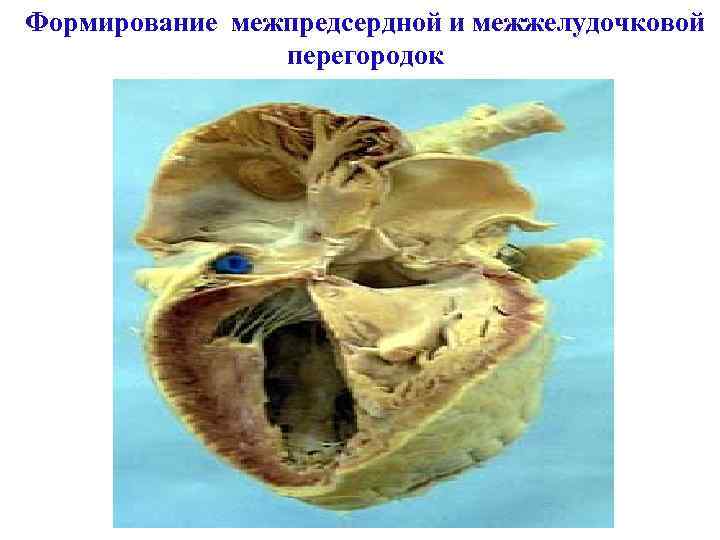 Формирование межпредсердной и межжелудочковой перегородок
Формирование межпредсердной и межжелудочковой перегородок
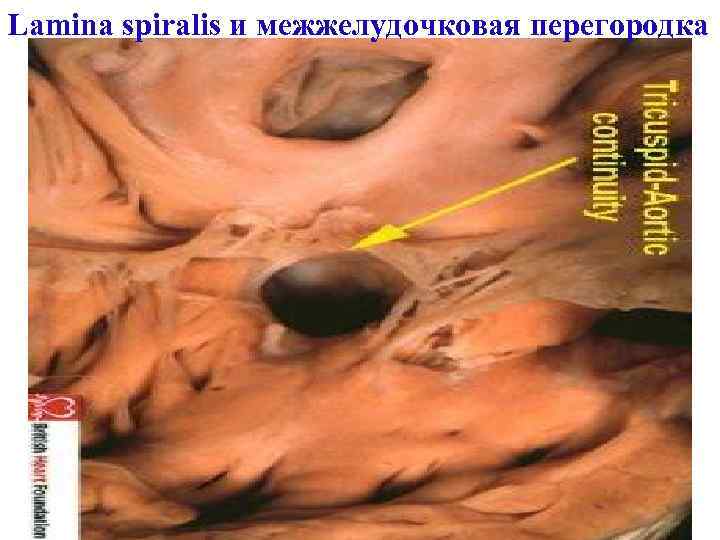 Lamina spiralis и межжелудочковая перегородка
Lamina spiralis и межжелудочковая перегородка
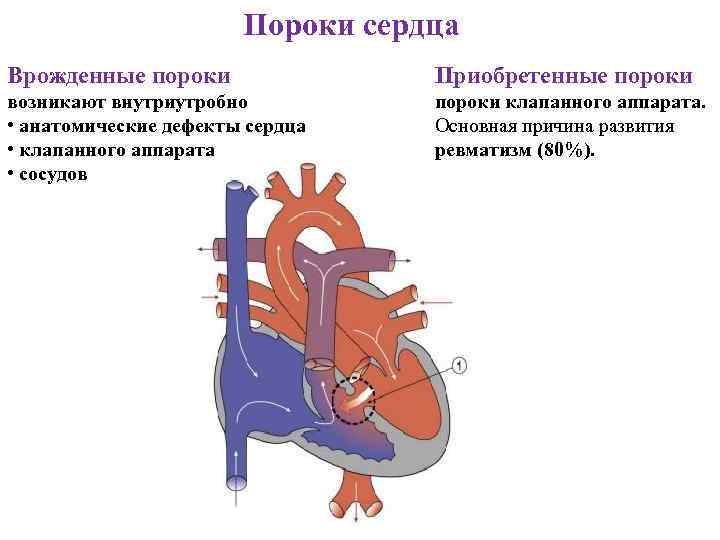 Пороки сердца Врожденные пороки Приобретенные пороки возникают внутриутробно • анатомические дефекты сердца • клапанного аппарата • сосудов пороки клапанного аппарата. Основная причина развития ревматизм (80%).
Пороки сердца Врожденные пороки Приобретенные пороки возникают внутриутробно • анатомические дефекты сердца • клапанного аппарата • сосудов пороки клапанного аппарата. Основная причина развития ревматизм (80%).
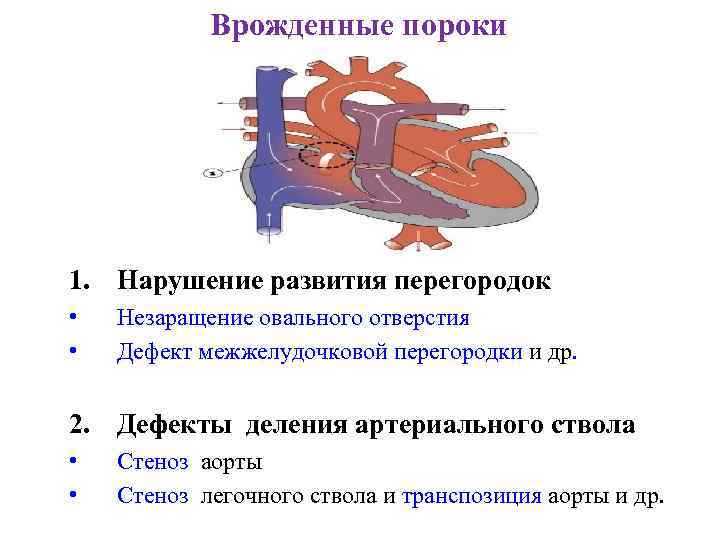 Врожденные пороки 1. Нарушение развития перегородок • • Незаращение овального отверстия Дефект межжелудочковой перегородки и др. 2. Дефекты деления артериального ствола • • Стеноз аорты Стеноз легочного ствола и транспозиция аорты и др.
Врожденные пороки 1. Нарушение развития перегородок • • Незаращение овального отверстия Дефект межжелудочковой перегородки и др. 2. Дефекты деления артериального ствола • • Стеноз аорты Стеноз легочного ствола и транспозиция аорты и др.
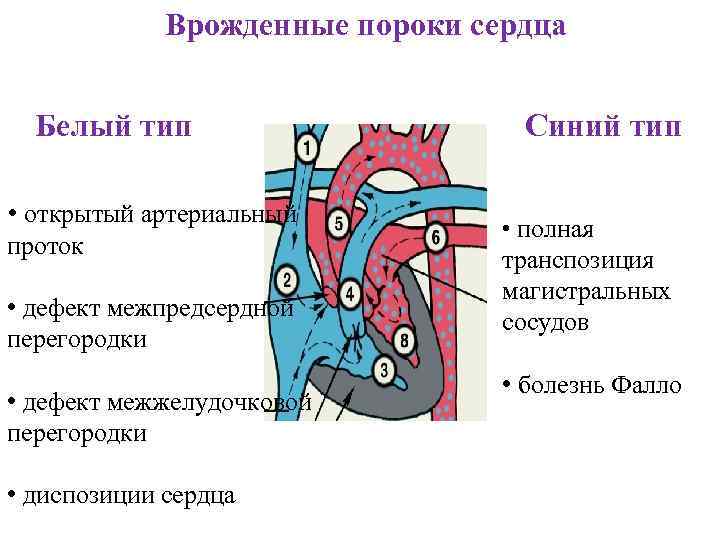 Врожденные пороки сердца Белый тип • открытый артериальный проток • дефект межпредсердной перегородки • дефект межжелудочковой перегородки • диспозиции сердца Синий тип • полная транспозиция магистральных сосудов • болезнь Фалло
Врожденные пороки сердца Белый тип • открытый артериальный проток • дефект межпредсердной перегородки • дефект межжелудочковой перегородки • диспозиции сердца Синий тип • полная транспозиция магистральных сосудов • болезнь Фалло
 Врожденные пороки сердца 1, 5 млн детей 10 человек на 1000 родившихся По данным на 2007 год
Врожденные пороки сердца 1, 5 млн детей 10 человек на 1000 родившихся По данным на 2007 год
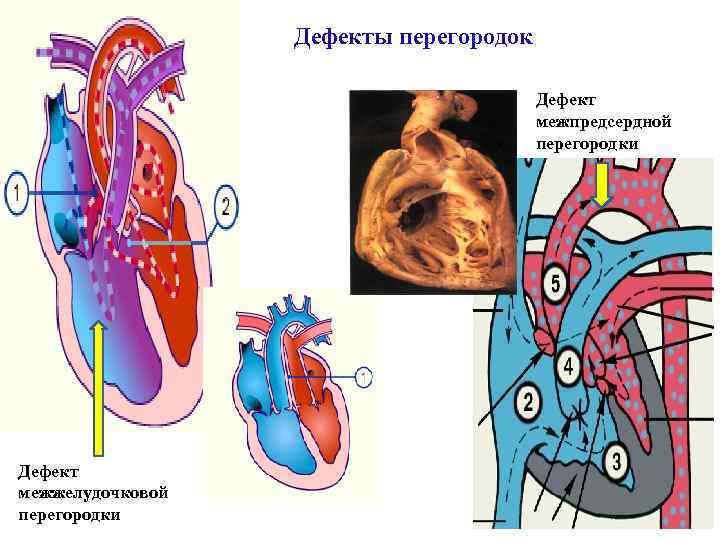 Дефекты перегородок Дефект межпредсердной перегородки Дефект межжелудочковой перегородки
Дефекты перегородок Дефект межпредсердной перегородки Дефект межжелудочковой перегородки
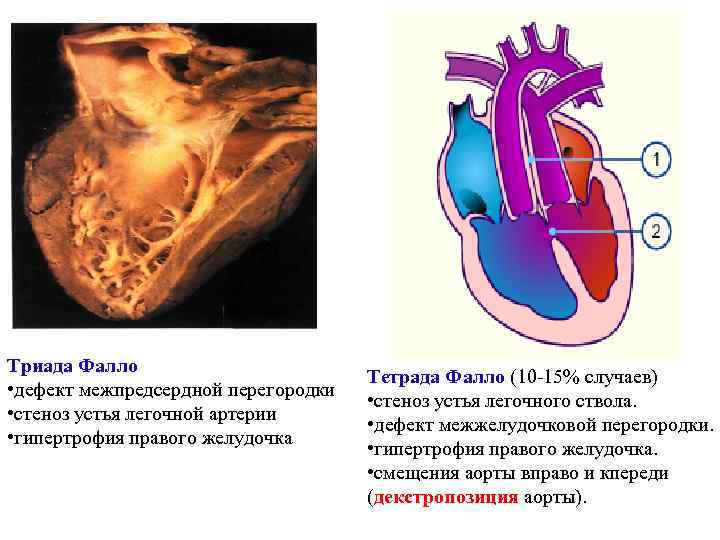 Триада Фалло • дефект межпредсердной перегородки • стеноз устья легочной артерии • гипертрофия правого желудочка Тетрада Фалло (10 -15% случаев) • стеноз устья легочного ствола. • дефект межжелудочковой перегородки. • гипертрофия правого желудочка. • смещения аорты вправо и кпереди (декстропозиция аорты).
Триада Фалло • дефект межпредсердной перегородки • стеноз устья легочной артерии • гипертрофия правого желудочка Тетрада Фалло (10 -15% случаев) • стеноз устья легочного ствола. • дефект межжелудочковой перегородки. • гипертрофия правого желудочка. • смещения аорты вправо и кпереди (декстропозиция аорты).
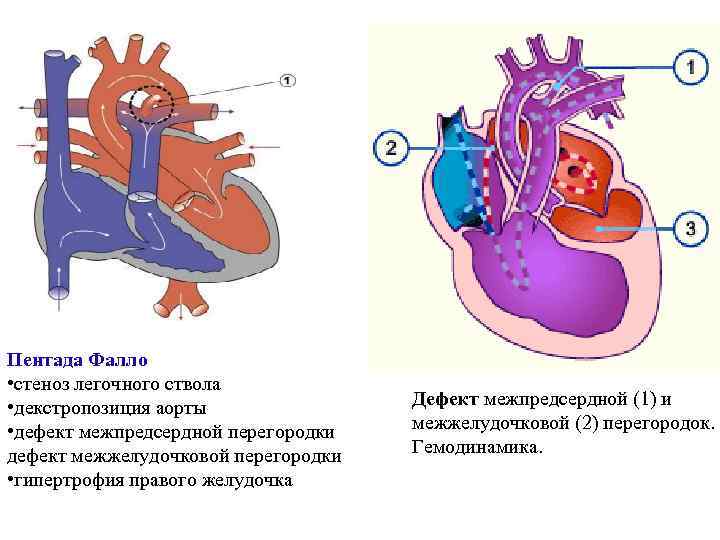 Пентада Фалло • стеноз легочного ствола • декстропозиция аорты • дефект межпредсердной перегородки дефект межжелудочковой перегородки • гипертрофия правого желудочка Дефект межпредсердной (1) и межжелудочковой (2) перегородок. Гемодинамика.
Пентада Фалло • стеноз легочного ствола • декстропозиция аорты • дефект межпредсердной перегородки дефект межжелудочковой перегородки • гипертрофия правого желудочка Дефект межпредсердной (1) и межжелудочковой (2) перегородок. Гемодинамика.
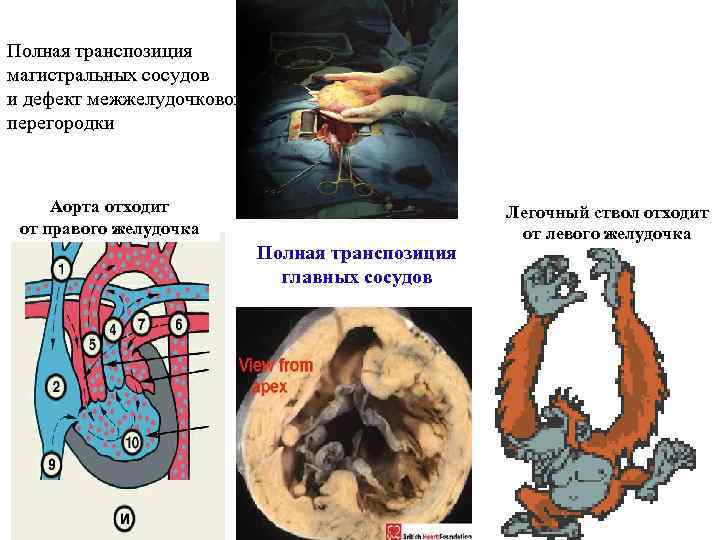 Полная транспозиция магистральных сосудов и дефект межжелудочковой перегородки Аорта отходит от правого желудочка Полная транспозиция главных сосудов Легочный ствол отходит от левого желудочка
Полная транспозиция магистральных сосудов и дефект межжелудочковой перегородки Аорта отходит от правого желудочка Полная транспозиция главных сосудов Легочный ствол отходит от левого желудочка
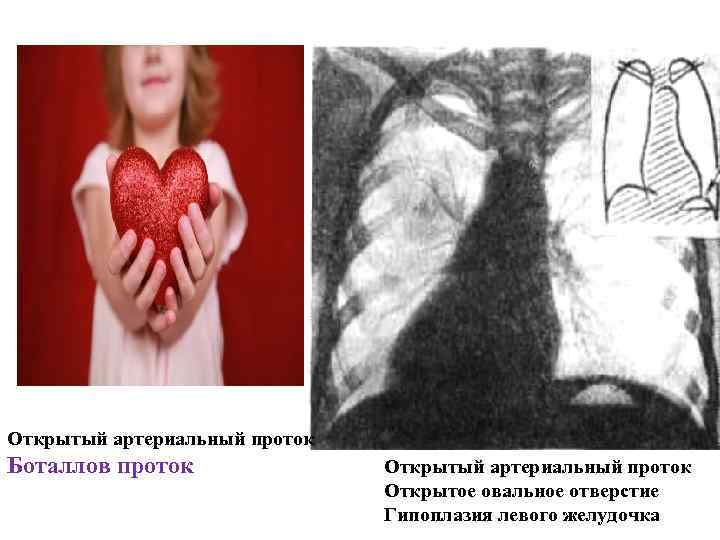 Открытый артериальный проток Боталлов проток Открытый артериальный проток Открытое овальное отверстие Гипоплазия левого желудочка
Открытый артериальный проток Боталлов проток Открытый артериальный проток Открытое овальное отверстие Гипоплазия левого желудочка
 Трёхкамерное сердце. Общий желудочек Вид со стороны предсердий.
Трёхкамерное сердце. Общий желудочек Вид со стороны предсердий.
 Дополнительная литература: 1. 2. 3. 4. 5. 6. 7. Грин Н. , Стаут У. , Тейлор Д. Биология: В 3 -х томах. Т. 2. : Пер. с англ. / Под ред. Р. Сопера. - М. : «Мир» , 1990. - 325 с. , ил Кнорре А. Г. Краткий очерк эмбриологии человека с элементами сравнительной, экспериментальной и патологической эмбриологии. 2 -е издание. Л. : «Медицина» , 1967. 267 с. с ил. Максимов В. И. Основы анатомии и физиологии человека. М. : Колос. С, 2004 – 167 с. Морфология развивающегося сердца (структура, ультраструктура, метаболизм) / Козлов В. А. , Твердохлеб И. В. , Шпонька И. С. , Мишалов В. Д. - Днепропетровск, 1995. - 220 с. Развитие кровеносных и лимфатических сосудов / Бобрик И. И. , Шевченко Е. А. , Черкасов В. Г. - К. : Здоровья, 1991. - 206 с. Федюкович Н. И. Анатомия и физиология человека. Ростов н/Дону: Феникс, 2005 – 478 с. Шпонька И. С. Гистогенетические процессы в развивающемся миокарде млекопитающих: Монография. - Днепропетровск: «Пороги» , 1996. - 228 с.
Дополнительная литература: 1. 2. 3. 4. 5. 6. 7. Грин Н. , Стаут У. , Тейлор Д. Биология: В 3 -х томах. Т. 2. : Пер. с англ. / Под ред. Р. Сопера. - М. : «Мир» , 1990. - 325 с. , ил Кнорре А. Г. Краткий очерк эмбриологии человека с элементами сравнительной, экспериментальной и патологической эмбриологии. 2 -е издание. Л. : «Медицина» , 1967. 267 с. с ил. Максимов В. И. Основы анатомии и физиологии человека. М. : Колос. С, 2004 – 167 с. Морфология развивающегося сердца (структура, ультраструктура, метаболизм) / Козлов В. А. , Твердохлеб И. В. , Шпонька И. С. , Мишалов В. Д. - Днепропетровск, 1995. - 220 с. Развитие кровеносных и лимфатических сосудов / Бобрик И. И. , Шевченко Е. А. , Черкасов В. Г. - К. : Здоровья, 1991. - 206 с. Федюкович Н. И. Анатомия и физиология человека. Ростов н/Дону: Феникс, 2005 – 478 с. Шпонька И. С. Гистогенетические процессы в развивающемся миокарде млекопитающих: Монография. - Днепропетровск: «Пороги» , 1996. - 228 с.
 Спасибо за внимание!!!
Спасибо за внимание!!!


 У зародышей позвоночных сердце исходно развивается в переднем отделе, в области спланхнической мезодермы; лишь позже оно перемещается в область груди. У амфибий две презумптивные области образования сердца вначале находятся в са мом переднем участке мезодермальной мантии. Во время нейруляции эти две области сходятся в вентральной части зародыша, формируя сердечную трубку и общую перикардиальную полость. У амниот птиц и млекопитающих — сердце также развивается путем слияния парных зачатков, но слияние происходит значительно позже в развитии. У этих позвоночных зародыш представляет собой уплощенный диск и мезодерма боковых пластинок не окружает желток полностью. Презумптивные клетки сердца начинают мигрировать из боковых участков мезодермы (на уровне гензеновского узелка), когда зародыш достигнет возраста всего 6— 7 ч. К этому времени зародыш еще относительно просто устроен, он состоит только из трех зародышевых листков. Клетки будущего сердца, двигаясь между эктодермой и энтодермой к середине зародыша, сохраняют тесный контакт с поверхностью энтодермы (рис. 6. 18; Linask, Lash, 1986). Когда же они достигают передней области зародыша, где находится кишка, их миграция прекращается. Два формирующих сердце зачатка независимо друг от друга претерпевают четко выраженную дифференцировку. У птиц и млекопитающих каждый из них превращается в трубку с двойными стенками: внутренней - эндокардом и наружной - эпимиокардом. Эндокард будет формировать внутреннюю выстилку сердца, а эпимиокард — мышцу сердца, которая в течение всей жизни организма будет служить насосом, перекачивающим кровь. Пока зародыш проходит период нейруляции, выпячивание складки спланхнической мезодермы приводит к обособлению передней кишки (рис. 6. 19). В результате две трубки сердца сближаются и в конце концов сливаются вместе, соединяя эпимиокард в одну трубку. Два эндокарда в течение короткого времени находятся в общей камере, но они также сольются. К этому времени исходно парные целомические камеры объединяются, образуя полость тела, в которой располагается сердце. Билатеральное происхождение сердца можно продемонстрировать результатами эксперимента, в котором хирургическим способом предотвращали слияние мезодермы боковых пластинок (Gräper, 1907; De. Haan, 1959). Опыт приводил к состоянию, известному под названием cardia bifida, при котором с каждой стороны тела формируется отдельное сердце (рис. 6. 20). Следующей ступенью формирования сердца является слияние эндокардиальных трубок в единую насосную камеру (см. рис. 6. 19. В. Г). Это слияние происходит у куриного зародыша примерно через 29 ч инкубации, а у человека — через три недели беременности. Неслившиеся задние участки эндокарда становятся отверстиями желточных вен в сердце (рис. 6. 21). Эти вены будут нести питательные вещества из желточного мешка в венозный синус. Затем кровь через похожий на створку клапан проходит в предсердный отдел сердца. Сокращения артериального ствола быстро прогоняют кровь в аорту. Пульсация сердца начинается еще во время слияния парных зачатков. Водителем ритма (пейсмекером) сердечных сокращений является венозный синус. Здесь начинается сокращение, а затем волна сокращений распространяется по трубчатому сердцу. Таким образом, сердце начинает перекачивать кровь еще до того, как завершится образование сложной системы клапанов. Клетки сердечной мышцы обладают собственной внутренне присущей им способностью к сокращению: изолированные мышечные клетки 7 -дневного зародыша крысы или куриного зародыша, помещенные в чашку Петри, продолжают сокращаться (Harary, Farley, 1963; De. Haan, 1967). У зародыша эти сокращения начинают регулироваться электрическими стимулами, поступающими из мозжечка через блуждающий нерв. Через 4 дня электрокардиограмма у куриного зародыша становится очень сходной с электрокардиограммой взрослой особи.
У зародышей позвоночных сердце исходно развивается в переднем отделе, в области спланхнической мезодермы; лишь позже оно перемещается в область груди. У амфибий две презумптивные области образования сердца вначале находятся в са мом переднем участке мезодермальной мантии. Во время нейруляции эти две области сходятся в вентральной части зародыша, формируя сердечную трубку и общую перикардиальную полость. У амниот птиц и млекопитающих — сердце также развивается путем слияния парных зачатков, но слияние происходит значительно позже в развитии. У этих позвоночных зародыш представляет собой уплощенный диск и мезодерма боковых пластинок не окружает желток полностью. Презумптивные клетки сердца начинают мигрировать из боковых участков мезодермы (на уровне гензеновского узелка), когда зародыш достигнет возраста всего 6— 7 ч. К этому времени зародыш еще относительно просто устроен, он состоит только из трех зародышевых листков. Клетки будущего сердца, двигаясь между эктодермой и энтодермой к середине зародыша, сохраняют тесный контакт с поверхностью энтодермы (рис. 6. 18; Linask, Lash, 1986). Когда же они достигают передней области зародыша, где находится кишка, их миграция прекращается. Два формирующих сердце зачатка независимо друг от друга претерпевают четко выраженную дифференцировку. У птиц и млекопитающих каждый из них превращается в трубку с двойными стенками: внутренней - эндокардом и наружной - эпимиокардом. Эндокард будет формировать внутреннюю выстилку сердца, а эпимиокард — мышцу сердца, которая в течение всей жизни организма будет служить насосом, перекачивающим кровь. Пока зародыш проходит период нейруляции, выпячивание складки спланхнической мезодермы приводит к обособлению передней кишки (рис. 6. 19). В результате две трубки сердца сближаются и в конце концов сливаются вместе, соединяя эпимиокард в одну трубку. Два эндокарда в течение короткого времени находятся в общей камере, но они также сольются. К этому времени исходно парные целомические камеры объединяются, образуя полость тела, в которой располагается сердце. Билатеральное происхождение сердца можно продемонстрировать результатами эксперимента, в котором хирургическим способом предотвращали слияние мезодермы боковых пластинок (Gräper, 1907; De. Haan, 1959). Опыт приводил к состоянию, известному под названием cardia bifida, при котором с каждой стороны тела формируется отдельное сердце (рис. 6. 20). Следующей ступенью формирования сердца является слияние эндокардиальных трубок в единую насосную камеру (см. рис. 6. 19. В. Г). Это слияние происходит у куриного зародыша примерно через 29 ч инкубации, а у человека — через три недели беременности. Неслившиеся задние участки эндокарда становятся отверстиями желточных вен в сердце (рис. 6. 21). Эти вены будут нести питательные вещества из желточного мешка в венозный синус. Затем кровь через похожий на створку клапан проходит в предсердный отдел сердца. Сокращения артериального ствола быстро прогоняют кровь в аорту. Пульсация сердца начинается еще во время слияния парных зачатков. Водителем ритма (пейсмекером) сердечных сокращений является венозный синус. Здесь начинается сокращение, а затем волна сокращений распространяется по трубчатому сердцу. Таким образом, сердце начинает перекачивать кровь еще до того, как завершится образование сложной системы клапанов. Клетки сердечной мышцы обладают собственной внутренне присущей им способностью к сокращению: изолированные мышечные клетки 7 -дневного зародыша крысы или куриного зародыша, помещенные в чашку Петри, продолжают сокращаться (Harary, Farley, 1963; De. Haan, 1967). У зародыша эти сокращения начинают регулироваться электрическими стимулами, поступающими из мозжечка через блуждающий нерв. Через 4 дня электрокардиограмма у куриного зародыша становится очень сходной с электрокардиограммой взрослой особи.



 Транспорт Са 2+ в кардиомиоците. В покое кальциевые каналы сарколеммы закрыты, а внутриклеточный Са 2+ находится в основном в саркоплазматическом ретикулуме. При возбуждении открываются потенциалзависимые натриевые (не показаны) и кальциевые каналы сарколеммы, Na+ и Са 2+ входят в клетку. Вход Са 2+ через каналы Ттрубочек вызывает выброс Са 2+ из саркоплазматического ретикулума, и мышца сокращается. Для расслабления необходим обратный захват Са 2+ при помощи Са 2+-АТФазы саркоплазматического ретикулума. Таким образом, пассивный перенос Са 2+ (по электрохимическому градиенту) отвечает за сокращение, активный - за расслабление. В диастолу действуют и другие процессы активного транспорта: Na+, K+-ATФaзa поддерживает трансмембранный градиент концентраций Na+ и К+, необходимый для обеспечения потенциала действия, а создающийся при этом электрохимический градиент для Na+ используется в работе На+/Са 2+обменника. Последний выводит Са 2+ из клетки. Ф - фосфат.
Транспорт Са 2+ в кардиомиоците. В покое кальциевые каналы сарколеммы закрыты, а внутриклеточный Са 2+ находится в основном в саркоплазматическом ретикулуме. При возбуждении открываются потенциалзависимые натриевые (не показаны) и кальциевые каналы сарколеммы, Na+ и Са 2+ входят в клетку. Вход Са 2+ через каналы Ттрубочек вызывает выброс Са 2+ из саркоплазматического ретикулума, и мышца сокращается. Для расслабления необходим обратный захват Са 2+ при помощи Са 2+-АТФазы саркоплазматического ретикулума. Таким образом, пассивный перенос Са 2+ (по электрохимическому градиенту) отвечает за сокращение, активный - за расслабление. В диастолу действуют и другие процессы активного транспорта: Na+, K+-ATФaзa поддерживает трансмембранный градиент концентраций Na+ и К+, необходимый для обеспечения потенциала действия, а создающийся при этом электрохимический градиент для Na+ используется в работе На+/Са 2+обменника. Последний выводит Са 2+ из клетки. Ф - фосфат.
 История открытия кровообращения Клавдий Гален (131 - 201 гг. до н. э. ) доказал, что в артериях течет кровь, а не воздух. Мигель Сервет (1511 -1553) открыл малый (легочной) круг кровообращения. Андреа Чезальпино (1519– 1603) дал правильное описание малого круга кровообращения
История открытия кровообращения Клавдий Гален (131 - 201 гг. до н. э. ) доказал, что в артериях течет кровь, а не воздух. Мигель Сервет (1511 -1553) открыл малый (легочной) круг кровообращения. Андреа Чезальпино (1519– 1603) дал правильное описание малого круга кровообращения
 Ульям Гарвей
Ульям Гарвей
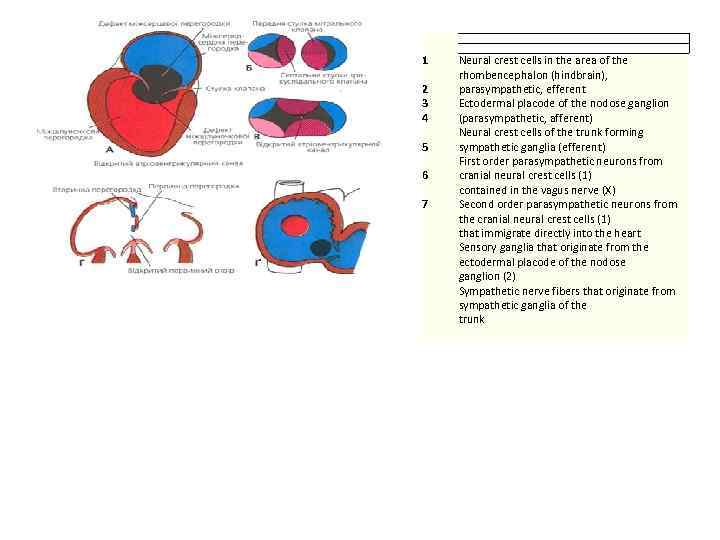 1 2 3 4 5 6 7 Neural crest cells in the area of the rhombencephalon (hindbrain), parasympathetic, efferent Ectodermal placode of the nodose ganglion (parasympathetic, afferent) Neural crest cells of the trunk forming sympathetic ganglia (efferent) First order parasympathetic neurons from cranial neural crest cells (1) contained in the vagus nerve (X) Second order parasympathetic neurons from the cranial neural crest cells (1) that immigrate directly into the heart Sensory ganglia that originate from the ectodermal placode of the nodose ganglion (2) Sympathetic nerve fibers that originate from sympathetic ganglia of the trunk
1 2 3 4 5 6 7 Neural crest cells in the area of the rhombencephalon (hindbrain), parasympathetic, efferent Ectodermal placode of the nodose ganglion (parasympathetic, afferent) Neural crest cells of the trunk forming sympathetic ganglia (efferent) First order parasympathetic neurons from cranial neural crest cells (1) contained in the vagus nerve (X) Second order parasympathetic neurons from the cranial neural crest cells (1) that immigrate directly into the heart Sensory ganglia that originate from the ectodermal placode of the nodose ganglion (2) Sympathetic nerve fibers that originate from sympathetic ganglia of the trunk
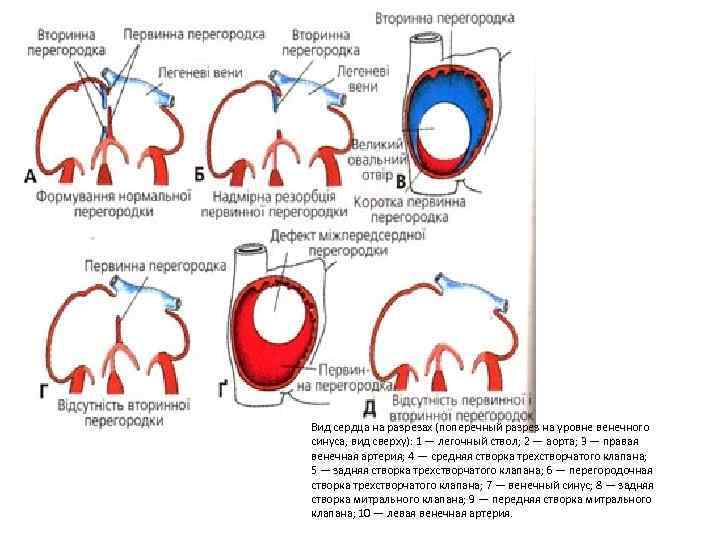 Вид сердца на разрезах (поперечный разрез на уровне венечного синуса, вид сверху): 1 — легочный ствол; 2 — аорта; 3 — правая венечная артерия; 4 — средняя створка трехстворчатого клапана; 5 — задняя створка трехстворчатого клапана; 6 — перегородочная створка трехстворчатого клапана; 7 — венечный синус; 8 — задняя створка митрального клапана; 9 — передняя створка митрального клапана; 10 — левая венечная артерия.
Вид сердца на разрезах (поперечный разрез на уровне венечного синуса, вид сверху): 1 — легочный ствол; 2 — аорта; 3 — правая венечная артерия; 4 — средняя створка трехстворчатого клапана; 5 — задняя створка трехстворчатого клапана; 6 — перегородочная створка трехстворчатого клапана; 7 — венечный синус; 8 — задняя створка митрального клапана; 9 — передняя створка митрального клапана; 10 — левая венечная артерия.
 Эпидемиология Частота ВПС среди новорожденных составляет около 1 % (1 на 100 новорожденных). ВПС по частоте встречаемости — на втором месте после врожденных пороков нервной системы. Этиология В основе возникновения ВПС (как и других врожденных пороков) лежат антенатальные мутации (генные, хромосомные), которые возникают вследствие действия трех основных мутагенов: 1. Физические мутагены (главным образом — ионизирующее излучение). 2. Химические мутагены (фенолы лаков, красок; нитраты; бензпирен при табакокурениии; тератогенные медикаменты — антибиотики и ХТП, НПВС и т. д. ). 3. Биологические мутагены (главным образом — вирус краснухи, ведущий к врожденной краснухе с характерной триадой Грега — ВПС, катаракта, глухота). В 1998 г. в России родилось 1 млн. 290 тыс. человек, из них 9000 - с ВПС.
Эпидемиология Частота ВПС среди новорожденных составляет около 1 % (1 на 100 новорожденных). ВПС по частоте встречаемости — на втором месте после врожденных пороков нервной системы. Этиология В основе возникновения ВПС (как и других врожденных пороков) лежат антенатальные мутации (генные, хромосомные), которые возникают вследствие действия трех основных мутагенов: 1. Физические мутагены (главным образом — ионизирующее излучение). 2. Химические мутагены (фенолы лаков, красок; нитраты; бензпирен при табакокурениии; тератогенные медикаменты — антибиотики и ХТП, НПВС и т. д. ). 3. Биологические мутагены (главным образом — вирус краснухи, ведущий к врожденной краснухе с характерной триадой Грега — ВПС, катаракта, глухота). В 1998 г. в России родилось 1 млн. 290 тыс. человек, из них 9000 - с ВПС.
 Частота врожденных пороков сердца достаточна высока. У разных авторов оценка частоты встречаемости колеблется, но, в среднем, она составляет 0, 8 - 1, 2% от всех новорожденных. Из числа всех встречающихся пороков развития она составляет до 30%. Врожденные пороки сердца (ВПС) представляют собой весьма обширную и разнородную группу заболеваний, в которую входят как относительно легкие формы, так и состояния, несовместимые с жизнью ребенка. Основная масса детей погибает в течении первого года жизни (до 70 -90%), а из них в течении первого месяца. После первого года жизни смертность резко снижается, и в период от 1 года до 15 лет погибают не более 5% детей. Понятно, что это большая и серьезная проблема. Мы с вами рассмотрим только некоторые ее аспекты. Прежде всего, какие причины могут приводить к рождению ребенка с ВПС. Некоторыми исследованиями показано, что существует определенная сезонность в рождении детей с ВПС. Например, есть данные, что открытый артериальный проток встречается преимущественно у девочек, родившихся во второй половине года, чаще всего с октября по январь. Мальчики с коарктацией аорты чаще рождаются в марте и апреле, наиболее редко - в сентябре и октябре. Бывают случаи, когда в определенной географической зоне рождается большое число детей с ВПС, что создает впечатление определенного рода эпидемии. Сезонные колебания возникновения ВПС и т. н. эпидемии, скорее всего, связаны с вирусными эпидемиями, а также воздействие экологических факторов (в первую очередь, ионизирующей радиации), оказывающих тератогенное (т. е. неблагоприятное для плода) действие. Так, например, доказано тератогенное действие вируса краснухи. Есть предположение, что и вирусы гриппа, а также некоторые другие, могут иметь значение в возникновении ВПС, в особенности, если их действие приходится на первые 3 месяца беременности. Безусловно, одного лишь наличия вирусного заболевания еще недостаточно для того, чтобы у будущего ребенка развился порок сердца, однако при условии дополнительных факторов (тяжести вирусного, да и бактериального заболевания, наличия генетической предрасположенности к неблагоприятным реакциям на пусковое воздействие данного фактора) вирусный агент может оказаться решающим в плане формирования врожденного порока сердца у новорожденного. Определенную роль в возникновении ВПС играет хронический алкоголизм матери. У 29 - 50% таких матерей рождаются дети с ВПС. У матерей, болеющих системной красной волчанкой, часто рождаются дети с врожденной блокадой проводящих путей сердца. Недостаток питательных веществ не влияет на образование пороков сердца у людей. У женщин, страдающих диабетом или преддиабетом, чаще, чем у здоровых, рождаются дети с пороками сердца. Обычно встречаются дефект межжелудочковой перегородки и транспозиция крупных сосудов. Особое значение имеет прием лекарственных препаратов во время беременности. В настоящее время абсолютно отказались от приема талидомида - этот препарат вызывал многочисленные врожденные уродства во время беременности (в том числе, и врожденные пороки сердца). Кроме того, тератогенным эффектом обладают алкоголь (вызывает дефекты межжелудочковой и межпредсердной перегородок, открытый артериальный проток), амфетамины (образуются чаще ДМЖП и транспозиция крупных сосудов), противосудорожные препараты - гидантоин (стеноз легочной артерии, коарктация аорты, открытый артериальный проток) и триметадион (транспозиция магистральных сосудов, тетрада Фалло, гипоплазия левого желудочка), литий (аномалия Эбштейна, атрезия трехстворчатого клапана), прогестагены (тетрада Фалло, сложные ВПС). Существует общее мнение, что наиболее опасными для развития ВПС являются первые 6 -8 недель беременности. При попадании тератогенного фактора в этот промежуток наиболее вероятно развитие тяжелого или сочетанного врожденного порока сердца. Однако не исключена возможность менее комплексного поражения сердца либо некоторых его структур на любом этапе беременности. Несомненным фактором риска является наличие генетической предрасположенности. Чаще всего при объяснении типа наследования прибегают к так называемой полигенно - мультифакториальной модели. По этой модели, чем более тяжелый порок сердца есть в семье, тем выше риск его повторения, чем больше родственников страдают ВПС, тем выше риск повторного поражения и т. д. Помимо подобного типа наследования, есть еще и генные мутации и хромосомные аномалии. Дать точную количественную оценку риска рождения ребенка с ВПС может (да и то не всегда) только генетик в процессе проведении медико-генетического консультирования. Факторами риска рождения ребенка с ВПС таким образом являются: возраст матери, эндокринные нарушения у супругов, токсикозы в I триместре и угрозы прерывания беременности, мертворождения в анамнезе, наличие других детей с врожденными пороками развития, прием женщиной эндокринных препаратов для сохранения беременности и др.
Частота врожденных пороков сердца достаточна высока. У разных авторов оценка частоты встречаемости колеблется, но, в среднем, она составляет 0, 8 - 1, 2% от всех новорожденных. Из числа всех встречающихся пороков развития она составляет до 30%. Врожденные пороки сердца (ВПС) представляют собой весьма обширную и разнородную группу заболеваний, в которую входят как относительно легкие формы, так и состояния, несовместимые с жизнью ребенка. Основная масса детей погибает в течении первого года жизни (до 70 -90%), а из них в течении первого месяца. После первого года жизни смертность резко снижается, и в период от 1 года до 15 лет погибают не более 5% детей. Понятно, что это большая и серьезная проблема. Мы с вами рассмотрим только некоторые ее аспекты. Прежде всего, какие причины могут приводить к рождению ребенка с ВПС. Некоторыми исследованиями показано, что существует определенная сезонность в рождении детей с ВПС. Например, есть данные, что открытый артериальный проток встречается преимущественно у девочек, родившихся во второй половине года, чаще всего с октября по январь. Мальчики с коарктацией аорты чаще рождаются в марте и апреле, наиболее редко - в сентябре и октябре. Бывают случаи, когда в определенной географической зоне рождается большое число детей с ВПС, что создает впечатление определенного рода эпидемии. Сезонные колебания возникновения ВПС и т. н. эпидемии, скорее всего, связаны с вирусными эпидемиями, а также воздействие экологических факторов (в первую очередь, ионизирующей радиации), оказывающих тератогенное (т. е. неблагоприятное для плода) действие. Так, например, доказано тератогенное действие вируса краснухи. Есть предположение, что и вирусы гриппа, а также некоторые другие, могут иметь значение в возникновении ВПС, в особенности, если их действие приходится на первые 3 месяца беременности. Безусловно, одного лишь наличия вирусного заболевания еще недостаточно для того, чтобы у будущего ребенка развился порок сердца, однако при условии дополнительных факторов (тяжести вирусного, да и бактериального заболевания, наличия генетической предрасположенности к неблагоприятным реакциям на пусковое воздействие данного фактора) вирусный агент может оказаться решающим в плане формирования врожденного порока сердца у новорожденного. Определенную роль в возникновении ВПС играет хронический алкоголизм матери. У 29 - 50% таких матерей рождаются дети с ВПС. У матерей, болеющих системной красной волчанкой, часто рождаются дети с врожденной блокадой проводящих путей сердца. Недостаток питательных веществ не влияет на образование пороков сердца у людей. У женщин, страдающих диабетом или преддиабетом, чаще, чем у здоровых, рождаются дети с пороками сердца. Обычно встречаются дефект межжелудочковой перегородки и транспозиция крупных сосудов. Особое значение имеет прием лекарственных препаратов во время беременности. В настоящее время абсолютно отказались от приема талидомида - этот препарат вызывал многочисленные врожденные уродства во время беременности (в том числе, и врожденные пороки сердца). Кроме того, тератогенным эффектом обладают алкоголь (вызывает дефекты межжелудочковой и межпредсердной перегородок, открытый артериальный проток), амфетамины (образуются чаще ДМЖП и транспозиция крупных сосудов), противосудорожные препараты - гидантоин (стеноз легочной артерии, коарктация аорты, открытый артериальный проток) и триметадион (транспозиция магистральных сосудов, тетрада Фалло, гипоплазия левого желудочка), литий (аномалия Эбштейна, атрезия трехстворчатого клапана), прогестагены (тетрада Фалло, сложные ВПС). Существует общее мнение, что наиболее опасными для развития ВПС являются первые 6 -8 недель беременности. При попадании тератогенного фактора в этот промежуток наиболее вероятно развитие тяжелого или сочетанного врожденного порока сердца. Однако не исключена возможность менее комплексного поражения сердца либо некоторых его структур на любом этапе беременности. Несомненным фактором риска является наличие генетической предрасположенности. Чаще всего при объяснении типа наследования прибегают к так называемой полигенно - мультифакториальной модели. По этой модели, чем более тяжелый порок сердца есть в семье, тем выше риск его повторения, чем больше родственников страдают ВПС, тем выше риск повторного поражения и т. д. Помимо подобного типа наследования, есть еще и генные мутации и хромосомные аномалии. Дать точную количественную оценку риска рождения ребенка с ВПС может (да и то не всегда) только генетик в процессе проведении медико-генетического консультирования. Факторами риска рождения ребенка с ВПС таким образом являются: возраст матери, эндокринные нарушения у супругов, токсикозы в I триместре и угрозы прерывания беременности, мертворождения в анамнезе, наличие других детей с врожденными пороками развития, прием женщиной эндокринных препаратов для сохранения беременности и др.
 Система венечных артерий Область кровоснабжения Правая венечная артерия • правое предсердие • часть передней стенки и всю заднюю стенку правого желудочка, • небольшой участок задней стенки левого желудочка, • межпредсердную перегородку, • заднюю треть межжелудочковой перегородки, • сосочковые мышцы правого желудочка • заднюю сосочковую мышцу левого желудочка.
Система венечных артерий Область кровоснабжения Правая венечная артерия • правое предсердие • часть передней стенки и всю заднюю стенку правого желудочка, • небольшой участок задней стенки левого желудочка, • межпредсердную перегородку, • заднюю треть межжелудочковой перегородки, • сосочковые мышцы правого желудочка • заднюю сосочковую мышцу левого желудочка.
 Система венечных артерий Область кровоснабжения Левая венечная артерия • левое предсердие, • всю переднюю стенку и большую часть задней стенки левого желудочка, • часть передней стенки правого желудочка, • передние 2/3 межжелудочковой перегородки • переднюю сосочковую мышцу левого желудочка.
Система венечных артерий Область кровоснабжения Левая венечная артерия • левое предсердие, • всю переднюю стенку и большую часть задней стенки левого желудочка, • часть передней стенки правого желудочка, • передние 2/3 межжелудочковой перегородки • переднюю сосочковую мышцу левого желудочка.
 Функциональная анатомия сердечно-сосудистой системы (цикл лекций читает старший преподаватель Хорошевская Я. А. ) ТЕМАТИКА ЛЕКЦИЙ 1. Фило - онтогенез и функциональная анатомия сердца 2. Фило- и онтогенез артериальной системы. 3. Фило- и онтогенез венозной системы. Микроциркуляция и регуляторные механизмы органного кровотока
Функциональная анатомия сердечно-сосудистой системы (цикл лекций читает старший преподаватель Хорошевская Я. А. ) ТЕМАТИКА ЛЕКЦИЙ 1. Фило - онтогенез и функциональная анатомия сердца 2. Фило- и онтогенез артериальной системы. 3. Фило- и онтогенез венозной системы. Микроциркуляция и регуляторные механизмы органного кровотока
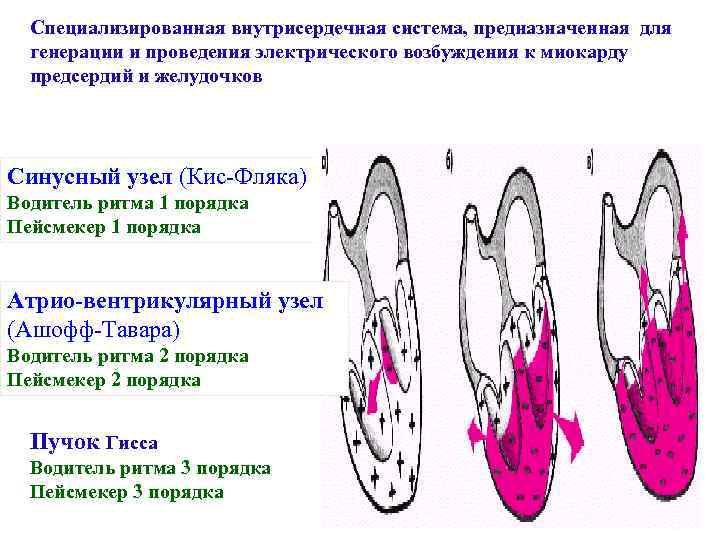 Специализированная внутрисердечная система, предназначенная для генерации и проведения электрического возбуждения к миокарду предсердий и желудочков Синусный узел (Кис-Фляка) Водитель ритма 1 порядка Пейсмекер 1 порядка Атрио-вентрикулярный узел (Ашофф-Тавара) Водитель ритма 2 порядка Пейсмекер 2 порядка Пучок Гисса Водитель ритма 3 порядка Пейсмекер 3 порядка
Специализированная внутрисердечная система, предназначенная для генерации и проведения электрического возбуждения к миокарду предсердий и желудочков Синусный узел (Кис-Фляка) Водитель ритма 1 порядка Пейсмекер 1 порядка Атрио-вентрикулярный узел (Ашофф-Тавара) Водитель ритма 2 порядка Пейсмекер 2 порядка Пучок Гисса Водитель ритма 3 порядка Пейсмекер 3 порядка
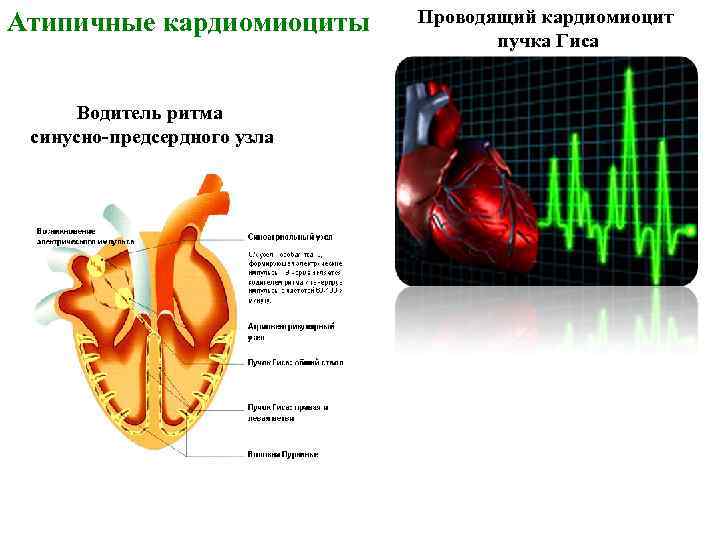 Атипичные кардиомиоциты Водитель ритма синусно-предсердного узла Проводящий кардиомиоцит пучка Гиса
Атипичные кардиомиоциты Водитель ритма синусно-предсердного узла Проводящий кардиомиоцит пучка Гиса
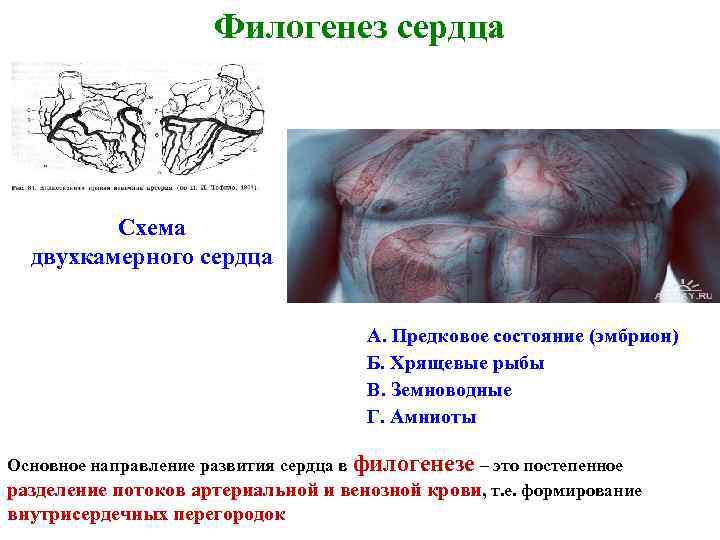 Филогенез сердца Схема двухкамерного сердца А. Предковое состояние (эмбрион) Б. Хрящевые рыбы В. Земноводные Г. Амниоты Основное направление развития сердца в филогенезе – это постепенное разделение потоков артериальной и венозной крови, т. е. формирование внутрисердечных перегородок
Филогенез сердца Схема двухкамерного сердца А. Предковое состояние (эмбрион) Б. Хрящевые рыбы В. Земноводные Г. Амниоты Основное направление развития сердца в филогенезе – это постепенное разделение потоков артериальной и венозной крови, т. е. формирование внутрисердечных перегородок
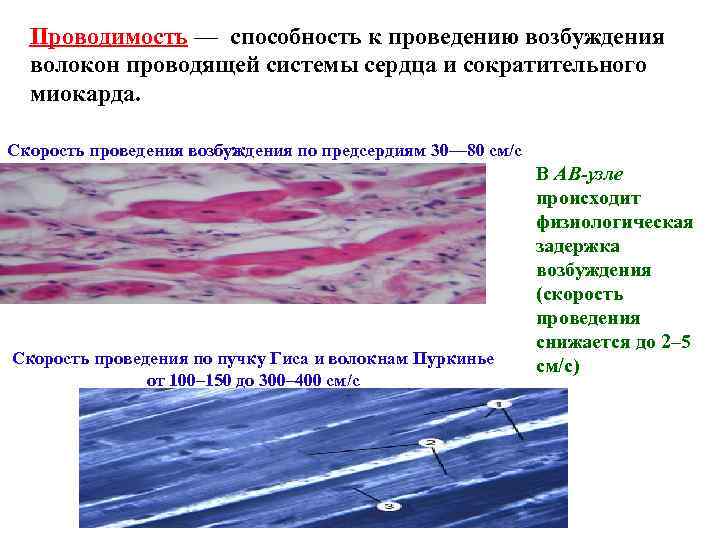 Проводимость — способность к проведению возбуждения волокон проводящей системы сердца и сократительного миокарда. Скорость проведения возбуждения по предсердиям 30— 80 см/с Скорость проведения по пучку Гиса и волокнам Пуркинье от 100– 150 до 300– 400 см/с В АВ-узле происходит физиологическая задержка возбуждения (скорость проведения снижается до 2– 5 см/с)
Проводимость — способность к проведению возбуждения волокон проводящей системы сердца и сократительного миокарда. Скорость проведения возбуждения по предсердиям 30— 80 см/с Скорость проведения по пучку Гиса и волокнам Пуркинье от 100– 150 до 300– 400 см/с В АВ-узле происходит физиологическая задержка возбуждения (скорость проведения снижается до 2– 5 см/с)
 Возбудимость - способность сердца возбуждаться под влиянием импульсов. Во время возбуждения возникает электрический ток, который регистрируется в виде ЭКГ. Сократимость - способность сердца сокращаться под влиянием импульсов и обеспечивать функцию насоса.
Возбудимость - способность сердца возбуждаться под влиянием импульсов. Во время возбуждения возникает электрический ток, который регистрируется в виде ЭКГ. Сократимость - способность сердца сокращаться под влиянием импульсов и обеспечивать функцию насоса.



 Сердечная мышца Поперечнополосатые волокна (1). Вставочные диски (2). Ядра овальной формы (3).
Сердечная мышца Поперечнополосатые волокна (1). Вставочные диски (2). Ядра овальной формы (3).


