khimtekh_4_voda_energia.ppt
- Количество слайдов: 26

Функции воды в химической и биологической промышленности Потребление воды – до 1 млн. м 3/сут. Преимущества воды • комплекс ценных свойств (высокая теплоемкость, малая вязкость, низкая температура кипения) • доступность и дешевизна (затраты исключительно на извлечение и очистку) • нетоксичность • удобство использования в производстве и транспортировке 1

Использование воды в химической промышленности: 1. Для технологических целей как: – растворитель твердых, жидких и газообразных веществ; – среда для осуществления физических и механических процессов (флотация, транспортировка твердых материалов в виде пульпы); – промывная жидкость для газов; – экстрагент и абсорбент различных веществ. 2

2. Как теплоноситель (в виде горячей воды и пара) и хладагента для обогрева и охлаждения аппаратуры. 3. В качестве сырья и реагента для производства различной химической продукции (водорода, ацетилена, серной и азотной кислот. ) 4. В качестве источника сырья для добычи многих химических веществ: из них извлекаются Na. Cl, Mg. Cl 2, Br 2, I 2 и др. продукты. 3

Классификация природных вод Атмосферная вода – вода дождевых и снеговых осадков. Примеси - СО 2, О 2 Н 2 S, в промышленных районах NOх, SОх. Почти не содержит растворенные соли. Поверхностная вода – речные, озерные, морские. Содержат различные минеральные и органические вещества, природа и концентрация которых зависят от климата, геоморфологических и гидротехнических мероприятий. Подземная вода – вода артезианских скважин, колодцев, ключей, гейзеров. Высокое содержание минеральных солей, выщелачиваемых из почвы и осадочных пород и малое содержание органических веществ. Морская вода - многокомпонентный раствор электролитов и содержит все элементы, входящие в состав литосферы. 4

Классификация технической воды Охлаждающая вода Служит для охлаждения жидких и газообразных продуктов в теплообменных аппаратах. Вода не соприкасается с материальными потоками Технологическая вода Средообразующая Для растворения и образования суспензий Промывная Для промывки газообразных (адсорбция), жидких (экстракция), твердых продуктов Реакционная В качестве реагента Энергетическая вода Используется для получения пара, как рабочее тело при передаче тепла от источника к потребителю (горячая вода) 5

Показатели промышленных вод: Солесодержание (сухой остаток, электропроводность) • пресные (с/с менее 1 г/кг), • солоноватые (с/с от 1 до 10 г/кг) • соленые (с/с более 10 г/кг) Жесткость - свойство воды, обусловленное присутствием в ней солей Са и Мg. -временная (устранимая, карбонатная), удаляемая при кипячении ( Жв) - постоянная (некарбонатная) (Жп) Общая жесткость воды Жо = Жв + Жп Классификация по жесткости: - мягкая (Са и Мg до 3 мгэкв/л) - умеренно-жесткая(3 -6 мгэкв/л) - жесткая (более 6 мгэкв/л) 6 р. Н

Содержание взвешенных веществ Взвешенные вещества - это вещества, которые остаются на фильтре при использовании того или иного способа фильтрования. Общепринятым является отнесение к ним частиц минерального и органического происхождения, остающихся на фильтре при фильтровании пробы через фильтр с диаметром пор 0, 45 мкм (РД 52. 24. 468 -2005). Окисляемость воды (ХПК) величина, характеризующая содержание в воде органических и минеральных веществ, окисляемых (при определенных условиях) одним из сильных химических окислителей Перманганатная (определяют для природных малозагрязненных вод) Бихроматная (определяют для сточных вод) 7
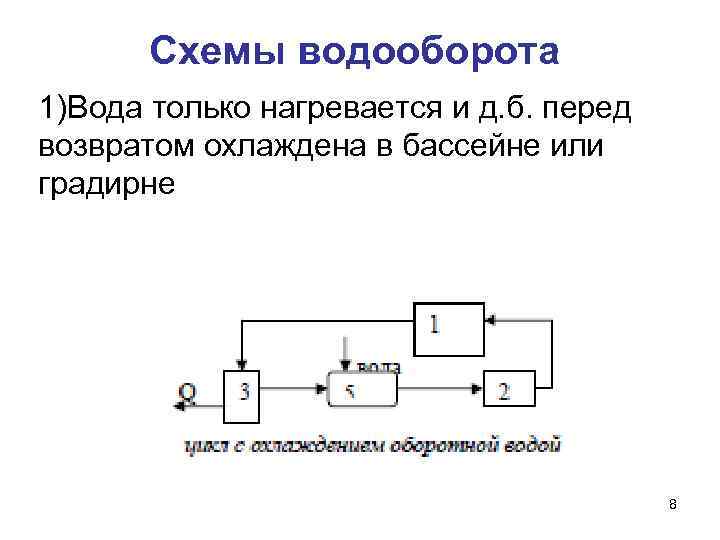
Схемы водооборота 1)Вода только нагревается и д. б. перед возвратом охлаждена в бассейне или градирне 8

Башенные градирни типа ТЭЦ, АЭС, металлургических заводов 9
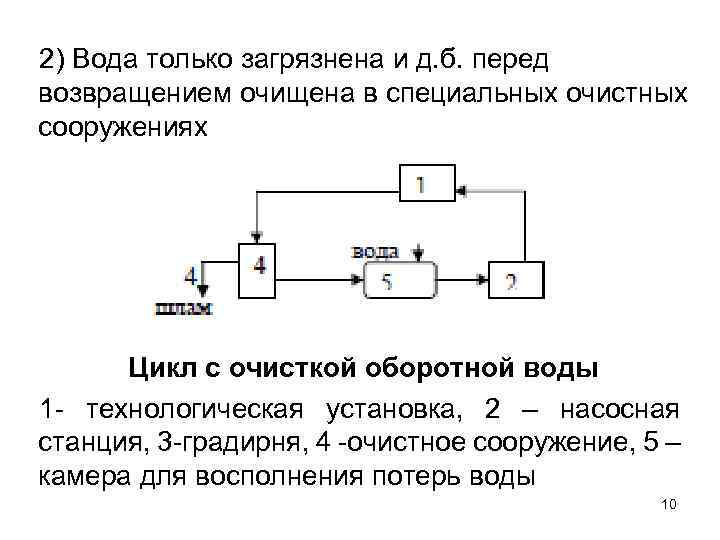
2) Вода только загрязнена и д. б. перед возвращением очищена в специальных очистных сооружениях Цикл с очисткой оборотной воды 1 - технологическая установка, 2 – насосная станция, 3 -градирня, 4 -очистное сооружение, 5 – камера для восполнения потерь воды 10
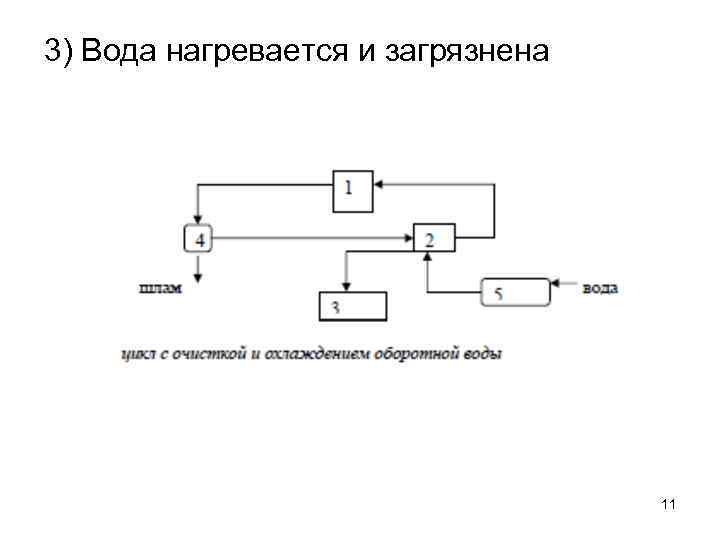
3) Вода нагревается и загрязнена 11

Промышленная водоподготовка - комплекс операций, обеспечивающих очистку воды – удаление из нее вредных примесей, находящихся в молекулярно-растворенном, коллоидном и взвешенном состоянии. Основные операции водоподготовки: Отстаивание удаление грубодисперсных веществ Фильтрация удаление мелких частиц Коагуляция введение в очищаемую воду небольших количеств веществ – коагулянтов, которые вызывают выпадение нерастворимого коллоидного осадка Обесцвечивание одновременно с коагуляцией идет процесс адсорбции на поверхности осадка органических красящих веществ, в 12 результате чего вода обесцвечивается

Умягчение обработка воды для понижения ее жесткости Физический способ: Са(НСО 3)2 =t Са. СО 3 + Н 2 О +СО 2 Химические способы: Фосфатный: 3 Са. SO 4 + 2 Na 3 PO 4 = 3 Na 2 SO 4 + Ca 3(PO 4)2 Известково-содовый: Са. SO 4 + Na 2 CO 3 = Ca. CO 3 +Na 2 SO 4 Физико-химические способы: ионно-обменный Нейтрализация Кислот и щелочей, содержащихся в сточных водах. Оптимальное значение р. Н: 6, 5 - 8, 5 Нейтрализаторы кислой среды: отходы металлургической промышленности (Са. О, Са(ОН)2, Mg. O, Mg(OH)2) Нейтрализаторы щелочной среды: техническая H 2 SO 4 13

Дегазация удаление из воды растворенных газов физическая: термическая деаэрация на воздухе или в вакууме. химическая: СО 2 + Са ( ОН)2 = Са. СО 3 +Н 2 О Обеззараживание хлорирование и озонирование 14

Обессоливание применяется в тех производствах, где к воде предъявляются особо жесткие требования по чистоте (при получении полупроводниковых материалов, химически чистых реактивов, фармацевтических препаратов) Метод ионного обмена основан на свойстве некоторых твердых тел (ионитов) поглощать из раствора ионы в обмен на эквивалентное количество других ионов того же знака. Иониты: катиониты (содержат подвижные Na+ и Н+), аниониты (содержат подвижные ОН-). 15

Катиониты: сульфоугли, алюмосиликаты, искусственные смолы Аниониты: исскуственные смолы процессы ионного обмена подразделяются: Н(Na)- катионирование, например: Na 2(Кат) + Са(НСО 3)2= Са(Кат) 2 +Na 2 CO 3 анионирование, например: Ан(ОН)+ НСl +Н 2 О =(Ан)Сl +Н 2 О где: (Кат) и (Ан) – не участвующая в обмене матрица ионита 16

Обменная емкость - количество ионов кальция и магния, которое может поглотить единица объема или массы ионита, выраженная грамм-эквивалентах: г-экв/м 3 и г-экв/кг. От величины обменной емкости при данном объеме ионита зависит время рабочего цикла ионитовых фильтров. Регенерация ионитов Катиониты: Са(Кат)+2 Na. Cl=Na 2(Кат)+ Ca. Cl 2 Аниониты: (Ан)Cl + KOH = (Ан)ОН + КСl 17
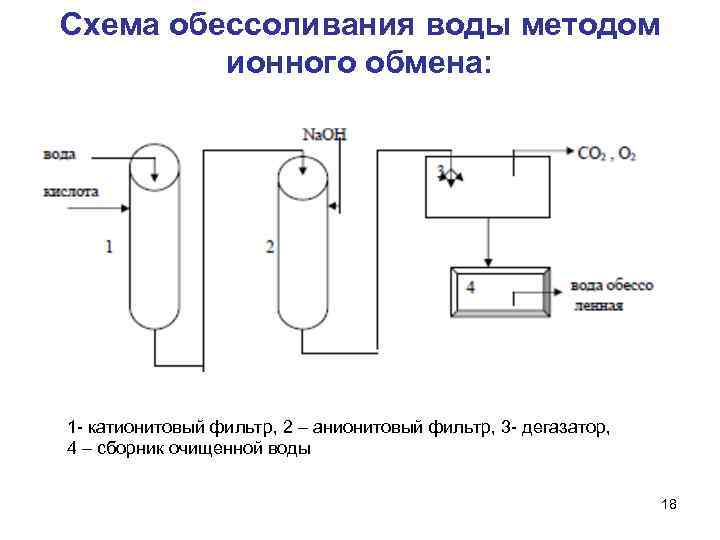
Схема обессоливания воды методом ионного обмена: 1 - катионитовый фильтр, 2 – анионитовый фильтр, 3 - дегазатор, 4 – сборник очищенной воды 18

Дистилляция – испарение жидкости с последующей конденсацией паров Дализ - удаление из коллоидных систем и растворов высокомолекулярных соединений примесей низкомолекулярных веществ с помощью полупроницаемых мембран, (перегородок), которые пропускают малые молекулы и ионы, но задерживают коллоидные частицы и макромолекулы. Электродиализ – процесс диализа под воздействием электрического поля. 19
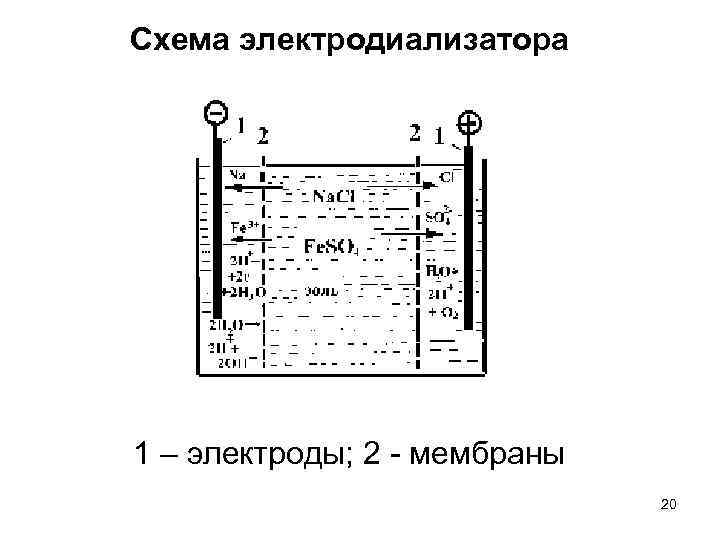
Схема электродиализатора 1 – электроды; 2 - мембраны 20
Энергия в химическом производстве Виды энергии Тепловая Электрическая Световая Атомная 21
Источники энергии Первичные Возобновляемые Вторичные Невозобновляемые 22

Энергетическая ценность источников энергии (2005 г. ) Невозобновляемые Каменный уголь – 8, 0 к. Вт. ч/кг Кокс – 7, 2 к. Вт. ч/кг Торф – 4, 0 к. Вт. ч/кг Коксовый газ – 4, 8 к. Вт. ч/кг Природный газ – 10, 8 к. Вт. ч/м 3 Нефть - Уран – 22, 5× 106 к. Вт. ч/кг Возобновляемые (в России) Ветроэнергетика – 4 м. Вт. год Геотермальная энергетика – 23 м. Вт. год Биоэнергетика (переработка отходов в биогаз) - Гидроэнергетика – 43940 м. Вт Солнечная энергетика – 23 0, 5 м. Вт
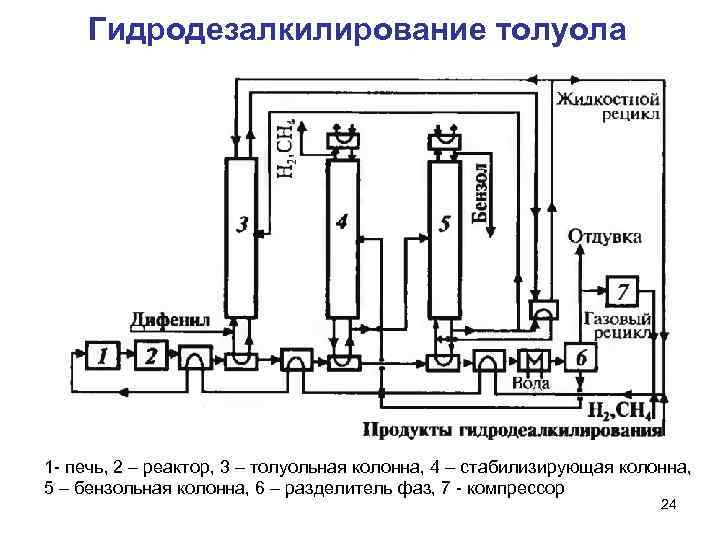
Гидродезалкилирование толуола 1 - печь, 2 – реактор, 3 – толуольная колонна, 4 – стабилизирующая колонна, 5 – бензольная колонна, 6 – разделитель фаз, 7 - компрессор 24
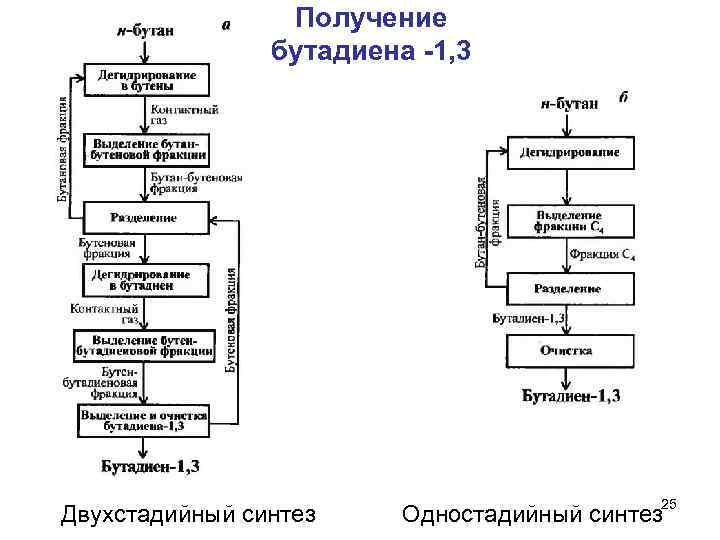
Получение бутадиена -1, 3 25 Двухстадийный синтез Одностадийный синтез
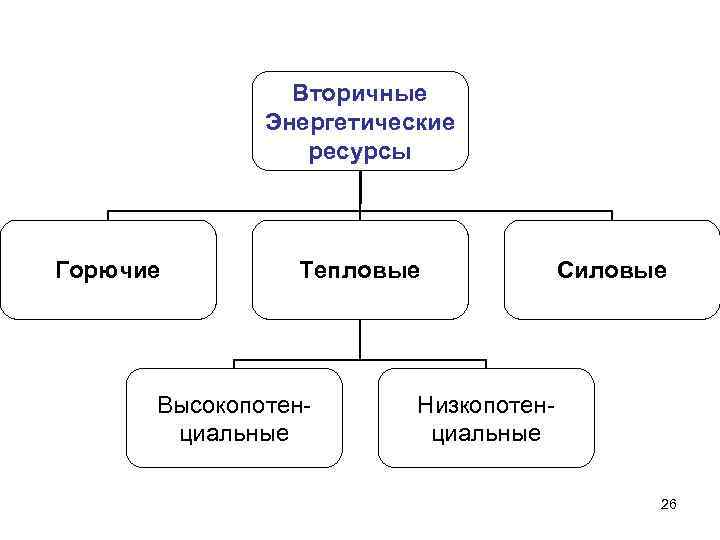
Вторичные Энергетические ресурсы Горючие Тепловые Высокопотенциальные Силовые Низкопотенциальные 26
khimtekh_4_voda_energia.ppt