Потенциал.ppt
- Количество слайдов: 29
 Функции клетки. Потенциалы действия Киев 2010
Функции клетки. Потенциалы действия Киев 2010
 Фактически существуют только два способа общения между клетками. Первый и наиболее очевидный способ — это химическое взаимодействие, при котором субстраты, продуцируемые одной клеткой, диффундируя к отдаленной (или соседней) клетке, вызывают в ней возникновение соответствующего ответа. В том случае, когда такие химические вещества (медиаторы) переносятся на достаточно большое расстояние, их традиционно называют гормонами. К сожалению, такого рода взаимодействия не обеспечивают достаточно быстрой реакции на стимул, особенно в том случае, когда взаимодействующие клетки находятся на значительном расстоянии друг от друга. В этих ситуациях организм использует «электрические» импульсы. Волна деполяризации, возникающая при передаче импульса по нерву и мышечной клетке, может достигать скорости свыше 100 м/с, т. е. скорости, значительно превосходящей скорость любой химической передачи. Тем не менее эта скорость существенно меньше скорости проведения «электричества» по медному проводнику.
Фактически существуют только два способа общения между клетками. Первый и наиболее очевидный способ — это химическое взаимодействие, при котором субстраты, продуцируемые одной клеткой, диффундируя к отдаленной (или соседней) клетке, вызывают в ней возникновение соответствующего ответа. В том случае, когда такие химические вещества (медиаторы) переносятся на достаточно большое расстояние, их традиционно называют гормонами. К сожалению, такого рода взаимодействия не обеспечивают достаточно быстрой реакции на стимул, особенно в том случае, когда взаимодействующие клетки находятся на значительном расстоянии друг от друга. В этих ситуациях организм использует «электрические» импульсы. Волна деполяризации, возникающая при передаче импульса по нерву и мышечной клетке, может достигать скорости свыше 100 м/с, т. е. скорости, значительно превосходящей скорость любой химической передачи. Тем не менее эта скорость существенно меньше скорости проведения «электричества» по медному проводнику.
 Потенциал действия Если нерв освободить от окружающей ткани и целиком погрузить в физиологический раствор, то он сохранит «функциональную» активность в течение длительного времени — иногда до нескольких дней. Под функционально активным состоянием подразумевается способность нерва к проведению импульса, а также то, что его стимуляция вызывает сокращение мышцы, если, конечно, нервное волокно продолжает оставаться связанным с мышцейэффектором.
Потенциал действия Если нерв освободить от окружающей ткани и целиком погрузить в физиологический раствор, то он сохранит «функциональную» активность в течение длительного времени — иногда до нескольких дней. Под функционально активным состоянием подразумевается способность нерва к проведению импульса, а также то, что его стимуляция вызывает сокращение мышцы, если, конечно, нервное волокно продолжает оставаться связанным с мышцейэффектором.
 Потенциал действия. Потенциал отводился от целого изолированного нерва. Первый зубец представляет собой артефакт стимуляции, вторая волна — потенциал действия, генерируемый нервным волокном. По мере возрастания амплитуды стимулирующего импульса амплитуда регистрируемого сигнала, отводимого от нервного волокна, также возрастает. Амплитуда первых двух стимулов лежит ниже порогового значения.
Потенциал действия. Потенциал отводился от целого изолированного нерва. Первый зубец представляет собой артефакт стимуляции, вторая волна — потенциал действия, генерируемый нервным волокном. По мере возрастания амплитуды стимулирующего импульса амплитуда регистрируемого сигнала, отводимого от нервного волокна, также возрастает. Амплитуда первых двух стимулов лежит ниже порогового значения.
 Самой важной особенностью волны возбуждения является ее двухфазный характер. В первый момент времени мембранный потенциал нервного волокна изменяется таким образом, что поверхность волокна под первым регистрирующим электродом приобретает отрицательный заряд (т. е. когда импульс достигает первого регистрирующего электрода, последний становится отрицательным по отношению к другому). Отрицательный знак потенциала этого участка сохраняется лишь в течение нескольких миллисекунд, а затем по мере дальнейшего прохождения импульса по нерву электроотрицательный участок оказывается расположенным уже между двумя электродами. Следовательно, система в этот момент возвращается к исходному состоянию, которое характеризовалось тем, что оба электрода имели одинаковые потенциалы (ниспадающий участок кривой). Однако как только импульс достигнет того участка волокна, который расположен под вторым отводящим электродом, этот электрод приобретает отрицательный по отношению к первому электроду потенциал, что выразится в дальнейшем снижении потенциала действия (второй участок кривой). После прохождения импульса под обоими электродами система возвращается в свое исходное состояние.
Самой важной особенностью волны возбуждения является ее двухфазный характер. В первый момент времени мембранный потенциал нервного волокна изменяется таким образом, что поверхность волокна под первым регистрирующим электродом приобретает отрицательный заряд (т. е. когда импульс достигает первого регистрирующего электрода, последний становится отрицательным по отношению к другому). Отрицательный знак потенциала этого участка сохраняется лишь в течение нескольких миллисекунд, а затем по мере дальнейшего прохождения импульса по нерву электроотрицательный участок оказывается расположенным уже между двумя электродами. Следовательно, система в этот момент возвращается к исходному состоянию, которое характеризовалось тем, что оба электрода имели одинаковые потенциалы (ниспадающий участок кривой). Однако как только импульс достигнет того участка волокна, который расположен под вторым отводящим электродом, этот электрод приобретает отрицательный по отношению к первому электроду потенциал, что выразится в дальнейшем снижении потенциала действия (второй участок кривой). После прохождения импульса под обоими электродами система возвращается в свое исходное состояние.
 Для того чтобы упростить систему и тем самым сделать ее более удобной для изучения, можно повредить нервное волокно в области второго электрода. Это устранит возникновение второй части кривой, превратив потенциал действия в однофазный. В большинстве случаев используется именно такой подход, и тот одиночный пик, который регистрируется при прохождении импульса под отводящим электродом, был назван потенциалом действия, или спайком.
Для того чтобы упростить систему и тем самым сделать ее более удобной для изучения, можно повредить нервное волокно в области второго электрода. Это устранит возникновение второй части кривой, превратив потенциал действия в однофазный. В большинстве случаев используется именно такой подход, и тот одиночный пик, который регистрируется при прохождении импульса под отводящим электродом, был назван потенциалом действия, или спайком.
 Мембранные потенциалы Хотя величина этого потенциала у разных организмов различна, она обычно составляет 60— 90 м. В; при этом содержимое клетки, как правило, заряжено отрицательно по отношению к ее наружной поверхности. Величина мембранного потенциала сохраняется неизменной в течение длительного времени, т. е. даже в отсутствие проведения клеткой импульсов, в связи с чем он и был назван потенциалом покоя. По-видимому, важная роль в возникновении этих потенциалов принадлежит мембране клетки. Передача импульса действительно сопряжена с перераспределением зарядов на поверхности мембраны, а не обусловлена прохождением электрического тока вдоль поверхности нерва.
Мембранные потенциалы Хотя величина этого потенциала у разных организмов различна, она обычно составляет 60— 90 м. В; при этом содержимое клетки, как правило, заряжено отрицательно по отношению к ее наружной поверхности. Величина мембранного потенциала сохраняется неизменной в течение длительного времени, т. е. даже в отсутствие проведения клеткой импульсов, в связи с чем он и был назван потенциалом покоя. По-видимому, важная роль в возникновении этих потенциалов принадлежит мембране клетки. Передача импульса действительно сопряжена с перераспределением зарядов на поверхности мембраны, а не обусловлена прохождением электрического тока вдоль поверхности нерва.
 Диффузионный потенциал Причиной возникновения мембранного потенциала служат различия в подвижности ионов. Если два одинаковых по составу, но различных по концентрации раствора (скажем, Na. Сl) привести в соприкосновение, то относительно быстро диффундирующие ионы будут покидать область высокой концентрации и переходить в область низкой концентрации со значительно большей скоростью, чем менее подвижные ионы. Это приведет к временному разделению заряда. Например, если подвижность ионов Cl- выше, чем ионов Nа+, то при соприкосновении двух одинаковых по составу, но различающихся концентрацией растворов распределение ионов Cl- и Nа+ на границе раздела этих растворов может оказаться неравномерным. Этим объясняется возникновение разности потенциалов между двумя растворами, или диффузионный потенциал. Возникновение такого крайне неустойчивого потенциала могло би и не иметь значения для клетки, если бы избирательная проницаемость плазматической мембраны не обусловливала поддержания заметных различий в скоростях диффузии различных ионов и тем самым не стабилизировала бы величину диффузионного потенциала.
Диффузионный потенциал Причиной возникновения мембранного потенциала служат различия в подвижности ионов. Если два одинаковых по составу, но различных по концентрации раствора (скажем, Na. Сl) привести в соприкосновение, то относительно быстро диффундирующие ионы будут покидать область высокой концентрации и переходить в область низкой концентрации со значительно большей скоростью, чем менее подвижные ионы. Это приведет к временному разделению заряда. Например, если подвижность ионов Cl- выше, чем ионов Nа+, то при соприкосновении двух одинаковых по составу, но различающихся концентрацией растворов распределение ионов Cl- и Nа+ на границе раздела этих растворов может оказаться неравномерным. Этим объясняется возникновение разности потенциалов между двумя растворами, или диффузионный потенциал. Возникновение такого крайне неустойчивого потенциала могло би и не иметь значения для клетки, если бы избирательная проницаемость плазматической мембраны не обусловливала поддержания заметных различий в скоростях диффузии различных ионов и тем самым не стабилизировала бы величину диффузионного потенциала.
 Наиболее удовлетворительным объяснением стабильности мембранного потенциала, характерного для клетки, является то, что мембрана клетки обладает суммарным зарядом, сосредоточенным в ее порах, или ячейках липидной решетки, и что асимметрия в распределении ионов поддерживается просто различиями в скорости их диффузии через мембрану
Наиболее удовлетворительным объяснением стабильности мембранного потенциала, характерного для клетки, является то, что мембрана клетки обладает суммарным зарядом, сосредоточенным в ее порах, или ячейках липидной решетки, и что асимметрия в распределении ионов поддерживается просто различиями в скорости их диффузии через мембрану
 Ионные насосы Еще одним фактором, определяющим величину мембранного потенциала, является активный транспорт ионов. Транспорт Na+ через внутреннюю мембрану клетки происходит только в присутствии К+ (К+-зависим). В то же время на уровне наружной мембраны К+ влияния не оказывает, поскольку система активного обмена ионов локализована на внутренней мембране. Однако для работы системы в целом важно, чтобы не происходило потерь К+, поэтому наружная мембрана должна быть непроницаемой для К+, не допуская его выхода из клетки. Еще более важно, чтобы на внутренней мембране выведению Na+ сопутствовало пассивное вхождение в клетку К+, т. е. процесс, обеспечивающий функционально активное состояние Na+-насоса.
Ионные насосы Еще одним фактором, определяющим величину мембранного потенциала, является активный транспорт ионов. Транспорт Na+ через внутреннюю мембрану клетки происходит только в присутствии К+ (К+-зависим). В то же время на уровне наружной мембраны К+ влияния не оказывает, поскольку система активного обмена ионов локализована на внутренней мембране. Однако для работы системы в целом важно, чтобы не происходило потерь К+, поэтому наружная мембрана должна быть непроницаемой для К+, не допуская его выхода из клетки. Еще более важно, чтобы на внутренней мембране выведению Na+ сопутствовало пассивное вхождение в клетку К+, т. е. процесс, обеспечивающий функционально активное состояние Na+-насоса.
 Na+/K+-нacoc Схема сопряженного транспорта Na+/K+-нacoc, локализованный внутри мембраны, выводит ионы Na+ из клетки, обменивая их на ноны К+. Движение Na+ из среды в клетку через наружную мембрану осуществляется посредством системы облегченной диффузии. Находящийся внутри клетки К+ может вновь выйти из нес через внутреннюю мембрану, поддерживая тем самым ионный насос в функционально активном состоянии.
Na+/K+-нacoc Схема сопряженного транспорта Na+/K+-нacoc, локализованный внутри мембраны, выводит ионы Na+ из клетки, обменивая их на ноны К+. Движение Na+ из среды в клетку через наружную мембрану осуществляется посредством системы облегченной диффузии. Находящийся внутри клетки К+ может вновь выйти из нес через внутреннюю мембрану, поддерживая тем самым ионный насос в функционально активном состоянии.
 Биоэлектрическая проводимость Известно, что мембрана относительно малопроницаема для К+. Скорость движения ионов внутри клетки лишь немногим меньше скорости их свободной диффузии, тогда как скорость диффузии ионов через мембрану очень мала. Высокое сопротивление мембраны потоку ионов естественно вытекает из ее липидной природы. Величина этого сопротивления очень хорошо согласуется с величинами электрического сопротивления и емкости мембраны. Емкость большинства мембран составляет примерно 1 мк. Ф/см 2. Приняв, что диэлектрическая проницаемость липидов, из которых состоит мембрана, приблизительно равна 6, получим, что такой емкостью должен обладать липидный слой толщиной около 50 А, что хорошо согласуется с данными о толщине липидного компонента мембраны. Так как сопротивление мембраны составляет около 1010 ом/см, т. е. почти в 108 раз больше сопротивления среды или аксоплазмы, следует согласиться с тем, что сопротивление потоку ионов, идущему через такую мембрану, должно быть действительно очень большим.
Биоэлектрическая проводимость Известно, что мембрана относительно малопроницаема для К+. Скорость движения ионов внутри клетки лишь немногим меньше скорости их свободной диффузии, тогда как скорость диффузии ионов через мембрану очень мала. Высокое сопротивление мембраны потоку ионов естественно вытекает из ее липидной природы. Величина этого сопротивления очень хорошо согласуется с величинами электрического сопротивления и емкости мембраны. Емкость большинства мембран составляет примерно 1 мк. Ф/см 2. Приняв, что диэлектрическая проницаемость липидов, из которых состоит мембрана, приблизительно равна 6, получим, что такой емкостью должен обладать липидный слой толщиной около 50 А, что хорошо согласуется с данными о толщине липидного компонента мембраны. Так как сопротивление мембраны составляет около 1010 ом/см, т. е. почти в 108 раз больше сопротивления среды или аксоплазмы, следует согласиться с тем, что сопротивление потоку ионов, идущему через такую мембрану, должно быть действительно очень большим.
 Большая величина электрического сопротивления мембраны означает, что по существу мы имеем дело с двумя растворами электролитов (гель внутри клетки и физиологический раствор снаружи), разделенными слоем изолятора. Медленная утечка ионов через этот слой будет приводить к возникновению диффузионного потенциала, который, несомненно, является частью потенциала покоя нервного волокна. Однако создание неравномерного распределения, а также изменения в этом распределении, которые должны происходить во время прохождения волны деполяризации, т. е. при передаче импульса, едва ли можно объяснить на основе действия каких-либо статических сил. К тому же, как только было установлено существование обмена К+ и Nа + через мембрану, стала очевидной недостаточность статической интерпретации возникновения потенциала действия.
Большая величина электрического сопротивления мембраны означает, что по существу мы имеем дело с двумя растворами электролитов (гель внутри клетки и физиологический раствор снаружи), разделенными слоем изолятора. Медленная утечка ионов через этот слой будет приводить к возникновению диффузионного потенциала, который, несомненно, является частью потенциала покоя нервного волокна. Однако создание неравномерного распределения, а также изменения в этом распределении, которые должны происходить во время прохождения волны деполяризации, т. е. при передаче импульса, едва ли можно объяснить на основе действия каких-либо статических сил. К тому же, как только было установлено существование обмена К+ и Nа + через мембрану, стала очевидной недостаточность статической интерпретации возникновения потенциала действия.
 Изучение мембраны нервного волокна показало присутствие в ней Nа+/К+зависимой системы активного транспорта. Интересен тот факт, что утечка ионов калия, происходящая через мембрану нервного волокна, намного превосходит утечку ионов натрия, при этом поток калия состоит из двух компонентов: потока, направленного внутрь клетки, обусловленного активным транспортом (сопряженным с транспортом Nа+), и пассивного, направленного в окружающую среду. Пассивная диффузия Na+ из внешней среды внутрь клетки очень мала, по все же много меньше скорости выхода К+ в окружающую среду. В общем представляется наиболее вероятным, что мембранный потенциал нервного волокна (и мышечной клетки) поддерживается активным выведением Na+ и активным включением К+. Эти процессы уравновешиваются одновременно происходящей утечкой этих ионов в противоположных направлениях. Более быстрый выход К+ из клетки по сравнению с поступлением в нее Nа+ создает суммарный отрицательный заряд содержимого клетки. Процесс активного транспорта можно блокировать, воздействуя каким-либо из многочисленных ингибиторов; это не приводит, однако, к немедленному исчезновению потенциала покоя. Напротив, величина этого потенциала снижается медленно, что обусловлено постепенным выравниванием концентраций Na+ и К+ путем утечки этих катионов через плазматическую мембрану. В мышечной клетке распределение Сl- и К+ довольно хорошо согласуется с величиной мембранного потенциала. Вместе с тем распределение ионов натрия далеко от равновесного. Как и в нервной клетке, скорость вхождения Na+ значительно ниже скорости выхода К+; очевидно, и в данном случае функционирование Nа+/К+- насоса поддерживает наблюдаемое значение потенциала покоя, уравновешивая утечку этих катионов.
Изучение мембраны нервного волокна показало присутствие в ней Nа+/К+зависимой системы активного транспорта. Интересен тот факт, что утечка ионов калия, происходящая через мембрану нервного волокна, намного превосходит утечку ионов натрия, при этом поток калия состоит из двух компонентов: потока, направленного внутрь клетки, обусловленного активным транспортом (сопряженным с транспортом Nа+), и пассивного, направленного в окружающую среду. Пассивная диффузия Na+ из внешней среды внутрь клетки очень мала, по все же много меньше скорости выхода К+ в окружающую среду. В общем представляется наиболее вероятным, что мембранный потенциал нервного волокна (и мышечной клетки) поддерживается активным выведением Na+ и активным включением К+. Эти процессы уравновешиваются одновременно происходящей утечкой этих ионов в противоположных направлениях. Более быстрый выход К+ из клетки по сравнению с поступлением в нее Nа+ создает суммарный отрицательный заряд содержимого клетки. Процесс активного транспорта можно блокировать, воздействуя каким-либо из многочисленных ингибиторов; это не приводит, однако, к немедленному исчезновению потенциала покоя. Напротив, величина этого потенциала снижается медленно, что обусловлено постепенным выравниванием концентраций Na+ и К+ путем утечки этих катионов через плазматическую мембрану. В мышечной клетке распределение Сl- и К+ довольно хорошо согласуется с величиной мембранного потенциала. Вместе с тем распределение ионов натрия далеко от равновесного. Как и в нервной клетке, скорость вхождения Na+ значительно ниже скорости выхода К+; очевидно, и в данном случае функционирование Nа+/К+- насоса поддерживает наблюдаемое значение потенциала покоя, уравновешивая утечку этих катионов.
 Возникновение и распространение импульса Проводимость цитоплазматического геля много ниже проводимости медной проволоки, а тонкая плазматическая мембрана значительно уступает по своим электроизоляционным свойствам тем материалам, которые применяются для покрытия электрических кабелей при эксплуатации их в соленой воде. В то же время известно, что нервные импульсы проводятся на достаточно большие расстояния; нельзя поэтому рассматривать нерв как простой проводник электрического импульса, генерируемого телом нейтрона и достигающего путем прохождения по аксону какого-либо эффекторного органа. Процесс проведения импульса можно объяснять исходя из гипотезы местных токов.
Возникновение и распространение импульса Проводимость цитоплазматического геля много ниже проводимости медной проволоки, а тонкая плазматическая мембрана значительно уступает по своим электроизоляционным свойствам тем материалам, которые применяются для покрытия электрических кабелей при эксплуатации их в соленой воде. В то же время известно, что нервные импульсы проводятся на достаточно большие расстояния; нельзя поэтому рассматривать нерв как простой проводник электрического импульса, генерируемого телом нейтрона и достигающего путем прохождения по аксону какого-либо эффекторного органа. Процесс проведения импульса можно объяснять исходя из гипотезы местных токов.
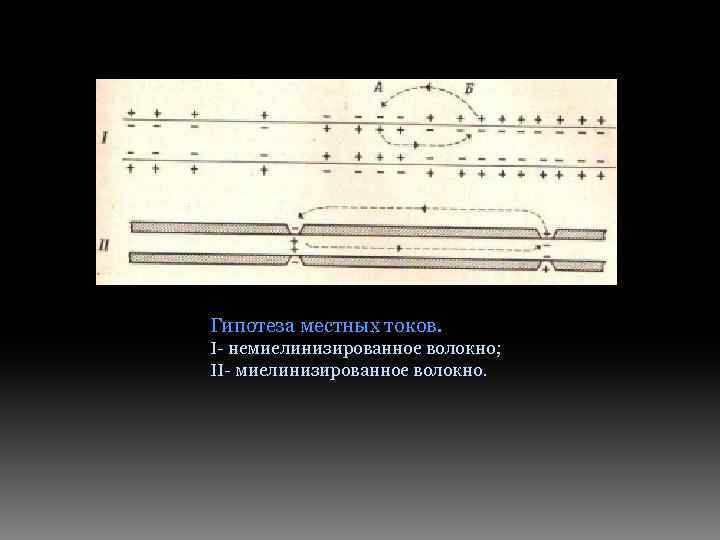 Гипотеза местных токов. Ι- немиелинизированное волокно; ΙΙ- миелинизированное волокно.
Гипотеза местных токов. Ι- немиелинизированное волокно; ΙΙ- миелинизированное волокно.
 Предполагается, что при прохождении нервного импульса имеет место локальное изменение величины мембранного потенциала, т. е. локальная деполяризация мембраны. Это приводит к тому, что на наружной стороне мембраны электроотрицательная область оказывается в непосредственной близости с областью, несущей положительный заряд. Возникновение тока между этими участками будет приводить к перераспределению положительных и отрицательных зарядов, т. с. восстановлению исходных условий; одновременно с этим будет наблюдаться распространение волны негативности вдоль аксона.
Предполагается, что при прохождении нервного импульса имеет место локальное изменение величины мембранного потенциала, т. е. локальная деполяризация мембраны. Это приводит к тому, что на наружной стороне мембраны электроотрицательная область оказывается в непосредственной близости с областью, несущей положительный заряд. Возникновение тока между этими участками будет приводить к перераспределению положительных и отрицательных зарядов, т. с. восстановлению исходных условий; одновременно с этим будет наблюдаться распространение волны негативности вдоль аксона.
 В миелинизированном нервном волокне местные токи могут возникать только в области перехватов Ранвье, так как только в этих местах мембрана нервного волокна непосредственно контактирует с омывающим его раствором. Это позволяет предположить, что возбуждение в этих условиях распространяется «скачком» от одного перехвата к другому и, таким образом, скорость его перемещения по нерву оказывается МНОГО выше, чем если бы нерв был лишен миелиновой оболочки. Такое проведение (от перехвата к перехвату) называют сальтаторным.
В миелинизированном нервном волокне местные токи могут возникать только в области перехватов Ранвье, так как только в этих местах мембрана нервного волокна непосредственно контактирует с омывающим его раствором. Это позволяет предположить, что возбуждение в этих условиях распространяется «скачком» от одного перехвата к другому и, таким образом, скорость его перемещения по нерву оказывается МНОГО выше, чем если бы нерв был лишен миелиновой оболочки. Такое проведение (от перехвата к перехвату) называют сальтаторным.
 Проведение импульса от клетки к клетке Специализированная зона контакта между нейронами, а также между нейроном и рецептором или эффектором называется синапсом. В случае нервно-мышечного синапса пространство (синаптическая щель), отделяющее окончание нервного волокна от мышечной клетки, может достигать 1000 А, что значительно больше расстояния, разделяющего две нервные клетки (200 А). Кроме того, в области нервно-мышечного синапса находится так называемая «базальная мембрана» , окружающая мышечное волокно и служащая барьером между этими двумя клетками. В некоторых синапсах контакт между его компонентами оказывается более тесным. Существуют два типа синаптической передачи. При одном типе (электрическая передача) степень физического контакта мембран достаточна для проведения потенциала действия от одной клетки к другой; при этом ток, возникающий под влиянием подходящего нервного импульса, вызывает деполяризацию и возбуждение мембраны прилежащей клетки. При втором типе передача осуществляется посредством особого химического вещества (посредника — медиатора).
Проведение импульса от клетки к клетке Специализированная зона контакта между нейронами, а также между нейроном и рецептором или эффектором называется синапсом. В случае нервно-мышечного синапса пространство (синаптическая щель), отделяющее окончание нервного волокна от мышечной клетки, может достигать 1000 А, что значительно больше расстояния, разделяющего две нервные клетки (200 А). Кроме того, в области нервно-мышечного синапса находится так называемая «базальная мембрана» , окружающая мышечное волокно и служащая барьером между этими двумя клетками. В некоторых синапсах контакт между его компонентами оказывается более тесным. Существуют два типа синаптической передачи. При одном типе (электрическая передача) степень физического контакта мембран достаточна для проведения потенциала действия от одной клетки к другой; при этом ток, возникающий под влиянием подходящего нервного импульса, вызывает деполяризацию и возбуждение мембраны прилежащей клетки. При втором типе передача осуществляется посредством особого химического вещества (посредника — медиатора).
 Медиатор ацетилхолин Это соединение обладает исключительно высокой активностью, стимулируя генерацию нервных импульсов или мышечного сокращения; в естественных условиях гиперстимуляция, как правило, не возникает благодаря наличию очень активного фермента — холинэстеразы. Высвобождающийся в нервных окончаниях ацетилхолин почти немедленно разрушается этим ферментом.
Медиатор ацетилхолин Это соединение обладает исключительно высокой активностью, стимулируя генерацию нервных импульсов или мышечного сокращения; в естественных условиях гиперстимуляция, как правило, не возникает благодаря наличию очень активного фермента — холинэстеразы. Высвобождающийся в нервных окончаниях ацетилхолин почти немедленно разрушается этим ферментом.
 Кроме ацетилхолина, в нервных окончаниях выделяются и другие соединения. Уже давно было показано, что ритм сердца находится под контролем двух противодействующих систем. Парасимпатическая система (блуждающий нерв) замедляет ритм сердца; в окончаниях этих волокон выделяется ацетилхолин; активация симпатических нервов сопровождается высвобождением норадреналина, который ускоряет ритм сердца. Это открытие обусловило развитие концепции о медиаторах, или нейрогормонах— специфических соединениях, вырабатываемых в нервных окончаниях, которые влияют на другие клетки (в частности, мышечные). Кроме ацетилхолина, адреналина и норадреналина, в различных областях центральной нервной системы были обнаружены также таминовая кислота и γ-аминомасляная кислота.
Кроме ацетилхолина, в нервных окончаниях выделяются и другие соединения. Уже давно было показано, что ритм сердца находится под контролем двух противодействующих систем. Парасимпатическая система (блуждающий нерв) замедляет ритм сердца; в окончаниях этих волокон выделяется ацетилхолин; активация симпатических нервов сопровождается высвобождением норадреналина, который ускоряет ритм сердца. Это открытие обусловило развитие концепции о медиаторах, или нейрогормонах— специфических соединениях, вырабатываемых в нервных окончаниях, которые влияют на другие клетки (в частности, мышечные). Кроме ацетилхолина, адреналина и норадреналина, в различных областях центральной нервной системы были обнаружены также таминовая кислота и γ-аминомасляная кислота.
 Нервно-мышечное соединение Электронно-микроскопическое исследование нервно-мышечного соединения выявило в пресинаптических нервных окончаниях массу пузырьков диаметром около 500 А. Они бывают рассеяны вдоль синаптической мембраны, но чаще всего накапливаются вблизи субсинаптических складок мембраны мышечного волокна. Неоднократные попытки обнаружить прохождение электрического тока через такие синапсы были безуспешными. Не наблюдалось также проведения и при подпороговой стимуляции. Вместе с тем посредством микроэлектрода, введенного в область синаптического контакта, удавалось при возбуждении нервного волокна зарегистрировать возникновение двух разделенных во времени токов. Первый из них совпадал с приходом нервного импульса к синапсу; за ним следовал другой, который возникал на мышечной стороне синапса спустя 0, 5— 0, 8 мс. Довольно любопытно, что второй импульс можно ингибировать, обработав мышцу каким-либо курареподобным веществом или изменив ионный состав среды (в частности, концентрацию Са 2+ и Мд 2+). Поскольку эти два тока могут быть разделены как пространственно, так и во времени, то представляется вероятным, что в течение очень короткого промежутка времени (синаптической задержки) передача сигнала через синапс осуществляется посредством некоторого процесса, имеющего неэлектрическую природу.
Нервно-мышечное соединение Электронно-микроскопическое исследование нервно-мышечного соединения выявило в пресинаптических нервных окончаниях массу пузырьков диаметром около 500 А. Они бывают рассеяны вдоль синаптической мембраны, но чаще всего накапливаются вблизи субсинаптических складок мембраны мышечного волокна. Неоднократные попытки обнаружить прохождение электрического тока через такие синапсы были безуспешными. Не наблюдалось также проведения и при подпороговой стимуляции. Вместе с тем посредством микроэлектрода, введенного в область синаптического контакта, удавалось при возбуждении нервного волокна зарегистрировать возникновение двух разделенных во времени токов. Первый из них совпадал с приходом нервного импульса к синапсу; за ним следовал другой, который возникал на мышечной стороне синапса спустя 0, 5— 0, 8 мс. Довольно любопытно, что второй импульс можно ингибировать, обработав мышцу каким-либо курареподобным веществом или изменив ионный состав среды (в частности, концентрацию Са 2+ и Мд 2+). Поскольку эти два тока могут быть разделены как пространственно, так и во времени, то представляется вероятным, что в течение очень короткого промежутка времени (синаптической задержки) передача сигнала через синапс осуществляется посредством некоторого процесса, имеющего неэлектрическую природу.
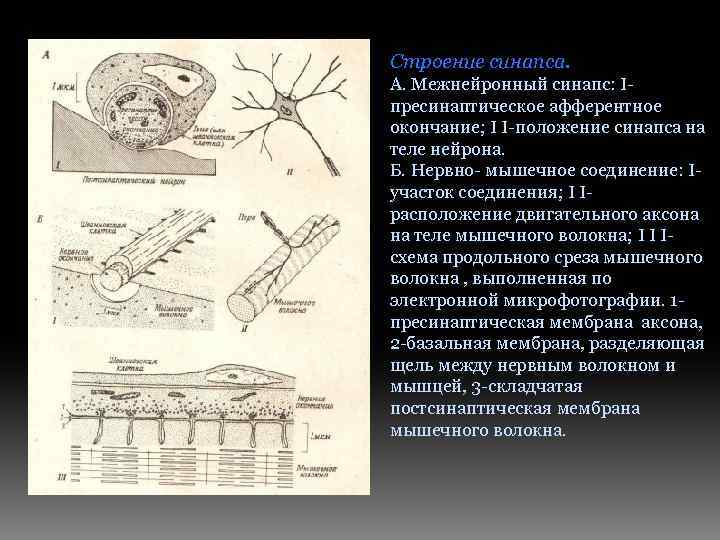 Строение синапса. А. Межнейронный синапс: Ιпресинаптическое афферентное окончание; Ι Ι-положение синапса на теле нейрона. Б. Нервно- мышечное соединение: Ιучасток соединения; Ι Ιрасположение двигательного аксона на теле мышечного волокна; Ι Ι Ιсхема продольного среза мышечного волокна , выполненная по электронной микрофотографии. 1 пресинаптическая мембрана аксона, 2 -базальная мембрана, разделяющая щель между нервным волокном и мышцей, 3 -складчатая постсинаптическая мембрана мышечного волокна.
Строение синапса. А. Межнейронный синапс: Ιпресинаптическое афферентное окончание; Ι Ι-положение синапса на теле нейрона. Б. Нервно- мышечное соединение: Ιучасток соединения; Ι Ιрасположение двигательного аксона на теле мышечного волокна; Ι Ι Ιсхема продольного среза мышечного волокна , выполненная по электронной микрофотографии. 1 пресинаптическая мембрана аксона, 2 -базальная мембрана, разделяющая щель между нервным волокном и мышцей, 3 -складчатая постсинаптическая мембрана мышечного волокна.
 Чаще всего в синаптическую щель выделяется ацетилхолин, изменяющий проницаемость постсинаптической мембраны. Ацетилхолин, выявляемый в синапсе образуется в нервных окончаниях, а не в самой мышце. По-видимому, ацетилхолин образуется заранее и хранится в мельчайших пузырьках нервных окончаний. В отсутствие ионов кальция высвобождение медиатора из пузырьков подавляется; в обычных же условиях это высвобождение обусловлено изменением свойств пресинаптической мембраны, которое в свою очередь возникает под влияния нервного импульса, проходящего по поверхности аксона.
Чаще всего в синаптическую щель выделяется ацетилхолин, изменяющий проницаемость постсинаптической мембраны. Ацетилхолин, выявляемый в синапсе образуется в нервных окончаниях, а не в самой мышце. По-видимому, ацетилхолин образуется заранее и хранится в мельчайших пузырьках нервных окончаний. В отсутствие ионов кальция высвобождение медиатора из пузырьков подавляется; в обычных же условиях это высвобождение обусловлено изменением свойств пресинаптической мембраны, которое в свою очередь возникает под влияния нервного импульса, проходящего по поверхности аксона.
 Выделение ацетилхолина Спонтанное выделение ацетилхолина из нервных окончаний происходит непрерывно, что приводит к возникновению небольших флуктуаций потенциала концевой пластинки, т. е. генерации так называемых миниатюрных потенциалов, амплитуда которых лежит значительно ниже порогового значения. В то же время их амплитуда слишком высокая для того, чтобы возникновение миниатюрных потенциалов можно было объяснить случайным поступлением в синаптическую щель отдельных молекул ацетилхолина. В самом деле, для образования каждого такого миниатюрного потенциала необходима порция из нескольких тысяч молекул медиатора. Время от времени один из пузырьков, обнаруженных в аксонах в области концевой пластинки, выделяется из нервного окончания, независимо от того, приходит по нерву импульс или нет. Во всех случаях выделение ацетилхолина в синаптическую щель происходит строго определенными порциями ( «квантами» ). По-видимому, нервный импульс просто увеличивает число таких порции, поступающих от нервного окончания к мышце, а не изменяет величину каждой из них.
Выделение ацетилхолина Спонтанное выделение ацетилхолина из нервных окончаний происходит непрерывно, что приводит к возникновению небольших флуктуаций потенциала концевой пластинки, т. е. генерации так называемых миниатюрных потенциалов, амплитуда которых лежит значительно ниже порогового значения. В то же время их амплитуда слишком высокая для того, чтобы возникновение миниатюрных потенциалов можно было объяснить случайным поступлением в синаптическую щель отдельных молекул ацетилхолина. В самом деле, для образования каждого такого миниатюрного потенциала необходима порция из нескольких тысяч молекул медиатора. Время от времени один из пузырьков, обнаруженных в аксонах в области концевой пластинки, выделяется из нервного окончания, независимо от того, приходит по нерву импульс или нет. Во всех случаях выделение ацетилхолина в синаптическую щель происходит строго определенными порциями ( «квантами» ). По-видимому, нервный импульс просто увеличивает число таких порции, поступающих от нервного окончания к мышце, а не изменяет величину каждой из них.
 Для непрерывного высвобождения содержимого пузырьков необходимо присутствие ионов кальция; в отсутствие этих ионов приход нервного импульса не увеличивает выделения ацетилхолина. Ионы напротив, действуют подобно конкурентному ингибитору этого процесса; вот почему отношение ионов Мg 2+/Са 2+ является важнейшим параметром, определяющим нормальную функцию нервномышечного соединения. Изменяя ионный состав среды для данного конкретного синапса, можно управлять количеством ацетилхолина, выделяющегося под действием данного импульса.
Для непрерывного высвобождения содержимого пузырьков необходимо присутствие ионов кальция; в отсутствие этих ионов приход нервного импульса не увеличивает выделения ацетилхолина. Ионы напротив, действуют подобно конкурентному ингибитору этого процесса; вот почему отношение ионов Мg 2+/Са 2+ является важнейшим параметром, определяющим нормальную функцию нервномышечного соединения. Изменяя ионный состав среды для данного конкретного синапса, можно управлять количеством ацетилхолина, выделяющегося под действием данного импульса.
 Cинапс способен к интеграции стимулов. После прохождения через синапс первоначального импульса следующие немедленно за ним импульсы вызывают прогрессивно возрастающий ответ мышцы, который достигает максимальной величины приблизительно после прохождения десятого импульса. Этот феномен часто называют облегчением. Вместе с тем после прохождения большого числа импульсов потенциал концевой пластинки постепенно уменьшается до тех пор, пока наконец мышца вообще не перестает отвечать на стимуляцию. Этот последний процесс часто называют нервно-мышечной депрессией. Изучение интегративного процесса, происходящего в мышце, показало, что изменение ответа полностью определяется количеством ацетилхолина, выделяемого пресинаптическим компонентом.
Cинапс способен к интеграции стимулов. После прохождения через синапс первоначального импульса следующие немедленно за ним импульсы вызывают прогрессивно возрастающий ответ мышцы, который достигает максимальной величины приблизительно после прохождения десятого импульса. Этот феномен часто называют облегчением. Вместе с тем после прохождения большого числа импульсов потенциал концевой пластинки постепенно уменьшается до тех пор, пока наконец мышца вообще не перестает отвечать на стимуляцию. Этот последний процесс часто называют нервно-мышечной депрессией. Изучение интегративного процесса, происходящего в мышце, показало, что изменение ответа полностью определяется количеством ацетилхолина, выделяемого пресинаптическим компонентом.
 Межнейронные синапсы Передача сигналов через межнейронные синапсы, в частности в центральной нервной системе, представляет собой относительно сложный процесс по сравнению с тем, который протекает в нервно-мышечном соединении. Однако отмечается и большое сходство в механизмах этой передачи. Первопричиной возникновения сигнала является изменение ионной проницаемости постсинаптической мембраны. Точно так же известно, что выделение медиаторов в межнейронном синапсе происходит порциями. В области центральных нейронов дело обстоит сложнее: здесь происходит поступление ряда импульсов; при этом постсинаптическая мембрана дендритов такого нейрона служит местом, где происходит алгебраичекая суммация всех синаптических потенциалов, генерируемых в ответ на импульсы, приходящие по различным (возбуждающим и тормозящым) окончаниям. Импульсы, поступающие по возбуждающим и тормозным волокнам, совершенно одинаковы. Различие в вызываемом ими эффекте определяется природой соответствующих синапсов (тормозных или возбуждающих), т. е. именно свойствами постсинаптического центрального нейрона. Наконец, суммация возможна в том случае, если все импульсы, приходящие к синапсам данного нейрона, являются подпороговыми; в центральном нейроне происходят алгебраическая суммация, которая и определяет знак и величину изменения потенциала постсинаптической мембраны. Это изменение может выразиться в столь значительной деполяризации мембраны, что приведет к генерации импульса; в других же условиях величина деполяризации не превысит порогового значения.
Межнейронные синапсы Передача сигналов через межнейронные синапсы, в частности в центральной нервной системе, представляет собой относительно сложный процесс по сравнению с тем, который протекает в нервно-мышечном соединении. Однако отмечается и большое сходство в механизмах этой передачи. Первопричиной возникновения сигнала является изменение ионной проницаемости постсинаптической мембраны. Точно так же известно, что выделение медиаторов в межнейронном синапсе происходит порциями. В области центральных нейронов дело обстоит сложнее: здесь происходит поступление ряда импульсов; при этом постсинаптическая мембрана дендритов такого нейрона служит местом, где происходит алгебраичекая суммация всех синаптических потенциалов, генерируемых в ответ на импульсы, приходящие по различным (возбуждающим и тормозящым) окончаниям. Импульсы, поступающие по возбуждающим и тормозным волокнам, совершенно одинаковы. Различие в вызываемом ими эффекте определяется природой соответствующих синапсов (тормозных или возбуждающих), т. е. именно свойствами постсинаптического центрального нейрона. Наконец, суммация возможна в том случае, если все импульсы, приходящие к синапсам данного нейрона, являются подпороговыми; в центральном нейроне происходят алгебраическая суммация, которая и определяет знак и величину изменения потенциала постсинаптической мембраны. Это изменение может выразиться в столь значительной деполяризации мембраны, что приведет к генерации импульса; в других же условиях величина деполяризации не превысит порогового значения.
 Синапсы ЦНС В ЦНС существует два типа торможения — пресинаптическое и постсинаптическое. При постсинаптическом торможении тормозный медиатор изменяет проницаемость постсинаптической мембраны для анионов (в частности, для Сl-), что противодействует ее деполяризации, обусловленной вхождением Na+, так как в этих условиях с возрастанием направленного внутрь клетки потока Na+ увеличивается и проникновение в нее Сl_. Явление пресинаптического торможения обусловлено уменьшением количества медиатора, высвобождающегося нейроном. Таким образом, возникновение этого эффекта можно связать с повышением проницаемости мембраны для Сl-. Как и в нервномышечном соединении, в ЦНС наблюдается эффект облегчения. Чем больше число проведенных импульсов, тем выше эффективность каждого последующего. Весьма интересно, что у центрального нейрона, участвующего сразу во многих синапсах, облегчение проведения в одном из них не сказывается на передаче через другие синапсы. Это позволяет предположить, что эффект облегчения обусловливается свойствами пресинаптического нейрона, а yе мембраны постсинаптической (рецепторной) клетки. Однако существует и иной феномен, обычно называемый суммацией, который выражается в том, что центральный нейрон способен алгебраически суммировать возникающие синаптические потенциалы.
Синапсы ЦНС В ЦНС существует два типа торможения — пресинаптическое и постсинаптическое. При постсинаптическом торможении тормозный медиатор изменяет проницаемость постсинаптической мембраны для анионов (в частности, для Сl-), что противодействует ее деполяризации, обусловленной вхождением Na+, так как в этих условиях с возрастанием направленного внутрь клетки потока Na+ увеличивается и проникновение в нее Сl_. Явление пресинаптического торможения обусловлено уменьшением количества медиатора, высвобождающегося нейроном. Таким образом, возникновение этого эффекта можно связать с повышением проницаемости мембраны для Сl-. Как и в нервномышечном соединении, в ЦНС наблюдается эффект облегчения. Чем больше число проведенных импульсов, тем выше эффективность каждого последующего. Весьма интересно, что у центрального нейрона, участвующего сразу во многих синапсах, облегчение проведения в одном из них не сказывается на передаче через другие синапсы. Это позволяет предположить, что эффект облегчения обусловливается свойствами пресинаптического нейрона, а yе мембраны постсинаптической (рецепторной) клетки. Однако существует и иной феномен, обычно называемый суммацией, который выражается в том, что центральный нейрон способен алгебраически суммировать возникающие синаптические потенциалы.


