Adsorbtsia5.pptx
- Количество слайдов: 22

Фундаментальная адсорбционная формула Гиббса так как а то Записываем его полный дифференциал 1

Уравнение (3) совместно с уравнением (1) лишь при условии следующей связи Если T=const, то Эти уравнение называются фундаментальными уравнениями Гиббса. Величины Us, Ss, зависят от величины поверхности раздела фаз. Поэтому для разных систем их трудно сравнивать, поэтому удобнее перейти к абсолютным величинам, относя их к единице поверхности 2

3

Величину - называется избытком чисел молей компонента i в объеме поверхностного слоя с площадью S=1. Эту величину называют абсолютной величиной гиббсовой адсорбции. Определим избыточную свободную энергию: Из (7) и (4) следует 4

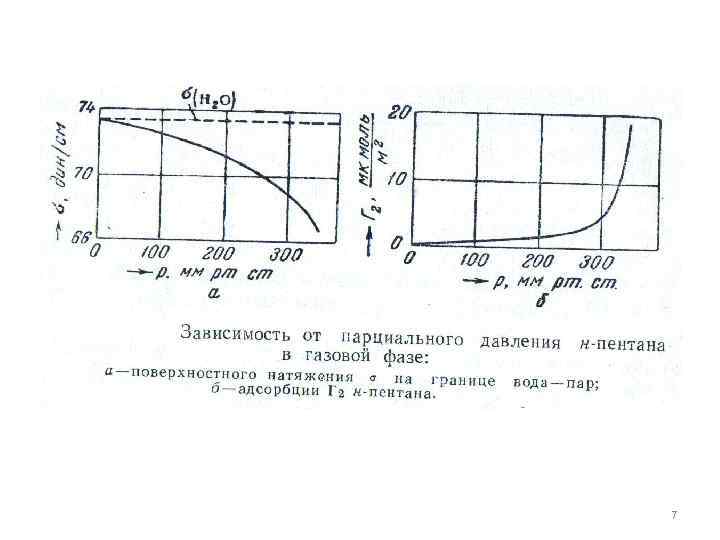
Если вспомнить применение поверхности раздела эта величина аналогична давлению δ=-Р из уравнений (4), (5) и (6) следует: Применение формулы Гиббса 1. Адсорбция на поверхности жидкости, не растворяющего в ней газа. Вода(1)+углеводород(2) , т. к. углеводород в ней не растворяется, поэтому (11) будет иметь вид: 5

Учитывая, что Получим То зная зависимость δ от P для жидкости нерастворяющейся в ней газа, можно по (12) определить ее адсорбцию 6
7

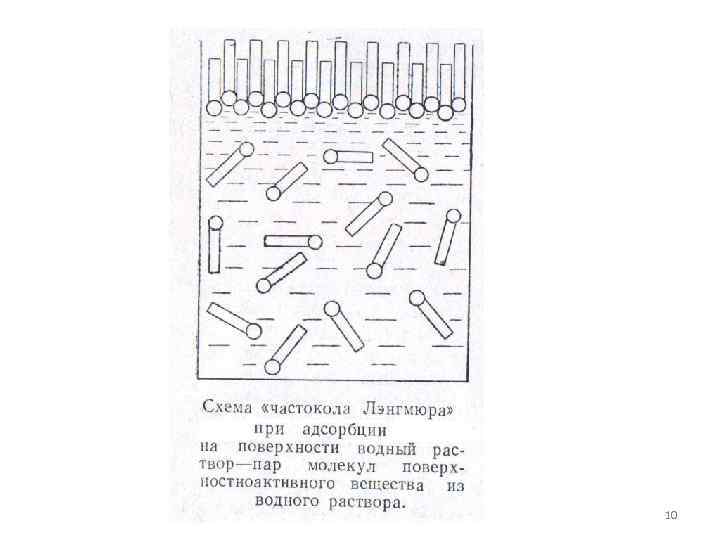
2. Адсорбция на поверхности жидкости растворенного в ней вещества Вода(1)+низкомолекулярный спирт(2) Можем ли пользоваться выражением (12) Необходимо выбрать положение поверхности S таким образом, чтобы величина адсорбция самого растворителя Для этого необходимо перемещать поверхность S в сторону фазы I или II до тех пор, пока положительный избыток количества по одну сторону поверхности S не будет точно компенсировать отрицательный его избыток по другую сторону, тогда (1) – фаза При малых концентрациях С 2 8

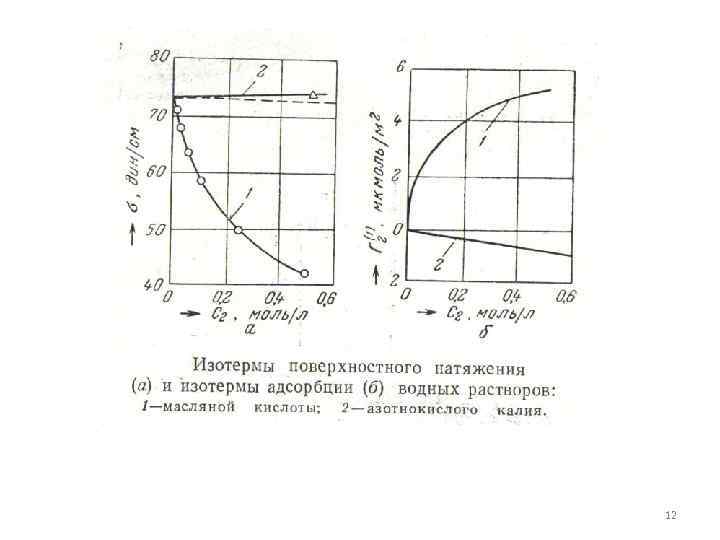
Из (13) можно определить вычислить изотерму при растворении в воде R-OH, R-COOH, R-NH 2, вещества, дающие положительные отклонения от закона Рауля, Поэтому молекулы этих соединений выталкивается из воды на поверхность, т. е. , δ с ростом с2 падает с увеличением R молекул еще сложнее выталкивается и еще сильнее понижают поверхностное натяжение. Вещества понижающие δ растворителя называют поверхностно-активными, для них и 9
10

Если растворить в I электролиты, дающие отрицательное отклонение от закона Рауля, ионы взаимодействует с молекулами , поэтому ионы распределяются в объемной фазе, тогда и Вещества, повышающие поверхностное натяжение растворителя называются поверхностно-инактивными. Концентрация воды в поверхностном слое меняется мало, так как даже попадающие в поверхностный слой ионы гидратированы, поэтому ионы мало уменьшают δ и их отрицательная адсорбция мала. 11
12
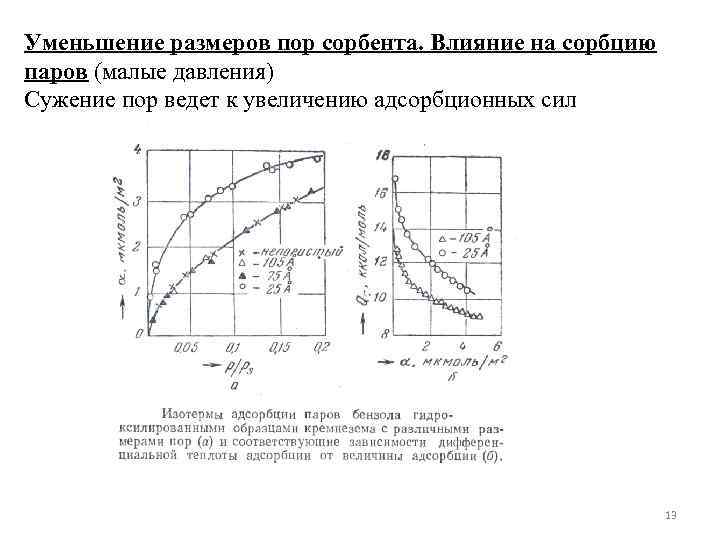
Уменьшение размеров пор сорбента. Влияние на сорбцию паров (малые давления) Сужение пор ведет к увеличению адсорбционных сил 13

. В случае тонкопористых сорбентов адсорбционный потенциал повышен по сравнению с широкой частью поры. Увеличение адсорбционного потенциала приводит к заполнению тонких пор уже при небольших На этом основа теория Поляньи. По мере увеличения количество адсорбата увеличивается и сорбат жидкость заполняет уже и широкие поры. Поляньи считает, что адсорбционный потенциал функция от объема жидкого сорбата: (работа против адсорбционных сил) 14
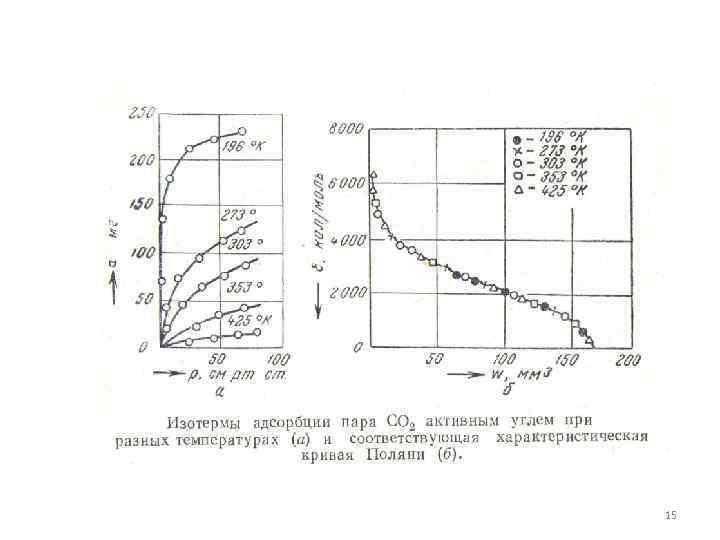
15
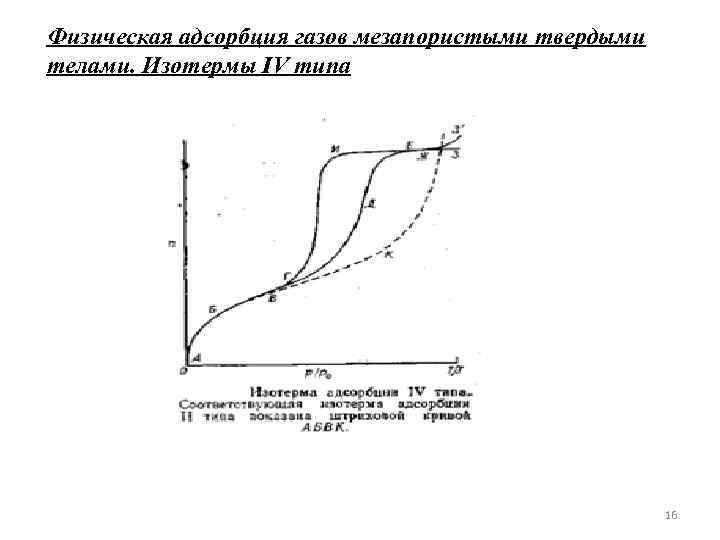
Физическая адсорбция газов мезапористыми твердыми телами. Изотермы IV типа 16

Чтобы выделит возможность конденсации на поверхности тонкой пленки адсорбата в порах надо найти зависимость давления пора от кривизны поверхности жидкости. Вспомним условия механического равновесия (14) Давления пара над этой поверхности в фазе равно При равновесии 17

Интегрируя от давления P'' (15) Для плоской поверхности И общее давление в газовой фазе не изменяется, то Из уравнений 14 и 15 получаем: (16) 18

Откуда Для вогнутого шаровидного мениска радиуса rш оба центра кривизны совпадают, т. е , поэтому Это уравнение называется формулой Томсона(Кельвина) В случае сферической капли Следовательно Для цилиндрического мениска одна из главных кривизн равна нулю, поэтому 19
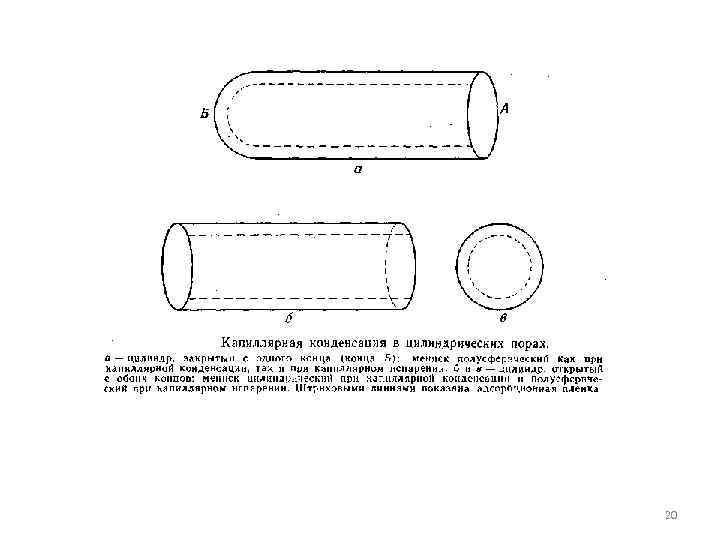
20
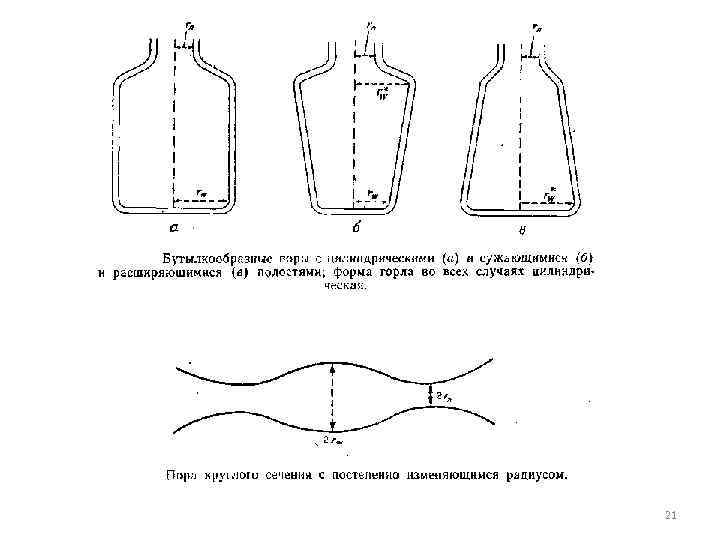
21
22
Adsorbtsia5.pptx